文档内容
第二章 海水中的重要元素—钠和氯
第三节 物质的量
第四课时 配制一定物质的量浓度的溶液
【学习目标】1.通过小组讨论交流,设计溶液的配制方案并进行评价,形成科学合理的配制溶液的方
案,培养学生从定量的角度认识“宏观辨识和微观探析”的核心素养。
2.通过问题探究、实验操作、分析归纳,知道使用容量瓶配制一定物质的量浓度的溶液的方法及注意
事项,学会误差分析,培养创新意识。形成善于合作、敢于质凝的科学探究意识。
【学习重点】学会一定物质的量浓度的溶液的配制方法。
【学习难点】实验中的误差分析。
【课前预习】
旧知回顾:配制100g质量分数0.9%的NaCl溶液需要的实验仪器有
,
实验步骤: 。
新知预习: 1.配制100ml 1.00mol/LNaCl溶液需要的主要仪器有:
___ 。配制步骤:
。
【课中探究】
情景导入:在日常生活生产中,很多物质具有的特殊作用,在浓度上都是有要求的。例如体积分数为
75%的酒精溶液可用于杀菌消毒;质量分数0.9%的氯化钠溶液可作生理盐水等。在实验室中,我们可以直
接用固体或液体试剂来配制一定物质的量浓度的溶液。(见PPT图片)
一、一定物质的量浓度溶液的配制
活动一、容量瓶的使用及实验步骤
任务一、一定物质的量浓度溶液的配制需要使用容积精确的仪器容量瓶,阅读教材P58-59页内容,结
合图2-24和“资料卡片”,观察实物样品,思考使用容量瓶的注意事项是什么?
①构造:
②常用规格:
③选用原则:
④用途:
⑤注意事项:任务二、应用探究:结合教材P59页【实验2-10】和P60页图2-26配制100mL1.00mol/LNaCl溶液。
①主要仪器:
②实验步骤:
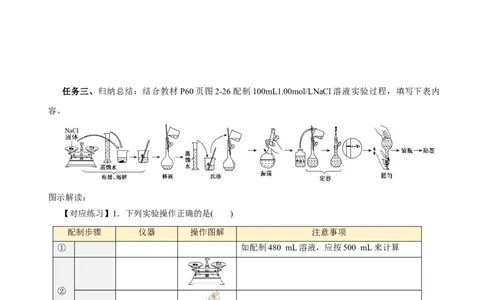
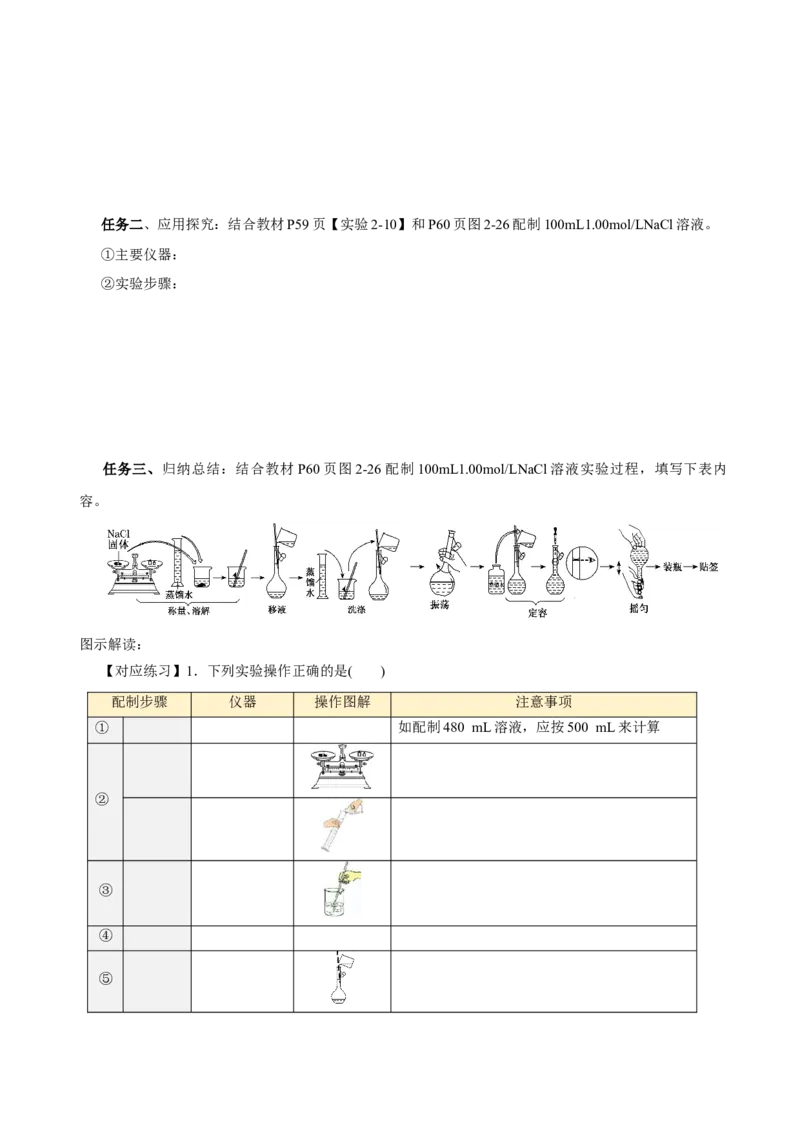
任务三、归纳总结:结合教材P60页图2-26配制100mL1.00mol/LNaCl溶液实验过程,填写下表内
容。
图示解读:
【对应练习】1.下列实验操作正确的是( )
配制步骤 仪器 操作图解 注意事项
① 如配制480 mL溶液,应按500 mL来计算
②
③
④
⑤【
对 应
练
⑥
习
】
1
. 下
⑦
列
实
验
操
⑧
作
正
确
的
⑨
是(
)
A
. 用
⑩
托
盘
天平称量11.50 g NaCl固体
B.用100 mL量筒量取5.5 mL稀盐酸
C.使用容量瓶配制溶液,移液时应洗涤烧杯2~3次
D.溶解后的氢氧化钠趁热转移到容量瓶中
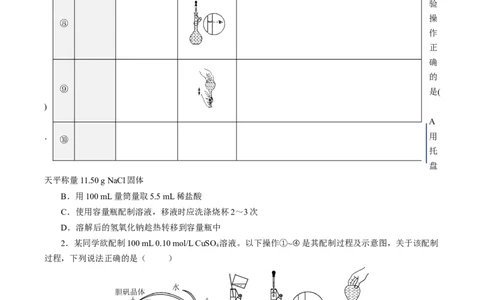
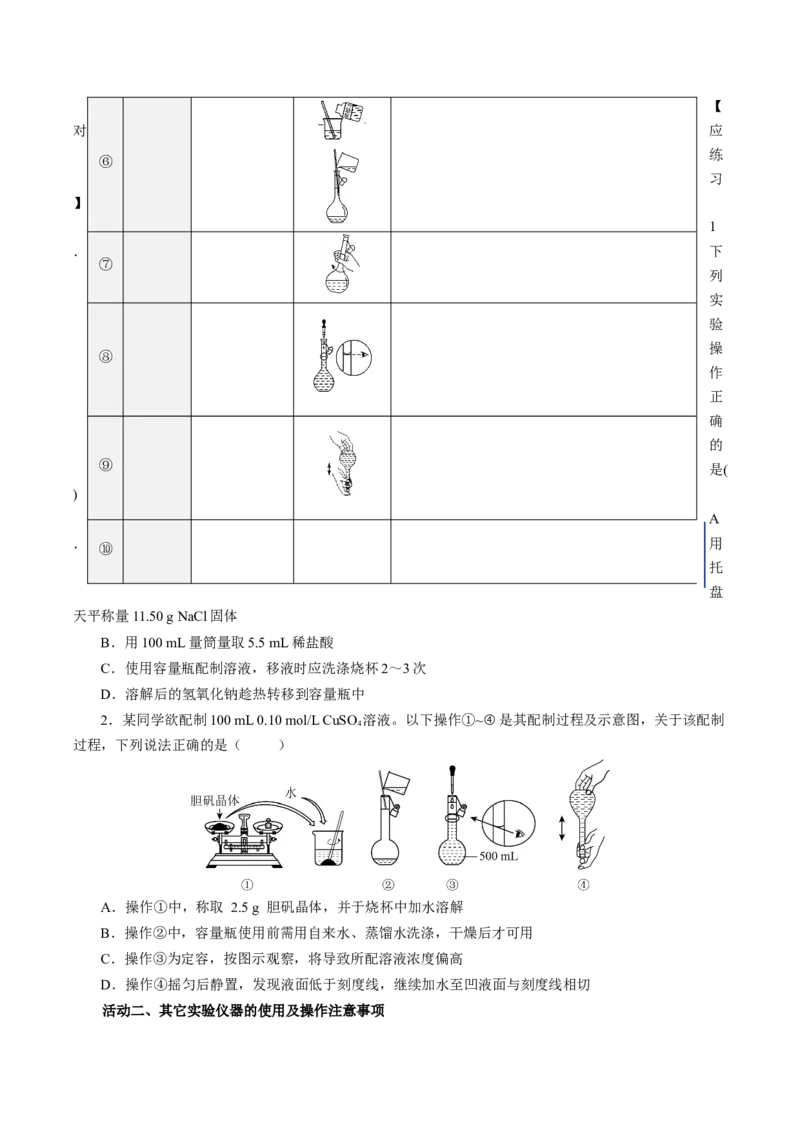
2.某同学欲配制100 mL 0.10 mol/L CuSO 溶液。以下操作①~④是其配制过程及示意图,关于该配制
4
过程,下列说法正确的是( )
A.操作①中,称取 2.5 g 胆矾晶体,并于烧杯中加水溶解
B.操作②中,容量瓶使用前需用自来水、蒸馏水洗涤,干燥后才可用
C.操作③为定容,按图示观察,将导致所配溶液浓度偏高
D.操作④摇匀后静置,发现液面低于刻度线,继续加水至凹液面与刻度线相切
活动二、其它实验仪器的使用及操作注意事项任务一、实验中计算需NaCl固体5.85g,为何用托盘天平称取5.9gNaCl固体?若用浓硫酸配制一定物
质的量浓度的稀硫酸有何不同?
任务二、问题探究:(1)配制480 mL溶液选用什么规格的容量瓶?
(2)要配制1 L 0.1 mol·L-1 CuSO 溶液,需要CuSO 粉末或CuSO ·5H O的质量一样吗?
4 4 4 2
(3)实验过程中,玻璃棒的作用是什么?溶解时要注意什么问题?
【对应练习】1.实验室中需要配制0.2 mol·L-1的硫酸铜溶液950 mL,配制时应选用的容量瓶的规格和
称取的胆矾的质量分别是( )
A.950 mL;30.4 g B.950 mL;47.5 g
C.1 000 mL;50.0 g D.1 000 mL;32.0 g
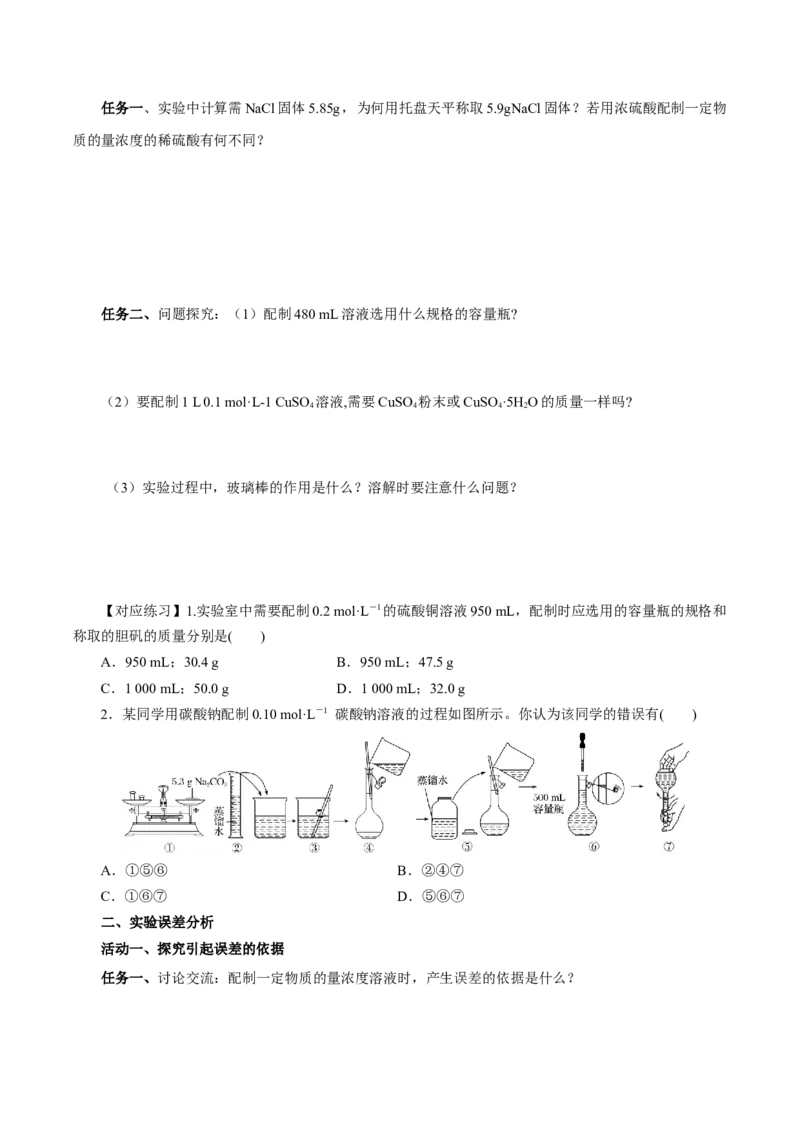
2.某同学用碳酸钠配制0.10 mol·L-1 碳酸钠溶液的过程如图所示。你认为该同学的错误有( )
A.①⑤⑥ B.②④⑦
C.①⑥⑦ D.⑤⑥⑦
二、实验误差分析
活动一、探究引起误差的依据
任务一、讨论交流:配制一定物质的量浓度溶液时,产生误差的依据是什么?任务二、问题探究:结合教材P60页“思考与讨论”,思考(1)为什么要用蒸馏水洗涤烧杯内壁和
玻璃棒2~3次,并将洗涤液也都注入容量瓶?
(2)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求
的大了还是小了?
(3)如果在读数时,仰视或者俯视容量瓶上的刻度线,最后配成的溶液中溶质的实际浓度比所要求的大了
还是小了?
【对应练习】1.某学生欲配制0.1 mol·L-1氢氧化钠溶液100 mL,下列操作会造成实际浓度偏高的是(
)
A.空盘时天平指针指向左边 B.把烧碱放在滤纸上称量
C.定容时俯视刻度线 D.使用部分变质的烧碱
2.配制250mL0.1mol/LCuSO 溶液,下列说法正确的是( )
4
A.先称取4.0gCuSO ,再将其溶于250mL蒸馏水
4
B.容量瓶未干燥即用来配制溶液会导致配制的溶液浓度偏低
C.转移溶液没有用蒸馏水洗涤烧杯,直接用蒸馏水定容,导致配制溶液浓度偏低
D.定容时俯视容量瓶刻度线使得溶液物质的量浓度偏低
活动二、探究引起误差的操作
任务一、讨论交流:配制一定物质的量浓度溶液时,哪些操作可能引起实验误差,完成表中内容。
能引起误差的一些操作 m V c
B
天平的砝码沾有其他物质或已生锈
托盘天平 药品、砝码左右位置颠倒,且使用了游码
称量易潮解的物质(如NaOH)时间过长用量筒量取液体时,仰视读数
量筒
用量筒量取液体时,俯视读数
烧杯和玻 搅拌时部分液体溅出
璃棒 未洗涤烧杯和玻璃棒
溶液未冷却到室温就注入容量瓶定容
向容量瓶转移溶液时有少量液体流出
容量瓶 定容时,水加多了,用滴管吸出
定容时,俯视刻度线
定容时,仰视刻度线
任务二、定容时仰视或俯视刻度线对实验结果会有哪些影响呢?
①图示分析:
②对结果的影响分析:
【对应练习】1.下列配制的溶液浓度偏高的是( )
A.配制盐酸用量筒量取盐酸时俯视刻度线
B.配制盐酸定容时,仰视容量瓶刻度线
C.配制烧碱溶液时,没有洗涤溶解烧碱的烧杯和玻璃棒
D.配制烧碱溶液时,烧碱溶解后未经冷却即注入容量瓶并加水至刻度线
2.实验室欲用NaCO·10H O晶体配制100 mL 1 mol·L-1的NaCO 溶液,下列说法正确的是( )
2 3 2 2 3
A.要完成实验需称取10.6 g Na CO·10H O晶体
2 3 2
B.本实验需用到的仪器有托盘天平、药匙、玻璃棒、烧杯、500 mL容量瓶
C.配制时若容量瓶不干燥,含有少量蒸馏水会导致溶液浓度偏低
D.定容时俯视刻度线会导致溶液浓度偏高
【课后巩固】1.(易)教材作业:P18-19页练习5、6、10
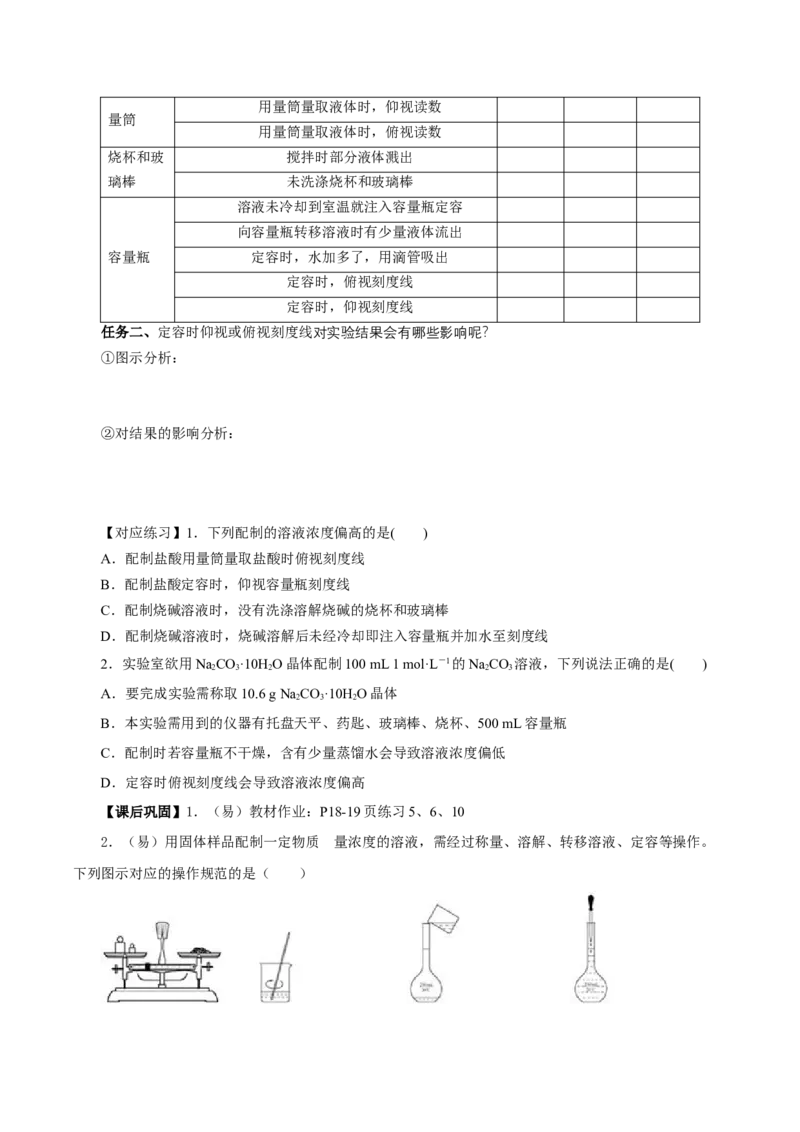
2.(易)用固体样品配制一定物质 的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。
下列图示对应的操作规范的是( )A.称量 B.溶解 C.转移 D.定容
3.(易)配制0.1 mol·L-1 NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是
A.称量时,左盘低,右盘高 B.定容时仰视读取刻度
C.原容量瓶洗净后未干燥 D.溶解NaCl时有溶液溅出
4.(易)关于容量瓶的几种叙述:①是配制一定物质的量浓度的溶液的仪器;②不宜贮存溶液;③
不能用来加热;④使用之前要检查是否漏水;⑤需要240 mL一定物质的量浓度的氯化钠溶液,用250 mL
的容量瓶配制;⑥用蒸馏水洗净后,再用待配溶液润洗。这些叙述正确的是( )
A.①②③④⑤ B.②③⑤⑥
C.①②④⑥ D.②③④⑥
5.(中)某实验需1 mol·L-1 NaOH 溶液90 mL,配制该NaOH溶液的几个关键实验步骤和操作示意
图如下:
下列说法正确的是( )
A.用托盘天平和滤纸称取3.6 g氢氧化钠固体
B.NaOH在烧杯中完全溶解,立即转移到容量瓶中
C.操作①时,若俯视容量瓶的刻度线,使配得的NaOH溶液浓度偏低
D.上述操作的先后顺序是③②④⑥①⑤
6.(中)实验室需要配制0.1 mol·L-1NaOH溶液450 mL时,使所配制的溶液浓度偏低的操作是(
)
①将NaOH固体放在称量纸上称量,再转移到烧杯中溶解
②烧杯中NaOH溶液移入容量瓶后没有洗涤烧杯
③实验用的容量瓶洗净后未干燥,里面含有少量水
④用天平准确称量1.8 g NaOH固体
⑤NaOH固体已潮解
A.①②③⑤ B.②③④
C.①③④ D.①②④⑤
7.(中)配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
A.容量瓶用蒸馏水洗净后,必须干燥才能用于配制溶液
B.配制1 L 0.1 mol·L-1的NaCl溶液时,用托盘天平称量5.85 g NaCl固体
C.配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高
D.用浓盐酸配制稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高
8.(难)配制480mL 0.2mol·L-1的FeSO 溶液,配制过程中有如下操作步骤:
4①把称量好的绿矾(FeSO ·7H O)放入小烧杯中,加适量蒸馏水溶解;
4 2
②把①所得溶液小心转入___________中;
③继续向容量瓶中加蒸馏水至液面距离刻度l~2cm处,改用________________滴加蒸馏水至液面与刻
度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,反复上下颠倒,摇匀; ⑥待溶液恢复到室温。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号)___________,完成此配制实验,除了量筒、烧杯、玻璃棒外还
需要的常见的玻璃仪器有_____________________。
(2)实验室用绿矾(FeSO ·7H O)来配制该溶液,用托盘天平称量绿矾___________g。
4 2
(3)由于错误操作,使得实际浓度比所要求的偏小的是_____________________(填写编号)。
A.称量绿矾时,左码右物
B.使用容量瓶配制溶液时,俯视液面定容,
C.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有干燥
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用