文档内容
第1讲 沉淀溶解平衡
1.知道难溶电解质的沉淀溶解平衡及其影响因素。
2.知道Ksp的意义,能根据Q和Ksp的大小关系判断难溶电解质的沉淀或溶解情
况。
重点:沉淀溶解平衡及其影响因素
难点:沉淀溶解平衡及其影响因素
1.难溶电解质的沉淀溶解平衡
(1)常温时,溶解性与溶解度的关系
(2)沉淀溶解平衡的建立
生成沉淀的离子反应之所以能够发生,在于生成物的溶解度很小,但生成的沉淀物并
不是绝对不溶。如AgCl在溶液中存在两个过程:一方面,在水分子作用下,少量 Ag + 和
Cl - 脱离AgCl 的表面进入水中——溶解;另一方面,溶液中的 Ag + 和 Cl - 受AgCl表面阴、
阳离子的吸引,回到AgCl 的表面析出——沉淀。在一定温度下,当沉淀和溶解速率相等
时,得到AgCl的饱和溶液。即建立下列动态平衡:AgCl(s)溶解,沉淀 Ag+(aq)+Cl-(aq)人
们把这种平衡称为沉淀溶解平衡。
(3)溶度积
①概念
在一定条件下,难溶电解质溶于水形成饱和溶液时,溶质的离子与该固态物质之间建
立动态平衡,这时可以用平衡常数来描述难溶电解质在水中的沉淀溶解平衡,其平衡常数
称为溶度积常数或溶度积,通常用K 来表示。
sp
②表达式
沉淀溶解平衡Ag S(s)⇌2Ag+(aq)+S2-(aq)的溶度积常数可表示为K = c 2 (Ag + )· c (S 2
2 sp
- )。
③意义
溶度积的大小与溶解度有关,它反映了难溶电解质在水中的溶解能力。
④应用——溶度积规则通过比较溶度积常数K 与溶液中有关离子浓度幂的乘积——离子积 Q的相对大小,
sp
可以判断难溶电解质在给定条件下沉淀能否生成或溶解,这就是溶度积规则。难溶电解质
Ag S的水溶液中,离子积Q表示为Q= c 2 (Ag + )· c (S 2 - ) 。
2
若QK ,溶液为过饱和溶液,体系中有沉淀析出。
sp
1.判断正误,正确的打“√”,错误的打“×”。
(1)可利用溶液混合后的Q与K 的相对大小来判断溶液混合后是否有沉淀生成。( )
sp
(2)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度。( )
(3)向NaSO 溶液中加入过量的BaCl 溶液,则SO2- 沉淀完全,溶液中只含Ba2+、Na+
2 4 2 4
和Cl-,不含SO2- 。( )
4
(4)洗涤沉淀时,洗涤次数越多越好。( )
(5)常温下,向BaCO 的饱和溶液中加入NaCO 固体,BaCO 的K 减小。( )
3 2 3 3 sp
(6)溶度积常数K 只受温度影响,温度升高,K 增大。( )
sp sp
答案 (1)√ (2)× (3)× (4)× (5)× (6)×
考点1沉淀溶解平衡的特征和K
sp
1.沉淀溶解平衡的特征
(1)“逆”——沉淀溶解平衡是一个可逆过程。
(2)“动”——动态平衡,溶解速率和沉淀速率不等于零。
(3)“等”——溶解速率和沉淀速率相等。
(4)“定”——平衡状态时,溶液中的离子浓度保持不变。
(5)“变”——当改变外界条件时,溶解平衡发生移动。
2.沉淀溶解平衡的移动
以BaCO (s)Ba2+(aq)+CO2- (aq) ΔH>0为例
3 4
移动、
外界条件 平衡后c(Ba2+) 平衡后c(CO2- )
4
方向
升高温度 正向 增大 增大
加水稀释 正向 不变 不变
加入少量
逆向 增大 减小
BaCl (s)
2
加入少量 逆向 减小 增大NaCO(s)
2 3
加入NaSO (s) 正向 减小 增大
2 4
2.K 的意义及其影响因素
sp
(1)K 的意义
sp
K 大小反映难溶电解质在水中的溶解能力。同一温度下,相同类型的电解质,溶度积
sp
越小,其溶解能力越弱;不同类型的电解质,溶度积小的电解质的溶解能力不一定比溶度
积大的溶解能力弱。
(2)影响K 的因素
sp
①内因:难溶物质本身的性质,这是决定因素。
②外因:只受温度的影响,绝大多数难溶物的溶解是吸热过程,升高温度,平衡向溶
解方向移动,K 增大。
sp
对饱和AgCl溶液(有AgCl固体存在)进行下列操作后,c(Ag+)保持不变的是
A.加少量水稀释 B.加热
C.加入少量浓盐酸 D.加入少量固体AgNO
3
【答案】A
【解析】A.加少量水稀释,平衡正向移动,但c(Ag+)保持不变,故A符合题意;
B.加热,平衡正向移动,c(Ag+)增大,故B不符合题意;
C.加入少量浓盐酸,平衡逆向移动,c(Ag+)减小,故C不符合题意;
D.加入少量固体AgNO,c(Ag+)增大,平衡逆向移动,c(Ag+)增大幅度减弱,故D不
3
符合题意。
综上所述,答案为A。
在一定温度下,当Mg(OH) 固体在水溶液中达到下列平衡时:Mg(OH) (s)⇌
2 2
Mg2+(aq)+2OH-(aq),要使Mg(OH) 固体减少而c(Mg2+)不变,可采取的措施是
2
A. 加MgSO 固体 B.通HCl气体
4
C.加NaOH固体 D.加少量水
【答案】D
【解析】A.MgSO 易溶于水,加MgSO 会增加c(Mg2+),A错误;
4 4
B.加HCl会中和OH-平衡右移,使c(Mg2+)增大,B错误;
C.加NaOH使c(OH-)增大平衡左移,c(Mg2+)减小,C错误;
D.加少量水时c(Mg2+)减少,平衡右移重新达到平衡时,c(Mg2+)又与原平衡相同,D正确;
故选D。
考点2沉淀溶解平衡图像类题的解题思路
1.明确图像中纵轴、横轴的含义
纵轴、横轴通常表示难溶电解质电离出的离子浓度或离子浓度的对数或离子浓度的负
对数。
2.理解图像中线上点、线外点的含义
(1)以AgCl为例,在该沉淀溶解平衡图像(如图所示)中,曲线上任意一点都表示达到了
沉淀溶解平衡状态,此时Q=K 。在温度不变时,无论改变哪种离子的浓度,另一种离子
sp
的浓度都只能在曲线上变化,不会出现在曲线以外。
(2)曲线上方区域的点均表示过饱和溶液,此时Q>K 。
sp
(3)曲线下方区域的点均表示不饱和溶液,此时Q5,故C错误;
c(H+
)
D.CaC O 的K =4.0×10-8,CaC O 难溶物存在溶解平衡,其CaC O 浊液中存在平
2 4 SP 2 4 2 4
衡:CaC O(s)⇌Ca2+(aq)+C O2- (aq),故D正确。
2 4 2 4
综上所述,答案为D。
4.下列对沉淀溶解平衡的描述正确的是
A.达到平衡时,沉淀溶解和离子沉淀停止
B.达到平衡时,溶液中溶质的离子浓度相等C.加水时,溶解平衡向溶解方向移动
D.升高温度,溶解平衡向溶解方向移动
【答案】C
【解析】A.沉淀溶解平衡是动态平衡,达到平衡时,沉淀溶解和离子沉淀仍在进
行,但速率相等,A项错误;
B.达到平衡时,溶液中溶质的离子浓度不变,但不一定相等,B项错误;
C.加水稀释时,沉淀溶解平衡向溶解的方向移动,即促进沉淀溶解,C项正确;
D.多数难溶电解质溶解于水时吸热的,升高温度,沉淀溶解平衡向溶解的方向移
动。但Ca(OH) 的溶解度随温度升高而降低,溶解平衡向沉淀方向移动,D项错误;
2
答案选C。
5.下列说法中正确的是
A.只有易溶电解质在溶液中才存在溶解平衡
B.难溶电解质在溶液中只存在溶解平衡,不存在电离平衡
C.溶解平衡只能通过电解质溶于水时建立
D.溶解平衡时,电解质表面上的离子或分子脱离电解质的速率与溶液中的离子或分
子回到电解质表面的速率相等
【答案】D
【解析】A.无论难溶电解质还是易溶电解质都存在沉淀溶解平衡,只要电解质在溶
液中溶解的速率等于结晶的速率,就达到了沉淀溶解平衡状态,故A错误;
B.难溶电解质在溶液中存在水的电离平衡,故B错误;
C.电解质溶于其它溶剂时,也能建立溶解平衡,故C错误;
D.达到沉淀溶解平衡时,溶解的速率和结晶的速率相等,故D正确;
故选D。
6.下列关于沉淀溶解平衡的说法正确的是
A.只有难溶电解质才存在沉淀溶解平衡
B.沉淀溶解平衡是可逆的
C.在平衡状态时v =v =0
溶解 沉淀
D.达到沉淀溶解平衡的溶液不一定是饱和溶液
【答案】B
【解析】A.易溶电解质作溶质时,如果是饱和溶液,也存在沉淀溶解平衡,A错
误;B.沉淀溶解平衡也属于动态平衡,是可逆过程,B正确;
C.沉淀溶解平衡为动态平衡,则在平衡状态时v =v ≠0,C错误;
溶解 沉淀
D.达到沉淀溶解平衡的溶液,沉淀溶解和生成的速率相等,则一定是饱和溶液,D
错误;
故选B。
7.饱和硫酸铜溶液中放入一块不规则胆矾晶体,保持温度不变,胆矾晶体形状逐渐变
为规则。下列有关描述正确的是( )
A.此过程中,胆矾晶体质量发生改变
B.比过程中,溶解速率大于结晶速率
C.此过程中,溶解速率小于结晶速率
D.此过程中,始终保持溶解平衡状态
【答案】D
【解析】向饱和硫酸铜溶液中放入一块不规则胆矾晶体,硫酸铜晶体和硫酸铜溶液形
成溶解平衡,此过程中始终保持溶解平衡状态,溶解速率等于结晶速率,晶体和溶液的质
量都是不变的,但硫酸铜晶体的形状会变得规则,故选D。
8.对“AgCl(s) ⇌Ag+(aq)+Cl-(aq)”的理解正确的是
①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底
A.③④ B.②③ C.①③ D.②④
【答案】B
【解析】氯化银在水溶液中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),其完整过
程为AgCl(s)⇌AgCl(aq)=Ag+(aq)+Cl-(aq),说明AgCl完全电离,是强电解质,故①错误,
②正确;由于存在沉淀溶解平衡,说明Ag+与Cl-的反应不能完全进行到底,故③正确,④
错误;所以只有②③正确;B正确;
综上所述,本题选B。
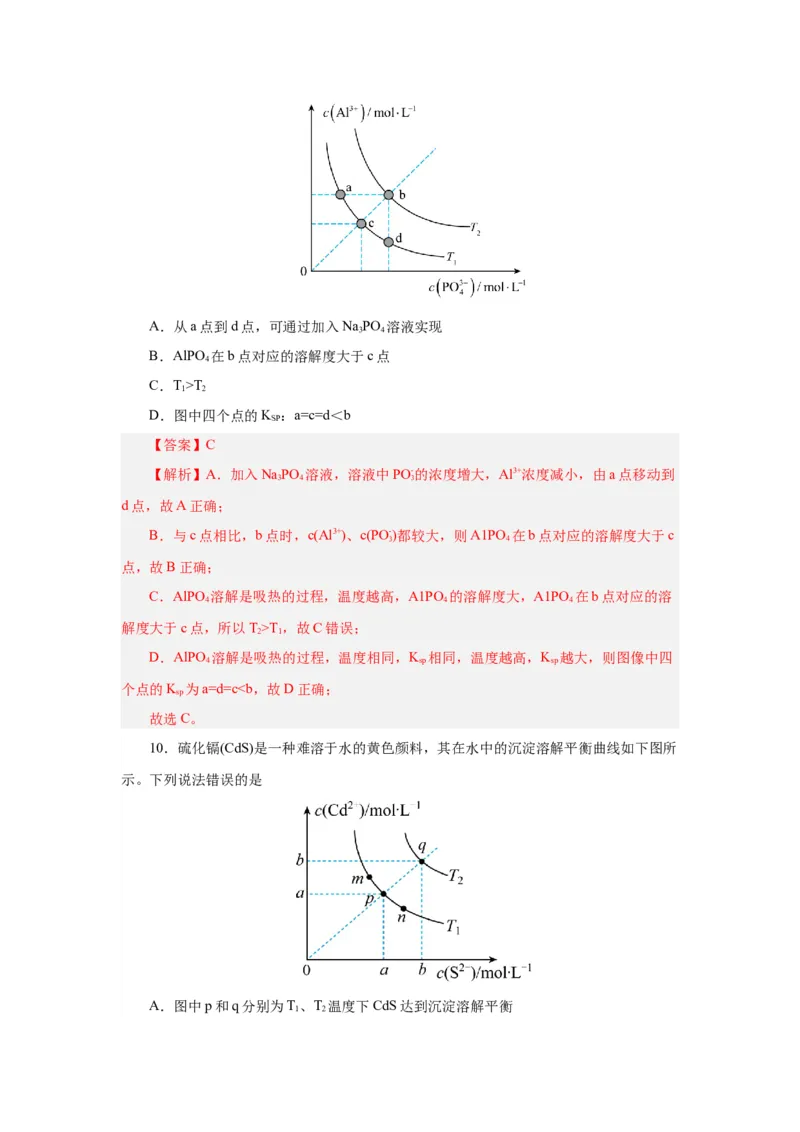
9. 溶解是吸热的过程,其沉淀溶解平衡曲线如图所示。下列说法不正确的是A.从a点到d点,可通过加入NaPO 溶液实现
3 4
B.AlPO 在b点对应的溶解度大于c点
4
C.T>T
1 2
D.图中四个点的K :a=c=d<b
SP
【答案】C
【解析】A.加入NaPO 溶液,溶液中PO- 的浓度增大,Al3+浓度减小,由a点移动到
3 4 3
d点,故A正确;
B.与c点相比,b点时,c(Al3+)、c(PO- )都较大,则A1PO 在b点对应的溶解度大于c
3 4
点,故B正确;
C.AlPO 溶解是吸热的过程,温度越高,A1PO 的溶解度大,A1PO 在b点对应的溶
4 4 4
解度大于c点,所以T>T,故C错误;
2 1
D.AlPO 溶解是吸热的过程,温度相同,K 相同,温度越高,K 越大,则图像中四
4 sp sp
个点的K 为a=d=c