文档内容
优秀领先 飞翔梦
想
2017年湖北省武汉市中考化学模拟试卷(五)
一、选择题(共8小题,每小题3分,满分24分)
1.下列变化中,不属于化学变化的是( )
A.葡萄酿酒 B.铁矿石炼铁 C.水结成冰 D.铁钉生锈
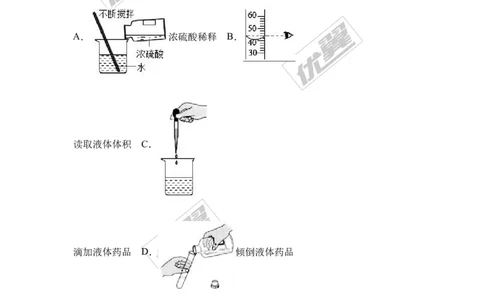
2.下列实验操作错误的是( )
A. 浓硫酸稀释 B.
读取液体体积 C.
滴加液体药品 D. 倾倒液体药品
3.化学与我们的日常生活有着密切的关系.下列有关说法或做法正确的是
( )
A.为治理空气污染,禁止使用化石燃料
B.二氧化碳灭火器原理是隔绝空气和提高可燃物的着火点
C.在金属表面刷油漆的目的是隔绝空气和水蒸气,防止金属腐蚀
D.硬水中含有较多的可溶性钙和镁的化合物,所以,长期饮用硬水有益于身体健
www.youyi100.com
第 1 页 共 21 页优秀领先 飞翔梦
想
康
4.对物质进行归类整理是化学学习的一种重要方法,下列归类关系不相符的是(
)
A.空气、海水﹣﹣纯净物
B.白磷、红磷﹣﹣可燃物
C.不锈钢、铜﹣﹣金属材料
D.合成橡胶、塑料﹣﹣有机合成材料
5.我国科学家屠呦呦因发现治疗疟疾的“青蒿素(C H O )”而获得诺贝尔奖.
15 22 5
青蒿素在氧气中完全燃烧
的化学方程式如下:aC H O +bO cCO +dH O,下列有关青蒿素的说法中
15 22 5 2 2 2
正确的是( )
A.青蒿素属于氧化物
B.青蒿素中C、H、O元素的质量比是9:11:4
C.青蒿素中所含氧元素的质量分数最小
D.青蒿素燃烧的化学方程式中,其化学计量数a、b、c、d分别是1、18、15、11
6.A~I都是初中化学中常见的物质,已知,A是一种无色无味的气体,C是应用
最广泛的金属,I是建筑材料的主要成分,F是实验室常用的溶剂,它们的转化关
系如图所示,其它有关物质未列出.下列说法错误的是( )
A.向物质G的水溶液中滴入无色酚酞试液,溶液变红色
B.②和③的化学反应类型相同
C.反应②是吸热反应,反应④是放热反应
D.物质A和物质E都具有可燃性
7.向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得
www.youyi100.com
第 2 页 共 21 页优秀领先 飞翔梦
想
溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
A.a点时,溶液中溶质为硝酸锌、硝酸铜、硝酸亚铁
B.b点时,所得固体只有银
C.c点时,溶液中一定有硝酸锌、硝酸亚铁,可能有硝酸铜
D.d点和e点所得固体均为银、铜、铁、锌
8.已知钠、钾都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入
质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说
法错误的是( )
A.分析曲线得出钠、钾与水反应产生氢气的速率不同
B.参加反应的钠的质量等于钾的质量
C.反应后的溶液都能使无色的酚酞变红
D.反应后NaOH溶液的溶质质量分数小于KOH溶液的溶质质量分数
二、非选择题:
9.图一是甲、乙两种元素的原子结构示意图.图二是实验室利用甲、乙两种元素
形成的一种化合物的溶
液制取某气体的微观示意图.
www.youyi100.com
第 3 页 共 21 页优秀领先 飞翔梦
想
请分析以上信息,回答下面的问题:
(1)在化学反应中甲元素通常形成的离子的符号是 ,乙元素原子最外层
电子数x= .
(2)请写出图二所示反应的化学方程式 .
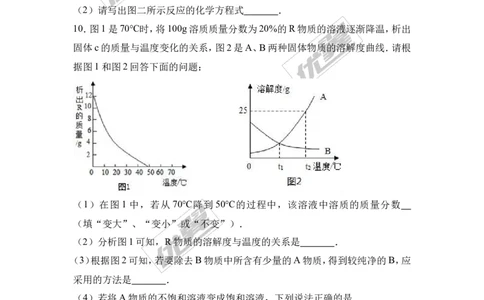
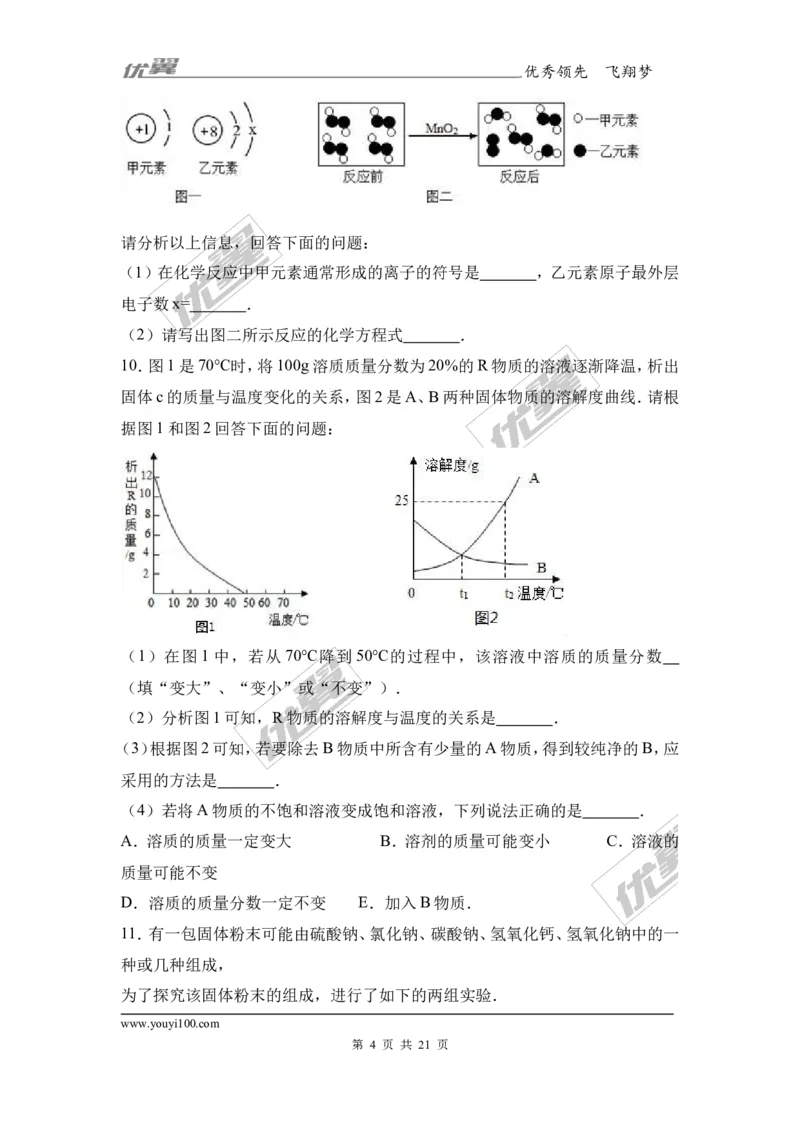
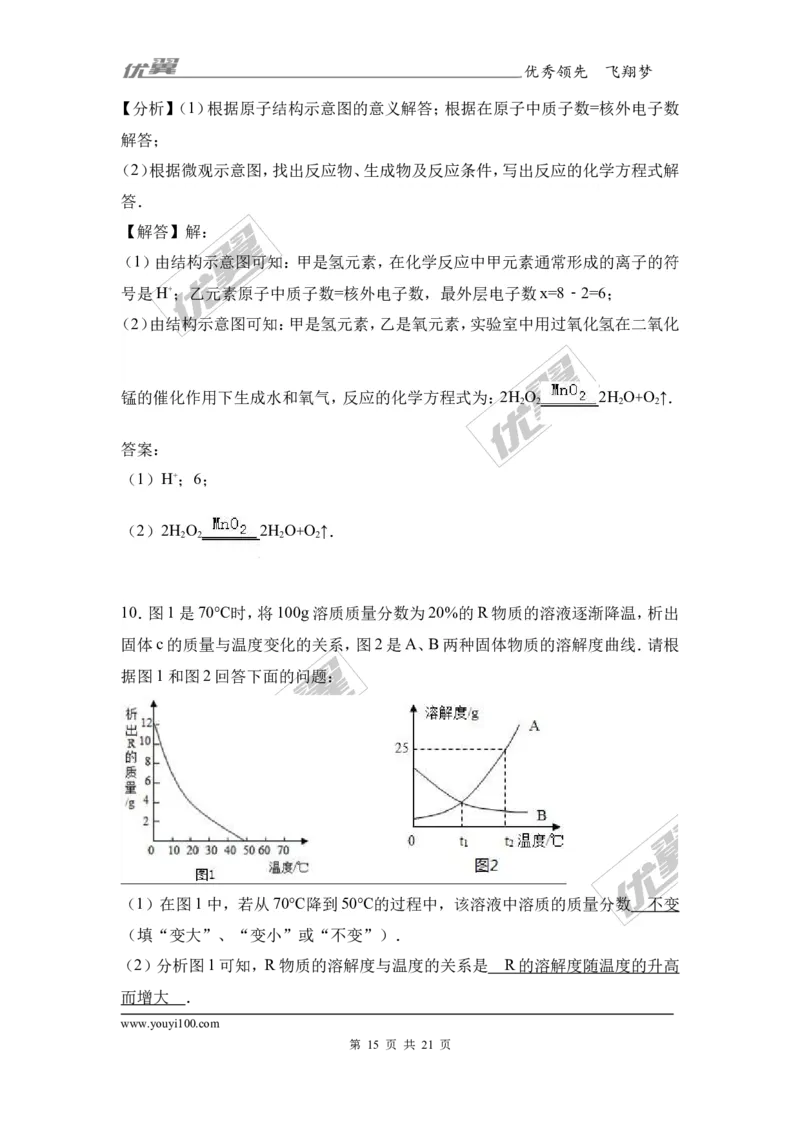
10.图1是70℃时,将100g溶质质量分数为20%的R物质的溶液逐渐降温,析出
固体c的质量与温度变化的关系,图2是A、B两种固体物质的溶解度曲线.请根
据图1和图2回答下面的问题:
(1)在图 1 中,若从 70℃降到 50℃的过程中,该溶液中溶质的质量分数
(填“变大”、“变小”或“不变”).
(2)分析图1可知,R物质的溶解度与温度的关系是 .
(3)根据图2可知,若要除去B物质中所含有少量的A物质,得到较纯净的B,应
采用的方法是 .
(4)若将A物质的不饱和溶液变成饱和溶液,下列说法正确的是 .
A.溶质的质量一定变大 B.溶剂的质量可能变小 C.溶液的
质量可能不变
D.溶质的质量分数一定不变 E.加入B物质.
11.有一包固体粉末可能由硫酸钠、氯化钠、碳酸钠、氢氧化钙、氢氧化钠中的一
种或几种组成,
为了探究该固体粉末的组成,进行了如下的两组实验.
www.youyi100.com
第 4 页 共 21 页优秀领先 飞翔梦
想
实验一:如图1.
实验二:
甲同学向白色沉淀B中加入稀硝酸,白色沉淀B的质量与加入稀硝酸的质量的
关系如图2所示;
乙同学,再向试管中滴入无色酚酞试液,溶液变红色.
根据以上实验,请回答下面的问题.
(1)该固体粉末中,一定存在的物质是 (填写化学式,下同),一定不存在
的物质是 .
(2)写出a、b段发生的化学反应方程式 .
(3)观察到a、c段发生的实验现象是 .
(4)通过上述实验仍无法判断的物质有 .要证明其是否存在,可采取的操
作是(若有多种物质,任选一种证明) .
12.工业铁红的主要成分是Fe O ,还含有少量的FeO、Fe O .为了测定铁红中铁
2 3 3 4
元素的质量分数,某兴
趣小组的同学在老师的指导下,用如下装置进行探究,整套装置气密性良好,反
应所需试剂均足量.
www.youyi100.com
第 5 页 共 21 页优秀领先 飞翔梦
想
【资料】I.草酸晶体(H C O •3H O)在浓硫酸作用下受热分解,化学方程式为:
2 2 4 2
H C O •3H O CO ↑+CO↑+4H O;
2 2 4 2 2 2
II.碱石灰是氧化钙和氢氧化钠的混合物.
请回答下列问题:
(1)装置A中装有 ,装置C的主要作用是 ;
(2)装置B的主要作用是 ;
(3)写出装置D中发生的主要化学反应方程式 ;
(4)称取铁红样品mg,用上述实验装置进行实验,若反应前后E装置质量增重了
ng,则此时铁红样品中铁元素的质量分数为 ;本实验中如果缺少C装置
(不考虑其它因素),则测得样品中铁的质量分数会 (填“偏小”、“不
变”或“偏大”).
(5)本实验装置的一个明显缺陷是 .
13.将1.80g氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶
液恰好完全反应,过滤后得
到溶质质量分数为20.0%的溶液5.85g.已知氯化铜与氢氧化钠溶液反应的化学
方程式为:
CuCl +2NaOH=Cu(OH) ↓+2NaCl.
2 2
求:(1)样品中氯化铜的质量;
(2)加入氢氧化钠溶液的质量.
www.youyi100.com
第 6 页 共 21 页优秀领先 飞翔梦
想
2017 年湖北省武汉市中考化学模拟试卷(五)
参考答案与试题解析
一、选择题(共8小题,每小题3分,满分24分)
1.下列变化中,不属于化学变化的是( )
A.葡萄酿酒 B.铁矿石炼铁 C.水结成冰 D.铁钉生锈
【考点】E3:化学变化和物理变化的判别.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、葡萄酿酒过程中有新物质酒精生成,属于化学变化;
B、铁矿石炼铁过程中有新物质生成,属于化学变化;
C、水结成冰过程中只是水的状态发生变化,没有新物质生成,属于物理变化.
D、铁钉生锈过程中有新物质铁锈生成,属于化学变化.
故选C.
2.下列实验操作错误的是( )
A. 浓硫酸稀释 B.
读取液体体积 C.
www.youyi100.com
第 7 页 共 21 页优秀领先 飞翔梦
想
滴加液体药品 D. 倾倒液体药品
【考点】4D:浓硫酸的性质及浓硫酸的稀释;42:测量容器﹣量筒;49:液体药品的
取用.
【分析】A、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判
断.
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
C、根据使用胶头滴管滴加少量液体的方法进行分析判断.
D、根据向试管中倾倒液体药品的方法进行分析判断.
【解答】解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒
不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正
确.
B、量取液体时,视线与液体的凹液面最低处保持水平,图中视线没有与液体的凹
液面最低处保持水平,操作错误.
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触
试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操
作正确.
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所
示操作正确.
故选:B.
3.化学与我们的日常生活有着密切的关系.下列有关说法或做法正确的是
( )
A.为治理空气污染,禁止使用化石燃料
B.二氧化碳灭火器原理是隔绝空气和提高可燃物的着火点
C.在金属表面刷油漆的目的是隔绝空气和水蒸气,防止金属腐蚀
www.youyi100.com
第 8 页 共 21 页优秀领先 飞翔梦
想
D.硬水中含有较多的可溶性钙和镁的化合物,所以,长期饮用硬水有益于身体健
康
【考点】8G:金属锈蚀的条件及其防护;65:防治空气污染的措施;77:硬水与软水;
H4:灭火的原理和方法.
【分析】A.根据禁止使用化石燃料是不现实的进行解答;
B.可燃物的着火点在一般情况下不能改变;
C.金属与水、氧气等物质同时接触时容易生锈;
D.根据硬水的危害来分析.
【解答】解:A.化石燃料是当今世界最重要的燃料,为治理空气污染,禁止使用化
石燃料是不现实的,故错误;
B.二氧化碳灭火器的灭火原理是:密度比空气大,不能燃烧,不支持燃烧,而着火
点不能改变,故错误;
C.在金属表面除油或刷漆的目的是隔绝氧气和水蒸气,防止腐蚀,故正确;
D.硬水中含有较多的可溶性钙镁化合物,长期饮用硬水会危害人体健康,故错误.
故选C.
4.对物质进行归类整理是化学学习的一种重要方法,下列归类关系不相符的是(
)
A.空气、海水﹣﹣纯净物
B.白磷、红磷﹣﹣可燃物
C.不锈钢、铜﹣﹣金属材料
D.合成橡胶、塑料﹣﹣有机合成材料
【考点】A5:纯净物和混合物的判别;89:金属材料及其应用;H1:燃烧与燃烧的条
件;I7:合成材料的使用及其对人和环境的影响.
【分析】A、根据纯净物与混合物的区别:是否由一种物质组成;B、能够燃烧的物
质属于可燃物;C、金属材料包括金属单质和合金;D、三大有机合成材料包括塑
料、合成纤维和合成橡胶.
【解答】解:空气中含有氧气、氮气、二氧化碳等物质,属于混合物;海水中含有水
氯化钠、氯化镁等物质,属于混合物,故A归类错误;
B、白磷、红磷都具有可燃性,属于可燃物,故B归类正确;
www.youyi100.com
第 9 页 共 21 页优秀领先 飞翔梦
想
C、不锈钢属于铁的合金,属于金属材料,铜属于金属单质也属于金属材料,故C
归类正确;
D、三大有机合成材料包括塑料、合成纤维和合成橡胶,故D归类正确.
故选A.
5.我国科学家屠呦呦因发现治疗疟疾的“青蒿素(C H O )”而获得诺贝尔奖.
15 22 5
青蒿素在氧气中完全燃烧
的化学方程式如下:aC H O +bO cCO +dH O,下列有关青蒿素的说法中
15 22 5 2 2 2
正确的是( )
A.青蒿素属于氧化物
B.青蒿素中C、H、O元素的质量比是9:11:4
C.青蒿素中所含氧元素的质量分数最小
D.青蒿素燃烧的化学方程式中,其化学计量数a、b、c、d分别是1、18、15、11
【考点】D1:化学式的书写及意义;A3:从组成上识别氧化物;D9:元素质量比的
计算;DA:元素的质量分数计算;G3:化学方程式的配平.
【分析】A.根据氧化物的概念来分析;
B.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分
析;
C.根据化合物中各元素的质量比来分析;
D.根据化学方程式的配平来分析.
【解答】解:A.根据氧化物的概念可知氧化物只有两种元素,且必须有氧元素.该
物质由三种元素组成,故错误;
B.青蒿素中C、H、O三种元素的质量比为(12×15):(1×22):(16×5)=90:11:
40,故错误;
C.青蒿素中C、H、0三种元素的质量比为(12×15):(1×22):(16×5)=90:11:
40,可见其中氢元素的质量分数最小,故错误;
D.青蒿素与氧气在点燃的条件下反应生成水和二氧化碳,化学方程式为:
www.youyi100.com
第 10 页 共 21 页优秀领先 飞翔梦
想
C H O +18O 15CO +11H O,故正确.
15 22 5 2 2 2
故选D.
6.A~I都是初中化学中常见的物质,已知,A是一种无色无味的气体,C是应用
最广泛的金属,I是建筑材料的主要成分,F是实验室常用的溶剂,它们的转化关
系如图所示,其它有关物质未列出.下列说法错误的是( )
A.向物质G的水溶液中滴入无色酚酞试液,溶液变红色
B.②和③的化学反应类型相同
C.反应②是吸热反应,反应④是放热反应
D.物质A和物质E都具有可燃性
【考点】AE:物质的鉴别、推断;FA:反应类型的判定.
【分析】本题属于推断题,根据题目给出的流程图和信息:已知,A是一种无色无
味的气体,C是应用最广泛的金属,I是建筑材料的主要成分,F是实验室常用的
溶剂,一氧化碳和氧化铁在高温下生成铁和二氧化碳,因此A是一氧化碳,B是
氧化铁,C是铁,D是二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和
水,因此I是碳酸钙;碳酸钙高温的条件下生成氧化钙和二氧化碳,因为H是氧化
钙;铁和硫酸反应生成硫酸亚铁和氢气,氢气和氧气在点燃的条件下生成水,因
此E是氢气,F是水;氧化钙和水反应生成氢氧化钙,因此G是氢氧化钙.
【解答】解:A、向物质G氢氧化钙的水溶液中滴入无色酚酞试液,溶液变红色,正
确但不符合题意,故选项错误;
B、②碳酸钙在高温的条件下生成氧化钙和二氧化碳,属于分解反应;③氢气和氧
气在点燃的条件下生成水,属于化合反应,②和③的化学反应类型相同错误,错
误符合题意,故选项正确;
www.youyi100.com
第 11 页 共 21 页优秀领先 飞翔梦
想
C、反应②碳酸钙高温的条件下生成氧化钙和二氧化碳,是吸热反应,反应④氧化
钙和水反应生成氢氧化钙,是放热反应正确,正确但不符合题意,故选项错误;
D、物质A一氧化碳和物质E氢气都具有可燃性,正确但不符合题意,故选项错误
故选B
7.向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得
溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
A.a点时,溶液中溶质为硝酸锌、硝酸铜、硝酸亚铁
B.b点时,所得固体只有银
C.c点时,溶液中一定有硝酸锌、硝酸亚铁,可能有硝酸铜
D.d点和e点所得固体均为银、铜、铁、锌
【考点】85:金属的化学性质.
【分析】加入锌粉后,锌先与硝酸银反应生成银和硝酸锌,溶液质量减少,锌把硝
酸银反应完,再与硝酸铜反应生成铜和硝酸锌,溶液质量增加,溶液质量增加的
幅度比较小,锌把硝酸铜反应完,再与硝酸亚铁反应生成铁和硝酸锌,溶液质量
增加,增加的幅度增大了,所以b点是锌和硝酸银恰好完全反应,bc段是锌和硝
酸铜反应,cd段是锌和硝酸亚铁反应,de段是锌过量.
【解答】解:A、b点是锌和硝酸银恰好完全反应,所以a点是锌与硝酸银反应了一
部分,所以溶液中溶质为没反应完的硝酸银,生成的硝酸锌和没有反应的硝酸铜
硝酸亚铁,故A错;
B、b点是锌和硝酸银恰好完全反应,锌与硝酸银反应生成银和硝酸锌,所以b点
时,所得固体只有银,故B正确;
C、bc段是锌和硝酸铜反应,c点时,锌和硝酸铜恰好完全反应,所以溶液中不存
在硝酸铜,故C错;
www.youyi100.com
第 12 页 共 21 页优秀领先 飞翔梦
想
D、d点是锌和硝酸亚铁恰好完全反应,所以固体中不含有锌,含有银、铜、铁;e点
所得固体为银、铜、铁、锌,故D错.
故选B.
8.已知钠、钾都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入
质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说
法错误的是( )
A.分析曲线得出钠、钾与水反应产生氢气的速率不同
B.参加反应的钠的质量等于钾的质量
C.反应后的溶液都能使无色的酚酞变红
D.反应后NaOH溶液的溶质质量分数小于KOH溶液的溶质质量分数
【考点】85:金属的化学性质.
【分析】由图可知两种金属产生的氢气的质量是相等的,根据金属活动性顺序和
反应的化学方程式计算出相关的量来解答此题.
【解答】解:A、在金属活动性顺序表中钾的活动性要大于钠,故钾反应的速度要
快,所消耗的时间要短.因此曲线b表示钠与水反应的图象,曲线a表示钾与水反
应的图象.故A说法正确;
B、由化学方程式:2Na+2H O═2NaOH+H ↑ 2K+2H O═2KOH+H ↑
2 2 2 2
46 36 80 2 78 36 112 2
可知:每产生2份质量的氢气需要消耗46份质量的钠和36份质量的水,同时产
生80份质量的氢氧化钠;同样每产生2份质量的氢气需要消耗78份质量的钾和
36份质量的水,同时产生112份质量的氢氧化钾.根据上图可知,二者产生的氢
气的质量是相等的,所以参加反应的钠的质量要小于参加反应的钾的质量,故B
说法错误;
C、钠与水反应生成氢氧化钠和氢气,氢氧化钠溶液属于碱,能使酚酞试液变红;
钾与水反应生成氢氧化钾和氢气,氢氧化钾溶液属于碱,能使酚酞试液变红,故C
www.youyi100.com
第 13 页 共 21 页优秀领先 飞翔梦
想
说法正确;
D、由化学方程式:2Na+2H O═2NaOH+H ↑ 2K+2H O═2KOH+H ↑
2 2 2 2
46 36 80 2 78 36 112 2
可知:每产生2份质量的氢气需要消耗46份质量的钠和36份质量的水,同时产
生80份质量的氢氧化钠;同样每产生2份质量的氢气需要消耗78份质量的钾和
36份质量的水,同时产生112份质量的氢氧化钾.根据上图可知,二者产生的氢
气的质量是相等的,所以参加反应的钠的质量要小于参加反应的钾的质量参加反
应的水的质量相等,同时生成的氢氧化钠的质量小于氢氧化钾的质量.根据公式
溶质的质量分数= ×100%,可知反应后NaOH溶液的溶质质量分数小
于KOH溶液的溶质质量分数,故D说法正确.
故选B.
二、非选择题:
9.图一是甲、乙两种元素的原子结构示意图.图二是实验室利用甲、乙两种元素
形成的一种化合物的溶
液制取某气体的微观示意图.
请分析以上信息,回答下面的问题:
(1)在化学反应中甲元素通常形成的离子的符号是 H + ,乙元素原子最外层电
子数x= 6 .
(2)请写出图二所示反应的化学方程式 2H O 2H O + O ↑ .
2 2 2 2
【考点】B8:原子结构示意图与离子结构示意图;B3:微粒观点及模型图的应用;
G5:书写化学方程式、.
www.youyi100.com
第 14 页 共 21 页优秀领先 飞翔梦
想
【分析】(1)根据原子结构示意图的意义解答;根据在原子中质子数=核外电子数
解答;
(2)根据微观示意图,找出反应物、生成物及反应条件,写出反应的化学方程式解
答.
【解答】解:
(1)由结构示意图可知:甲是氢元素,在化学反应中甲元素通常形成的离子的符
号是H+;乙元素原子中质子数=核外电子数,最外层电子数x=8﹣2=6;
(2)由结构示意图可知:甲是氢元素,乙是氧元素,实验室中用过氧化氢在二氧化
锰的催化作用下生成水和氧气,反应的化学方程式为:2H O 2H O+O ↑.
2 2 2 2
答案:
(1)H+;6;
(2)2H O 2H O+O ↑.
2 2 2 2
10.图1是70℃时,将100g溶质质量分数为20%的R物质的溶液逐渐降温,析出
固体c的质量与温度变化的关系,图2是A、B两种固体物质的溶解度曲线.请根
据图1和图2回答下面的问题:
(1)在图1中,若从70℃降到50℃的过程中,该溶液中溶质的质量分数 不变
(填“变大”、“变小”或“不变”).
(2)分析图1可知,R物质的溶解度与温度的关系是 R 的溶解度随温度的升高
而增大 .
www.youyi100.com
第 15 页 共 21 页优秀领先 飞翔梦
想
(3)根据图2可知,若要除去B物质中所含有少量的A物质,得到较纯净的B,应
采用的方法是 升高温度 .
(4)若将A物质的不饱和溶液变成饱和溶液,下列说法正确的是 BC .
A.溶质的质量一定变大 B.溶剂的质量可能变小 C.溶液的
质量可能不变
D.溶质的质量分数一定不变 E.加入B物质.
【考点】7N:固体溶解度曲线及其作用;4H:结晶的原理、方法及其应用;7J:饱和
溶液和不饱和溶液相互转变的方法;7R:溶质的质量分数.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和
溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从
而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:(1)由图象可以看出:从70℃降到50℃的过程中无固体析出,所以该
溶液中溶质的质量分数不变;
(2)由图象可知:温度越低,析出固体R的质量越多;由此可推出R的溶解度随温
度的升高而增大;
(3)B物质的溶解度随温度的升高而减小,所以若要除去B物质中所含有少量的
A物质,得到较纯净的B,应采用的方法是升高温度;
(4)将A物质的不饱和溶液变成饱和溶液,
A、降温的方法,溶质的质量不变,故错误;
B、蒸发溶剂的方法,溶剂的质量变小,故正确;
C、降温的方法,溶液的质量可能不变,故正确;
D、增加溶质的方法,溶质质量分数增大,故错误;
E、饱和溶液、不饱和溶液对应的是具体的溶质,加入B物质,不能将A物质的不
饱和溶液变成饱和溶液,故E错误.
故选:BC.
故答案为:(1)不变;
(2)R的溶解度随温度的升高而增大;
(3)升高温度;
www.youyi100.com
第 16 页 共 21 页优秀领先 飞翔梦
想
(4)BC.
11.有一包固体粉末可能由硫酸钠、氯化钠、碳酸钠、氢氧化钙、氢氧化钠中的一
种或几种组成,
为了探究该固体粉末的组成,进行了如下的两组实验.
实验一:如图1.
实验二:
甲同学向白色沉淀B中加入稀硝酸,白色沉淀B的质量与加入稀硝酸的质量的
关系如图2所示;
乙同学,再向试管中滴入无色酚酞试液,溶液变红色.
根据以上实验,请回答下面的问题.
(1)该固体粉末中,一定存在的物质是 N a SO 和 N a CO (填写化学式,下同),
2 4 2 3
一定不存在的物质是 C a ( OH ) .
2
(2)写出a、b段发生的化学反应方程式 BaCO + 2HNO =Ba ( NO ) + H O + CO ↑
3 3 3 2 2 2
.
(3)观察到a、c段发生的实验现象是 固体部分溶解,有气泡冒出 .
(4)通过上述实验仍无法判断的物质有 氯化钠和氢氧化钠 .要证明其是否存
在,可采取的操作是(若有多种物质,任选一种证明) 要证明氯化钠的存在:可
以向滤液 C 中滴加硝酸银溶液和稀硝酸,有白色沉淀生成,证明有氯化钠 .
【考点】AE:物质的鉴别、推断;G5:书写化学方程式、.
【分析】根据题目给出的流程图和信息:加足量的水溶解得溶液A,因此碳酸钠、
氢氧化钙不能共存;甲一定量的硝酸钡溶液,得到白色沉淀B,甲同学向白色沉淀
B中加入稀硝酸,白色沉淀B的质量先减小后不变,说明碳酸钡和硫酸钡都有,
www.youyi100.com
第 17 页 共 21 页优秀领先 飞翔梦
想
即该固体粉末中,一定有硫酸钠和碳酸钠,一定没有氢氧化钙;乙同学,再向试管
中滴入无色酚酞试液,溶液变红色,说明溶液显碱性,碳酸钠和氢氧化钠都显碱
性;图2中,ab段发生的化学反应是碳酸钡和硝酸反应生成硝酸钡和水和二氧化
碳,配平即可;观察到a、c段发生的实验现象是:固体部分溶解,有气泡冒出;通
过上述实验仍无法判断的物质有:氯化钠和氢氧化钠;要证明氯化钠的存在:可
以向滤液C中滴加硝酸银溶液和稀硝酸,有白色沉淀生成,证明有氯化钠.
【解答】解:(1)加足量的水溶解得溶液A,因此碳酸钠、氢氧化钙不能共存;甲一
定量的硝酸钡溶液,得到白色沉淀B,甲同学向白色沉淀B中加入稀硝酸,白色
沉淀B的质量先减小后不变,说明碳酸钡和硫酸钡都有,即该固体粉末中,一定
有硫酸钠和碳酸钠,一定没有氢氧化钙;故答案为:Na SO 和Na CO ;Ca(OH);
2 4 2 3 2
(2)图2中,ab段发生的化学反应是碳酸钡和硝酸反应生成硝酸钡和水和二氧化
碳,配平即可;故答案为:BaCO +2HNO =Ba(NO ) +H O+CO ↑;
3 3 3 2 2 2
(3)观察到a、c段发生的实验现象是:固体部分溶解,有气泡冒出;故答案为:固
体部分溶解,有气泡冒出;
(4)通过上述实验仍无法判断的物质有:氯化钠和氢氧化钠;要证明氯化钠的存
在:可以向滤液C中滴加硝酸银溶液和稀硝酸,有白色沉淀生成,证明有氯化钠;
故答案为:氯化钠和氢氧化钠;
12.工业铁红的主要成分是Fe O ,还含有少量的FeO、Fe O .为了测定铁红中铁
2 3 3 4
元素的质量分数,某兴趣小组的同学在老师的指导下,用如下装置进行探究,整
套装置气密性良好,反应所需试剂均足量.
【资料】I.草酸晶体(H C O •3H O)在浓硫酸作用下受热分解,化学方程式为:
2 2 4 2
www.youyi100.com
第 18 页 共 21 页优秀领先 飞翔梦
想
H C O •3H O CO ↑+CO↑+4H O;
2 2 4 2 2 2
II.碱石灰是氧化钙和氢氧化钠的混合物.
请回答下列问题:
(1)装置A中装有 氢氧化钠溶液 ,装置C的主要作用是 吸收水蒸气 ;
(2)装置B的主要作用是 检验二氧化碳是否被氢氧化钠溶液完全吸收 ;
(3)写出装置D中发生的主要化学反应方程式 F e O + 3CO 2Fe + 3CO ;
2 3 2
(4)称取铁红样品mg,用上述实验装置进行实验,若反应前后E装置质量增重了
ng,则此时铁红样品中铁元素的质量分数为 % ;本实验中如果缺
少C装置(不考虑其它因素),则测得样品中铁的质量分数会 偏小 (填“偏
小”、“不变”或“偏大”).
(5)本实验装置的一个明显缺陷是 没有处理尾气 .
【考点】34:化学实验方案设计与评价;4Q:常见气体的检验与除杂方法;6U:一氧
化碳的化学性质;G5:书写化学方程式、.
【分析】(1)装置A中装有氢氧化钠溶液,用来除去混合气体中的二氧化碳;
装置C的主要作用是吸收水蒸气;
(2)装置B的主要作用是检验二氧化碳是否被氢氧化钠溶液完全吸收;
(3)装置D中发生的主要化学反应是:高温条件下,氧化铁和一氧化碳反应生成
铁和二氧化碳;
(4)根据反应的化学方程式及其提供的数据可以进行相关方面的计算;
(5)一氧化碳有毒,扩散到空气中污染环境.
【解答】解:(1)装置A中装有氢氧化钠溶液,装置C的主要作用是吸收水蒸气.
故填:氢氧化钠溶液;吸收水蒸气.
(2)装置B的主要作用是检验二氧化碳是否被氢氧化钠溶液完全吸收.
故填:检验二氧化碳是否被氢氧化钠溶液完全吸收.
(3)装置D中发生的主要化学反应是:高温条件下,氧化铁和一氧化碳反应生成
www.youyi100.com
第 19 页 共 21 页优秀领先 飞翔梦
想
铁和二氧化碳,反应的化学性方程式为:Fe O +3CO 2Fe+3CO .
2 3 2
故填:Fe O +3CO 2Fe+3CO .
2 3 2
(4)氧化铁、氧化亚铁、四氧化三铁和一氧化碳反应的化学方程式为:
Fe O +3CO 2Fe+3CO , FeO+CO Fe+CO , Fe O +4CO
2 3 2 2 3 4
3Fe+4CO ,
2
由反应的化学方程式可知,反应生成的二氧化碳中,氧元素一半来自于铁的氧化
物,因此铁红样品中氧元素质量为:ng× × = ng,
铁红样品中铁元素质量为:mg﹣ ng= g,
则此时铁红样品中铁元素的质量分数为:( g÷mg)×100%=
%,
本实验中如果缺少C装置,会导致测定的二氧化碳质量偏大,从而导致测得样品
中铁的质量分数偏小.
故填: %;偏小.
(5)本实验装置的一个明显缺陷是没有处理尾气.
故填:没有处理尾气.
13.将1.80g氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶
液恰好完全反应,过滤后得
到溶质质量分数为20.0%的溶液5.85g.已知氯化铜与氢氧化钠溶液反应的化学
www.youyi100.com
第 20 页 共 21 页优秀领先 飞翔梦
想
方程式为:
CuCl +2NaOH=Cu(OH) ↓+2NaCl.
2 2
求:(1)样品中氯化铜的质量;
(2)加入氢氧化钠溶液的质量.
【考点】G6:根据化学反应方程式的计算.
【分析】氯化铜与一定量的氢氧化钠溶液恰好完全反应,所得溶液为氯化钠溶液,
根据得到溶溶质质量分数为20.0%的溶液5.85g,计算出反应生成氯化钠的质量,
根据反应的化学方程式,由氯化钠的质量可计算样品中氯化铜的质量及所消耗氢
氧化钠溶液中氢氧化钠的质量和生成氢氧化铜的质量,及一步求解样品中氯化铜
的质量和加入氢氧化钠溶液的质量.
【解答】解:NaCl的质量为5.85g×20.0%=1.17g
设样品中CuCl 的质量为x;NaOH溶液中含NaOH质量为y,生成氢氧化铜的质
2
量为z,
CuCl +2NaOH═Cu(OH) ↓+2NaCl
2 2
135 80 98 117
x y z 1.17g
x=1.35g,y=0.80g,z=0.98g
样品中CuCl 的质量分数为 =75%
2
(2)NaOH溶液的质量为:5.85g+0.98g﹣1.35g=5.48g,
故答案为:(1)样品中CuCl 的质量分数为75%;
2
(2)NaOH溶液的质量为5.48g.
www.youyi100.com
第 21 页 共 21 页