文档内容
化学方程式
【考纲要求】
1.认识质量守恒定律,能说明化学反应中的质量关系。
2.能正确书写简单的化学方程式。
3.能根据化学反应方程式进行简单的计算
4.认识定量研究对于化学科学发展的重大作用。
【命题趋势】
本单元内容是化学学科的核心内容,是中考化学必考的主干知识,质量守恒
定律要求能利用定律说明常见化学反应的质量关系,能用粒子观点对该定律作出
解释;化学方程式之一考点要求能正确书写化学方程式,并能准确从化学方程式
中获取相关信息;根据化学方程式的简单计算更加注重与日常生活,工农业生产
的联系,以数据处理型为主,更加注重同学们对图表、数据、信息、实验综合分析
的考查;题型涉及选择题、填空题、探究题和计算题。
【考点精析】
一.选择题
1.煤油中含有噻吩(用X表示),噻吩令人不愉快的气味,其燃烧时发生反应的化
学方程式表示为:X+6O 4CO +SO +2H O,则噻吩的化学式为( )
2 2 2 2
A.C H SB.C H SC.C H S D.C H S
4 6 4 4 4 4 2 8 8
【考点】G1:质量守恒定律及其应用.
【分析】根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前各原
子的数目之和等于反应后各原子的数目之和,据此可推断X的化学式.
【解答】解:反应后生成物中,共有4个碳原子、1个硫原子、12个氧原子、4个氢原
子,根据质量守恒定律,反应前物质中原子的种类和数目不变,X+6O 中已有12
2
个氧原子,则1个X分子中含有4个碳原子、1个硫原子、4个氢原子,所以X化学
式是C H S.
4 4
故选:B.
2.FeCl 溶液常用于蚀刻印刷电路,反应原理为aFeCl +bCu═cCuCl +dX.向含溶质
3 3 2
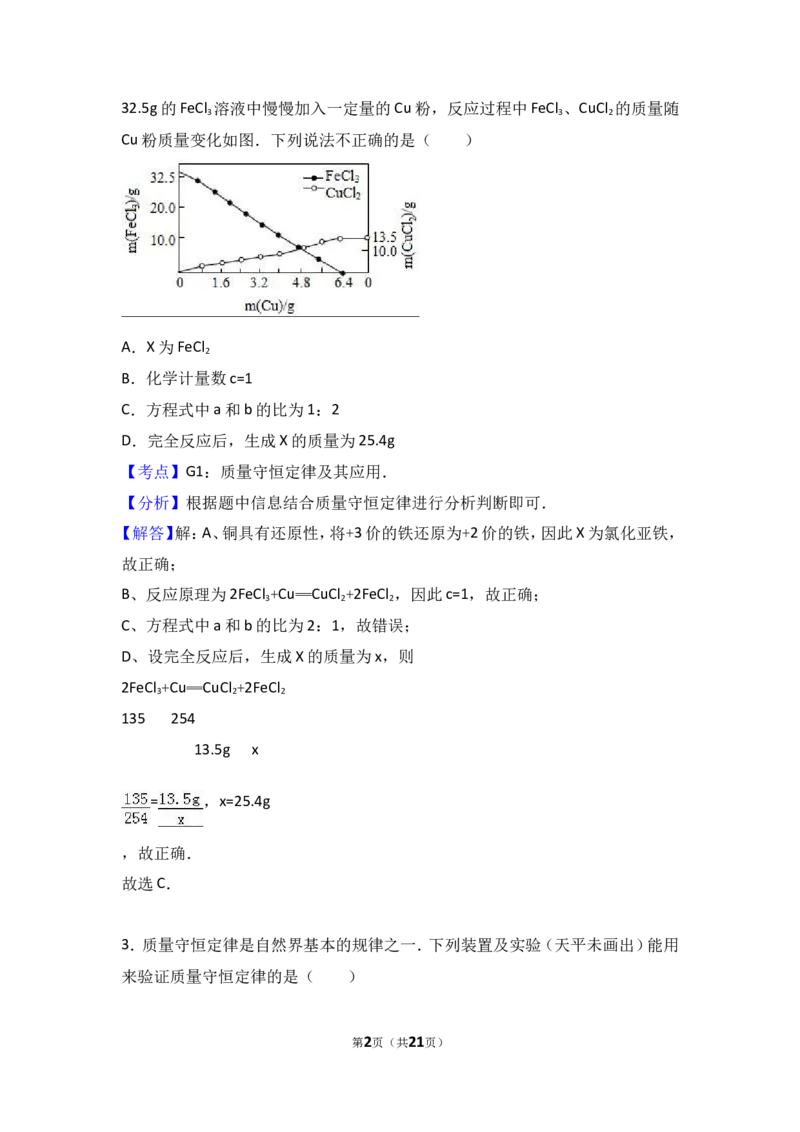
第1页(共21页)32.5g的FeCl 溶液中慢慢加入一定量的Cu粉,反应过程中FeCl 、CuCl 的质量随
3 3 2
Cu粉质量变化如图.下列说法不正确的是( )
A.X为FeCl
2
B.化学计量数c=1
C.方程式中a和b的比为1:2
D.完全反应后,生成X的质量为25.4g
【考点】G1:质量守恒定律及其应用.
【分析】根据题中信息结合质量守恒定律进行分析判断即可.
【解答】解:A、铜具有还原性,将+3价的铁还原为+2价的铁,因此X为氯化亚铁,
故正确;
B、反应原理为2FeCl +Cu═CuCl +2FeCl ,因此c=1,故正确;
3 2 2
C、方程式中a和b的比为2:1,故错误;
D、设完全反应后,生成X的质量为x,则
2FeCl +Cu═CuCl +2FeCl
3 2 2
135 254
13.5g x
= ,x=25.4g
,故正确.
故选C.
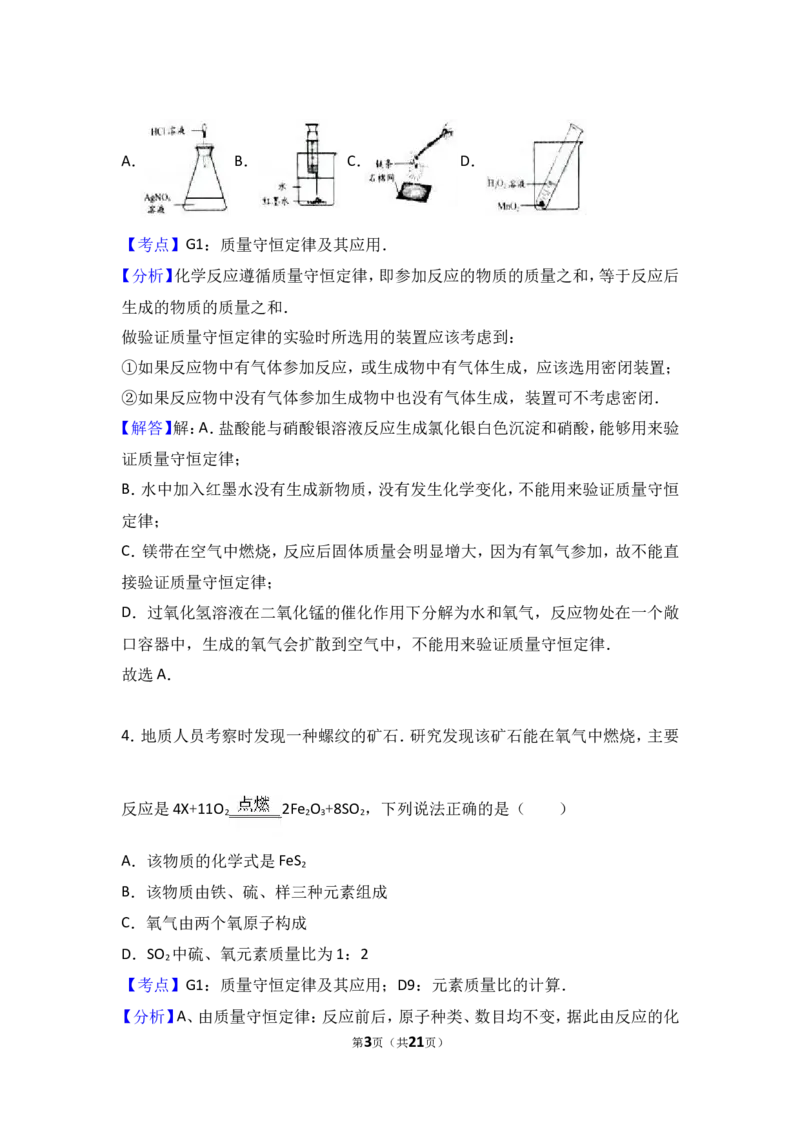
3.质量守恒定律是自然界基本的规律之一.下列装置及实验(天平未画出)能用
来验证质量守恒定律的是( )
第2页(共21页)A. B. C. D.
【考点】G1:质量守恒定律及其应用.
【分析】化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后
生成的物质的质量之和.
做验证质量守恒定律的实验时所选用的装置应该考虑到:
①如果反应物中有气体参加反应,或生成物中有气体生成,应该选用密闭装置;
②如果反应物中没有气体参加生成物中也没有气体生成,装置可不考虑密闭.
【解答】解:A.盐酸能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,能够用来验
证质量守恒定律;
B.水中加入红墨水没有生成新物质,没有发生化学变化,不能用来验证质量守恒
定律;
C.镁带在空气中燃烧,反应后固体质量会明显增大,因为有氧气参加,故不能直
接验证质量守恒定律;
D.过氧化氢溶液在二氧化锰的催化作用下分解为水和氧气,反应物处在一个敞
口容器中,生成的氧气会扩散到空气中,不能用来验证质量守恒定律.
故选A.
4.地质人员考察时发现一种螺纹的矿石.研究发现该矿石能在氧气中燃烧,主要
反应是4X+11O 2Fe O +8SO ,下列说法正确的是( )
2 2 3 2
A.该物质的化学式是FeS
2
B.该物质由铁、硫、样三种元素组成
C.氧气由两个氧原子构成
D.SO 中硫、氧元素质量比为1:2
2
【考点】G1:质量守恒定律及其应用;D9:元素质量比的计算.
【分析】A、由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化
第3页(共21页)学方程式推断反应物X的化学式;
B、根据物质的化学式可知其元素组成;
C、氧气由氧元素组成;
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分
析判断.
【解答】解:A、由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学
方程式4X+11O 2Fe O +8SO ,反应前氧原子个数为22,反应后的生成物中
2 2 3 2
铁、氧、硫原子个数分别为4、22、8,根据反应前后原子种类、数目不变,则,4X分
子中含有4个铁原子和8个硫原子,则每个X分子由1个铁原子和2个硫原子构
成,则物质X的化学式为FeS ,故选项说法正确;
2
B、该物质由铁、硫两种元素组成,错误;
C、氧气由氧元素组成,错误;
D、SO 中的硫、氧元素的质量比为32:(16×2)=1:1,错误.
2
故选A
5.在一密闭容器中发生某反应,容器中各物质的质量变化如表所示,其中未知数
据正确的是( )
阶段/物质 甲的质量/g 乙的质量/g 丙的质量/g 丁的质量/g
反应前 40 40 0 0
反应中 M M M 10.8
1 2 3
反应后 23 M 30 27
4
A.m =30.8 B.m =24 C.m =13.6 D.m =34
1 2 3 4
【考点】G1:质量守恒定律及其应用.
【分析】根据质量守恒定律可得出m 的值,然后根据反应中各物质的质量比进行
4
分析解答即可.
【解答】解:A、由质量守恒定律,m =40+40﹣23﹣30﹣27=0,由反应前与反应中甲
4
丁的质量关系,则(40﹣23)g:27g=(40﹣m )g:10.8g,解得m =33.2,故选项说法
1 1
错误.
第4页(共21页)B、由反应前与反应中乙、丁的质量关系,则40g:27g=(40﹣m )g:10.8g,解得
2
m =24,故选项说法正确.
2
C、由反应前与反应中丙丁的质量关系,则30g:27g=m :10.8g,解得m =12,故选
3 3
项说法错误.
D、由质量守恒定律,m =40+40﹣23﹣30﹣27=0,故选项说法错误.
4
故选:B.
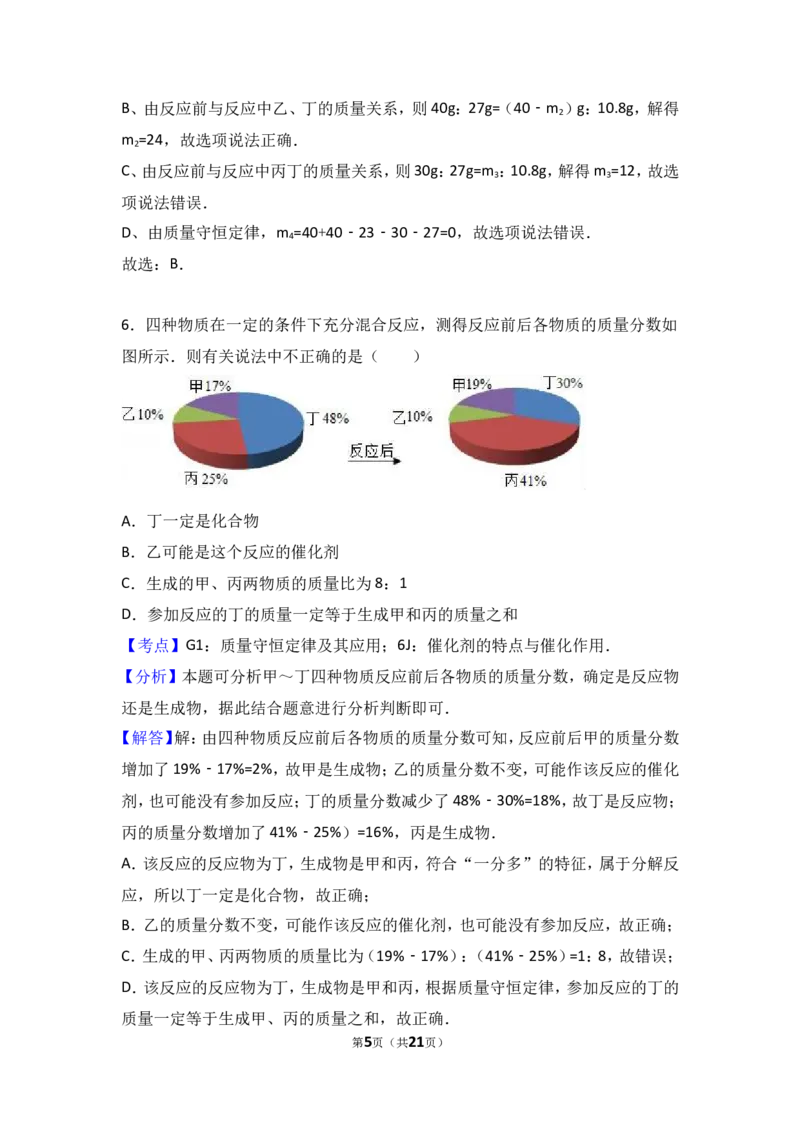
6.四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如
图所示.则有关说法中不正确的是( )
A.丁一定是化合物
B.乙可能是这个反应的催化剂
C.生成的甲、丙两物质的质量比为8:1
D.参加反应的丁的质量一定等于生成甲和丙的质量之和
【考点】G1:质量守恒定律及其应用;6J:催化剂的特点与催化作用.
【分析】本题可分析甲~丁四种物质反应前后各物质的质量分数,确定是反应物
还是生成物,据此结合题意进行分析判断即可.
【解答】解:由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数
增加了19%﹣17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化
剂,也可能没有参加反应;丁的质量分数减少了48%﹣30%=18%,故丁是反应物;
丙的质量分数增加了41%﹣25%)=16%,丙是生成物.
A.该反应的反应物为丁,生成物是甲和丙,符合“一分多”的特征,属于分解反
应,所以丁一定是化合物,故正确;
B.乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,故正确;
C.生成的甲、丙两物质的质量比为(19%﹣17%):(41%﹣25%)=1:8,故错误;
D.该反应的反应物为丁,生成物是甲和丙,根据质量守恒定律,参加反应的丁的
质量一定等于生成甲、丙的质量之和,故正确.
第5页(共21页)故选:C.
二.填空题(共4小题)
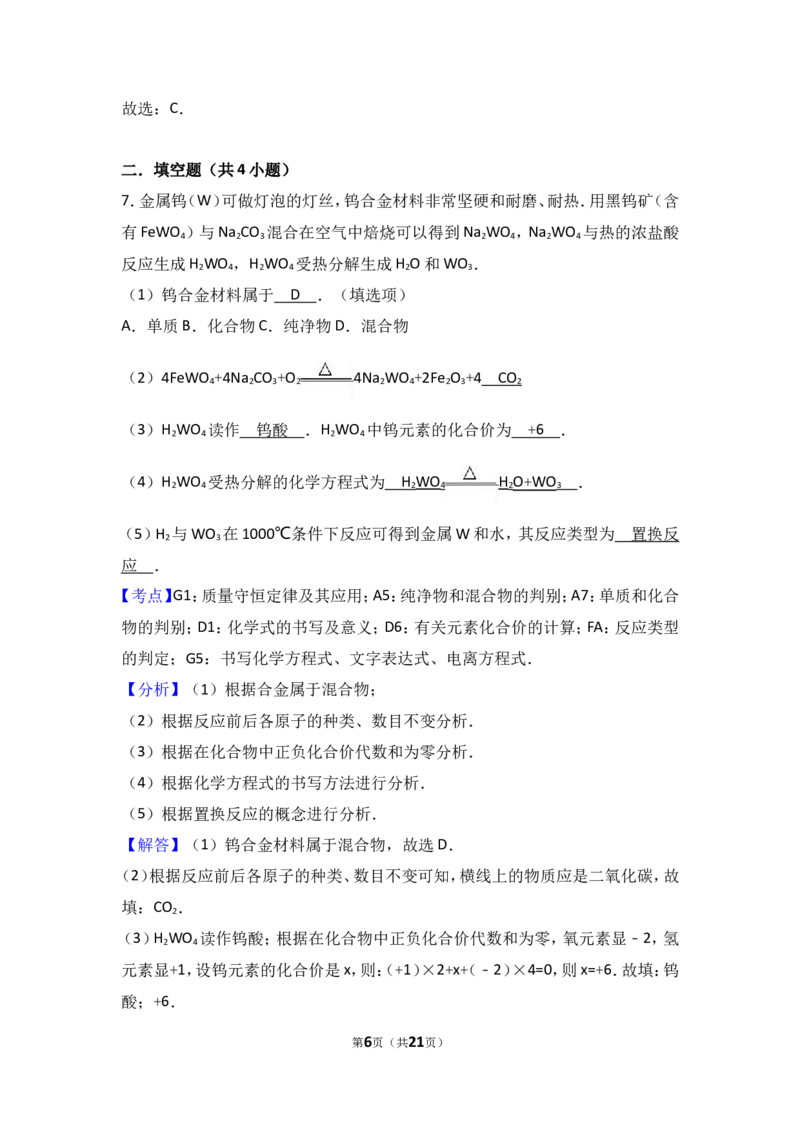
7.金属钨(W)可做灯泡的灯丝,钨合金材料非常坚硬和耐磨、耐热.用黑钨矿(含
有FeWO )与Na CO 混合在空气中焙烧可以得到Na WO ,Na WO 与热的浓盐酸
4 2 3 2 4 2 4
反应生成H WO ,H WO 受热分解生成H O和WO .
2 4 2 4 2 3
(1)钨合金材料属于 D .(填选项)
A.单质B.化合物C.纯净物D.混合物
(2)4FeWO +4Na CO +O 4Na WO +2Fe O +4 CO
4 2 3 2 2 4 2 3 2
(3)H WO 读作 钨酸 .H WO 中钨元素的化合价为 + 6 .
2 4 2 4
(4)H WO 受热分解的化学方程式为 H WO H O + WO .
2 4 2 4 2 3
(5)H 与WO 在1000℃条件下反应可得到金属W和水,其反应类型为 置换反
2 3
应 .
【考点】G1:质量守恒定律及其应用;A5:纯净物和混合物的判别;A7:单质和化合
物的判别;D1:化学式的书写及意义;D6:有关元素化合价的计算;FA:反应类型
的判定;G5:书写化学方程式、文字表达式、电离方程式.
【分析】(1)根据合金属于混合物;
(2)根据反应前后各原子的种类、数目不变分析.
(3)根据在化合物中正负化合价代数和为零分析.
(4)根据化学方程式的书写方法进行分析.
(5)根据置换反应的概念进行分析.
【解答】(1)钨合金材料属于混合物,故选D.
(2)根据反应前后各原子的种类、数目不变可知,横线上的物质应是二氧化碳,故
填:CO .
2
(3)H WO 读作钨酸;根据在化合物中正负化合价代数和为零,氧元素显﹣2,氢
2 4
元素显+1,设钨元素的化合价是x,则:(+1)×2+x+(﹣2)×4=0,则x=+6.故填:钨
酸;+6.
第6页(共21页)(4)H WO 受热分解生成H O和WO ,H WO 受热分解的化学方程式为H WO
2 4 2 3 2 4 2 4
H O+WO .故填:H WO H O+WO .
2 3 2 4 2 3
(5)H 与WO 在1000℃条件下反应可得到金属W和水,反应物是一种单质和一
2 3
种化合物,生成物也是一种单质和化合物,该反应属于置换反应,故填:置换反应
8.2017年5月18 日,我国首次在南海海域试采可燃冰成功,消息传出,举世关注.
可燃冰外观似冰,主要含有的是甲烷水合物.请写出甲烷完全燃烧的化学方程式
CH + 2O CO + 2H O .
4 2 2 2
【考点】G5:书写化学方程式、文字表达式、电离方程式.
【分析】甲烷在点燃条件下燃烧生成二氧化碳和水,写出反应的化学方程式即可.
【解答】解:甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为
CH +2O CO +2H O.
4 2 2 2
故答案为:CH +2O CO +2H O.
4 2 2 2
9.硝酸可发生反应:4HNO 4NO ↑+X+2H O.据此回答:
3 2 2
(1)反应的基本类型属于 分解 反应.
(2)X的化学式为 O ,推断的依据为 质量守恒定律 .
2
(3)硝酸的保存应注意 避光 、 低温 .
第7页(共21页)【考点】G1:质量守恒定律及其应用;E4:化学性质与物理性质的差别及应用;FA:
反应类型的判定.
【分析】(1)反应类型有四个:化合反应、分解反应、置换反应和复分解反应.置换
反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的化学反应;
化合反应是多变一;分解反应是一变多;复分解反应是两种化合物互相交换成分
生成另外两种化合物.4HNO ═4NO ↑+X↑+2H O是一变多,属于分解反应;
3 2 2
(2)根据质量守恒定律解答;
(3)硝酸的保存应注意:低温、避光保存.
【解答】解:
(1)根据4HNO ═4NO ↑+X↑+2H O是“一变多”,属于分解反应;
3 2 2
(2)根据质量守恒定律和4HNO ═4NO ↑+X↑+2H O,可知:反应前后原子的种类,
3 2 2
原子的数目,原子的质量都不变,
反应前有氢原子4个,氮原子4个,氧原子12个,反应后有氮原子4个,氢原子4
个,氧原子10个,因此X含有两个氧原子是氧气;
(3)硝酸见光和受热易分解,因此应注意:低温、避光保存;故答案为:避光;低温
故答案为:
(1)分解;
(2)O ;质量守恒定律;
2
(3)避光,低温.
10.(1)某物质在空气中完全燃烧,生成CO 和H O,则该物质中一定含有 C 、 H
2 2
元素(填元素符号).
(2)烹饪鱼时通常将鱼煎过后,再加少许食醋和酒,这是因为它们可以反应生成
具有特殊香味的乙酸乙酯(化学式为C H O ),每个乙酸乙酯分子是由 1 4 个
4 8 2
原子构成的,乙酸乙酯的相对分子质量是 8 8 ;在乙酸乙酯中碳元素和氧元素
的最简质量比是 3 : 2 ;17.6g乙酸乙酯中所含氧元素的质量为 6. 4 g.
【考点】G1:质量守恒定律及其应用;D8:相对分子质量的概念及其计算;D9:元素
质量比的计算;DB:化合物中某元素的质量计算.
【分析】(1)根据质量守恒定律,反应前后元素种类不变,结合题意进行分析解答.
(2)根据每个乙酸乙酯分子的构成、相对分子质量为构成分子的各原子的相对原
第8页(共21页)子质量之和,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,
化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
【解答】解:(1)某物质在空气中完全燃烧,生成CO 和H O,CO 和H O中含有碳、
2 2 2 2
氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,则该物质中一定
含有碳、氢两种元素(群殴元素符号分别是C、H),可能含有氧元素.
(2)1个乙酸乙酯分子由4个碳原子、8个氢原子和2个氧原子构成的,则每个乙
酸乙酯分子是由14个原子构成.
乙酸乙酯的相对分子量为12×4+8+16×2=88;在乙酸乙酯中碳元素和氧元素的
最简质量比是(12×4):(16×2)=3:2;17.6g乙酸乙酯中所含氧元素的质量为
17.6g× 100%=6.4g.
故答案为:(1)C、H;(2)14,88;3:2;6.4.
三.实验探究题(共3小题)
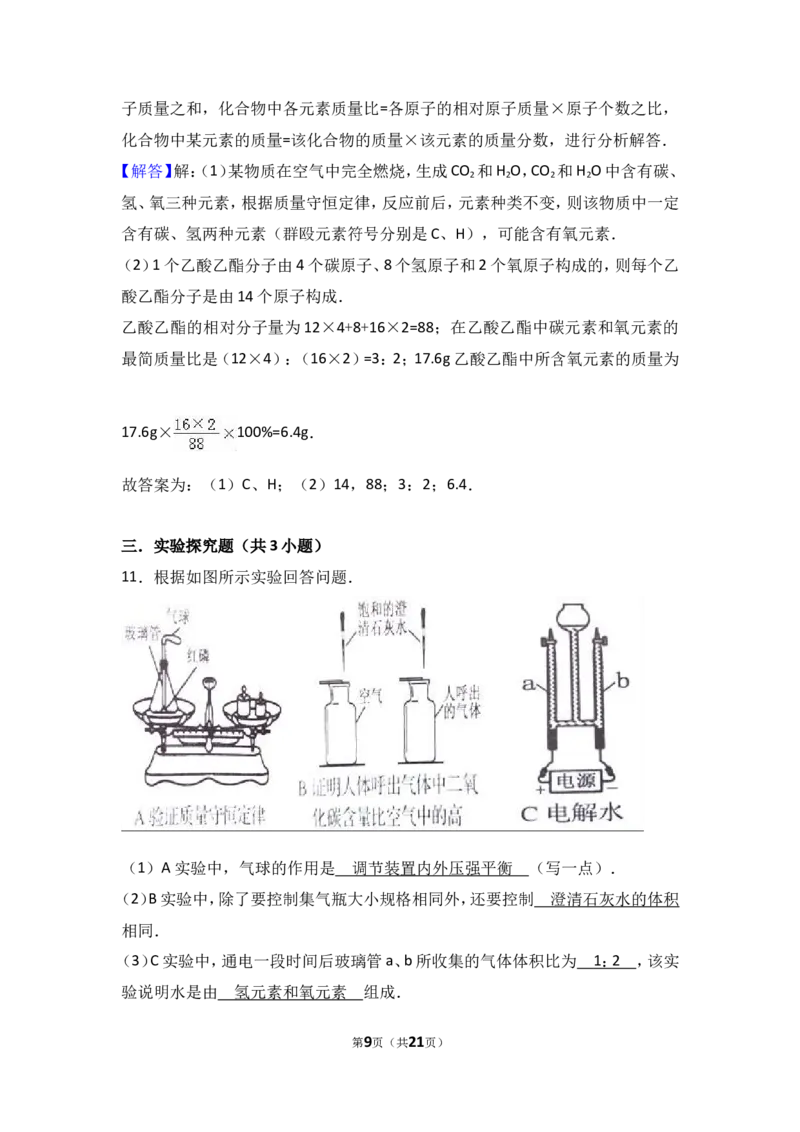
11.根据如图所示实验回答问题.
(1)A实验中,气球的作用是 调节装置内外压强平衡 (写一点).
(2)B实验中,除了要控制集气瓶大小规格相同外,还要控制 澄清石灰水的体积
相同.
(3)C实验中,通电一段时间后玻璃管a、b所收集的气体体积比为 1 : 2 ,该实
验说明水是由 氢元素和氧元素 组成.
第9页(共21页)【考点】G1:质量守恒定律及其应用;56:吸入空气与呼出气体的比较;71:电解水
实验.
【分析】(1)根据验证质量守恒定律实验注意事项来分析;
(2)根据控制变量的实验方法进行分析;
(3)根据电解水实验进行分析.
【解答】解:(1)验证质量守恒定律实验中,气球的作用是调节装置内外压强平衡;
(2)探究人体呼出气体中二氧化碳含量比空气中的高时,实验条件除了要控制两
个盛装气体样品的集气瓶大小规格相同外,还要控制滴加的饱和石灰水的体积相
同;故填:澄清石灰水的体积;
(3)据图可以知道,b试管与电源负极相连,生成气体是氢气,a试管有电源正极
相连,生成气体时氧气,氧气和氢气的体积比是1:2,氢气由氢元素组成,氧气有
氧元素组成,该实验说明水是由氢元素和氧元素组成的.
故填:(1)调节装置内外压强平衡;(2)澄清石灰水的体积;(3)1:2;氢元素和氧
元素.
12.实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数已模糊不清
小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
⑧将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克.
请根据上述实验回答:(相关反应的化学方程式为:KCl+AgNO ═AgCl↓+KNO )
3 3
(1)在过滤操作中使用的玻璃仪器有:烧杯、 漏斗 和玻璃棒.
(2)样品中氯化钾的质量分数为多少?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是多少克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小
于计算得出的理论值.造成这种结果的原因可能是 BC . (选填编号)
A.晶体没有干燥 B.蒸发时液体飞溅 C.硝酸钾残留在玻璃棒上.
【考点】G6:根据化学反应方程式的计算;4G:过滤的原理、方法及其应用.
【分析】过滤需要的玻璃仪器有玻璃棒、漏斗和烧杯;
根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
第10页(共21页)【解答】解:(1)在过滤操作中使用的玻璃仪器有:烧杯、漏斗和玻璃棒.
故填:漏斗.
(2)设氯化钾质量为x,生成硝酸钾质量为y,
KCl+AgNO ═AgCl↓+KNO ,
3 3
74.5 143.5 101
x 14.35g y
= = ,
x=7.45g,y=10.1g,
样品中氯化钾的质量分数为: ×100%=74.5%,
答:样品中氯化钾的质量分数为74.5%.
(3)完全反应后,混合液中的硝酸钾质量是:10g﹣7.45g+10.1g=12.65g,
答:完全反应后,混合液中的硝酸钾质量是12.65g.
(4)A.晶体没有干燥会导致结果偏大;
B.蒸发时液体飞溅会导致结果偏小;
C.硝酸钾残留在玻璃棒上会导致结果偏小.
故选:BC.
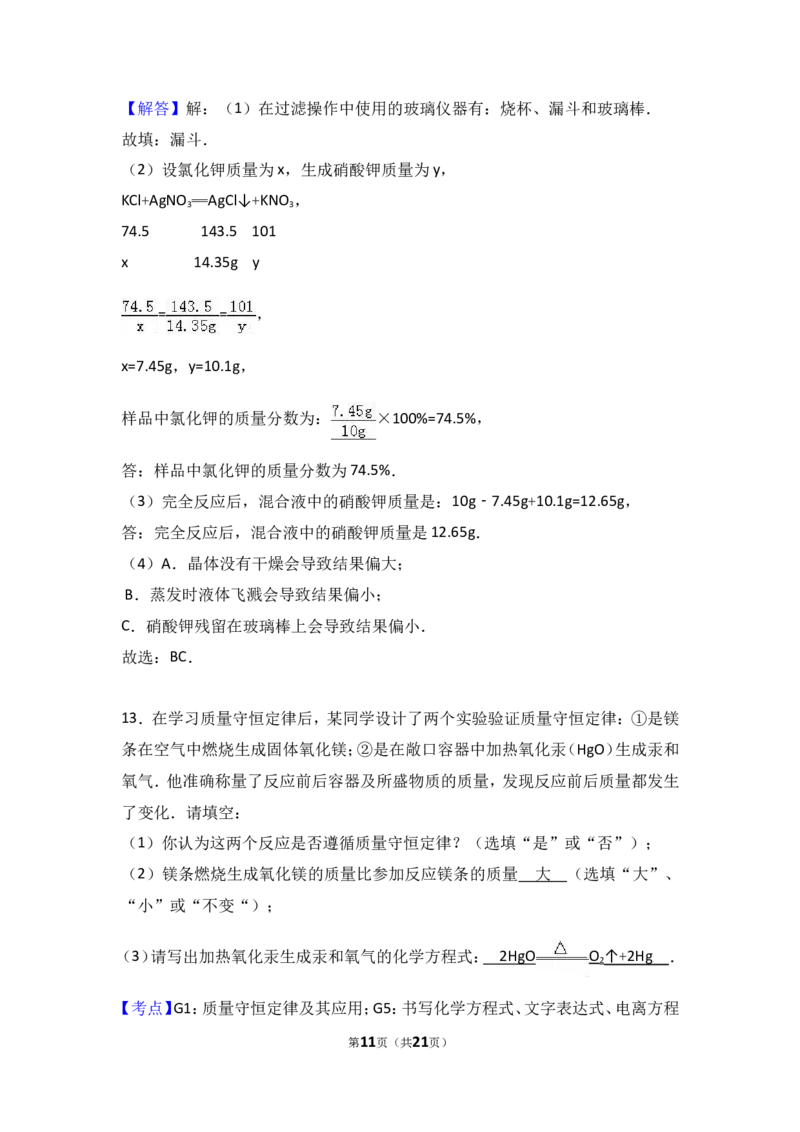
13.在学习质量守恒定律后,某同学设计了两个实验验证质量守恒定律:①是镁
条在空气中燃烧生成固体氧化镁;②是在敞口容器中加热氧化汞(HgO)生成汞和
氧气.他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生
了变化.请填空:
(1)你认为这两个反应是否遵循质量守恒定律?(选填“是”或“否”);
(2)镁条燃烧生成氧化镁的质量比参加反应镁条的质量 大 (选填“大”、
“小”或“不变“);
(3)请写出加热氧化汞生成汞和氧气的化学方程式: 2HgO O ↑ + 2Hg .
2
【考点】G1:质量守恒定律及其应用;G5:书写化学方程式、文字表达式、电离方程
第11页(共21页)式.
【分析】化学反应遵循质量守恒定律,即参加化学反应的物质质量之和,一定等于
反应后生成的各种物质质量之和;
【解答】解:(1)这两个反应都遵循质量守恒定律.
故填:是.
(2)因为镁燃烧时和空气中的氧气反应,因此生成氧化镁的质量比参加反应镁条
的质量大.
故填:大.
(3)氧化汞在加热的条件下生成汞和氧气,故答案为:2HgO O ↑+2Hg;故
2
答案为:2HgO O ↑+2Hg;
2
四.计算题(共1小题)
14.醋的主要成分是醋酸,其化学式为CH COOH,醋不仅是调味品,而且还有较强
3
的灭菌、抑毒的作用.
小明为判断家中的米醋含酸量是否合格,取100mL米醋(见标签)于锥形瓶中,然
后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加
入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩余物质的质量进
行了记录,测得的部分数据如下,请根据有关信息回答问题(提示:化学方程式为
CH COOH+NaHCO ═CH COONa+H O+CO ↑)
3 3 3 2 2
加入碳酸氢钠溶液质量(g) 25 50 100 155 175
锥形瓶内剩余物质质量(g) 123.9 147.8 195.6 248.4 m
(1)醋酸中碳、氢、氧三种元素的质量比为 6 : 1 : 8 .
(2)100mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为 6. 6 g,表中
m的数值为 268.4 .
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)
第12页(共21页)【考点】G6:根据化学反应方程式的计算;D9:元素质量比的计算.
【分析】(1)一个醋酸CH COOH分子中含有2个C,4个H,2个O,求出相对质量
3
比即为醋酸中C、H、O元素的质量比.
(2)根据表中数据分析加入加入碳酸氢钠溶液质量155g时,醋酸已完全反应,根
据质量守恒定律即可解答;
(3)根据生成二氧化碳的质量,结合化学方程式即可解答.
【解答】解:(1)醋酸CH COOH中碳、氢、氧元素三种元素的质量比为(12×2):
3
(1×4):(16×2)=6:1:8;
(2)由图示可知米醋的密度是1g/mL,故100mL米醋即为100g;
表中数据分析可知每加入25g碳酸氢钠溶液最多生成二氧化碳质量是:100g+25g
﹣123.9g=1.1g;
加入加入碳酸氢钠溶液质量 155g 时,生成二氧化碳质量是:100g+155g﹣
248.4g=6.6g,说明醋酸已完全反应,故m的值就是175g+100g﹣6.6g=268.4g;
(3)设100mL米醋中醋酸的质量为x;
CH COOH+NaHCO ═CH COONa+H O+CO ↑
3 3 3 2 2
60 44
x 6.6g
x=9g
因为100mL米醋含酸量9g,故该产品含酸量合格.
答案:(1)6:1:8;
(2)6.6;268.4;
第13页(共21页)(3)该产品含酸量合格.
五.推断题(共1小题)
15.质量守恒定律的发现对化学的发展做出了重要贡献.
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定
律的是 ③ (填数字序号).
①食盐和水 ②氯化钠溶液和硝酸钾溶液 ③铁和氯化铜溶液
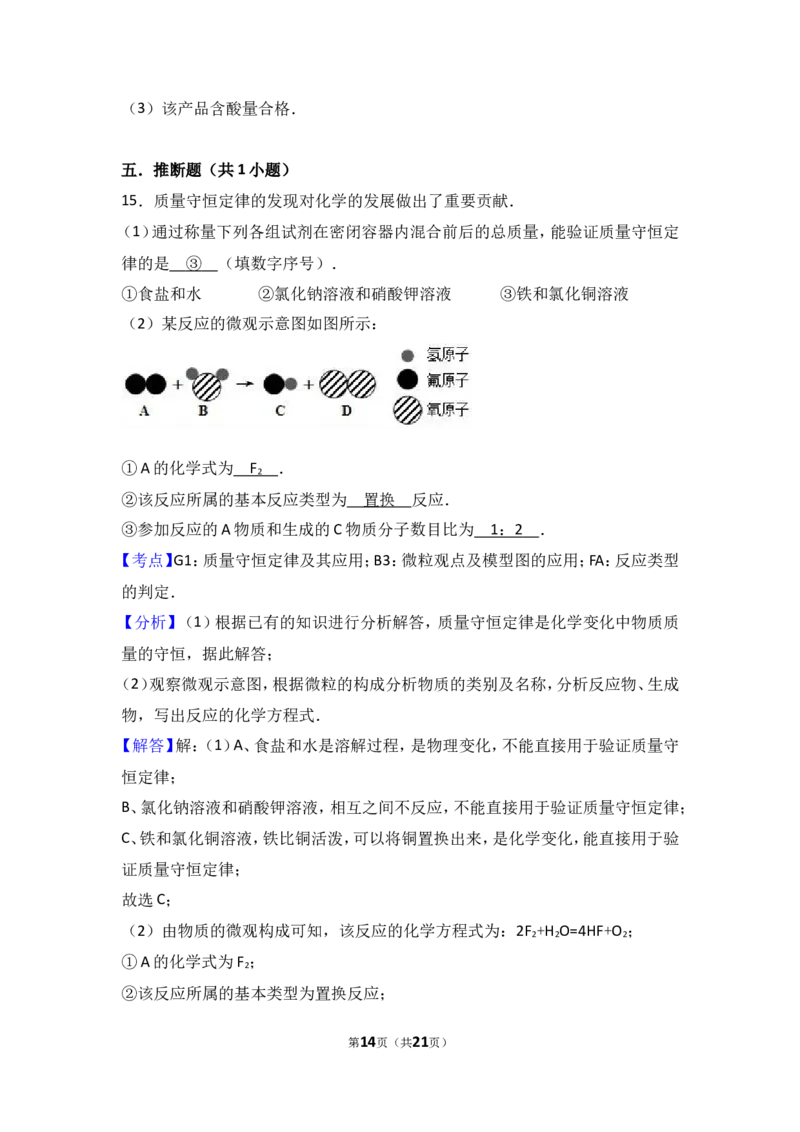
(2)某反应的微观示意图如图所示:
①A的化学式为 F .
2
②该反应所属的基本反应类型为 置换 反应.
③参加反应的A物质和生成的C物质分子数目比为 1 : 2 .
【考点】G1:质量守恒定律及其应用;B3:微粒观点及模型图的应用;FA:反应类型
的判定.
【分析】(1)根据已有的知识进行分析解答,质量守恒定律是化学变化中物质质
量的守恒,据此解答;
(2)观察微观示意图,根据微粒的构成分析物质的类别及名称,分析反应物、生成
物,写出反应的化学方程式.
【解答】解:(1)A、食盐和水是溶解过程,是物理变化,不能直接用于验证质量守
恒定律;
B、氯化钠溶液和硝酸钾溶液,相互之间不反应,不能直接用于验证质量守恒定律;
C、铁和氯化铜溶液,铁比铜活泼,可以将铜置换出来,是化学变化,能直接用于验
证质量守恒定律;
故选C;
(2)由物质的微观构成可知,该反应的化学方程式为:2F +H O=4HF+O ;
2 2 2
①A的化学式为F ;
2
②该反应所属的基本类型为置换反应;
第14页(共21页)③参加反应的A物质和生成的C物质分子数目比为:2:4=1:2.
故答案为:(1)③
(2)①F ;
2
②置换;
③1:2
六.解答题(共4小题)
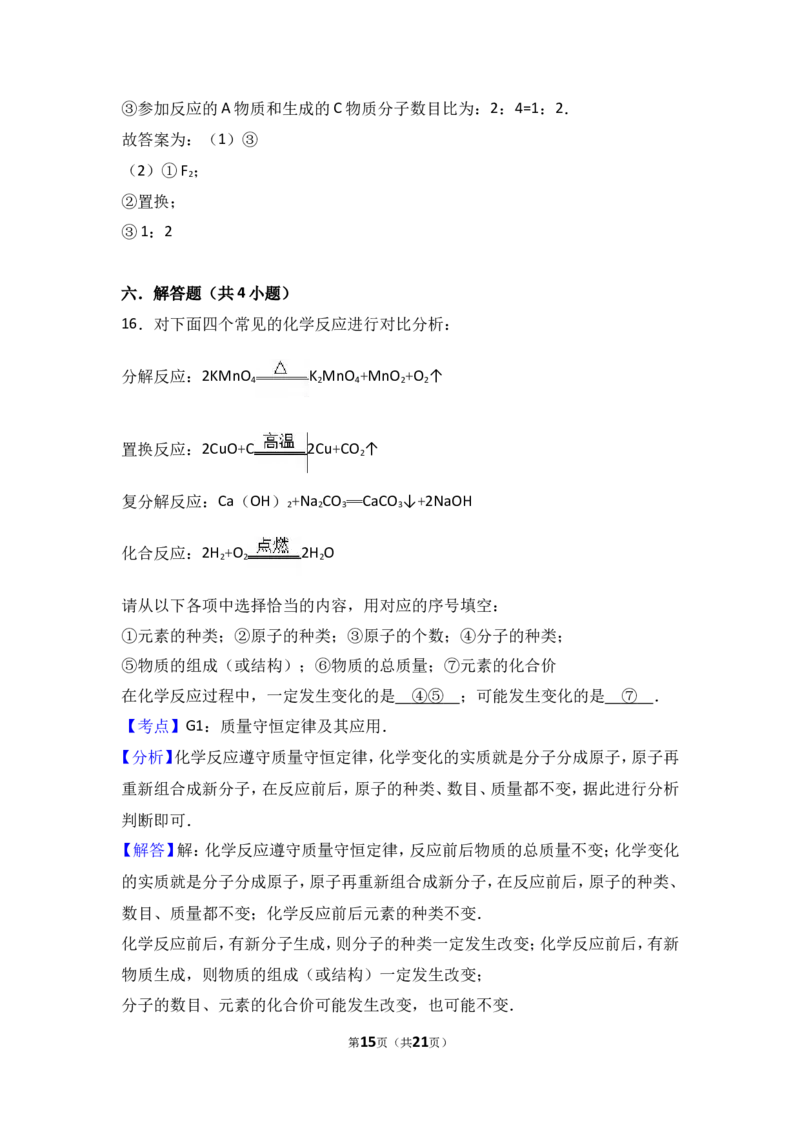
16.对下面四个常见的化学反应进行对比分析:
分解反应:2KMnO K MnO +MnO +O ↑
4 2 4 2 2
置换反应:2CuO+C 2Cu+CO ↑
2
复分解反应:Ca(OH) +Na CO ═CaCO ↓+2NaOH
2 2 3 3
化合反应:2H +O 2H O
2 2 2
请从以下各项中选择恰当的内容,用对应的序号填空:
①元素的种类;②原子的种类;③原子的个数;④分子的种类;
⑤物质的组成(或结构);⑥物质的总质量;⑦元素的化合价
在化学反应过程中,一定发生变化的是 ④⑤ ;可能发生变化的是 ⑦ .
【考点】G1:质量守恒定律及其应用.
【分析】化学反应遵守质量守恒定律,化学变化的实质就是分子分成原子,原子再
重新组合成新分子,在反应前后,原子的种类、数目、质量都不变,据此进行分析
判断即可.
【解答】解:化学反应遵守质量守恒定律,反应前后物质的总质量不变;化学变化
的实质就是分子分成原子,原子再重新组合成新分子,在反应前后,原子的种类、
数目、质量都不变;化学反应前后元素的种类不变.
化学反应前后,有新分子生成,则分子的种类一定发生改变;化学反应前后,有新
物质生成,则物质的组成(或结构)一定发生改变;
分子的数目、元素的化合价可能发生改变,也可能不变.
第15页(共21页)故填:④⑤;⑦.
17.小金进行如图所示实验来验证质量守恒定律.在实验中用电子天平和量筒准
确测量出表中m 、m 、m 、m 和V.(实验中操作正确.O 的密度为ρg/cm3)
1 2 3 4 2
实验序号 1 2 …
m (MnO )/g
1 2
m (KClO )/g
2 3
m (试管)/g
3
m (试管+加热后剩余固
4
体)/g
量筒内收集气体的体积V/c
m3
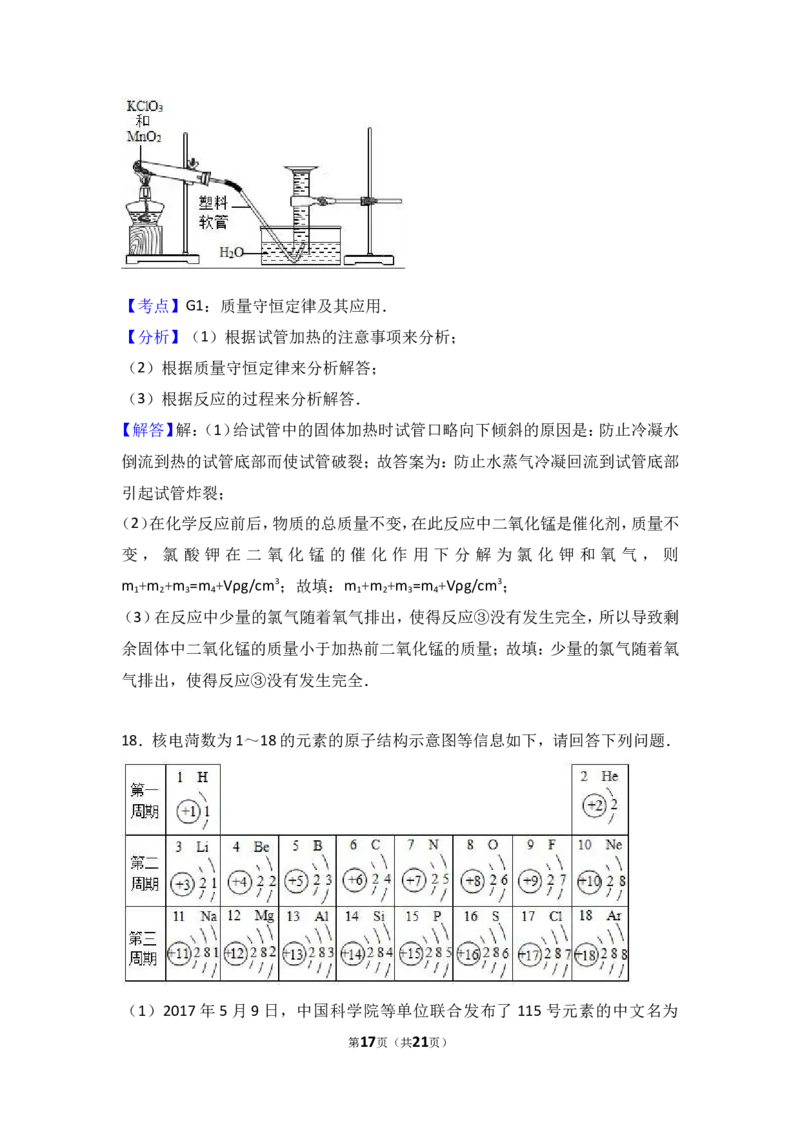
(1)装置中试管口略向下倾斜的原因是 防止水蒸气冷凝回流到试管底部引起
试管炸裂 .
(2)根据质量守恒定律,m 、m 、m 、m 和 V 之间应存在的等量关系为
1 2 3 4
m + m + m =m + Vρg/cm 3 .
1 2 3 4
(3)每次实验结束后,小金在拆卸装置时总能闻到刺激性气味.他将加热后剩余
固体中的 MnO 分离并测量其质量.发现总小于加热前MnO 的质量,查阅资料
2 2
后发现,一般认为加热KC1O ,和MnO 混合物的反应过程如下:
3 2
第1步:2MnO +2KC1O 2KMnO +Cl ↑+O ↑;(其中Cl 有刺激性气味)
2 3 4 2 2 2
第 2 步 2KMnO K MnO +MnO +O ↑:
4 2 4 2 2
第3 步:K MnO +Cl 2KCl+MnO +O ↑.
2 4 2 2 2
写出加热后剩余固体中MnO 质量小于加热前MnO 质量的原因 少量的氯气随
2 2
着氧气排出,使得反应 ③ 没有发生完全 .
第16页(共21页)【考点】G1:质量守恒定律及其应用.
【分析】(1)根据试管加热的注意事项来分析;
(2)根据质量守恒定律来分析解答;
(3)根据反应的过程来分析解答.
【解答】解:(1)给试管中的固体加热时试管口略向下倾斜的原因是:防止冷凝水
倒流到热的试管底部而使试管破裂;故答案为:防止水蒸气冷凝回流到试管底部
引起试管炸裂;
(2)在化学反应前后,物质的总质量不变,在此反应中二氧化锰是催化剂,质量不
变 , 氯 酸 钾 在 二 氧 化 锰 的 催 化 作 用 下 分 解 为 氯 化 钾 和 氧 气 , 则
m +m +m =m +Vρg/cm3;故填:m +m +m =m +Vρg/cm3;
1 2 3 4 1 2 3 4
(3)在反应中少量的氯气随着氧气排出,使得反应③没有发生完全,所以导致剩
余固体中二氧化锰的质量小于加热前二氧化锰的质量;故填:少量的氯气随着氧
气排出,使得反应③没有发生完全.
18.核电菏数为1~18的元素的原子结构示意图等信息如下,请回答下列问题.
(1)2017年5月9日,中国科学院等单位联合发布了 115号元素的中文名为
第17页(共21页)“镆”.此元素原子的核电荷数为 11 5 ,核外电子数为 11 5 .
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
依次增多 .
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化
学式各一个,并标出所写化学式中氮元素的化合价:单质 、氧化物 O 、
2
酸 H O 或者 H O 、碱 H •H O 或者 H OH 、盐 H HCO .
2 3 3 2 4 4 3
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层 7 个电子,容易得到一个电子.结构决定性质. .
(5)国产C919大型客机上使用了大量的铝合金.工业上用电解氧化铝(Al O )得
2 3
到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(写出计算过
程)
【考点】G6:根据化学反应方程式的计算;B8:原子结构示意图与离子结构示意图;
C5:元素周期表的特点及其应用.
【分析】(1)在元素的相关数据中,元素序数=原子的核电荷数=原子的核外电子
数.
(2)周期表中,同一周期,随着原子序数的递增,元素原子核外电子排布的变化规
律是 依次增多.
(3)注意化合价与化学式的一一对应和答案的不唯一.
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层7个电子,容易得到一个电子.结构决定性质..
(5)根据反应物的质量和对应的化学方程式求算生成物铝的质量.
【解答】解:
(1)“镆”为115号元素,根据元素序数=原子的核电荷数=原子的核外电子数,
可知此元素原子的核电荷数为 115,核外电子数为 115.
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
依次增多.
第18页(共21页)(3)注意物质的分类,同时要注意根据化合价书写对应化学式,本题答案有的不
是唯一的.单质 、氧化物 O(不唯一)、酸 H O 或者H O 、碱 H •H O或
2 2 3 3 2
者 H OH、盐 H HCO (不唯一).
4 4 3
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层7个电子,容易得到一个电子.结构决定性质..
(5)设电解102t氧化铝最多能生成铝的质量为x
2Al O 4Al+3O ↑
2 3 2
204 108
102t x
=
x=54t
故答案为:
(1)115,115.
(2)依次增多.
(3)(唯一); O(不唯一,化学式和化合价对应即可); H O 或者H O ;
2 2 3
H •H O或者 H OH; H HCO (不唯一).
3 2 4 4 3
(4)钠原子最外层一个电子,容易失去一个电子.而氯原子最外层7个电子,容易
得到一个电子.结构决定性质..
(5)54t
第19页(共21页)19.二氧化氯(ClO )在生产、生活中具有广泛应用.
2
(1)ClO 可用于工业制备高效氧化剂、漂白剂亚氯酸钠(NaClO ).
2 2
①ClO 中氯元素的化合价为 + 4 .
2
②工业生产NaClO 的主要反应的化学方程式为2ClO +2X Cl +2NaClO ,其
2 2 2 2
中X的化学式为 NaC l .
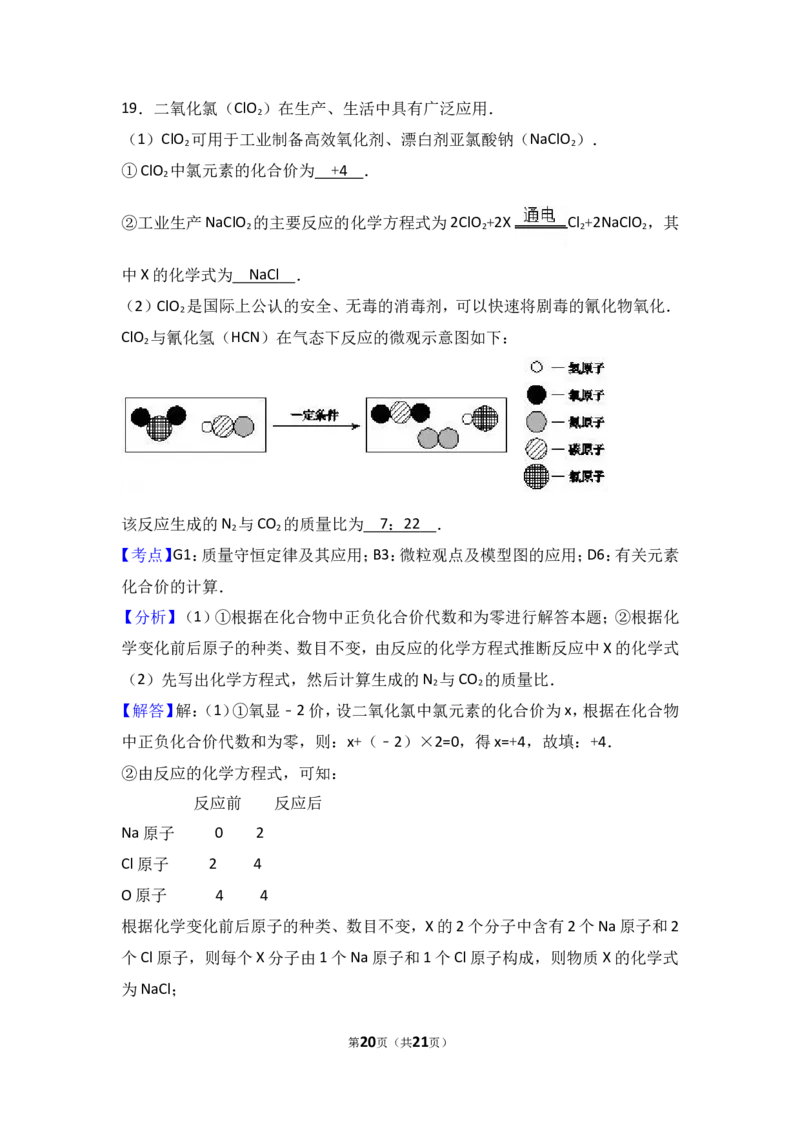
(2)ClO 是国际上公认的安全、无毒的消毒剂,可以快速将剧毒的氰化物氧化.
2
ClO 与氰化氢(HCN)在气态下反应的微观示意图如下:
2
该反应生成的N 与CO 的质量比为 7 : 2 2 .
2 2
【考点】G1:质量守恒定律及其应用;B3:微粒观点及模型图的应用;D6:有关元素
化合价的计算.
【分析】(1)①根据在化合物中正负化合价代数和为零进行解答本题;②根据化
学变化前后原子的种类、数目不变,由反应的化学方程式推断反应中X的化学式
(2)先写出化学方程式,然后计算生成的N 与CO 的质量比.
2 2
【解答】解:(1)①氧显﹣2价,设二氧化氯中氯元素的化合价为x,根据在化合物
中正负化合价代数和为零,则:x+(﹣2)×2=0,得x=+4,故填:+4.
②由反应的化学方程式,可知:
反应前 反应后
Na原子 0 2
Cl原子 2 4
O原子 4 4
根据化学变化前后原子的种类、数目不变,X的2个分子中含有2个Na原子和2
个Cl原子,则每个X分子由1个Na原子和1个Cl原子构成,则物质X的化学式
为NaCl;
第20页(共21页)(2)HClO 与氰化氢(HCN)在气态下反应的方程式是2ClO +2HCN
2 2
N +2CO +2HCl,该反应生成的N 与CO 的质量比为28:(44×2)=7:22:.
2 2 2 2
故答案为:(1)①+4; ②NaCl;(2)7:22.
第21页(共21页)