文档内容
第二节 氮及其化合物
第一课时 氮的氧化物
[明确学习目标] 1.了解氮气的性质及固氮方法。2.认识一氧化氮、二氧化
氮的性质,熟知氮的氧化物溶于水反应的化学方程式。
学生自主学习
氮气与氮的固定
1.氮气无色、无味、不溶于水,约占空气体积的。通常情况下,化学性质
很稳定,与其他物质难以反应。在放电或高温下,与氧气反应的化学方程式为
□N +O =====2NO。
2 2
N 与镁、氢气反应的方程式分别是:□N +3Mg=====Mg N ;□N +
2 2 3 2 2
3H ((((2NH 。
2 3
2.氮的固定
(1)定义:使 □ 游离态 的氮转化为 □ 氮的化合物 的过程。
(2)类别
一氧化氮与二氧化氮
1.一氧化氮是 □ 无 色、无味、不溶于水的有毒气体,与氧气反应的化学方程
式为□2NO+O ===2NO 。
2 2
2.二氧化氮是 □ 红棕 色、有 □ 刺激性 气味的有毒气体,易液化, □ 易溶 于水,
与水反应的化学方程式为□3NO +H O===2HNO +NO,工业上利用这一原理生
2 2 3
产 □ 硝酸 。
[特别提醒] (1)实验室里收集NO气体是用排水集气法而不能用排空气法。(2)检验NO气体的方法是向气体中通入O (或空气),气体由无色变为红棕色。
2
1.实验室能否用排空气法收集NO气体?能否用排水法收集NO ?为什么?
2
提示:不能。NO与空气的密度十分接近且易与空气中的O 反应,故不能用
2
排空气法收集,一般用排水法收集;NO 易与H O发生反应,故不能用排水法收
2 2
集,一般用向上排空气法收集。
2.如何除去NO气体中混有的少量NO 气体杂质?
2
提示:根据NO 与H O反应能生成NO,既能除去NO 杂质,又不引入其他
2 2 2
杂质,故可将混合气体通入盛有水的洗气瓶,然后重新收集气体。
课堂互动探究
氮的氧化物与水反应的实验探究
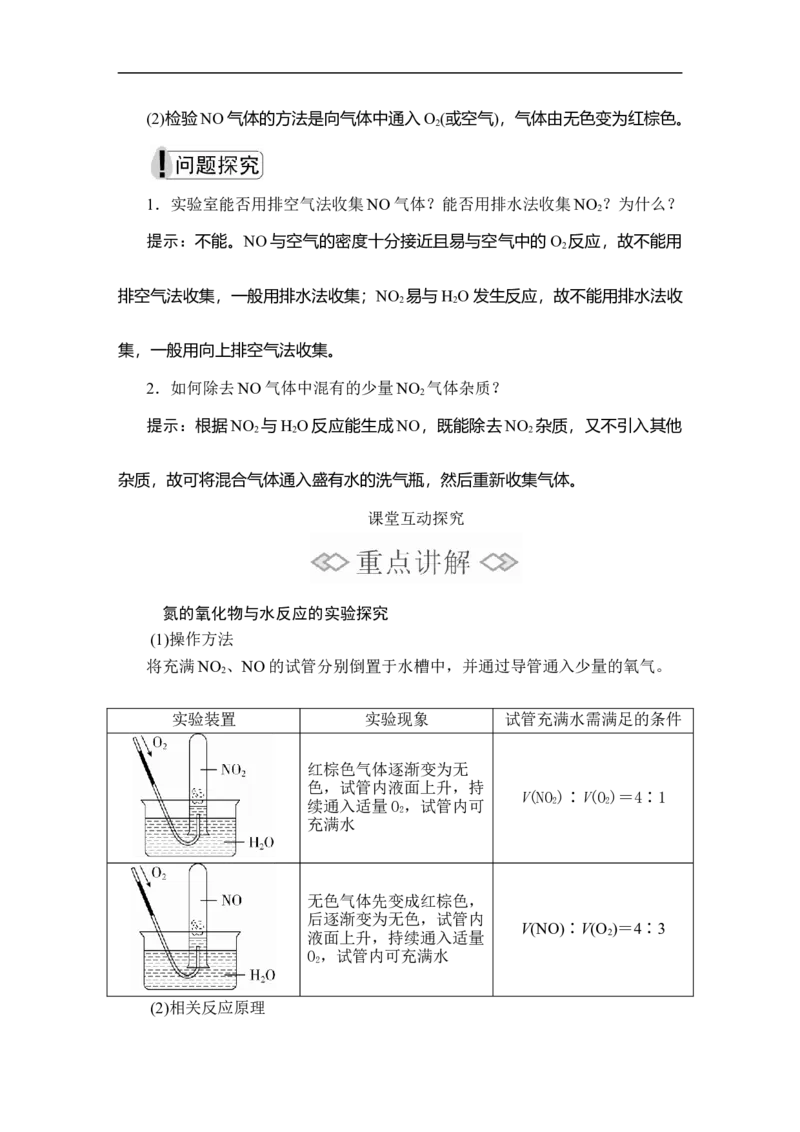
(1)操作方法
将充满NO 、NO的试管分别倒置于水槽中,并通过导管通入少量的氧气。
2
实验装置 实验现象 试管充满水需满足的条件
红棕色气体逐渐变为无
色,试管内液面上升,持
V(NO )∶V(O )=4∶1
续通入适量O ,试管内可 2 2
2
充满水
无色气体先变成红棕色,
后逐渐变为无色,试管内
V(NO)∶V(O )=4∶3
液面上升,持续通入适量 2
O ,试管内可充满水
2
(2)相关反应原理3NO +H O===2HNO +NO①
2 2 3
2NO+O ===2NO ②
2 2
由方程式①×2+②得:
4NO +O +2H O===4HNO ③
2 2 2 3
由方程式①×2+②×3得:
4NO+3O +2H O===4HNO ④
2 2 3
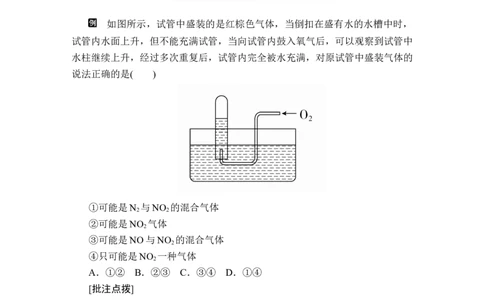
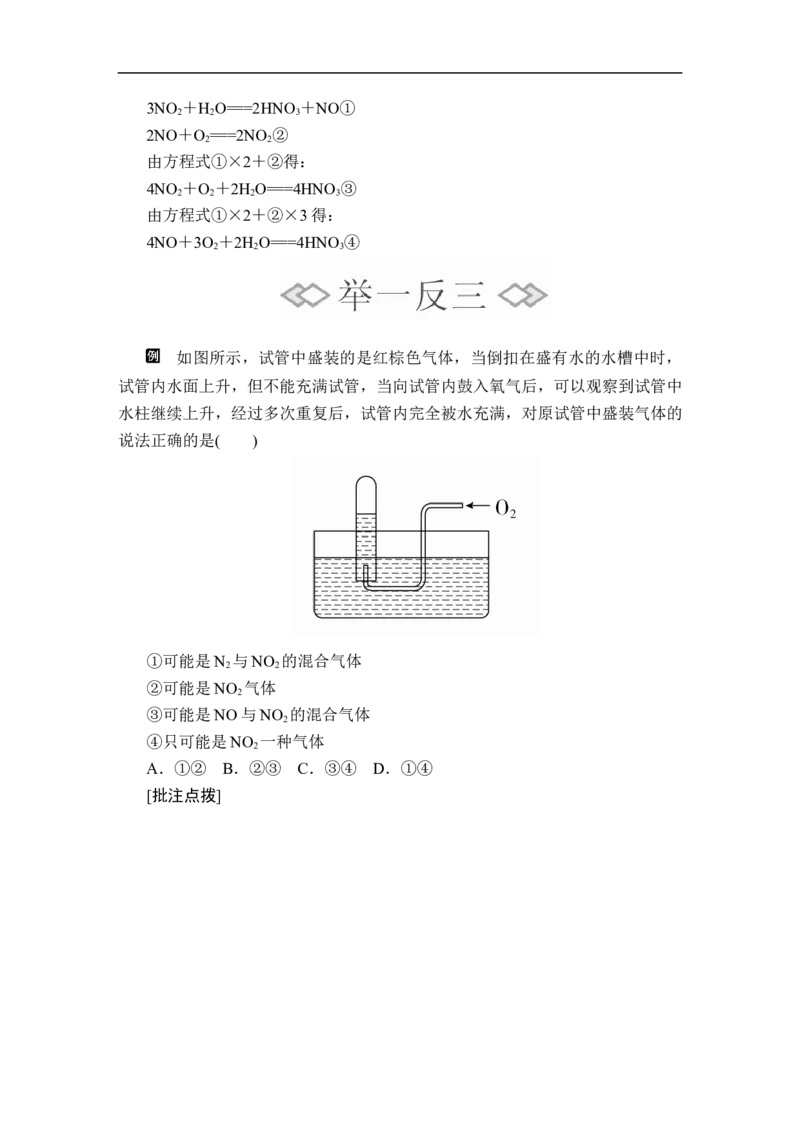
如图所示,试管中盛装的是红棕色气体,当倒扣在盛有水的水槽中时,
试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中
水柱继续上升,经过多次重复后,试管内完全被水充满,对原试管中盛装气体的
说法正确的是( )
①可能是N 与NO 的混合气体
2 2
②可能是NO 气体
2
③可能是NO与NO 的混合气体
2
④只可能是NO 一种气体
2
A.①② B.②③ C.③④ D.①④
[批注点拨][解析] 是红棕色气体,那么一定有二氧化氮的存在,与水反应后生成一氧
化氮,所以没有充满试管,继续通入氧气,最终充满试管,则①肯定错误;③中
通入足量的氧气,NO也可以全部被吸收。
[答案] B
[练1] 在一定温度和压强下,将一容积为 15 mL的试管充满NO 后,倒置
2
于一个盛有水的水槽中。当试管内液面上升至一定高度不再变化时,在相同条件
下再通入O ,若要使试管内液面仍保持在原高度,则通入O 的体积为( )
2 2
A.3.75 mL B.7.5 mL
C.8.75 mL D.10.5 mL
答案 C
解析 15 mL NO 与水反应后生成 5 mL NO,根据反应 4NO+3O +
2 2
2H O===4HNO ,使5 mL NO完全被氧化需O 体积为5 mL×=3.75 mL。据题
2 3 2意,通入的O 应过量5 mL,则共需通入O 8.75 mL。
2 2
[练2] 将10 mL充满NO 和O 的混合气体的试管,倒置在水槽中,反应停
2 2
止后试管内剩余2 mL的无色气体,求原混合气体中NO 和O 各多少毫升?
2 2
答案 剩余 2 mL 气体可能是 NO 或 O ,分两种情况讨论:(1)剩余的是
2
NO,可以看成先发生了反应:4NO +O +2H O===4HNO ,剩余的NO 又与水
2 2 2 3 2
作用,最终有2 mL NO产生。由反应3NO +H O===2HNO +NO得剩余的NO
2 2 3 2
体积为2 mL×3=6 mL。则原有O 体积为(10 mL-6 mL)×=0.8 mL,NO 体积
2 2
为10 mL-0.8 mL=9.2 mL。
(2)剩余的是O ,则有10 mL-2 mL=8 mL是NO 和O 的混合气体,按反应:
2 2 2
4NO +O +2H O===4HNO 进行计算。所以NO 的体积为8 mL×=6.4 mL,O
2 2 2 3 2 2
体积为10 mL-6.4 mL=3.6 mL。
氮的氧化物与水反应的计算规律
(1)NO 单独溶于水(按反应3NO +H O===2HNO +NO计算)
2 2 2 3
剩余气体是NO,V(NO)=V(NO )。
2
(2)NO 与O 的混合气体溶于水(按反应4NO +O +2H O===4HNO 计算)
2 2 2 2 2 3
(3)NO与O 的混合气体溶于水(按反应4NO+3O +2H O===4HNO 计算)
2 2 2 3
本课归纳总结
1.一氧化氮是无色、无味、不溶于水的有毒气体,易与空气中的氧气反应生
成二氧化氮,即2NO+O ===2NO 。
2 2
2.二氧化氮是红棕色有刺激性气味的有毒气体,易
溶于水生成HNO 和NO,化学方程式为3NO +H O===2HNO +NO。
3 2 2 3
3.氮的氧化物溶于水的总反应为 4NO+3O +2H O===4HNO 4NO +O +
2 2 3, 2 2
2H O===4HNO 。
2 3
学习效果检测
1.湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体可能是下列气体中
的( )
①Cl ②NO ③H S ④SO ⑤溴蒸气 ⑥HCl
2 2 2 2
A.①③④ B.①②⑤ C.①②⑥ D.②④⑥
答案 B解析 显蓝色表明接触过程中发生氧化还原反应生成了单质I 。其反应如下:
2
① Cl +2KI===I +2KCl,② 3NO +H O===2HNO +NO,HNO 将 KI 氧化成
2 2 2 2 3 3
I ,⑤Br +2KI===I +2KBr。
2 2 2
2.将盛有30 mL NO和NO 混合气体的试管倒置于放满水的水槽中,最后试
2
管中气体的体积是20 mL,则原混合气体中NO的体积是( )
A.24 mL B.15 mL C.18 mL D.12 mL
答案 B
解析 NO 与水反应 3NO +H O===2HNO +NO,设原混合气体中 NO 与
2 2 2 3
NO 的体积分别为x、y,则据题意,剩余气体体积20 mL是原NO气体与上述反
2
应生成的NO气体的总体积,列方程即可得NO和NO 体积都是15 mL。
2
3.在NO 被水吸收的反应中,发生还原反应的物质和发生氧化反应的物质
2
的物质的量之比为( )
A.3∶1 B.1∶3 C.1∶2 D.2∶1
答案 C
解析 3NO +H O===2HNO +NO,3 mol NO 中,有2 mol氮原子的价态升
2 2 3 2
高,1 mol氮原子的价态降低,所以发生还原反应的NO 与发生氧化反应的NO
2 2
的物质的量之比为1∶2。
4.下列物质的转化必须加入氧化剂且通过一步反应就能完成的是( )
①N →NO ②NO →NO ③NO →HNO
2 2 2 2 3
④N →NO ⑤N →NH
2 2 3
A.① B.②⑤ C.④ D.③④
答案 C
解析 该题有两个要求:(1)必须加入氧化剂;(2)通过一步反应就能完成。
反应①、③、④从化合价角度来看都是升高,但反应①N →NO 不能通过一步
2 2反应完成;而反应③NO →HNO 虽然氮的化合价升高,但不加氧化剂也能完成,
2 3
如3NO +H O===2HNO +NO,在该反应中,NO 既是氧化剂又是还原剂;只
2 2 3 2
有反应④N →NO必须加入氧化剂且通过一步反应就能完成。
2
5.一氧化氮是大气污染物之一。目前,有一种治理方法是在400 ℃左右、
有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水。请写出该反应的化学
方程式:__________________________________。
答案 6NO+4NH =====5N +6H O
3 2 2
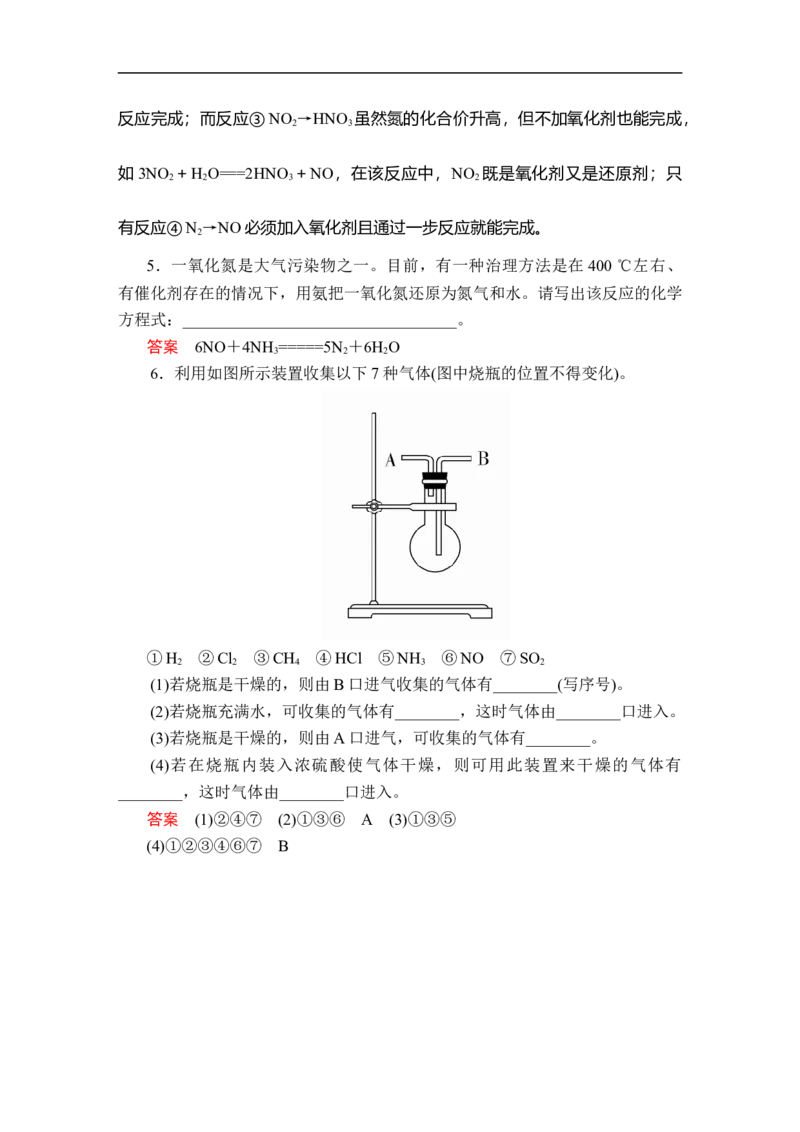
6.利用如图所示装置收集以下7种气体(图中烧瓶的位置不得变化)。
①H ②Cl ③CH ④HCl ⑤NH ⑥NO ⑦SO
2 2 4 3 2
(1)若烧瓶是干燥的,则由B口进气收集的气体有________(写序号)。
(2)若烧瓶充满水,可收集的气体有________,这时气体由________口进入。
(3)若烧瓶是干燥的,则由A口进气,可收集的气体有________。
(4)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有
________,这时气体由________口进入。
答案 (1)②④⑦ (2)①③⑥ A (3)①③⑤
(4)①②③④⑥⑦ B