文档内容
第二课时 氨和铵盐
[明确学习目标] 1.知道NH 的物理性质以及氨水显碱性的原因。2.学会氨气
3
的实验室制取、收集和检验方法。3.学会铵盐的性质及NH的检验方法。
学生自主学习
氨的性质及用途
1.氨的性质
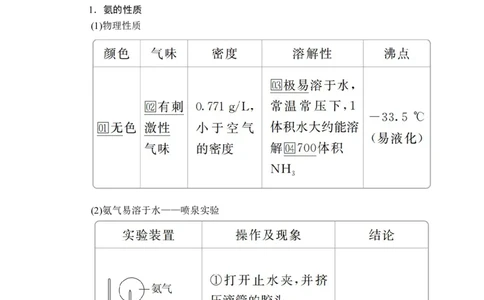
(1)物理性质
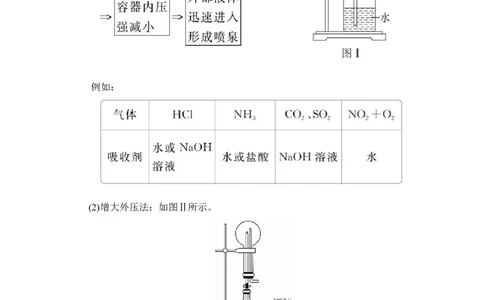
(2)氨气易溶于水——喷泉实验(3)化学性质
2.氨水的性质
3.氨的用途
(1)氨是氮肥工业、有机合成工业及制造硝酸、铵盐和纯碱的原料。
(2)氨易液化,可作 □ 制冷剂 。
铵盐的性质
1.物理性质
绝大多数铵盐都是 □ 易溶 于水的白色或无色晶体。
2.化学性质(写化学方程式)
(1)不稳定性,受热易分解,如
NH Cl:□NH Cl=====NH ↑+HCl↑;
4 4 3
NH HCO :□NH HCO =====NH ↑+H O+CO ↑。
4 3 4 3 3 2 2
(2)与碱反应(如氢氧化钠与硝酸铵溶液反应)
NH NO +NaOH=====NaNO +NH ↑+H O。
4 3 3 3 2
氨的实验室制法
1.实验原理
□2NH Cl+Ca(OH) =====CaCl +2H O+2NH ↑。
4 2 2 2 32.收集方法
□ 向下 排空气法。
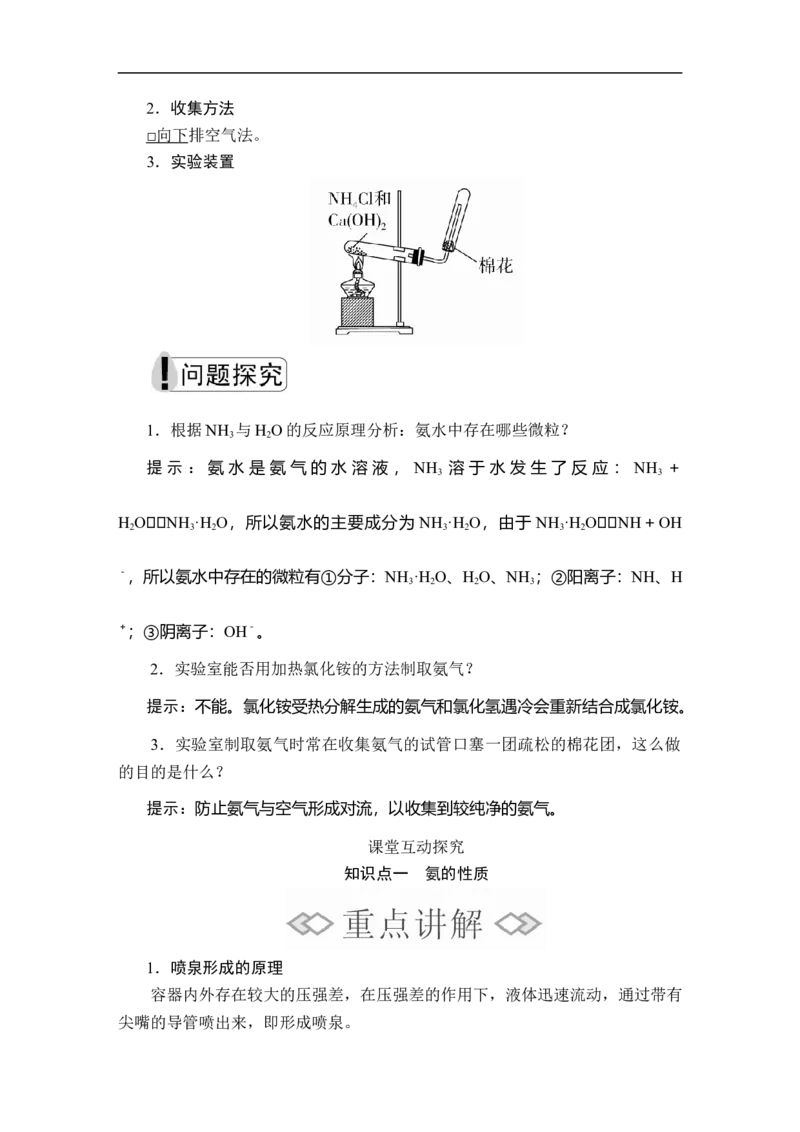
3.实验装置
1.根据NH 与H O的反应原理分析:氨水中存在哪些微粒?
3 2
提 示 : 氨 水 是 氨 气 的 水 溶 液 , NH 溶 于 水 发 生 了 反 应 : NH +
3 3
H ONH ·H O,所以氨水的主要成分为 NH ·H O,由于 NH ·H ONH+OH
2 3 2 3 2 3 2
-,所以氨水中存在的微粒有①分子:NH ·H O、H O、NH ;②阳离子:NH、H
3 2 2 3
+;③阴离子:OH-。
2.实验室能否用加热氯化铵的方法制取氨气?
提示:不能。氯化铵受热分解生成的氨气和氯化氢遇冷会重新结合成氯化铵。
3.实验室制取氨气时常在收集氨气的试管口塞一团疏松的棉花团,这么做
的目的是什么?
提示:防止氨气与空气形成对流,以收集到较纯净的氨气。
课堂互动探究
知识点一 氨的性质
1.喷泉形成的原理
容器内外存在较大的压强差,在压强差的作用下,液体迅速流动,通过带有
尖嘴的导管喷出来,即形成喷泉。2.使容器内外产生较大压强差的两种方法
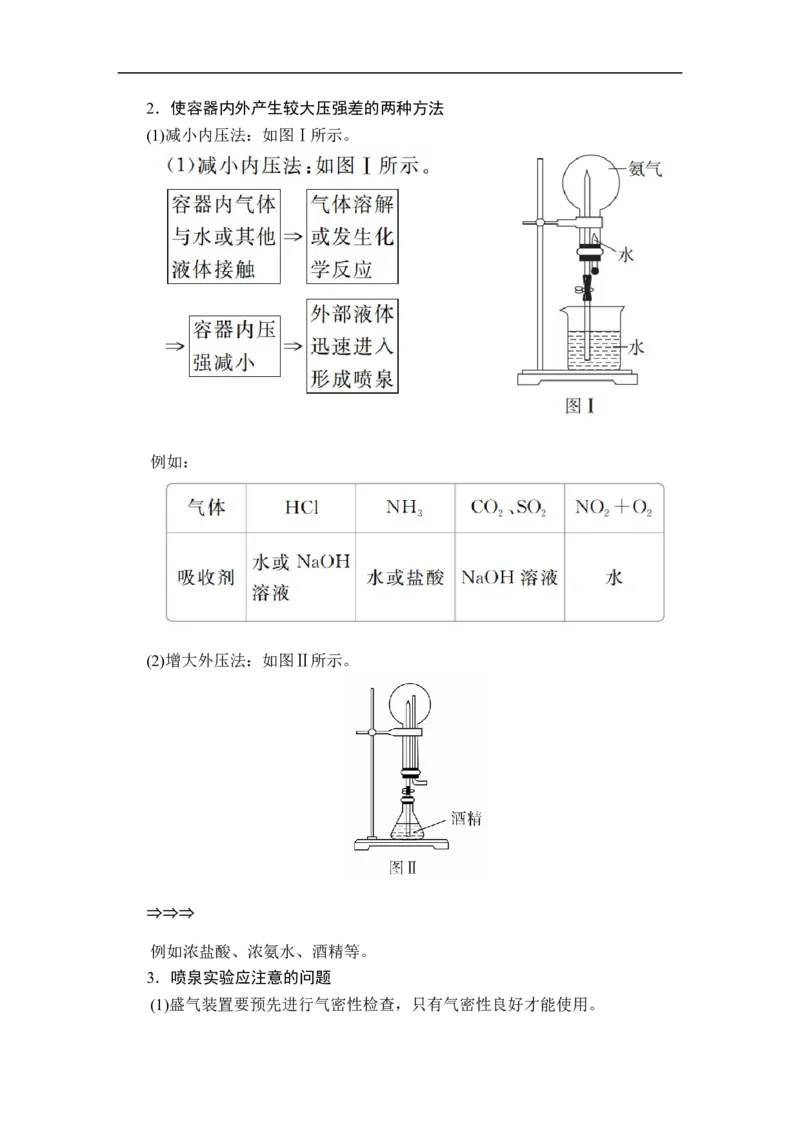
(1)减小内压法:如图Ⅰ所示。
例如:
(2)增大外压法:如图Ⅱ所示。
⇒⇒⇒
例如浓盐酸、浓氨水、酒精等。
3.喷泉实验应注意的问题
(1)盛气装置要预先进行气密性检查,只有气密性良好才能使用。(2)圆底烧瓶在充入氨气前应是干燥的,否则会浪费氨气。
(3)圆底烧瓶内要充满氨气,氨气过少往往不能形成喷泉。
(4)玻璃导管插入滴加酚酞溶液的水中的部分不能太短,以防导管过早地与
水脱离而导致喷泉停喷。
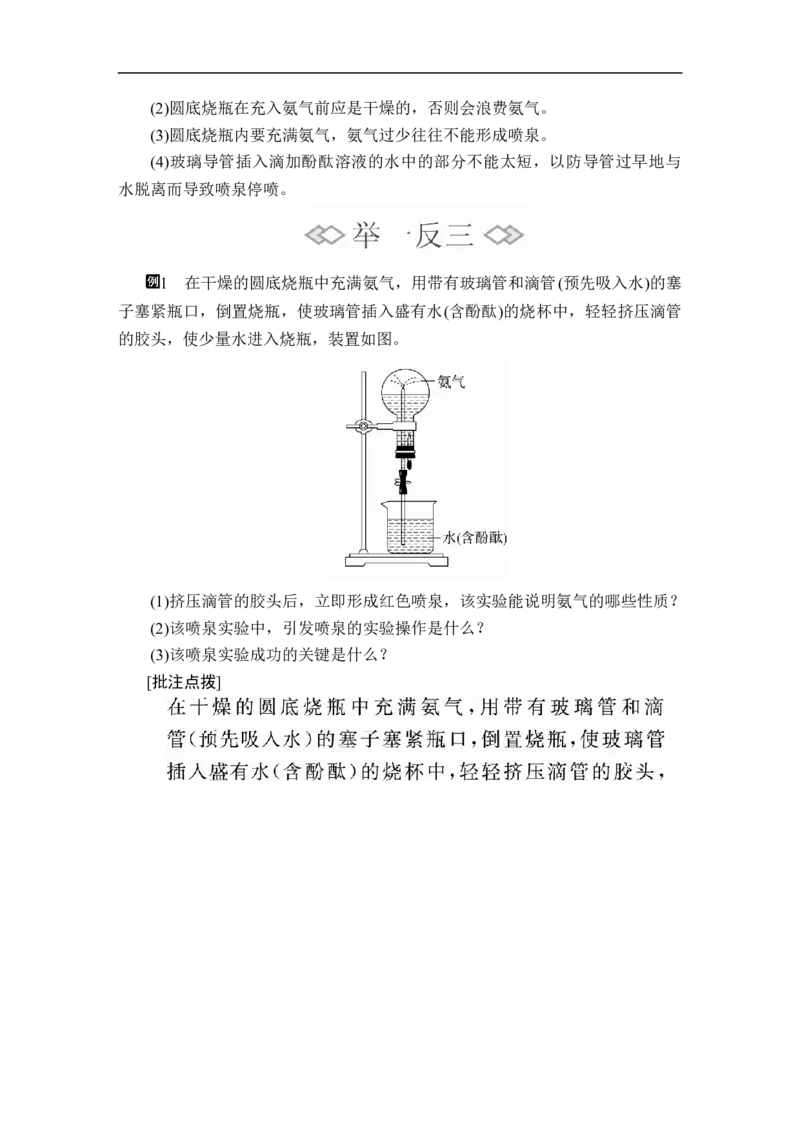
1 在干燥的圆底烧瓶中充满氨气,用带有玻璃管和滴管(预先吸入水)的塞
子塞紧瓶口,倒置烧瓶,使玻璃管插入盛有水(含酚酞)的烧杯中,轻轻挤压滴管
的胶头,使少量水进入烧瓶,装置如图。
(1)挤压滴管的胶头后,立即形成红色喷泉,该实验能说明氨气的哪些性质?
(2)该喷泉实验中,引发喷泉的实验操作是什么?
(3)该喷泉实验成功的关键是什么?
[批注点拨][答案] (1)能说明氨气极易溶于水;氨气与水反应生成的氨水呈碱性。
(2)打开止水夹,挤压胶头滴管的胶头。
(3)①装置气密性良好。
②圆底烧瓶要干燥。
③装置内气体的纯度要高。
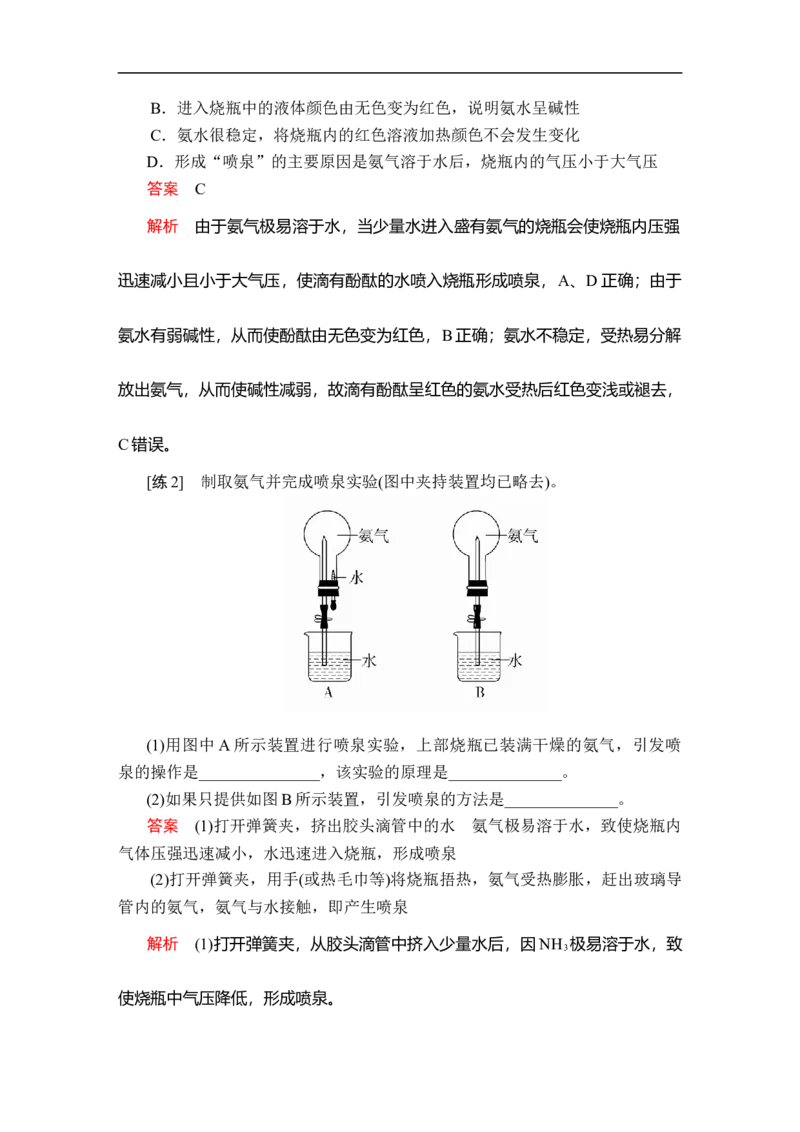
[练1] 如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正
确的是( )
A.该实验说明氨气极易溶于水B.进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C.氨水很稳定,将烧瓶内的红色溶液加热颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
答案 C
解析 由于氨气极易溶于水,当少量水进入盛有氨气的烧瓶会使烧瓶内压强
迅速减小且小于大气压,使滴有酚酞的水喷入烧瓶形成喷泉,A、D正确;由于
氨水有弱碱性,从而使酚酞由无色变为红色,B正确;氨水不稳定,受热易分解
放出氨气,从而使碱性减弱,故滴有酚酞呈红色的氨水受热后红色变浅或褪去,
C错误。
[练2] 制取氨气并完成喷泉实验(图中夹持装置均已略去)。
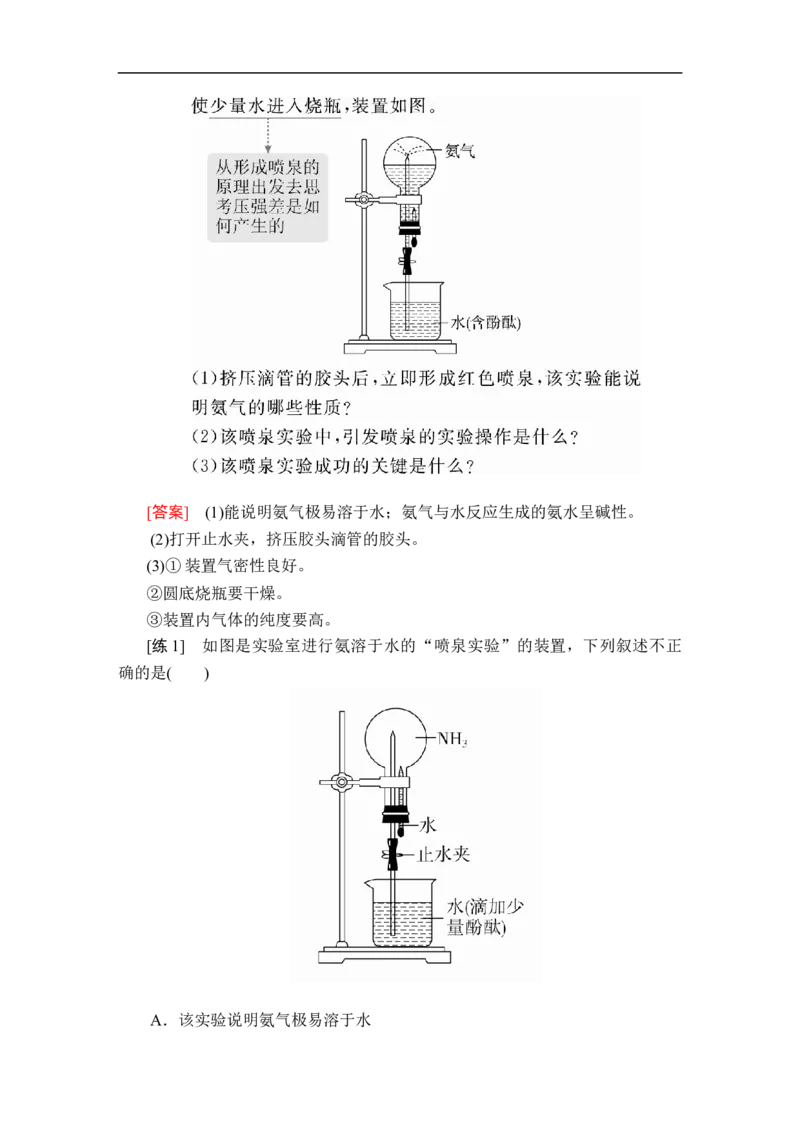
(1)用图中A所示装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发喷
泉的操作是_______________,该实验的原理是______________。
(2)如果只提供如图B所示装置,引发喷泉的方法是______________。
答案 (1)打开弹簧夹,挤出胶头滴管中的水 氨气极易溶于水,致使烧瓶内
气体压强迅速减小,水迅速进入烧瓶,形成喷泉
(2)打开弹簧夹,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导
管内的氨气,氨气与水接触,即产生喷泉
解析 (1)打开弹簧夹,从胶头滴管中挤入少量水后,因NH 极易溶于水,致
3
使烧瓶中气压降低,形成喷泉。(2)B装置与A装置相比,B装置没有胶头滴管,引发该喷泉可用热毛巾捂热
圆底烧瓶,赶出导管内的氨气,使NH 与水接触,从而形成喷泉。
3
知识点二 铵盐 氨的实验室制法
一、铵盐的性质
1.铵盐易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处。
2.NH的检验方法
(1)原理
(2)方法
取少量样品或溶液于试管中,再加入浓的 NaOH溶液,加热产生能使湿润的
红色石蕊试纸变蓝色的气体(或将蘸有浓盐酸的玻璃棒靠近管口,有白烟产生),
证明样品或溶液中含有NH。
二、氨的实验室制法
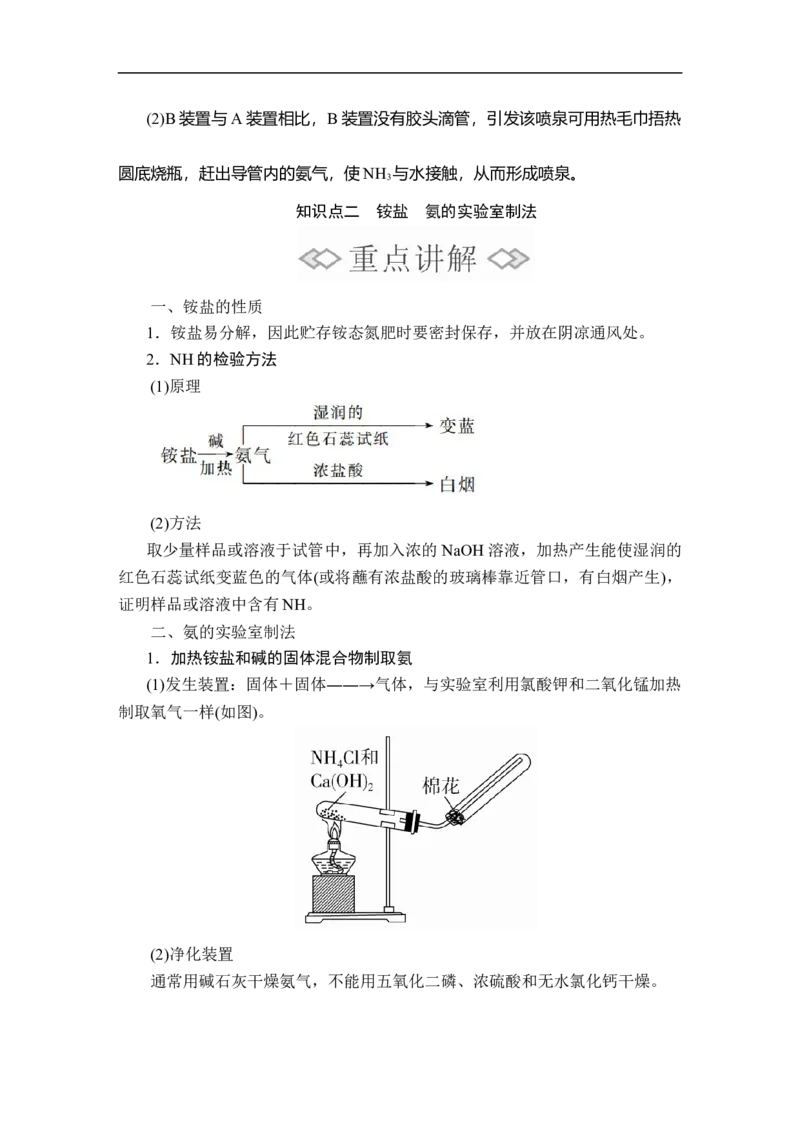
1.加热铵盐和碱的固体混合物制取氨
(1)发生装置:固体+固体――→气体,与实验室利用氯酸钾和二氧化锰加热
制取氧气一样(如图)。
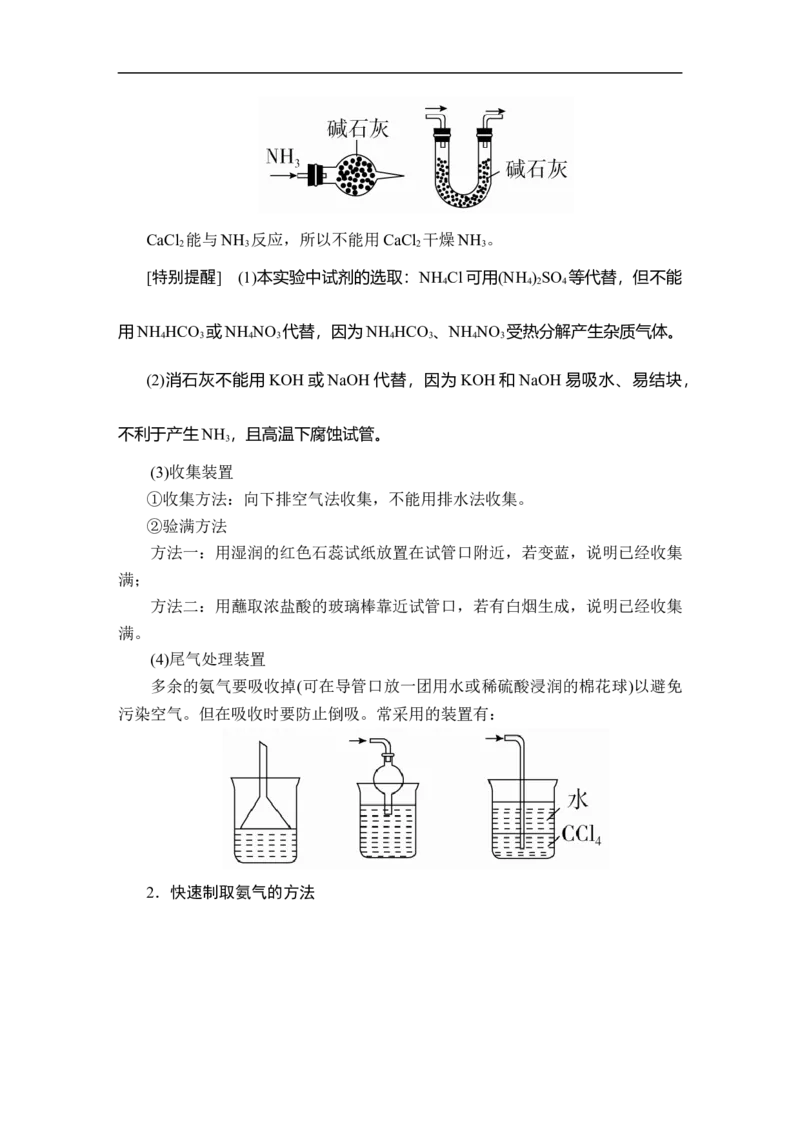
(2)净化装置
通常用碱石灰干燥氨气,不能用五氧化二磷、浓硫酸和无水氯化钙干燥。CaCl 能与NH 反应,所以不能用CaCl 干燥NH 。
2 3 2 3
[特别提醒] (1)本实验中试剂的选取:NH Cl可用(NH ) SO 等代替,但不能
4 4 2 4
用NH HCO 或NH NO 代替,因为NH HCO 、NH NO 受热分解产生杂质气体。
4 3 4 3 4 3 4 3
(2)消石灰不能用KOH或NaOH代替,因为KOH和NaOH易吸水、易结块,
不利于产生NH ,且高温下腐蚀试管。
3
(3)收集装置
①收集方法:向下排空气法收集,不能用排水法收集。
②验满方法
方法一:用湿润的红色石蕊试纸放置在试管口附近,若变蓝,说明已经收集
满;
方法二:用蘸取浓盐酸的玻璃棒靠近试管口,若有白烟生成,说明已经收集
满。
(4)尾气处理装置
多余的氨气要吸收掉(可在导管口放一团用水或稀硫酸浸润的棉花球)以避免
污染空气。但在吸收时要防止倒吸。常采用的装置有:
2.快速制取氨气的方法续表
2 试管中盛有白色晶体,检验它是不是铵盐的方法中不可行的是( )A.加热,将湿润的红色石蕊试纸放在管口
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口
[批注点拨]
[答案] A
[练3] 下列关于氨、铵盐的说法正确的是( )
A.氨水是一种弱碱,可以使酚酞变红
B.所有铵盐都不稳定,均可分解得到NH
3
C.实验室可用:N +3H ((((2NH 反应来制取NH
2 2 3 3
D.可用加热的方法来分离NaCl和NH Cl
4
答案 D
解析 氨水的溶质NH ·H O为一种弱碱,而氨水为混合物,不是一种弱碱,
3 2
A错误;铵盐不稳定,但分解产物并不是都有NH ,如NH NO 分解发生氧化还
3 4 3
原反应,无NH 产生,B错误;工业上以 N +3H ((((2NH 来生产NH ,但实验
3 2 2 3 3
室中难以达到该反应条件,不能用此原理产生NH ,C错误;利用NH Cl的不稳
3 4定性,可分离二者。
规律方法
检验NH时注意:(1)必须先加碱溶液,将NH转化为NH ,而不能直接加热
3
固体药品,因为有的铵盐受热分解不一定产生 NH ,如NH NO 分解产物较复杂,
3 4 3
其中不含有NH 。
3
(2)必须加热且用浓碱溶液,因为碱液浓度较小和不加热时生成NH ·H O。
3 2
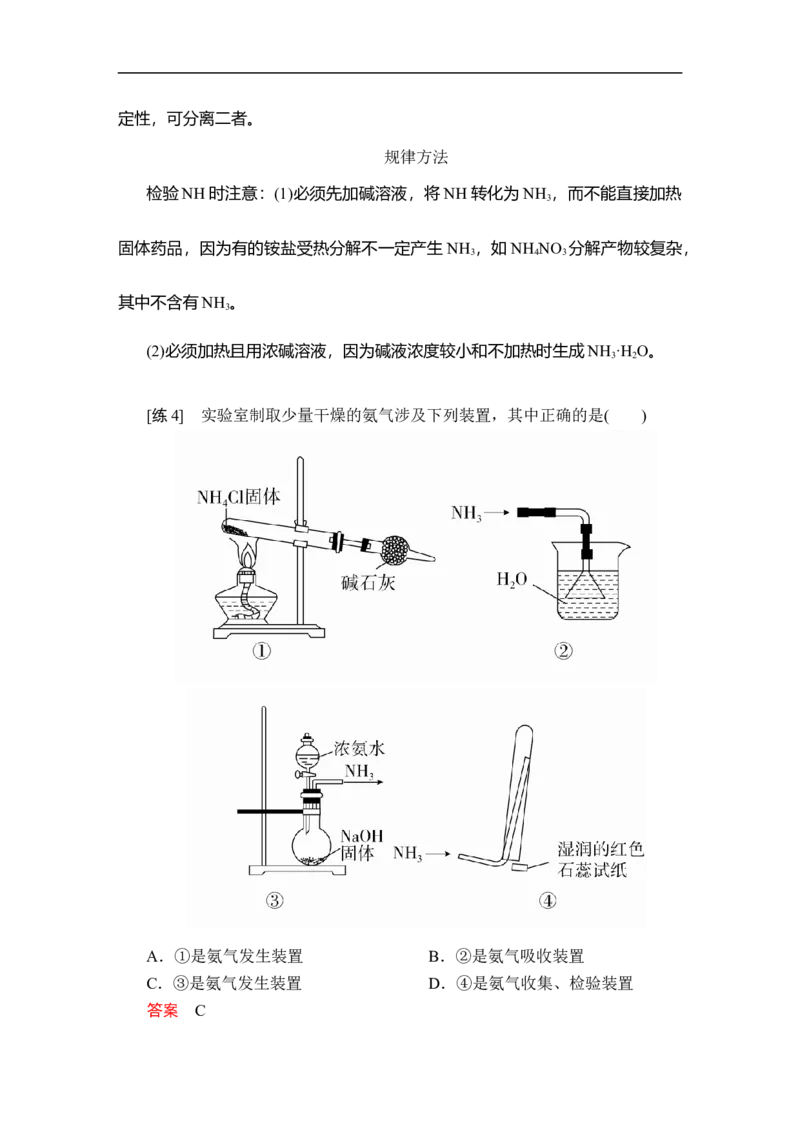
[练4] 实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
答案 C解析 ①NH Cl受热分解为NH 和HCl,但在试管口NH 、HCl又会重新化
4 3 3
合为NH Cl,得不到NH ;②不能用于吸收氨气,会引起倒吸;④收集氨气的试
4 3
管口应放置一团棉花,以防止氨气与空气形成对流。
规律方法
判断实验装置是否有错的一般方法
(1)看发生装置是否有错:①实验是否需要加热;②酒精灯部位是否有错(酒
精量、外焰加热、是否缺灯芯);③仪器放置是否有错;④夹持仪器的位置是否
有错。
(2)看试剂是否符合实验原理(包括反应物、干燥剂、尾气吸收剂)。
(3)看收集方法是否有错(排水法、向上排气法、向下排气法、导管伸入的位
置等)。
(4)看是否缺少尾气吸收装置,对于有毒气体,一定要设计尾气吸收装置,
并选择合适的吸收剂,同时注意防倒吸。
本课归纳总结
1.NH 极易溶于水,是能使湿润的红色石蕊试纸变蓝的唯一气体。
3
2.牢记4个方程式:
(1)N +3H ((((2NH 。
2 2 3
(2)NH ·H ONH+OH-。
3 2
(3)NH+OH-=====NH ↑+H O。
3 2
(4)4NH +5O =====4NO+6H O。
3 2 2
3.实验室常用加热 NH Cl 与 Ca(OH) 固体混合物的方法制备 NH ,干燥
4 2 3
NH 用碱石灰,检验NH 常用湿润的红色石蕊试纸,并用向下排空气法收集,制
3 3
取反应方程式为2NH Cl+Ca(OH) =====CaCl +2NH ↑+2H O。
4 2 2 3 2
4.NH的检验方法:取少量待测溶液于试管中,再加入浓的 NaOH溶液,加热产生能使湿润红色石蕊试纸变蓝的气体(或将蘸有浓盐酸的玻璃棒靠近试管口,
有白烟产生),则该溶液中存在NH。
学习效果检测
1.下列反应属于氮的固定的是( )
A.空气在雷电作用下产生NO
B.NO和O 生成NO
2 2
C.铜与浓硝酸反应产生NO
2
D.NH Cl与Ca(OH) 反应生成NH
4 2 3
答案 A
2.氨水显弱碱性的主要原因是( )
A.通常状况下,氨的溶解度不大
B.氨水中的NH ·H O电离出少量的OH-
3 2
C.溶于水的氨分子只有少量电离
D.氨本身的碱性弱
答案 B
解析 氨气溶于水后,大部分与水结合生成一水合氨(NH ·H O),NH ·H O
3 2 3 2
仅有少部分电离成NH和OH-,因此显弱碱性。
3.下列关于铵盐的叙述中正确的是( )
①所有铵盐中,氮元素化合价都是-3价
②所有铵盐都溶于水
③铵态氮肥不宜与草木灰混合使用
④铵盐都是离子化合物
⑤铵盐都能与碱反应,不能与酸反应
A.①③④ B.②③④
C.①②③④ D.①②③④⑤
答案 B
解析 NH NO 中的NO,氮元素是+5价,①错误;NH HCO 也能与酸反应,
4 3 4 3
⑤错误;草木灰主要成分为K CO ,显碱性,混合使用会产生NH ,从而降低肥
2 3 3
效,③正确。
4.只用一种试剂就能将NH Cl、(NH ) SO 、NaCl、Na SO 四种溶液区分开,
4 4 2 4 2 4这种试剂是( )
A.NaOH溶液 B.AgNO 溶液
3
C.Ba(OH) 溶液 D.BaCl 溶液
2 2
答案 C
解析 四种盐溶液中有四种离子:NH、Na+、Cl-、SO,区分Na+与NH使
用碱溶液,区分Cl-和SO用Ba2+,故选用Ba(OH) 溶液。
2
5.有A、B、C三种气体,A气体在一定条件下能与O 反应生成B;B不溶
2
于水,但易与O 反应生成C;A、C气体皆易溶于水,所得的溶液可以相互反应
2
生成盐和水,则A是________,B是________,C是________(写化学式)。
答案 NH NO NO
3 2
解析 由“A、C气体皆易溶于水,所得的溶液可以相互反应生成盐和水”
推知A、C的水溶液一个显碱性,一个显酸性,显碱性的气体只有NH 。
3
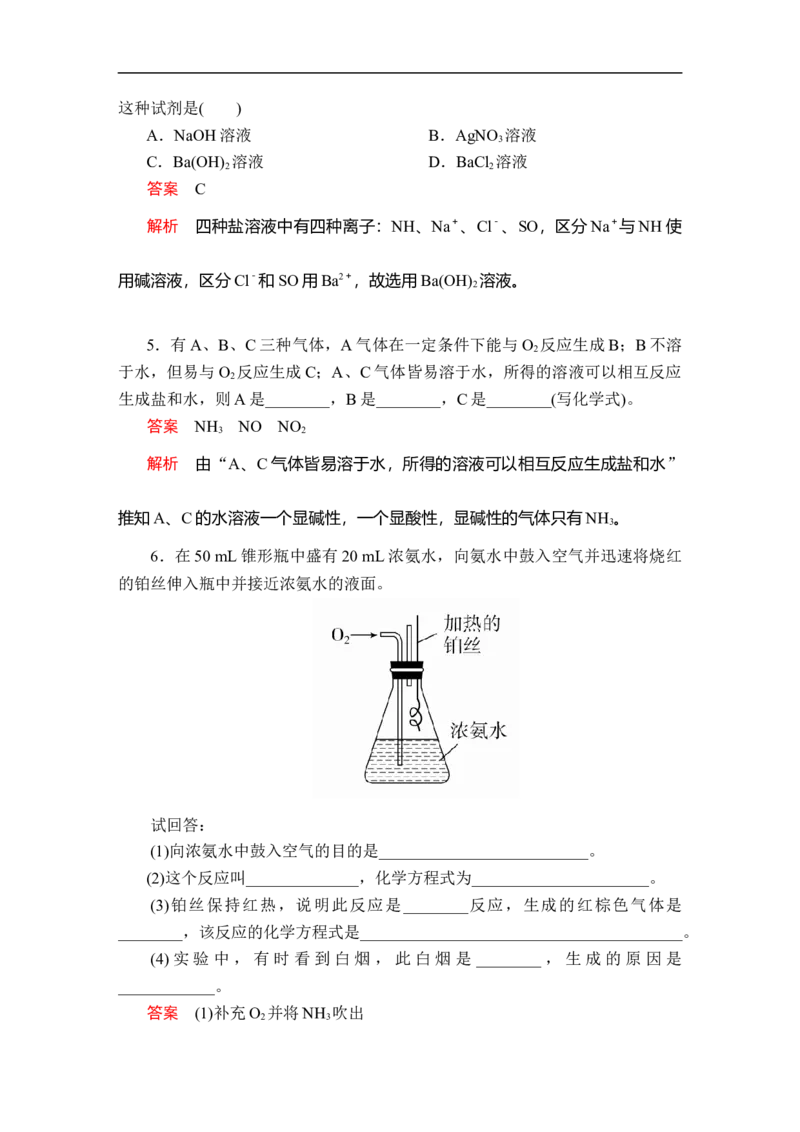
6.在50 mL锥形瓶中盛有20 mL浓氨水,向氨水中鼓入空气并迅速将烧红
的铂丝伸入瓶中并接近浓氨水的液面。
试回答:
(1)向浓氨水中鼓入空气的目的是__________________________。
(2)这个反应叫______________,化学方程式为______________________。
(3)铂丝保持红热,说明此反应是________反应,生成的红棕色气体是
________,该反应的化学方程式是________________________________________。
(4) 实验中,有时 看到 白烟,此白烟是 ________,生成的原因是
____________。
答案 (1)补充O 并将NH 吹出
2 3(2)氨的催化氧化 4NH +5O =====4NO+6H O
3 2 2
(3)放热 NO 2NO+O ===2NO
2 2 2
(4)NH NO 3NO +H O===2HNO +NO,NH +HNO ===NH NO
4 3 2 2 3 3 3 4 3
解析 浓氨水有挥发性,鼓入空气一是通入O ,二是将NH 吹出。铂丝为
2 3
NH 与O 反应的催化剂,二者反应生成 NO,NO再与O 反应生成NO ,NO 与
3 2 2 2 2
水蒸气反应生成HNO ,HNO 遇NH 产生NH NO 小颗粒而产生白烟。
3 3 3 4 3