文档内容
第三单元 物质构成的奥秘 课题2 原子的结构(第一课时)导学案
学习目标:
1、了解原子的构成,并记住原子中各微粒的带电情况。
2、记住在原子中,核电荷数=质子数=核外电子数
3、认识相对原子质量,掌握相对原子质量的计算。
导学案
认真阅读课文P53、56页,回答下列问题:
1、科学实验证明,原子是由居于原子中心的 和 构成的。原子核由
和 构成的。
2、构成原子的各种粒子是否带电?若带电,是带正电荷,还是带负电荷?
小结: 用框图形式表示原子的构成情况,并标明各微粒的带电情况。
带 电
原子
带 电
3、什么是相对原子质量?(56页)
4、相对原子质量的标准是什么?标准是多少?相对原子质量的单位是什么?(56页)
预习自测:
1、下列有关相对原子质量的说法中正确的是 ( )
A.相对原子质量就是一个原子的真实质量
B.相对原子质量决定了原子的种类
C.氧原子的相对原子质量是16g
D.相对原子质量是一个比值,单位不是g或kg探究案
探究一、
阅读P53页表3-1,思考下列问题:
1、原子中核电荷数、质子数和核外电子数有何关系?用等量关系式表示。
由上述关系我们可以推出的结论是:整个原子 电性。
2、原子中质子数和中子数是否相等?
3、原子是否都含有中
子?举例说明。
探究二、
1、原子是一个实心球体吗?相对于原子来说,原子核所占空间有多大?(参考图3-9)
2、质子、中子、电子的质量分别是多少?由此可得出整个原子的质量主要集中在哪个部位?
(56页)
探究三、
1、相对原子质量的计算公式是什么?相对原子质量的符号是什么?
2、相对原子质量的近似计算方法?
巩固训练
1、已知下列原子的质量,计算其相对原子质量
O原子质量为2.657×10-26千克 Fe原子质量为9.288×10-26千克
3、已知下列原子的质子数和中子数,计算其相对原子质量
氧原子的质子数8,中子数8; 钠原子的质子数11,中子数12班级 姓名
课题2 原子的结构Ⅰ
测试案
1.已知原子的核电荷数,可以确定它的 ( )
A、原子质量 B、质子数 C、中子数 D、相对原子质量
2.原子核(普通的氢除外)是 ( )
A、由电子和质子构成 B、由质子和中子构成
C、由电子和中子构成 D、不能再分
3.在原子里质子数等于 ( )
A、中子数 B、电子数
C、中子数和电子数之和 D、原子质量
4.美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数
目恰好与铱元素(Ir)的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是
( )
A. 铱原子的质子数为70 B. 铱原子的相对原子量质量为77
C. 铱原子的核电荷数为77D. 铱元素为非金属元素
5、1991年我国科学家张青莲教授与另一位科学家合作,测定了铟元素的相对原子质量新值,
铟的核电荷数为49,相对原子质量为115,则铟的中子数为
( )
A.164 B.115 C.66 D.49
6、已知一个质子数和中子数都是6的碳原子的质量是1.993 × 10-26 kg,M原子的质量是
6.64× 10-26 kg,则其相对原子质量为多少?
7、已知碳 原子的质量为1.993 × 10-26 kg,而一个铁原子的实际质量为9.288 ×10-26
12
kg,求铁的相对原子质量。班级 姓名
课题2 原子的结构Ⅱ
测试案
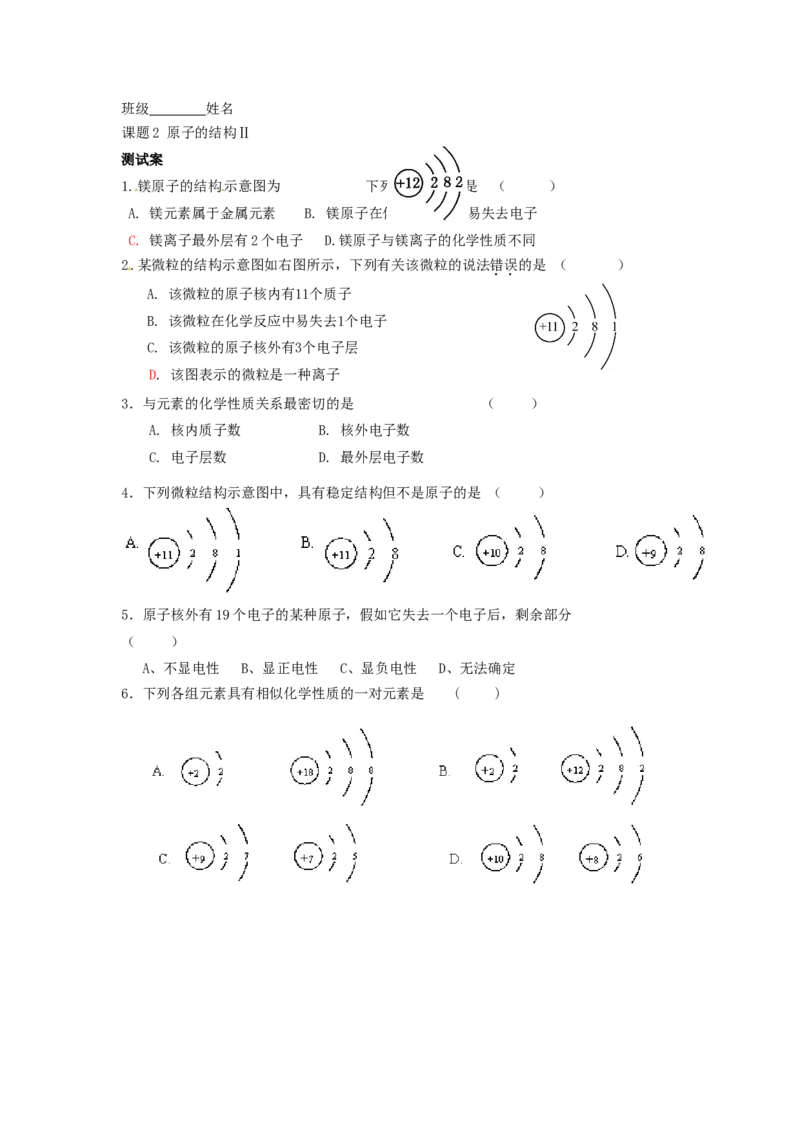
1.镁原子的结构示意图为 下列说法错误的是 ( )
A. 镁元素属于金属元素 B. 镁原子在化学反应中容易失去电子
C. 镁离子最外层有2个电子 D.镁原子与镁离子的化学性质不同
2.某微粒的结构示意图如右图所示,下列有关该微粒的说法错误的是 ( )
A. 该微粒的原子核内有11个质子
B. 该微粒在化学反应中易失去1个电子
C. 该微粒的原子核外有3个电子层
D. 该图表示的微粒是一种离子
3.与元素的化学性质关系最密切的是 ( )
A. 核内质子数 B. 核外电子数
C. 电子层数 D. 最外层电子数
4.下列微粒结构示意图中,具有稳定结构但不是原子的是 ( )
5.原子核外有19个电子的某种原子,假如它失去一个电子后,剩余部分
( )
A、不显电性 B、显正电性 C、显负电性 D、无法确定
6.下列各组元素具有相似化学性质的一对元素是 ( )