文档内容
北京 101 中学 2019-2020 学年上学期高一年级期末考试化学试卷
本试卷分为I卷、II卷,共26个小题,满分100分;答题时间为90分钟
可能用到的相对原子质量:H 1 O 16 Na 23
I卷 选择题(共42分)
共21道小题,每小题只有一个选项符合题意,每小题2分
1.2017年7月,清华大学宁存政教授课题组在硅基纳米激光器和光放大器研究上获得重大突破,对世界科
技具有重要意义。下列分散系中分散质的微粒直径与纳米级(1-100nm)粒子具有相同数量级的是
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
2.下列物质在化学反应中只能做还原剂的是
A. 浓HSO B. Cl C. Fe D. HNO
2 4 2 3
3.下列类型的反应,一定属于氧化还原反应的是
A. 复分解反应 B. 分解反应
C. 化合反应 D. 置换反应
4.下列物质中,不能用浓硫酸干燥的是
A. NH B. CO C. Cl D. SO
3 2 2 2
5.下列工业生产的反应原理不涉及氧化还原反应的是
A. 铝热反应冶炼铁:Fe O+2Al 2Fe+Al O
2 3 2 3
B. 工业上以NH 、CO、饱和食盐水为原料生产NaHCO :NH +CO +NaCl+HO=NaHCO ↓+NHCl
3 2 3 3 2 2 3 4
C. 硝酸厂以氨气为原料制取硝酸:NH →NO→NO →HNO
3 2 3
D. 工业电解Al O 制备金属铝:2Al O(熔融) 4Al+3O ↑
2 3 2 3 2
6.下列叙述错误的是
A. 自然界中的硫都是以化合态存在
B. 硫既有氧化性,又有还原性
C. 附着在试管壁上的硫,可用CS 洗涤
2
D. 硫黄主要用于制造硫酸、化肥等
7.最新研究发现,人体内自身产生的NO能促进全身血液循环,预防动脉粥样硬化,恢复血管柔软性和弹
性。下列有关NO的叙述中,正确的是
A. NO能溶于水,不能用排水法收集B. NO暴露在空气中,气体由无色变为红棕色,发生的是物理变化
C. “雷雨发庄稼”的谚语涉及到NO,生成NO的过程属于自然固氮
.
D 由信息知人可吸入大量NO,有利于身体健康
8.下列有关物质用途的说法中,不正确的是
A. NH NO 常用作氮肥 B. Fe O 做红色颜料
4 3 2 3
C. 氨可用作制冷剂 D. 用SO 可漂白馒头
2
的
9.下列有关浓硫酸、浓盐酸、浓硝酸 认识不正确的是
A. 浓硫酸、浓硝酸与金属反应时,分别是S、N得电子
B. 蔗糖与浓硫酸混合后,白色蔗糖固体逐渐变成黑色疏松的碳,体现了浓硫酸的脱水性
C. 浓盐酸、浓硝酸具有挥发性,而浓硫酸难挥发
D. 常温下,浓硫酸或浓HNO 中投入Fe片,均会产生大量的气体
3
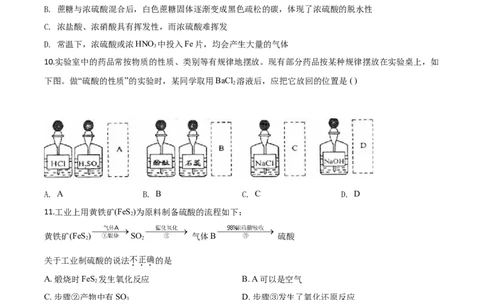
10.实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律摆放在实验桌上,如
下图。做“硫酸的性质”的实验时,某同学取用BaCl 溶液后,应把它放回的位置是 ( )
2
A. A B. B C. C D. D
11.工业上用黄铁矿(FeS )为原料制备硫酸的流程如下:
2
黄铁矿(FeS ) SO 气体B 硫酸
2 2
关于工业制硫酸的说法不正确的是
A. 煅烧时FeS 发生氧化反应 B. A可以是空气
2
C. 步骤②产物中有SO D. 步骤③发生了氧化还原反应
3
12.下列物质长期露置于空气中会变质,且变质过程中涉及氧化还原反应的是
①Na ②NaOH ③FeSO ④氯水
4
A. ①② B. ②③ C. ①③④ D. ②③④
13.最近,科学家开发出一种低成本光伏材料——蜂窝状石墨烯。生产原理是:NaO+2CO
2
NaCO+C(石墨烯),然后除去NaCO,即可制得蜂窝状石墨烯。下列说法不正确的是
2 3 2 3A. 石墨烯与金刚石互为同素异形体
B. 该生产石墨烯的反应中CO只体现了还原性
C. NaO属于碱性氧化物,NaCO 属于盐
2 2 3
D. 自然界中碳元素有游离态和化合态两种存在形式
14.化学与科技、社会、生产有密切联系,下列说法不正确的是
A. 减少燃煤的使用可减少二氧化硫的排放,减少酸雨的危害
B. 铵盐具有受热易分解的性质,在储存铵态氮肥时,应密封包装并放在阴凉通风处
C. 84消毒液与洁厕灵(其中含有盐酸)可以混合使用
D. 二氧化氯(ClO )具有氧化性,可用于自来水的杀菌消毒
2
15.只用一种试剂就能将NH Cl、(NH )SO 、NaCl、NaSO 四种溶液区别,这种试剂是
4 4 2 4 2 4
A. NaOH溶液 B. AgNO 溶液
3
C. Ba(OH) 溶液 D. BaCl 溶液
2 2
16.下列离子方程式不正确的是
A. 用稀盐酸除铁锈:Fe O+6H+=2Fe3++3H O
2 3 2
B. Cl 通入水中:Cl+H O H++Cl-+HClO
2 2 2
C. 铜与浓硝酸反应生成红⇌棕色气体:3Cu+8H++2NO
3
-=3Cu2++2NO
2
↑+4H
2
O
D. 实验室用MnO 和浓盐酸制Cl:MnO +4H++2Cl- Mn2++Cl↑+2H O
2 2 2 2 2
17.下列说法不正确的是
A. 氨水使酚酞溶液变红是因为溶液中NH ∙H O电离出OH-
3 2
B. KNO 溶于水电离出K+和NO -
3 3
C. 电离时生成的阳离子有H+的化合物不一定是酸
D. SO 溶于水能导电,所以SO 是电解质
2 2
18.下列关于NaO 的说法不正确的是
2 2
A. NaO 中Na与O的化合价分别为+1,-1
2 2
B. NaO 与水反应,NaO 既是氧化剂,又是还原剂
2 2 2 2
.
C NaO 投入NaHSO 溶液,产生气泡,生成NaSO 溶液
2 2 3 2 3
D. NaO 投入酚酞溶液中,可以观察到有气体产生,溶液变红的现象
2 2
19.设N 代表阿伏加德罗常数的数值,下列说法不正确的是
A
A. 常温常压下,2 g氢气所含原子数目为2N
A
B. 1 mol NH +含有的电子数为10 N
4 A
C. 一定量铁粉与水蒸气反应生成1 g氢气,反应中转移的电子数为N
AD. 标准状况下,0.3 mol NO 通入足量水中完全反应,生成气体体积约为4.48 L
2
20.下列实验方案能达到实验目的的是(部分夹持装置已略去)
A. 验证木炭和浓硫酸反应生成CO
2
B. 实验室制备Fe(OH) 并能较长时间观察到白色固体
2
C. 实验室制备和收集氨气并验满
D. 证明补铁口服液中存在+2价的铁
21.食盐中的碘以碘酸钾(KlO )形式存在,可根据反应:IO -+5I-+6H+=3I +3H O验证食盐中存在IO -。根据
3 3 2 2 3
上述反应,下列说法错误的是
A. IO -作氧化剂,发生还原反应
3
B. I 既是氧化产物又是还原产物
2
C. 该条件下氧化性:IO ->I
3 2
D. 每生成3 mol I ,转移电子的物质的量为6 mol
2
II卷 非选择题(共58分)
22.分类法在化学学习中应用广泛。属于同一类的物质具有相似的性质,CO、SiO、SO 、SO 都属于酸性
2 2 2 3
氧化物。由CO+Ca(OH) =CaCO ↓+H O,可得出SO 与NaOH反应的化学方程式为__________。
2 2 3 2 3
23.实验室验证Ba(NO ) 固体中含有NO -的一种方案是:取少量固体加入蒸馏水完全溶解,加入一滴管稀
3 2 3
硫酸后再加入一小块铜片,微微加热后观察到试管口有浅棕色气体出现,即可证明。请从微观角度解释该
实验方案能验证NO -存在的原因__________。
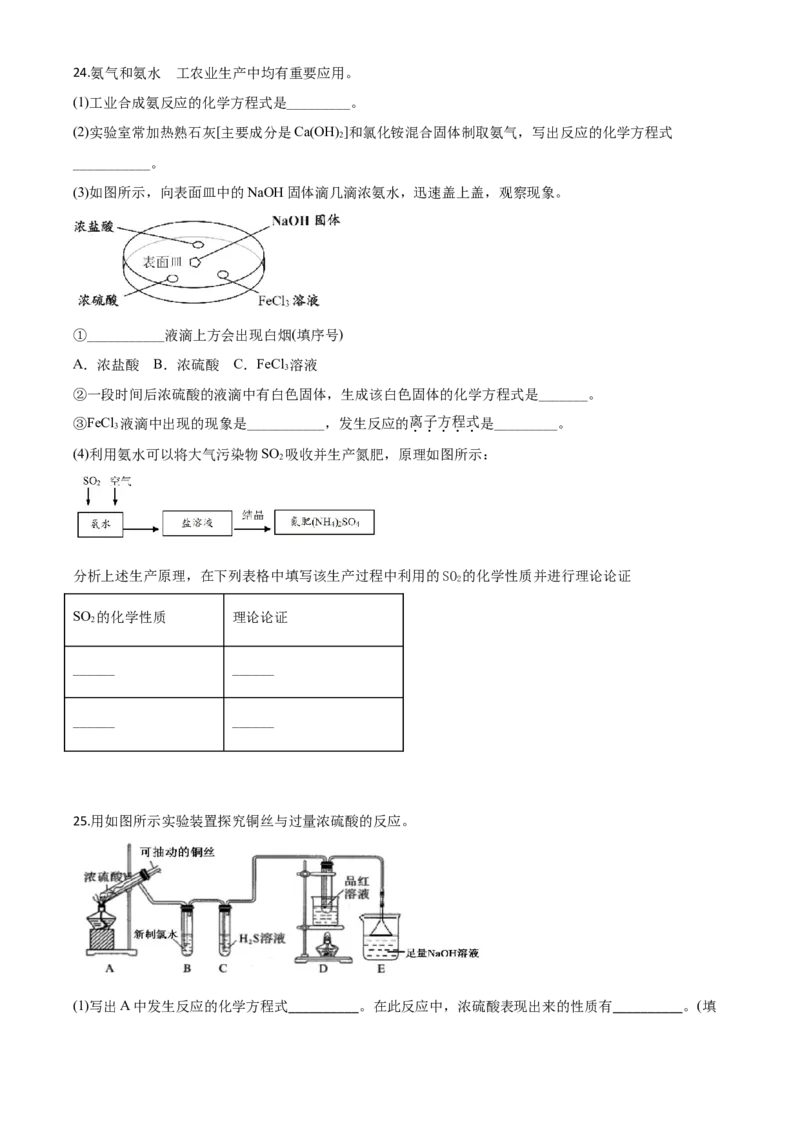
324.氨气和氨水 在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH) ]和氯化铵混合固体制取氨气,写出反应的化学方程式
2
___________。
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。
①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl 溶液
3
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl 液滴中出现的现象是___________,发生反应的离子方程式是_________。
3
(4)利用氨水可以将大气污染物SO 吸收并生产氮肥,原理如图所示:
2
分析上述生产原理,在下列表格中填写该生产过程中利用的SO 的化学性质并进行理论论证
2
SO 的化学性质 理论论证
2
______ ______
______ ______
25.用如图所示实验装置探究铜丝与过量浓硫酸的反应。
(1)写出A中发生反应的化学方程式__________。在此反应中,浓硫酸表现出来的性质有__________。(填字母序号)
A.强氧化性 B.酸性 C.吸水性 D.脱水性
(2)一段时间后,观察到B中溶液黄绿色褪去,B中反应的化学方程式为__________。C中的实验现象为
__________。
(3)D中的实验现象是__________,一段时间后,点燃D处酒精灯,可以观察到__________。
(4)E装置中NaOH溶液的作用是__________。
(5)研究小组认为可以用HO 溶液来验证E中溶液含有SO2-,进行了实验i。
2 2 3
实验序号 操作 现象
a. 取少量E中溶液,向其中加入适量HO 溶
2 2 无明显现象
液,振荡,观察。
i
b. 然后滴加__________,振荡,观察。 无明显现象
c. 再滴加__________,振荡,观察。 白色沉淀
通过实验i可证明E中溶液含有SO 2-,写出操作b、c中滴加的试剂是__________、__________。
3
(6)研究小组反思实验方案i不够严谨,设计了对比实验,证明了E中含有SO 2-。该对比实验方案是
3
__________。
26.某兴趣小组研究含铁元素的盐类物质的制备、保存和性质。
实验I. 配制FeCl 溶液:向0.1 mol·L-1 FeCl 溶液中加入足量铁粉,充分振荡,备用。
2 3
(1)FeCl 溶液与铁粉反应的离子方程式是__________。
3
(2)在老师的指导下,配制的FeCl 溶液底部仍保留一层铁粉,请说明该操作的必要性__________。
2
实验II. 通过Fe(NO) 的性质实验,探究试剂添加顺序的不同对现象和反应的影响。
3 2
试剂及操作
实验 现象
试管 滴管
实验i:
先滴加1.0 mL 0.5 mol·L-1
i. 滴加NaOH溶液后__________;加酸后
NaOH溶液;
. 溶液变为黄色
再滴加15mL 1.0 mol·L-1
HSO 溶液
2 4
0.1 mol/L Fe(NO )
3 2
溶液
实验ii:
先滴加1.5 mL 1.0 mol·L-1
ii. 加酸时溶液无明显现象;加碱后溶液依
HSO 溶液;
2 4 然没有明显变化
再滴加1.0 mL 0.5 mol·L-1
NaOH溶液(3)实验i中滴加NaOH溶液后出现的一系列现象是__________;请用化学或离子方程式说明Fe(NO ) 溶液
3 2
中滴加碱溶液后出现此系列现象的原因__________、__________。
(4)探究实验ii中先滴加HSO 溶液时Fe(NO ) 溶液中是否发生了反应:
2 4 3 2
A. 向1.0 mL 0.1 mol·L-1 Fe(NO) 溶液中__________(填写具体实验方法),溶液立即变红,说明加酸时溶液
3 2
中发生了反应,生成了Fe3+。
B. 推测溶液中产生Fe3+的可能原因有两种:
a. 酸性条件下,__________;
b. 酸性条件下,Fe2+可能被空气中的O 氧化,写出相应的离子方程式:___________。
2
27.氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含NH +废水和
4
工业废气(主要含NO、CO、CO、SO 、N)的流程如图:
2 2 2
已知:NO+NO +2NaOH=2NaNO +H O 2NO +2NaOH=NaNO +NaNO +H O
2 2 2 2 3 2 2
(1)固体1的主要成分有Ca(OH) 、__________(填化学式)。
2
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为__________g。
(3)用NaNO 溶液处理含NH +废水反应的离子方程式为__________。
2 4
(4)验证废水中NH +已基本除净的方法是___________(写出操作、现象与结论)。
4
(5)气体1转化为气体2时空气不能过量的原因是__________。
(6)捕获剂捕获的气体主要是__________(填化学式)。
(7)流程中生成的NaNO 因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO 能发生如下反应:
2 2
2NaNO +4HI=2NO↑+I +2NaI+2H O;I 可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试
2 2 2 2
剂进行实验,以鉴别NaNO 和NaCl。需选用的物质是__________(填序号)。
2
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤