文档内容
2023年贵州省中考化学试卷
参考答案与试题解析
1.【答案】B
【解析】A、分类回收垃圾,能节约资源、减少污染,做法与助推生态文明建设相符,故选项
错误。
B、发展高耗能产业,会浪费化石燃料,产生大量的空气污染物,做法与助推生态文明建设
不相符,故选项正确。
C、积极植树造林,有利于保护空气,做法与助推生态文明建设相符,故选项错误。
D、增加光伏发电,能减少化石燃料的使用,减少空气污染,做法与助推生态文明建设相符,
故选项错误。
故选:B。
2.【答案】A
【解析】A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴试管外壁,若导管
口有气泡冒出,装置不漏气,图中所示操作正确。
B、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,再慢慢将
试管竖立起来,图中所示操作错误。
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口;图中瓶塞
没有倒放,图中所示操作错误。
D、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试
管容积的三分之一,图中液体超过试管容积的三分之一,图中所示操作错误。
故选:A。
3.【答案】A
【解析】SiC中C的化合价为﹣4,设硅元素的化合价是x,根据在化合物中正负化合价代
数和为零,可得:x+(﹣4)=0,则x=+4价。
故选:A。
4.【答案】C
【解析】A、黄酮素是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
B、黄酮素中只含有黄酮素一种物质,属于纯净物,不含氧气,故选项说法错误。
C、分子是由原子构成的,黄酮素分子由碳原子、氢原子和氧原子构成,故选项说法正确。
D、黄酮素中碳元素与氢元素的质量比为(12×15):(1×10)≠3:2,故选项说法错误。
故选:C。
5.【答案】D
【解析】A、燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应,属于化学变化,
产生的能量被广泛应用,故选项说法正确。
B、把煤块粉碎成煤粉使用,增大了煤和氧气的接触面积,可以使煤充分燃烧,故选项说法
正确。
C、炒菜油锅着火时,立刻盖上锅盖,能隔绝氧气,可以灭火,故选项说法正确。
D、把蜡烛伸入装有氧气的集气瓶中,若不点燃,蜡烛不能燃烧,故选项说法错误。
第1页(共7页)故选:D。
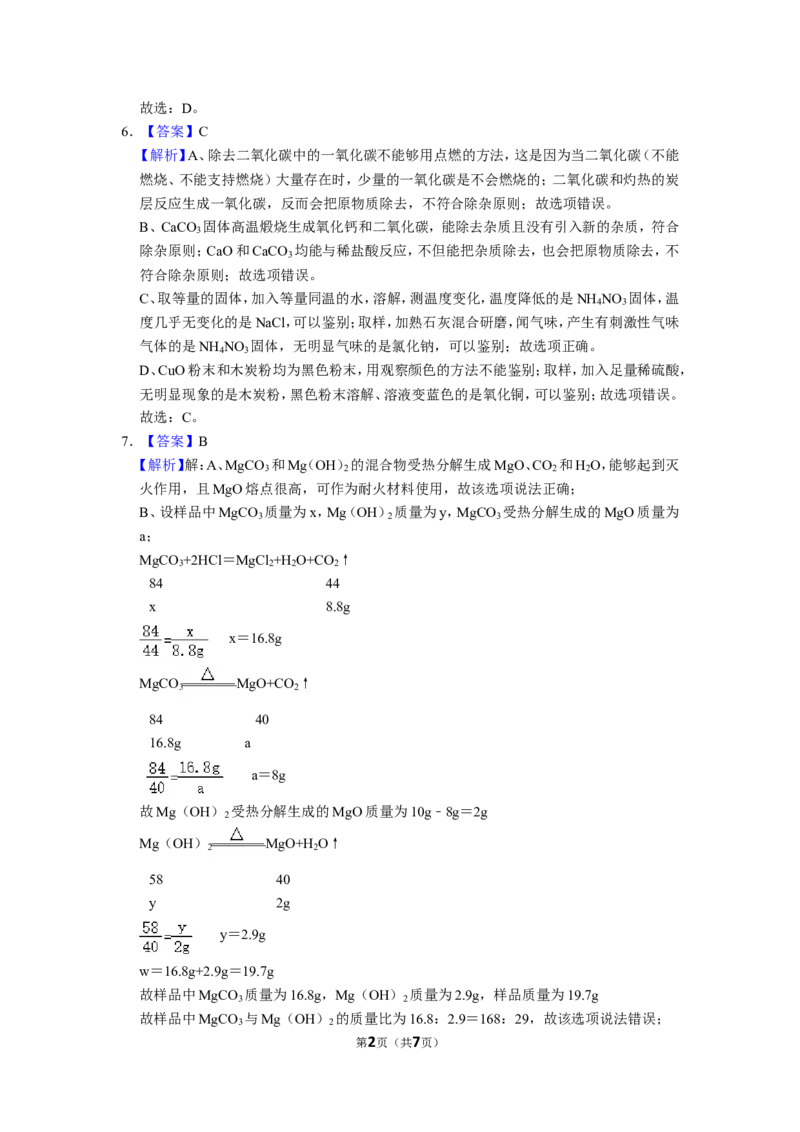
6.【答案】C
【解析】A、除去二氧化碳中的一氧化碳不能够用点燃的方法,这是因为当二氧化碳(不能
燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;二氧化碳和灼热的炭
层反应生成一氧化碳,反而会把原物质除去,不符合除杂原则;故选项错误。
B、CaCO 固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合
3
除杂原则;CaO和CaCO 均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不
3
符合除杂原则;故选项错误。
C、取等量的固体,加入等量同温的水,溶解,测温度变化,温度降低的是NH NO 固体,温
4 3
度几乎无变化的是NaCl,可以鉴别;取样,加熟石灰混合研磨,闻气味,产生有刺激性气味
气体的是NH NO 固体,无明显气味的是氯化钠,可以鉴别;故选项正确。
4 3
D、CuO粉末和木炭粉均为黑色粉末,用观察颜色的方法不能鉴别;取样,加入足量稀硫酸,
无明显现象的是木炭粉,黑色粉末溶解、溶液变蓝色的是氧化铜,可以鉴别;故选项错误。
故选:C。
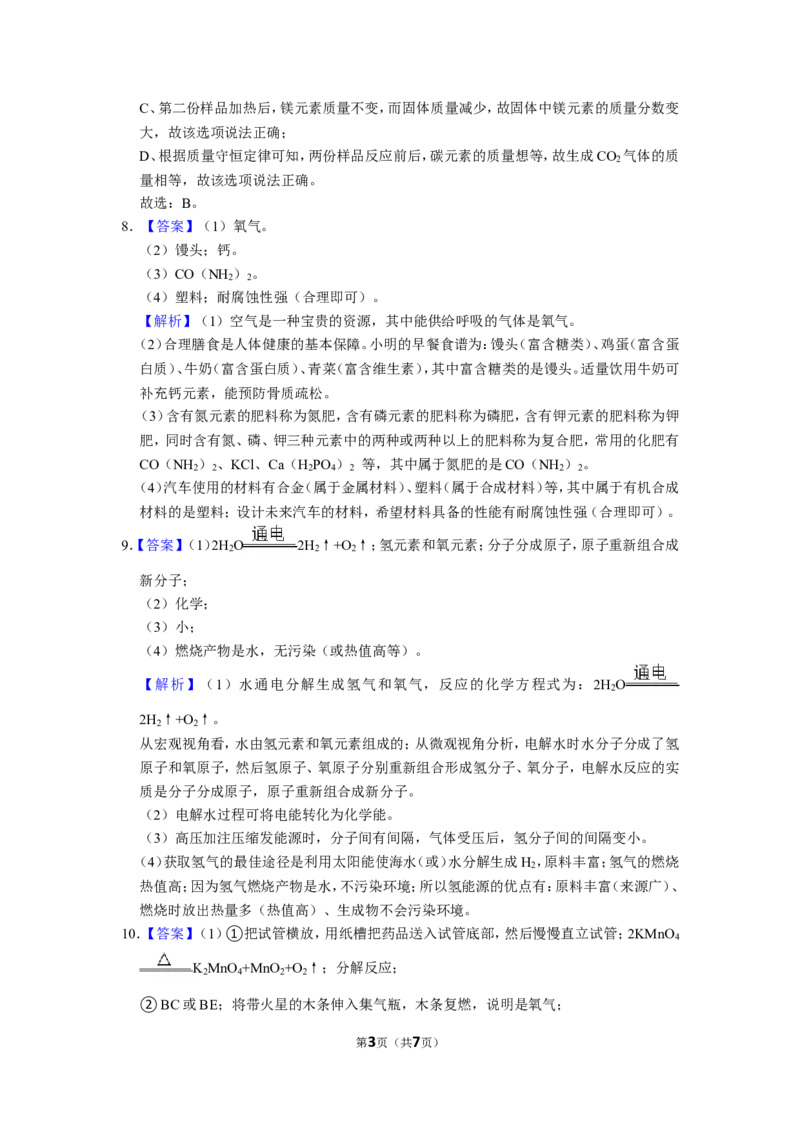
7.【答案】B
【解析】解:A、MgCO 和Mg(OH)的混合物受热分解生成MgO、CO 和H O,能够起到灭
3 2 2 2
火作用,且MgO熔点很高,可作为耐火材料使用,故该选项说法正确;
B、设样品中MgCO 质量为x,Mg(OH)质量为y,MgCO 受热分解生成的MgO质量为
3 2 3
a;
MgCO +2HCl=MgCl +H O+CO ↑
3 2 2 2
84 44
x 8.8g
x=16.8g
MgCO MgO+CO ↑
3 2
84 40
16.8g a
a=8g
故Mg(OH) 受热分解生成的MgO质量为10g﹣8g=2g
2
Mg(OH) MgO+H O↑
2 2
58 40
y 2g
y=2.9g
w=16.8g+2.9g=19.7g
故样品中MgCO 质量为16.8g,Mg(OH) 质量为2.9g,样品质量为19.7g
3 2
故样品中MgCO 与Mg(OH) 的质量比为16.8:2.9=168:29,故该选项说法错误;
3 2
第2页(共7页)C、第二份样品加热后,镁元素质量不变,而固体质量减少,故固体中镁元素的质量分数变
大,故该选项说法正确;
D、根据质量守恒定律可知,两份样品反应前后,碳元素的质量想等,故生成CO 气体的质
2
量相等,故该选项说法正确。
故选:B。
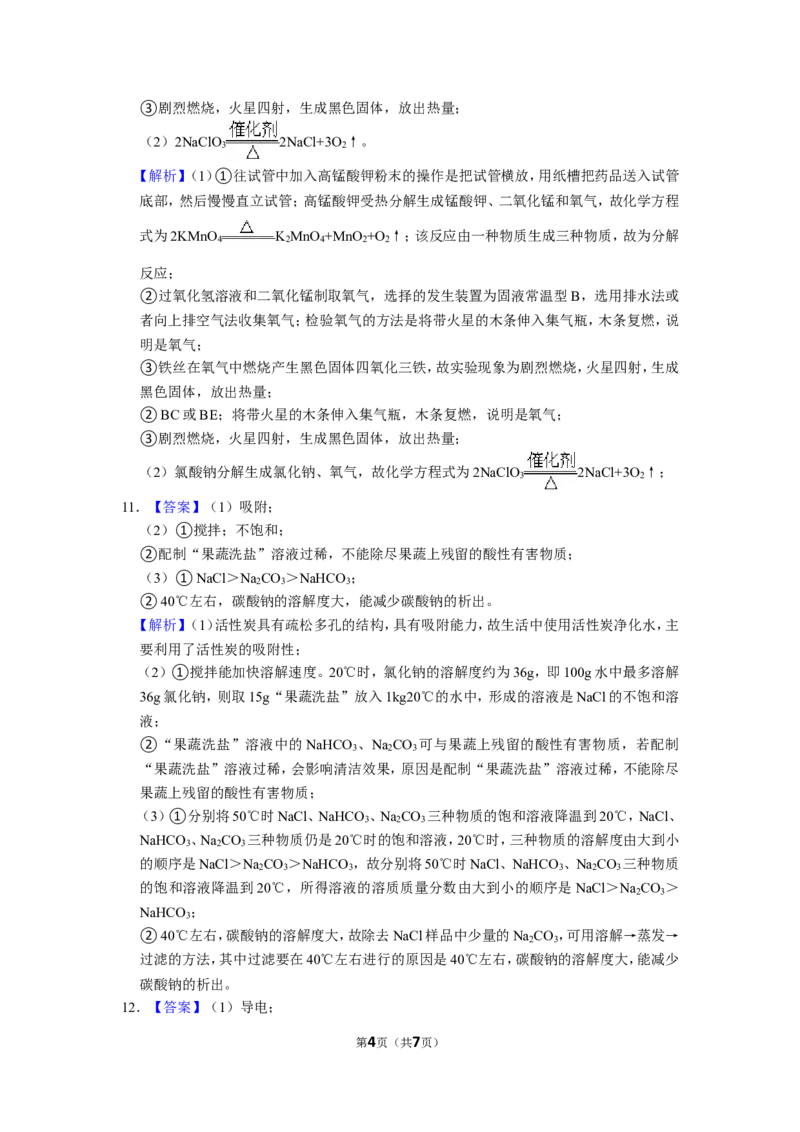
8.【答案】(1)氧气。
(2)馒头;钙。
(3)CO(NH ) 。
2 2
(4)塑料;耐腐蚀性强(合理即可)。
【解析】(1)空气是一种宝贵的资源,其中能供给呼吸的气体是氧气。
(2)合理膳食是人体健康的基本保障。小明的早餐食谱为:馒头(富含糖类)、鸡蛋(富含蛋
白质)、牛奶(富含蛋白质)、青菜(富含维生素),其中富含糖类的是馒头。适量饮用牛奶可
补充钙元素,能预防骨质疏松。
(3)含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾
肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥,常用的化肥有
CO(NH ) 、KCl、Ca(H PO ) 等,其中属于氮肥的是CO(NH ) 。
2 2 2 4 2 2 2
(4)汽车使用的材料有合金(属于金属材料)、塑料(属于合成材料)等,其中属于有机合成
材料的是塑料;设计未来汽车的材料,希望材料具备的性能有耐腐蚀性强(合理即可)。
9.【答案】(1)2H O 2H ↑+O ↑;氢元素和氧元素;分子分成原子,原子重新组合成
2 2 2
新分子;
(2)化学;
(3)小;
(4)燃烧产物是水,无污染(或热值高等)。
【解析】(1)水通电分解生成氢气和氧气,反应的化学方程式为:2H O
2
2H ↑+O ↑。
2 2
从宏观视角看,水由氢元素和氧元素组成的;从微观视角分析,电解水时水分子分成了氢
原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,电解水反应的实
质是分子分成原子,原子重新组合成新分子。
(2)电解水过程可将电能转化为化学能。
(3)高压加注压缩发能源时,分子间有间隔,气体受压后,氢分子间的间隔变小。
(4)获取氢气的最佳途径是利用太阳能使海水(或)水分解生成H ,原料丰富;氢气的燃烧
2
热值高;因为氢气燃烧产物是水,不污染环境;所以氢能源的优点有:原料丰富(来源广)、
燃烧时放出热量多(热值高)、生成物不会污染环境。
10.【答案】(1)①把试管横放,用纸槽把药品送入试管底部,然后慢慢直立试管;2KMnO
4
K MnO +MnO +O ↑;分解反应;
2 4 2 2
②BC或BE;将带火星的木条伸入集气瓶,木条复燃,说明是氧气;
第3页(共7页)③剧烈燃烧,火星四射,生成黑色固体,放出热量;
(2)2NaClO 2NaCl+3O ↑。
3 2
【解析】(1)①往试管中加入高锰酸钾粉末的操作是把试管横放,用纸槽把药品送入试管
底部,然后慢慢直立试管;高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,故化学方程
式为2KMnO K MnO +MnO +O ↑;该反应由一种物质生成三种物质,故为分解
4 2 4 2 2
反应;
②过氧化氢溶液和二氧化锰制取氧气,选择的发生装置为固液常温型B,选用排水法或
者向上排空气法收集氧气;检验氧气的方法是将带火星的木条伸入集气瓶,木条复燃,说
明是氧气;
③铁丝在氧气中燃烧产生黑色固体四氧化三铁,故实验现象为剧烈燃烧,火星四射,生成
黑色固体,放出热量;
②BC或BE;将带火星的木条伸入集气瓶,木条复燃,说明是氧气;
③剧烈燃烧,火星四射,生成黑色固体,放出热量;
(2)氯酸钠分解生成氯化钠、氧气,故化学方程式为2NaClO 2NaCl+3O ↑;
3 2
11.【答案】(1)吸附;
(2)①搅拌;不饱和;
②配制“果蔬洗盐”溶液过稀,不能除尽果蔬上残留的酸性有害物质;
(3)①NaCl>Na CO >NaHCO ;
2 3 3
②40℃左右,碳酸钠的溶解度大,能减少碳酸钠的析出。
【解析】(1)活性炭具有疏松多孔的结构,具有吸附能力,故生活中使用活性炭净化水,主
要利用了活性炭的吸附性;
(2)①搅拌能加快溶解速度。20℃时,氯化钠的溶解度约为36g,即100g水中最多溶解
36g氯化钠,则取15g“果蔬洗盐”放入1kg20℃的水中,形成的溶液是NaCl的不饱和溶
液;
②“果蔬洗盐”溶液中的NaHCO 、Na CO 可与果蔬上残留的酸性有害物质,若配制
3 2 3
“果蔬洗盐”溶液过稀,会影响清洁效果,原因是配制“果蔬洗盐”溶液过稀,不能除尽
果蔬上残留的酸性有害物质;
(3)①分别将50℃时NaCl、NaHCO 、Na CO 三种物质的饱和溶液降温到20℃,NaCl、
3 2 3
NaHCO 、Na CO 三种物质仍是20℃时的饱和溶液,20℃时,三种物质的溶解度由大到小
3 2 3
的顺序是NaCl>Na CO >NaHCO ,故分别将50℃时NaCl、NaHCO 、Na CO 三种物质
2 3 3 3 2 3
的饱和溶液降温到20℃,所得溶液的溶质质量分数由大到小的顺序是NaCl>Na CO >
2 3
NaHCO ;
3
②40℃左右,碳酸钠的溶解度大,故除去NaCl样品中少量的Na CO ,可用溶解→蒸发→
2 3
过滤的方法,其中过滤要在40℃左右进行的原因是40℃左右,碳酸钠的溶解度大,能减少
碳酸钠的析出。
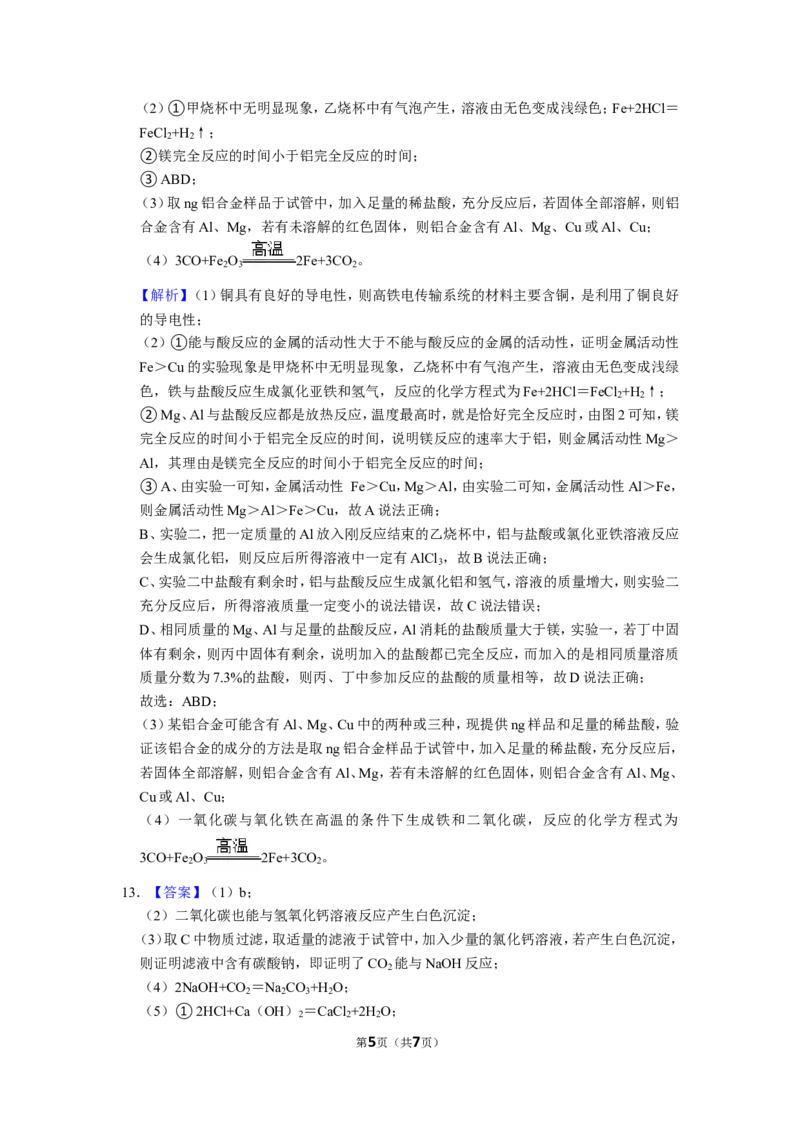
12.【答案】(1)导电;
第4页(共7页)(2)①甲烧杯中无明显现象,乙烧杯中有气泡产生,溶液由无色变成浅绿色;Fe+2HCl=
FeCl +H ↑;
2 2
②镁完全反应的时间小于铝完全反应的时间;
③ABD;
(3)取ng铝合金样品于试管中,加入足量的稀盐酸,充分反应后,若固体全部溶解,则铝
合金含有Al、Mg,若有未溶解的红色固体,则铝合金含有Al、Mg、Cu或Al、Cu;
(4)3CO+Fe O 2Fe+3CO 。
2 3 2
【解析】(1)铜具有良好的导电性,则高铁电传输系统的材料主要含铜,是利用了铜良好
的导电性;
(2)①能与酸反应的金属的活动性大于不能与酸反应的金属的活动性,证明金属活动性
Fe>Cu的实验现象是甲烧杯中无明显现象,乙烧杯中有气泡产生,溶液由无色变成浅绿
色,铁与盐酸反应生成氯化亚铁和氢气,反应的化学方程式为Fe+2HCl=FeCl +H ↑;
2 2
②Mg、Al与盐酸反应都是放热反应,温度最高时,就是恰好完全反应时,由图2可知,镁
完全反应的时间小于铝完全反应的时间,说明镁反应的速率大于铝,则金属活动性Mg>
Al,其理由是镁完全反应的时间小于铝完全反应的时间;
③A、由实验一可知,金属活动性 Fe>Cu,Mg>Al,由实验二可知,金属活动性Al>Fe,
则金属活动性Mg>Al>Fe>Cu,故A说法正确;
B、实验二,把一定质量的Al放入刚反应结束的乙烧杯中,铝与盐酸或氯化亚铁溶液反应
会生成氯化铝,则反应后所得溶液中一定有AlCl ,故B说法正确;
3
C、实验二中盐酸有剩余时,铝与盐酸反应生成氯化铝和氢气,溶液的质量增大,则实验二
充分反应后,所得溶液质量一定变小的说法错误,故C说法错误;
D、相同质量的Mg、Al与足量的盐酸反应,Al消耗的盐酸质量大于镁,实验一,若丁中固
体有剩余,则丙中固体有剩余,说明加入的盐酸都已完全反应,而加入的是相同质量溶质
质量分数为7.3%的盐酸,则丙、丁中参加反应的盐酸的质量相等,故D说法正确;
故选:ABD;
(3)某铝合金可能含有Al、Mg、Cu中的两种或三种,现提供ng样品和足量的稀盐酸,验
证该铝合金的成分的方法是取ng铝合金样品于试管中,加入足量的稀盐酸,充分反应后,
若固体全部溶解,则铝合金含有Al、Mg,若有未溶解的红色固体,则铝合金含有Al、Mg、
Cu或Al、Cu;
(4)一氧化碳与氧化铁在高温的条件下生成铁和二氧化碳,反应的化学方程式为
3CO+Fe O 2Fe+3CO 。
2 3 2
13.【答案】(1)b;
(2)二氧化碳也能与氢氧化钙溶液反应产生白色沉淀;
(3)取C中物质过滤,取适量的滤液于试管中,加入少量的氯化钙溶液,若产生白色沉淀,
则证明滤液中含有碳酸钠,即证明了CO 能与NaOH反应;
2
(4)2NaOH+CO =Na CO +H O;
2 2 3 2
(5)①2HCl+Ca(OH) =CaCl +2H O;
2 2 2
第5页(共7页)②ad;
(6)碱能与某些非金属氧化物反应,碱能与酸反应,碱能与指示剂反应,碱能与某些盐反
应;
(7)CO +3H CH OH+H O。
2 2 3 2
【解析】(1)二氧化碳的密度比油小,则连接A、B装置,将CO 从b端通入装有油的广口
2
瓶中封存,油被压入烧杯中;
(2)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,碳酸钠溶液与氢氧化钙溶液反应生成
碳酸钙沉淀和氢氧化钠,甲同学根据打开k ,观察到D中部分氢氧化钙溶液进入C中,有
2
白色沉淀产生,得出CO 能与NaOH反应,而二氧化碳也能与氢氧化钙溶液反应产生白色
2
沉淀,故乙同学认为甲同学得出结论的证据不足,理由是二氧化碳也能与氢氧化钙溶液反
应产生白色沉淀;
(3)要证明CO 能与NaOH反应,就是要证明反应生成了碳酸钠,则乙同学的方案是取C
2
中物质过滤,取适量的滤液于试管中,加入少量的氯化钙溶液,若产生白色沉淀,证明滤
液中含有碳酸钠,即证明了CO 能与NaOH反应;
2
(4)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,则用NaOH溶液“捕集CO ”的化学
2
方程式为2NaOH+CO =Na CO +H O;
2 2 3 2
(5)①氢氧化钙溶液显碱性,能使无色酚酞溶液变红,打开k ,观察到E中稀盐酸进入D
3
中,溶液变为无色,说明氢氧化钙与稀盐酸反应生成氯化钙和水,反应的化学方程式为
2HCl+Ca(OH) =CaCl +2H O;
2 2 2
②溶液变为无色,说明溶液中不存在氢氧化钙,则反应后的溶质成分是CaCl 或CaCl 和
2 2
HCl,氯化钙溶液呈中性,
a、酸性溶液能使紫色石蕊溶液变红,则可用紫色石蕊溶液来确定溶质成分,故a符合题意;
b、CuSO 溶液与盐酸不反应,无明显现象,故b不符合题意;
4
c、AgNO 溶液与氯化钙反应产生白色沉淀,与盐酸反应也能产生白色沉淀,现象相同,故
3
c不符合题意;
d、Fe O 固体能与盐酸反应生成氯化铁和水,可观察到固体逐渐溶解,溶液变成黄色,
2 3
Fe O 固体与氯化钙不反应,故d符合题意;
2 3
故选:ad;
(6)通过探究二,可归纳出碱的化学性质有碱能与某些非金属氧化物反应,碱能与酸反应,
碱能与指示剂反应,碱能与某些盐反应;
(7)利用CO 与H 在一定条件下反应生成甲醇(CH OH)和水,反应的化学方程式为
2 2 3
CO +3H CH OH+H O。
2 2 3 2
14.【解析】根据参加反应的氢气的质量,由反应的化学方程式列式计算出需要氧气的质量即
可。
解:设需要氧气的质量为x。
2H +O 2H O
2 2 2
第6页(共7页)4 32
40g x
x=320g
答:需要氧气的质量为320g。
第7页(共7页)