文档内容
命题猜想
本题考查元素周期律及相关知识,从今年的试题来看,命题方式趋向更加灵活多变,备
考时千万不要仅限于键线式! 特别提示:涉足多情境的呈现形式,典例力求全面,广开思路。
难点重点热点
熟知前20号元素及化合价的递变、非金属元素的成键数、粒子半径的比较、金属性与
非金属性的比较及相关的判据(如最简单氢化物的稳定性、最高价氧化物水化物
的酸碱性)、留意氢键、失重率。
重难录 点击 蓄势
重难 而发
1.【2022·江西·高三】 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、
Z为元素周期表前20号元素,已知W、X形成的化合物种类最多,Y原子最外层电子数是其电子层
数3倍,人体血液中缺乏Z离子易造成肌肉抽搐, 热分解可制备ZY,该化合物的热重
曲线如图所示。下列叙述不正确的是
A.150℃~200℃阶段热分解失去
B.400℃~600℃热分解后生成固体化合物
C.W、Y可形成具有杀菌消毒作用的化合物
D.化合物 具有还原性和强酸性
【答案】D【分析】W、X、Y、Z为元素周期表前20号元素,已知W、X形成的化合物种类最多,Y原子最外
层电子数是其电子层数3倍,说明为氧元素,W为碳元素,人体血液中缺乏Z离子易造成肌肉抽搐,
说明Z为钙元素。 应该为CaC O·H O,其相对分子质量为146,结合图可知原始固体质
2 4 2
量为146g,即1mol,据此分析。
【详解】A.150℃~200℃阶段热分解,质量从146克变为128克,少了1mol水的质量,即
1molCaC O·H O失去1molH O,故只是失去水,A正确;
2 4 2 2
B.400℃~600℃热分解,质量从128克变成100克,即1mol CaC O 固体失去1molCO,故生成固体
2 4
化合物为1molCaCO,B正确;
3
C.氢和氧可以形成过氧化氢,具有杀菌消毒的作用,C正确;
D.化合物 为草酸,具有还原性和弱酸性,D错误;
故选D。
2.【2022·全国·模拟预测】已知A、B、C、D、E是五种短周期主族元素,其原子半径与原子序数的
关系如图1,且A、B、C、D可形成化合物X如图2,C与E同主族。下列说法错误的是
A.A、B、D均可与C形成常见的两种二元化合物
B.简单离子的半径:E>D>C
C.最高价氧化物对应水化物的酸性:E>B
D.化合物X在低温的碱性溶液中更加稳定
【答案】B
【分析】根据原子半径与原子序数的关系图,A是第一周期元素,B、C是第二周期元素,C、D是
第三周期元素,A是H元素;根据A、B、C、D形成化合物X的结构图,B能形成4个共价键,B
是C元素;C能形成2个共价键,C是O元素;D能形成+1价阳离子,D是Na元素,O与E同主族,
E是S元素,以此来解析;
【详解】A.H与O能形成化合物HO、HO,Na与O能形成化合物NaO、NaO,C与O能形成
2 2 2 2 2 2
化合物CO、CO,A正确;
2
B.电子层数越多半径越大,电子层数相同,质子数越多半径越小,简单离子的半径:S2->O2->Na+,
B错误;
C.非金属性越强对应的最高价氧化物的水化物酸性越强,非金属性S>C,最高价氧化物的水化物酸
性HSO >H CO,C正确;
2 4 2 3
D.X为NaCO·H O,HO 受热易分解,NaCO 易与酸反应,化合物X在低温的碱性溶液中更加稳
2 3 2 2 2 2 2 3
定,D正确;故选B。
3.【2022·河南·焦作市第一中学模拟预测】X、Y、Z、W是原子序数依次增大的四种短周期元素,且
Y、Z、W位于同周期,甲、乙、丁、戊、己是由这些元素组成的常见二元化合物,丙是一种气体单
质,已知它们有如下转化关系(反应条件略):
下列说法错误的是
A.元素Z与元素W至少可组成5种化合物
B.乙可能是无色气体,也可能是有色气体
C.上述四种元素可以组成离子化合物
D.生成等物质的量的丙,反应①与反应②转移电子数相等
【答案】D
【分析】丁既是氧化物又是氢化物,因此丁是HO,戊是14电子分子,因此戊为CO,产物己为22
2
电子分子的氧化物,可推知己是CO。即X、Y、Z、W中,X是氢元素,Y、Z、W这三种同周期元
2
素中有两种元素是C、O,另一种元素与O形成了氧化物乙,因此另一种元素应该是N。故X、Y、
Z、W分别为H、C、N、O。
【详解】A.N与O两种元素可形成的化合物中,N有+1~+5五种价态,所以至少可以组合成5种化
合物,A正确;
B.由分析可知,乙是氮的氧化物,若是NO,则无色,若是NO ,则为红棕色,B正确;
2
C.上述四种元素可以形成离子化合物NH HCO ,C正确;
4 3
D.两个反应中,乙为氧化剂,乙得电子数即为反应转移电子数。反应①中,氮气中的氮元素来自甲、
乙两种物质,而反应②中,氮气中的氮元素来自乙,因此生成等物质的量的氮气,消耗的乙物质不
等量,故反应转移电子数不相等,D错误。
故本题选D。
4.【2023·全国·模拟预测】最近,科学家发现一种高能盐,该盐由X、Y、Z、M四种原子序数依次增
大的短周期元素组成,其化学式为(Y)(X Z)(YX )M.该盐的两种阳离子均为10电子离子,分别是
5 6 3 3 4 4
由X与Y、X与Z组成。化合物XM是18电子分子。下列说法错误的是
A.X与Y、X与Z还分别可形成10电子分子
B.该盐中存在离子键、极性共价键和非极性共价键
C.该盐的阴离子均可破坏水的电离平衡D.四种元素所形成的简单离子的半径由大到小为M>Y>Z>X
【答案】C
【分析】该盐由X、Y、Z、M四种原子序数依次增大的短周期元素组成,其化学式为
(Y)(X Z)(YX )M.该盐的两种阳离子均为10电子离子,分别是由X与Y、X与Z组成。化合物
5 6 3 3 4 4
XM是18电子分子,则X为H、Y为N、Z为O、M为Cl,X与Y、X与Z组成的10电子离子分别
为NH +、HO+。
4 3
【详解】A.X与Y、X与Z还分别可形成10电子分子分别为NH 、H0,A正确;
3 2
B.N-内存在非极性共价键,NH +、HO+内存在极性共价键,N-、Cl-、NH +、HO+阴、阳离子之间
5 4 3 5 4 3
存在离子键,B正确;
C.Cl-为强酸的酸根离子,在溶液中不会发生水解反应,不会破坏水的电离平衡,C错误;
D.四种元素所形成的简单离子的半径由大到小为Cl->N3->O2->H+,D正确;
答案选C。
【点睛】在比较主族元素原子、离子半径大小的时候注意以下几点:①电子层数越多,粒子半径越
大;②当电子层数相同、核外电子数相同时,核电荷数越大,粒子的半径越小;③当电子层数相同、
核电荷数相同时,核外电子数越多,半径越大。
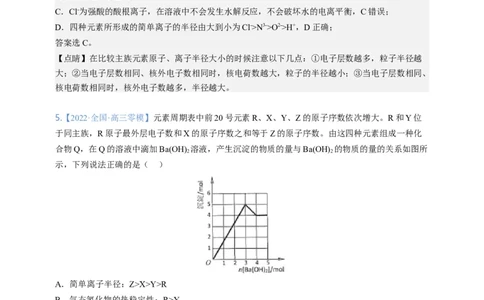
5.【2022·全国·高三零模】元素周期表中前20号元素R、X、Y、Z的原子序数依次增大。R和Y位
于同主族,R原子最外层电子数和X的原子序数之和等于Z的原子序数。由这四种元素组成一种化
合物Q,在Q的溶液中滴加Ba(OH) 溶液,产生沉淀的物质的量与Ba(OH) 的物质的量的关系如图所
2 2
示,下列说法正确的是( )
A.简单离子半径:Z>X>Y>R
B.气态氢化物的热稳定性:R>Y
C.Q的溶液中两种阳离子浓度相等
D.ZR 是含一种极性键的离子化合物
2 2
【答案】B
【分析】R、X、Y、Z为原子序数依次增大的前20号元素,R和Y位于同主族,R原子最外层电子
数和X的原子序数之和等于Z的原子序数,根据由四种元素组成一种化合物Q溶液中滴加Ba(OH)
2
溶液,产生沉淀的物质的量与Ba(OH) 的物质的量的关系图分析,先产生沉淀,后沉淀部分溶解,沉
2
淀可能是BaSO 和Al(OH) ,则Q为KAl(SO ),R为O元素,X为Al元素,Y为S元素,Z为K元
4 3 4 2
素,据此分析解答问题。【详解】A.R、X、Y、Z形成的简单离子分别为:O2-、Al3+、S2-、K+,O2-、Al3+电子层数均为2层,
而O的核电荷数小,则r(O2-)>r(Al3+),S2-、K+的电子层均为3层,S的核电荷数小,则r(S2-)>r(K+),
r(S2-)>r(K+)>r(O2-)>r(Al3+),即离子半径:Y>Z>R>X,A选项错误;
B.非金属性越强,气态氢化物的热稳定性越强,非金属性O>S,气态氢化物的热稳定性HO>HS,
2 2
即R>Y,B选项正确;
C.Q溶液为KAl(SO ) 溶液,由于Al3+水解,所以导致K+离子浓度大于Al3+浓度,C选项错误;
4 2
D.ZR 是KO,含有离子键和非极性共价键,D选项错误;
2 2 2 2
答案选B。
6.【2022·全国·模拟预测】已知X、Y、Z、W、M均为短周期元素。25℃时,其最高价氧化物对应的
水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是( )
A.X、M简单离子半径大小顺序:X>M
B.Z的最高价氧化物水化物的化学式为HZO
2 4
C.X、Y、Z、W、M五种元素中只有一种是金属元素
D.X的最简单氢化物与Z的氢化物反应后生成的化合物中既含离子键又含共价键
【答案】B
【分析】X、Y、Z、W、M均为短周期元素,由图象分析可知,原子半径:M>W>Z>Y>X,M的原
子半径最大且0.01mol/L最高价氧化物对应水化物溶液的pH=12,则M为Na元素,0.01mol/LW的最
高价氧化物对应水化物溶液的pH<2,则W为S元素,0.01mol/LZ的最高价氧化物对应水化物溶液的
pH=2,则Z为Cl元素,X的半径最小,其0.01mol/L的最高价氧化物对应水化物溶液的pH=2,则X
为N元素,0.01mol/LY的最高价氧化物对应水化物溶液的2Na+,A选项正确;
B.Z为Cl元素,其的最高价氧化物的水化物的化学式为HClO,B选项错误;
4
C.X、Y、Z、W、M五种元素中只有Na元素一种金属元素,C选项正确;
D.X的最简单氢化物为NH ,Z的氢化物为HCl,两者反应后生成的化合物为NH Cl,是离子化合
3 4
物,既含离子键由含有共价键,D选项正确;
答案选B。
【点睛】本题要求学生能够掌握原子半径变化规律、酸碱性与pH的关系等,并且能够将这些变化及
性质结合起来进行相关元素的判断,对学生的综合能力要求很高,在平时的学习中,要注意对相关知识点的总结归纳。
7.【2022·江西九江·高三】短周期常见元素X、Y、W、Z原子半径及主要化合价如图所示,下列叙
述正确的是
A.最高价氧化物水化物的碱性X小于Y
B.常温下,X、Y的单质都能溶于Z最高价氧化物对应水化物的浓溶液
C.氢化物的热稳定性W大于Z
D.X的单质在其所在周期的元素中还原性最强
【答案】C
【分析】W的化合价为−2价,没有最高正化合价+6价,故W为O元素;Z元素的化合价为
+5、+3、−3,Z处于第ⅤA族,原子半径与氧元素相差不大,则Z与氧元素处于同一周期,故Z为
N元素;X的化合价为+2价,则X应为ⅡA族元素,Y的化合价为+3价,Y处于第ⅢA族,二者原
子半径相差较小,可知两者位于同一周期相邻主族,由于X、Y的原子半径与W、Z原子半径相差很
大,则X、Y应在第三周期,所以X为Mg元素,Y为Al元素,以此解答。
【详解】A.同周期主族元素随原子序数增大,金属性减弱,故金属性Mg>Al,则碱性
Mg(OH) >Al(OH) ,故A错误;
2 3
B.常温下,Al能溶于NaOH溶液,但Mg不能和氢氧化钠溶液反应,故B错误;
C.非金属性O>N,则氢化物的热稳定性HO>NH ,故C正确;
2 3
D.Mg的单质在其所在周期为第三周期,该周期元素中还原性最强的是Na,故D错误;
故选C。
8.【2022·广东广州·模拟预测】短周期元素X、Y、Z、M的原子序数依次增大,它们组成一种团簇分
子,结构如图所示。X、M的族序数均等于周期序数,Y原子核外最外层电子数为6,下列说法正确
的是A.简单离子半径:Z>M>Y
B.第一电离能:Y>M>Z
C.工业上常用电解熔融物ZY制取Z单质
D.Z为镁元素
【答案】D
【分析】短周期元素X、Y、Z、M的原子序数依次增大,X、M的族序数均等于周期序数,Y原子
核外最外层电子数为6,则X是H,M是Al,Y是O,根据团簇分子结构发现Z的原子半径大于
M,大于Y,所以Z元素应该和M同周期,再结合团簇分子发现,H原子2个,O原子6个,Al原
子2个,Z原子2个,根据化合物化合价总和推断出Z元素是Mg。
【详解】A.电子层结构相同时,核电荷数越大半径越小,则简单离子半径:Y>Z>M,A错误;
B.非金属元素第一电离能通常大于金属元素第一电离能,Mg最外层电子排布式为3s2全满而稳定,
第一电离能比Al大,即第一电离能Y>Z>M,B错误;
C.MgCl 熔点远低于MgO,为节约能耗用电解熔融MgCl 制取Mg单质,C错误;
2 2
D.据分析知,Z为镁元素,D正确;
故选D。
9.【2022·四川乐山·一模】X、Y、Z、W四种短周期元素在周期表中的位置如图所示,元素Z的核电
荷数是元素Y的两倍,下列有关说法不正确的是
X Y
Z W
A.原子半径:X> Y
B.简单阴离子还原性:Z> W
C.元素X、Y的单质在放电条件下生成红棕色气体
D.四种元素的简单氢化物中,Y的氢化物沸点最高
【答案】C
【分析】由题干信息结合四种元素在周期表中的位置可知,元素Z的核电荷数是元素Y的两倍,则
Y是O,Z为S,X为N,W为Cl,据此分析解答。
【详解】A.X为N,Y是O,原子半径:N>O,故A错误;
B.Z的简单阴离子:S2-、W的简单阴离子:Cl-还原性:S2-> Cl-,故B正确;C.元素X、Y的单质即氮气和氧气,在放电条件下生成一氧化氮,为无色气体,故C错误;
D.四种元素的简单氢化物分别为:NH 、HO、HS、HCl,其中HO中存在氢键,沸点最高,故D
3 2 2 2
正确;
故答案选C。
10.【2022·四川巴中·一模】短周期元素R、X、Y、Z、M原子序数依次递增,最外层电子数:
3Z+M=X+Y,其中元素R、X、Y、M形成的化合物(结构式)具有如图所示转化关系。下列说法错误
的是
A.简单气态氢化物的稳定性: Y>X
B.在该化合物中X最外层均满足8e-的结构
C.M的最高价氧化物对应水化物为强酸
D.Y分别与R、X、Z、M形成的化合物中均属于共价化合物
【答案】D
【分析】短周期元素R、X、Y、Z、M原子序数依次递增,由图知,R、X、Y、M的共用电子对数
分别为1、4、2和1,则R、X、Y、M分别为H、C、O和Cl,按最外层电子数:3Z+M=X+Y,可得
Z最外层为1电子,则Z为Na,据此回答;
【详解】A.X为C、Y为O,非金属性越强,简单氢化物越稳定,则简单气态氢化物的稳定性:
Y>X,A正确;
B.X为C,在该化合物中C都能共用四对电子对,则最外层均满足8e-的结构,B正确;
C.M为Cl,M的最高价氧化物对应水化物即高氯酸为强酸,C正确;
D.Z即Na与Y即O形成的化合物过氧化钠中既含离子键又有共价键,属于离子化合物,D错误;
答案选D。
热点集 点击 核心
热点 猜想
11.【2022·河南·模拟预测】已知W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半
径在元素周期表中最小, 可以与 反应生成一种常见的气体。化合物( )在 和
气氛中的热重曲线(样品质量随温度变化的曲线)如图所示。下列有关说法错误的是A.原子半径:Z>X>Y>W
B.A,B、C是三种不同的盐
C.无论是 气氛还是 气氛,A→B阶段均发生了氧化还原反应,但两者的气态产物不同
D.在酸性 溶液中加入少量A固体样品时,溶液褪色且有少量气泡产生
【答案】B
【分析】W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半径在元素周期表中最小,
W是H元素; 可以与 反应生成一种常见的气体,CaO 和CO 反应生成碳酸钙和氧气,所以
2 2
X是C元素、Y是O元素、Z是Ca元素。
【详解】A.原子半径:Ca>C>O>H,故A正确;
B. 中 的质量分数为87.7%,所以A是 ; 中CaCO 的质量
3
分数为68.5%,所以B是CaCO ; 中CaO的质量分数为38.4%,所以C是CaO,故B
3
错误;
C.无论是 气氛还是 气氛,A→B阶段均发生反应 ,C元素化合价改变,都发
生氧化还原反应,在 气氛中生成的气体产物是CO,在O 氛围中气态产物是CO,故C正确;
2 2
D.在酸性 溶液中加入少量 固体样品时, 被氧化为二氧化碳,溶液褪色且有
少量气泡产生,故D正确;
选B。
12.【2022·新疆·(华中师大一附中博乐分校)三模】X、Y、Z、R、M为原子序数依次增大的短周
期元素,其原子的最外层电子数与原子半径的关系如图所示。下列说法不正确的是A.X的原子与Y、Z、R、M的原子均可形成共价化合物
B.Y形成的化合物种类最多
C.R与M形成的化合物溶于水,会促进水的电离
D. 在同周期元素的简单阳离子中,半径最大
【答案】A
【分析】X、Y、Z、R、M为原子序数依次增大的短周期元素,一般来说,原子电子层数越多,原子
半径越大,同一周期从左到右,原子半径依次减小,最外层电子数等于主族序数,结合原子的最外
层电子数与原子半径的关系图可知,X与R在IA族,R的半径更大,X半径比其它元素原子小,故
X为H,R为Na;M在VIA族,半径比Y、Z的大,Y在IVA族,Z在VA族,则Y为C,Z为N,
M为S。
【详解】A.H与C,N,Na和S均可以形成化合物,但NaH为离子化合物,A错误;
B.Y为C元素,可形成有机物,种类繁多,B正确;
C.NaS为钠盐,溶于水,同时硫离子对应的酸为二元弱酸,所以硫离子会水解,促进水的电离,C
2
正确;
D.Na+为第三周期离子半径最大的阳离子,D正确;
故答案选A。
13.【2022·广西玉林·一模】原子序数依次增大的短周期元素X、Y、Z、R,含0.9%YR的水溶液称
为生理盐水,X、Y、Z三种元素组成两种化合物a、b的性质如图,Z的质子数是X质子数的2倍。
下列说法错误的是
A.原子半径:Y>Z>R>X
B.简单气态氢化物的稳定性:R>Z
C.化合物a的水溶液呈中性
D.X、Y形成的一种化合物中可能含有离子键和共价键
【答案】C
【分析】原子序数依次增大的短周期元素X、Y、Z、R,含0.9%YR的水溶液称为生理盐水,则Y为Na、R为Cl;X、Y、Z三种元素组成两种化合物a、b,a与HCl反应生成的气体可使品红褪色,
该气体为二氧化硫,a为亚硫酸钠;a与R (Cl)或X的氢化物反应生成b,则b为硫酸钠,则X为
2 2
O,Z为S元素,满足“Z的质子数是X质子数的2倍”。
【详解】A.同周期元素原子半径随核电荷数的增大而减小,电子层数越多原子半径越大,因此原子
半径Na>S>Cl>O,A正确;
B.Cl非金属性强于S,因此简单气态氢化物稳定性R>Z,B正确;
C.a为亚硫酸钠,其水解呈碱性,C错误;
D.O和Na可以形成NaO,其中含有离子键和共价键,D正确;
2 2
故答案选C。
14.【2022·上海静安·二模】X、Y、Z、R、M为原子序数依次增大的五种短周期元素,其原子半径
和最外层电子数之间的关系如图所示。下列说法正确的是
A.Y、Z、M属于同一周期,非金属性依次增强
B.Z、M的氧化物对应水化物均为强酸
C.X、M形成的化合物具有还原性,水溶液呈酸性
D.X与其他四种元素都能形成共价键
【答案】C
【分析】根据半径大小及最外层电子数可推断,X为H,Y为C,Z为N,R为Na,M为S;
【详解】A.同周期元素随原子序数递增,原子半径递减(除去0族元素),M原子半径大于Z,说明
不是同周期元素,A错误;
B.Z为氮元素,其氧化物多种,且水化物也存在HNO 这类的弱酸,M为硫元素,其氧化物有
2
SO 、SO ,SO 的水化物HSO 是弱酸,B错误;
2 3 2 2 3
C.HS有强还原性,溶于水具有酸性,溶液称为氢硫酸,C正确;
2
D.H元素与Na元素的原子之间无法形成共价键,D错误;
综上,本题选C。
15.【2022·河北·高考真题】两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依次增大的
五种短周期主族元素,下列说法错误的是A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
【答案】A
【分析】X、Y、Z、R、Q是原子序数依次增大的五种短周期主族元素,由两种化合物的结构示意图
可知,X、Y、Z、R、Q形成共价键的数目分别为4、3、2、1、5,则五种元素分别为C元素、N元
素、O元素、F元素、P元素。
【详解】A.由两种化合物的结构示意图可知,化合物中磷原子的最外层电子数为10,不满足最外
层8电子稳定结构,故A错误;
B.C元素、N元素、O元素、F元素、P元素中位于元素周期表右上角的氟元素的非金属性最强,
元素的非金属性越强,简单氢化物的稳定性最强,故B正确;
C.红棕色二氧化氮转化为无色四氧化二氮的反应为放热反应,降低温度,平衡向正反应方向移动,
气体的颜色变浅,则将装有二氧化氮气体的透明密闭容器浸入冰水中,气体颜色变浅,故C正确;
D.氧气和臭氧是氧元素形成的不同种单质,互为同素异形体,臭氧层破坏会造成环境污染,则臭氧
在大气中的含量与环境污染密切相关,故D正确;
故选A。
16.【2022·全国·模拟预测】离子液体具有电导率高、熔点低、不燃烧、热稳定性高等优越性能,在
电池电解质领域展现了良好的应用前景。某离子液体W的结构如图所示,其中M、N、Y、Z、Q、
X是原子序数依次递增的短周期主族元素。下列分析错误的是
A.原子半径:M>Y>Z>Q
B.最高价氧化物对应的水化物的酸性强弱:Y<X<Z<Q
C.少量M单质的保存方法是密封在固体石蜡中
D.常温下元素Q对应的单质可以发生置换反应生成Z的单质
【答案】B
【分析】由W的结构可知,M+可能为Li+或Na+,根据成键特点,Q形成一根键,Q可能为H、F或
Cl,N形成四根键,可能为C或Si,Z形成两根键,可能为O或S,X形成六根键,X为S,则Z为O,Y形成两根键同时得到一个电子,Y为N或P,其中M、N、Y、Z、Q、X是原子序数依次递增
的短周期主族元素,则M为Li,N为C,Y为N,Z为O,Q为F,X为S,据此解答。
【详解】A. 同周期元素从左至右原子半径逐渐减小,故原子半径:M>Y>Z>Q,故A正确;
B.O没有最高正价,F没有正价,故B错误;
C.M为Li,锂的密度比煤油小,则少量锂单质的保存方法是密封在固体石蜡中,故C正确;
D.氟气很活泼,常温下氟气与水可以发生置换反应生成氧气, ,故D正确;
故选B。
17.【2022·江西赣州·高三】X、Y、Z、W的原子序数依次增大, 为10电子化合物,Y与Z是位
于同一主族的短周期元素。取 g由这四种元素组成的固体物质------- (摩尔质量为
)逐渐升温加热,得到固体质量与温度的关系如图所示,下列说法正确的是
A.最简单氢化物的沸点:
B.Y与X、Z、W均能形成两种化合物
C.b点对应的物质为
D.向e点对应的固体中加入稀硫酸后生成蓝色溶液和红色固体,发生了非氧化还原反应
【答案】B
【分析】由 为10电子化合物,再结合 的分子组成可知, 为 , 为 ,Y与Z
是位于同一主族的短周期元素, 为 ,再根据 的摩尔质量为250g/mol推出 为 。
【详解】A.水分子间能形成氢键,水的沸点高于 ,故A错误;
B.O与H能形成HO、HO 两种混合物;O与S能形成SO 、SO 两种混合物;O与Cu能形成
2 2 2 2 3
Cu O、CuO两种混合物,故B正确;
2
C.从图中可以看出,b点对应的物质的摩尔质量为 ,则该物质的化学式为 ,
故C错误;
D.根据铜元素守恒,e对应固体中铜元素的质量为 ,则氧元素的质量为
,n(Cu):n(O)= , 点对应的物质为 ,加入稀硫酸后发生反应:,该反应为氧化还原反应,故D错误;
选B。
18.【2022·四川雅安·模拟预测】短周期主族元素X、Y、Z、W的原子序数依次增大。X是地壳中含
量最高的元素,Z与X同主族,W的最外层电子数等于Y与Z的最外层电子数之和。下列说法错误
的是
A.简单离子的还原性:X>W>Z
B.简单氢化物的沸点:X>Z
C.X、Y形成的化合物一定含离子键
D.X、Y、W形成的一种化合物可用于消毒杀菌
【答案】A
【分析】短周期主族元素X、Y、Z、W的原子序数依次增大。X是地壳中含量最高的元素,为氧;
Z与X同主族,则Z为硫、W为氯;W的最外层电子数等于Y与Z的最外层电子数之和,则Y为钠。
【详解】A.同周期从左到右,金属性减弱,非金属性变强;同主族由上而下,金属性增强,非金属
性变弱;元素非金属越强,对应简单离子的还原性越弱,简单离子的还原性:Z >W> X,A错误;
B.水分子能形成氢键,导致沸点升高,故简单氢化物的沸点:X>Z,B正确;
C.X、Y形成的化合物可以为氧化钠或过氧化钠,一定含离子键,C正确;
D.X、Y、W形成的一种化合物NaClO具有强氧化性,可用于消毒杀菌,D正确;
故选A。
19.【2022·广东·东莞市东华中学模拟预测】W、X、Y、Z是原子序数依次增大的短周期主族元素,
其最外层电子数之和为19。W与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是W原
子内层电子数的2倍。下列说法正确的是
A.原子半径:Y>X>W B.单质的熔点:Y>X>W
C.简单氢化物的沸点:Z>W D.Z的最高价含氧酸一定是强酸
【答案】B
【分析】W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X、Y、Z不在同一周期,Y原
子最外层电子数为W原子内层电子数的2倍,则W应为第二周期元素,X、Y、Z位于第三周期,Y
的最外层电子数为4,则Y为Si元素;X、Y相邻,且X的原子序数小于Y,则X为Al元素;W、
X、Y、Z的最外层电子数之和为19,则W、Z的最外层电子数之和为19-3-4=12,主族元素的最外层
电子数最多为7,若W的最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若W的
最外层电子数为6,为O元素,则Z的最外层电子数为6,为S元素,若W的最外层电子数为5,为
N元素,Z的最外层电子数为7,为Cl元素,则W为N元素或O元素或F元素,X为Al元素,Y为
Si元素,Z为Cl元素或S元素或P元素,以此分析解答。
【详解】
A.同周期从左至右,原子半径减小,原子半径Al>Si,A错误;B.单质熔点Si>Al>W,W单质为氮气或氧气或氟气,B正确;
C.W的简单氢化物分子间存在氢键,简单氢化物的沸点W>Z,C错误;
D.若Z为P元素,最高价含氧酸磷酸是弱酸,D错误;
故选B。
20.【2022·河南焦作·一模】X、Y、Z、W、Q、R是原子序数依次增大的短周期主族元素,同主族的
元素只有X和Q;它们组成的常见二元化合物A、B、C、D、G有如下转化关系。常温下A是一种
常见液体,B、C、G是气体,D是常用的食品调味剂和防腐剂。下列说法中错误的是
A.由H与G在溶液中的反应可以判断R的非金属性强于Y
B.化合物的稳定性:A>C
C.E、H的溶液呈碱性,F的溶液呈酸性
D.实验室一般不用加热F固体的方法制备C气体
【答案】A
【分析】X、Y、Z、W、Q、R是原子序数依次增大的短周期主族元素,同主族的元素只有X和Q;
它们组成的常见二元化合物A、B、C、D、G有如下转化关系。常温下A是一种常见液体,A为
HO, D是常用的食品调味剂和防腐剂,则D为NaCl,B、C、G是气体,结合流程可推出B为
2
CO,C为NH ,饱和食盐水中通入氨气和二氧化碳反应生成氯化铵F和碳酸氢钠E,E受热分解生成碳
2 3
酸钠H、和二氧化碳、水;氯化铵受热分解生成氨气C和氯化氢G,氯化氢与碳酸钠反应生成氯化
钠、二氧化碳和水。故涉及元素X、Y、Z、W、Q、R分别是H、C、N、O、Na、Cl。
【详解】A. 盐酸不是氯元素的最高价氧化物的水化合,不能由H(Na CO)与G(HCl)在溶液中的反应
2 3
可以判断R的非金属性强于Y,选项A错误;
B. 元素非金属性越强其气态氢化物的稳定性越强,故化合物的稳定性:A(H O)>C(NH ),选项B正
2 3
确;
C. E、H分别为碳酸氢钠、碳酸钠,均为强碱弱酸盐,溶液呈碱性,F为氯化铵,为强酸弱碱盐,溶
液呈酸性,选项C正确;
D. 实验室一般不用加热F(氯化铵)固体的方法制备C气体,因产生的氯化氢和氨气遇冷又反应生成
氯化铵,选项D正确;
答案选A。