文档内容
命题猜想
本题注重思维的开放性与创新性,尤其关注探究性实验。必须要有针对性的训练。
难点重点热点
小流程形式的考查,突出主干知识,同时兼顾实验方法的选择。面对探究式实验,一定
要多留意条件与结果的逻辑关联,强调变量的控制。
重难录 点击 蓄势
重难 而发
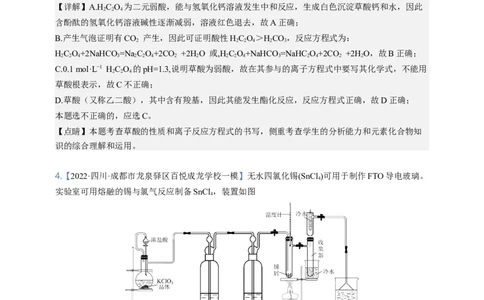
1.【2022·广东佛山·一模】某同学利用下图装置制备 并进行相关性质探究。下列说法错误的是
A.装置a中反应为非氧化还原反应B.装置b的作用是防止倒吸
C.装置c中最终有沉淀生成 D.装置d中反应:
【答案】C
【详解】A.装置a中反应是复分解反应,为非氧化还原反应,A正确;
B.装置b是安全瓶,作用是防止倒吸,B正确;
C.二氧化硫与氯化铁发生氧化还原反应,没有沉淀生成,C错误;
D.二氧化硫使高锰酸钾溶液褪色发生反应 ,D正确;
故选C。2.【2022·全国·模拟预测】价类二维图是学习元素及其化合物知识的重要模型和工具。图1为某常见
金属单质及其部分化合物的价类二维图。下列推断不合理的是
A.b,c均可与氢碘酸反应,但反应原理不同
B.h具有强氧化性,可用于饮用水的消毒,还原产物可以净水
C.可通过图2装置制备物质e,且较长时间不易被氧化
D.a→f→g→d的每步转化均可一步实现
【答案】C
【分析】根据该金属元素的价类二维图,该元素的化合价有0、+2、+3、+6价,可知该元素为Fe,a
为铁单质、b为FeO,c为Fe(OH) 、f为亚铁盐、d为Fe(OH) 、e为Fe O,g为铁盐,h为高铁盐。
3 3 2 3
【详解】A.根据分析,b、e分别为FeO和Fe O,HI与FeO的反应为酸与碱性氧化物的反应,而
2 3
HI与Fe O 反应时,由于Fe3+可以氧化I-,还会发生氧化还原反应,原理不同,A正确;
2 3
B.根据分析,h为高铁盐,+6价的铁具有强氧化性,可用于饮用水的消毒,还原产物Fe3+可以形成
Fe(OH) 胶体,可以净水,B正确;
3
C.图2装置A管中的导管没有插到液面以下,生成的FeSO 无法压入B管中,不能形成Fe(OH) ,
4 2
C错误;
D.Fe与硫酸或盐酸反应可以生成亚铁盐(Fe2+),可以被Cl、HO 等氧化剂氧化为铁盐(Fe3+),
2 2 2
铁盐中加强碱(NaOH等)可以生成Fe(OH) ,均可以一步实现,D正确;
3
故选C。
3.【2019·北京】探究草酸(HC O)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 HC O 的
2 2 4 2 2 4
pH=1.3)
实验 装置 试剂a 现象
① Ca(OH) 溶液(含酚酞) 溶液褪色,产生白色沉淀
2
② 少量NaHCO 溶液 产生气泡
3
③ 酸性KMnO 溶液 紫色溶液褪色
4
④ C HOH和浓硫酸 加热后产生有香味物质
2 5由上述实验所得草酸性质所对应的方程式不正确的是A.HC O 有酸性,Ca(OH) + H C O
2 2 4 2 2 2 4
CaC O↓+2H O
2 4 2
B.酸性:HC O> H CO,NaHCO + H C O NaHC O+CO ↑+H O
2 2 4 2 3 3 2 2 4 2 4 2 2
C.HC O 具有还原性,2 +5 +16H+ 2Mn2++10CO ↑+ 8H O
2 2 4 2 2
D.HC O 可发生酯化反应,HOOCCOOH+2C HOH C HOOCCOOC H+2H O
2 2 4 2 5 2 5 2 5 2
【答案】C
【分析】草酸(又称乙二酸)为一种二元弱酸,具有酸的通性,因此能发生中和反应,具有还原性,
因为乙二酸中含有羧基因此能发生酯化反应,据此解题;
【详解】A.HC O 为二元弱酸,能与氢氧化钙溶液发生中和反应,生成白色沉淀草酸钙和水,因此
2 2 4
含酚酞的氢氧化钙溶液碱性逐渐减弱,溶液红色退去,故A正确;
B.产生气泡证明有CO 产生,因此可证明酸性HC O>HCO,反应方程式为:
2 2 2 4 2 3
HC O+2NaHCO=Na C O+2CO +2H O 或,H C O+NaHCO=NaHC O+2CO +2H O,故B正确;
2 2 4 3 2 2 4 2 2 2 2 4 3 2 4 2 2
C.0.1 mol·L−1 HC O 的pH=1.3,说明草酸为弱酸,故在其参与的离子方程式中要写其化学式,不能用
2 2 4
草酸根表示,故C不正确;
D.草酸(又称乙二酸),其中含有羧基,因此其能发生酯化反应,反应方程式正确,故D正确;
本题选不正确的,应选C。
【点睛】本题考查草酸的性质和离子反应方程式的书写,侧重考查学生的分析能力和元素化合物知
识的综合理解和运用。
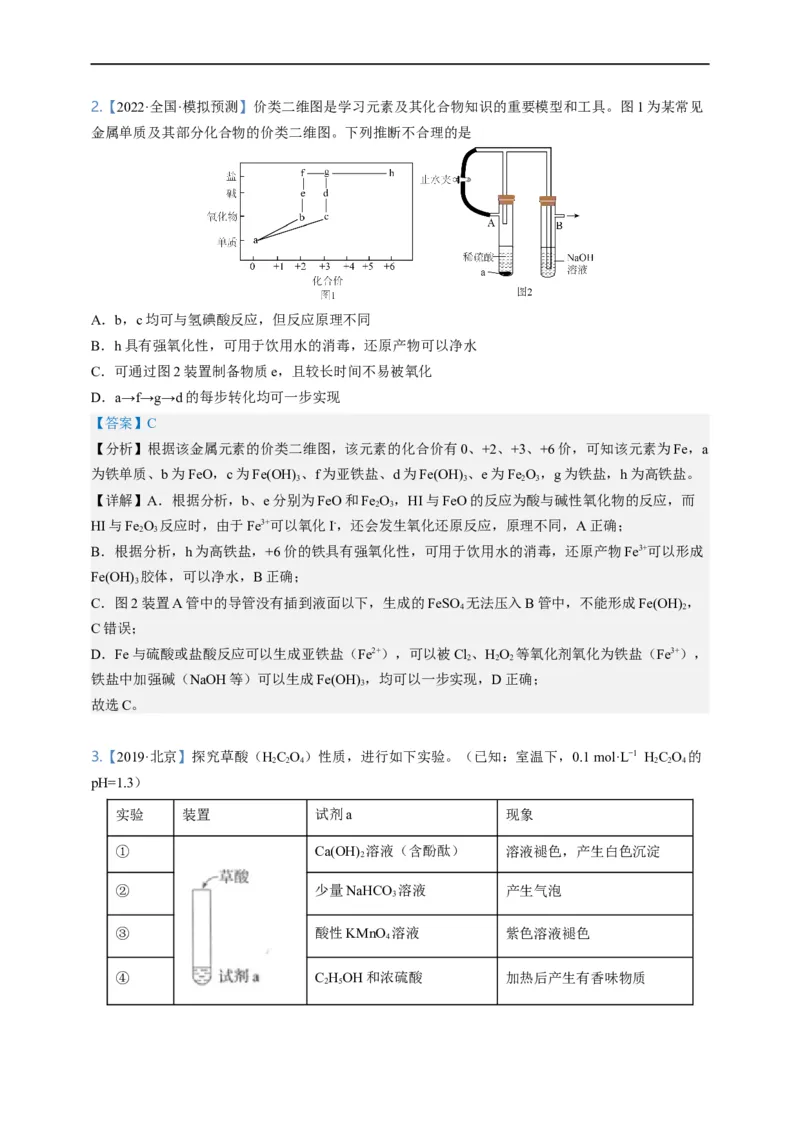
4.【2022·四川·成都市龙泉驿区百悦成龙学校一模】无水四氯化锡(SnCl )可用于制作FTO导电玻璃。
4
实验室可用熔融的锡与氯气反应制备SnCl ,装置如图
4
已知:①Sn、SnCl 、SnCl 有关的物理性质如下表所示:
2 4
物质 熔点/℃ 沸点/℃ 颜色、状态
Sn 232 2260 银白色固体
246 623 无色晶体114 无色液体
②Sn的性质与Fe相似;SnCl 在空气中极易水解;Cl 易溶于SnCl 。
4 2 4
下列关于上述实验说法错误的是A.A装置不能换成启普发生器,C中盛放浓硫酸,F中盛放浓
NaOH溶液
B.收集器中收集到的液体略显黄色,是因为有部分Cl 溶解在了SnCl 中,可加入饱和NaSO 溶液
2 4 2 3
萃取提纯SnCl
4
C.当观察到装置F上方出现黄绿色气体现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,
目的是加快反应速率
D.本实验装置有缺陷,需要改进,应在装置E、F之间添加一个装浓硫酸的洗气瓶
【答案】B
【分析】A制备氯气,B装置除氯气中的氯化氢,C装置干燥氯气,D中锡和氯气在加热条件下反应
生成SnCl 蒸气,E装置收集SnCl ,F装置吸收氯气,防止污染。
4 4
【详解】A.KClO 晶体不是块状固体,它和浓盐酸反应的发生装置不能使用启普发生器,B中盛放
3
饱和食盐水,除去 中的氯化氢气体;C中盛放浓硫酸,除去 中的水蒸气;F中盛放浓NaOH溶
液,用于尾气 的吸收,故A正确;
B. 极易水解,故除去 中的部分 应选择蒸馏操作,故B错误;
C.当观察到装置F上方出现黄绿色气体现象时,此时装置中的空气被排空,才开始点燃酒精灯,则
可防止锡被O 氧化,待锡熔化后适当增大氯气流量,目的是加快反应速率,故C正确;
2
D.为防止F装置中的水蒸气进入收集器,使 水解,产品变质,在装置E、F之间添加一个装浓
硫酸的洗气瓶,故D正确;
选B。
5.【2022·河南·模拟预测】某同学设计下列装置制备少量 (沸点为128.7℃,能与水、乙
醇以任意比混溶)。下列说法正确的是
A.配制乙醇与浓硫酸混合液的方法是:在不断搅拌下向浓硫酸中加入乙醇B.装置b中可盛放酸性 溶液以除去 杂质
C.装置c中发生的反应为
D.最后用分液的方法从装置c中分离出
【答案】C
【详解】A.浓硫酸的密度比乙醇的大,应在不断搅拌下向乙醇中加入浓硫酸,A项错误;
B.装置b中应盛放浓的 溶液,因高锰酸钾溶液可氧化乙烯,B项错误;
C. 先与水反应生成 , 再与乙烯加成,C项正确;
D. 与水互溶,应先中和再蒸馏,D项错误;
答案选C。
6.【2022·广东广州·模拟预测】实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中
含有 和白色物质X,下列说法正确的是
A.X溶液显无色 B.NO和Y均为还原产物
C.浓硫酸在反应中表现出氧化性和酸性 D.NO与Y的物质的量之和可能为2mol
【答案】C
【分析】由图知,铜与足量浓硫酸反应生成Cu S和白色物质X,无气体生成,生成Cu S时铜元素从
2 2
0价升高到+1价、硫元素从+6价降低到-2价,则按得失电子数守恒、必定存在其他产物(所含元素
化合价升高)、按元素质量守恒只能为CuSO ,则白色物质X为CuSO ,配平得到该反应方程式为:
4 4
5Cu+4H SO (浓) 3CuSO +Cu S+4HO,据此回答。
2 4 4 2 2
【详解】A.据分析,白色物质X为CuSO ,溶液为蓝色,故A错误;
4
B.Cu S和白色物质CuSO 加稀硫酸和稀硝酸时溶解,存在反应:3Cu S+16H++4NO =6Cu2+
2 4 2
+3S↓+4NO↑+8H O,Y为S单质,则NO为还原产物、Y为氧化产物,故B错误;
2
C.由5Cu+4H SO (浓) 3CuSO +Cu S+4HO可知,硫元素从+6价降低到-2价时表现氧化性,有
2 4 4 2 2
硫酸铜生成表现出酸性,故C正确;
D.由5Cu+4H SO (浓) 3CuSO +Cu S+4HO知,3molCu生成0.6molCu S,0.6molCu S发生反应
2 4 4 2 2 2 2
3Cu S+16H++4NO =6Cu2++3S↓+4NO↑+8H O得到0.8mol NO与0.6mol S,NO与S物质的量之和为
2 2
1.4mol,故D错误;故选C。
7.【2022·河北·霸州市第一中学模拟预测】化学振荡反应是指在化学反应中出现其反应物(或生成物)
的浓度均匀一致地随时间而来回振荡的现象。碘钟反应是常见的振荡反应,在烧杯中加入HO 溶液、
2 2
酸性KIO 溶液、MnSO 和丙二酸的混合溶液、少许可溶性淀粉试剂后,碘钟反应正式开启,初始颜
3 4
色为无色,溶液颜色变化如图。下列说法错误的是
A.无色变为琥珀色过程中,已知涉及反应2HIO+2Mn2++2H+=I +2Mn3++2H O,则氧化性:HIO>
2 2
Mn3+
B.反应由琥珀色变为蓝色过程中有氧化还原反应发生
C.出现蓝色,是因为此时反应生成了大量I
2
D.该碘钟反应的振荡周期与温度无关
【答案】D
【详解】A.在氧化还原反应中,物质的氧化性:氧化剂>氧化产物。在反应2HIO+2Mn2+
+2H+=I +2Mn3++2H O中,氧化剂是HIO,氧化产物是Mn3+,所以氧化性:HIO>Mn3+,A正确;
2 2
B.反应由琥珀色变为蓝色过程中会发生反应:5HO+2HIO=I +5O ↑+6H O,该反应过程中元素化合
2 2 3 2 2 2
价会发生变化,因此反应属于氧化还原反应,B正确;
C.溶液中含有淀粉溶液,由于I 遇淀粉溶液变为蓝色,故出现蓝色,是由于此时反应生成了大量
2
I,C正确;
2
D.HO 不稳定,温度升高,HO 发生分解反应,导致HO 的浓度降低,浓度降低,会使反应速率
2 2 2 2 2 2
减慢,故该碘钟反应的振荡周期与温度有关,D错误;
故合理选项是D。
8.【2020·北京】某同学进行如下实验:
实验步骤 实验现象
将NH Cl固体加入试管中,并将湿润的pH试 试纸颜色变化:黄色→蓝色
4
I 纸置于试管口,试管口略向下倾斜,对试管底 (pH≈10)→黄色→红色(pH≈2);试
部进行加热 管中部有白色固体附着
试纸颜色变化:黄色→橙黄色
II 将饱和NH Cl溶液滴在pH试纸上
4
(pH≈5)
下列说法不正确的是A.根据I中试纸变蓝,说明NH Cl发生了分解反应
4
B.根据I中试纸颜色变化,说明氨气比氯化氢气体扩散速率快C.I中试纸变成红色,是由于NH Cl水解造成的
4
D.根据试管中部有白色固体附着,说明不宜用加热NH Cl的方法制备NH
4 3
【答案】C
【分析】实验I中对NH Cl固体试管加热,湿润的pH试纸黄色→蓝色(pH≈10)→黄色→红色(pH≈2),
4
说明加热过程中生成了氨气,氨气遇水形成一水合氨,一水合氨为弱碱,使试纸变蓝,同时产生了
氯化氢气体,氯化氢极易溶于水形成盐酸,中和了一水合氨恢复到黄色,最后变为红色,该过程可
证明氯化铵受热发生分解生成氨气和氯化氢气体,试纸先变蓝后变红,说明氨气扩散的速度比氯化
氢快;试管中部有白色固体附着,说明氯化铵分解产生的氨气和氯化氢在扩散过程中由化合生成氯
化铵;
实验II中将氯化铵溶液滴在pH试纸上,试纸颜色变化:黄色→橙黄色(pH≈5),说明氯化铵溶液中铵
根离子水解使溶液显酸性,据此分析解答。
【详解】A.氯化铵是强酸弱碱盐,其水溶液显酸性,会使湿润的pH试纸变红,根据I中试纸变蓝,
说明NH Cl发生了分解反应,故A正确;
4
B.根据分析,根据I中试纸颜色变化,说明氨气比氯化氢气体扩散速率快,故B正确;
C.根据分析,I中试纸变成红色,是由于NH Cl分解产生的氯化氢造成的,故C错误;
4
D.根据分析,根据试管中部有白色固体附着,说明氯化铵分解产生的氨气和氯化氢在扩散过程中由
化合生成氯化铵,则不宜用加热NH Cl的方法制备NH ,故D正确;
4 3
答案选C。
9.【2018·北京】验证牺牲阳极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
① ② ③
在Fe表面生成蓝色沉淀 试管内无明显变化 试管内生成蓝色沉淀
下列说法不正确的是A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
【答案】D
【详解】分析:A项,对比②③,②Fe附近的溶液中加入K[Fe(CN)]无明显变化,②Fe附近的
3 6
溶液中不含Fe2+,③Fe附近的溶液中加入K[Fe(CN)]产生蓝色沉淀,③Fe附近的溶液中含
3 6
Fe2+,②中Fe被保护;B项,①加入K[Fe(CN)]在Fe表面产生蓝色沉淀,Fe表面产生了Fe2+,对
3 6比①②的异同,①可能是K[Fe(CN)]将Fe氧化成Fe2+;C项,对比①②,①也能检验出Fe2+,不
3 6
能用①的方法验证Zn保护Fe;D项,由实验可知K[Fe(CN)]可能将Fe氧化成Fe2+,将Zn换成
3 6
Cu不能用①的方法证明Fe比Cu活泼。
详解:A项,对比②③,②Fe附近的溶液中加入K[Fe(CN)]无明显变化,②Fe附近的溶液中不
3 6
含Fe2+,③Fe附近的溶液中加入K[Fe(CN)]产生蓝色沉淀,③Fe附近的溶液中含Fe2+,②中Fe
3 6
被保护,A项正确;B项,①加入K[Fe(CN)]在Fe表面产生蓝色沉淀,Fe表面产生了Fe2+,对比
3 6
①②的异同,①可能是K[Fe(CN)]将Fe氧化成Fe2+,B项正确;C项,对比①②,①加入K[Fe
3 6 3
(CN)]在Fe表面产生蓝色沉淀,①也能检验出Fe2+,不能用①的方法验证Zn保护Fe,C项正确;
6
D项,由实验可知K[Fe(CN)]可能将Fe氧化成Fe2+,将Zn换成Cu不能用①的方法证明Fe比Cu
3 6
活泼,D项错误;答案选D。
点睛:本题通过实验验证牺牲阳极的阴极保护法,考查Fe2+的检验、实验方案的对比,解决本题的关
键是用对比分析法。要注意操作条件的变化,如①中没有取溶液,②中取出溶液,考虑Fe对实验结
果的影响。要证明Fe比Cu活泼,可用②的方法。
10.【2022·河南·模拟预测】 遇 会生成 蓝色沉淀,因此
常用于 的检验。文献显示: 具有氧化性,可以氧化 ;还原性Fe
大于 。
某科研小组探究Fe与 能否直接反应的实验如下:
实验1:取加热至沸腾并快速冷却的 溶液(加热、冷却过程中溶液颜色无
变化)于试管中,并加入1mL的苯,再加入铁粉,长时间无蓝色沉淀出现。
实验2:在“实验1”中,若使用砂纸打磨过的铁粉,一会儿就出现蓝色沉淀。
实验3:在“实验1”中,若加少量NaCl,立即出现蓝色沉淀;若换成加入 或 ;则不出
现蓝色沉淀。
实验4:在“实验1”中,若将铁粉换成在稀硫酸中反应一段时间的铁片,立即出现蓝色沉淀。
下列说法错误的是
A.实验1中长时间无蓝色沉淀出现,可能是因为铁粉表面有氧化膜
B. 可能起破坏铁粉表面氧化膜的作用
C.Fe与 可以直接反应
D.在Fe、C、NaCl溶液组成的原电池中,通过直接滴加 溶液至电解质溶液中的方法,
可以检验是否发生原电池反应
【答案】D
【分析】实验2、3、4说明铁与铁氰化钾溶液能直接反应,实验1说明铁粉表面氧化膜阻碍了铁与铁
氰化钾溶液的反应,实验3说明氯离子能破坏铁粉表面的氧化膜,有利于铁与铁氰化钾溶液的反应。【详解】A.由分析可知,实验1中长时间无蓝色沉淀出现能是因为铁粉表面的氧化膜阻碍了铁与铁
氰化钾溶液的反应,故A正确;
B.由分析可知,氯离子能破坏铁粉表面的氧化膜,有利于铁与铁氰化钾溶液的反应,故B正确;
C.由分析可知,实验2、3、4说明铁与铁氰化钾溶液能直接反应,故C正确;
D.铁、碳、氯化钠溶液组成的原电池中,氯化钠溶液电离出的氯离子会破坏铁表面的氧化膜,若直
接向原电池中滴加铁氰化钾溶液,铁与铁氰化钾溶液能直接反应,无法检验溶液中是否存在亚铁离
子,不能检验是否发生原电池反应,故D错误;
故选D。
热点集 点击 核心
热点 猜想
11.【2022·江苏·南京市第十三中学模拟预测】侯德榜是我国近代化学工业的奠基人之一,他将氨碱
法和合成氨工艺联合起来,发明了“联合制碱法”。氨碱法中涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
下列制取少量 相关的实验原理和装置能达到实验目的的是
A.制取 B.除去 中HCl C.制取并收集氨气 D.制取
A.A B.B C.C D.D
【答案】B
【详解】A.装置中试剂是稀盐酸和大理石反应生成二氧化碳气体,但装置中长颈漏斗未插入溶液,
生成的二氧化碳气体会从长颈漏斗处逸出,不能制得二氧化碳气体,故A错误;
B.除去CO 中HCl,可以把混合气体通入饱和碳酸氢钠溶液,导气管应长进短出,装置图正确,可
2
以达到除杂目的,故B正确;
C.氯化铵受热分解,但在试管口又化合生成氯化铵,不能利用氯化铵分解制取氨气,则不能完成实
验,应利用氯化铵和碱共热制备氨气,故C错误;
D.碳酸氢钠固体受热分解过程中生成碳酸钠、二氧化碳和水,装置中生成的水会倒流炸裂试管,应
试管口略向下倾斜,故D错误;故选:B。
12.【2022·青海·海东市第一中学一模】1971年,John.J.Bishop等通过3Mg2++4ClO-+2Cl-
+2H O=Mg(ClO) ·2Mg(OH) +2Cl↑反应制得Mg(ClO) ·2Mg(OH) (BMHs,微溶于水),而1921年,
2 2 2 2 2 2
Georg.Kereszty等将Cl 通入Mg(OH) 悬浊液进行制备BMHs却宣告失败。用下列装置制取BMHs,
2 2
相关叙述错误的是
A.向装置a烧瓶中滴入浓盐酸之前,应打开K
B.装置b的广口瓶盛放的是饱和食盐水
C.开始时,不断搅拌下先向三口烧瓶中加入MgCl 溶液,然后通入Cl
2 2
D.从反应完成后的三口烧瓶中分离得到BMHs,需经过过滤、洗涤及干燥等操作
【答案】C
【详解】A.打开K可使浓盐酸顺利滴入烧瓶并使气体进入后续装置,A正确;
B.浓盐酸具有挥发性,得到氯气中含有氯化氢杂质,用饱和食盐水除去氯气中的氯化氢,B正确;
C.先加入 会生成 悬浊液,由题给信息, 难以与 反应,几乎得不到
,C错误;
D.由于 微溶于水,先过滤,再经洗涤和干燥得到产品,D正确;
故选C。
13.【2022·广东广州·模拟预测】实验室从废定影液[含 和 等]中回收 和 的主要步
骤为:向废定影液中加入 溶液沉银,过滤、洗涤及干燥,灼烧 制 ,制取 并通入滤
液氧化 ,用苯萃取分液。其中部分操作的装置如图,下列叙述正确的是
A.用装置甲分离 时,用玻璃棒不断搅拌
B.用装置乙在空气中高温灼烧 制取C.用装置丙制备用于氧化滤液中 的
D.用装置丁分液时,从下口放出有机相
【答案】C
【详解】A.用装置甲过滤分离硫化银时,若用玻璃棒不断搅拌会容易损坏滤纸,故A错误;
B.蒸发皿不能用于高温灼烧固体,否则会受热不均而炸裂,应选用坩埚灼烧,故B错误;
C.高锰酸钾与浓盐酸不需加热就能反应生成氯气,则用装置丙制备用于氧化滤液中溴离子的氯气,
故C正确;
D.苯的密度比水小,溴的苯溶液在上层,则用装置丁分液时,先放出水相,再从分液漏斗上口倒出
有机相,故D错误;
故选C。
14.【2022·江西江西·模拟预测】氨基甲酸铵( )可用于生产医药试剂、发酵促进剂、电子
元件等,是一种可贵的氨化剂,某化学小组用下列实验装置模拟工业制备少量氨基甲酸铵。下列说
法错误的是
查阅资料:氨基甲酸铵的性质及工业制法如表所示。
物理性质 白色粉末,易溶于水,难溶于四氯化碳
化学性质 水解生成碳酸氢铵,受热分解生成尿素
工业制法
A.装置Ⅰ中胶皮管a的作用为平衡压强,使液体顺利滴下
B.装置Ⅱ、Ⅲ、Ⅴ中盛放的试剂依次为饱和 溶液、浓硫酸、碱石灰
C.装置Ⅳ的反应温度过高,会导致氨基甲酸铵的产量降低
D.装置Ⅵ中发生反应的化学方程式为
【答案】B
【详解】A.装置Ⅰ中胶皮管a的作用为平衡压强,使液体顺利滴下,选项A正确;
B.装置Ⅱ的作用为吸收 中的HCl,应盛放饱和 溶液,因为二氧化碳也能与碳酸钠溶液
反应,装置Ⅲ的作用为吸收 中的水蒸气,应盛放浓硫酸,装置Ⅴ的作用为吸收 中的水蒸气,应盛放碱石灰,选项B错误;
C.制备氨基甲酸铵的反应为放热反应,为提高其产量,应降低温度,使平衡正向移动,同时也可防
止其受热分解生成尿素,选项C正确;
D.装置Ⅵ中发生反应的化学方程式为 ,选项D正确;
答案选B。
15.【2022·青海·模拟预测】实验室可用 KNO 固体与酸反应制取硝酸,其实验装置如下图所示(加热
3
装置已省略)。
下列说法错误的是
A.该装置不用橡皮塞和橡皮管,可避免被酸腐蚀
B.制取硝酸时曲颈甑中盛放的是硝酸钾和稀硫酸
C.用流水冷却,可促进硝酸蒸汽冷凝,避免酸雾
D.该装置用于制取液溴时,可在曲颈甑中加入 NaBr、MnO 及浓硫酸
2
【答案】B
【详解】A.硝酸具有强氧化性,会腐蚀橡皮塞和橡皮管,A项正确;
B.该反应的原理是利用高沸点浓硫酸制备低沸点的硝酸,则曲颈甑中盛放的是硝酸钾和浓硫酸,B
项错误;
C.硝酸沸点低,用流水冷却,可促进硝酸蒸汽冷凝,避免酸雾,C项正确;
D.NaBr、MnO 及浓硫酸发生氧化还原反应生成硫酸钠、溴单质、硫酸锰和水,溴单质易挥发,则
2
可用该装置制取液溴,D项正确;
答案选B。
16.【2022·广东广州·模拟预测】室温下,某同学用下图中装置在通风棚中进行如下实验:
实验 现象
试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应越来越剧烈,试
管口上方出现红棕色气体,溶液呈蓝色。
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色:之后向溶液中持续通入 ,溶液又变为蓝色。
下列说法不正确的是A.试管Ⅰ中浅红棕色气体为 ,由铜还原硝酸生成
B.等质量的Cu完全溶解时,Ⅰ中消耗的 更少
C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有
D.蓝色的 呈平面四边形结构,中心离子不可能为 杂化
【答案】A
【详解】A.试管 Ⅰ 中Cu与稀硝酸反应生成NO,然后NO与氧气反应生成浅红棕色气体NO A
2,
错误;
B.3mol Cu消耗8mol稀硝酸,1molCu消耗4mol浓硝酸,则等质量的Cu完全溶解时,I中消耗的
HNO 更少,B正确;
3
C.二氧化氮为红棕色气体,则II中反应后溶液颜色与试管I中的不同,是由于溶有NO ,C正确;
2
D.蓝色的 呈平面四边形结构,中心离子应是sp2杂化,D正确;
故选A。
17.【2022·四川攀枝花·模拟预测】由含硒废料(主要 含S、Se 、Fe O、CuO 、ZnO 、SiO 等)制取
2 3 2
硒的流程如图:
下列有关说法正确的是
A.“分离”时得到含硫煤油的方法是蒸馏
B.“酸溶”时能除去废料中的全部氧化物杂质
C.“酸化”的离子反应为: +2H+=Se↓+SO ↑+H O
2 2
D.若向“酸溶”所得的滤液中加入少量铜,铜不会溶解
【答案】C
【分析】由流程可知,煤油溶解S后,过滤分离出含硫的煤油,分离出Se、Fe O、CuO、ZnO、
2 3
SiO 后,加硫酸溶解、过滤,滤液含硫酸铜、硫酸锌、硫酸铁,滤渣含Se、SiO,再加亚硫酸钠浸
2 2
取Se生成NaSeSO ,最后酸化生成粗硒。
2 3
【详解】A. 煤油溶解S后,过滤分离出含硫的煤油,滤渣为Se、Fe O、CuO、ZnO、SiO,“分
2 3 2
离”时得到含硫煤油的方法是过滤,故A错误;
B.加硫酸溶解、过滤,滤液含硫酸铜、硫酸锌、硫酸铁,滤渣含Se、SiO,“酸溶”时能除去废料
2中的部分氧化物杂质,二氧化硅不溶于硫酸,故B错误;
C. NaSeSO 酸化生成粗硒,“酸化”的离子反应为: +2H+=Se↓+SO ↑+H O,故C正确;
2 3 2 2
D. 若向“酸溶”所得的滤液中加入少量铜,滤液含硫酸铁,铜会溶解,2Fe3++Cu=Cu2++2Fe2+,故
D错误;
故选C。
18.【2022·吉林·抚松县第一中学模拟预测】向碘水、淀粉的混合液中加入AgNO 溶液,蓝色褪去。
3
为探究褪色原因,实验如图:
下列分析不正确的是
A.过程①后溶液pH明显变小
B.过程③中加入NaCl溶液的目的是除去Ag+
C.综合上述实验,过程①中蓝色褪去的原因是Ag+氧化了I
2
D.不能判断4H++4I-+O =2H O+2I 是过程④中溶液变蓝的原因
2 2 2
【答案】C
【分析】在碘水中存在如下平衡:I+H O HI+HIO,I-与Ag+反应生成AgI沉淀,促进I 与水的反
2 2 2
应不断正向进行;过滤,所得滤液1中含有HIO和HNO,还有未反应完的AgNO,加入NaCl溶液,
3 3
Ag+与Cl-生成AgCl沉淀,往滤液2中加入KI溶液,发生I-、HIO、H+的氧化还原反应,同时发生反
应4H++4I-+O =2H O+2I ,生成I,使溶液再次变蓝色。
2 2 2 2
【详解】A.由分析可知,过程①后,溶液的主要成分为HIO、HNO 及未反应的AgNO,所以pH
3 3
明显变小,故A正确;
B.过程③中加入NaCl溶液,可与Ag+反应生成AgCl沉淀,排除Ag+可能对后续实验产生的干扰,
所以目的是除去Ag+,故B正确;
C.过程①中蓝色褪去的原因可能是Ag+氧化了I,也可能是Ag+促进了I 与HO的反应,故C错误;
2 2 2
D.过程④中,加入KI,发生HIO、H+、I-的氧化还原反应,同时发生反应4H++4I-+O =2H O+2I ,
2 2 2
因此氧化I-的物质不只有O,故D正确;
2
答案选C。
19.【2022·湖南·石门县第一中学二模】燃煤烟气中含有SO 和SO 等物质,用如图装置测定SO 含量。
2 3 3
已知异丙醇溶液可选择性吸收SO 并转化为SO ,也可溶解少量SO 实验中应尽快除去SO 。
3 2. 2下列说法错误的是
A.用空气吹出异丙醇溶液中溶解的SO B.通过测定BaSO 的质量检测SO 含量
2 4 3
C.该过程中涉及到反应:HO+SO=H SO D.0℃冰浴不可以减少异丙醇的挥发
2 2 2 2 4
【答案】AD
【分析】0℃的冰浴可减少异丙醇的挥发,烟气通过80%异丙醇后SO 被吸收,烟气再通过双氧水后
3
SO 被吸收。
2
【详解】A.空气中的氧气能将溶解的SO 氧化为SO ,不能用空气吹出异丙醇溶液中溶解的SO ,
2 2
A错误;
B.根据S原子守恒可通过测定BaSO 的质量计算SO 的质量,从而检测SO 含量,B正确;
4 3 3
C.未被异丙醇溶液吸收的SO 和过氧化氢发生氧化还原反应,反应的化学方程式为
2
HO+SO=H SO ,因此过程中涉及到HO+SO=H SO ,C正确;
2 2 2 2 4 2 2 2 2 4
D.异丙醇易挥发,0∘C冰浴温度较低,可减少异丙醇的挥发,D错误;
答案选AD。
20.【2022·河北·霸州市第一中学模拟预测】铼(Re)是一种极其稀少的贵金属。一种以辉钼矿(主要含
有MoS 以及少量ReS 、CuReS 、FeS、SiO 等)为原料制备铼的工艺流程如下:
2 2 4 2
已知“氧化焙烧”后成分有:SiO、Re O、MoO 、CuO、Fe O,其中Re O、MoO 与氨水反应分
2 2 7 3 3 4 2 7 3
别生成NH ReO、(NH )MoO 。
4 4 4 2 4
下列说法错误的是
A.“氧化焙烧”时,ReS 反应后的氧化产物为Re O 和SO
2 2 7 2
B.若改用NaOH溶液代替氨水“浸出”,滤渣成分不变
C.由MoS 生成1mol MoO ,转移14mol电子
2 3
D.“电沉积”后,金属铼在阴极生成
【答案】B
【分析】辉钼矿(主要含有MoS 以及少量ReS 、CuReS 、FeS、SiO 等)在空气中氧化焙烧,生成SO
2 2 4 2 2
和SiO、Re O、MoO 、CuO、Fe O 等;用氨水浸出,Re O、MoO 转化为NH ReO、
2 2 7 3 3 4 2 7 3 4 4
(NH )MoO ,SiO、CuO、Fe O 成为滤渣;浸出液采用离子交换、解吸,可得到NH ReO,重结晶
4 2 4 2 3 4 4 4
去除杂质,进行电沉积,在阴极得到铼。【详解】A.ReS 中Re显+2价、S显-1价,“氧化焙烧”时,Re O 中Re显+7价,SO 中S显+4价,
2 2 7 2
则ReS 反应后的氧化产物为Re O 和SO ,A正确;
2 2 7 2
B.若改用NaOH溶液代替氨水“浸出”,则SiO 也会溶解在NaOH溶液中,滤渣成分将发生改变,
2
B错误;
C.由MoS 生成MoO ,Mo由+2价升高到+6价,S由-1价升高到+4价,则生成1mol MoO ,转移
2 3 3
14mol电子,C正确;
D.“电沉积”后,NH ReO 中+7价铼将获得电子,所以在阴极生成金属铼,D正确;
4 4
故选B。