文档内容
重难录 点击 蓄势
重难 而发
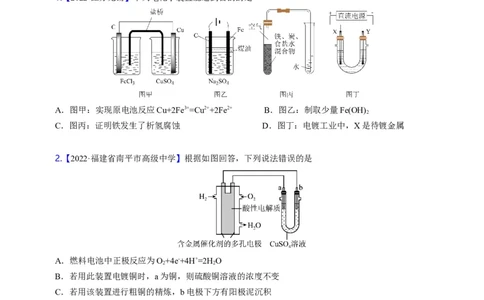
1.【2022·江苏无锡】下列电化学装置能达到目的的是
A.图甲:实现原电池反应Cu+2Fe3+=Cu2++2Fe2+ B.图乙:制取少量Fe(OH)
2
C.图丙:证明铁发生了析氢腐蚀 D.图丁:电镀工业中,X是待镀金属
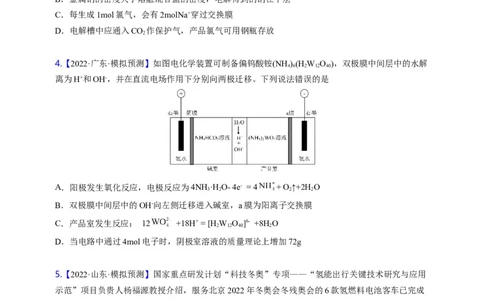
2.【2022·福建省南平市高级中学】根据如图回答,下列说法错误的是
A.燃料电池中正极反应为O+4e-+4H+=2H O
2 2
B.若用此装置电镀铜时,a为铜,则硫酸铜溶液的浓度不变
C.若用该装置进行粗铜的精炼,b电极下方有阳极泥沉积
D.若用该装置进行粗铜的精炼,当有1mol水生成时,可得到64g精铜
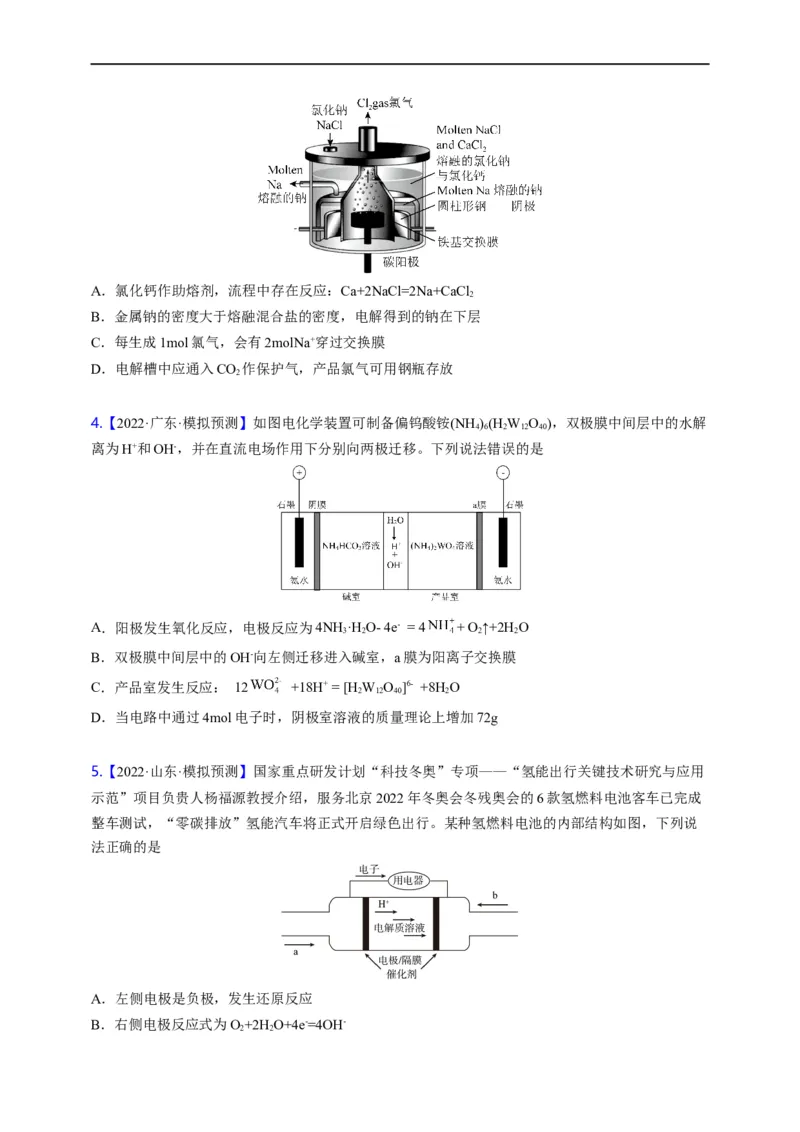
3.【2022·广东茂名·模拟预测】当斯法是经典的制钠方法,电解熔盐(氯化钠和氯化钙)装置如图所示。
阳极为碳棒,阴极为圆柱形钢,两极间有交换膜隔开。下列叙述正确的是A.氯化钙作助熔剂,流程中存在反应:Ca+2NaCl=2Na+CaCl
2
B.金属钠的密度大于熔融混合盐的密度,电解得到的钠在下层
C.每生成1mol氯气,会有2molNa+穿过交换膜
D.电解槽中应通入CO 作保护气,产品氯气可用钢瓶存放
2
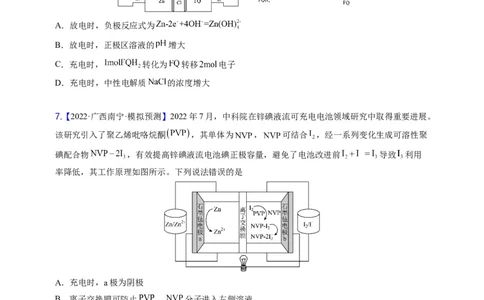
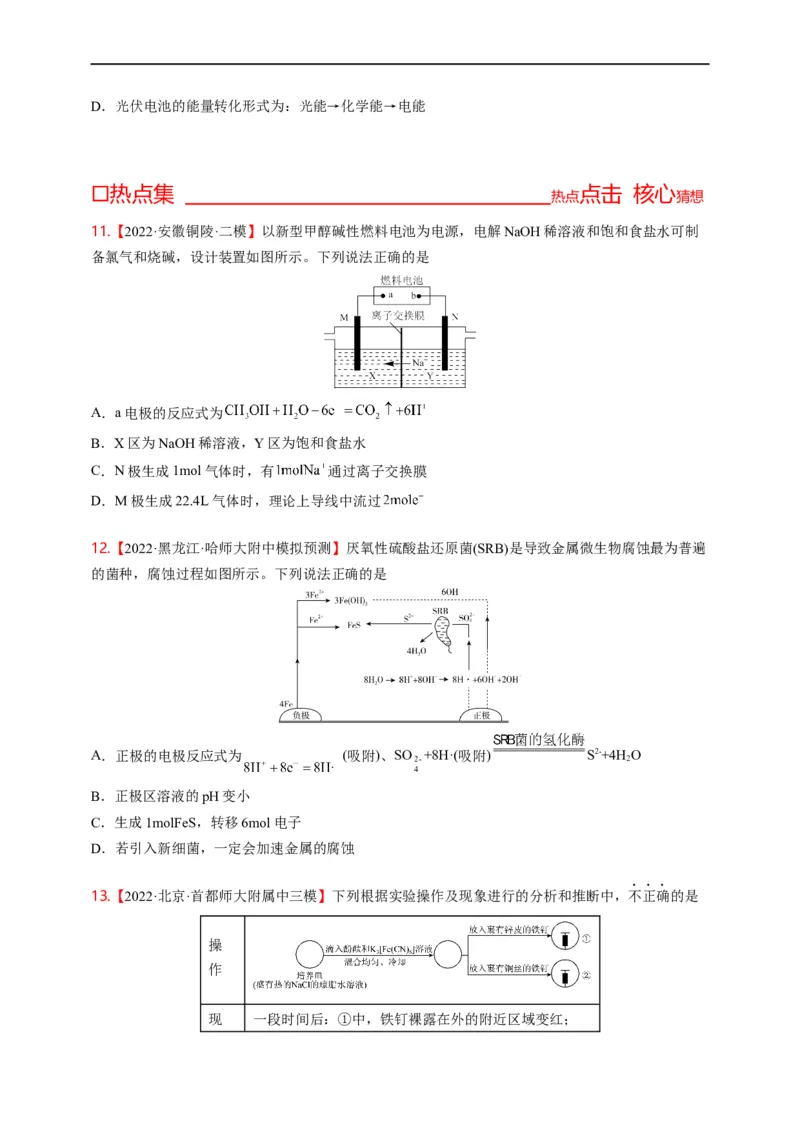
4.【2022·广东·模拟预测】如图电化学装置可制备偏钨酸铵(NH )(H W O ),双极膜中间层中的水解
4 6 2 12 40
离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法错误的是
A.阳极发生氧化反应,电极反应为4NH ·H O- 4e- = 4 + O ↑+2H O
3 2 2 2
B.双极膜中间层中的OH-向左侧迁移进入碱室,a膜为阳离子交换膜
C.产品室发生反应: 12 +18H+ = [H W O ]6- +8H O
2 12 40 2
D.当电路中通过4mol电子时,阴极室溶液的质量理论上增加72g
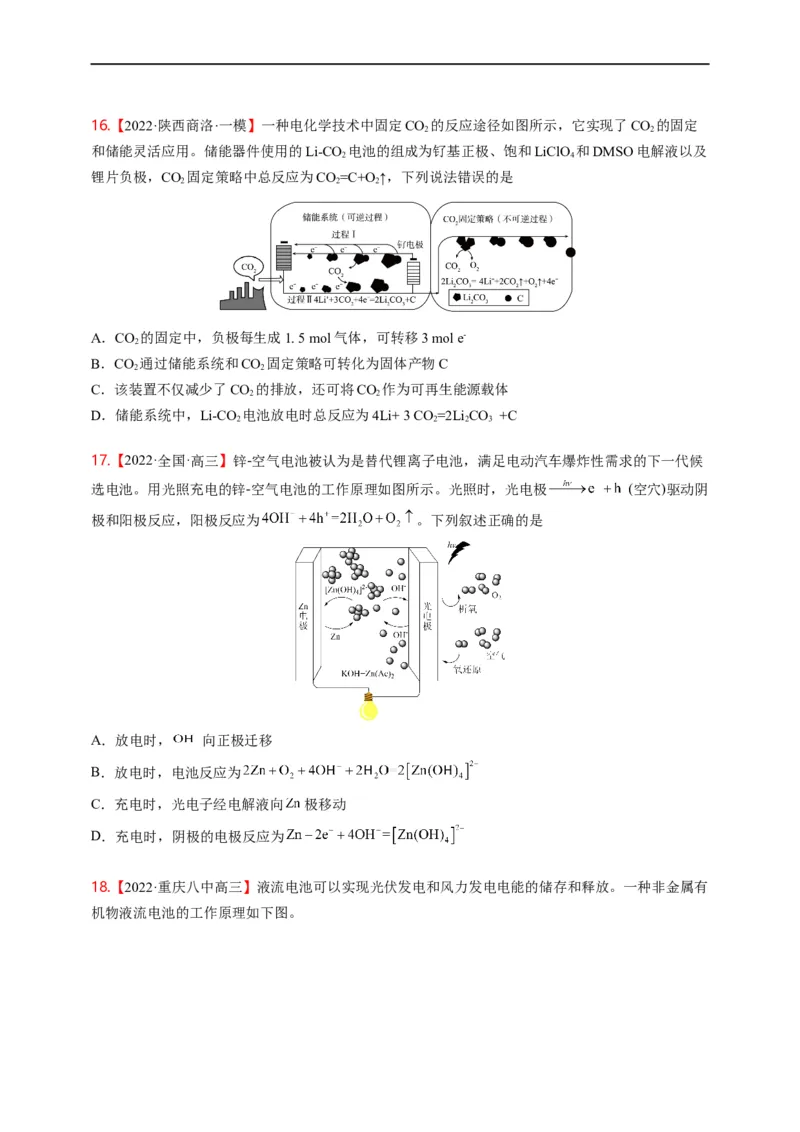
5.【2022·山东·模拟预测】国家重点研发计划“科技冬奥”专项——“氢能出行关键技术研究与应用
示范”项目负贵人杨福源教授介绍,服务北京2022年冬奥会冬残奥会的6款氢燃料电池客车已完成
整车测试,“零碳排放”氢能汽车将正式开启绿色出行。某种氢燃料电池的内部结构如图,下列说
法正确的是
A.左侧电极是负极,发生还原反应
B.右侧电极反应式为O+2H O+4e-=4OH-
2 2C.当有0.1mol电子通过导线时,左侧消耗标准状况下1.12L气体
D.电子由a极流出经用电器达到b极,再由b极经电解质溶液流回a极形成闭合回路
6.【2022·江苏·启东中学模拟预测】高电压水系锌—有机混合液流电池的装置如图所示。下列说法错
误的是
A.放电时,负极反应式为
B.放电时,正极区溶液的 增大
C.充电时, 转化为 转移 电子
D.充电时,中性电解质 的浓度增大
7.【2022·广西南宁·模拟预测】2022年7月,中科院在锌碘液流可充电电池领域研究中取得重要进展。
该研究引入了聚乙烯吡咯烷酮 ,其单体为 , 可结合 ,经一系列变化生成可溶性聚
碘配合物 ,有效提高锌碘液流电池碘正极容量,避免了电池改进前 导致 利用
率降低,其工作原理如图所示。下列说法错误的是
A.充电时,a极为阴极
B.离子交换膜可防止 、 分子进入左侧溶液
C.放电时,b极反应:
D.电池改进前,放电时 转化为 ,转移 电子
8.【2022·贵州·模拟预测】利用浓差电池电解NaSO 溶液(a、b电极均为石墨电极),可制得O、H、
2 4 2 2
HSO 和NaOH,反应原理如图所示。下列说法正确的是
2 4A.b电极的电极反应为2HO+2e- =H ↑+2OH-
2 2
B.c、d分别为阳离子交换膜和阴离子交换膜
C.浓差电池放电过程中,Cu(1)电极上的电极反应为Cu-2e- =Cu2+
D.当阴极产生2.24L气体时,电路中转移0.2mol电子
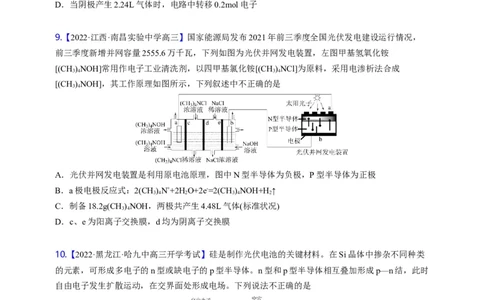
9.【2022·江西·南昌实验中学高三】国家能源局发布2021年前三季度全国光伏发电建设运行情况,
前三季度新增并网容量2555.6万千瓦,下列如图为光伏并网发电装置,左图甲基氢氧化铵
[(CH )NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成
3 4 3 4
[(CH )NOH],其工作原理如图所示,下列叙述中不正确的是
3 4
A.光伏并网发电装置是利用原电池原理,图中N型半导体为负极,P型半导体为正极
B.a极电极反应式:2(CH)N++2H O+2e-=2(CH )NOH+H ↑
3 4 2 3 4 2
C.制备18.2g(CH )NOH,两极共产生4.48L气体(标准状况)
3 4
D.c、e为阳离子交换膜,d均为阴离子交换膜
10.【2022·黑龙江·哈九中高三开学考试】硅是制作光伏电池的关键材料。在Si晶体中掺杂不同种类
的元素,可形成多电子的n型或缺电子的p型半导体。n型和p型半导体相互叠加形成p—n结,此时
自由电子发生扩散运动,在交界面处形成电场。下列说法不正确的是
A.1molSi晶体中含有的Si—Si键数目为2NA
B.若在Si晶体中掺入某些金属元素,可得p型半导体
C.p-n结在导电过程中,n型一侧带正电,p型一侧带负电D.光伏电池的能量转化形式为:光能→化学能→电能
热点集 点击 核心
热点 猜想
11.【2022·安徽铜陵·二模】以新型甲醇碱性燃料电池为电源,电解NaOH稀溶液和饱和食盐水可制
备氯气和烧碱,设计装置如图所示。下列说法正确的是
A.a电极的反应式为
B.X区为NaOH稀溶液,Y区为饱和食盐水
C.N极生成1mol气体时,有 通过离子交换膜
D.M极生成22.4L气体时,理论上导线中流过
12.【2022·黑龙江·哈师大附中模拟预测】厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为普遍
的菌种,腐蚀过程如图所示。下列说法正确的是
A.正极的电极反应式为 (吸附)、SO +8H·(吸附) S2-+4H O
2
B.正极区溶液的pH变小
C.生成1molFeS,转移6mol电子
D.若引入新细菌,一定会加速金属的腐蚀
13.【2022·北京·首都师大附属中三模】下列根据实验操作及现象进行的分析和推断中,不正确的是
操
作
现 一段时间后:①中,铁钉裸露在外的附近区域变红;象
②中……
A.NaCl的琼脂水溶液为离子迁移的通路
B.①中变红是因为发生反应 ,促进了水的电离
C.②中可观察到铁钉裸露在外的附近区域产生蓝色沉淀,铜丝附近区域变红
D.①和②中发生的氧化反应均可表示为 (M代表锌或铁)
14.【2022·福建·高三阶段练习】如图,科学家基于 易溶于 的性质,发展了一种无需离子交
换膜的新型氯流电池,可作储能设备,总方程式为: 。
下列说法正确的是
A.放电时 溶液的 减小
B.放电时 透过多孔活性炭电极向 中迁移
C.充电时的阴极反应为
D.充电时,电路中每转移 ,理论上从 中释放
15.【2022·云南·昆明市第三中学高三阶段练习】钒氧化还原流电池,是一种活性物质呈循环流动液
态的二次电池,可用于固定储能设备。放电时工作原理如图所示。下列有关叙述错误的是
A.放电时,H+通过质子交换膜向a极迁移
B.放电时,a电极反应方程式为VO +e-+2H+=VO2++H O
2
C.充电时,电极b与外接电源的负极相连
D.电池的总反应可以表示为:VO +V2++2H+ VO2++V3++H O
216.【2022·陕西商洛·一模】一种电化学技术中固定CO 的反应途径如图所示,它实现了CO 的固定
2 2
和储能灵活应用。储能器件使用的Li-CO 电池的组成为钌基正极、饱和LiClO 和DMSO电解液以及
2 4
锂片负极,CO 固定策略中总反应为CO=C+O ↑,下列说法错误的是
2 2 2
A.CO 的固定中,负极每生成1. 5 mol气体,可转移3 mol e-
2
B.CO 通过储能系统和CO 固定策略可转化为固体产物C
2 2
C.该装置不仅减少了CO 的排放,还可将CO 作为可再生能源载体
2 2
D.储能系统中,Li-CO 电池放电时总反应为4Li+ 3 CO=2Li CO +C
2 2 2 3
17.【2022·全国·高三】锌-空气电池被认为是替代锂离子电池,满足电动汽车爆炸性需求的下一代候
选电池。用光照充电的锌-空气电池的工作原理如图所示。光照时,光电极 (空穴)驱动阴
极和阳极反应,阳极反应为 。下列叙述正确的是
A.放电时, 向正极迁移
B.放电时,电池反应为
C.充电时,光电子经电解液向 极移动
D.充电时,阴极的电极反应为
18.【2022·重庆八中高三】液流电池可以实现光伏发电和风力发电电能的储存和释放。一种非金属有
机物液流电池的工作原理如下图。下列说法不正确的是
A.放电时,正极反应式为Br +2e-=2Br-
2
B.充电时,物质a为AQDSH
2
C.放电时,AQDS/AQDSH 储液罐中的pH减小,H+通过质子交换膜到达溴极室
2
D.增大储液罐体积,可提高液流电池的储能容量
19.【2022·黑龙江·鹤岗一中高三阶段练习】电镀行业产生的酸性废水含有毒性较强的Cr(Ⅵ),图所
示为电解处理酸性含铬废水的装置,应用该装置使Cr(Ⅵ)转化为 沉淀除去。图为不同pH的
溶液中铬元素去除率与通电时间(t)的关系。下列说法错误的是
A.铁板为阳极,电极反应为
B.电解法去除Cr(Ⅵ)的最佳pH范围为4~6
C.曲线Ⅳ铬元素去除率低的原因可能是 氧化性较弱
D.除去Cr(Ⅵ)的主要反应为
20.【2022·青海·海东市一中一模】一种以Fe O 为催化剂的简单高效电合成NH 工艺如图所示(已知
2 3 3
Fe O/石墨电极上发生的化学反应为2Fe+N +3H O=Fe O+2NH),装置工作时,下列说法错误的是
2 3 2 2 2 3 3A.OH-向Pt电极迁移
B.Fe O/石墨电极上的电极反应为Fe O+6e-+3H O=2Fe+6OH-
2 3 2 3 2
C.2.24 L N 与Fe反应生成NH ,转移了0.6 mol电子
2 3
D.总反应为2N+6H O 4NH +3O
2 2 3 2