文档内容
命题猜想
本题属于高考热门题型,考查化学实验基础,涉及实验操作、主干元素化合物的性质、
有机基础、化学反应原理等必备学识。落实科学探究与创新意识、宏观辨识与微观探析、
证据获取等化学核心素养的测量。
难点重点热点
重视基础知识、避免脱离教材,掌握重要离子、单质、化合物的性质及验证方法,留意
一些物质的特性,掌握评价类实验解决路径。
重难录 点击 蓄势
重难 而发
1.【2022·山东·模拟预测】某固体混合物可能由 、 、 、 、 、 中的
若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的
是
A.气体A中一定含有
B.固体 中可能含有
C.该固体混合物中 和 至少有其中一种
D.该固体混合物一定含有 、 、
【答案】C
【分析】由气体A通过酸性高锰酸钾溶液气体体积缩小可知,气体A中一定含有二氧化硫,气体B
可能为氢气和二氧化碳中的一种或两种,则固体混合物中一定含有亚硫酸钠和铁、碳酸钠中的一种或两种;由溶液A中加入氢氧化钠溶液生成一段时间后颜色加深的白色沉淀B可知,白色沉淀B为
氢氧化亚铁,溶液A中一定含有亚铁离子,则固体混合物中氧化铁和铁至少有其中一种;由溶液B
中加入硝酸钡溶液得到沉淀C和溶液C,溶液C与酸化的硝酸银溶液生成沉淀D可知,沉淀C为硫
酸钡沉淀、沉淀D为氯化银沉淀,溶液B和溶液C中含有氯离子,则固体混合物中一定含有氯化钡,
固体A中一定含有硫酸钡,可能含有二氧化硅。
【详解】A.由分析可知,气体A中一定含有二氧化硫,气体B可能为氢气和二氧化碳中的一种或
两种,故A错误;
B.由分析可知,固体A中一定含有硫酸钡,可能含有二氧化硅,故B错误;
C.由分析可知,溶液A中一定含有亚铁离子,固体混合物中氧化铁和铁至少有其中一种,故C正
确;
D.由分析可知,固体混合物中一定含有亚硫酸钠、氯化钡,可能含有碳酸钠,故D错误;
故选C。
2.【2022·北京高三模拟】某无色强碱性溶液中仅含有 、Na+、Mg2+、Cu2+、Cl-、OH-、 、
中的若干种,为了确定该溶液的组成,某同学进行如下实验:
①取少量溶液,加入过量BaCl 溶液,有白色沉淀产生;
2
②向①所得白色沉淀中加入足量盐酸,沉淀部分溶解,并有无色气体生成;
③将②所得混合物过滤,向滤液中加入AgNO 溶液,有白色沉淀生成。
3
分析上述实验,下列说法正确的是
A.一定含有OH-、 、Cl- B.无法确定是否含有Cl-、
C.可能含有Mg2+、Cu2+ D.一定含有Na+、OH-、 、
【答案】D
【分析】Cu2+水溶液显蓝色,在无色溶液中不能大量存在;强碱性溶液中含有大量OH-,与OH-反应
的 不能大量存在。①取少量溶液,加入过量BaCl 溶液,有白色沉淀产生,说明溶液中可能含有
2
、 中至少一种离子;②向①所得白色沉淀中加入足量盐酸,沉淀部分溶解,并有无色气体
生成,说明沉淀为BaCO 、BaSO 的混合物,则原溶液中含有 、 ;由于Mg2+与 会反应
3 4
产生MgCO 沉淀,则该溶液中一定不存在Mg2+;③将②所得混合物过滤,向滤液中加入AgNO 溶液,
3 3
有白色沉淀生成,该白色沉淀是AgCl,则说明滤液中含有Cl-,由于在反应过程中加入了盐酸、过量
BaCl 溶液,因此不能确定原溶液中是否含有Cl-。根据溶液呈电中性,已经确定含有的离子OH-、
2
、 都是阴离子,则一定存在阳离子Na+,然后对选项逐一分析解答。
【详解】根据上述分析可知:该溶液中一定含有Na+、OH-、 、 ,一定不含Cu2+、Mg2+、
,可能含有的离子是Cl-。
A.根据上述分析可知原溶液中一定含有OH-、 ,但不能确定是否含有Cl-,A错误;B.根据上述分析可知溶液中一定不含有 ,可能含有Cl-,B错误;
C.根据上述分析可知溶液中一定不含有Cu2+、Mg2+,C错误;
D.根据上述分析可知:该溶液中一定含有的离子是Na+、OH-、 、 ,D正确;
故合理选项是D。
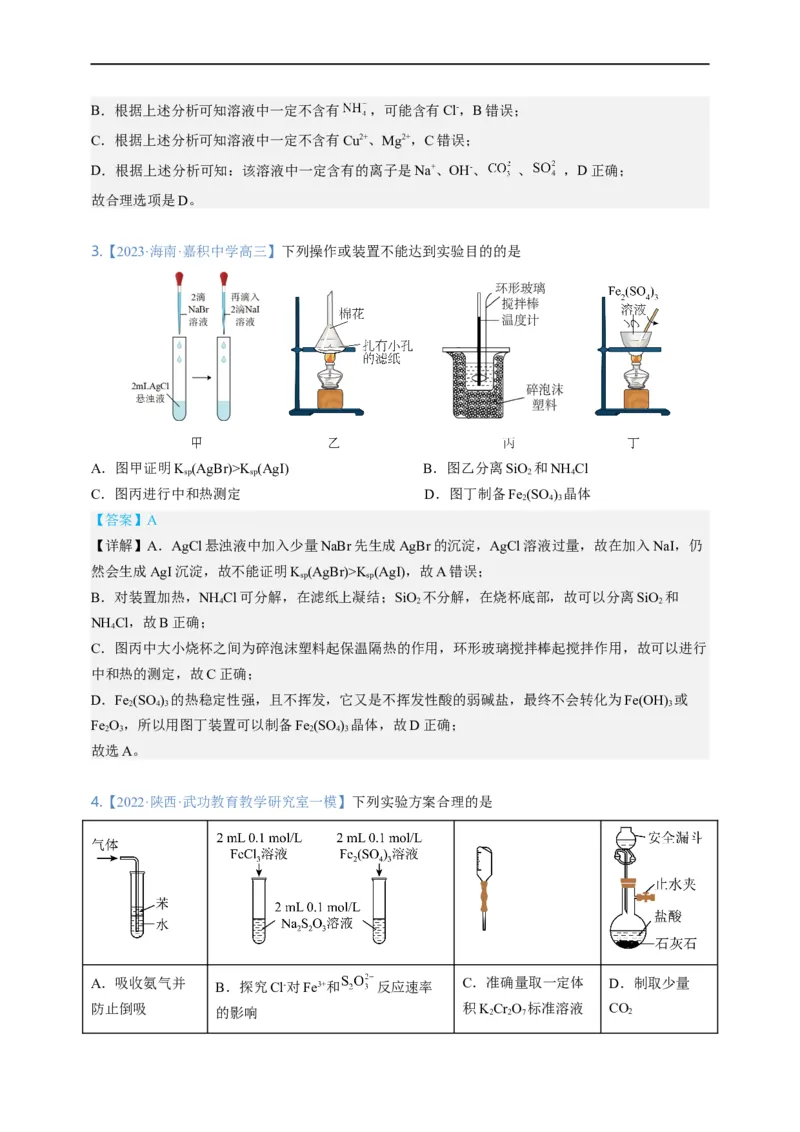
3.【2023·海南·嘉积中学高三】下列操作或装置不能达到实验目的的是
A.图甲证明K (AgBr)>K (AgI) B.图乙分离SiO 和NH Cl
sp sp 2 4
C.图丙进行中和热测定 D.图丁制备Fe (SO ) 晶体
2 4 3
【答案】A
【详解】A.AgCl悬浊液中加入少量NaBr先生成AgBr的沉淀,AgCl溶液过量,故在加入NaI,仍
然会生成AgI沉淀,故不能证明K (AgBr)>K (AgI),故A错误;
sp sp
B.对装置加热,NH Cl可分解,在滤纸上凝结;SiO 不分解,在烧杯底部,故可以分离SiO 和
4 2 2
NH Cl,故B正确;
4
C.图丙中大小烧杯之间为碎泡沫塑料起保温隔热的作用,环形玻璃搅拌棒起搅拌作用,故可以进行
中和热的测定,故C正确;
D.Fe (SO ) 的热稳定性强,且不挥发,它又是不挥发性酸的弱碱盐,最终不会转化为Fe(OH) 或
2 4 3 3
Fe O,所以用图丁装置可以制备Fe (SO ) 晶体,故D正确;
2 3 2 4 3
故选A。
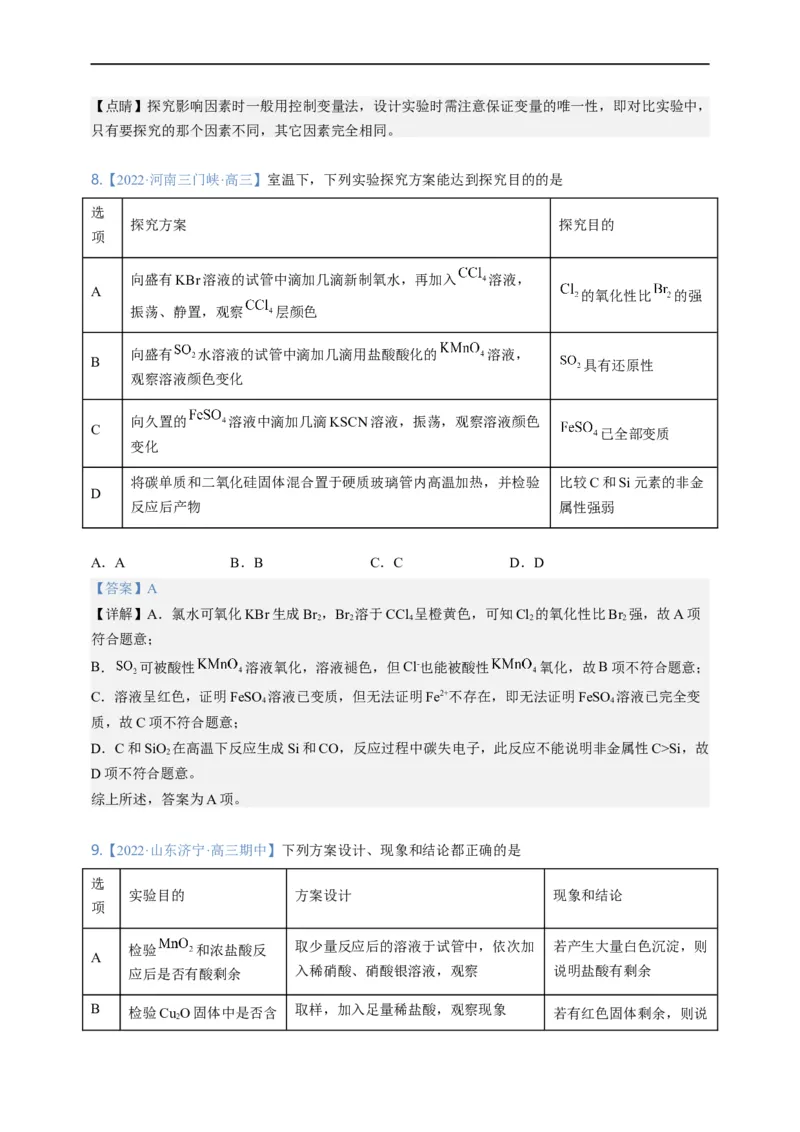
4.【2022·陕西·武功教育教学研究室一模】下列实验方案合理的是
A.吸收氨气并 B.探究Cl-对Fe3+和 反应速率 C.准确量取一定体 D.制取少量
防止倒吸 的影响 积K 2 Cr 2 O 7 标准溶液 CO 2A.A B.B C.C D.D
【答案】D
【详解】A.氨气易溶于水,苯起不到防倒吸作用,最终仍然产生倒吸,A不合理;
B.在两支试管中,c(Fe3+)不相同,会影响实验结果,B不合理;
C.KCr O 溶液具有强氧化性,会腐蚀橡胶,不能使用碱式滴定管盛装,C不合理;
2 2 7
D.安全漏斗虽然没有活塞,但使用过程中,弯管内存留一定量的盐酸,能起到液封作用,D合理;
故选D。
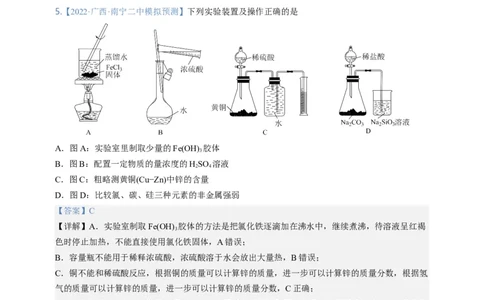
5.【2022·广西·南宁二中模拟预测】下列实验装置及操作正确的是
A.图A:实验室里制取少量的Fe(OH) 胶体
3
B.图B:配置一定物质的量浓度的HSO 溶液
2 4
C.图C:粗略测黄铜(Cu−Zn)中锌的含量
D.图D:比较氯、碳、硅三种元素的非金属强弱
【答案】C
【详解】A.实验室制取Fe(OH) 胶体的方法是把氯化铁逐滴加在沸水中,继续煮沸,待溶液呈红褐
3
色时停止加热,不能直接使用氯化铁固体,A错误;
B.容量瓶不能用于稀释浓硫酸,浓硫酸溶于水会放出大量热,B错误;
C.铜不能和稀硫酸反应,根据铜的质量可以计算锌的质量,进一步可以计算锌的质量分数,根据氢
气的质量可以计算锌的质量,进一步可以计算锌的质量分数,C正确;
D.盐酸易挥发,盐酸与硅酸钠反应,则该装置发生强酸制取弱酸的反应,但不能比较C、Si的非金
属性,故D错误;
故答案选C。
6.【2022·吉林一模】用下列实验装置进行相应的实验,能达到实验目的的是A.利用图甲验证浓硫酸具有脱水性、强氧化性,SO 具有漂白性、还原性
2
B.利用图乙制备并收集干燥的氢气
C.利用图丙制备并收集少量的NO
2
D.利用图丁制取碳酸氢钠
【答案】A
【详解】A.图甲中浓硫酸具有脱水性使蔗糖转化为碳,碳和浓硫酸生成二氧化硫气体,可以验证浓
硫酸具有脱水性、强氧化性;品红溶液、高锰酸钾溶液褪色, 可以验证SO 具有漂白性、还原性,
2
A正确;
B.氢气密度小于空气,应该用向下排空气法收集,B错误;
C.二氧化氮和水反应,不能用排水法收集,C错误;
D.氨气极易溶于水应该使用防倒吸装置,D错误;
故选A。
7.【2022·山东济南高三】下列实验装置能达到实验目的的是
A.甲:除去 中的HCl B.乙:探究浓度对反应速率的影响
C.丙:配制 的 溶液 D.丁:探究温度对化学平衡的影响
【答案】D
【详解】A.甲中NaOH溶液会将HCl和CO 都吸收掉,A不能达到实验目的;
2
B.乙中两个试管内的HSO 浓度不同,锌的颗粒大小也不同,变量不唯一,无法探究浓度对反应速
2 4
率的影响,B不能达到实验目的;
C.丙中固体溶解的过程需在烧杯中进行,不能在容量瓶中进行,C不能达到实验目的;
D.丁中两个烧杯中分别盛有热水和冰水,可以通过观察气体的颜色深浅来探究温度对2NO NO
2 2 4
平衡的影响,D能达到实验目的;故选D。【点睛】探究影响因素时一般用控制变量法,设计实验时需注意保证变量的唯一性,即对比实验中,
只有要探究的那个因素不同,其它因素完全相同。
8.【2022·河南三门峡·高三】室温下,下列实验探究方案能达到探究目的的是
选
探究方案 探究目的
项
向盛有KBr溶液的试管中滴加几滴新制氧水,再加入 溶液,
A 的氧化性比 的强
振荡、静置,观察 层颜色
向盛有 水溶液的试管中滴加几滴用盐酸酸化的 溶液,
B 具有还原性
观察溶液颜色变化
向久置的 溶液中滴加几滴KSCN溶液,振荡,观察溶液颜色
C 已全部变质
变化
将碳单质和二氧化硅固体混合置于硬质玻璃管内高温加热,并检验 比较C和Si元素的非金
D
反应后产物 属性强弱
A.A B.B C.C D.D
【答案】A
【详解】A.氯水可氧化KBr生成Br ,Br 溶于CCl 呈橙黄色,可知Cl 的氧化性比Br 强,故A项
2 2 4 2 2
符合题意;
B. 可被酸性 溶液氧化,溶液褪色,但Cl-也能被酸性 氧化,故B项不符合题意;
C.溶液呈红色,证明FeSO 溶液已变质,但无法证明Fe2+不存在,即无法证明FeSO 溶液已完全变
4 4
质,故C项不符合题意;
D.C和SiO 在高温下反应生成Si和CO,反应过程中碳失电子,此反应不能说明非金属性C>Si,故
2
D项不符合题意。
综上所述,答案为A项。
9.【2022·山东济宁·高三期中】下列方案设计、现象和结论都正确的是
选
实验目的 方案设计 现象和结论
项
检验 和浓盐酸反 取少量反应后的溶液于试管中,依次加 若产生大量白色沉淀,则
A
应后是否有酸剩余 入稀硝酸、硝酸银溶液,观察 说明盐酸有剩余
B 检验Cu O固体中是否含 取样,加入足量稀盐酸,观察现象 若有红色固体剩余,则说
2有单质Cu 明样品中有单质Cu
鉴别NaCl与NaNO 溶 分别取少量溶液于试管中,再滴加 若溶液的紫红色不褪去,
2
C
液 KMnO 酸性溶液 则为NaCl溶液
4
比较氧和硫的非金属性 若溶液变浑浊,说明氧的
D 将氧气通入 S的水溶液中
强弱 非金属性大于硫
A.A B.B C.C D.D
【答案】D
【详解】A. 和浓盐酸反应产生氯化锰,无论有没有盐酸剩余,加入稀硝酸、硝酸银溶液,都
会有白色沉淀,故A错误;
B.Cu O在酸性条件会歧化生成Cu和Cu2+,不能确定是否混有单质Cu,故B错误;
2
C.Cl-和NO 都能使酸性高锰酸钾褪色,不能鉴别NaCl与NaNO 溶液,故C错误;
2
D.氧气能置换出HS溶液的S,说明氧的非金属性大于硫,故D正确;
2
故答案为D。
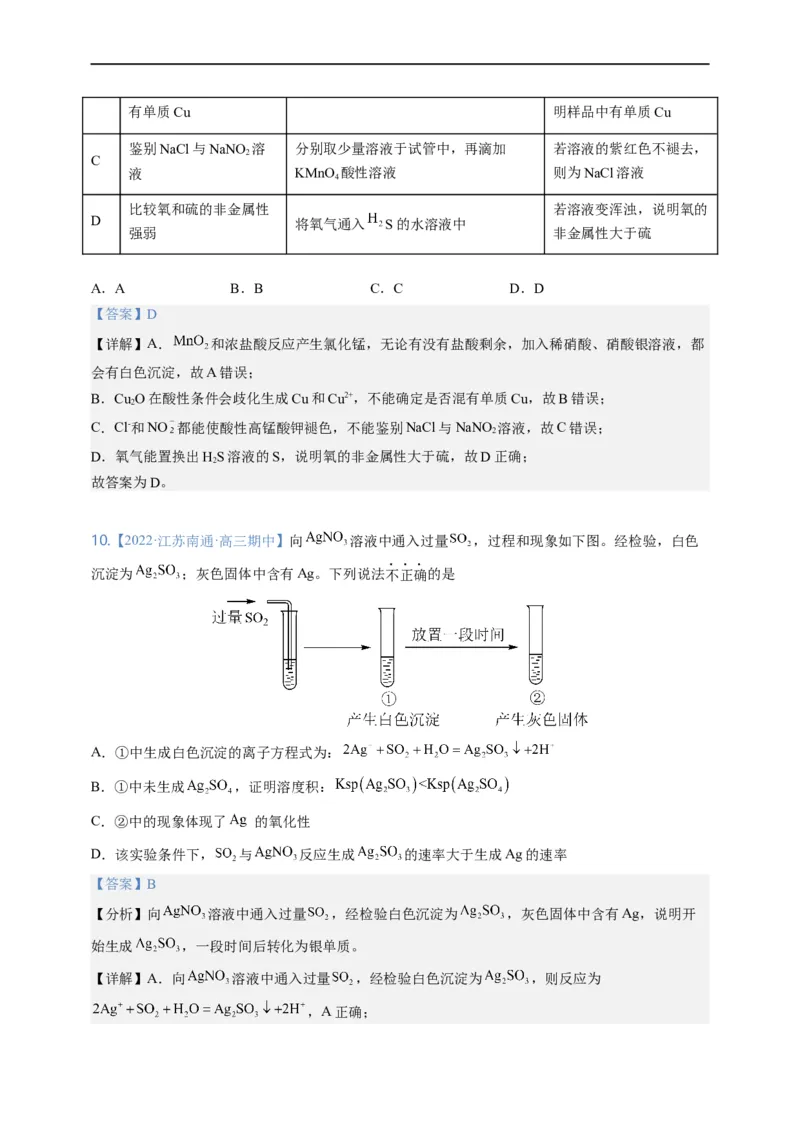
10.【2022·江苏南通·高三期中】向 溶液中通入过量 ,过程和现象如下图。经检验,白色
沉淀为 ;灰色固体中含有Ag。下列说法不正确的是
A.①中生成白色沉淀的离子方程式为:
B.①中未生成 ,证明溶度积:
C.②中的现象体现了 的氧化性
D.该实验条件下, 与 反应生成 的速率大于生成Ag的速率
【答案】B
【分析】向 溶液中通入过量 ,经检验白色沉淀为 ,灰色固体中含有Ag,说明开
始生成 ,一段时间后转化为银单质。
【详解】A.向 溶液中通入过量 ,经检验白色沉淀为 ,则反应为
,A正确;B.开始生成 ,一段时间后转化为银单质,说明实验中生成 的速率大于生成Ag的速
率,①中开始没有生成 ,不能说明溶度积: ,B错误;
C.灰色固体中含有Ag,则银离子化合价降低发生还原反应生成银单质,银离子为氧化剂,故②中
的现象体现了 的氧化性,C正确;
D.该实验条件下, 与 反应开始生成 ,一段时间后转化为银单质,说明实验中生
成 的速率大于生成Ag的速率,D正确;
故选B。
热点集 点击 核心
热点 猜想
11.【2022内蒙古锡盟二中高三统考】固体化合物X由3种元素组成。某学习小组进行了如下实验。
下列推断不正确的是
A.由现象1得出化合物X含有氢元素
B.固体混合物Y的成分是Cu和KOH
C. 的化学式KCuO
2
D.若X与浓盐酸反应产生黄绿色气体,则反应中X作氧化剂
【答案】A
【分析】由现象1可知混合气体含水蒸气,根据元素守恒可知X中含有O元素;固体混合物Y溶于
水,生成紫红色固体单质,则固体单质为Cu,并得到碱性溶液,焰色反应呈紫色,说明含有K元素,
与盐酸发生中和反应,应为KOH,则X含有K、Cu、O等元素,2.70g X中含Cu原子的物质的量为
,根据KOH+HCl=KCl+H O可知X中所含K原子的物质的量为0.02mol,根据质
2
量守恒可知X中O元素的质量为2.7g-1.28g-0.02mol×39g/mol=0.64g,O原子的物质的量为
,X中K、Cu、O原子物质的量之比为0.02mol:0.02mol:0.04mol=1:1:2,因
此X的化学式为KCuO 。
2
【详解】A.X与过量H 反应生成的混合气体含水蒸气,则现象1说明X中含O元素,故A项错误;
2
B.由上述分析可知,固体混合物Y的成分是Cu和KOH,故B项正确;
C.由上述分析可知,X的化学式为KCuO ,故C项正确;
2D.若KCuO 与浓盐酸反应产生黄绿色气体(Cl ),则在反应过程中Cl元素被氧化,HCl作还原剂,
2 2
根据化合价升降守恒可知反应过程中KCuO 内部分元素化合价降低被还原,KCuO 作氧化剂,故D
2 2
项正确;
综上所述,不正确的是A项。
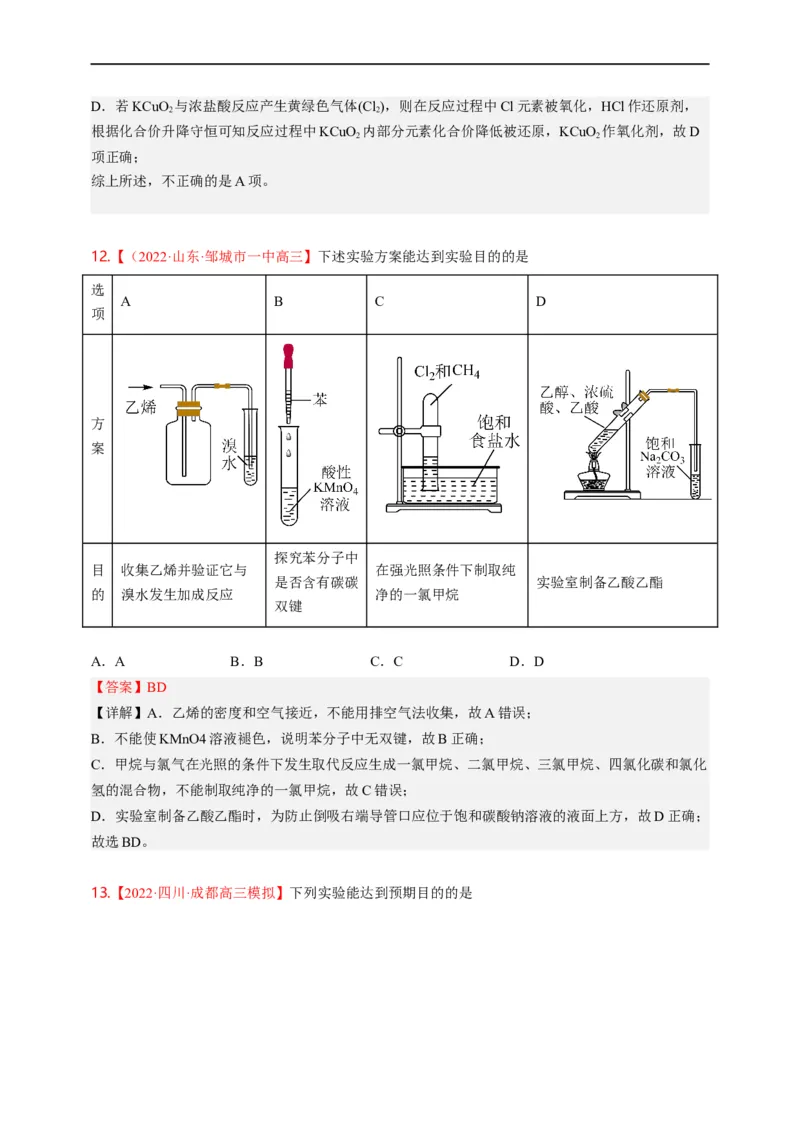
12.【(2022·山东·邹城市一中高三】下述实验方案能达到实验目的的是
选
A B C D
项
方
案
探究苯分子中
目 收集乙烯并验证它与 在强光照条件下制取纯
是否含有碳碳 实验室制备乙酸乙酯
的 溴水发生加成反应 净的一氯甲烷
双键
A.A B.B C.C D.D
【答案】BD
【详解】A.乙烯的密度和空气接近,不能用排空气法收集,故A错误;
B.不能使KMnO4溶液褪色,说明苯分子中无双键,故B正确;
C.甲烷与氯气在光照的条件下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化
氢的混合物,不能制取纯净的一氯甲烷,故C错误;
D.实验室制备乙酸乙酯时,为防止倒吸右端导管口应位于饱和碳酸钠溶液的液面上方,故D正确;
故选BD。
13.【2022·四川·成都高三模拟】下列实验能达到预期目的的是A.甲:分离己烷和水
B.乙:从 处移到 处,观察到铜丝由黑变红
C.丙:检验无水乙醇中是否有水
D.丁:分离含碘的四氯化碳溶液,最终在锥形瓶中可获得碘
【答案】B
【详解】A.己烷和水是互不相溶的两种液体,不能用过滤法分离,A不符合题意;
B.火焰的外焰处氧气充足,铜丝受热被氧化生成黑色氧化铜,火焰的内焰处氧气不足,铜丝仍然以
红色的单质存在,B符合题意;
C.乙醇与水均能与金属钠反应生成氢气,不能用该方法检验无水乙醇中是否有水,C不符合题意;
D.碘单质从四氯化碳溶液中蒸发出来,进入冷凝管发生凝华得到固体,锥形瓶中得不到碘,D不符
合题意;
故选B。
14.【2022·广西·桂平市浔州高级中学高三期中】下列除杂试剂的选择无法达到除杂目的的是
选项 物质 杂质 除杂试剂
A 盐酸 硫酸 适量BaCl 溶液
2
B NaCl溶液 CuCl 适量KOH溶液
2
C NaOH溶液 NaCO 适量Ba(OH) 溶液
2 3 2
D 铜粉 CuO CO
A.A B.B C.C D.D
【答案】B
【详解】A.HSO 与适量BaCl 溶液混合,发生反应产生HCl、BaSO 沉淀,过量,除去BaSO 沉淀,
2 4 2 4 4
就得到纯净的盐酸,A不符合题意;
B.CuCl 与适量KOH溶液混合,会发生反应产生Cu(OH) 沉淀和KCl,不能得到纯净NaCl溶液,B
2 2
符合题意;
C.杂质NaCO 与适量Ba(OH) 溶液反应产生BaCO 沉淀和NaOH,然后过滤除去BaCO 沉淀,就
2 3 2 3 3
得到纯净的NaOH溶液,C不符合题意;D.CuO与足量CO在加热时发生反应产生Cu、CO,就得到纯净的Cu单质,D不符合题意;
2
故合理选项是B。
15.【2022·黑龙江·哈师大附中高三阶段练习】下列实验操作不能达到实验目的的是
选
实验操作
项
A 说明 具有还原性 向酸性 溶液中滴加 溶液,观察紫色褪去
B 除去 溶液中的 先加入双氧水,再加入氧化铜调 ,搅拌、过滤
取样,加入盐酸酸化的 溶液,观察是否产生白色
C 检验X溶液中是否含
沉淀
说明浓硫酸有脱水性和强氧化
D 一定量蔗糖中滴入浓硫酸,搅拌,观察现象
性
A.A B.B C.C D.D
【答案】C
【详解】A.向酸性KMnO 溶液中滴加HO 溶液,观察紫色褪去,说明HO 具有还原性,将
4 2 2 2 2
KMnO 还原,故 A 正确;
4
B.除 溶液中的FeCl ,先加入双氧水,将 Fe2+氧化为 Fe3+,再加入氧化铜调 pH ,使
2
平衡正向移动,搅拌、过滤除去 Fe ( OH ) 沉淀,故 B 正确;
3
C.取样,加入盐酸酸化的 ,溶液,观察是否产生白色沉淀,不能检验 X溶液中是否含
,可能含有 或 Ag+,故 C 错误;
D.一定量蔗糖中滴入浓硫酸,搅拌,蔗糖变黑并膨胀且产生刺激性气味气体,说明浓硫酸使蔗糖脱
水炭化,然后浓硫酸将碳氧化: ,能说明浓硫酸有脱水性和
强氧化性,故D正确;
故本题选C。
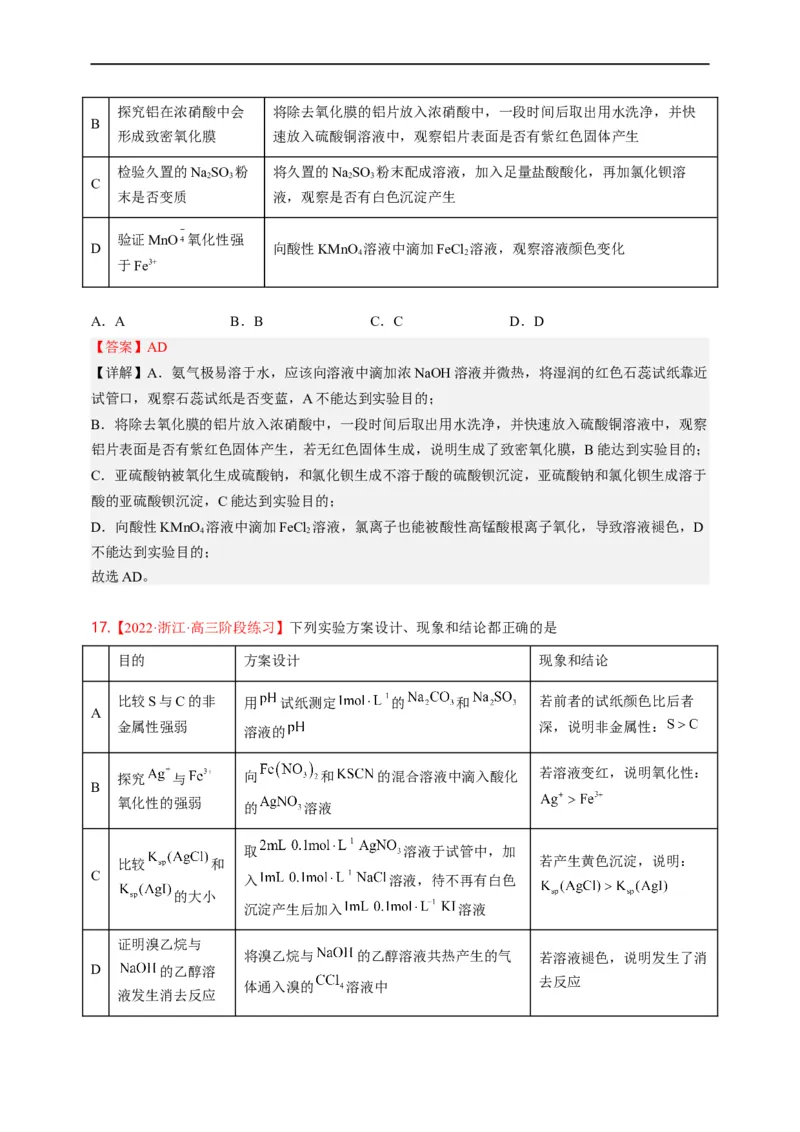
16.【2022·山东济南·高三期中】下列实验方法或操作不能达到目的的是
实验目的 实验方法或操作
检验溶液中是否存在 向溶液中滴加少量NaOH稀溶液,将湿润的红色石蕊试纸靠近试管
A
NH 口,观察石蕊试纸是否变蓝探究铝在浓硝酸中会 将除去氧化膜的铝片放入浓硝酸中,一段时间后取出用水洗净,并快
B
形成致密氧化膜 速放入硫酸铜溶液中,观察铝片表面是否有紫红色固体产生
检验久置的NaSO 粉 将久置的NaSO 粉末配成溶液,加入足量盐酸酸化,再加氯化钡溶
2 3 2 3
C
末是否变质 液,观察是否有白色沉淀产生
验证MnO 氧化性强
D 向酸性KMnO 溶液中滴加FeCl 溶液,观察溶液颜色变化
4 2
于Fe3+
A.A B.B C.C D.D
【答案】AD
【详解】A.氨气极易溶于水,应该向溶液中滴加浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近
试管口,观察石蕊试纸是否变蓝,A不能达到实验目的;
B.将除去氧化膜的铝片放入浓硝酸中,一段时间后取出用水洗净,并快速放入硫酸铜溶液中,观察
铝片表面是否有紫红色固体产生,若无红色固体生成,说明生成了致密氧化膜,B能达到实验目的;
C.亚硫酸钠被氧化生成硫酸钠,和氯化钡生成不溶于酸的硫酸钡沉淀,亚硫酸钠和氯化钡生成溶于
酸的亚硫酸钡沉淀,C能达到实验目的;
D.向酸性KMnO 溶液中滴加FeCl 溶液,氯离子也能被酸性高锰酸根离子氧化,导致溶液褪色,D
4 2
不能达到实验目的;
故选AD。
17.【2022·浙江·高三阶段练习】下列实验方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
比较S与C的非 用 试纸测定 的 和 若前者的试纸颜色比后者
A
金属性强弱 深,说明非金属性:
溶液的
探究 与 向 和 的混合溶液中滴入酸化 若溶液变红,说明氧化性:
B
氧化性的强弱
的 溶液
取 溶液于试管中,加
比较 和 若产生黄色沉淀,说明:
C
入 溶液,待不再有白色
的大小
沉淀产生后加入 溶液
证明溴乙烷与
将溴乙烷与 的乙醇溶液共热产生的气 若溶液褪色,说明发生了消
D 的乙醇溶
去反应
体通入溴的 溶液中
液发生消去反应A.A B.B C.C D.D
【答案】D
【详解】A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,要根据钠盐溶液 pH 大小
确定非金属性强弱时必须是其最高价含氧酸的盐,亚硫酸钠不是S元素最高价氧化物的水化物的盐
溶液,所以不能根据等物质的量浓度的 Na2CO3和Na2SO3溶液的 pH 值判断非金属的非金属性
强弱,故A错误;
B.NO 也有氧化性,也可以氧化Fe2+,溶液变红不能证明Ag+氧化了Fe2+还是NO 氧化Fe2+,故B
错误;
C. 溶液过量,加入I-后,过量的Ag+与I-直接生成了 沉淀,不是沉淀的转化,故C错误;
D.溴乙烷与 的乙醇溶液发生消去反应生成乙烯,乙烯通入溴的 溶液中发生加成反应,
溶液褪色说明发生了消去反应,故D正确;
故答案为D
18.【2022·北京四中】下列实验方案不能达到相应目的的是
目的 A.验证Fe是否被氧化 B.研究浓度对FeCl 水解平衡的影响
3
实验
方案
C.比较CHCOOH和HBO(硼酸,一元弱酸)酸
3 3 3
目的 D.比较AgCl和AgI溶解度的大小
性的强弱
实验
方案
A.A B.B C.C D.D
【答案】D
【详解】A.取Fe电极附近溶液放入试管,加入K[Fe(CN) ]溶液,试管内无明显现象,表明溶液中
3 6
不含有Fe2+,从而表明Fe没有被氧化,A不符合题意;B.0.1mol/LFeCl 溶液的pH=1.43,加水稀释10倍后,若不存在水解平衡,pH=2.43,现在溶液的
3
pH=2.19<2.43,则表明加水稀释后溶液中H+的物质的量增大,从而表明减小浓度,FeCl 的水解平
3
衡正向移动,B不符合题意;
C.CHCOOH溶液中有气泡产生,表明酸性CHCOOH>HCO,HBO 溶液中无气泡产生,表明酸
3 3 2 3 3 3
性HBO<HCO,从而证明CHCOOH的酸性比HBO 强,C不符合题意;
3 3 2 3 3 3 3
D.2mL0.1mol/LAgNO 溶液中加入3滴0.1mol/LNaCl溶液后,AgNO 大量剩余,再加入KI溶液,
3 3
直接与AgNO 反应,而不是与AgCl反应,所以不能比较AgCl和AgI溶解度的大小,D符合题意;
3
故选D。
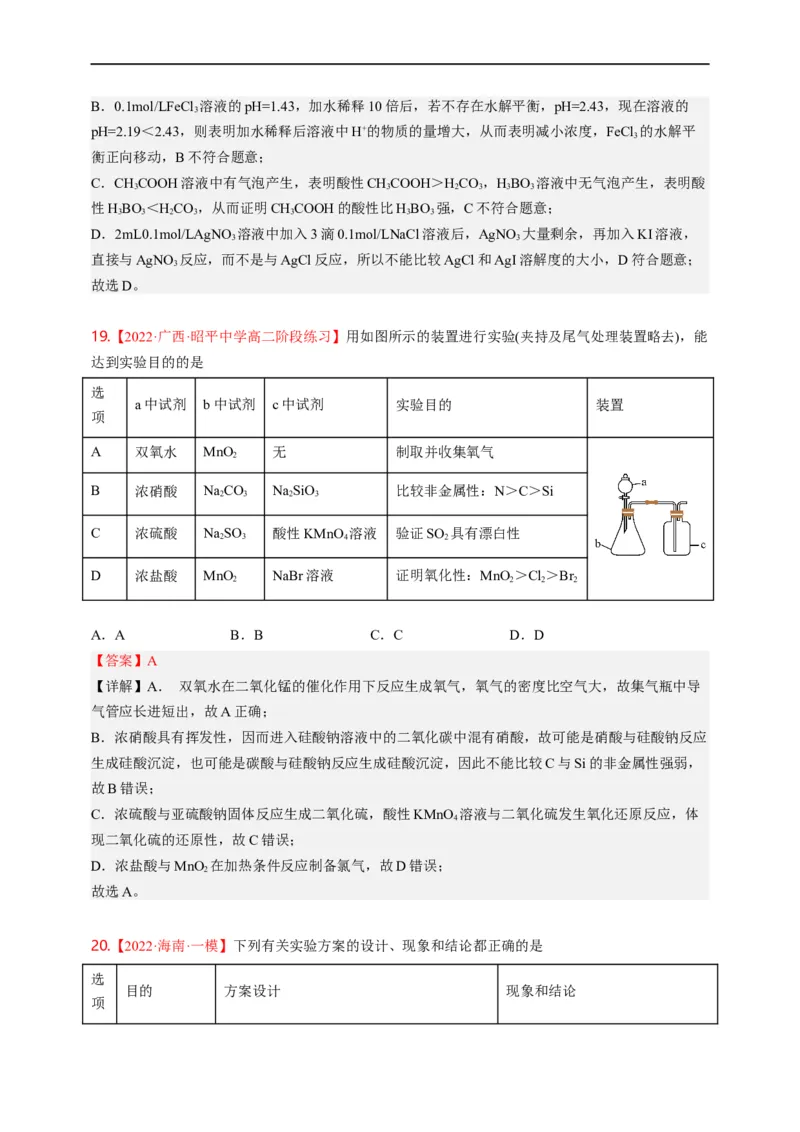
19.【2022·广西·昭平中学高二阶段练习】用如图所示的装置进行实验(夹持及尾气处理装置略去),能
达到实验目的的是
选
a中试剂 b中试剂 c中试剂 实验目的 装置
项
A 双氧水 MnO 无 制取并收集氧气
2
B 浓硝酸 NaCO NaSiO 比较非金属性:N>C>Si
2 3 2 3
C 浓硫酸 NaSO 酸性KMnO 溶液 验证SO 具有漂白性
2 3 4 2
D 浓盐酸 MnO NaBr溶液 证明氧化性:MnO >Cl>Br
2 2 2 2
A.A B.B C.C D.D
【答案】A
【详解】A. 双氧水在二氧化锰的催化作用下反应生成氧气,氧气的密度比空气大,故集气瓶中导
气管应长进短出,故A正确;
B.浓硝酸具有挥发性,因而进入硅酸钠溶液中的二氧化碳中混有硝酸,故可能是硝酸与硅酸钠反应
生成硅酸沉淀,也可能是碳酸与硅酸钠反应生成硅酸沉淀,因此不能比较C与Si的非金属性强弱,
故B错误;
C.浓硫酸与亚硫酸钠固体反应生成二氧化硫,酸性KMnO 溶液与二氧化硫发生氧化还原反应,体
4
现二氧化硫的还原性,故C错误;
D.浓盐酸与MnO 在加热条件反应制备氯气,故D错误;
2
故选A。
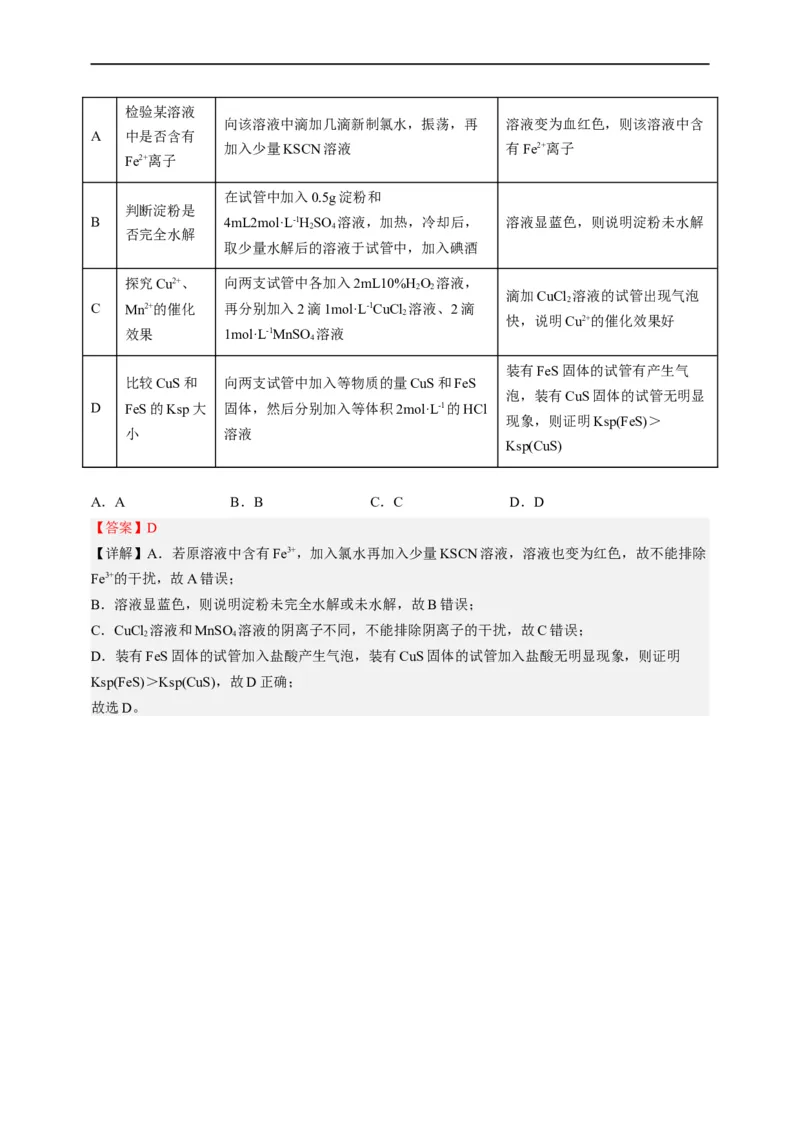
20.【2022·海南·一模】下列有关实验方案的设计、现象和结论都正确的是
选
目的 方案设计 现象和结论
项检验某溶液
向该溶液中滴加几滴新制氯水,振荡,再 溶液变为血红色,则该溶液中含
A 中是否含有
加入少量KSCN溶液 有Fe2+离子
Fe2+离子
在试管中加入0.5g淀粉和
判断淀粉是
B 4mL2mol·L-1HSO 溶液,加热,冷却后, 溶液显蓝色,则说明淀粉未水解
2 4
否完全水解
取少量水解后的溶液于试管中,加入碘酒
探究Cu2+、 向两支试管中各加入2mL10%H O 溶液,
2 2
滴加CuCl 溶液的试管出现气泡
2
C Mn2+的催化 再分别加入2滴1mol·L-1CuCl 溶液、2滴
2
快,说明Cu2+的催化效果好
效果 1mol·L-1MnSO 溶液
4
装有FeS固体的试管有产生气
比较CuS和 向两支试管中加入等物质的量CuS和FeS
泡,装有CuS固体的试管无明显
D FeS的Ksp大 固体,然后分别加入等体积2mol·L-1的HCl
现象,则证明Ksp(FeS)>
小 溶液
Ksp(CuS)
A.A B.B C.C D.D
【答案】D
【详解】A.若原溶液中含有Fe3+,加入氯水再加入少量KSCN溶液,溶液也变为红色,故不能排除
Fe3+的干扰,故A错误;
B.溶液显蓝色,则说明淀粉未完全水解或未水解,故B错误;
C.CuCl 溶液和MnSO 溶液的阴离子不同,不能排除阴离子的干扰,故C错误;
2 4
D.装有FeS固体的试管加入盐酸产生气泡,装有CuS固体的试管加入盐酸无明显现象,则证明
Ksp(FeS)>Ksp(CuS),故D正确;
故选D。