文档内容
绝密★启用前
2024 年中考押题预测卷 02【福建卷】
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
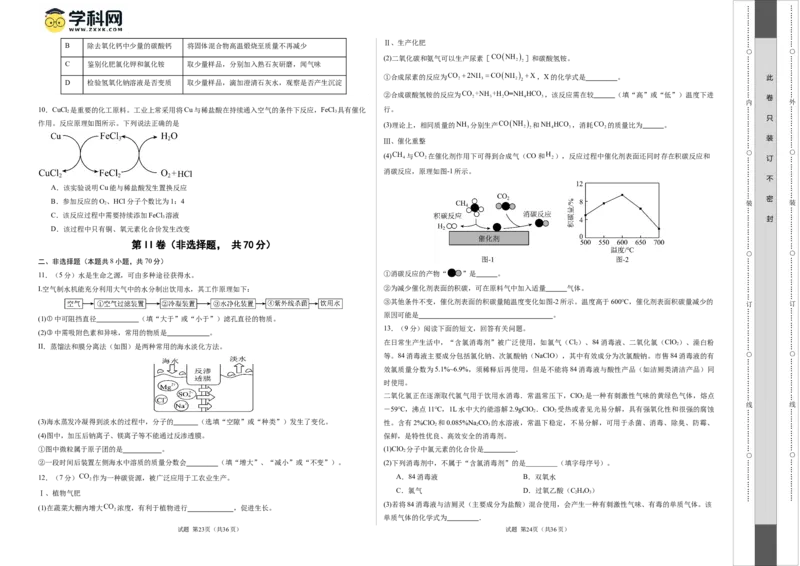
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。 A.X可表示氮气
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动, B.Y可用于医疗急救
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。 C.纵坐标表示气体质量分数
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。 D.稀有气体通电时能发出不同颜色的光,可用于电光源制造
4.考试结束后,将本试卷和答题卡一并交回。 6.铯原子钟是目前世界上最精确的时钟。铯元素的原子结构示意图及其在元素周期表中的信息如下图所
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 K-39 示。下列说法错误的是
第I卷(选择题, 共30分)
一、选择题(本题共10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1.下列做法不符合“健康、安全、绿色、舒适”生活理念的是
A.海鲜防腐,甲醛浸泡 B.油锅着火,锅盖盖灭
C.垃圾分类,资源再生 D.限放鞭炮,保护环境
2.滑雪运动可锻炼平衡力和意志力。滑雪板中的玻璃纤维增强塑料属于
A.铯元素属于金属元素 B.铯原子核内有55个质子
A.天然材料 B.复合材料 C.金属材料 D.非金属材料
C.铯离子有6个电子层 D.铯元素的相对原子质量为132.9
3.《天工开物)中记载有我国历史上出现的下列造物过程,其中涉及化学变化的是
7.银杏果中含有银杏酸 ,以下基于化学观念对银杏酸的认识正确的是
A.织衣布 B.钉术舟 C.炼生铁 D.晒海盐
A.元素观:银杏酸分子由碳、氢、氧三种元素组成
4.稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是
B.微粒观:银杏酸由22个碳原子、34个氢原子和3个氧原子构成
C.变化观:银杏酸不完全燃烧的产物有 和炭黑等
D.质量观:银杏酸中碳元素和氢元素的质量比为
8.基于证据的推理是化学的核心素养之一,下列有关推断不正确的是
A.化学反应常伴随能量的变化,像铁生锈、食物腐烂均放出热量
B.燃气与空气混合点燃常会发生爆炸, 与空气混合点燃也可能爆炸
A.稀释浓硫酸 B.测稀硫酸的pH C.倾倒稀硫酸 D.滴加稀硫酸
C.碱性溶液中都含有 ,纯碱溶液呈碱性,其溶液中也一定含有
5.如图表示空气中各成分的含量,下列有关说法错误的是
D.有机物中都含有碳元素,所以含有碳元素的化合物一定是有机物
9.下列实验方案设计不合理的是
选
实验目的 实验方案
项
A 比较铝和锌的金属活动性强弱 将铝片和锌粒分别放入硫酸铜溶液中,观察现象………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
Ⅱ、生产化肥
B 除去氧化钙中少量的碳酸钙 将固体混合物高温煅烧至质量不再减少
(2)二氧化碳和氨气可以生产尿素[ ]和碳酸氢铵。
C 鉴别化肥氯化钾和氯化铵 取少量样品,分别加入熟石灰研磨,闻气味
①合成尿素的反应为 ,X的化学式是 。 此
D 检验氢氧化钠溶液是否变质 取少量样品,滴加澄清石灰水,观察是否产生沉淀
②合成碳酸氢铵的反应为 ,该反应需在较 (填“高”或“低”)温度下进
卷
10.CuCl 是重要的化工原料。工业上常采用将Cu与稀盐酸在持续通入空气的条件下反应,FeCl 具有催化 行。
2 3
只
作用。反应原理如图所示。下列说法正确的是 (3)理论上,相同质量的 分别生产 和 ,消耗 的质量比为 。
装
Ⅲ、催化重整
(4) 与 在催化剂作用下可得到合成气(CO和 ),反应过程中催化剂表面还同时存在积碳反应和
订
消碳反应,原理如图-1所示。
不
A.该实验说明Cu能与稀盐酸发生置换反应
B.参加反应的O、HCl分子个数比为1:4 密 2
C.该反应过程中需要持续添加FeCl 溶液
3 封
D.该过程中只有铜、氧元素化合价发生改变
第II卷(非选择题, 共70分)
二、非选择题(本题共8小题,共70分)
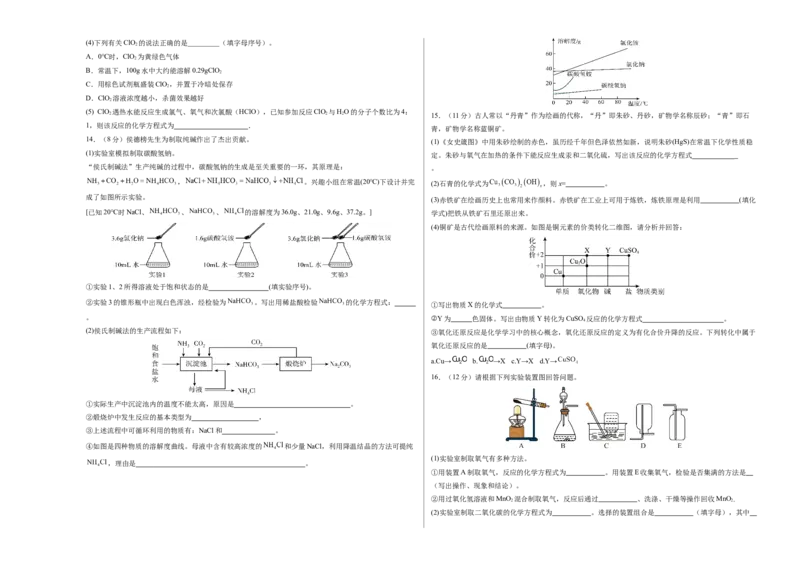
11.(5分)水是生命之源,可由多种途径获得水。 ①消碳反应的产物“ ”是 。
I.空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下: ②为减少催化剂表面的积碳,可在原料气中加入适量 气体。
③其他条件不变,催化剂表面的积碳量随温度变化如图-2所示。温度高于600℃,催化剂表面积碳量减少的
原因可能是 。
(1)①中可阻挡直径 (填“大于”或“小于”)滤孔直径的物质。
13.(9分)阅读下面的短文,回答有关问题。
(2)③中需吸附色素和异味,常用的物质是 。
在日常生产生活中,“含氯消毒剂”被广泛使用,如氯气(Cl )、84消毒液、二氧化氯(ClO )、澡白粉
II.蒸馏法和膜分离法(如图)是两种常用的海水淡化方法。 2 2
等。84消毒液主要成分包括氯化钠、次氯酸钠(NaClO),其中有效成分为次氯酸钠。市售84消毒液的有
效氯质量分数为5.1%~6.9%,须稀释后再使用,但是不能将84消毒液与酸性产品(如洁厕类清洁产品)同
时使用。
二氧化氯正在逐渐取代氯气用于饮用水消毒.常温常压下,ClO 是一种有刺激性气味的黄绿色气体,熔点
2
-59℃,沸点11℃,1L水中大约能溶解2.9gClO .ClO 受热或者见光易分解,具有强氧化性和很强的腐蚀
2 2
(3)海水蒸发冷凝得到淡水的过程中,分子的 (选填“空隙”或“种类”)发生了变化。 性。含有2%ClO 和0.085%Na CO 的水溶液,常温下稳定,不易分解,可用于杀菌、消毒、除臭、防霉、
2 2 3
(4)图中,加压后钠离子、镁离子等不能通过反渗透膜。 保鲜,是特性优良、高效安全的消毒剂。
①图中微粒属于原子团的是 。 (1)ClO 分子中氯元素的化合价是 .
2
②一段时间后装置左侧海水中溶质的质量分数会 (填“增大”、“减小”或“不变”)。 (2)下列消毒剂中,不属于“含氯消毒剂”的是_________(填字母序号)。
12.(7分) 作为一种碳资源,被广泛应用于工农业生产。 A.84消毒液 B.双氧水
C.氯气 D.过氧乙酸(C HO)
Ⅰ、植物气肥 2 4 3
(3)若将84消毒液与洁厕灵(主要成分为盐酸)混合使用,会产生一种有刺激性气味、有毒的单质气体。该
(1)在蔬菜大棚内增大 浓度,有利于植物进行 ,促进生长。
单质气体的化学式为 .
试题 第23页(共36页) 试题 第24页(共36页)(4)下列有关ClO 的说法正确的是_________(填字母序号)。
2
A.0℃时,ClO 为黄绿色气体
2
B.常温下,100g水中大约能溶解0.29gClO
2
C.用棕色试剂瓶盛装ClO ,并置于冷暗处保存
2
D.ClO 溶液浓度越小,杀菌效果越好
2
(5) ClO 遇热水能反应生成氯气、氧气和次氯酸(HClO),已知参加反应ClO 与HO的分子个数比为4:
2 2 2 15.(11分)古人常以“丹青”作为绘画的代称,“丹”即朱砂、丹砂,矿物学名称辰砂;“青”即石
1,则该反应的化学方程式为 .
青,矿物学名称蓝铜矿。
14.(8分)侯德榜先生为制取纯碱作出了杰出贡献。
(1)《女史箴图》中用朱砂绘制的赤色,虽历经千年但色泽依然如新,说明朱砂(HgS)在常温下化学性质稳
(1)实验室模拟制取碳酸氢钠。
定。朱砂与氧气在加热的条件下能反应生成汞和二氧化硫,写出该反应的化学方程式
“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是: 。
, 。兴趣小组在常温(20℃)下设计并完 (2)石青的化学式为 ,则x= 。
成了如图所示实验。
(3)赤铁矿在绘画历史上也常用来作颜料。赤铁矿在工业上可用于炼铁,炼铁原理是利用 (填化
[已知20℃时NaCl、 、 、 的溶解度为36.0g、21.0g、9.6g、37.2g。] 学式)把铁从铁矿石里还原出来。
(4)铜矿是古代绘画原料的来源。如图是铜元素的价类转化二维图,请分析并回答:
①实验1、2所得溶液处于饱和状态的是 (填实验序号)。
②实验3的锥形瓶中出现白色浑浊,经检验为 。写出用稀盐酸检验 的化学方程式:
①写出物质X的化学式 。
。 ②Y为 色固体。写出由物质Y转化为CuSO 反应的化学方程式 。
4
(2)侯氏制碱法的生产流程如下: ③氧化还原反应是化学学习中的核心概念,氧化还原反应的定义为有化合价升降的反应。下列转化中属于
氧化还原反应的是 (填字母)。
a.Cu→ b. →X c.Y→X d.Y→
16.(12分)请根据下列实验装置图回答问题。
①实际生产中沉淀池内的温度不能太高,原因是 。
②煅烧炉中发生反应的基本类型为 ,
③上述流程中可循环利用的物质有:NaCl和 。
④如图是四种物质的溶解度曲线。母液中含有较高浓度的 和少量NaCl,利用降温结晶的方法可提纯
(1)实验室制取氧气有多种方法。
,理由是 。
①用装置A制取氧气,反应的化学方程式为 。用装置E收集氧气,检验是否集满的方法是
(写出操作、现象和结论)。
②用过氧化氢溶液和MnO 混合制取氧气,反应后通过 、洗涤、干燥等操作回收MnO
2 2。
(2)实验室制取二氧化碳的化学方程式为 。选择的装置组合是 (填字母),其中………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
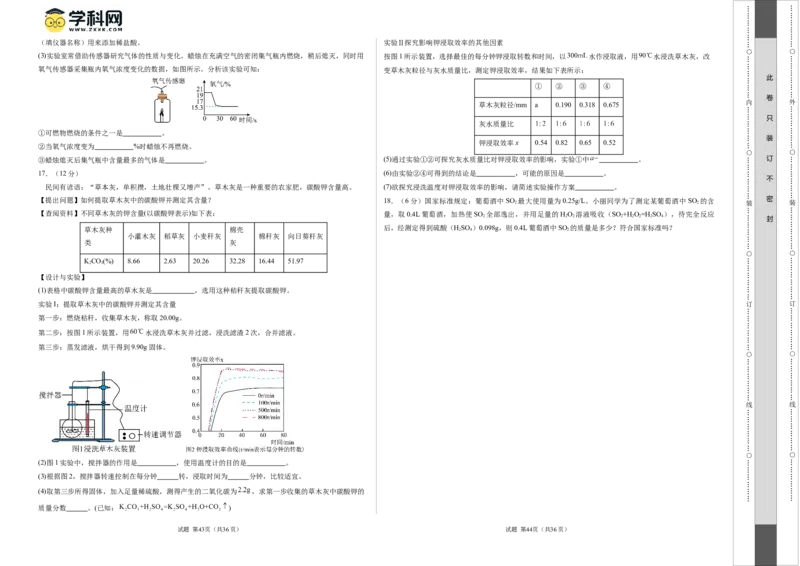
(填仪器名称)用来添加稀盐酸。 实验Ⅱ探究影响钾浸取效率的其他因素
(3)实验室常借助传感器研究气体的性质与变化。蜡烛在充满空气的密闭集气瓶内燃烧,稍后熄灭,同时用 按图1所示装置,选择最佳的每分钟钾浸取转数和时间,以 水作浸取液,用 水浸洗草木灰,改
氧气传感器采集瓶内氧气浓度变化的数据,如图所示。分析该实验可知: 变草木灰粒径与灰水质量比,测定钾浸取效率,结果如下表所示:
此
① ② ③ ④
卷
草木灰粒径/mm a 0.190 0.318 0.675
只
灰水质量比
①可燃物燃烧的条件之一是 。
装
钾浸取效率x 0.54 0.82 0.65 0.52
②当氧气浓度变为 %时蜡烛不再燃烧。
③蜡烛熄灭后集气瓶中含量最多的气体是 。 (5)通过实验①②可探究灰水质量比对钾浸取效率的影响,实验①中 。 订
17.(12分) (6)由实验②④可得到的结论是 ,可能的原因是 。
不
民间有谚语:“草本灰,单积攒,土地壮棵又增产”。草木灰是一种重要的农家肥,碳酸钾含量高。 (7)欲探究浸洗温度对钾浸取效率的影响,请简述实验操作方案 。
【提出问题】如何提取草木灰中的碳酸钾并测定其含量? 18.(6分)国家标准规定:葡萄酒中SO 最大使用量为0.25g/L。小丽同学为了测定某葡萄酒中SO 的含 密 2 2
【查阅资料】不同草木灰的钾含量(以碳酸钾表示)如下表: 量,取0.4L葡萄酒,加热使SO 全部逸出,并用足量的HO 溶液吸收(SO +H O=H SO ),待完全反应
2 2 2 2 2 2 2 4
封
草木灰种 棉壳 后,经测定得到硫酸(H 2 SO 4 )0.098g,则0.4L葡萄酒中SO 2 的质量是多少?符合国家标准吗?
小灌木灰 稻草灰 小麦秆灰 棉秆灰 向日葵杆灰
类 灰
KCO(%) 8.66 2.63 20.26 32.28 16.44 51.97
2 3
【设计与实验】
(1)表格中碳酸钾含量最高的草木灰是 ,选用这种秸秆灰提取碳酸钾。
实验I:提取草木灰中的碳酸钾并测定其含量
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:按图1所示装置,用 水浸洗草木灰并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
(2)图1实验中,搅拌器的作用是 ,使用温度计的目的是 。
(3)根据图2,搅拌器转速控制在每分钟 转,浸取时间为 分钟,比较适宜。
(4)取第三步所得固体,加入足量稀硫酸,测得产生的二氧化碳为 ,求第一步收集的草木灰中碳酸钾的
质量分数 。(已知: )
试题 第43页(共36页) 试题 第44页(共36页)