文档内容
第四讲 溶液的浓度
模块一 溶质的质量分数
知识精讲
知识点一 溶质的质量分数
1.一般溶液的溶质质量分数
思考与交流
(1)溶液是由什么组成的?
(2)溶液的质量怎么计算?
溶质的质量分数计算公式:
公式变形:
【练1】完成下列表格:
溶质 溶剂 溶液 溶质的质量分数
10g 90g
5g 100g
3g 15%
480g 500g
200g 2%2.饱和溶液的溶质质量分数
思考与交流
已知20℃时,NaCl的溶解度是36g。
(1)若向100g水中,加入36g NaCl固体,此时溶液的质量是多少g?
(2)溶质NaCl的质量分数多少?
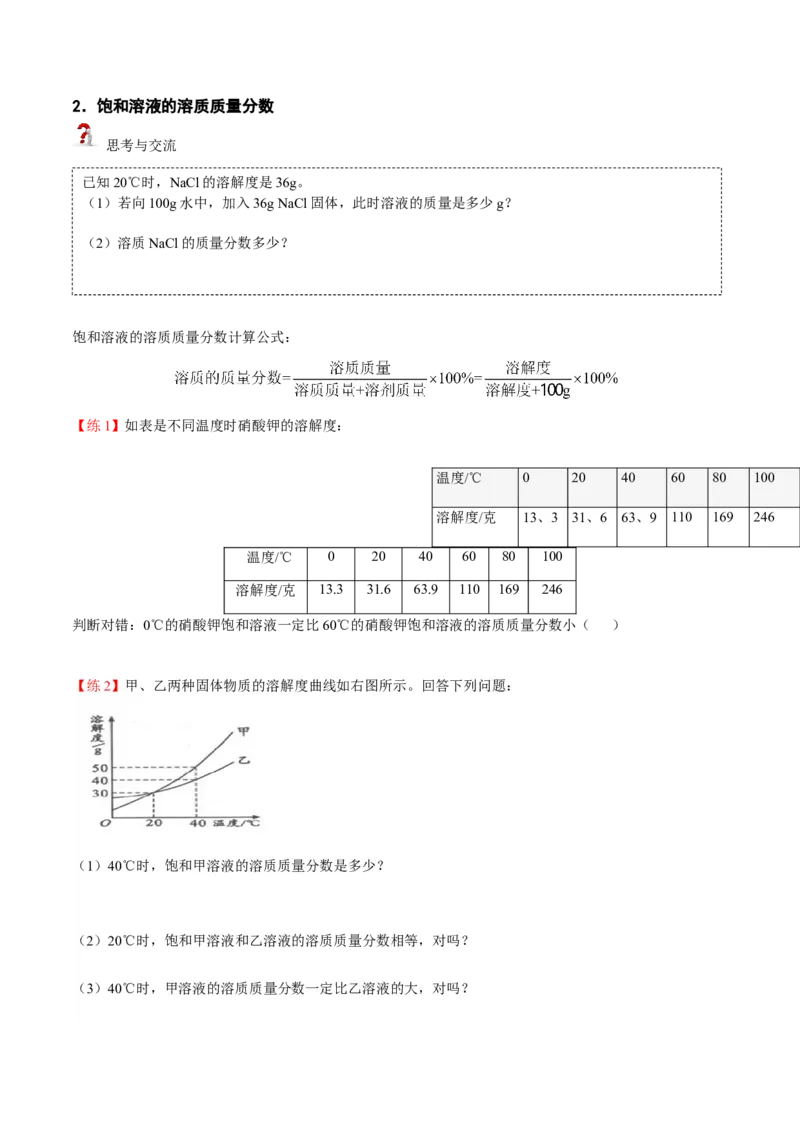
饱和溶液的溶质质量分数计算公式:
【练1】如表是不同温度时硝酸钾的溶解度:
温度/℃ 0 20 40 60 80 100
溶解度/克 13、3 31、6 63、9 110 169 246
温度/℃ 0 20 40 60 80 100
溶解度/克 13.3 31.6 63.9 110 169 246
判断对错:0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小( )
【练2】甲、乙两种固体物质的溶解度曲线如右图所示。回答下列问题:
(1)40℃时,饱和甲溶液的溶质质量分数是多少?
(2)20℃时,饱和甲溶液和乙溶液的溶质质量分数相等,对吗?
(3)40℃时,甲溶液的溶质质量分数一定比乙溶液的大,对吗?(4)甲、乙都是等质量的饱和溶液,若温度从40℃降至20℃,假设溶剂水的质量不变,谁减少的质量多?
谁的质量分数大?
3.温度变化导致溶质质量、质量分数变化
思考与交流
【思考1】如图为甲物质的溶解度曲线,据图回答:
溶解度/g
甲
C
70
D
B
50
A
30
0 t 1 t 2 温度/℃
(1)在t℃时,A点是 溶液(填‘饱和’或‘不饱和’),此时溶液含有甲物质的质量分数是
1
;若温度从t 升高到t,溶液中含有甲物质的质量是 g,质量分数 (填‘变大’、‘变
1 2
小’或‘不变’);
(2)在t℃时,B点是 溶液(填‘饱和’或‘不饱和’),若温度从t 升高到t,甲物质的质
1 1 2
量分数 (填‘变大’、‘变小’或‘不变’);
(3)在t℃时,C点是 溶液(填‘饱和’或‘不饱和’),此温度下,最多能溶解 g甲物
1
质,若温度从t 升高到t,在t 时,能溶解 g甲物质,则甲物质的质量分数 (填‘变大’、
1 2 2
‘变小’或‘不变’);
【思考2】如图为乙物质的溶解度曲线,据图回答:
溶解度/g
C
70
50
B
D
A
30 乙
0 t t
1 2 温度/℃
(1)乙物质在A点时,若温度从t 升高到t,从A→D点,乙物质的质量分数 (填‘变大’、
1 2
‘变小’或‘不变’,下同);
(2)乙物质在B点时,若温度从t 升高到t,150g乙溶液析出乙物质的质量 g,乙物质的质量分数
1 2
;
(3)乙物质在C点时,升高温度,乙物质的质量分数 ;
经典例题 一般溶液的溶质质量分数
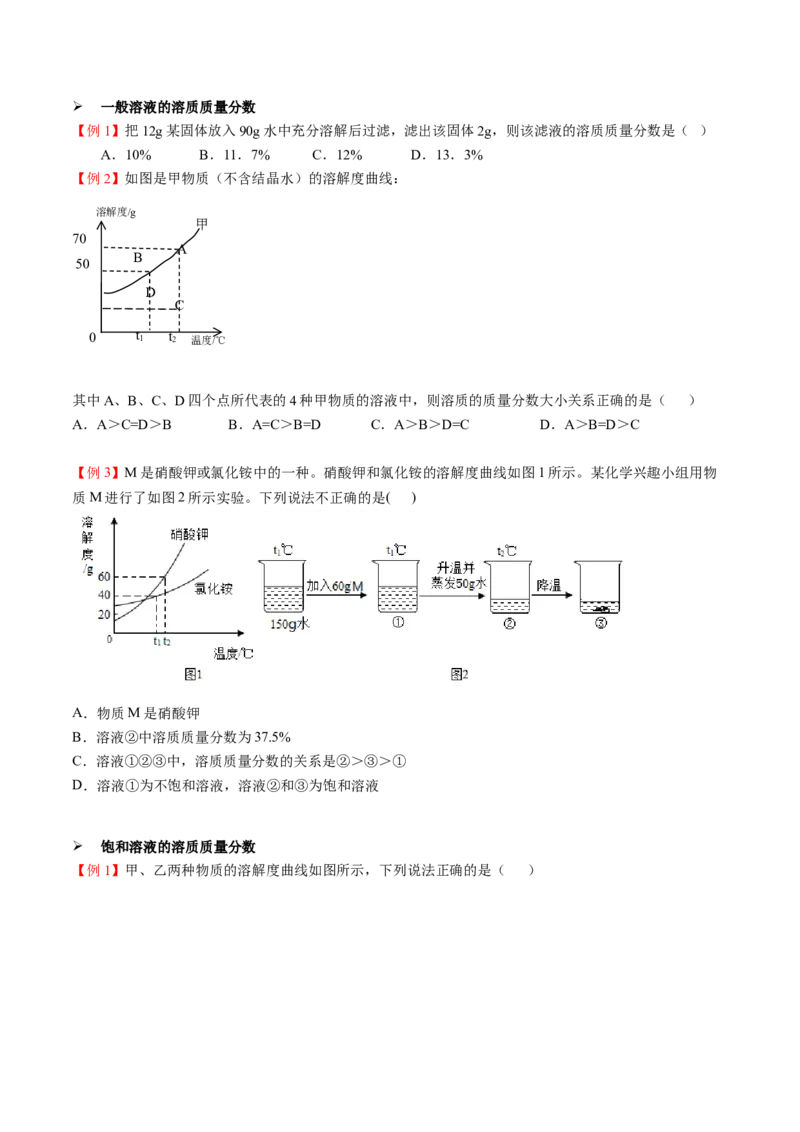
【例1】把12g某固体放入90g水中充分溶解后过滤,滤出该固体2g,则该滤液的溶质质量分数是(A)
A.10% B.11.7% C.12% D.13.3%
【例2】如图是甲物质(不含结晶水)的溶解度曲线:
溶解度/g
甲
70
A
B
50
D
C
0 t 1 t 2 温度/℃
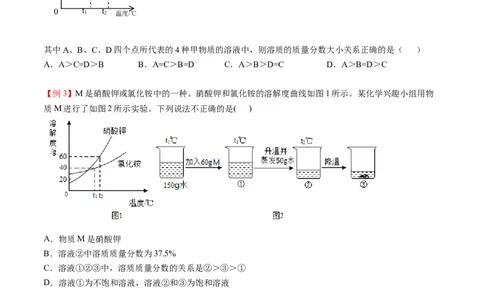
其中A、B、C、D四个点所代表的4种甲物质的溶液中,则溶质的质量分数大小关系正确的是( )
A.A>C=D>B B.A=C>B=D C.A>B>D=C D.A>B=D>C
【例3】M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物
质M进行了如图2所示实验。下列说法不正确的是( )
A.物质M是硝酸钾
B.溶液②中溶质质量分数为37.5%
C.溶液①②③中,溶质质量分数的关系是②>③>①
D.溶液①为不饱和溶液,溶液②和③为饱和溶液
饱和溶液的溶质质量分数
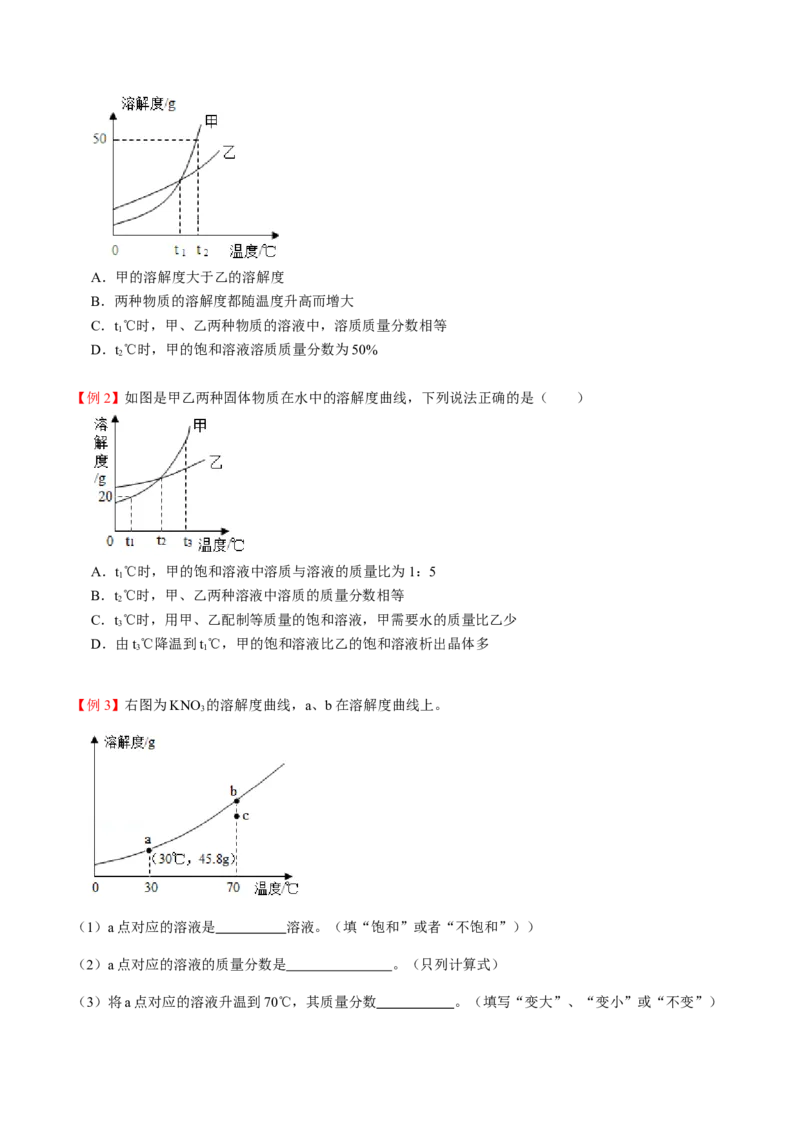
【例1】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )A.甲的溶解度大于乙的溶解度
B.两种物质的溶解度都随温度升高而增大
C.t℃时,甲、乙两种物质的溶液中,溶质质量分数相等
1
D.t℃时,甲的饱和溶液溶质质量分数为50%
2
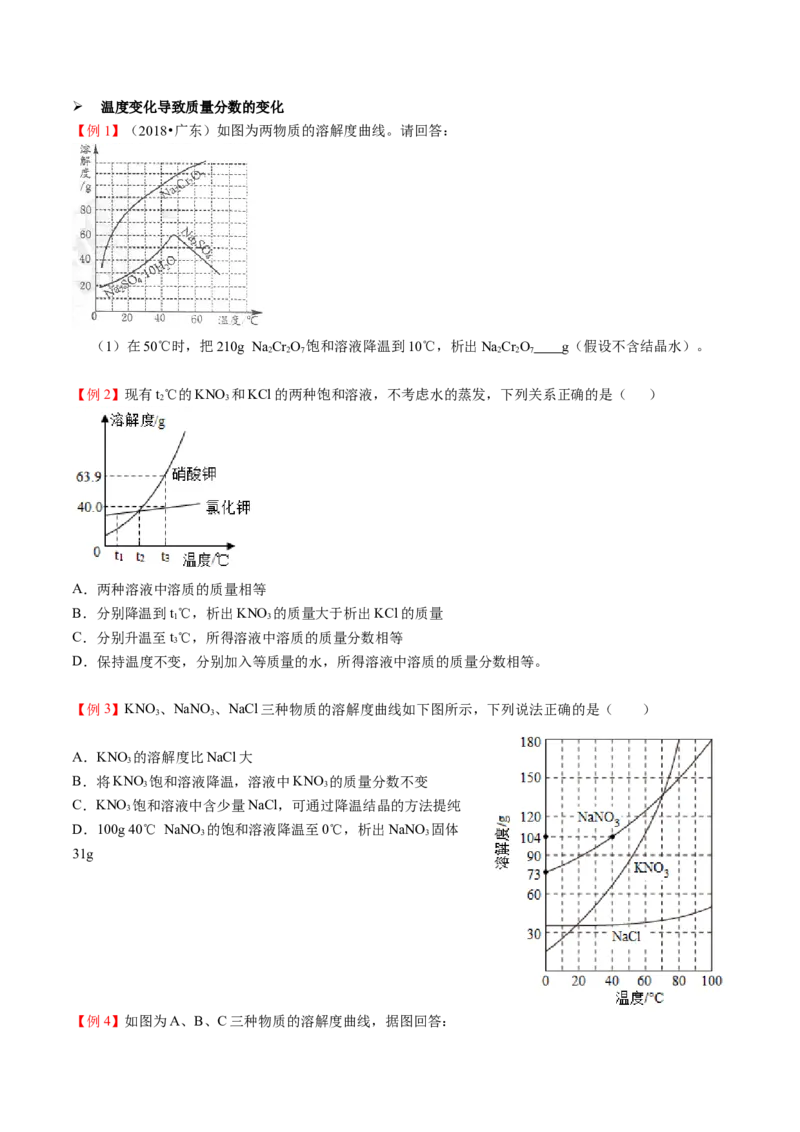
【例2】如图是甲乙两种固体物质在水中的溶解度曲线,下列说法正确的是( )
A.t℃时,甲的饱和溶液中溶质与溶液的质量比为1:5
1
B.t℃时,甲、乙两种溶液中溶质的质量分数相等
2
C.t℃时,用甲、乙配制等质量的饱和溶液,甲需要水的质量比乙少
3
D.由t℃降温到t℃,甲的饱和溶液比乙的饱和溶液析出晶体多
3 1
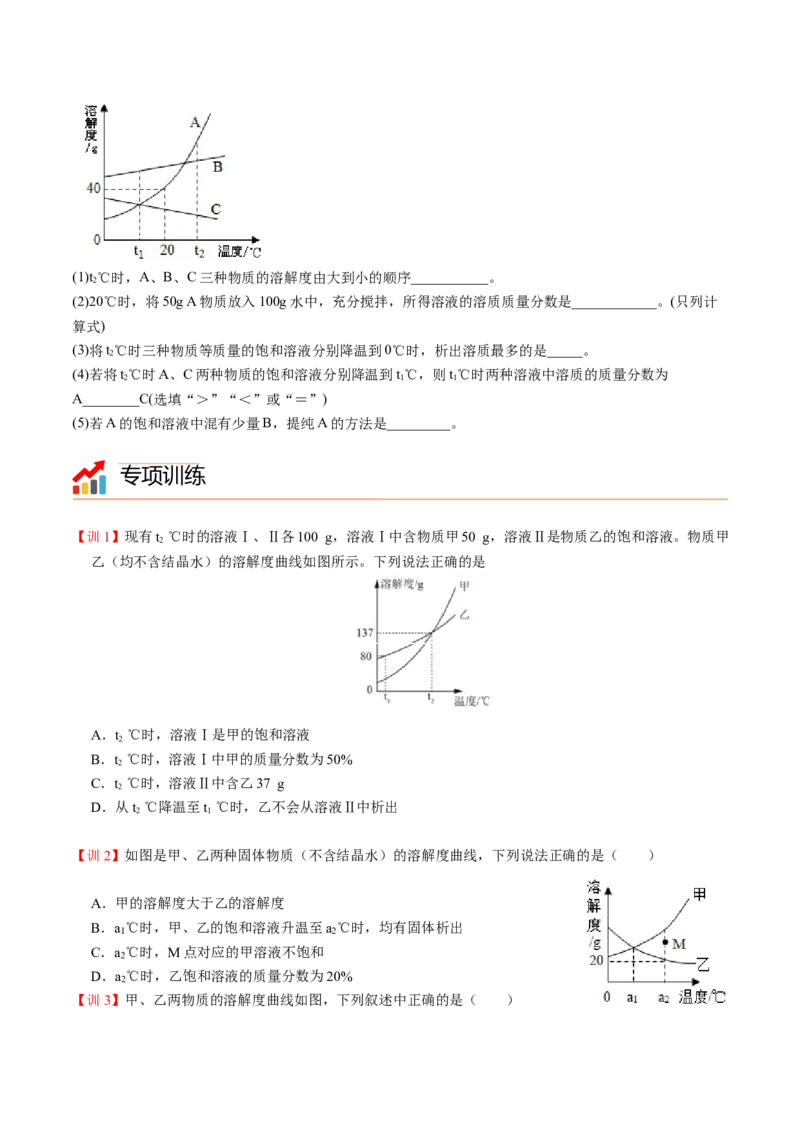
【例3】右图为KNO 的溶解度曲线,a、b在溶解度曲线上。
3
(1)a点对应的溶液是 溶液。(填“饱和”或者“不饱和”))
(2)a点对应的溶液的质量分数是 。(只列计算式)
(3)将a点对应的溶液升温到70℃,其质量分数 。(填写“变大”、“变小”或“不变”) 温度变化导致质量分数的变化
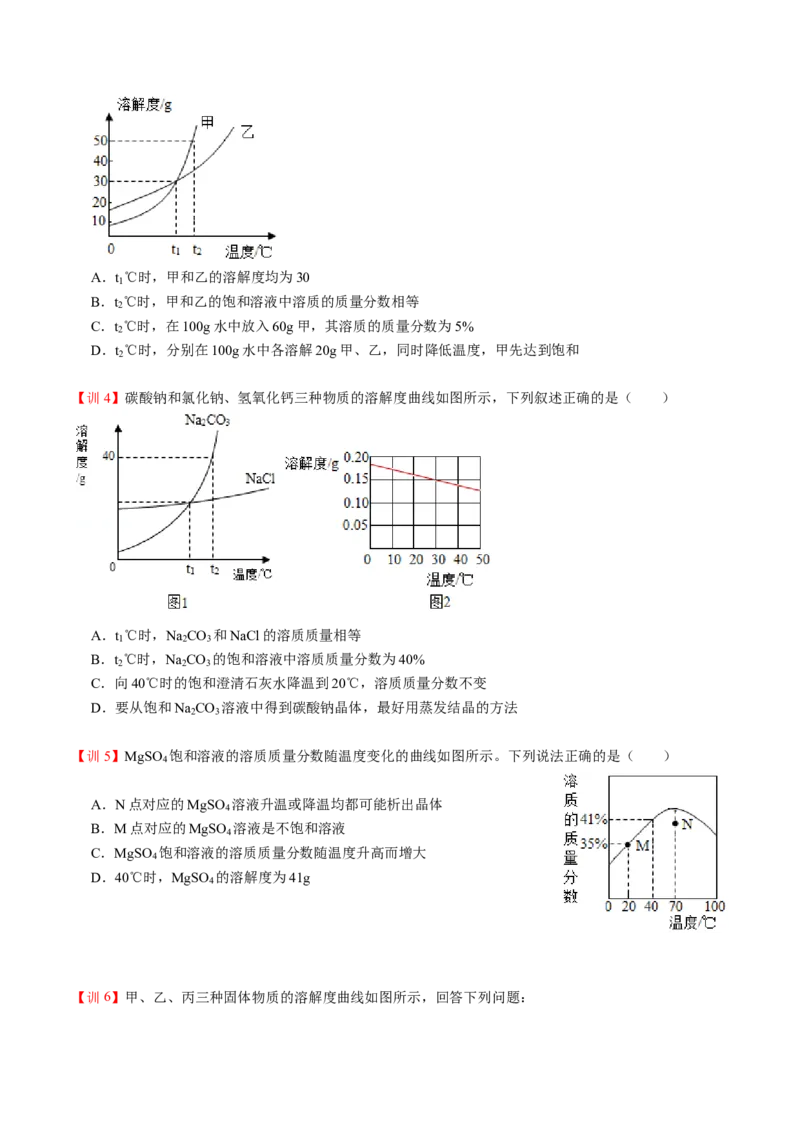
【例1】(2018•广东)如图为两物质的溶解度曲线。请回答:
(1)在50℃时,把210g NaCr O 饱和溶液降温到10℃,析出NaCr O g(假设不含结晶水)。
2 2 7 2 2 7
【例2】现有t℃的KNO 和KCl的两种饱和溶液,不考虑水的蒸发,下列关系正确的是( )
2 3
A.两种溶液中溶质的质量相等
B.分别降温到t℃,析出KNO 的质量大于析出KCl的质量
1 3
C.分别升温至t℃,所得溶液中溶质的质量分数相等
3
D.保持温度不变,分别加入等质量的水,所得溶液中溶质的质量分数相等。
【例3】KNO、NaNO 、NaCl三种物质的溶解度曲线如下图所示,下列说法正确的是( )
3 3
A.KNO 的溶解度比NaCl大
3
B.将KNO 饱和溶液降温,溶液中KNO 的质量分数不变
3 3
C.KNO 饱和溶液中含少量NaCl,可通过降温结晶的方法提纯
3
D.100g 40℃ NaNO 的饱和溶液降温至0℃,析出NaNO 固体
3 3
31g
【例4】如图为A、B、C三种物质的溶解度曲线,据图回答:(1)t ℃时,A、B、C三种物质的溶解度由大到小的顺序___________。
2
(2)20℃时,将50g A物质放入100g水中,充分搅拌,所得溶液的溶质质量分数是____________。(只列计
算式)
(3)将t℃时三种物质等质量的饱和溶液分别降温到0℃时,析出溶质最多的是_____。
2
(4)若将t℃时A、C两种物质的饱和溶液分别降温到t℃,则t℃时两种溶液中溶质的质量分数为
2 1 1
A________C(选填“>”“<”或“=”)
(5)若A的饱和溶液中混有少量B,提纯A的方法是_________。
专项训练
【训1】现有t ℃时的溶液Ⅰ、Ⅱ各100 g,溶液Ⅰ中含物质甲50 g,溶液Ⅱ是物质乙的饱和溶液。物质甲
2
乙(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
A.t ℃时,溶液Ⅰ是甲的饱和溶液
2
B.t ℃时,溶液Ⅰ中甲的质量分数为50%
2
C.t ℃时,溶液Ⅱ中含乙37 g
2
D.从t ℃降温至t ℃时,乙不会从溶液Ⅱ中析出
2 1
【训2】如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.a ℃时,甲、乙的饱和溶液升温至a ℃时,均有固体析出
1 2
C.a ℃时,M点对应的甲溶液不饱和
2
D.a ℃时,乙饱和溶液的质量分数为20%
2
【训3】甲、乙两物质的溶解度曲线如图,下列叙述中正确的是( )A.t ℃时,甲和乙的溶解度均为30
1
B.t ℃时,甲和乙的饱和溶液中溶质的质量分数相等
2
C.t ℃时,在100g水中放入60g甲,其溶质的质量分数为5%
2
D.t ℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
2
【训4】碳酸钠和氯化钠、氢氧化钙三种物质的溶解度曲线如图所示,下列叙述正确的是( )
A.t ℃时,Na CO 和NaCl的溶质质量相等
1 2 3
B.t ℃时,Na CO 的饱和溶液中溶质质量分数为40%
2 2 3
C.向40℃时的饱和澄清石灰水降温到20℃,溶质质量分数不变
D.要从饱和Na CO 溶液中得到碳酸钠晶体,最好用蒸发结晶的方法
2 3
【训5】MgSO 饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是( )
4
A.N点对应的MgSO 溶液升温或降温均都可能析出晶体
4
B.M点对应的MgSO 溶液是不饱和溶液
4
C.MgSO 饱和溶液的溶质质量分数随温度升高而增大
4
D.40℃时,MgSO 的溶解度为41g
4
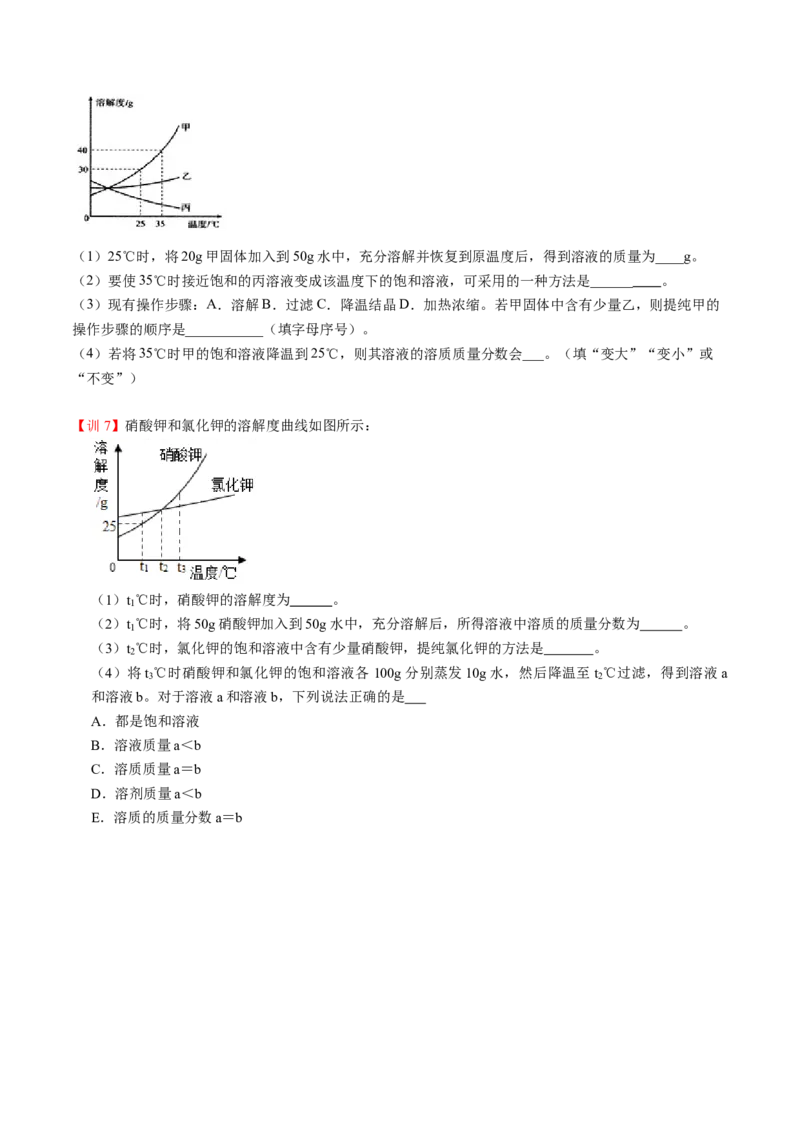
【训6】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:(1)25℃时,将20g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为____g。
(2)要使35℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是______ 。
(3)现有操作步骤:A.溶解B.过滤C.降温结晶D.加热浓缩。若甲固体中含有少量乙,则提纯甲的
操作步骤的顺序是___________(填字母序号)。
(4)若将35℃时甲的饱和溶液降温到25℃,则其溶液的溶质质量分数会___。(填“变大”“变小”或
“不变”)
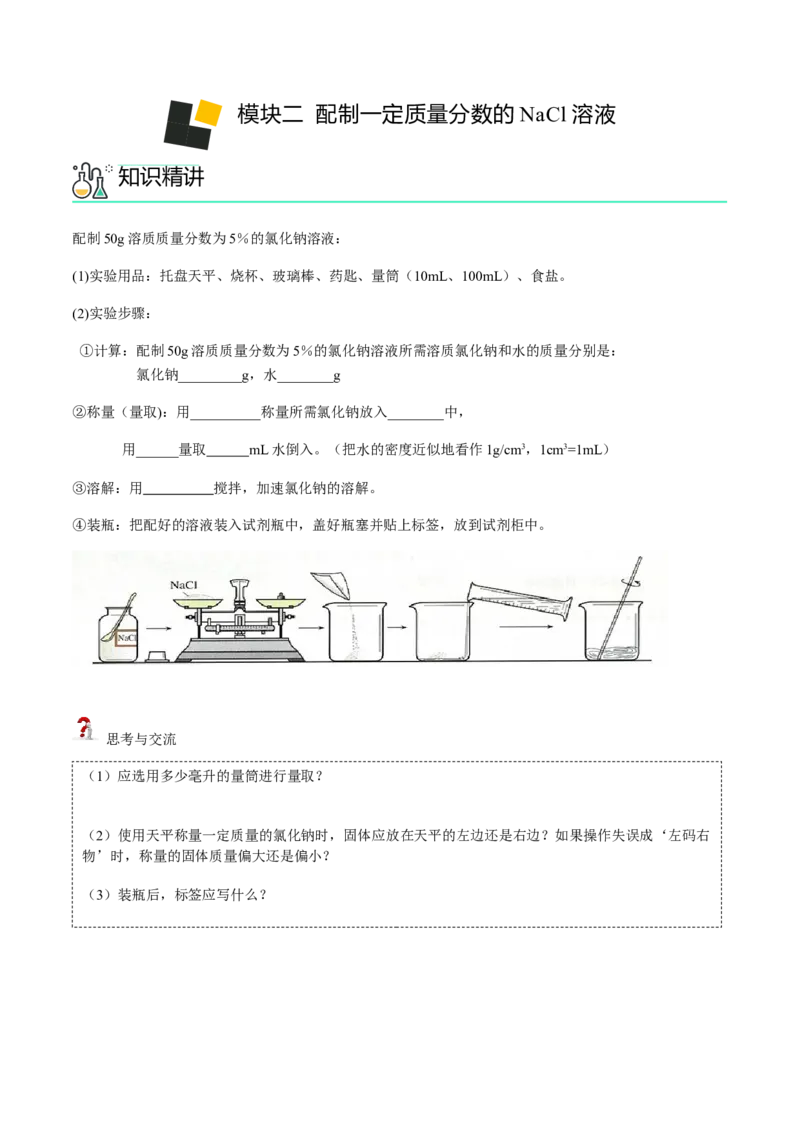
【训7】硝酸钾和氯化钾的溶解度曲线如图所示:
(1)t ℃时,硝酸钾的溶解度为 。
1
(2)t ℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为 。
1
(3)t ℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是 。
2
(4)将t ℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t ℃过滤,得到溶液a
3 2
和溶液b。对于溶液a和溶液b,下列说法正确的是
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a=b模块二 配制一定质量分数的 NaCl 溶液
知识精讲
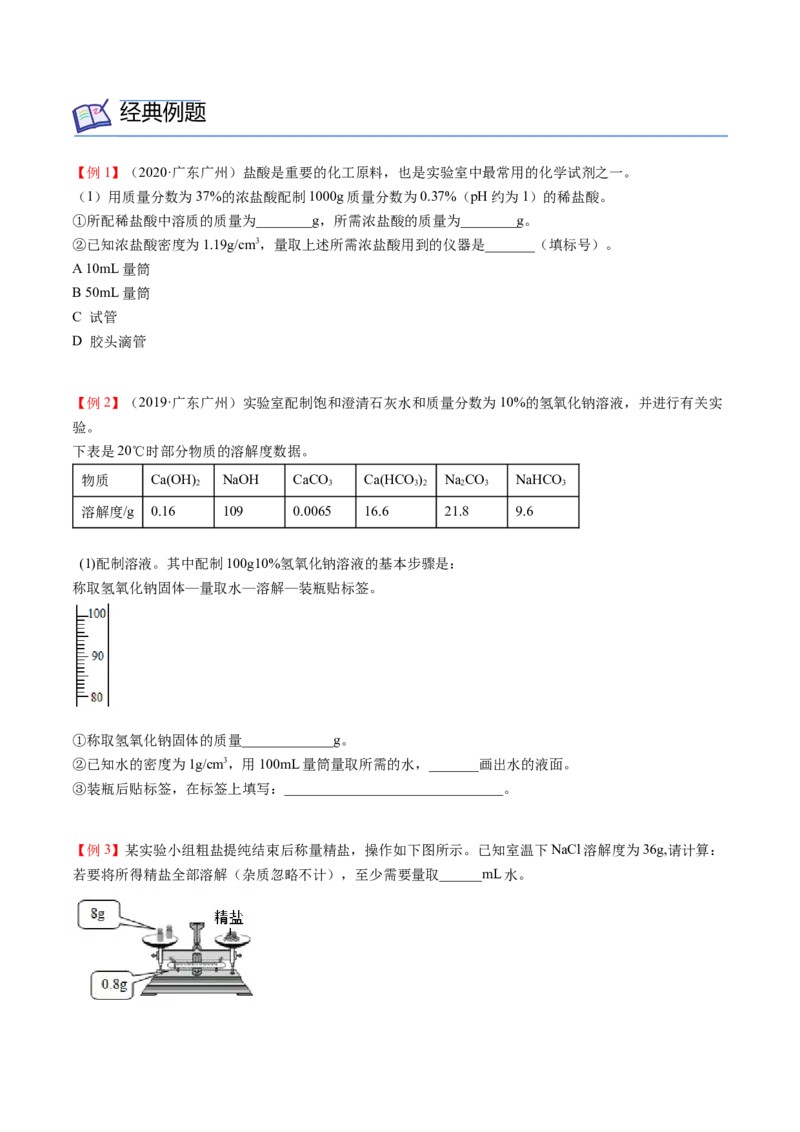
配制50g溶质质量分数为5%的氯化钠溶液:
(1)实验用品:托盘天平、烧杯、玻璃棒、药匙、量筒(10mL、100mL)、食盐。
(2)实验步骤:
①计算:配制50g溶质质量分数为5%的氯化钠溶液所需溶质氯化钠和水的质量分别是:
氯化钠_________g,水________g
②称量(量取):用__________称量所需氯化钠放入________中,
用______量取 mL水倒入。(把水的密度近似地看作1g/cm3,1cm3=1mL)
③溶解:用 搅拌,加速氯化钠的溶解。
④装瓶:把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签,放到试剂柜中。
思考与交流
(1)应选用多少毫升的量筒进行量取?
(2)使用天平称量一定质量的氯化钠时,固体应放在天平的左边还是右边?如果操作失误成‘左码右
物’时,称量的固体质量偏大还是偏小?
(3)装瓶后,标签应写什么?经典例题
【例1】(2020·广东广州)盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一。
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为________g,所需浓盐酸的质量为________g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是_______(填标号)。
A 10mL量筒
B 50mL量筒
C 试管
D 胶头滴管
【例2】(2019·广东广州)实验室配制饱和澄清石灰水和质量分数为10%的氢氧化钠溶液,并进行有关实
验。
下表是20℃时部分物质的溶解度数据。
物质 Ca(OH) NaOH CaCO Ca(HCO ) NaCO NaHCO
2 3 3 2 2 3 3
溶解度/g 0.16 109 0.0065 16.6 21.8 9.6
(1)配制溶液。其中配制100g10%氢氧化钠溶液的基本步骤是:
称取氢氧化钠固体—量取水—溶解—装瓶贴标签。
①称取氢氧化钠固体的质量_____________g。
②已知水的密度为1g/cm3,用100mL量筒量取所需的水,_______画出水的液面。
③装瓶后贴标签,在标签上填写:_______________________________。
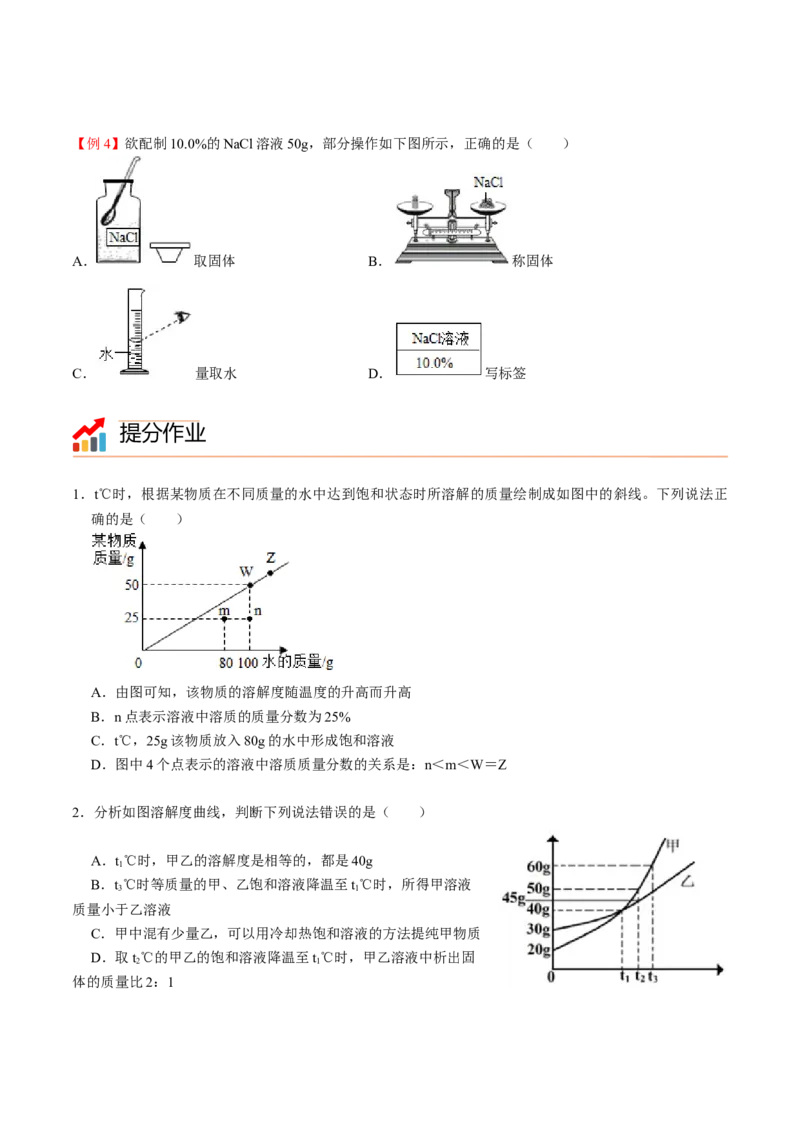
【例3】某实验小组粗盐提纯结束后称量精盐,操作如下图所示。已知室温下NaCl溶解度为36g,请计算:
若要将所得精盐全部溶解(杂质忽略不计),至少需要量取______mL水。【例4】欲配制10.0%的NaCl溶液50g,部分操作如下图所示,正确的是( )
A. 取固体 B. 称固体
C. 量取水 D. 写标签
提分作业
1.t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成如图中的斜线。下列说法正
确的是( )
A.由图可知,该物质的溶解度随温度的升高而升高
B.n点表示溶液中溶质的质量分数为25%
C.t℃,25g该物质放入80g的水中形成饱和溶液
D.图中4个点表示的溶液中溶质质量分数的关系是:n<m<W=Z
2.分析如图溶解度曲线,判断下列说法错误的是( )
A.t℃时,甲乙的溶解度是相等的,都是40g
1
B.t℃时等质量的甲、乙饱和溶液降温至t℃时,所得甲溶液
3 1
质量小于乙溶液
C.甲中混有少量乙,可以用冷却热饱和溶液的方法提纯甲物质
D.取t℃的甲乙的饱和溶液降温至t℃时,甲乙溶液中析出固
2 1
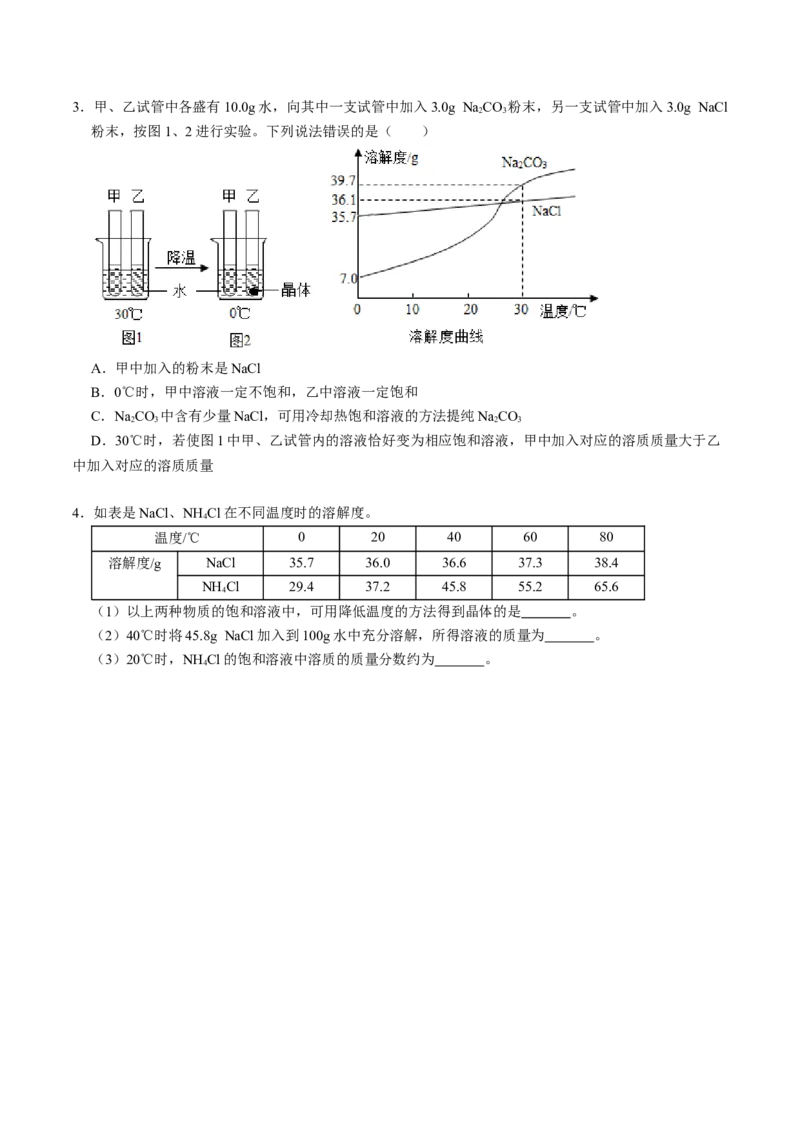
体的质量比2:13.甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0g NaCO 粉末,另一支试管中加入3.0g NaCl
2 3
粉末,按图1、2进行实验。下列说法错误的是( )
A.甲中加入的粉末是NaCl
B.0℃时,甲中溶液一定不饱和,乙中溶液一定饱和
C.NaCO 中含有少量NaCl,可用冷却热饱和溶液的方法提纯NaCO
2 3 2 3
D.30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙
中加入对应的溶质质量
4.如表是NaCl、NH Cl在不同温度时的溶解度。
4
温度/℃ 0 20 40 60 80
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4
NH Cl 29.4 37.2 45.8 55.2 65.6
4
(1)以上两种物质的饱和溶液中,可用降低温度的方法得到晶体的是 。
(2)40℃时将45.8g NaCl加入到100g水中充分溶解,所得溶液的质量为 。
(3)20℃时,NH Cl的饱和溶液中溶质的质量分数约为 。
4