文档内容
微信公众号:上海通优教案资料中心
化学部分
相对原子质量:H-1 C-12 O-16 Na-23 Si-28 Cl-35.5
三、诗词与化学(8分)
中华诗词,不仅是文学的瑰宝,更是古人观察自然、记录生活的智慧结晶。许多流传千古的诗句,蕴
含着朴素而深刻的化学道理,化学为诗词赋予了科学的内涵。
1. 刘禹锡《浪淘沙》“千淘万漉虽辛苦,吹尽狂沙始到金。”“淘金” 利用金和沙子的密度不同进行分离,该
过程属于____。
A. 物理变化 B. 化学变化 C. 物理性质 D. 化学性质
2. 汉书记载 “高奴县有洧水,可燃。” 洧水中含有石油,石油属于____。
A. 单质 B. 化合物 C. 纯净物 D. 混合物
3. 王安石《梅花》“遥知不是雪,为有暗香来。” 从微观角度解释 “暗香来” 的原因是____。
A. 分子质量小 B. 分子在不断运动 C. 分子可以再分 D. 分子间存在间隙
4. 孟浩然《过故人庄》“故人具鸡黍,邀我至田家。” 诗句中 “鸡肉” 富含的营养素为____。
A. 蛋白质 B. 糖类 C. 矿物质 D. 维生素
5. 《本草经集注》记载 “强烧之,紫青烟起…… 云是真硝石也。”“硝石” 主要成分是 KNO₃,KNO₃不属
于____。
A. 氮肥 B. 钾肥 C. 磷肥 D. 复合肥
6.《三国志》记载 “扬汤止沸,不如去薪。”“薪” 指柴草等燃料,“去薪” 灭火的原理是________________。
7.《天工开物》记载 “煤饼烧石成灰。”“石” 主要成分是CaCO₃,“灰” 指CaO,“烧石成灰” 的另一种产物
是CO₂,而不是O₂。请解释原因____________________________________。
四、氧气从哪里来(11分)
在生产实践、日常生活以及科学研究领域,氧气有着重要的用途。不同的需求场景,获取氧气的方式
也不同。
8. 工业上通过分离液态空气获得氧气和氮气,依据的原理是____。
A. 质量不同 B. 熔点不同 C. 沸点不同 D. 颜色不同
9. 实验室用高锰酸钾制取氧气。
(1)化学方程式书写正确的是____。
A. 2KMnO =K MnO +MnO +O ↑ B. KMnO
MnO2
K MnO + O ↑
4 2 4 2 2 4 2 4 2
△ △
C. 2KMnO K MnO +MnO +O D. 2KMnO K MnO +MnO +O ↑
4 2 4 2 2 4 2 4 2 2
第 1 页 共 5 页微信公众号:上海通优教案资料中心
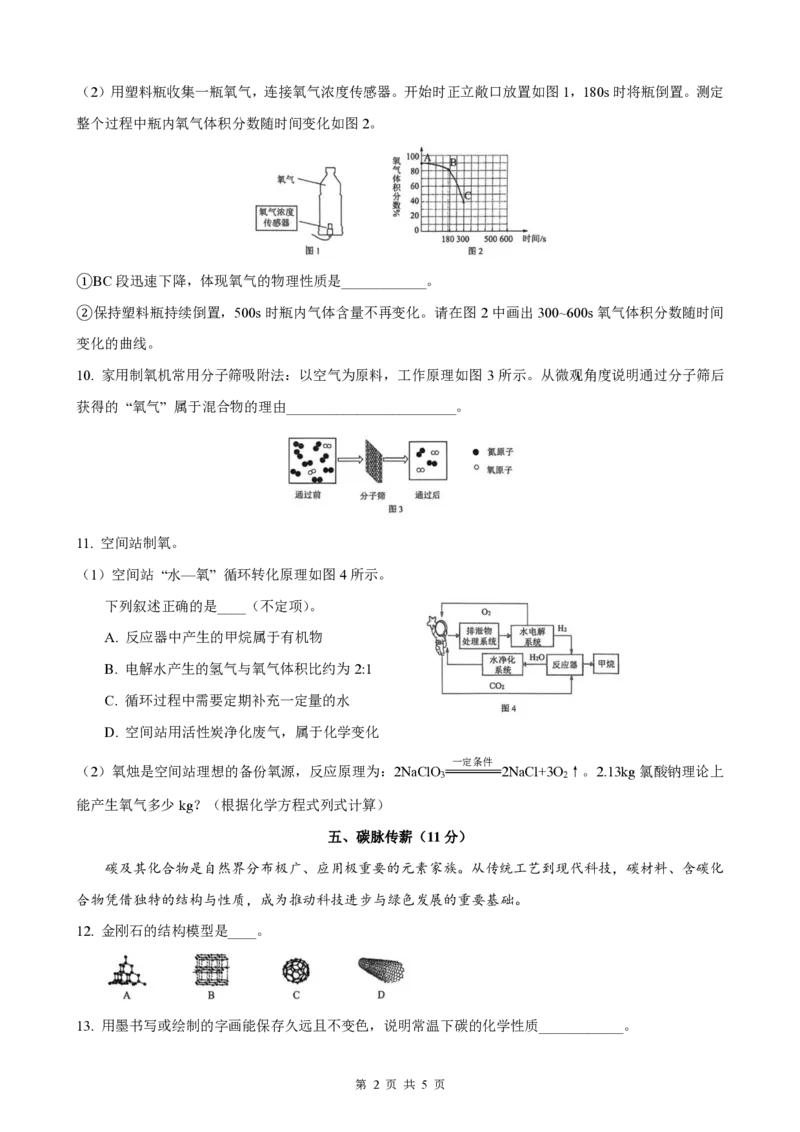
(2)用塑料瓶收集一瓶氧气,连接氧气浓度传感器。开始时正立敞口放置如图1,180s时将瓶倒置。测定
整个过程中瓶内氧气体积分数随时间变化如图2。
①BC段迅速下降,体现氧气的物理性质是____________。
②保持塑料瓶持续倒置,500s时瓶内气体含量不再变化。请在图2中画出300~600s氧气体积分数随时间
变化的曲线。
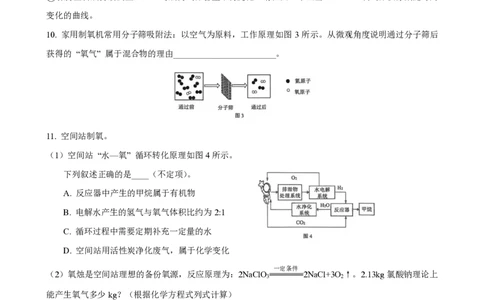
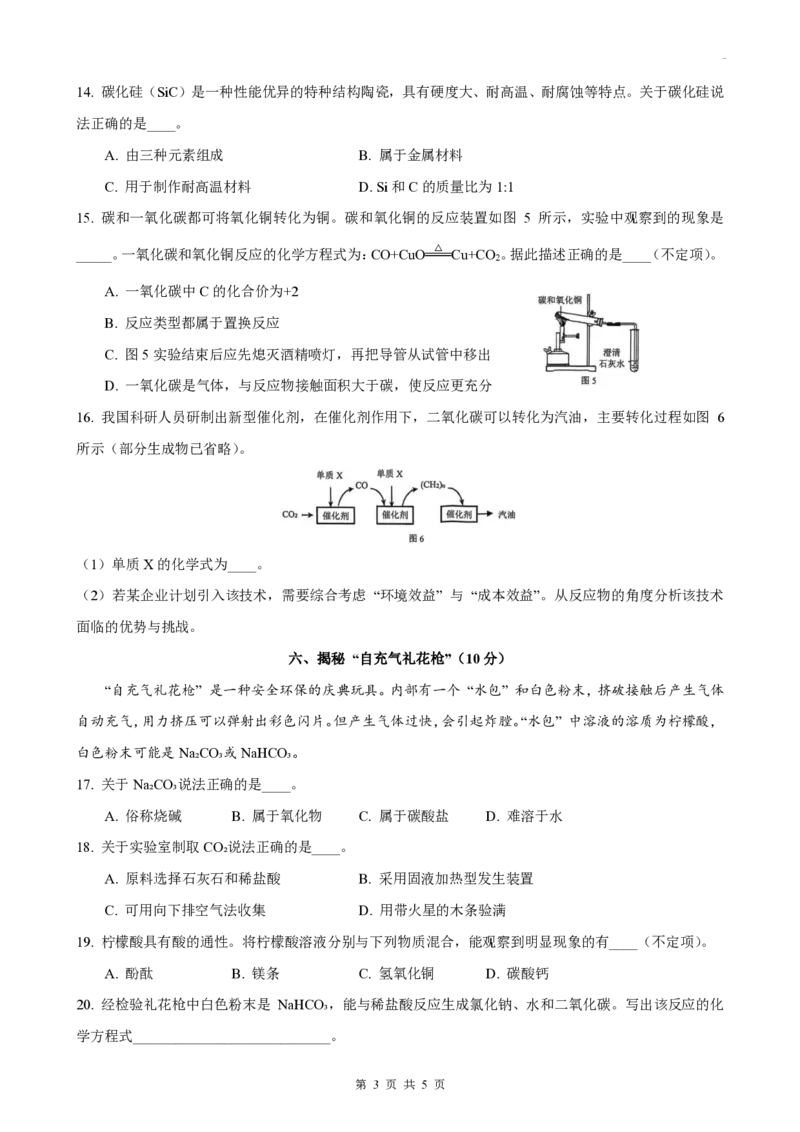
10. 家用制氧机常用分子筛吸附法:以空气为原料,工作原理如图 3 所示。从微观角度说明通过分子筛后
获得的 “氧气” 属于混合物的理由________________________。
11. 空间站制氧。
(1)空间站 “水—氧” 循环转化原理如图4所示。
下列叙述正确的是____(不定项)。
A. 反应器中产生的甲烷属于有机物
B. 电解水产生的氢气与氧气体积比约为2:1
C. 循环过程中需要定期补充一定量的水
D. 空间站用活性炭净化废气,属于化学变化
一定条件
(2)氧烛是空间站理想的备份氧源,反应原理为:2NaClO 2NaCl+3O ↑。2.13kg氯酸钠理论上
3 2
能产生氧气多少kg?(根据化学方程式列式计算)
五、碳脉传薪(11分)
碳及其化合物是自然界分布极广、应用极重要的元素家族。从传统工艺到现代科技,碳材料、含碳化
合物凭借独特的结构与性质,成为推动科技进步与绿色发展的重要基础。
12. 金刚石的结构模型是____。
13. 用墨书写或绘制的字画能保存久远且不变色,说明常温下碳的化学性质____________。
第 2 页 共 5 页微信公众号:上海通优教案资料中心
14. 碳化硅(SiC)是一种性能优异的特种结构陶瓷,具有硬度大、耐高温、耐腐蚀等特点。关于碳化硅说
法正确的是____。
A. 由三种元素组成 B. 属于金属材料
C. 用于制作耐高温材料 D. Si和C的质量比为1:1
15. 碳和一氧化碳都可将氧化铜转化为铜。碳和氧化铜的反应装置如图 5 所示,实验中观察到的现象是
△
_____。一氧化碳和氧化铜反应的化学方程式为:CO+CuO Cu+CO 。据此描述正确的是____(不定项)。
2
A. 一氧化碳中C的化合价为+2
B. 反应类型都属于置换反应
C. 图5实验结束后应先熄灭酒精喷灯,再把导管从试管中移出
D. 一氧化碳是气体,与反应物接触面积大于碳,使反应更充分
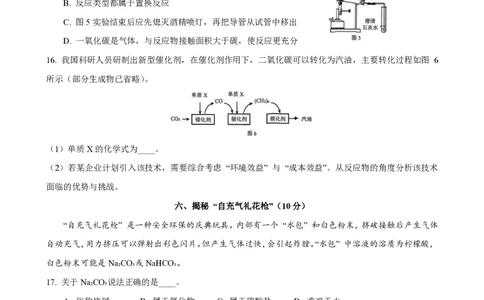
16. 我国科研人员研制出新型催化剂,在催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图 6
所示(部分生成物已省略)。
(1)单质X的化学式为____。
(2)若某企业计划引入该技术,需要综合考虑 “环境效益” 与 “成本效益”。从反应物的角度分析该技术
面临的优势与挑战。
六、揭秘 “自充气礼花枪”(10分)
“自充气礼花枪” 是一种安全环保的庆典玩具。内部有一个 “水包” 和白色粉末,挤破接触后产生气体
自动充气,用力挤压可以弹射出彩色闪片。但产生气体过快,会引起炸膛。“水包” 中溶液的溶质为柠檬酸,
白色粉末可能是Na₂CO₃或NaHCO₃。
17. 关于Na₂CO₃说法正确的是____。
A. 俗称烧碱 B. 属于氧化物 C. 属于碳酸盐 D. 难溶于水
18. 关于实验室制取CO₂说法正确的是____。
A. 原料选择石灰石和稀盐酸 B. 采用固液加热型发生装置
C. 可用向下排空气法收集 D. 用带火星的木条验满
19. 柠檬酸具有酸的通性。将柠檬酸溶液分别与下列物质混合,能观察到明显现象的有____(不定项)。
A. 酚酞 B. 镁条 C. 氢氧化铜 D. 碳酸钙
20. 经检验礼花枪中白色粉末是 NaHCO₃,能与稀盐酸反应生成氯化钠、水和二氧化碳。写出该反应的化
学方程式____________________________。
第 3 页 共 5 页微信公众号:上海通优教案资料中心
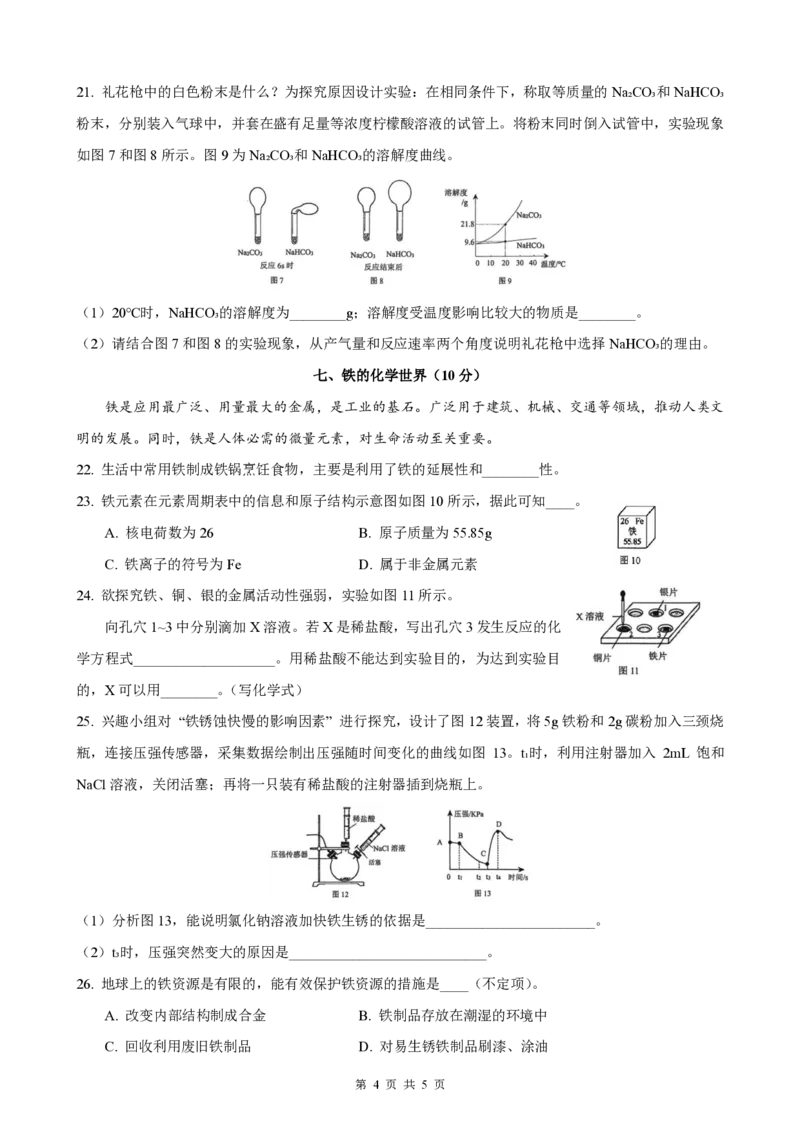
21. 礼花枪中的白色粉末是什么?为探究原因设计实验:在相同条件下,称取等质量的Na₂CO₃和NaHCO₃
粉末,分别装入气球中,并套在盛有足量等浓度柠檬酸溶液的试管上。将粉末同时倒入试管中,实验现象
如图7和图8所示。图9为Na₂CO₃和NaHCO₃的溶解度曲线。
(1)20℃时,NaHCO₃的溶解度为________g;溶解度受温度影响比较大的物质是________。
(2)请结合图7和图8的实验现象,从产气量和反应速率两个角度说明礼花枪中选择NaHCO₃的理由。
七、铁的化学世界(10分)
铁是应用最广泛、用量最大的金属,是工业的基石。广泛用于建筑、机械、交通等领域,推动人类文
明的发展。同时,铁是人体必需的微量元素,对生命活动至关重要。
22. 生活中常用铁制成铁锅烹饪食物,主要是利用了铁的延展性和________性。
23. 铁元素在元素周期表中的信息和原子结构示意图如图10所示,据此可知____。
A. 核电荷数为26 B. 原子质量为55.85g
C. 铁离子的符号为Fe D. 属于非金属元素
24. 欲探究铁、铜、银的金属活动性强弱,实验如图11所示。
向孔穴1~3中分别滴加X溶液。若X是稀盐酸,写出孔穴3发生反应的化
学方程式____________________。用稀盐酸不能达到实验目的,为达到实验目
的,X可以用________。(写化学式)
25. 兴趣小组对 “铁锈蚀快慢的影响因素” 进行探究,设计了图12装置,将5g铁粉和2g碳粉加入三颈烧
瓶,连接压强传感器,采集数据绘制出压强随时间变化的曲线如图 13。t₁时,利用注射器加入 2mL 饱和
NaCl溶液,关闭活塞;再将一只装有稀盐酸的注射器插到烧瓶上。
(1)分析图13,能说明氯化钠溶液加快铁生锈的依据是________________________。
(2)t₃时,压强突然变大的原因是____________________________。
26. 地球上的铁资源是有限的,能有效保护铁资源的措施是____(不定项)。
A. 改变内部结构制成合金 B. 铁制品存放在潮湿的环境中
C. 回收利用废旧铁制品 D. 对易生锈铁制品刷漆、涂油
第 4 页 共 5 页微信公众号:上海通优教案资料中心
参考答案
三、
1. A 2. D 3. B 4. A 5. C
6. 清除可燃物
7. 根据质量守恒定律,化学反应前后元素种类不变,CaCO 由钙、碳、氧三种元素组成,分解生成CaO(含
3
钙、氧元素)和另一种产物,该产物必然含有碳、氧元素,因此是CO ,而非只含氧元素的O
2 2
四、
8. C
9.(1)D
(2)①氧气密度比空气大 ②图略
10. 通过分子筛后的气体含有氮气和氧气两种分子
11.(1)ABC (2)0.96 kg
五、
12. A
13. 稳定(不活泼)
14. C
15. 黑色固体变红,澄清石灰水变浑浊;AD
16.(1)H₂
(2)优势:以CO 为原料,可减少碳排放,缓解温室效应;
2
挑战:反应物CO 性质稳定,反应能耗高;H 的制取、储运成本较高
2 2
六、
17. C 18. A 19. BCD
20. NaHCO₃+HCl=NaCl+H₂O+CO₂↑
21.(1)9.6;Na₂CO₃ (2)NaHCO₃反应速率更快、产气量更多
七、
22. 导热
23. A
24. Fe+2HCl=FeCl₂+H₂↑;CuSO₄(合理即可)
25.(1)加入NaCl溶液后压强迅速减小 (2)稀盐酸与铁反应生成氢气,压强骤增
26. ACD
第 5 页 共 5 页