文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V: jiajiao6767 )
上海市延安中学 2022 学年第一学期期末考试
高二年级 化学试卷(等级)
(考试时间:60 分钟 满分 100 分)
相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5
一、单项选择题(每小题只有 1 个选项符合题意,每小题 2 分)
1. 等物质的量的下列物质中,内能最大的是
A.水蒸气 B.液态水 C.冰 D.冰水混合物
2. 下列反应属于吸热反应的是
A.二氧化碳与灼热的炭反应生成一氧化碳 B.葡萄糖在人体内氧化分解
C.生石灰制熟石灰 D.氢气和氯气合成氯化氢
3. 下列说法中正确的是
A.自发反应速率一定快 B.非自发反应一定不可能发生
C.自发反应实际可能没有发生 D.自发反应的限度一定大
4. 下列反应或过程属于熵减的是
A.氯化钠从溶液中结晶析出 B.胆矾晶体溶于水
C.固态碘升华 D.碳酸钙分解
5. 下列现象与氧化还原反应无关的是
A.钢铁生锈 B.食物变质 C.溶洞形成 D.氯气消毒
6. 电解 CuSO 4 溶液时,所用的阳极为铜,而阴极为碳棒,则实验过程中会出现的情况是
A.溶液中Cu2+的浓度保持不变 B.溶液中H+的浓度上升
C.在阳极上析出O D.在阴极上析出H
2 2
7. 在醋酸溶液中,CH 3 COOH 电离达到平衡的标志是
A.溶液显电中性 B.氢离子浓度恒定不变
C.c(H+)=c(CH COO-) D.溶液中检测不出CH COOH 分子存在
3 3
8. 某溶液pH=4,并含有较多 Fe2+、Cu2+,那么溶液中不可能含有的负离子是
A.Cl- B.SO 2- C.NO - D.Br-
4 3
9. 下列说法错误的是
A.当碰撞的分子具有足够的能量适当的取向时,才能发生化学反应
B.发生有效碰撞的分子一定是活化分子
C. 活化分子间的碰撞一定是有效碰撞
D. 活化分子间每次碰撞不一定发生化学反应
10. 已知 298 K 时,Mg(OH) 2 的溶度积常数 K sp =5.6×10-12,取适量的 MgCl 2 溶液,加入一定量的烧碱溶
液达到沉淀溶解平衡,测得 pH=13.0,则下列说法不正确的是
.
A.所得溶液中的 c(H+)=1.0×10-13 mol·L -1
B. 所得溶液中由水电离产生的 c(H+)=10-13 mol·L -1
第 1 页 共 4 页
学学科科网网((北北京京))股股份份有有限限公公司司上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V: jiajiao6767 )
C. 所加的烧碱溶液 pH=13.0
D.所得溶液中的 c(Mg2+)=5.6×10-10 mol·L -1
二、综合题(共 13 分)
11.(1)正交硫和单斜硫是硫常见的两种单质,它们互为 。
已知:S (正交) =S (单斜) ∆H =2.64 kJ·mol-1。正交硫与单斜硫相比,相对比较稳定的是
8 8
(2)通常状况下 4g 硫粉完全燃烧放出 37 kJ 的热量,写出反应的热化学方程式 。
12. 同温同浓度的 Na 2 SO 3 、(NH 4 ) 2 SO 3 、NaHSO 3 三种溶液,c(SO 2-) 3 最大的是 ;经测定
NaHSO
3
溶液中 c(H
2
SO
3
)<c(SO 2
3
-),则NaHSO
3
溶液呈 (填“酸”或“碱”)性;
13. 等物质的量浓度的下列 3 种溶液:①Ba(OH) 2 ②KHSO 3 ③KHCO 3 ,溶液中水的电离程度由大到小排列
顺序为 。
三、综合题(共 13 分)
化学电源在生产生活中有广泛用途。
14. 用右图所示装置研究原电池原理。下列叙述错误的是( ) Zn Cu
A. Cu 棒和Zn 棒用导线连接时,铜片上有气泡逸出 稀硫酸
B. Cu 棒和Zn 棒不连接时,锌片上有气泡逸出
C. 无论Cu 棒和Zn 棒是否用导线连接,装置中所涉及的总反应都相同
D. 无论Cu 棒和 Zn 棒是否用导线连接,装置都是把化学能转化为电能
15.(1)已知甲醇的化学式为 CH OH,甲醇的燃烧热 ΔH=-726.5 kJ·mol -1,在直接以甲醇为燃料的电池
3
中,电解质溶液为酸性,正极的电极反应式为 。
(2)理想状态下,该燃料电池消耗 1 mol 甲醇所能产生的最大电能为 702.1 kJ,则该燃料电池的理论
效率为 (用小数表示,保留 3 位小数。燃料电池的理论效率是指电池所产生的最大电能与
燃料电池反应所能释放的全部能量之比)。
16. 氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完
全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。
氢能具有的优点包括( )
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
17. 关于铅蓄电池的说法正确的是( )
A.在放电时,正极发生的反应是 Pb+SO42--2e- = PbSO4
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO +2e- = Pb+SO 2-
4 4
第 2 页 共 4 页
学学科科网网((北北京京))股股份份有有限限公公司司上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V: jiajiao6767 )
18. 关于锂电池的叙述正确的是( )
A.电能转化为化学能 B.电容量大,质量轻
C.不可循环充电使用 D.废旧锂电池是干垃圾
四、综合题(共 20 分)
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子
交换膜法电解食盐水的示意图,图中的离子交换膜只允许正离子通过。
○ +
Cl2 H2
○-
19.(1)写出电解饱和食盐水的离子方程式
c d
(2)写出阴极的电极反应式
Cl― H+
20. 离子交换膜的作用为 、 Na+ Na+
。
Cl―
OH―
21. 精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中
离子交换膜
位置流出。(选填“a”、“b”、“c”或“d”) a b
氯气和烧碱溶液反应可以制得“84”消毒液,可杀灭新冠病毒。
已知:H
2
SO
3
K
i1
=1.54×10 -2 K
i2
=1.02×10 -7 HClO K
i
=2.95×10 -8
H
2
CO
3
K
i1
=4.3×10 -7 K
i2
=5.6×10-11
22. 生活中不可将NaClO 与洁厕灵(含有盐酸)混合使用,是因为二者会反应生成( )
A.次氯酸 B.高氯酸 C.氯气 D.氧气
23. 室温下,0.1 mol·L-1 NaClO 溶液的 pH 0.1 mol·L-1 Na 2 SO 3 溶液的 pH。(选填“大于”、“小于”
或“等于”)
24. 浓度均为 0.1 mol·L-1 的 Na 2 SO 3 和Na 2 CO 3 的混合溶液中,SO 3 2–、CO 3 2–浓度从大到小的顺序为
。
五、综合题(共 17 分)
工业上常用氮气与氢气来合成氨气,温度控制在 500℃,采用铁催化剂,压强控制在 20~50 MPa
25.(1)该反应的化学方程式为 。
(2)它的平衡常数表达式为 。
26. 工业合成氨时,采用氮氢循环操作的主要目的是( )
A.加快反应速率 B.提高氨气的平衡浓度 C.降低氨气的沸点 D.提高N 和H 的利用率
2 2
27. 在一体积 10L 的密闭容器中充入了 280g N 2 、100g H 2 ,反应 10 分钟后,测得有 34 g NH 3 生成,则用
H 表示该反应的速率为 。
2
28. 下列判断可以作为该反应达到平衡的标志的是( )
A.单位时间内每消耗 1 摩尔氮气的同时消耗 3 摩尔氢气
B.混合气体的平均分子量不再发生变化
C.混合气体的密度保持不变
D.体系的温度不再变化
第 3 页 共 4 页
学学科科网网((北北京京))股股份份有有限限公公司司29. 氨气常用来生产化肥 NH 4 Cl,铵态氮肥不宜长期施用,请结合化学用语解释
。
30. 工业上常用氨气来制备硝酸,其中第 1 步是用氨气与纯氧在 Cr 2 O 3 的催化作用加热下制得 NO 和水。
请写出这个反应的化学方程式并配平 。该反应中,还原剂
是 。
六、综合题(共 17 分)
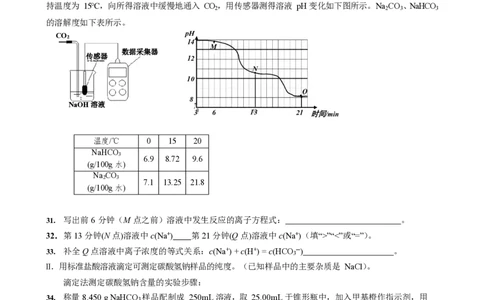
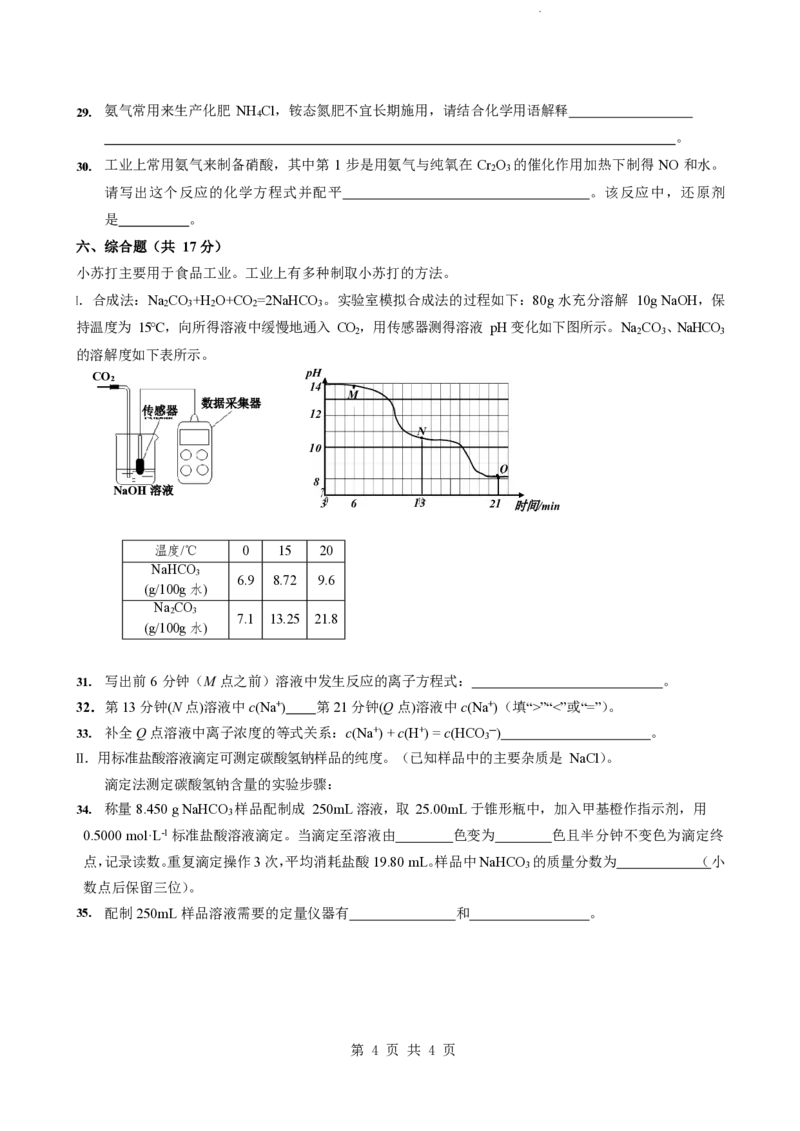
小苏打主要用于食品工业。工业上有多种制取小苏打的方法。
Ⅰ.合成法:Na CO +H O+CO =2NaHCO 。实验室模拟合成法的过程如下:80g 水充分溶解 10g NaOH,保
2 3 2 2 3
持温度为 15℃,向所得溶液中缓慢地通入 CO,用传感器测得溶液 pH 变化如下图所示。Na CO 、NaHCO
2 2 3 3
的溶解度如下表所示。
CO2 pH
14
M
传感器
数据采集器
12
N
●
10
Q
•
8 ●
NaOH 溶液
3 6 13 21 时间/min
温度/℃ 0 15 20
NaHCO
3
6.9 8.72 9.6
(g/100g 水)
Na CO
2 3
7.1 13.25 21.8
(g/100g 水)
31. 写出前 6 分钟(M 点之前)溶液中发生反应的离子方程式: 。
32.第 13 分钟(N 点)溶液中 c(Na+) 第 21 分钟(Q 点)溶液中 c(Na+)(填“>”“<”或“=”)。
33. 补全 Q 点溶液中离子浓度的等式关系:c(Na+) + c(H+) = c(HCO 3 ─) 。
Ⅱ.用标准盐酸溶液滴定可测定碳酸氢钠样品的纯度。(已知样品中的主要杂质是 NaCl)。
滴定法测定碳酸氢钠含量的实验步骤:
34. 称量 8.450 g NaHCO 3 样品配制成 250mL 溶液,取 25.00mL 于锥形瓶中,加入甲基橙作指示剂,用
0.5000 mol·L-1 标准盐酸溶液滴定。当滴定至溶液由 色变为 色且半分钟不变色为滴定终
点,记录读数。重复滴定操作 3 次,平均消耗盐酸 19.80 mL。样品中NaHCO 的质量分数为 (小
3
数点后保留三位)。
35. 配制 250mL 样品溶液需要的定量仪器有 和 。
第 4 页 共 4 页
学学科科网网((北北京京))股股份份有有限限公公司司