文档内容
大庆铁人中学2025级高一年级上学期期中考试
化 学
2025.11
注意事项:
1.答题前,考生先将自己的姓名、班级、考场号/座位号填写在答题卡上,如有条形码,认
真核对条形码上的姓名、准考证号,并将条形码粘贴在答题卡的指定位置上。
2.选择题答案使用2B铅笔填涂,如需改动,用橡皮擦干净后,再选涂其它答案的标号;非
选择题答案使用0.5毫米黑色中性(签字)笔或碳素笔书写,字体工整,笔迹清楚。
3.请按照题号在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效。
4.保持卷面及答题卡清洁,不折叠,不破损,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量 H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Cu 64 Ba 137
一、选择题: 本题共15小题,共45分。在每小题给出的四个选项中,只有一项符合题目要求。
1.中国传统文化博大精深,对人类文化贡献巨大。关于古籍文献下列有关说法错误的是
A.“雾失楼台,月迷津渡”,雾属于胶体,能产生丁达尔效应
B.《本草纲目拾遗》中有关氨水的记载:“贮以玻璃瓶,紧塞其口,勿使泄气……气甚辛烈,
触人脑”,这里的“气”——NH 是一种常见的非电解质
3
C.《本草经集注》中记载了区分硝石(KNO)和朴消(NaSO )的方法:“以火烧之,紫青烟起,
3 2 4
乃真硝石也”,该方法应用了焰色试验
D.“熬胆矾(CuSO ·5H O)铁釜,久之亦化为铜”,该过程发生了复分解反应
4 2
2.下列化学用语或图示表述正确的是
A.NaCl溶液中的水合离子:
B.NaHSO 在水中的电离:
4
C.Na+的离子结构示意图:
D.钠着火用二氧化碳灭火器灭火:
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 1 页 共 10 页3.用硫酸酸化的三氧化铬(CrO )遇酒精后,其颜色由红色变为蓝绿色,反应如下:
3
4CrO +3C HOH +6HSO = 2Cr (SO ) + 3CHCOOH + 9HO,用此反应现象可测得司机是否是
3 2 5 2 4 2 4 3 3 2
酒后驾车。此反应的氧化剂是
A.CrO B.HSO C.Cr (SO ) D.C HOH
3 2 4 2 4 3 2 5
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.14 g乙烯(C H)和丙烯(C H)的混合物中含有碳原子数目为N
2 4 3 6 A
B.4.6 g Na与0.1 L 1 mol/L盐酸充分反应,产生气体分子数目为0.05 N
A
C.常温下,500 mL 0.1 mol/L NaCl溶液中,含有的离子数为0.5 N
A
D.常温常压下,0.1 mol/L硫酸钾溶液中钾离子和硫酸根离子总数为0.3 N
A
5.类比和推理是化学研究的重要方法。下列类比或推理正确的是
A.液氯可以储存在钢瓶中,则氯水也能储存在钢瓶中
B.H 在O 中燃烧的火焰为淡蓝色,则H 在Cl 中燃烧的火焰也为淡蓝色
2 2 2 2
C.Cl−能使酸性高锰酸钾溶液褪色,则I−也能使酸性高锰钾溶液褪色
D.NaHCO 分别能与盐酸、NaOH溶液反应,则NaHSO 也能与盐酸、NaOH溶液反应
3 4
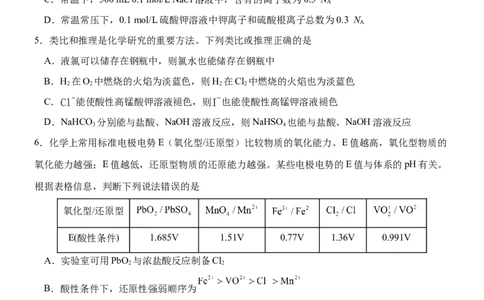
6.化学上常用标准电极电势E(氧化型/还原型)比较物质的氧化能力。E值越高,氧化型物质的
氧化能力越强;E值越低,还原型物质的还原能力越强。某些电极电势的E值与体系的pH有关。
根据表格信息,判断下列说法错误的是
氧化型/还原型
E(酸性条件) 1.685V 1.51V 0.77V 1.36V 0.991V
A.实验室可用PbO 与浓盐酸反应制备Cl
2 2
B.酸性条件下,还原性强弱顺序为
C.向HSO 酸化的含足量FeCl 的溶液中加入少量PbO ,可观察到黄绿色气体氯气产生
2 4 2 2
D.该反应能发生:
7.下列反应的离子方程式正确的是
A.向NaHSO 中滴加少量Ba(HCO ) 溶液:HCO−+H+ +SO2− + Ba2+=CO ↑+ HO +BaSO ↓
4 3 2 3 4 2 2 4
B.将CO 通入BaCl 溶液中:CO+ Ba2+ +H O=BaCO ↓+2H+
2 2 2 2 3
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 2 页 共 10 页C.同物质的量浓度同体积NH HSO 溶液与NaOH溶液混合:NH+ +OH−=NH·H O
4 4 4 3 2
D.Ca(HCO ) 溶液与过量的NaOH溶液混合:Ca2++2HCO−+2OH−=CaCO ↓+CO2− + 2HO
3 2 3 3 3 2
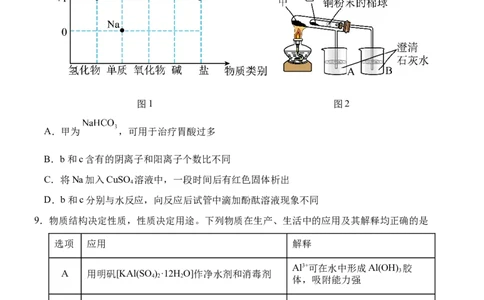
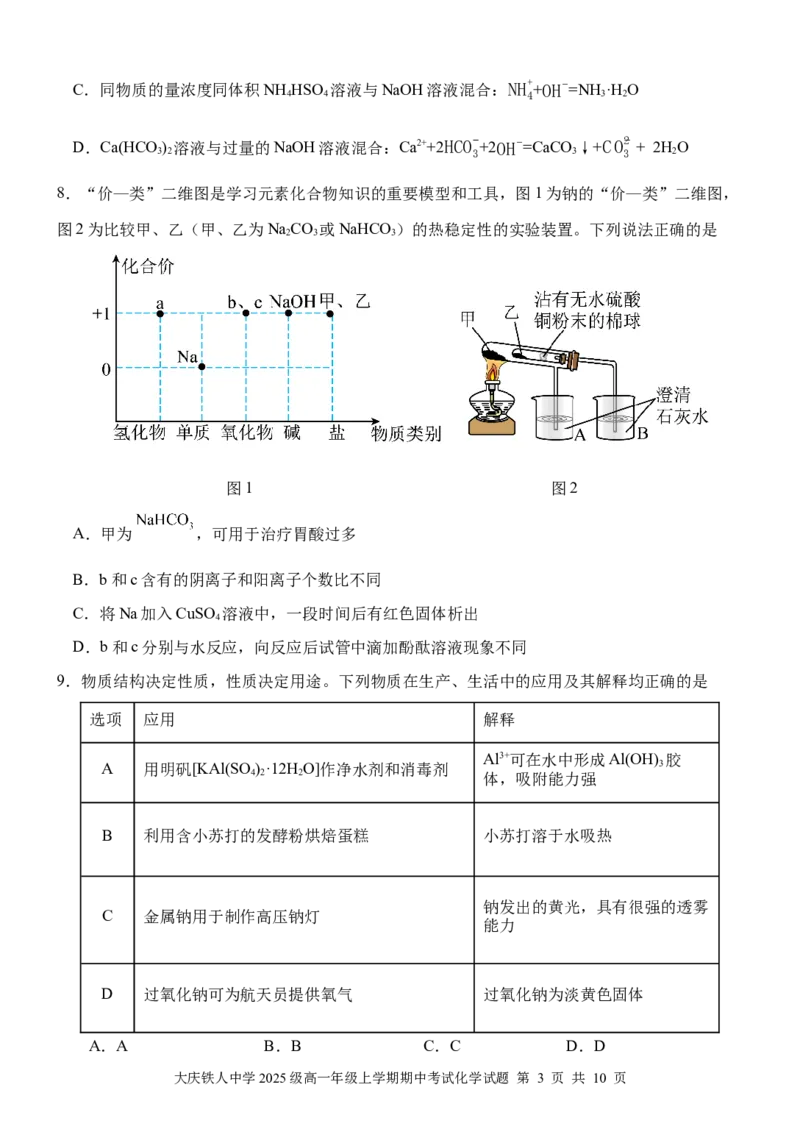
8.“价—类”二维图是学习元素化合物知识的重要模型和工具,图1为钠的“价—类”二维图,
图2为比较甲、乙(甲、乙为NaCO 或NaHCO )的热稳定性的实验装置。下列说法正确的是
2 3 3
图1 图2
A.甲为 ,可用于治疗胃酸过多
B.b和c含有的阴离子和阳离子个数比不同
C.将Na加入CuSO 溶液中,一段时间后有红色固体析出
4
D.b和c分别与水反应,向反应后试管中滴加酚酞溶液现象不同
9.物质结构决定性质,性质决定用途。下列物质在生产、生活中的应用及其解释均正确的是
选项 应用 解释
Al3+可在水中形成Al(OH) 胶
A 用明矾[KAl(SO)·12H O]作净水剂和消毒剂 3
4 2 2 体,吸附能力强
B 利用含小苏打的发酵粉烘焙蛋糕 小苏打溶于水吸热
钠发出的黄光,具有很强的透雾
C 金属钠用于制作高压钠灯
能力
D 过氧化钠可为航天员提供氧气 过氧化钠为淡黄色固体
A.A B.B C.C D.D
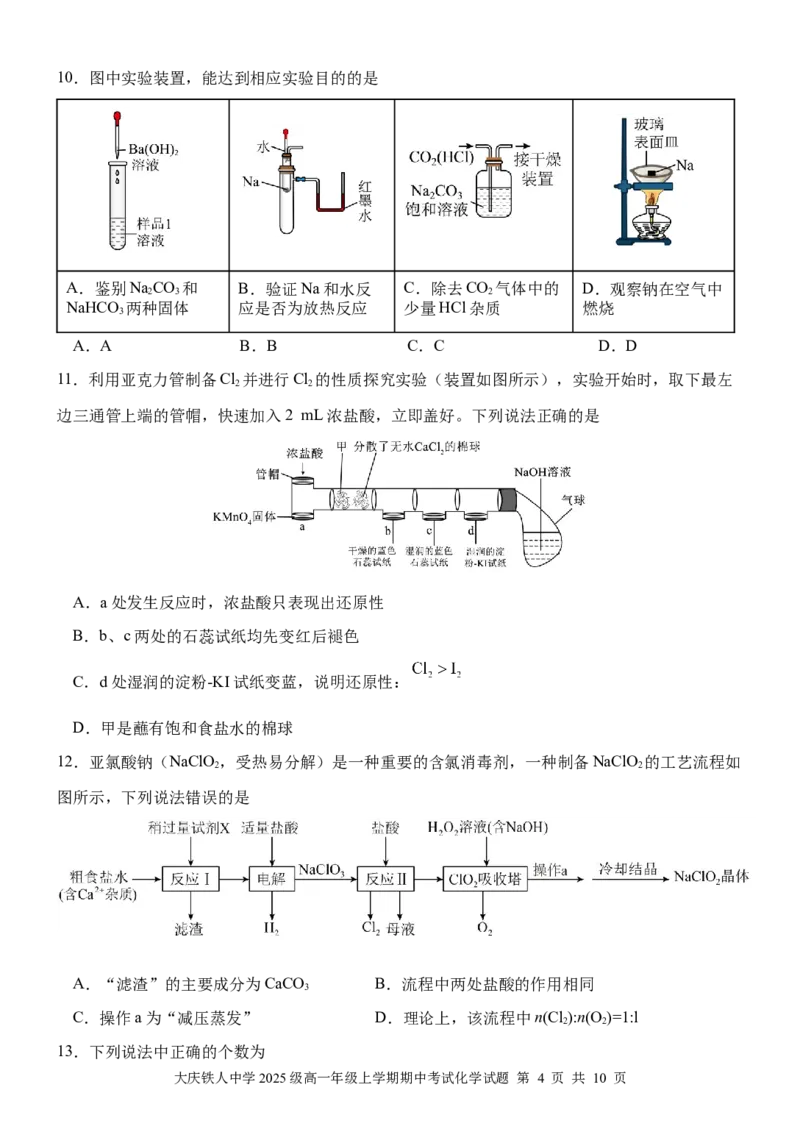
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 3 页 共 10 页10.图中实验装置,能达到相应实验目的的是
A.鉴别NaCO 和 B.验证Na和水反 C.除去CO 气体中的 D.观察钠在空气中
2 3 2
NaHCO 两种固体 应是否为放热反应 少量HCl杂质 燃烧
3
A.A B.B C.C D.D
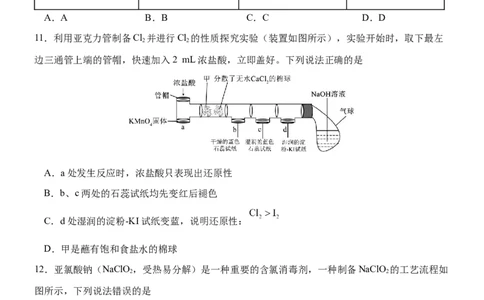
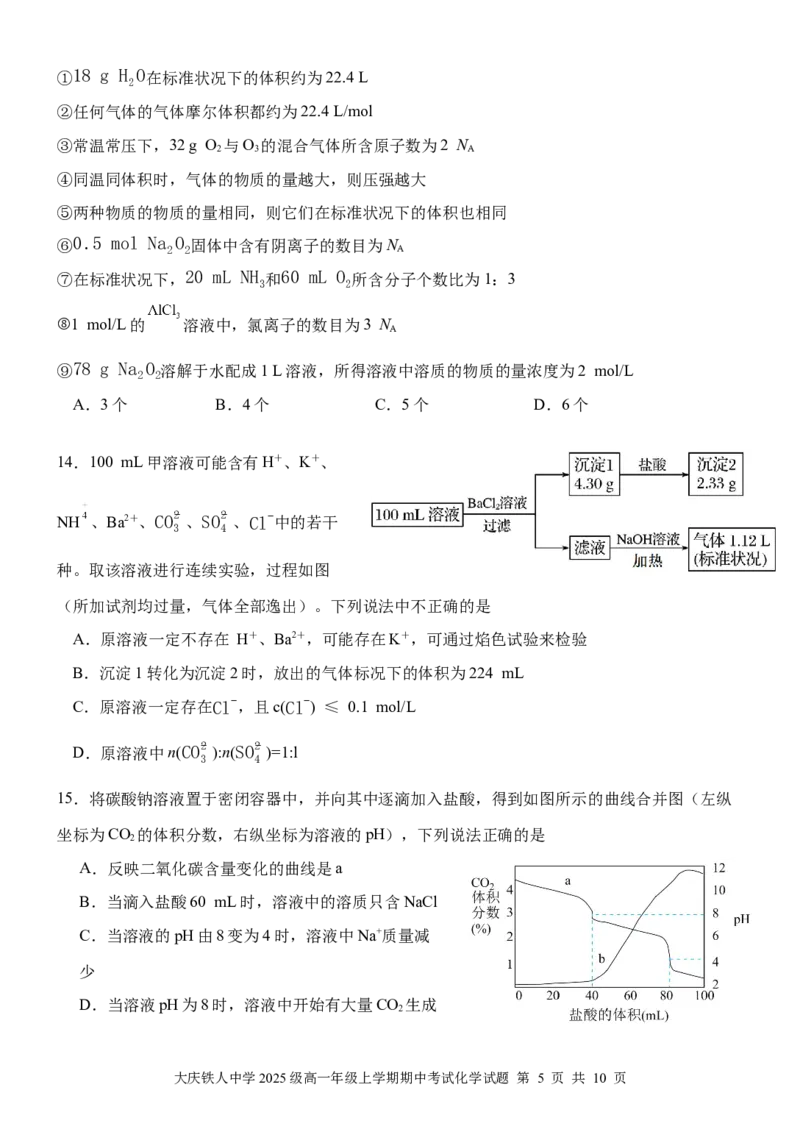
11.利用亚克力管制备Cl 并进行Cl 的性质探究实验(装置如图所示),实验开始时,取下最左
2 2
边三通管上端的管帽,快速加入2 mL浓盐酸,立即盖好。下列说法正确的是
A.a处发生反应时,浓盐酸只表现出还原性
B.b、c两处的石蕊试纸均先变红后褪色
C.d处湿润的淀粉-KI试纸变蓝,说明还原性:
D.甲是蘸有饱和食盐水的棉球
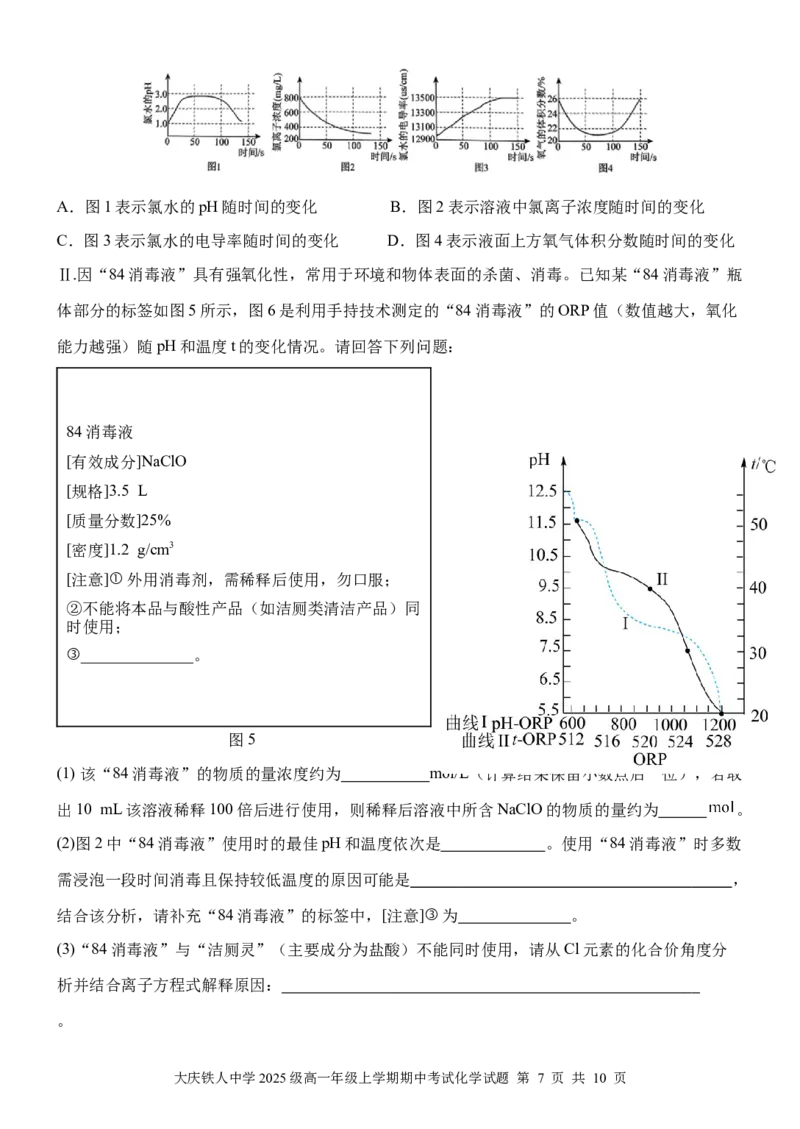
12.亚氯酸钠(NaClO,受热易分解)是一种重要的含氯消毒剂,一种制备NaClO 的工艺流程如
2 2
图所示,下列说法错误的是
A.“滤渣”的主要成分为CaCO B.流程中两处盐酸的作用相同
3
C.操作a为“减压蒸发” D.理论上,该流程中n(Cl ):n(O )=1:l
2 2
13.下列说法中正确的个数为
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 4 页 共 10 页①18 g H O在标准状况下的体积约为22.4 L
2
②任何气体的气体摩尔体积都约为22.4 L/mol
③常温常压下,32 g O 与O 的混合气体所含原子数为2 N
2 3 A
④同温同体积时,气体的物质的量越大,则压强越大
⑤两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑥0.5 mol Na O 固体中含有阴离子的数目为N
2 2 A
⑦在标准状况下,20 mL NH 和60 mL O 所含分子个数比为1:3
3 2
⑧1 mol/L的 溶液中,氯离子的数目为3 N
A
⑨78 g Na O 溶解于水配成1 L溶液,所得溶液中溶质的物质的量浓度为2 mol/L
2 2
A.3个 B.4个 C.5个 D.6个
14.100 mL甲溶液可能含有H+、K+、
NH 、Ba2+、CO2− 、SO2− 、Cl−中的若干
3 4
种。取该溶液进行连续实验,过程如图
(所加试剂均过量,气体全部逸出)。下列说法中不正确的是
A.原溶液一定不存在 H+、Ba2+,可能存在K+,可通过焰色试验来检验
B.沉淀1转化为沉淀2时,放出的气体标况下的体积为224 mL
C.原溶液一定存在Cl−,且c(Cl−) ≤ 0.1 mol/L
D.原溶液中n(CO2− ):n(SO2−
)=1:l
3 4
15.将碳酸钠溶液置于密闭容器中,并向其中逐滴加入盐酸,得到如图所示的曲线合并图(左纵
坐标为CO 的体积分数,右纵坐标为溶液的pH),下列说法正确的是
2
A.反映二氧化碳含量变化的曲线是a
B.当滴入盐酸60 mL时,溶液中的溶质只含NaCl
C.当溶液的pH由8变为4时,溶液中Na+质量减
少
D.当溶液pH为8时,溶液中开始有大量CO 生成
2
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 5 页 共 10 页二、非选择题(本题共4小题,共55分)
16.(14分)化学与生产、生活息息相关,根据你在铁人中学积累的化学知识,回答以下问题。
(1)天然气的主要成分是CH,标准状况下,CH 的密度为 (保留3位有效数字),家用天
4 4
然气会添加微量的有特殊臭味的泄漏警告剂四氢噻吩(C HS),四氢噻吩的摩尔质量为 。
4 8
(2)铅笔芯主要成分是石墨和黏土。铅笔芯质量的一半是石墨(其余组成物质不含碳),用铅笔写
“石室”两个字消耗的质量约为2 mg,则“石室”两字中所含的碳原子数约为
个( 取6×1023 mol—1)。
(3)亚硝酸钠会与人体中的血红蛋白作用,将 氧化为 ,从而使血红蛋白丧失输送氧气的功
能而使人体中毒。一旦发生亚硝酸盐中毒,立即注射美蓝溶液进行治疗,则美蓝溶液具有
(填“氧化”或“还原”)性。
(4)制备氢氧化铁胶体实验中会出现 和 等图标,前者表示 ,后者表示
。
(5)纺织工业中常用氯气作漂白剂,NaSO 可作为漂白布匹后的“脱氯剂”,NaSO 和Cl 反应的
2 2 3 2 2 3 2
产物是HSO 、NaCl和HCl,则还原剂与氧化剂的粒子个数之比为 。
2 4
(6)我国科学家实现了CO 高选择性、高稳定性加氢合成甲醇(CHOH)。甲醇在点燃的条件下,完
2 3
全燃烧生成CO 和HO,则16 g CHOH完全燃烧需要消耗O 的体积约为 (标准状况)。
2 2 3 2
(7)查阅资料发现碱性环境下,Cl 可将水中的CN-转化为两种无毒的气体,请写出该反应的离子方
2
程式 。
17.(14分)手持技术:利用便携设备辅助学习,实现数据实时采集与分析,提升学习效率与互动
性,是化学研究中常利用的图像。
Ⅰ.验证次氯酸光照分解的产物可以设计成数字化实验。实验步骤如下:(1)将pH传感器、氯离子
传感器、电导率传感器、氧气传感器分别与数据采集器、计算机连接;(2)将四种传感器分别插
入盛有氯水的广口瓶中;(3)用强光照射氯水,同时开始采集数据。下列图像变化最有可能是其
采集的数据的是_______。
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 6 页 共 10 页A.图1表示氯水的pH随时间的变化 B.图2表示溶液中氯离子浓度随时间的变化
C.图3表示氯水的电导率随时间的变化 D.图4表示液面上方氧气体积分数随时间的变化
Ⅱ.因“84消毒液”具有强氧化性,常用于环境和物体表面的杀菌、消毒。已知某“84消毒液”瓶
体部分的标签如图5所示,图6是利用手持技术测定的“84消毒液”的ORP值(数值越大,氧化
能力越强)随pH和温度t的变化情况。请回答下列问题:
84消毒液
[有效成分]NaClO
[规格]3.5 L
[质量分数]25%
[密度]1.2 g/cm3
[注意]①外用消毒剂,需稀释后使用,勿口服;
②不能将本品与酸性产品(如洁厕类清洁产品)同
时使用;
③______________。
图5 图6
(1) 该“84消毒液”的物质的量浓度约为 mol/L(计算结果保留小数点后一位),若取
出10 mL该溶液稀释100倍后进行使用,则稀释后溶液中所含NaClO的物质的量约为 。
(2)图2中“84消毒液”使用时的最佳pH和温度依次是 。使用“84消毒液”时多数
需浸泡一段时间消毒且保持较低温度的原因可能是 ,
结合该分析,请补充“84消毒液”的标签中,[注意]③为 。
(3)“84消毒液”与“洁厕灵”(主要成分为盐酸)不能同时使用,请从Cl元素的化合价角度分
析并结合离子方程式解释原因:
。
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 7 页 共 10 页(4)不能将“84消毒液”与双氧水两种消毒剂混用,否则会产生O,写出反应的化学方程式:
2
,该反应说明氧化性: (填“>”或“<”)。
18.(14分)二草酸合铜(Ⅱ)酸钾(K [Cu(C O)])可用于无机合成、功能材料制备。实验室制备二草酸
2 2 4 2
合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取210 mL 0.2 mol/L的CuSO 溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,
4
沉淀转变成黑色,过滤。
Ⅱ.向草酸(H C O)溶液中加入适量KCO 固体,制得KHC O 和KC O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至80~85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥得到二草酸合铜(Ⅱ)酸钾晶体,进行表
征和分析。
(1)由胆矾(化学式为CuSO ·5HO)配制Ⅰ中的CuSO 溶液。
4 2 4
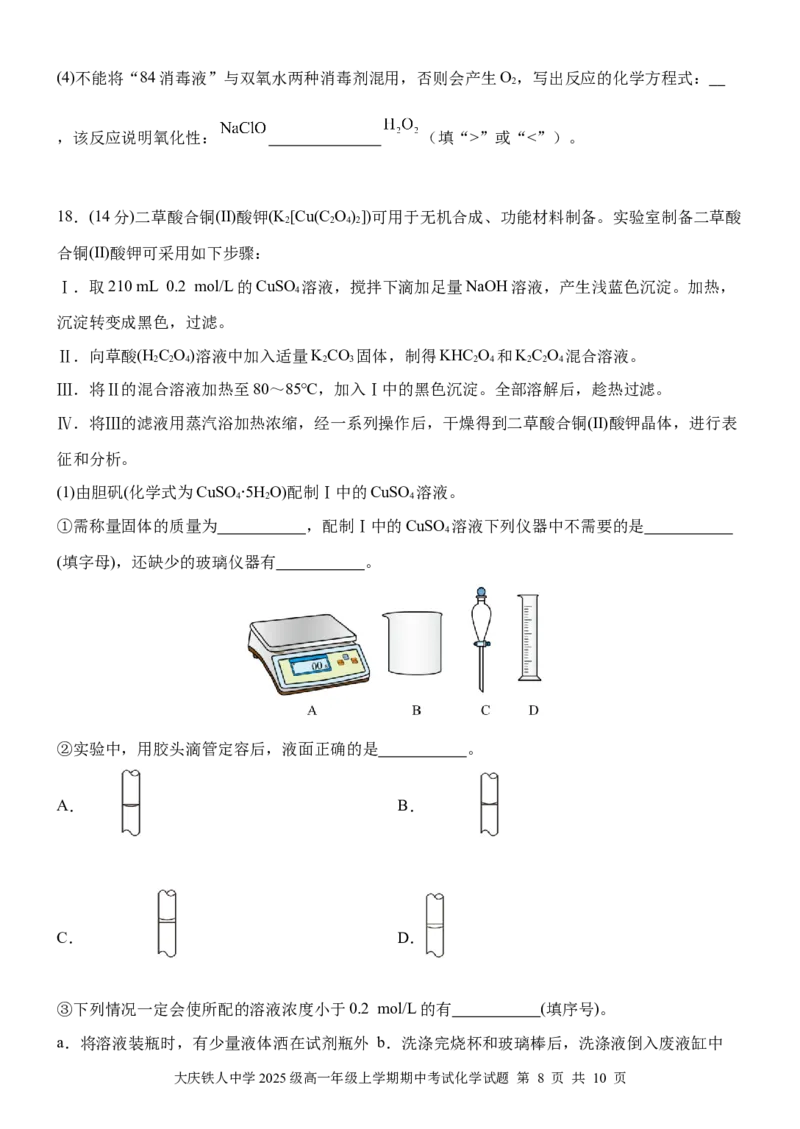
①需称量固体的质量为 ,配制Ⅰ中的CuSO 溶液下列仪器中不需要的是
4
(填字母),还缺少的玻璃仪器有 。
②实验中,用胶头滴管定容后,液面正确的是 。
A. B.
C. D.
③下列情况一定会使所配的溶液浓度小于0.2 mol/L的有 (填序号)。
a.将溶液装瓶时,有少量液体洒在试剂瓶外 b.洗涤完烧杯和玻璃棒后,洗涤液倒入废液缸中
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 8 页 共 10 页c.转移溶液前容量瓶内有少量蒸馏水 d.定容时俯视容量瓶的刻度线
e.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(2)长期存放的CuSO ·5HO中,会出现少量白色固体,原因是 。
4 2
(3)Ⅰ中的黑色沉淀是 (填化学式)。
(4)Ⅱ中原料配比为 ,写出反应的化学方程式 。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入KCO 应采取 的方法。
2 3
(6)Ⅳ中“一系列操作”包括 。
19.(13分)金属钠及其化合物在材料和工业生产方面覆盖面大,在重要化工领域发挥重要作用。
Ⅰ.我国近代化学工业的奠基人侯德榜先生,设计出“侯氏制碱法”,工艺流程如下:
(1)“侯氏制碱法”工艺中先氨化后碳酸化的顺序不能颠倒的原因是 。
(2)碳酸化过程中发生反应的化学方程式为 。
(3)蒸馏水洗涤“过滤”后所得的固体,证明固体洗涤干净的实验操作为
。
(4)生产中可循环利用的物质为 (填化学式)。
Ⅱ.碳酸氢钠用途广泛,某化学兴趣小组对碳酸氢钠性质展开探究。
【提出问题】小组成员推测NaHCO 能与CaCl 反应产生沉淀,并就此展开探究。
3 2
【猜想与假设】假设1:NaHCO 能与CaCl 反应生成Ca(HCO ) 沉淀
3 2 3 2
假设2:
【实验验证】为验证假设,甲同学设计如下实验方案:分别取1 mL不同浓度NaHCO 溶液于试管
3
中,向其中滴加1 mL CaCl 溶液
2
实验 NaHCO 溶液浓度 CaCl 溶液浓度 实验现象
3 2
1 0.1 mol/L 0.1 mol/L 溶液变浑浊
2 0.2 mol/L 0.2 mol/L 溶液出现白色胶状物质
3 0.5 mol/L 0.5 mol/L 有明显白色胶状物质生成
4 1.0 mol/L 1.0 mol/L 有白色胶状物质生成,并有气泡冒出
(5)补全假设2: 。
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 9 页 共 10 页(6)用离子方程式解释实验4中的现象 。
【结果分析】甲同学认为:反应物浓度较低时,假设1成立;反应物浓度较高时,假设2成立。
【继续探究】为进一步探究NaHCO 与CaCl 反应产物,丙同学设计如下实验:
3 2
实验步骤 现象 结论
取实验1反应产物,向试管中 假设1不成立,假设2成
溶液逐渐变澄清
。 立。
(7)补全实验步骤: 。
大庆铁人中学2025级高一年级上学期期中考试化学试题 第 10 页 共 10 页