文档内容
化学部分
相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40 Mn-55
一、选择题(1-44每题均只有一个正确选项,15-77每题均有1~2个正确选项)
1. 属于化学性质的是( )
A. 沸点 B. 熔点 C. 可燃性 D. 密度
【答案】C
【解析】
【分析】物质通过化学变化表现出来的性质就是物质的化学性质,不需要通过化学变化表现出来的性质是
物理性质。
【详解】A、物质的沸点属于物理性质,A选项错误,不符合题意;
B、物质的熔点属于物理性质,B选项错误,不符合题意;
C、物质的可燃性属于化学性质,C选项正确,符合题意;
D、物质的密度属于物理性质,D选项错误,不符合题意。故选C。
2. 会造成酸雨的物质是
A. SO B. CO C. O D. N
2 2 2
【答案】A
【解析】
【详解】煤燃烧时排放出的二氧化硫、二氧化氮等污染物,这些气体或气体在空气中发生反应后的生成物
溶于雨水,会形成酸雨,故选A。
3. 生活中的白醋呈酸性,室温时,白醋的pH可能为
A. 3 B. 7 C. 10 D. 13
【答案】A
【解析】
【详解】生活中的白醋呈酸性,pH<7,故室温时,白醋的pH可能为3。
故选A 。
的
4. 在水 净化过程中,属于化学变化的是
A. 挥发 B. 过滤 C. 消毒 D. 吸附
【答案】C
【解析】
【详解】A、挥发的过程是水由液态变为气态,是状态的改变,没有新物质生成,属于物理变化,不符合
题意;
第1页/共15页
学科网(北京)股份有限公司B、过滤的过程中只是将不溶物与水分离,没有新物质生成,属于物理变化,不符合题意;
C、消毒的过程中消毒剂能破坏细菌中的物质,从而使细菌失去活性,杀菌消毒的过程中有新物质生成,
属于化学变化,符合题意;
D、吸附是利用了活性炭的吸附性,没有新物质生成,属于物理变化,不符合题意,
故选C。
5. 与金刚石互为同素异形体的是
A. 木炭 B. 石墨 C. 一氧化碳 D. 二氧化碳
【答案】B
【解析】
【分析】同素异形体是指由同种元素组成的不同单质,互为同素异形体的物质要符合以下两个条件:同种
元素形成,不同单质。
【详解】A、木炭的主要成分是碳,属于混合物,与金刚石不属于同素异形体,故选项错误。
B、石墨和金刚石均是碳元素形成的不同单质,互为同素异形体,故选项正确。
C、一氧化碳是化合物,与金刚石不属于同素异形体,故选项错误。
D、二氧化碳是化合物,与金刚石不属于同素异形体,故选项错误。
故选:B。
6. 对食品中各种“剂”的物质描述错误的是
A. 食盐作调味剂 B. 生石灰作干燥剂
C. 干冰作制冷剂 D. 氧气作防腐剂
【答案】D
【解析】
【详解】A、氯化钠是重要的调味品,食盐的主要成分是氯化钠,所以食盐作调味剂。A正确;
B、生石灰与水反应生成氢氧化钙,所以生石灰作干燥剂吸收某些物质中的水分。B正确;
C、固态二氧化碳叫干冰,干冰升华制冷,所以干冰作制冷剂。C正确;
D、氧气具有氧化性, 是氧化剂,不能用作防腐剂。D错误。
综上所述:选择D。
7. 工业上常把煤块粉碎后使其充分燃烧,其目的是
A. 减少氧气的消耗 B. 提高煤的利用率
C. 减少二氧化碳的排放 D. 减少酸雨的形成
【答案】B
【解析】
【详解】工业上常把煤块粉碎,其目的是增大煤和氧气的接触面积,使其充分燃烧提高煤的利用率。
第2页/共15页
学科网(北京)股份有限公司故选B。
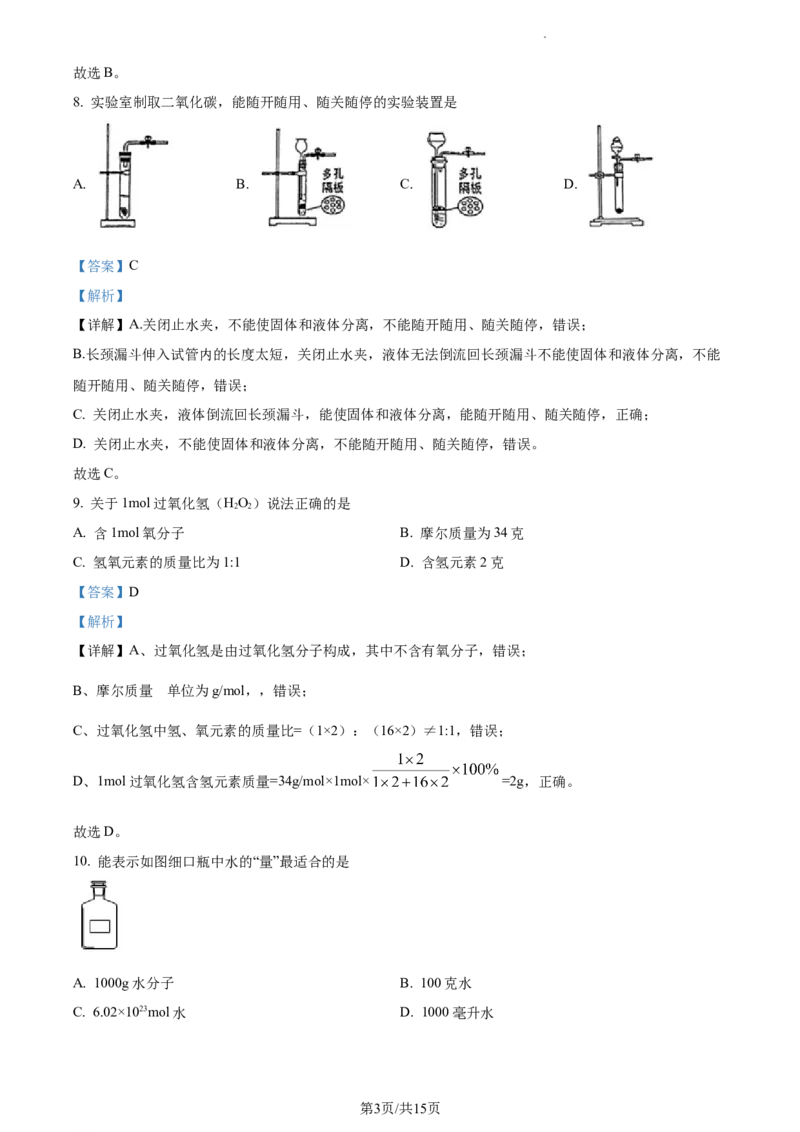
8. 实验室制取二氧化碳,能随开随用、随关随停的实验装置是
A. B. C. D.
【答案】C
【解析】
【详解】A.关闭止水夹,不能使固体和液体分离,不能随开随用、随关随停,错误;
B.长颈漏斗伸入试管内的长度太短,关闭止水夹,液体无法倒流回长颈漏斗不能使固体和液体分离,不能
随开随用、随关随停,错误;
C. 关闭止水夹,液体倒流回长颈漏斗,能使固体和液体分离,能随开随用、随关随停,正确;
D. 关闭止水夹,不能使固体和液体分离,不能随开随用、随关随停,错误。
故选C。
9. 关于1mol过氧化氢(HO)说法正确的是
2 2
A. 含1mol氧分子 B. 摩尔质量为34克
C. 氢氧元素的质量比为1:1 D. 含氢元素2克
【答案】D
【解析】
【详解】A、过氧化氢是由过氧化氢分子构成,其中不含有氧分子,错误;
的
B、摩尔质量 单位为g/mol,,错误;
C、过氧化氢中氢、氧元素的质量比=(1×2):(16×2)≠1:1,错误;
D、1mol过氧化氢含氢元素质量=34g/mol×1mol× =2g,正确。
故选D。
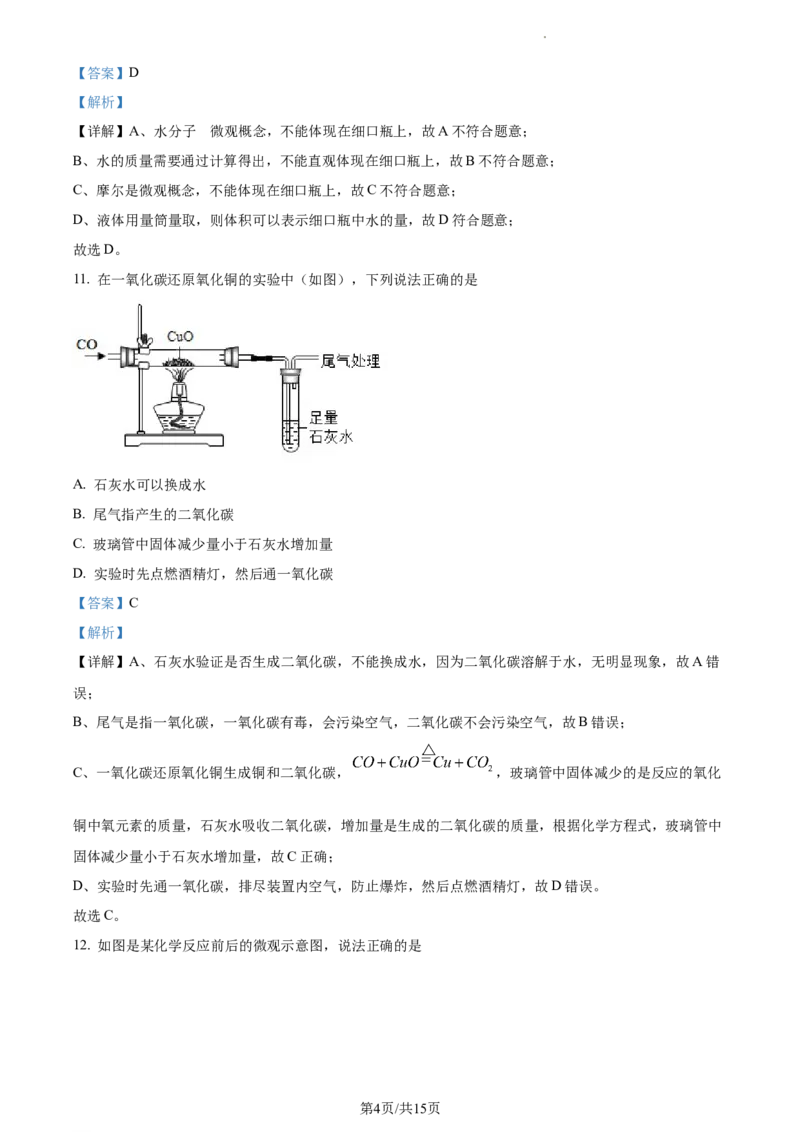
10. 能表示如图细口瓶中水的“量”最适合的是
A. 1000g水分子 B. 100克水
C. 6.02×1023mol水 D. 1000毫升水
第3页/共15页
学科网(北京)股份有限公司【答案】D
【解析】
【详解】A、水分子 是微观概念,不能体现在细口瓶上,故A不符合题意;
B、水的质量需要通过计算得出,不能直观体现在细口瓶上,故B不符合题意;
C、摩尔是微观概念,不能体现在细口瓶上,故C不符合题意;
D、液体用量筒量取,则体积可以表示细口瓶中水的量,故D符合题意;
故选D。
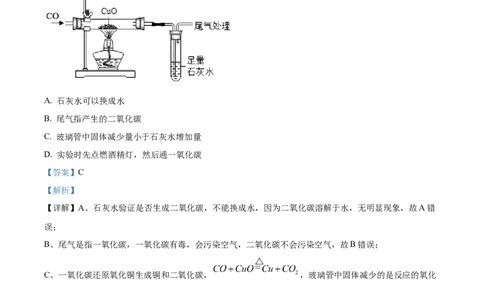
11. 在一氧化碳还原氧化铜的实验中(如图),下列说法正确的是
A. 石灰水可以换成水
B. 尾气指产生的二氧化碳
C. 玻璃管中固体减少量小于石灰水增加量
D. 实验时先点燃酒精灯,然后通一氧化碳
【答案】C
【解析】
【详解】A、石灰水验证是否生成二氧化碳,不能换成水,因为二氧化碳溶解于水,无明显现象,故A错
误;
B、尾气是指一氧化碳,一氧化碳有毒,会污染空气,二氧化碳不会污染空气,故B错误;
C、一氧化碳还原氧化铜生成铜和二氧化碳, ,玻璃管中固体减少的是反应的氧化
铜中氧元素的质量,石灰水吸收二氧化碳,增加量是生成的二氧化碳的质量,根据化学方程式,玻璃管中
固体减少量小于石灰水增加量,故C正确;
D、实验时先通一氧化碳,排尽装置内空气,防止爆炸,然后点燃酒精灯,故D错误。
故选C。
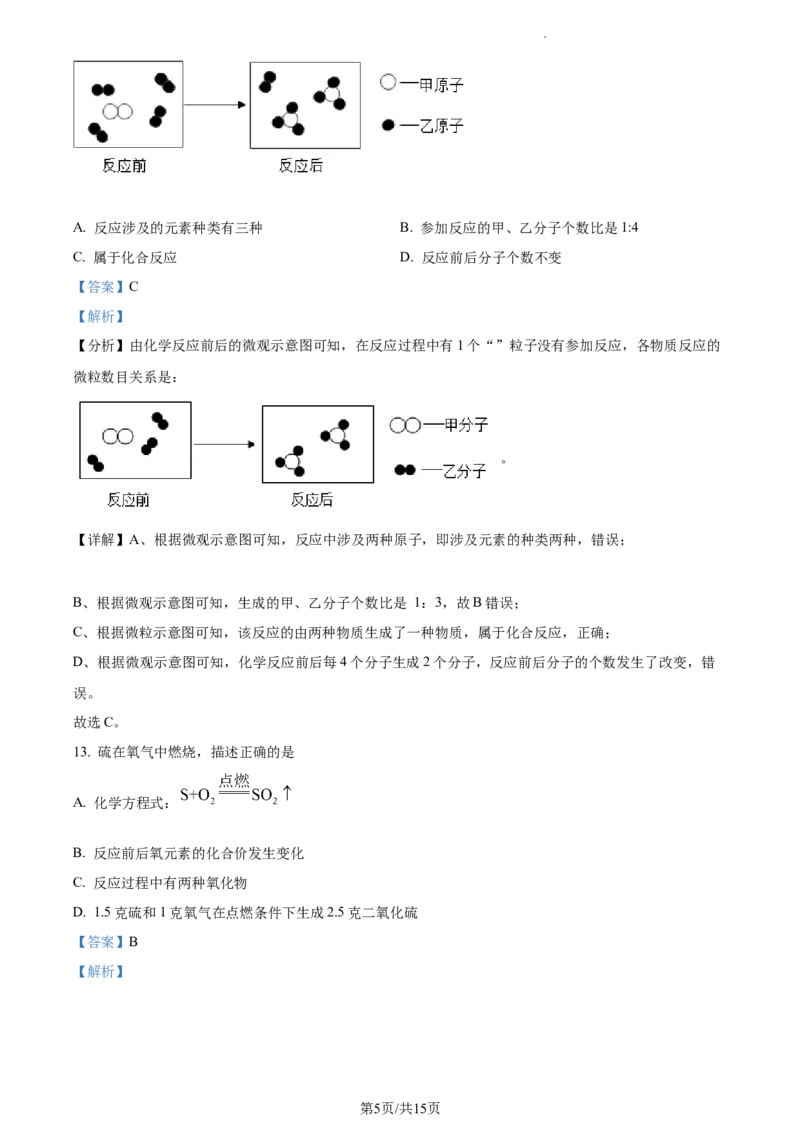
12. 如图是某化学反应前后的微观示意图,说法正确的是
第4页/共15页
学科网(北京)股份有限公司A. 反应涉及的元素种类有三种 B. 参加反应的甲、乙分子个数比是1:4
C. 属于化合反应 D. 反应前后分子个数不变
【答案】C
【解析】
【分析】由化学反应前后的微观示意图可知,在反应过程中有1个“”粒子没有参加反应,各物质反应的
微粒数目关系是:
。
【详解】A、根据微观示意图可知,反应中涉及两种原子,即涉及元素的种类两种,错误;
B、根据微观示意图可知,生成的甲、乙分子个数比是 1:3,故B错误;
C、根据微粒示意图可知,该反应的由两种物质生成了一种物质,属于化合反应,正确;
D、根据微观示意图可知,化学反应前后每4个分子生成2个分子,反应前后分子的个数发生了改变,错
误。
故选C。
13. 硫在氧气中燃烧,描述正确的是
A. 化学方程式:
B. 反应前后氧元素的化合价发生变化
C. 反应过程中有两种氧化物
D. 1.5克硫和1克氧气在点燃条件下生成2.5克二氧化硫
【答案】B
【解析】
第5页/共15页
学科网(北京)股份有限公司【详解】A、硫和氧气在点燃条件下生成二氧化硫,反应的化学方程式为: ,故选项A错
误;
B、反应前氧元素的化合价为0价,反应后氧元素化合价为-2价,反应前后氧元素的化合价发生变化,故
选项B正确;
C、反应过程中只有二氧化硫这一种氧化物,故选项C错误;
D、由反应的化学方程式可知,1克硫和1克氧气在点燃条件下生成2克二氧化硫,故选项D错误;
故选:B。
14. 一定能改变某溶液溶质质量分数的方法是
A. 降温 B. 恒温蒸发 C. 加入该种溶质 D. 加水
【答案】D
【解析】
【详解】A、若该溶液溶质的溶解度随着温度的降低而增大,降温时溶解度增大,溶液的组成未发生改变,
溶质的质量分数不变,若该溶液溶质的溶解度随着温度的降低而减小,降温时溶解度减小,有溶质析出时,
溶质的质量分数变小,降温不一定能改变某溶液溶质质量分数,不符合题意;
B、若溶液为不饱和溶液,恒温蒸发,溶剂质量减少,所得溶液的溶质质量分数变大,若溶液为饱和溶液,
恒温蒸发后仍为该温度下的饱和溶液,溶质的质量分数不变,恒温蒸发不一定能改变某溶液溶质质量分数,
不符合题意;
C、若溶液为不饱和溶液,加入该种溶质,溶质质量变大,所得溶液的溶质质量分数变大,若溶液为饱和
溶液,加入该种溶质后仍为该温度下的饱和溶液,溶质的质量分数不变,加入该种溶质不一定能改变某溶
液溶质质量分数,不符合题意;
D、溶液中加水,溶质不变,溶剂增加,溶质的质量分数变小,加水一定能改变某溶液溶质质量分数,符
合题意。
故选D。
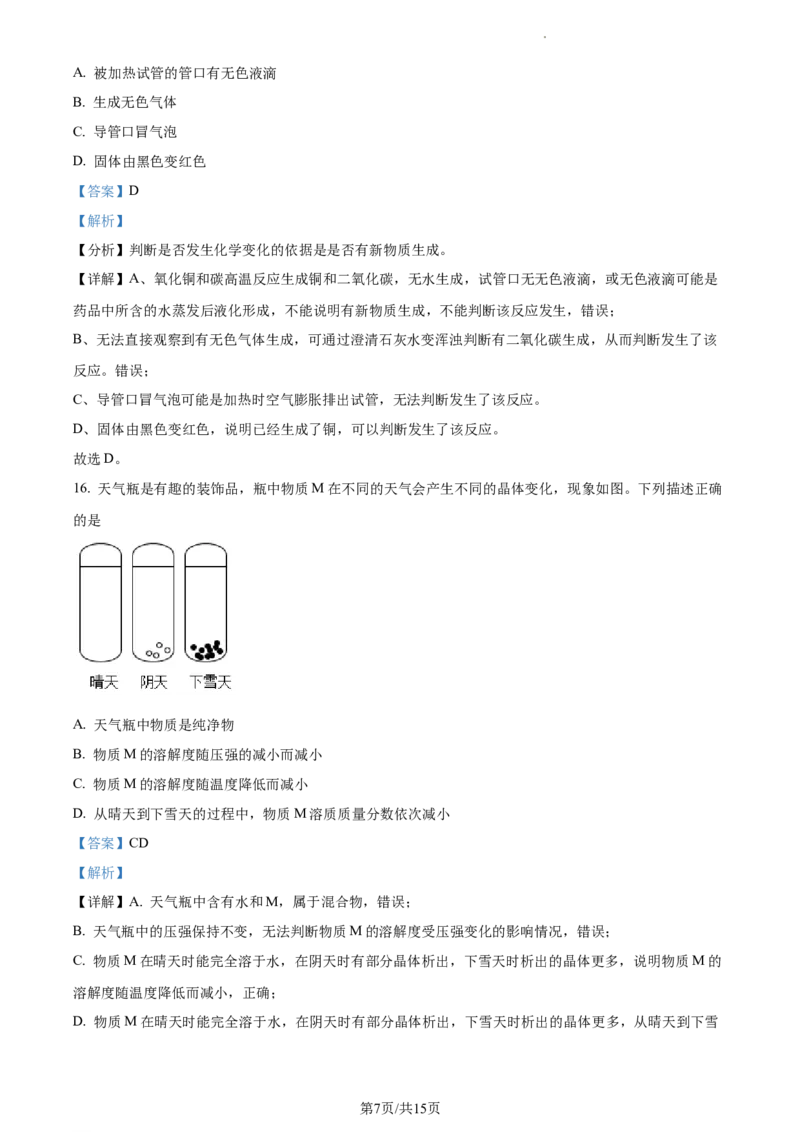
15. 碳还原氧化铜如图所示,判断该反应发生的现象是
第6页/共15页
学科网(北京)股份有限公司A. 被加热试管的管口有无色液滴
B. 生成无色气体
C. 导管口冒气泡
D. 固体由黑色变红色
【答案】D
【解析】
【分析】判断是否发生化学变化的依据是是否有新物质生成。
【详解】A、氧化铜和碳高温反应生成铜和二氧化碳,无水生成,试管口无无色液滴,或无色液滴可能是
药品中所含的水蒸发后液化形成,不能说明有新物质生成,不能判断该反应发生,错误;
B、无法直接观察到有无色气体生成,可通过澄清石灰水变浑浊判断有二氧化碳生成,从而判断发生了该
反应。错误;
C、导管口冒气泡可能是加热时空气膨胀排出试管,无法判断发生了该反应。
D、固体由黑色变红色,说明已经生成了铜,可以判断发生了该反应。
故选D。
16. 天气瓶是有趣的装饰品,瓶中物质M在不同的天气会产生不同的晶体变化,现象如图。下列描述正确
的是
A. 天气瓶中物质是纯净物
B. 物质M的溶解度随压强的减小而减小
C. 物质M的溶解度随温度降低而减小
D. 从晴天到下雪天的过程中,物质M溶质质量分数依次减小
【答案】CD
【解析】
【详解】A. 天气瓶中含有水和M,属于混合物,错误;
B. 天气瓶中的压强保持不变,无法判断物质M的溶解度受压强变化的影响情况,错误;
C. 物质M在晴天时能完全溶于水,在阴天时有部分晶体析出,下雪天时析出的晶体更多,说明物质M的
溶解度随温度降低而减小,正确;
D. 物质M在晴天时能完全溶于水,在阴天时有部分晶体析出,下雪天时析出的晶体更多,从晴天到下雪
第7页/共15页
学科网(北京)股份有限公司天的过程中,溶解在水中的物质M不断减少,故物质M溶质质量分数依次减小,正确。
故选CD。
17. 取24.5克氯酸钾和一定量二氧化锰混合,加热,收集一瓶氧气后停止实验,测得剩余固体的质量为m
克。下列分析正确的是
A. 生成氧气质量是(24.5-m)克 B. 生成氯化钾质量小于m克
C. 二氧化锰质量可能是8.7克 D. m可能是14.9
【答案】BC
【解析】
【详解】A、根据质量守恒定律,化学反应前后,物质的总质量不变,则生成氧气的质量为:24.5g+二氧
化锰的质量-剩余固体的质量,故生成氧气的质量大于(24.5-m)克,不符合题意;
B、剩余固体包括反应生成的氯化钾、二氧化锰、以及未反应的氯酸钾(如果氯酸钾未完全反应),故生
成氯化钾质量小于m克,符合题意;
C、根据题给信息,无法计算得出二氧化锰的质量,故二氧化锰的质量可能是8.7g,也可能不是,符合题
意;
D、如果氯酸钾完全反应,生成氯化钾的质量为: ,但是剩余固体中还包括
二氧化锰,故m不可能是14.9,不符合题意。
故选BC。
二、简答题
18. 人类生活在空气中,空气与人类的生存休戚相关。
(1)空气中最多的气体是______,空气是_________(选填“纯净物”或“混合物”)。
(2)自然界中既有消耗氧气又有产生氧气的变化,使空气中氧气的含量基本保持不变,为人类的生存提
供保证。请分别写出你学过的一个消耗氧气和一个产生氧气的化学方程式_______;_______。
(3)空气质量对人体健康有直接影响。雷电时,空气中产生少量臭氧气体,臭氧具有杀菌消毒的作用。
臭氧的化学式为O,氧元素的存在形态是_______(选填“游离态”或“化合态”),1mol臭氧分子的个数约
3
为______个。
(4)我国承诺将力争2030年前实现“碳达峰”,在2060年前实现“碳中和”。其中“碳”代表的物质是
_______。
【答案】(1) ①. 氮气##N
2
②. 混合物
第8页/共15页
学科网(北京)股份有限公司(2) ①. (答案合理即可)
②. (答案合理即可)
(3) ①. 游离态 ②. 6.02×1023
(4)二氧化碳##CO
2
【解析】
【小问1详解】
根据空气中各组成的体积分数可知,氮气的体积分数最大约是78%,所以空气中最多的气体是氮气;
由于空气中含有氮气、氧气、二氧化碳等多种物质,所以空气属于混合物;
故答案为:氮气或N;混合物;
2
【小问2详解】
消耗氧气的反应有很多,例如:硫与氧气在点燃的条件下反应,生成二氧化硫、铁与氧气在点燃的条件下
反应,生成四氧化三铁等合理即可;
产生氧气的反应也有很多,例如:水在通电的条件下分解,生成氢气和氧气、高锰酸钾在加热的条件下分
解,生成锰酸钾、二氧化锰和氧气等合理即可;
故答案为: (答案合理即可); (答案合理即可);
【小问3详解】
元素以单质形式存在的,属于元素的游离态;以化合物形式存在的,属于元素的化合态,由于臭氧中的氧
元素以单质形式存在,所以氧元素的存在形态是游离态;
1 mol任何物质中含有 个分子,所以1 mol臭氧分子的个数约为 个;
故答案为:游离态; ;
【小问4详解】
“碳达峰”就是指在某一个时点,二氧化碳的排放不再增长达到峰值,之后逐步回落; “碳中和”是指
向大气中排放的二氧化碳的总量,通过植树造林、节能减排等形式,以抵消自身产生的二氧化碳或温室气
体的排放,实现正负抵消,达到相对“零排放”;“碳达峰”与 “碳中和”一起,简称“双碳”,其中
“碳”指的是二氧化碳;
第9页/共15页
学科网(北京)股份有限公司故答案为:二氧化碳或CO。
2
19. 实验室制取气体是化学学习的重要内容。
(1)大理石和稀盐酸制取二氧化碳的化学方程式是______;收集二氧化碳的方法是______,将点燃的木
条伸入盛有二氧化碳的集气瓶中,现象是______,由此_____(选填“能”或“不能”)判断集气瓶中集满二氧
化碳。
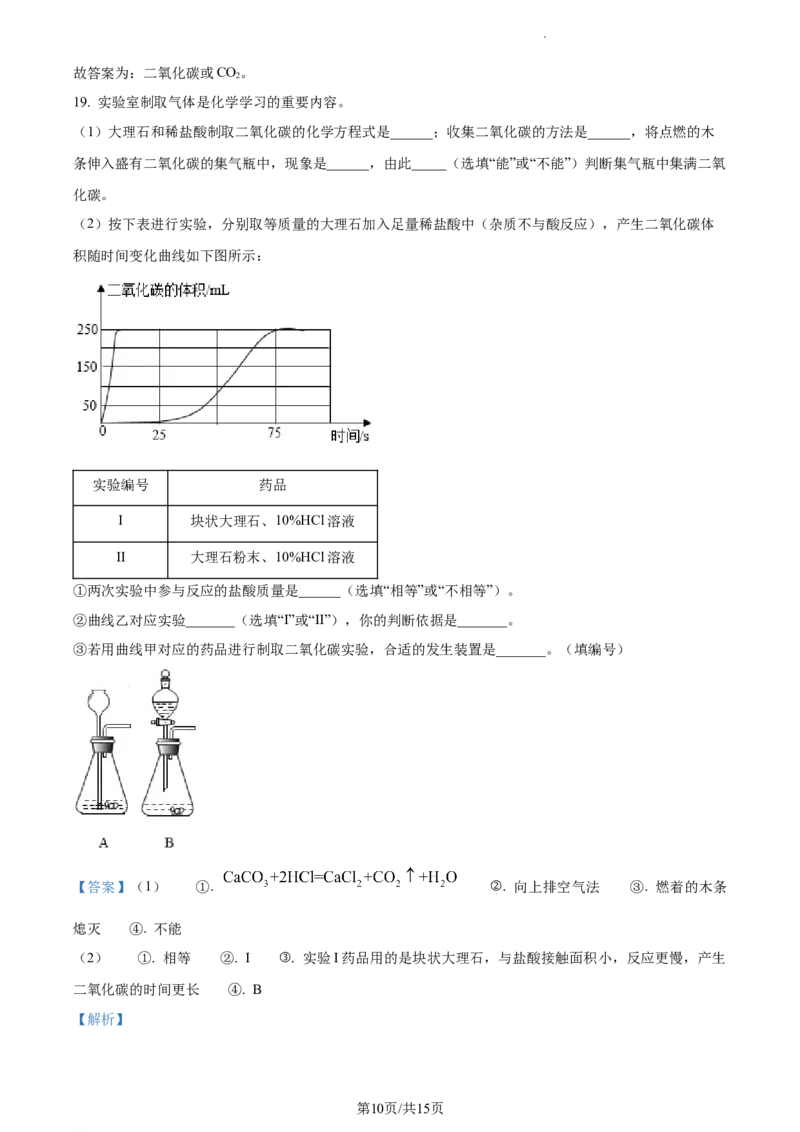
(2)按下表进行实验,分别取等质量的大理石加入足量稀盐酸中(杂质不与酸反应),产生二氧化碳体
积随时间变化曲线如下图所示:
实验编号 药品
I 块状大理石、10%HCl溶液
II 大理石粉末、10%HCl溶液
①两次实验中参与反应的盐酸质量是______(选填“相等”或“不相等”)。
②曲线乙对应实验_______(选填“I”或“II”),你的判断依据是_______。
③若用曲线甲对应的药品进行制取二氧化碳实验,合适的发生装置是_______。(填编号)
【答案】(1) ①. ②. 向上排空气法 ③. 燃着的木条
熄灭 ④. 不能
(2) ①. 相等 ②. I ③. 实验I药品用的是块状大理石,与盐酸接触面积小,反应更慢,产生
二氧化碳的时间更长 ④. B
【解析】
第10页/共15页
学科网(北京)股份有限公司【小问1详解】
大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙水和二氧化碳,反应的化学方程式为:
;
二氧化碳密度比空气大,且能溶于水,故可用向上排空气法收集;
将点燃的木条伸入盛有二氧化碳的集气瓶中会看到燃着的木条熄灭,由此不能判断集气瓶中集满二氧化碳,
应该将燃着的木条放在集气瓶口处,若木条熄灭则收集满。
【小问2详解】
①由图像可知,甲乙曲线最终生成二氧化碳的体积相等,故两次实验中参与反应的盐酸质量是相等的;
②曲线乙对应实验I,因为实验I药品用的是块状大理石,与盐酸接触面积小,反应更慢,产生二氧化碳的
时间更长;
③由图像可知曲线甲产生二氧化碳的反应时间非常快,故曲线甲是实验II,药品是大理石粉末,合适的发
生装置是B,因为大理石粉末与盐酸接触面积大,反应迅速,装置B可以控制盐酸的滴加速率来控制反应
的速率,还能防止生成的二氧化碳气体逸出。
20. 依据硝酸钾和氯化钠的溶解度曲线,回答问题。
(1)氯化钠属于_______(选填“易溶物”或“难溶物”)。
(2)60℃时,把接近饱和的氯化钠溶液变成饱和溶液的方法是______。
(3)60℃时,100克硝酸钾饱和溶液的溶质质量分数为______(列式即可),倒出部分该溶液,从“量”的
角度对比剩余溶液和原溶液。剩余溶液中的溶质质量比原溶液中溶质质量_______(选填“大”“小”或“相
等”);剩余溶液中的______与原溶液相同。
(4)某溶液中含有硝酸钾和氯化钠,对该溶液进行如下操作:
第11页/共15页
学科网(北京)股份有限公司①操作X的名称是_____(选填“蒸发结晶”或“降温结晶”)。
②有关说法正确的是______。
A.滤渣一定含硝酸钾
B.滤渣一定含氯化钠
C.原溶液是硝酸钾的饱和溶液
D.滤液甲和滤液乙中都含有两种溶质
【答案】(1)易溶物 (2)蒸发溶剂或加溶质
(3) ①. ②. 小 ③. 溶质质量分数
(4) ①. 蒸发结晶 ②. A
【解析】
【小问1详解】
通常把在室温(20℃)下,溶解度在l0g以上的物质称为易溶物,由图可知,在20℃时,氯化钠的溶解度
大于10g,为易溶物;故填:易溶物;
【小问2详解】
由图可知氯化钠的溶解度随温度上升而上升,故把接近饱和的氯化钠溶液变成饱和溶液的方法是蒸发溶剂
或加溶质;故填:蒸发溶剂或加溶质;
【小问3详解】
,由图知60℃,硝酸钾的溶解度为110g,故100克
硝酸钾饱和溶液的溶质质量分数= ;溶液是均一、稳定的混合物,倒出部分该溶液,剩
余溶液中的溶质质量比原溶液中溶质质量小;剩余溶液中的溶质质量分数与原溶液相同;故填:
第12页/共15页
学科网(北京)股份有限公司;小;溶质质量分数;
【小问4详解】
①硝酸钾的溶解度随温度升高而大幅度升高,氯化钠溶解度随温度变化不大,要分离硝酸钾和氯化钠,并
趁热过滤得到氯化钠,应采用蒸发结晶的方法,即升高温度,蒸发水分,氯化钠以晶体的形式析出,而硝
酸钾仍在滤液中,所以操作X的名称是蒸发结晶;故填:蒸发结晶;
②酸钾的溶解度随温度升高而大幅度升高,氯化钠溶解度随温度变化不大,经蒸发结晶,并趁热过滤得到
氯化钠和滤液甲,该过程中氯化钠可能完全析出或部分析出,滤液甲中可能有氯化钠,不能确定;经降温
结晶得到滤渣硝酸钾(不一定有氯化钠)和滤液乙,滤液乙中可能含有氯化钠,不能确定。因此有关说法
正确的是:
A、硝酸钾的溶解度随温度降低而减小,降温结晶后,滤渣中一定有硝酸钾,故A正确,符合题意;
B、滤液甲中可能不含有氯化钠,故降温结晶后,滤渣中不一定含氯化钠,故B不正确,不符合题意;
C、该过程不能判断原溶液是硝酸钾的饱和溶液,故C不正确,不符合题意;
D、滤液甲和滤液乙中可能都不含有氯化钠,只含有硝酸钾,只有一种溶质,故D不正确,不符合题意。
故选A。
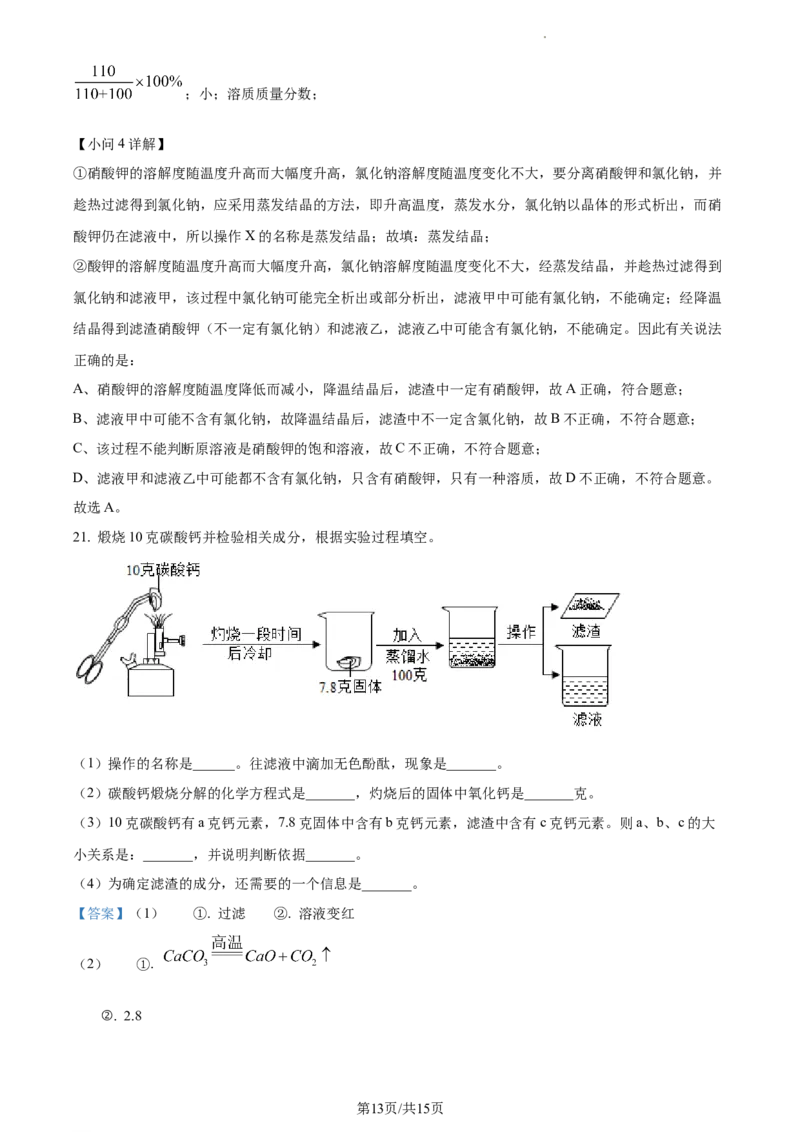
21. 煅烧10克碳酸钙并检验相关成分,根据实验过程填空。
(1)操作的名称是______。往滤液中滴加无色酚酞,现象是_______。
(2)碳酸钙煅烧分解的化学方程式是_______,灼烧后的固体中氧化钙是_______克。
(3)10克碳酸钙有a克钙元素,7.8克固体中含有b克钙元素,滤渣中含有c克钙元素。则a、b、c的大
小关系是:_______,并说明判断依据_______。
(4)为确定滤渣的成分,还需要的一个信息是_______。
【答案】(1) ①. 过滤 ②. 溶液变红
(2) ①.
②. 2.8
第13页/共15页
学科网(北京)股份有限公司(3) ①. a=b>c ②. 根据质量守恒定律a=b,滤液为氢氧化钙的饱和溶液,其中含有部分钙元素,
因此cc;
【小问4详解】
为确定滤渣的成分,还需要的一个信息是实验温度下氢氧化钙的溶解度,要确定溶解的氢氧化钙的质量。
第14页/共15页
学科网(北京)股份有限公司第15页/共15页
学科网(北京)股份有限公司