文档内容
黄浦区 2022 学年第二学期初三质量调研
(2023.04)
(满分50分,考试时间40分钟)
相对原子质量:相对原子质量:H-1 C-12 O-16 Ca-40
一、选择题(1~14每题只有1个正确选项,每题1分,共14分)
1. 空气中含量最多的气体是
A. O B. N C. He D. CO
2 2 2
【答案】B
【解析】
【详解】空气中含量最多的气体是氮气,氮气属于气态非金属单质,在元素符号的右下角写上表示分子中
所含原子数的数字,其化学式为:N,故选B。
2
2. 能在水中形成溶液的物质是
A. 花生油 B. 葡萄糖 C. 面粉 D. 碳酸钙
【答案】B
【解析】
【详解】A、花生油不溶于水,无法形成溶液;
B、葡萄糖溶于水,形成均一稳定的混合物,能形成溶液;
C、面粉不溶于水,无法形成溶液;
D、碳酸钙不溶于水,无法形成溶液;
故选B。
3. 属于有机物的是
A. CO B. CH C. KCO D. NaHCO
2 4 2 3 3
【答案】B
【解析】
【详解】有机物为含碳元素的化合物,但二氧化碳、一氧化碳、碳酸、碳酸盐、碳酸氢盐等除外,故选
B。
4. 以下最清洁的能源是
A. 氢能 B. 石油 C. 煤 D. 天然气
【答案】A
【解析】
【详解】A、氢气的燃烧产物是水,无污染,属于最清洁的能源。A符合题意;
B、石油在燃烧时能产生二氧化硫、一氧化碳、烟尘等空气污染物。B不符合题意;
第1页/共13页
学科网(北京)股份有限公司C、煤在燃烧时能产生二氧化硫、一氧化碳、氮氧化物等空气污染物。C不符合题意;
D、天然气燃烧时产生的二氧化碳排放过多会造成温室效应增强。D不符合题意。
综上所述:选择A。
5. 与金刚石互为同素异形体的物质是
A. 黄金 B. 木炭 C. 炭黑 D. 石墨
【答案】D
【解析】
【分析】同素异形体是相同元素组成,不同形态的单质。互为同素异形体的物质要符合以下两个条件:同
种元素形成,不同单质。
【详解】A 、黄金由金元素组成,金刚石由碳元素组成,所以黄金与金刚石不是互为同素异形体,A不符
合题意;
B、木炭主要成分是碳,含有其它杂质,属于混合物,和金刚石不属于同素异形体,B不符合题意;
C、炭黑主要成分是碳,含有其它杂质,属于混合物,和金刚石不属于同素异形体,C不符合题意;
D、石墨和金刚石都是由碳元素形成的不同物质,都是单质,互为同素异形体。D符合题意。
综上所述:选择D。
6. 某溶液呈棕黄色,该溶液可能是
A. 氯化铁溶液 B. 硫酸铜溶液 C. 石蕊溶液 D. 氯化钠溶液
【答案】A
【解析】
【详解】A.含Fe3+的盐溶液呈棕黄色,某溶液呈棕黄色,该溶液可能是氯化铁溶液,故A正确;
B.硫酸铜溶液呈蓝色,故B错误;
C.石蕊溶液呈紫色,故C错误;
D.氯化钠溶液为无色溶液,故D错误。
故选:A。
7. 自来水厂净水过程中,发生化学变化的方法是
A. 沉淀 B. 过滤 C. 吸附 D. 消毒
【答案】D
【解析】
【分析】
【详解】A、沉淀过程中只是将水中固体杂质与水分离,没有新物质生成,属于物理变化,不符合题意;
第2页/共13页
学科网(北京)股份有限公司B、过滤过程中只是将水中固体杂质与水分离,没有新物质生成,属于物理变化,不符合题意;
C、吸附过程中只是将水中色素与异味与水分离,没有新物质生成,属于物理变化,不符合题意;
D、消毒过程中杀死了水中微生物,微生物中蛋白质变性,有新物质生成,属于化学变化,符合题意。
故选:D。
8. 氯酸钾与二氧化锰混合制取氧气,化学方程式书写正确的是
A. 2KClO 3KCl+2O ↑ B. 2KClO KCl+3O
3 2 3 2
C. KClO KClO+O D. 2KCIO 2KCl+3O ↑
3 2 3 2
【答案】D
【解析】
【分析】化学方程式要注意反应前后原子 的种类数目均不变,当反应物中没有气体生成物中有气体时,需
要加气体符号,且反应要符合客观事实。
【详解】氯酸钾在二氧化锰及加热条件下分解生成氯化钾和氧气,化学方程式为
。故选D。
9. 用“ ”代表氢原子,能表示2个氢分子的微粒图示是
A. B. C. D.
【答案】D
【解析】
【分析】根据微粒的构成分析,1个氢分子是由两个氢原子构成的。
【详解】A、该图示表示1个H 分子,A不符合题意;
4
B、该图示表示4个氢原子,B不符合题意;
C、该图示表示2个氢原子,1个氢分子,C不符合题意;
D、该图示表示2个氢分子,D符合题意。
综上所述:选择D。
10. 一般情况下,金属越活泼越难冶炼。铁、铜、钠、铝这四种金属最晚开始冶炼的是
第3页/共13页
学科网(北京)股份有限公司A. 铁 B. 铜 C. 钠 D. 铝
【答案】C
【解析】
【详解】金属越活泼越难冶炼,根据金属活动性顺序表,铁、铜、钠、铝的活动顺序为钠>铝>铁>铜,所
以最晚开始冶炼的是钠,故选C。
11. 有关生石灰的说法正确的是
A. 属于碱 B. 能干燥氧气 C. 能治疗胃酸过多 D. 能与CO反应
【答案】B
【解析】
【详解】A、生石灰为氧化钙的俗称,氧化钙属于氧化物,该选项说法不正确;
B、氧化钙能与水反应,则可用于干燥氧气,该选项说法正确;
C、氧化钙和水反应会放出大量热,不能用于治疗胃酸过多,该选项说法不正确;
D、氧化钙不能与一氧化碳反应,该选项说法不正确。
故选B。
12. 酒精(C HO)在空气燃烧,不可能生成的是
2 6
A. SO B. CO C. CO D. HO
2 2 2
【答案】A
【解析】
【详解】A、根据质量守恒定律可知,酒精(C HO)在空气充分燃烧生成二氧化碳和水。酒精中不含硫元
2 6
素,不能生成二氧化硫。A符合题意;
B、根据质量守恒定律可知,酒精(C HO)在空气充分燃烧生成二氧化碳和水。B不符合题意;
2 6
C、根据质量守恒定律可知,酒精(C HO)在空气不充分燃烧生成二氧化碳、一氧化碳和水。C不符合题
2 6
意;
D、根据质量守恒定律可知,酒精(C HO)在空气充分燃烧生成二氧化碳和水。D不符合题意。
2 6
综上所述:选择A。
13. 只含一种分子的物质一定是
A. 单质 B. 化合物 C. 纯净物 D. 混合物
【答案】C
【解析】
【详解】只含有一种分子的物质一定是纯净物,该纯净物中如只含有一种元素,则是单质,如含有多种元
素,则是化合物,故选C。
第4页/共13页
学科网(北京)股份有限公司【点睛】由同种物质组成的物质是纯净物,由同种元素组成的纯净物是单质,由不同种元素组成的纯净物
是化合物。
14. 关于一氧化碳与氧化铜发生反应的实验,说法正确的是
A. 反应前先通入一氧化碳是为了实验能安全进行
B. 尾气处理的方法是将其通入足量的澄清石灰水
C. 反应前后固体减少的质量等于生成气体的质量
D. 反应前后每种元素均从化合态转变为了游离态
【答案】A
【解析】
【分析】一氧化碳还原氧化铜生成铜和二氧化碳,反应的方程式为 。
【详解】A、反应前先通入一氧化碳是为了排尽管内空气,防止一氧化碳不纯导致玻璃管炸裂,说法正确;
B、一氧化碳不与石灰水反应,故不能将其通入足量的澄清石灰水进行尾气处理,说法错误;
C、根据方程式可知,氧化铜固体变成单质铜,减少的只是氧元素的质量,生成的气体二氧化碳的质量等
于参与反应的一氧化碳的质量加上减少的氧化铜中氧元素的质量,说法错误;
D、分析方程式可知,反应前后铜元素由化合态变成了游离态,而碳、氧元素仍为化合态,说法错误。
故选A。
15~17每题均有1~2个正确选项(选对1个得1分,多选或错选得0分)
15. 有关碱性氧化物的说法正确的是
A. 均能与水反应 B. 均能与酸反应
C. 含有金属元素 D. 含有氢、氧元素
【答案】BC
【解析】
【分析】碱性氧化物是指能与酸反应生成盐和水的物质,且碱性氧化物一定为金属氧化物。
【详解】A、碱性氧化物不一定能与水反应,该选项说法不正确;
B、碱性氧化物均能与酸反应,该选项说法正确;
C、碱性氧化物一定是金属氧化物,则一定含有金属元素,该选项说法正确;
D、氧化物是指含有两种元素,且一种元素为氧元素,则碱性氧化物中不含氢元素,该选项说法不正确。
故选BC。
16. 为探究X、Y两种金属的金属活动性强弱,取X、Y进行实验,根据结果,一定能达成实验目的的是
A B C D
操作 观察颜色 测定密度 分别与稀硫酸混合 X与Y的盐溶液混合
第5页/共13页
学科网(北京)股份有限公司结果 X红色、Y银白色 X的密度大于Y 均无明显现象 X的表面析出Y
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A 、观察颜色,不能探究X、Y两种金属的金属活动性强弱。A不符合题意;
B、测定密度,不能探究X、Y两种金属的金属活动性强弱。B不符合题意;
C、分别与稀硫酸混合后均无明显现象,不能探究X、Y两种金属的金属活动性强弱。C不符合题意;
D、X与Y的盐溶液混合,X的表面析出Y,说明X的金属的金属活动性比Y强。D符合题意。
综上所述:选择D。
17. 通过以下方法,能配制得到100g、20%的氯化钠溶液的是
A. 将20g氯化钠与80mL水混合,充分搅拌
B. 将80g、25%的氯化钠溶液与20mL水充分混合
C. 将10g氯化钠加入至90g、20%的氯化钠溶液,充分搅拌
D. 将10g氯化钠加入至200g、5%的氯化钠溶液,充分搅拌后取出一半质量的溶液
【答案】AB
【解析】
【详解】A、80mL水的质量为80mL×1g/cm3=80g,则将20g氯化钠与80mL水混合,所得溶液质量为
100g,质量分数为 ,该选项符合题意;
B、稀释前后溶质质量不变,将80g、25%的氯化钠溶液与20mL水充分混合,所得溶液质量为100g,质量
分数为 ,该选项符合题意;
C、将10g氯化钠加入至90g、20%的氯化钠溶液,溶液质量为10g+90g=100g,溶质质量分数为
,该选项不符合题意;
第6页/共13页
学科网(北京)股份有限公司D、将10g氯化钠加入至200g、5%的氯化钠溶液,溶液质量为10g+200g=210g,取出一半为
210g÷2=105g,且溶质质量分数为 ,该选项不符合题意。
故选AB。
二、简答题(共30分)
18. 人类社会发展和进步离不开各种材料。
(1)玻璃制品随处可见。玻璃制造中发生的反应之一为:CaCO +SiO CaSiO +X↑。X的化学式是
3 2 3
______,SiO 中Si的化合价为______; 2molSiO 约含______个硅原子。
2 2
(2)铝箔可用于食品包装。铝的元素符号是______。将铝压制成铝箔,是因为其具有良好的延展性,
“延展性”属于______(选填“物理性质”或“化学性质”)。微波炉加热食物忌用金属器皿,铝制容器
______(选填“能”或“不能”)放在微波炉里加热。
(3)锂(Li)电池广泛应用于数码产品、电动汽车等领域。
电池
钴酸锂(LiCoO ) 锰酸锂(LiMn O) 磷酸铁锂(LiFePO )
2 2 4 4
特点
可循环次数 500 300 2000
低温特性 优 优 差
高温特性 优 差 优
安全性 差 好 好
成本 高 较低 低
钴酸锂中含有______种元素:锰酸锂______(选填“属于”或“不属于”)氧化物;磷酸铁锂相比钴酸锂
应用更广泛,是因为其具有的特点有______。
【答案】(1) ①. CO ②. +4 ③. 1.204×1024
2
(2) ①. Al ②. 物理性质 ③. 不能
(3) ①. 3##三 ②. 不属于 ③. 可循环使用,安全性好、成本低(合理给分)
【解析】
【小问1详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Ca、C、O、Si的个数分别是
1、1、5、1,生成物中含Ca、C、O、Si的个数分别是1、0、3、1,故生成物中还应含1个C、2个O,故
第7页/共13页
学科网(北京)股份有限公司X的化学式为:CO;
2
二氧化硅中氧元素显-2价,设硅元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:
x+(-2)×2=0,x=+4;
2mol二氧化硅中硅原子的个数为:2mol×6.02×1023=1.204×1024;
【小问2详解】
由两个字母表示的元素符号,第一个字母大写,第二个字母必须小写,故铝的元素符号是:Al;
延展性不需要通过化学变化就能表现出来,属于物理性质;
微波炉加热食物忌用金属器皿,铝属于金属,故铝制容器不能放在微波炉里加热;
【小问3详解】
由化学式可知,钴酸锂中含Li、Co、O三种元素;
锰酸锂由Li、Mn、O三种元素组成,不属于氧化物;
由表可知,磷酸铁锂相比钴酸锂应用更广泛,是因为其具有的特点有可循环使用,安全性好、成本低。
19. 某溶液M中可能含氢氧化钠、碳酸钠、硫酸钠。为验证其成分,进行如下实验。
(1)实验1:取样于试管中,滴入酚酞溶液,观察到溶液变红。请分析说明,用该方法证明溶液M中含
有氢氧化钠的可行性。______
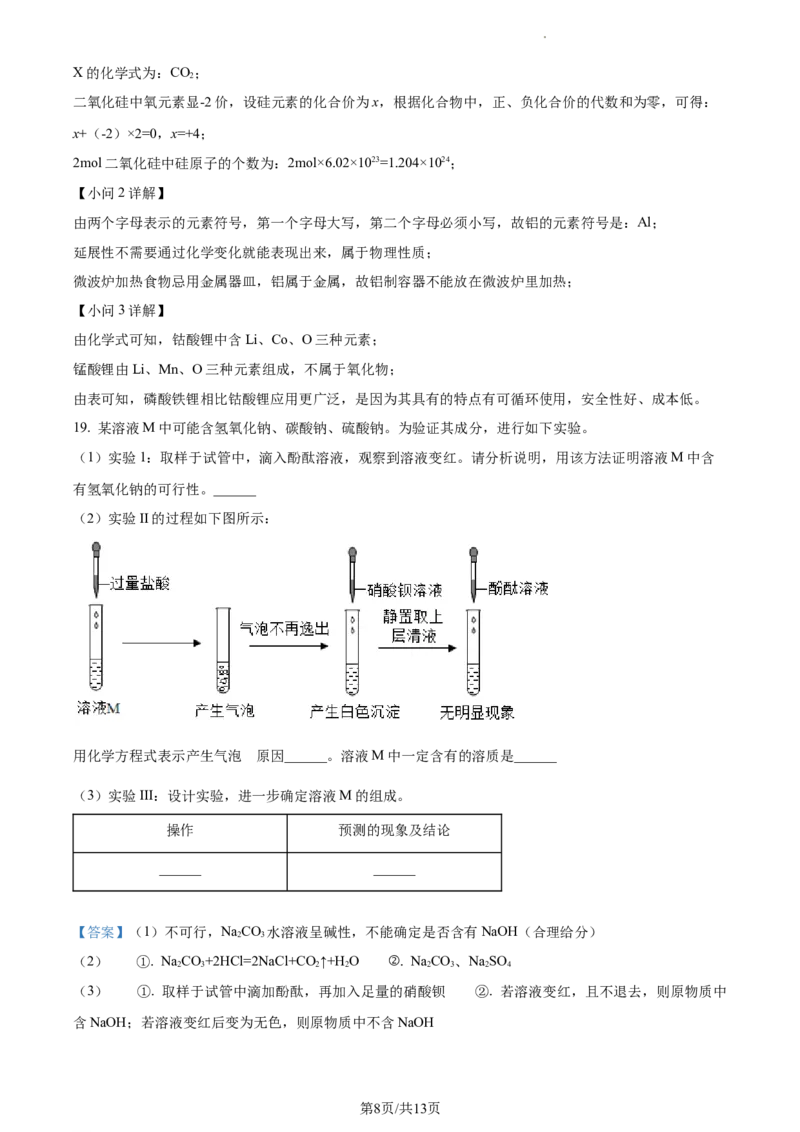
(2)实验II的过程如下图所示:
的
用化学方程式表示产生气泡 原因______。溶液M中一定含有的溶质是______
(3)实验III:设计实验,进一步确定溶液M的组成。
操作 预测的现象及结论
______ ______
【答案】(1)不可行,NaCO 水溶液呈碱性,不能确定是否含有NaOH(合理给分)
2 3
(2) ①. NaCO+2HCl=2NaCl+CO ↑+H O ②. NaCO、NaSO
2 3 2 2 2 3 2 4
(3) ①. 取样于试管中滴加酚酞,再加入足量的硝酸钡 ②. 若溶液变红,且不退去,则原物质中
含NaOH;若溶液变红后变为无色,则原物质中不含NaOH
第8页/共13页
学科网(北京)股份有限公司【解析】
【小问1详解】
不可行,NaCO 水溶液呈碱性,所以溶液显碱性不能确定是否含有NaOH。
2 3
【小问2详解】
可能含有的成分中,能与稀盐酸反应产生气泡的只有碳酸钠,碳酸钠和盐酸反应生成氯化钠、二氧化碳和
水,化学方程式为:NaCO+2HCl=2NaCl+CO ↑+H O。
2 3 2 2
加入稀盐酸有气泡产生,说明溶液 M中一定含有碳酸钠,继续加入硝酸钡溶液,产生白色沉淀不溶于盐
酸,说明生成的是硫酸钡沉淀,则说明溶液 M中一定含有硫酸钠,再加入酚酞,无明显现象,但由于实
验时加入了过量的稀盐酸,所以无法证明溶液 M 中是否含有氢氧化钠。即溶液 M中一定含有的溶质是
碳酸钠和硫酸钠。
【小问3详解】
可以另取适量溶液M于试管中,滴加酚酞,再加入足量的硝酸钡,硝酸钡溶液会与与M中的碳酸钠充分
反应后过滤,若溶液变红,且不退去,则原物质中含NaOH;若溶液变红后变为无色,则原物质中不含
NaOH
20. 氯化钾在工业、农业等方面有着重要的作用。
(1)验证性质
取氯化钾溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈______色;在氯化钾溶液中滴加硝酸银溶液,反
应的化学方程式是______。
(2)粗制氯化钾
氯化钾、氯化钠部分溶解度数据(g/100g水)
氯化钾、氯化钠部分溶解度数据(g/100g水)
温度(℃) 20 40 80 100
氯化钾 34.2 40.1 51.3 56.3
氯化钠 35.9 36.4 38.0 39.2
第9页/共13页
学科网(北京)股份有限公司以某种钾石盐(含氯化钾25%、氯化钠75%)为原料,粗制氯化钾的流程上图所示。实验室模拟上述流程,
最初投料时加入100g该钾石盐及50mL水,分析首次析出晶体X的组成及质量______。
(3)用途
氯化钾可作化肥,保存时需防止被雨淋的原因是______。
【答案】(1) ①. 紫 ②.
(2)氯化钾7.9g,氯化钠1.65g
(3)KCl的溶解度比较大,雨淋能使大量的KCl溶解流失
【解析】
【小问1详解】
取氯化钾溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈紫色,因为钾离子的颜色反应是紫色;
氯化钾和硝酸银反应生成硝酸钾和氯化银沉淀,反应的方程式为 ;
【小问2详解】
该钾石盐含氯化钾25%、氯化钠75%,故100g钾石盐中含有氯化钾 ,含有氯化钠
;
分析流程图:100℃时,氯化钾的溶解度为56.3g,氯化钠的溶解度为39.2g,故50mL水中最多溶解氯化钾
28.15g,最多溶解氯化钠19.6g,由于 ,氯化钾完全溶解,而 ,氯化钠有晶体析
第10页/共13页
学科网(北京)股份有限公司出,析出氯化钠的质量为 ;此时溶液中只溶解25g的氯化钾和19.6g的氯化钠;
冷却至20℃后,氯化钾的溶解度为34.2g,氯化钠的溶解度为35.9g,故50mL水中此时最多溶解氯化钾
17.1g,最多溶解氯化钠17.95g,由于 ,故氯化钾、氯化钠均有晶体析出,析
出质量为 ;
故首次析出晶体X为氯化钾7.9g,氯化钠1.65g;
【
小问3详解】
分析溶解度表格可知,KCl的溶解度比较大,雨淋能使大量的KCl溶解流失,故保存时需防止被雨淋。
21. 如图是实验室常用的气体发生装置。
(1)双氧水和二氧化锰混合制取氧气的化学方程式是______;反应的基本类型是______;收集氧气可以
用向上排气法,该方法所利用的氧气的物理性质是______。
的
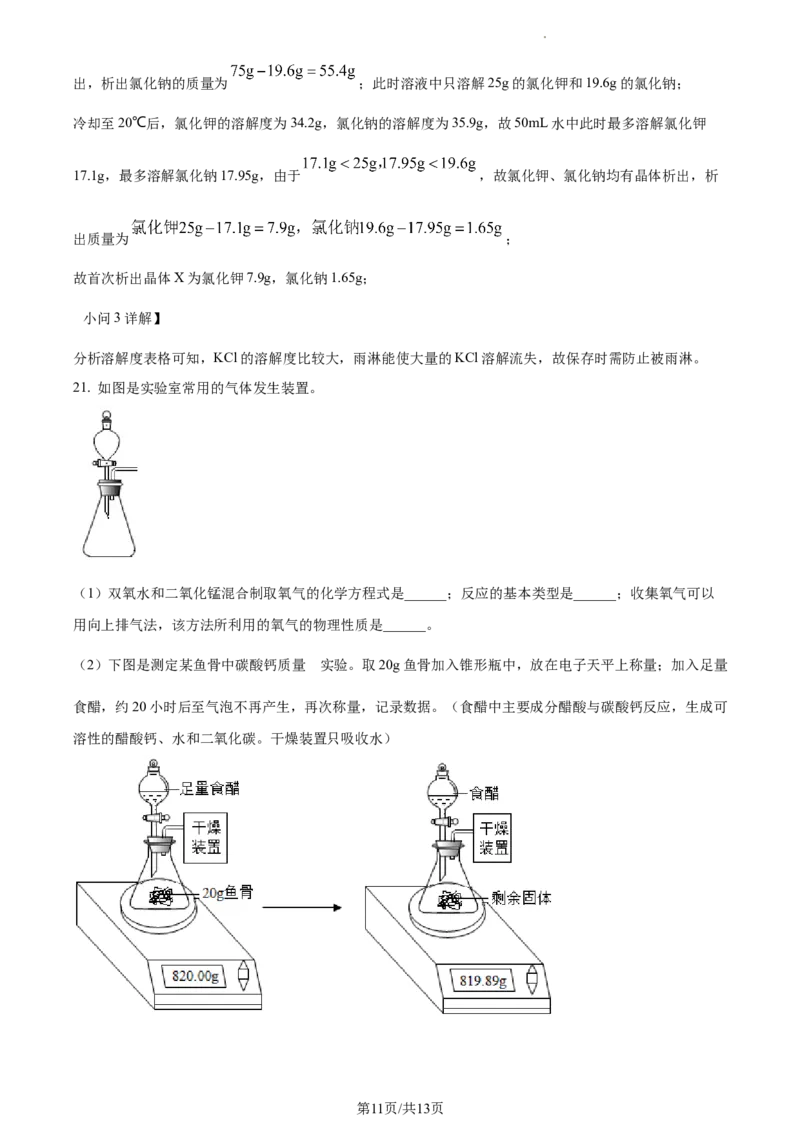
(2)下图是测定某鱼骨中碳酸钙质量 实验。取20g鱼骨加入锥形瓶中,放在电子天平上称量;加入足量
食醋,约20小时后至气泡不再产生,再次称量,记录数据。(食醋中主要成分醋酸与碳酸钙反应,生成可
溶性的醋酸钙、水和二氧化碳。干燥装置只吸收水)
第11页/共13页
学科网(北京)股份有限公司上述实验逸出的二氧化碳为0.11g,由该数据计算碳酸钙的物质的量为______mol。
(3)同学认为反应前锥形瓶中气体是空气,反应结束后瓶内气体是二氧化碳,因此鱼骨中实际所含碳酸
钙的质量______(选填“高于”或“低于”)实验所测得的值。
(4)服用食醋溶解卡在喉咙处鱼骨的方法是否可行并说明理由(写出一条即可)______。
【答案】(1) ①.
②. 分解反应 ③. 氧气的密度大于空气
(2)0.0025 (3)高于
(4)不可行;食醋与鱼骨反应缓慢。需要溶解的时间长(食醋中含醋酸的量比较低,需要大量的食醋)
【解析】
【
小问1详解】
双氧水在二氧化锰催化下生成氧气和水,化学方程式是 ,该反应由一种物质
生成两种物质,故反应基本类型为分解反应,收集氧气可以用向上排气法是利用氧气密度大于空气的物理
性质。
【小问2详解】
解:设碳酸钙质量为x
已知碳酸钙相对分子质量为100,质量为0.25g,物质的量等于质量与相对分子质量的比值,故相对分子质
量为0.0025mol。
【小问3详解】
由于二氧化碳密度大于空气,因此第二次称量的剩余固体质量数值偏大 (反应生成的二氧化碳不能完全溢
出瓶外),计算溢出的二氧化碳质量比实际产生的偏小,所以鱼骨中实际所含碳酸钙的质量高于实验所测得
的值。
【小问4详解】
不可行;食醋与鱼骨反应缓慢。需要溶解的时间长,或者由实验可知,食醋不能完全溶解鱼骨头。(其他答
案合理亦可)
第12页/共13页
学科网(北京)股份有限公司第13页/共13页
学科网(北京)股份有限公司