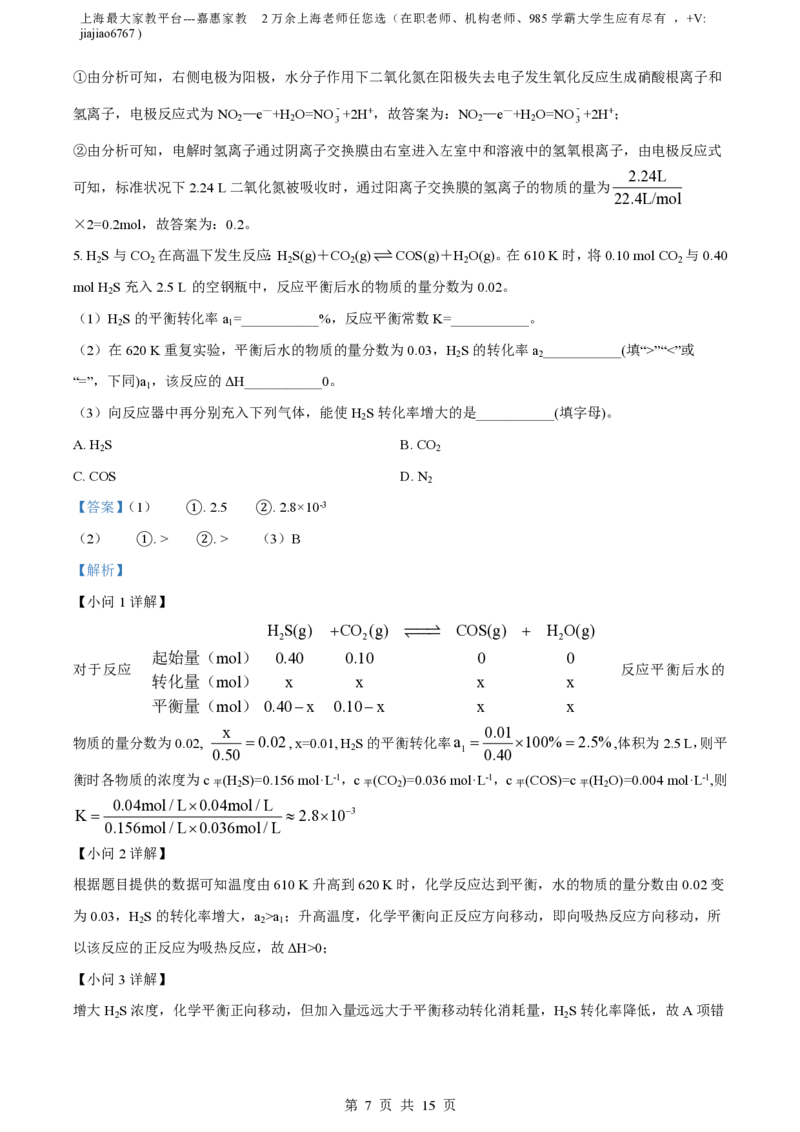文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
华东师大二附中 2023 学年高三 9 月考试卷
化学
(考试时间:60分钟 卷面满分:100分)
说明:题目标注“单选”即只有 1个正确选项,标注“不定项”即本题有 1或 2个正确选项。
可能用到的原子量:H-1 C-12 O-16 Cl-35.5 Ca-40
1. 海水中的卤素资源。地球是一颗蓝色星球,浩瀚的海洋覆盖了70%以上的地球表面,是蕴藏着极为丰富
化学资源的“聚宝盆”,其中氯化物含量很高,氯和同族的氟、溴、碘、砹总称为卤素。
(1)氯气是一种重要的化工原料,可用以下几种方法制取氯气。
a.实验室可用二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:___________。
b.工业上电解饱和食盐水制氯气,写出其反应的离子方程式:___________。
c.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为___________。
(2)将氯气分别通入含下列离子的溶液中,离子浓度减小的是___________。
A. SO2 B. HCO C. Mg2 D. Fe3
3 3
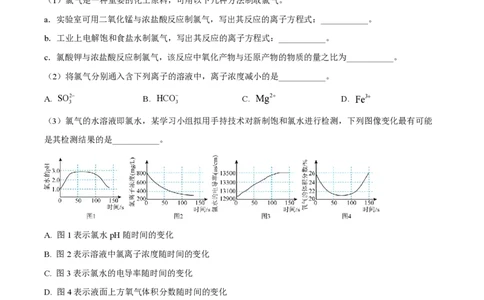
(3)氯气的水溶液即氯水,某学习小组拟用手持技术对新制饱和氯水进行检测,下列图像变化最有可能
是其检测结果的是___________。
A. 图1表示氯水pH随时间的变化
B. 图2表示溶液中氯离子浓度随时间的变化
C. 图3表示氯水的电导率随时间的变化
D. 图4表示液面上方氧气体积分数随时间的变化
Δ 电解
【答案】(1) ①. MnO +4H++2Cl— Mn2++Cl ↑+2H O ②. 2Cl—+2H O 2OH—+Cl ↑+H ↑
2 2 2 2 2 2
③. 5:1 (2)AB (3)C
【解析】
【小问1详解】
a.实验室用二氧化锰与浓盐酸反应制氯气的反应为二氧化锰与浓盐酸共热反应生成氯化锰、氯气和水,
第 1 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
Δ Δ
反应的离子方程式为MnO +4H++2Cl— Mn2++Cl ↑+2H O,故答案为:MnO +4H++2Cl—
2 2 2 2
Mn2++Cl ↑+2H O;
2 2
b.工业上电解饱和食盐水制氯气的反应为电解饱和食盐水生成氢氧化钠、氯气和氢气,反应的离子方程
电解 电解
式为2Cl—+2H O 2OH—+Cl ↑+H ↑,故答案为:2Cl—+2H O 2OH—+Cl ↑+H ↑;
2 2 2 2 2 2
c.氯酸钾与浓盐酸反应制氯气的反应为氯酸钾与浓盐酸反应生成氯化钾、氯气和水,反应的化学方程式
为KClO +6HCl(浓)=KCl+3Cl ↑+3H O,反应中氯酸钾中氯元素化合价降低被还原,氯酸钾是反应的氧化
3 2 2
剂,氯化氢中氯元素化合价部分升高被氧化,盐酸表现还原性和酸性,氯气是反应的氧化产物,也是还原
产物,则氧化产物与还原产物的物质的量之比为5:1,故答案为:5:1;
【小问2详解】
A.氯气与溶液中的亚硫酸根离子反应生成氯离子、硫酸根离子和水,则氯气通入溶液中,溶液中亚硫酸
根离子的浓度减小,故正确;
B.氯气与水反应生成盐酸和次氯酸,盐酸能与溶液中碳酸氢根离子反应生成二氧化碳和水,则氯气通入
溶液中,溶液中碳酸氢根离子浓度减小,故正确;
C.氯气与溶液中的镁离子不反应,氯气通入溶液中,溶液中镁离子浓度不变,故错误;
D.氯气与溶液中的铁离子不反应,氯气通入溶液中,溶液中铁离子浓度不变,故错误;
故选AB;
【小问3详解】
新制氯水中含有强酸盐酸和弱酸次氯酸,放置时,次氯酸不稳定,遇光分解生成盐酸和氧气,则新制氯水
中氢离子、氯离子浓度增大,溶液的导电性增强,液面上方氧气体积分数增大;
A.由分析可知,新制氯水放置时,溶液中氢离子浓度增大,溶液pH减小,则图1不能表示氯水pH随时
间的变化,故错误;
B.由分析可知,新制氯水放置时,溶液中氯离子浓度增大,则图2不能表示溶液中氯离子浓度随时间的
变化,故错误;
C.由分析可知,新制氯水放置时,溶液中离子浓度增大,导电性增强,则图3能表示氯水的电导率随时
间的变化,故正确;
D.由分析可知,新制氯水放置时,溶液液面上方氧气体积分数增大,则图4不能表示液面上方氧气体积
分数随时间的变化,故错误;
故选C。
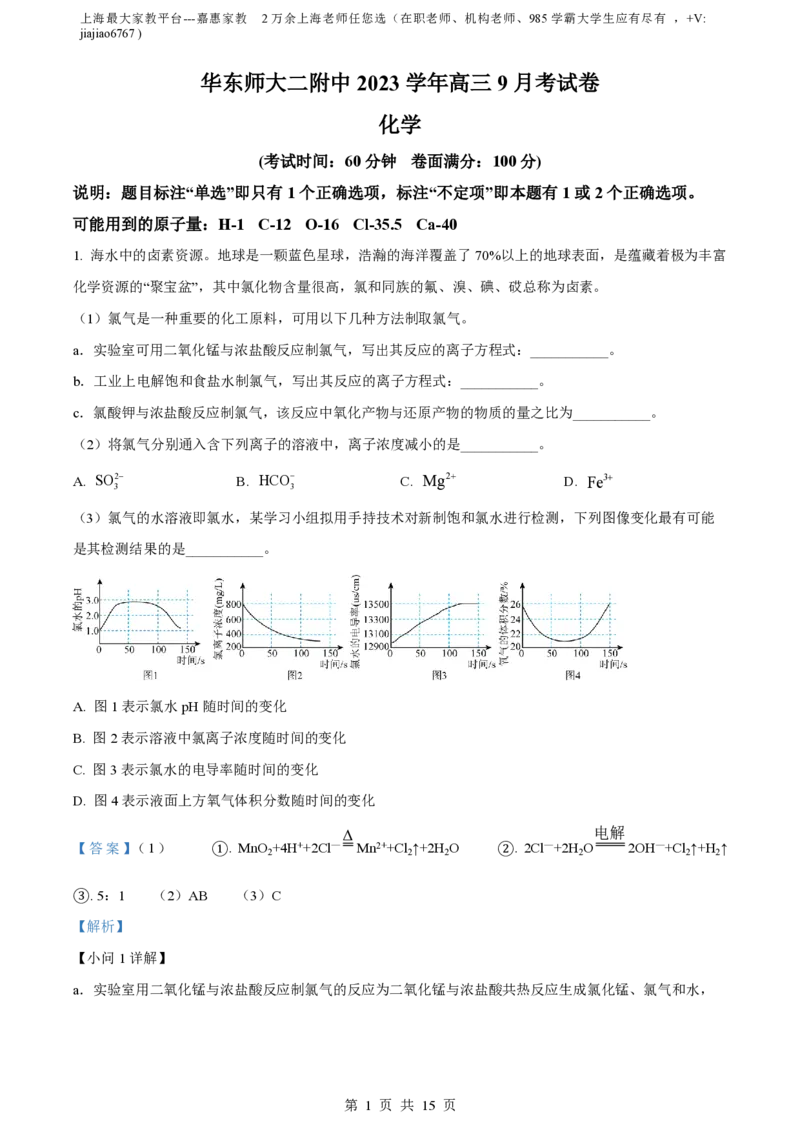
2. 含氯消毒剂在日常生产和生活中有着重要应用,某研究性学习小组利用下列装置制备漂白粉,并进行漂
第 2 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
白粉有效成分的质量分数的测定。
(1)装置④中的X试剂为___________。
(2)装置③中多孔陶瓷的作用是___________,漂白粉的有效成分是___________(用化学式表示)。
(3)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以
淀粉为指示剂,用0.1000 mol·L1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点,反应原理为:
3ClO I 3Cl IO,IO 5I 3H O6OH 3I ,实验测得数据如下表所示。
3 3 2 2
滴定次数 1 2 3
2000
KI溶液体积/mL 19.98 20.02 .
该漂白粉中有效成分的质量分数为___________;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止
滴定,则测定结果将___________(填“偏高”“偏低”或“无影响”)。
(4)卤化银因具有感光性,可用于制造感光材料。已知室温下,K AgCl1.81010,
sp
K AgI 8.51017,将AgCl与AgI的饱和溶液等体积混合,再加入足量浓AgNO 溶液,关于所生
sp 3
成的沉淀说法正确的是___________。
A. 只有AgI生成 B. AgCl和AgI等量生成
C AgCl沉淀少于AgI沉淀 D. AgCl沉淀多于AgI沉淀
.
【答案】(1)NaOH溶液
(2) ①. 增大氯气与石灰浆的接触面积,有利于氯气充分反应 ②. Ca(ClO)
2
(3) ①. 42.9% ②. 偏低 (4)D
【解析】
【分析】由实验装置图可知,装置①中高锰酸钾固体与浓盐酸共热反应制备氯气,浓盐酸具有挥发性,制
得的氯气中混有氯化氢,装置②中盛有的饱和食盐水用于除去氯化氢气体,装置③中氯气与石灰浆反应制
备漂白粉,装置④中盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气。
【小问1详解】
第 3 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
由分析可知,装置④中盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气,故答案为:NaOH溶
液;
【小问2详解】
由实验装置图可知,装置③中多孔陶瓷可以增大氯气与石灰浆的接触面积,有利于氯气与石灰浆充分反应
制备漂白粉,故答案为:增大氯气与石灰浆的接触面积,有利于氯气充分反应;
【小问3详解】
由题意可知,当溶液变蓝色时,漂白粉中的次氯酸钙完全反应,由题给数据可知,滴定消耗碘化钾溶液的
(19.98+20.00+20.02)mL
平均体积为 =20.00mL,则由方程式可知,漂白粉中有效成分的质量分数为
3
1
0.1000mol/L0.0200L3 143g/mol
2 ×100%=42.9%,若滴定过程中未充分振荡溶液局部变浅蓝色
1.000g
时就停止滴定,会使滴定消耗碘化钾的物质的量偏少导致测定结果偏低,故答案为:42.9%;偏低;
【小问4详解】
由氯化银的溶度积大于碘化银溶度积可知,氯化银饱和溶液中氯离子离子浓度大于碘化银的饱和溶液中碘
离子浓度,等体积混合后,向溶液中加入足量硝酸银溶液,溶液中氯离子浓度大于碘离子,则生成氯化银
沉淀的物质的量大于碘化银,故选D。
3. 自然界中的硫、氮循环。硫和氮两种元素与人们的生活密切相关,是生命物质的重要组成元素,自然界
中硫、氮的循环是维持生态平衡的重要物质基础。
(1)下列属于氮的固定的是___________(填序号)。
①工业上N 和H 合成NH ②N 和O 放电条件下生成NO
2 2 3 2 2
③NH 催化氧化生成NO ④汽车尾气中的NO和CO在催化剂作用下反应生成N
3 2
⑤氮气在豆科植物的根瘤菌所含的固氮酶作用下还原为氨
(2)热塑性聚氨酯(TPU)是具有高弹性,高拉伸强度,耐低温性,耐磨性和耐腐蚀能力的聚合物。一种基
于二硫键(-S-S-)的自修复热塑性聚氨酯材料的结构如下:
该聚合物由X( )和Y( )聚合而成,
下列说法正确的是___________。
第 4 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. X中碳氮双键比碳氧双键更容易与Y发生反应
B. 生成该聚合物的反应属于缩聚反应
C. 废弃的该聚合物若直接高温焚烧处理,可能会产生氮氧化物、硫氧化物等有毒气体
D. 该聚合物不能发生水解反应
【答案】(1)①②⑤ (2)AC
【解析】
【小问1详解】
氮的固定是指游离态氮元素转化为化合态氮元素;
①工业上N 和H 合成NH 属于氮的固定,故①正确;
2 2 3
②N 和O 放电条件下生成NO,属于氮的固定,故②正确;
2 2
③NH 催化氧化生成NO,是化合态氮元素之间的变化,不是氮的固定,故③错误;
3
④汽车尾气中的NO和CO在催化剂作用下反应生成N ,是化合态氮元素转化为游离态,不是氮的固定,
2
故④错误;
⑤氮气在豆科植物的根瘤菌所含的固氮酶作用下还原为氨,是氮的固定,故⑤正确;
故答案为:①②⑤;
【小问2详解】
A.根据生成物结构分析,X中碳氮双键比碳氧双键更容易与Y发生反应,故A正确;
B.生成该聚合物的反应属于加聚反应,不属于缩聚反应,故B错误;
C.废弃的该聚合物若直接高温焚烧处理,可能会产生氮氧化物、硫氧化物等有毒气体,污染环境,故C
正确;
D.该聚合物含酰胺基,一定条件下能发生水解反应,故D错误;
故答案为:AC。
4. 含硫、含氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用电解原理处理氮氧化
物、硫氧化物等废气,具有重要意义。
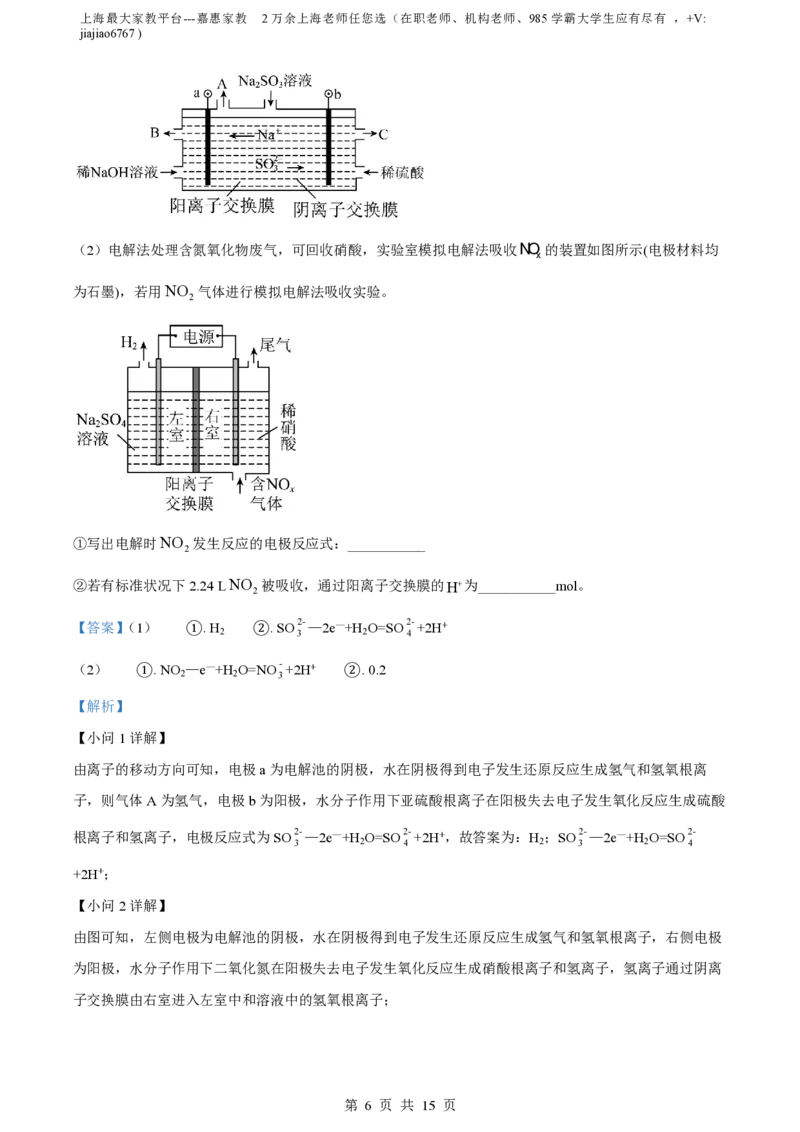
(1)用NaOH溶液吸收烟气中的SO ,将所得Na SO 溶液进行电解(电极材料均为石墨),可循环再生
2 2 3
NaOH,同时得到H SO ,其原理如下图所示,气体A为___________(填化学式),b极的电极反应式为
2 4
___________。
第 5 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(2)电解法处理含氮氧化物废气,可回收硝酸,实验室模拟电解法吸收NO的装置如图所示(电极材料均
x
为石墨),若用NO 气体进行模拟电解法吸收实验。
2
①写出电解时NO 发生反应的电极反应式:___________
2
②若有标准状况下2.24 LNO 被吸收,通过阳离子交换膜的H为___________mol。
2
【答案】(1) ①. H ②. SO2-—2e—+H O=SO2-+2H+
2 3 2 4
(2) ①. NO —e—+H O=NO-+2H+ ②. 0.2
2 2 3
【解析】
【小问1详解】
由离子的移动方向可知,电极a为电解池的阴极,水在阴极得到电子发生还原反应生成氢气和氢氧根离
子,则气体A为氢气,电极b为阳极,水分子作用下亚硫酸根离子在阳极失去电子发生氧化反应生成硫酸
根离子和氢离子,电极反应式为SO2-—2e—+H O=SO2-+2H+,故答案为:H ;SO2-—2e—+H O=SO2-
3 2 4 2 3 2 4
+2H+;
【小问2详解】
由图可知,左侧电极为电解池的阴极,水在阴极得到电子发生还原反应生成氢气和氢氧根离子,右侧电极
为阳极,水分子作用下二氧化氮在阳极失去电子发生氧化反应生成硝酸根离子和氢离子,氢离子通过阴离
子交换膜由右室进入左室中和溶液中的氢氧根离子;
第 6 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
①由分析可知,右侧电极为阳极,水分子作用下二氧化氮在阳极失去电子发生氧化反应生成硝酸根离子和
氢离子,电极反应式为NO —e—+H O=NO-+2H+,故答案为:NO —e—+H O=NO-+2H+;
2 2 3 2 2 3
②由分析可知,电解时氢离子通过阴离子交换膜由右室进入左室中和溶液中的氢氧根离子,由电极反应式
2.24L
可知,标准状况下2.24 L二氧化氮被吸收时,通过阳离子交换膜的氢离子的物质的量为
22.4L/mol
×2=0.2mol,故答案为:0.2。
5. H
2
S与CO
2
在高温下发生反应:H
2
S(g)+CO
2
(g)COS(g)+H
2
O(g)。在610 K时,将0.10 mol CO
2
与0.40
mol H S充入2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为0.02。
2
(1)H S的平衡转化率a =___________%,反应平衡常数K=___________。
2 1
(2)在620 K重复实验,平衡后水的物质的量分数为0.03,H S的转化率a ___________(填“>”“<”或
2 2
“=”,下同)a ,该反应的ΔH___________0。
1
(3)向反应器中再分别充入下列气体,能使H S转化率增大的是___________(填字母)。
2
A. H S B. CO
2 2
C. COS D. N
2
【答案】(1) ①. 2.5 ②. 2.8×10-3
(2) ①. > ②. > (3)B
【解析】
【小问1详解】
H S(g) CO (g) COS(g) H O(g)
2 2 2
起始量(mol) 0.40 0.10 0 0
对于反应 反应平衡后水的
转化量(mol) x x x x
平衡量(mol) 0.40x 0.10x x x
x 0.01
物质的量分数为0.02, 0.02, x=0.01, H S的平衡转化率a 100%2.5%,体积为2.5 L,则平
0.50 2 1 0.40
衡时各物质的浓度为c (H S)=0.156 mol·L-1,c (CO )=0.036 mol·L-1,c (COS)=c (H O)=0.004 mol·L-1,则
平 2 平 2 平 平 2
0.04mol/L0.04mol/L
K 2.8103
0.156mol/L0.036mol/L
【小问2详解】
根据题目提供的数据可知温度由610 K升高到620 K时,化学反应达到平衡,水的物质的量分数由0.02变
为0.03,H S的转化率增大,a >a ;升高温度,化学平衡向正反应方向移动,即向吸热反应方向移动,所
2 2 1
以该反应的正反应为吸热反应,故ΔH>0;
【小问3详解】
增大H S浓度,化学平衡正向移动,但加入量远远大于平衡移动转化消耗量,H S转化率降低,故A项错
2 2
第 7 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
误;增大CO 浓度,化学平衡正向移动,H S转化率增大,故B项正确;增大COS浓度,化学平衡逆向
2 2
移动,H S转化率降低,故C项错误;充入N ,反应混合物各物质浓度不变,不能使化学平衡发生移动,
2 2
H S转化率不变,故D项错误。
2
6. 生活中的铁。铁是地壳中含量最高的金属元素,铁及其化合物在人类文明进步和社会发展中起着至关重
要的作用。
(1)基态铁原子的价电子排布式为___________,基态铁原子中所含未成对电子有___________个。
(2)配合物FeCO 与NH 在一定条件下可合成一种具有磁性的铁氮化合物,FeCO 所含三种元素
5 3 5
的电负性由大到小的顺序是___________,NH 分子的立体构型为___________,1 mol FeCO 分子中
3 5
含有σ键为___________mol。
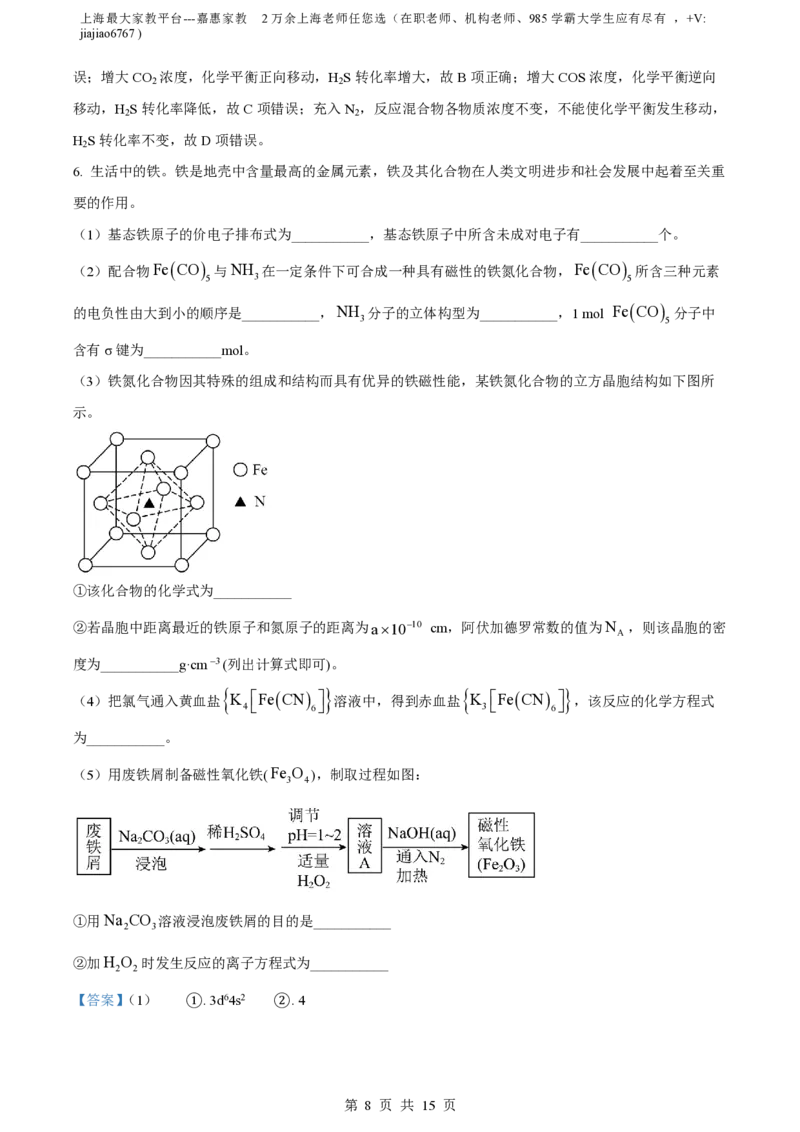
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结构如下图所
示。
①该化合物的化学式为___________
②若晶胞中距离最近的铁原子和氮原子的距离为a1010 cm,阿伏加德罗常数的值为N ,则该晶胞的密
A
度为___________g·cm3(列出计算式即可)。
(4)把氯气通入黄血盐 K
4
FeCN
6
溶液中,得到赤血盐 K
3
FeCN
6
,该反应的化学方程式
为___________。
(5)用废铁屑制备磁性氧化铁(Fe O ),制取过程如图:
3 4
①用Na CO 溶液浸泡废铁屑的目的是___________
2 3
②加H O 时发生反应的离子方程式为___________
2 2
【答案】(1) ①. 3d64s2 ②. 4
第 8 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(2) ①. O>C>Fe ②. 三角锥形 ③. 10
14564
(3) ①. Fe 4 N ②. N 2a10103
A
(4)Cl
2
+2K
4
FeCN
6
=2KCl+2K
3
FeCN
6
(5) ①. 除去废铁屑表面的油污 ②. H O 2Fe2 2H 2H O2Fe3
2 2 2
【解析】
【小问1详解】
Fe是26号元素,基态铁原子的价电子排布式为3d64s2;根据价电子排布式可知,基态铁原子中所含未成
对电子有4个;
【小问2详解】
非金属性越强,电负性越大,FeCO 所含三种元素的电负性由大到小的顺序是:O>C>Fe;NH 分子
5 3
513
中N原子的价层电子数为3 =4,有一个孤电子对,分子构型为三角锥形;FeCO 分子中,
2 5
Fe与C原子形成5个配位键,C原子与O原子间形成1个σ键,则1个FeCO
分子含有10个σ键,
5
则1 mol
FeCO
分子中含有σ键为10 mol;
5
【小问3详解】
1 1
①晶胞中,Fe原子个数为8 6 =4,N原子个数为1,则该化合物的化学式为Fe N;
8 2 4
②晶胞中距离最近的铁原子和氮原子的距离为晶胞边长的一半,则晶胞边长为2a1010cm,晶胞体积为
14564
g
14564
2a10103 cm3,晶胞质量为 g,则晶胞密度为 N A =
N
A 2a10103 cm3
14564
gcm-3
N
2a10103 ;
A
【小问4详解】
把氯气通入黄血盐 K
4
FeCN
6
溶液中,得到赤血盐 K
3
FeCN
6
,K
4
FeCN
6
中Fe元素
化合价为+2价,K FeCN 中Fe元素化合价为+3价,根据得失电子守恒配平得到化学方程式:
3
6
Cl 2 +2K 4 FeCN 6 =2KCl+2K 3 FeCN 6 ;
【小问5详解】
第 9 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
废铁屑表面含有油污,用Na CO 溶液浸泡废铁屑,可除去废铁屑表面的油污;加入稀硫酸,是废铁屑中
2 3
的铁转化为Fe2+;调节溶液pH,加入适量H O ,将Fe2+转化为Fe3+;加入NaOH溶液通入N 加热,最
2 2 2
终得到Fe O ;
3 4
①废铁屑表面含有油污,用Na CO 溶液浸泡废铁屑,可除去废铁屑表面的油污;
2 3
②加入适量H O ,将Fe2+转化为Fe3+,离子方程式为H O 2Fe2 2H 2H O2Fe3。
2 2 2 2 2
7. 有机合成在制药中的应用。现代有机合成不仅能制备自然界中存在的天然有机物,还能根据人类需求创
造自然界中不存在的新物质,满足医药、生命科学等领域的需求,对人类健康具有积极意义。
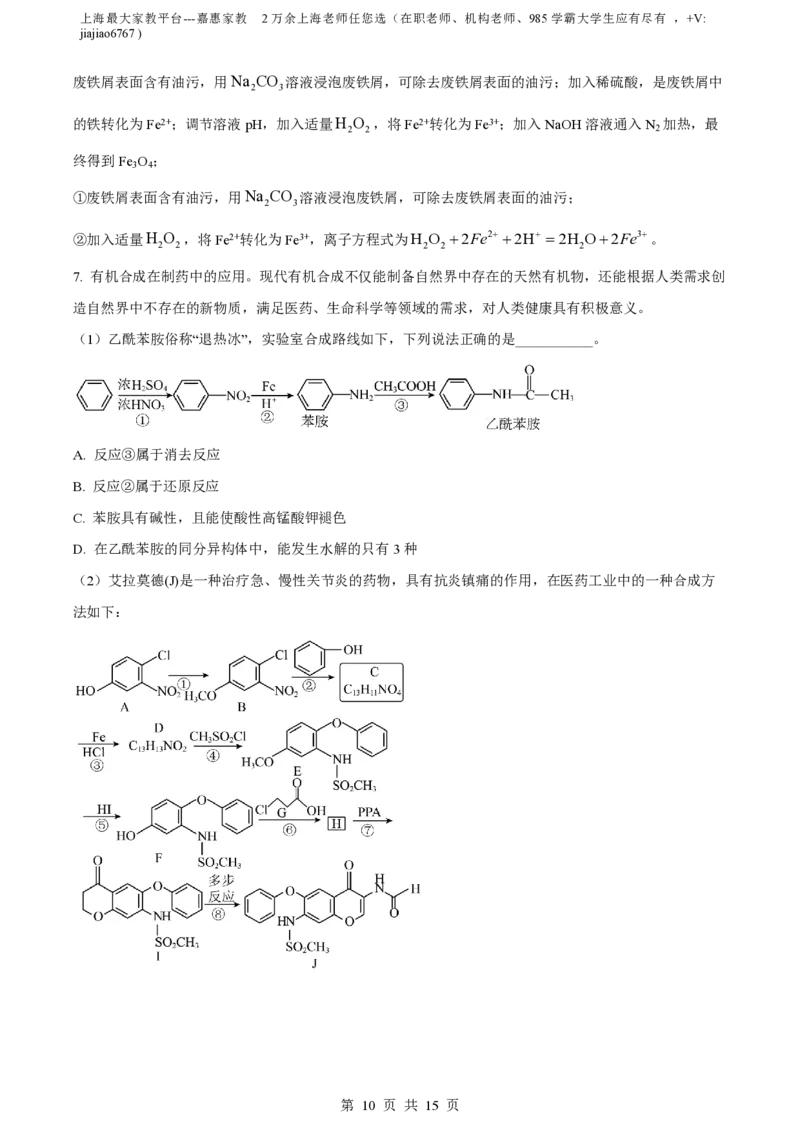
(1)乙酰苯胺俗称“退热冰”,实验室合成路线如下,下列说法正确的是___________。
A. 反应③属于消去反应
B. 反应②属于还原反应
C. 苯胺具有碱性,且能使酸性高锰酸钾褪色
D. 在乙酰苯胺的同分异构体中,能发生水解的只有3种
(2)艾拉莫德(J)是一种治疗急、慢性关节炎的药物,具有抗炎镇痛的作用,在医药工业中的一种合成方
法如下:
第 10 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
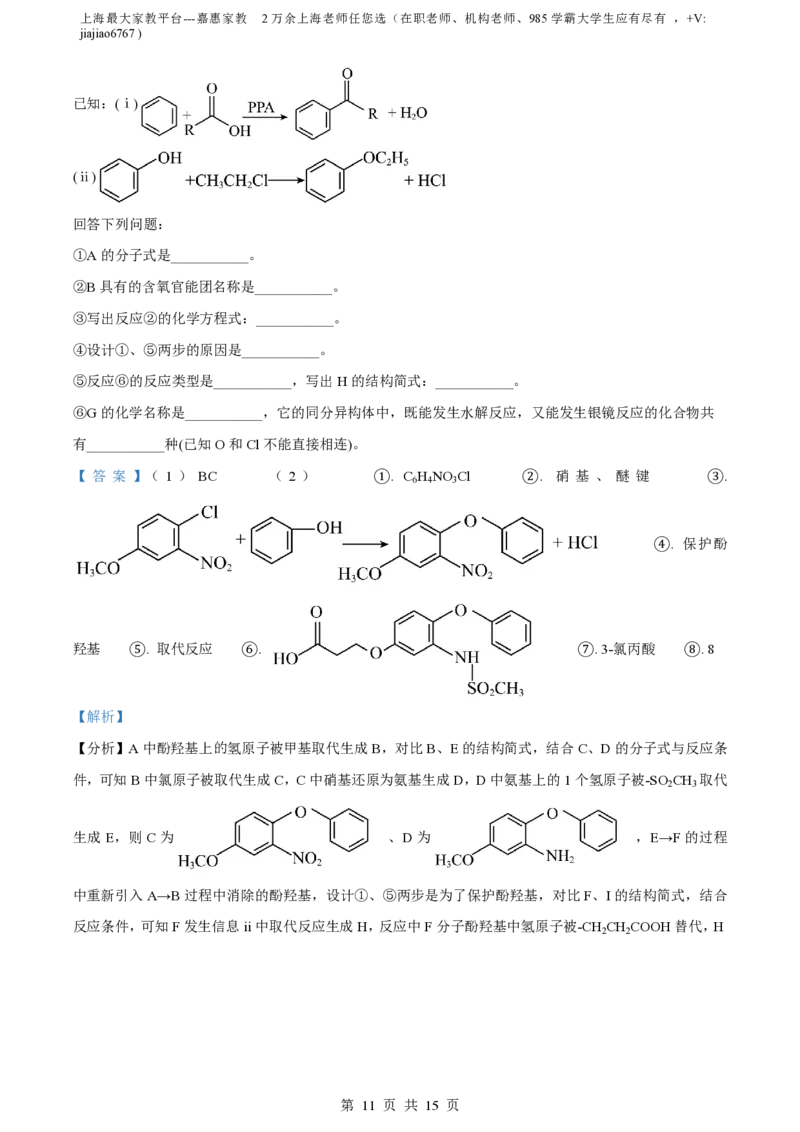
已知:(ⅰ)
(ⅱ)
回答下列问题:
①A的分子式是___________。
②B具有的含氧官能团名称是___________。
③写出反应②的化学方程式:___________。
④设计①、⑤两步的原因是___________。
⑤反应⑥的反应类型是___________,写出H的结构简式:___________。
⑥G的化学名称是___________,它的同分异构体中,既能发生水解反应,又能发生银镜反应的化合物共
有___________种(已知O和Cl不能直接相连)。
【 答 案 】( 1 ) BC ( 2 ) ①. C H NO Cl ②. 硝 基 、 醚 键 ③.
6 4 3
④. 保护酚
羟基 ⑤. 取代反应 ⑥. ⑦. 3-氯丙酸 ⑧. 8
【解析】
【分析】A中酚羟基上的氢原子被甲基取代生成B,对比B、E的结构简式,结合C、D的分子式与反应条
件,可知B中氯原子被取代生成C,C中硝基还原为氨基生成D,D中氨基上的1个氢原子被-SO CH 取代
2 3
生成E,则C为 、D为 ,E→F的过程
中重新引入A→B过程中消除的酚羟基,设计①、⑤两步是为了保护酚羟基,对比F、I的结构简式,结合
反应条件,可知F发生信息ii中取代反应生成H,反应中F分子酚羟基中氢原子被-CH CH COOH替代,H
2 2
第 11 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
发生信息i中取代反应形成环状生成I,可知H为 ,I多步
反应后引入-NHCHO生成J。
【小问1详解】
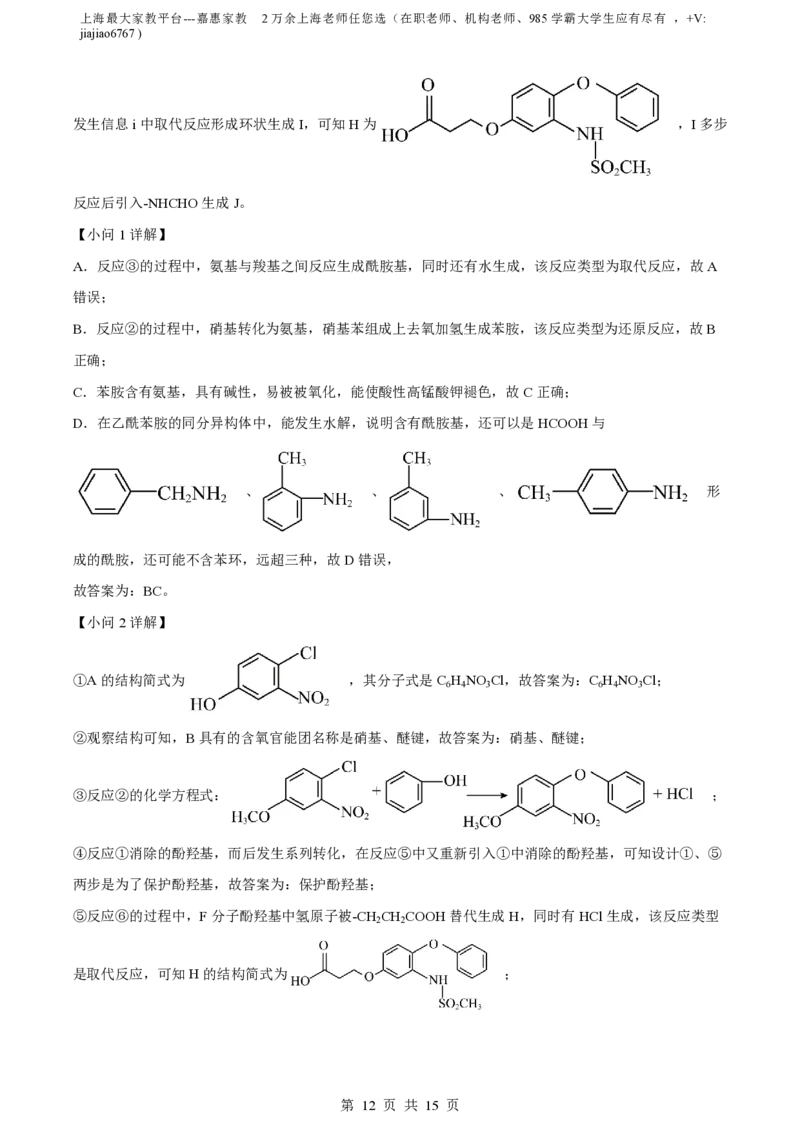
A.反应③的过程中,氨基与羧基之间反应生成酰胺基,同时还有水生成,该反应类型为取代反应,故A
错误;
B.反应②的过程中,硝基转化为氨基,硝基苯组成上去氧加氢生成苯胺,该反应类型为还原反应,故B
正确;
C.苯胺含有氨基,具有碱性,易被被氧化,能使酸性高锰酸钾褪色,故C正确;
D.在乙酰苯胺的同分异构体中,能发生水解,说明含有酰胺基,还可以是HCOOH与
、 、 、 形
成的酰胺,还可能不含苯环,远超三种,故D错误,
故答案为:BC。
【小问2详解】
①A的结构简式为 ,其分子式是C H NO Cl,故答案为:C H NO Cl;
6 4 3 6 4 3
②观察结构可知,B具有的含氧官能团名称是硝基、醚键,故答案为:硝基、醚键;
③反应②的化学方程式: ;
④反应①消除的酚羟基,而后发生系列转化,在反应⑤中又重新引入①中消除的酚羟基,可知设计①、⑤
两步是为了保护酚羟基,故答案为:保护酚羟基;
⑤反应⑥的过程中,F分子酚羟基中氢原子被-CH CH COOH替代生成H,同时有HCl生成,该反应类型
2 2
是取代反应,可知H的结构简式为 ;
第 12 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
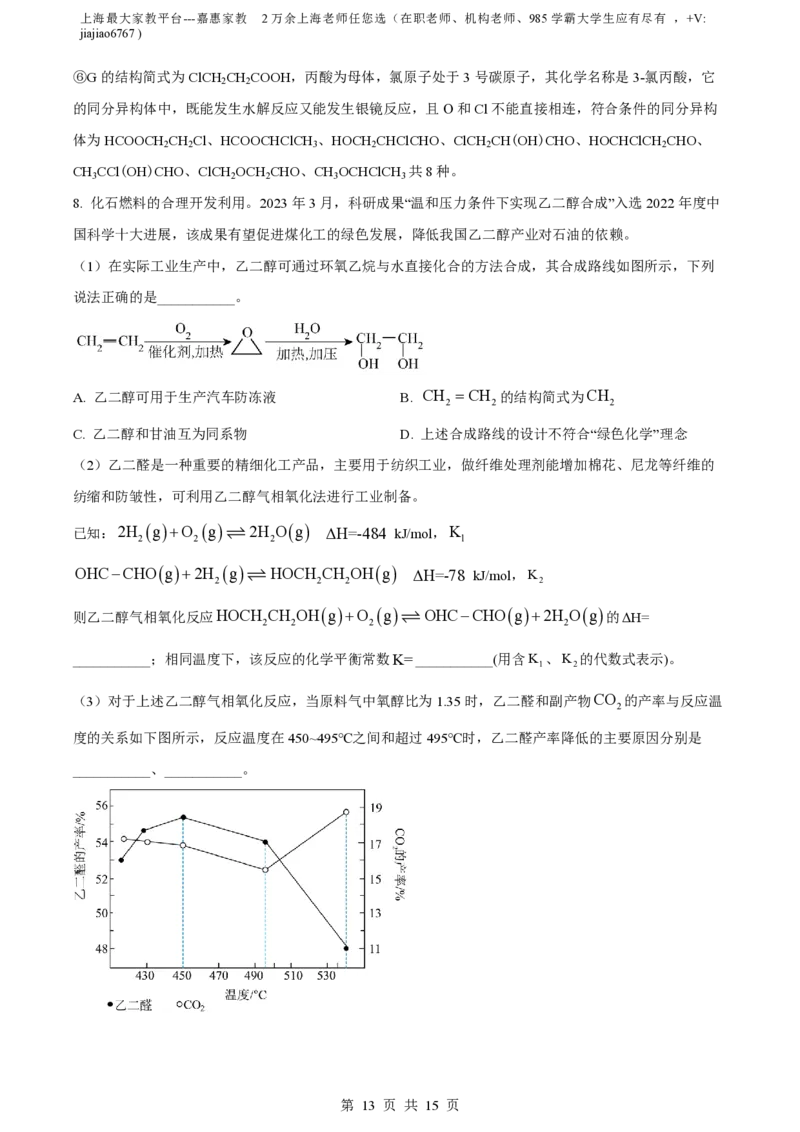
⑥G的结构简式为ClCH CH COOH,丙酸为母体,氯原子处于3号碳原子,其化学名称是3-氯丙酸,它
2 2
的同分异构体中,既能发生水解反应又能发生银镜反应,且О和Cl不能直接相连,符合条件的同分异构
体为HCOOCH CH Cl、HCOOCHClCH 、HOCH CHClCHO、ClCH CH(OH)CHO、HOCHClCH CHO、
2 2 3 2 2 2
CH CCl(OH)CHO、ClCH OCH CHO、CH OCHClCH 共8种。
3 2 2 3 3
8. 化石燃料的合理开发利用。2023年3月,科研成果“温和压力条件下实现乙二醇合成”入选2022年度中
国科学十大进展,该成果有望促进煤化工的绿色发展,降低我国乙二醇产业对石油的依赖。
(1)在实际工业生产中,乙二醇可通过环氧乙烷与水直接化合的方法合成,其合成路线如图所示,下列
说法正确的是___________。
A. 乙二醇可用于生产汽车防冻液 B. CH CH 的结构简式为CH
2 2 2
C. 乙二醇和甘油互为同系物 D. 上述合成路线的设计不符合“绿色化学”理念
(2)乙二醛是一种重要的精细化工产品,主要用于纺织工业,做纤维处理剂能增加棉花、尼龙等纤维的
纺缩和防皱性,可利用乙二醇气相氧化法进行工业制备。
已知:2H
2
gO
2
g
2H
2
Og ΔH=-484 kJ/mol,K
l
OHCCHOg2H 2 g HOCH 2 CH 2 OHg ΔH=-78 kJ/mol,K 2
则乙二醇气相氧化反应HOCH 2 CH 2 OHgO 2 g OHCCHOg2H 2 Og 的ΔH=
___________;相同温度下,该反应的化学平衡常数K=___________(用含K 、K 的代数式表示)。
1 2
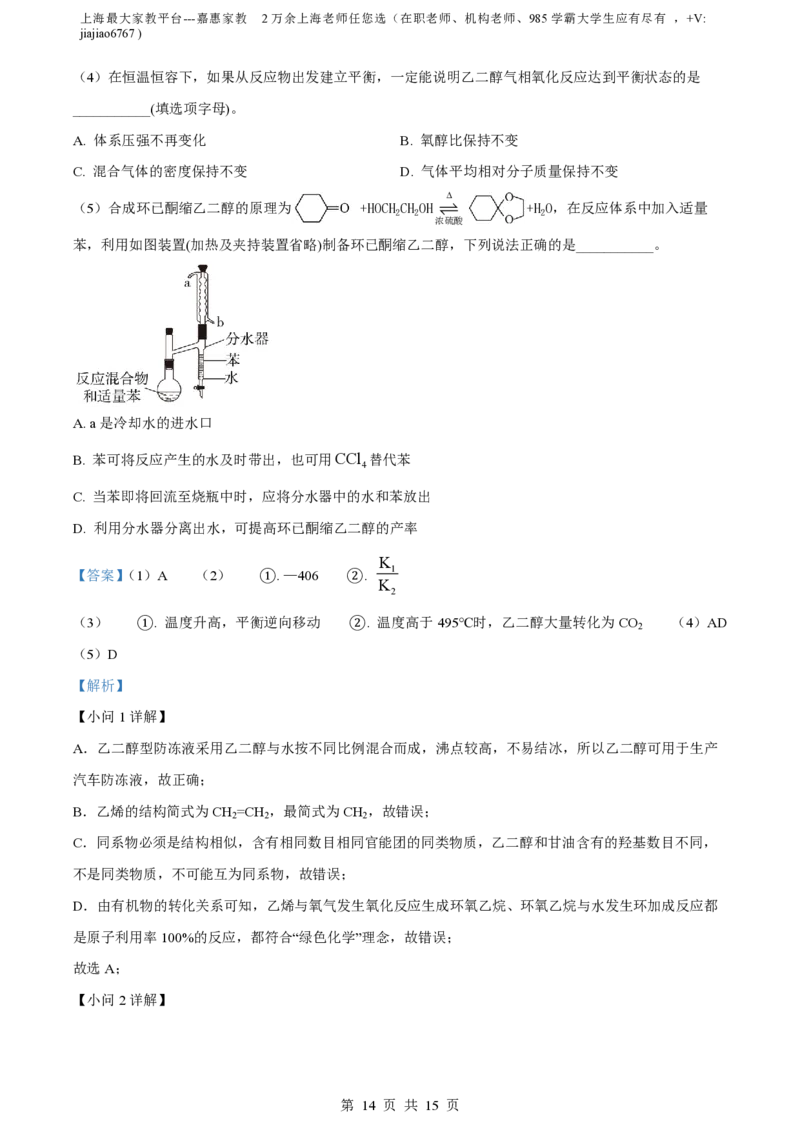
(3)对于上述乙二醇气相氧化反应,当原料气中氧醇比为1.35时,乙二醛和副产物CO 的产率与反应温
2
度的关系如下图所示,反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是
___________、___________。
第 13 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)在恒温恒容下,如果从反应物出发建立平衡,一定能说明乙二醇气相氧化反应达到平衡状态的是
___________(填选项字母)。
A. 体系压强不再变化 B. 氧醇比保持不变
C. 混合气体的密度保持不变 D. 气体平均相对分子质量保持不变
(5)合成环已酮缩乙二醇的原理为 +HOCH
2
CH
2
OH
+H
2
O,在反应体系中加入适量
浓硫酸
苯,利用如图装置(加热及夹持装置省略)制备环已酮缩乙二醇,下列说法正确的是___________。
A. a是冷却水的进水口
B. 苯可将反应产生的水及时带出,也可用CCl 替代苯
4
C. 当苯即将回流至烧瓶中时,应将分水器中的水和苯放出
D. 利用分水器分离出水,可提高环已酮缩乙二醇的产率
K
【答案】(1)A (2) ①. —406 ②. 1
K
2
(3) ①. 温度升高,平衡逆向移动 ②. 温度高于495℃时,乙二醇大量转化为CO (4)AD
2
(5)D
【解析】
【小问1详解】
A.乙二醇型防冻液采用乙二醇与水按不同比例混合而成,沸点较高,不易结冰,所以乙二醇可用于生产
汽车防冻液,故正确;
B.乙烯的结构简式为CH =CH ,最简式为CH ,故错误;
2 2 2
C.同系物必须是结构相似,含有相同数目相同官能团的同类物质,乙二醇和甘油含有的羟基数目不同,
不是同类物质,不可能互为同系物,故错误;
D.由有机物的转化关系可知,乙烯与氧气发生氧化反应生成环氧乙烷、环氧乙烷与水发生环加成反应都
是原子利用率100%的反应,都符合“绿色化学”理念,故错误;
故选A;
【小问2详解】
第 14 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
将已知反应依次编号为①②,由盖斯定律可知,反应①—②得到乙二醇气相氧化反应,则反应△H=(—
K K
484kJ/mol)—(—78kJ/mol)=—406 kJ/mol,反应的化学平衡常数K= 1 ,故答案为:—406; 1 ;
K K
2 2
【小问3详解】
乙二醇气相氧化反应为放热反应,升高温度,平衡向逆反应方向移动,所以50~495℃之间乙二醛产率降
低;由图可知,温度高于495℃时,乙二醇的产率减小,二氧化碳的产率增大说明乙二醇大量转化为副产
物二氧化碳导致乙二醛产率降低,故答案为:温度升高,平衡逆向移动;温度高于495℃时,乙二醇大量
转化为CO ;
2
【小问4详解】
A.该反应是气体体积减小的反应,反应中体系压强减小,则体系压强保持不变说明正逆反应速率相等,
反应已达到平衡,故正确;
B.由方程式可知,若起始氧醇比为1:1,反应中氧醇比始终为1:1,则氧醇比保持不变不能说明正逆反
应速率相等,无法判断反应是否达到平衡,故错误;
C.由质量守恒定律可知,反应前后气体的质量相等,在恒容密闭容器中混合气体的密度始终不变,则混
合气体的密度保持不变不能说明正逆反应速率相等,无法判断反应是否达到平衡,故错误;
D.由质量守恒定律可知,反应前后气体的质量相等,该反应是气体体积减小的反应,反应中气体平均相
对分子质量增大,则气体平均相对分子质量保持不变说明正逆反应速率相等,反应已达到平衡,故正确;
故选AD;
【小问5详解】
A.由实验装置图可知,下口b是冷却水的进水口,故错误;
B.四氯化碳的密度大于水,则用四氯化碳代替苯,不可能在分离水器中将反应产生的水及时带出,故错
误;
C.分水器中的苯回流烧瓶中可提高苯的利用率,当分水器中的水即将回流烧瓶中时,必须将分水器中的
水放出,故错误;
D.利用分水器分离出水可以减少生成物的浓度,有利于平衡平衡向正反应方向移动,提高环已酮缩乙二
醇的产率,故正确;
故选D。
第 15 页 共 15 页