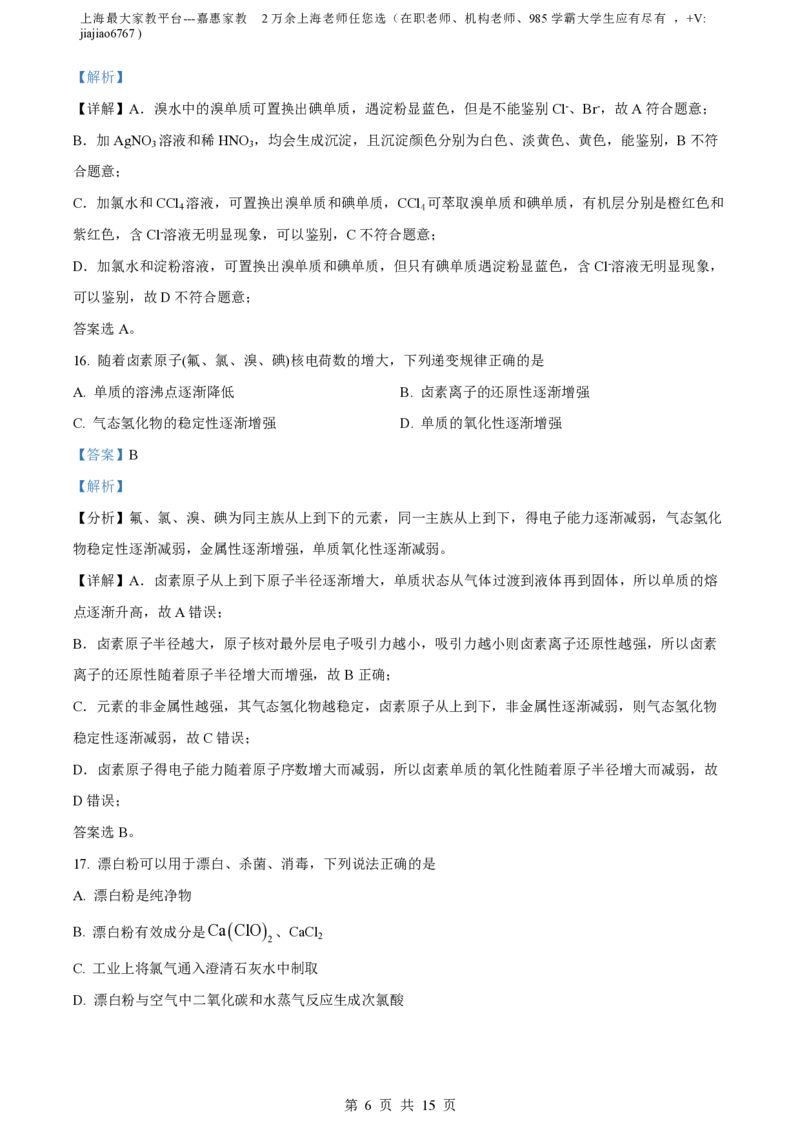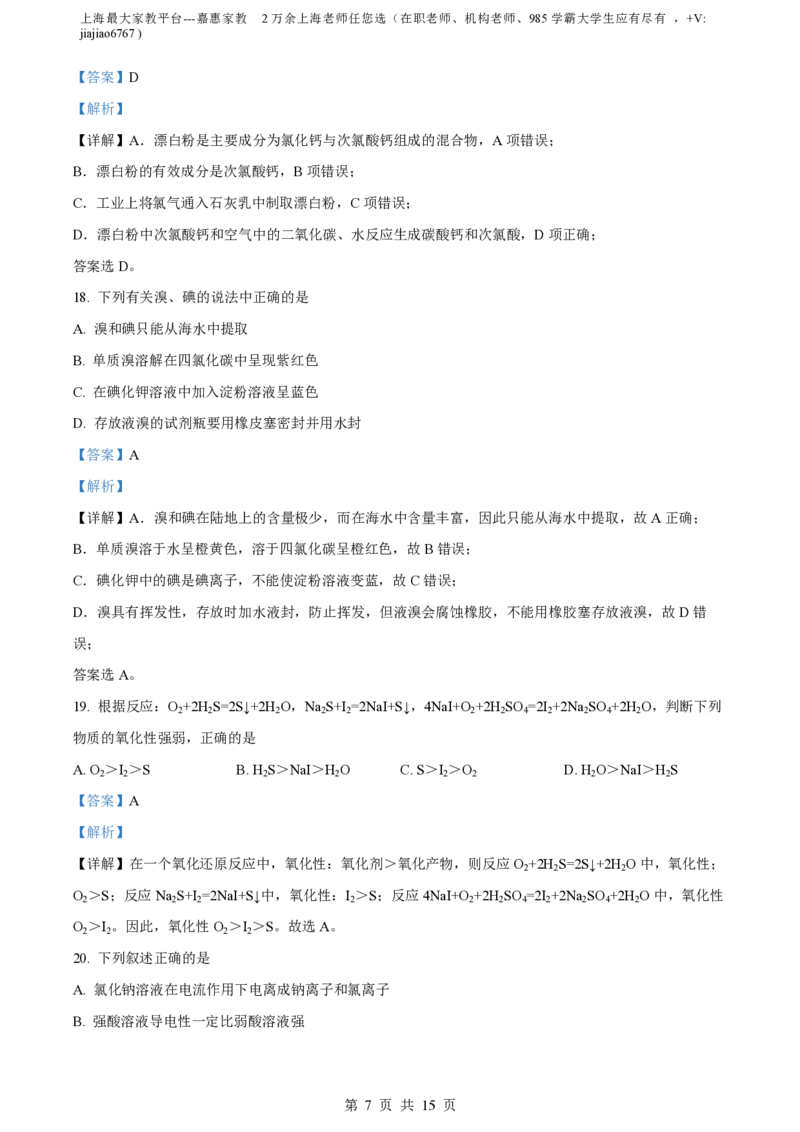文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市延安中学 2021 学年第一学期期末考试
高一年级化学试卷
(考试时间:60分钟 满分:100分)
相对原子质量:H-1 C-12 N-14 O-16 S-32 Br-80 Cl-35.5 Mn-55
一、选择题(本题共 50分,每小题 2分,每小题只有一个正确选项)
1. 下列物质中属于电解质的是
A. 氢氧化钡 B. 铜 C. 氯气 D. 二氧化碳
【答案】A
【解析】
【分析】在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物
为非电解质,无论电解质还是非电解质,都一定为化合物,单质和混合物既不是电解质,也不是非电解
质。
【详解】A.氢氧化钡在水溶液和熔融状态下都能够导电,且属于化合物,属于电解质,故A符合题意;
B.铜为单质,既不是电解质,也不是非电解质,故B不符合题意;
C.氯气为单质,既不是电解质,也不是非电解质,故C不符合题意;
D. 二氧化碳为化合物,但二氧化碳不能电离产生自由移动的离子,是非电解质,故D不符合题意;
答案选A。
2. 下列物质中,导电性能最差的是
A. 熔融NaOH B. 固态氯化钾 C. 盐酸 D. 石墨棒
【答案】B
【解析】
【详解】A.熔融NaOH中存在自由移动的钠离子和氢氧根离子,导电性好,故A不符合题意;
B.固态氯化钾中存在离子,但不能自由移动,不能导电,故B符合题意;
C.盐酸溶液中存在自由移动的氢离子和氯离子,导电性好,故C不符合题意;
D.石墨的层与层之间存在自由移动的电子,则石墨具有良好的导电性,故D不符合题意;
答案选B。
3. 下列物质在水溶液只能部分电离为离子的是
A. 硫酸 B. 硫酸铵 C. 次氯酸 D. 次氯酸钠
【答案】C
【解析】
第 1 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【详解】A.硫酸为强电解质,在溶液中完全电离成硫酸根离子和氢离子,故A不符合题意;
B.硫酸铵为强电解质,在溶液中完全电离成硫酸根离子和铵根离子,故B不符合题意;
C.次氯酸为弱酸,在溶液中部分电离出氢离子和次氯酸跟离子,故C符合题意;
D.次氯酸钠为强电解质,在溶液中完全电离成钠离子和次氯酸根离子,故D不符合题意;
答案选C。
4. 用准确称量的NaCl固体配制1.00mol/L的NaCl溶液时,一定用到的定量仪器是
A. 胶头滴管 B. 容量瓶 C. 分液漏斗 D. 试管
【答案】B
【解析】
【详解】用氯化钠固体配制1.00mol/L的NaCl溶液需要用到的玻璃仪器为烧杯、玻璃棒、容量瓶、胶头滴
管,其中容量瓶为定量仪器,故选B。
5. 在标准状况下,如果V升氨气中由n个原子,则阿伏加德罗常数为
A. Vn/22.4 B. 22.4n/V C. Vn/5.6 D. 5.6n/V
【答案】D
【解析】
V V
【详解】标准状况下,VL氨气的物质的量为n= = mol,每个NH 分子含有4个原子,故原子的
V 22.4 3
m
V V V 5.6n
物质的量为 mol4= mol,故n= mol×N ,解得N = mol-1,故选:D。
A A
22.4 5.6 5.6 V
6. 可以由两种单质直接化合得到的物质是
A. 硫化铜 B. 氯化亚铁 C. 硫化亚铁 D. 三氧化硫
【答案】C
【解析】
【详解】A.铜与硫单质反应生成Cu S,所以硫化铜不能由单质直接化合得到,故A不符合题意;
2
B.铁与氯气反应生成氯化铁,所以氯化亚铁不能通过单质直接化合得到,故B不符合题意;
C.铁与硫单质反应生成硫化亚铁,所以硫化亚铁能由单质直接化合得到,故C符合题意;
D.硫和氧气反应生成二氧化硫,二氧化硫和氧气在催化剂作用下可生成三氧化硫,三氧化硫不能由两种
单质直接化合得到,故D不符合题意;
答案选C。
7. 下列变化,必须加入适当的氧化剂才能完成的是
A. CuO→Cu B. Cl →HClO C. H SO →CuSO D. Fe→FeCl
2 2 4 4 2
第 2 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】D
【解析】
【分析】必须加入适当的氧化剂才能完成,则选项中应为还原剂发生的氧化反应,还原剂在反应的过程中
有元素的化合价升高。
【详解】A.CuO→Cu中,Cu元素的化合价降低,需加还原剂,故A不符合题意;
B. Cl →HClO中Cl元素的化合价升高,氯气与水反应生成HClO,反应中氯气既是氧化剂又是还原剂,
2
所以不需要加氧化剂也可实现,故B不符合题意;
C. H SO →CuSO 中没有元素的化合价发生变化,不需要加入氧化剂,故C不符合题意;;
2 4 4
D.Fe→FeCl 中,Fe元素化合价升高,被氧化,应加入氧化剂才能实现,故D符合题意;
2
答案选D。
8. 电影《长津湖》催人泪下,志愿军精神永存,观影时从放映室到银幕产生光柱,该现象下列哪种分散系
有关
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
【答案】B
【解析】
【详解】电影《长津湖》催人泪下,志愿军精神永存,观影时从放映室到银幕产生光柱,这是空气中的固
体小颗粒形成的胶体使光线发生散射作用的结果,故合理选项是B。
9. 下列电离方程式正确的是
A. CH COONH CH COO NH B. NaHCO Na H CO2
3 4 3 4 3 3
C. KAlSO 4 2 K Al3 SO2 4 D. H 2 S 2H S2
【答案】A
【解析】
【详解】A.醋酸铵是强电解质,在水中完全电离,电离方程式为:
CH COONH CH COO NH,故A正确;
3 4 3 4
B.碳酸氢钠是强电解质,在水中电离出钠离子和碳酸氢根离子,电离方程式为:NaHCO ═Na++HCO-,
3 3
故B错误;
C.电离方程式应遵循电荷守恒,电离方程式为:KAlSO K Al3 2SO2 ,故C错误;
4 2 4
D.H
2
S是二元弱酸,分两步电离,电离方程式为:H
2
S
H HS、HS
H S2,故D错误;
故选A。
第 3 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
10. 在氢硫酸溶液中加入少量下列物质:①O ,②Cl ,③SO ,④CuSO ,能使溶液酸性增强的是
2 2 2 4
A. ①③ B. ②④ C. ②③④ D. ①
【答案】B
【解析】
【详解】题给物质的有关化学方程式为①2H S+O =2S↓+2H O;②H S +Cl =2HCl+S↓;
2 2 2 2 2
③2H S+SO =3S↓+2H O;④H S+CuSO =CuS↓+H SO ,②和④加入后有强酸生成,故使溶液酸性增强,因
2 2 2 2 4 2 4
此符合题意的是②④;答案选B。
11. 下列反应中,属于离子反应的是
A. H 和O 的反应 B. 锌片投入稀硫酸中
2 2
C. KClO 和MnO 混合加热 D. NaOH溶液与K SO 溶液混合
3 2 2 4
【答案】B
【解析】
【分析】有离子参加的反应叫做离子反应,离子反应的条件:生成气体、沉淀、难电离的物质,具备条件
之一反应即可发生。
【详解】A.氢气和氧气反应生成水,没有离子参与反应,不属于离子反应,故A不符合题意;
B.锌片投入稀硫酸中会和硫酸电离的氢离子反应生成氢气,属于离子反应,故B符合题意;
C. 氯酸钾和二氧化锰在加热条件下生成氯化钾和氧气,反应中没有离子参加或生成,不属于离子反应,
故C不符合题意;
D.NaOH溶液与K SO 溶液混合不会发生反应,故D不符合题意;
2 4
答案选B。
12. 用化学方法鉴别氯化氢和氯气,不能选用的是
A. 湿润蓝色石蕊试纸 B. 湿润红色石蕊试纸
C. 湿润的淀粉KI试纸 D. 硝酸银溶液
【答案】D
【解析】
【详解】A.氯气可与水反应生成具有漂白性的次氯酸,可以使湿润的有色物质褪色,HCl不能使湿润的
蓝色石蕊试纸褪色,能鉴别,故A不选;
B.氯气能使湿润红色石蕊试纸褪色,通入HCl试纸不褪色,可以鉴别,故B不选;
C.氯气具有氧化性,可氧化碘离子生成单质碘,试纸变蓝,HCl无现象,可以鉴别,故C不选;
D.氯化氢通入硝酸银溶液中反应生成氯化银白色程沉淀,氯气通入也会和水反应生成氯化氢与硝酸银反
应生成白色沉淀,不能鉴别,故D选;
第 4 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故选:D。
13. 下列物质分类合理的是
A. 酸性氧化物:SO 、CO 、CO
2 2
B. 碱:烧碱、纯碱、氢氧化钾
C. 电解质:氨水、氢氧化钠、氧化钠
D. 混合物:矿泉水、纯牛奶、氢氧化铁胶体
【答案】D
【解析】
【详解】A. 与碱反应只生成盐和水的氧化物为酸性氧化物,CO与碱不反应,不是酸性氧化物,故A不
符合题意;
B.纯碱是碳酸钠,碳酸钠属于盐不是碱,故B不符合题意;
C.氨水为混合物,既不是电解质也不是非电解质,故C不符合题意;
D.矿泉水、纯牛奶、氢氧化铁胶体均是由两种或两种以上物质组成的,为混合物,故D符合题意;
答案选D。
14. 下列关于氯气的说法不正确的是( )
A. 氯气化学性质很活泼,但是干燥的液氯能用钢瓶贮存
B. 氯气和液氯是两种不同物质
C. 可以用浓硫酸除去氯气中的水蒸气
D. 氯气有毒,它曾在战争中被用于制造毒气弹
【答案】B
【解析】
【详解】A.在通常状况下,干燥的液氯与铁不反应,可以用钢瓶储运,故A正确;
B.氯气和液氯是同一种物质的不同状态,故B错误;
C.除去氯气中混有的水蒸气应选用不能和氯气反应的干燥剂,因为氯气气体呈酸性,不宜选用碱性干燥
剂,如碱石灰等,常选用酸性或中性干燥剂,如:浓硫酸、无水氯化钙等,故C正确;
D.氯气有毒,对人体有害,可以用于制造毒气弹应用于战争中,故D正确;
综上所述答案为B。
15. 鉴别Cl-、Br-、I-三种离子,不宜选用的试剂组是( )
A. 溴水和淀粉溶液 B. AgNO 溶液和稀HNO
3 3
C. 氯水和CCl 溶液 D. 氯水和淀粉溶液
4
【答案】A
第 5 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【详解】A.溴水中的溴单质可置换出碘单质,遇淀粉显蓝色,但是不能鉴别Cl-、Br-,故A符合题意;
B.加AgNO 溶液和稀HNO ,均会生成沉淀,且沉淀颜色分别为白色、淡黄色、黄色,能鉴别,B不符
3 3
合题意;
C.加氯水和CCl 溶液,可置换出溴单质和碘单质,CCl 可萃取溴单质和碘单质,有机层分别是橙红色和
4 4
紫红色,含Cl-溶液无明显现象,可以鉴别,C不符合题意;
D.加氯水和淀粉溶液,可置换出溴单质和碘单质,但只有碘单质遇淀粉显蓝色,含Cl-溶液无明显现象,
可以鉴别,故D不符合题意;
答案选A。
16. 随着卤素原子(氟、氯、溴、碘)核电荷数的增大,下列递变规律正确的是
A. 单质的溶沸点逐渐降低 B. 卤素离子的还原性逐渐增强
C. 气态氢化物的稳定性逐渐增强 D. 单质的氧化性逐渐增强
【答案】B
【解析】
【分析】氟、氯、溴、碘为同主族从上到下的元素,同一主族从上到下,得电子能力逐渐减弱,气态氢化
物稳定性逐渐减弱,金属性逐渐增强,单质氧化性逐渐减弱。
【详解】A.卤素原子从上到下原子半径逐渐增大,单质状态从气体过渡到液体再到固体,所以单质的熔
点逐渐升高,故A错误;
B.卤素原子半径越大,原子核对最外层电子吸引力越小,吸引力越小则卤素离子还原性越强,所以卤素
离子的还原性随着原子半径增大而增强,故B正确;
C.元素的非金属性越强,其气态氢化物越稳定,卤素原子从上到下,非金属性逐渐减弱,则气态氢化物
稳定性逐渐减弱,故C错误;
D.卤素原子得电子能力随着原子序数增大而减弱,所以卤素单质的氧化性随着原子半径增大而减弱,故
D错误;
答案选B。
17. 漂白粉可以用于漂白、杀菌、消毒,下列说法正确的是
A. 漂白粉是纯净物
B.
漂白粉有效成分是CaClO
、CaCl
2 2
C. 工业上将氯气通入澄清石灰水中制取
D. 漂白粉与空气中二氧化碳和水蒸气反应生成次氯酸
第 6 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】D
【解析】
【详解】A.漂白粉是主要成分为氯化钙与次氯酸钙组成的混合物,A项错误;
B.漂白粉的有效成分是次氯酸钙,B项错误;
C.工业上将氯气通入石灰乳中制取漂白粉,C项错误;
D.漂白粉中次氯酸钙和空气中的二氧化碳、水反应生成碳酸钙和次氯酸,D项正确;
答案选D。
18. 下列有关溴、碘的说法中正确的是
A. 溴和碘只能从海水中提取
B. 单质溴溶解在四氯化碳中呈现紫红色
C. 在碘化钾溶液中加入淀粉溶液呈蓝色
D. 存放液溴的试剂瓶要用橡皮塞密封并用水封
【答案】A
【解析】
【详解】A.溴和碘在陆地上的含量极少,而在海水中含量丰富,因此只能从海水中提取,故A正确;
B.单质溴溶于水呈橙黄色,溶于四氯化碳呈橙红色,故B错误;
C.碘化钾中的碘是碘离子,不能使淀粉溶液变蓝,故C错误;
D.溴具有挥发性,存放时加水液封,防止挥发,但液溴会腐蚀橡胶,不能用橡胶塞存放液溴,故D错
误;
答案选A。
19. 根据反应:O +2H S=2S↓+2H O,Na S+I =2NaI+S↓,4NaI+O +2H SO =2I +2Na SO +2H O,判断下列
2 2 2 2 2 2 2 4 2 2 4 2
物质的氧化性强弱,正确的是
A. O >I >S B. H S>NaI>H O C. S>I >O D. H O>NaI>H S
2 2 2 2 2 2 2 2
【答案】A
【解析】
【详解】在一个氧化还原反应中,氧化性:氧化剂>氧化产物,则反应O +2H S=2S↓+2H O中,氧化性;
2 2 2
O >S;反应Na S+I =2NaI+S↓中,氧化性:I >S;反应4NaI+O +2H SO =2I +2Na SO +2H O中,氧化性
2 2 2 2 2 2 4 2 2 4 2
O >I 。因此,氧化性O >I >S。故选A。
2 2 2 2
20. 下列叙述正确的是
A. 氯化钠溶液在电流作用下电离成钠离子和氯离子
B. 强酸溶液导电性一定比弱酸溶液强
第 7 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 溶于水后能电离出氢离子的化合物都是酸
D. 硫酸钡难溶于水,属于强电解质
【答案】D
【解析】
【详解】A.氯化钠在水分子的作用下电离成钠离子和氯离子,无须通电,故A错误;
B.导电能力取决于溶液中离子浓度大小和所带电荷的多少,与电解质强弱无关,故B错误;
C.溶于水后能电离出氢离子的化合物不一定是酸,如NaHSO 在水中电离出钠离子、氢离子、硫酸根离
4
子,但NaHSO 不是酸,故C错误;
4
D.硫酸钡难溶于水,但溶解的部分完全电离,属于强电解质,故D正确;
答案选D。
21. 下列离子方程式中,正确的是
A. 向氯化亚铁溶液中通入氯气:Fe2 Cl Fe3 2Cl
2
通直流电
B. 电解饱和食盐水:2Cl-+2HO H↑+Cl ↑+2OH-
2 2 2
C. 碳酸氢钠溶液跟稀盐酸反应:NaHCO H Na H OCO
3 2 2
D. 盐酸滴在石灰石上:2H CO2 CO H O
3 2 2
【答案】B
【解析】
【详解】A.离子方程式两边电荷不守恒,正确的离子方程式为:2Fe2 Cl 2Fe3 2Cl,故A错
2
误;
通电
B.电解饱和食盐水生成氢氧化钠、氢气和氯气,离子方程式为:2Cl-+2HO H↑+Cl ↑+2OH- ,
2 2 2
故B正确;
C.碳酸氢钠应拆写成离子形式,正确的离子方程式为:HCO H H OCO ,故C错误;
3 2 2
D.碳酸钙难溶,应写化学式,正确的离子方程式为:2H CaCO =Ca2 CO H O,故D错
3 2 2
误;
答案选B。
22. 相同条件下,下列各组中分子数相同的是
第 8 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 14 gN 与32 gNO B. 34 gNH 与4 gH
2 2 3 2
C. 2 LCO 与2 L H O D. 11.2 L CO与0.5 molO
2 2 2
【答案】B
【解析】
【详解】根据NnN ,可知分子物质的量相同时,分子数一定相同。
A
m 14g
A.14 gN 的物质的量为n= = =0.5mol,32 g NO 的物质的量为mol
2 M 28g/mol 2
m 32g
n= = 1.01mol,二者物质的量不同,分子数一定不同,故A不符合题意;
M 30g/mol
m 34g m 4g
B.34 g NH 的物质的量为n= = =2mol,4 gH 的物质的量为n= = =2mol,二
3 M 17g/mol 2 M 2g/mol
者物质的量相同,分子数一定相同,故B符合题意;
C.未指明二氧化碳和水所处的状态,不能计算两者物质的量,不能确定两者分子数是否相等,故C不符
合题意;
D.未说明CO处于标准状况,11.2 L CO的物质的量不一定为0.5 mol,11.2 L CO与0.5 mol O 分子数不
2
一定相同,故D不符合题意;
答案选B。
23. 实验室用下列两种方法制氯气:①用含146 g HCl的浓盐酸与足量的MnO 反应,②用87 gMnO 与
2 2
足量浓盐酸反应。所得的氯气
A. ①比②多 B. ②比①多 C. 一样多 D. 无法比较
【答案】B
【解析】
【详解】浓盐酸与MnO 反应的方程式是MnO 4HCl(浓)==MnCl Cl 2H O,稀盐酸和MnO
2 2
2 2 2 2
m 146g
不反应,①用含146 g HCl即物质的量n= = =4mol的浓盐酸与足量的MnO 反应,HCl不能
M 36.5g/mol 2
完全反应,参加反应的 HCl 小于 4mol,放出氯气的物质的量小于 1 mol;②用 87 g MnO 即物质的量
2
m 87g
n= = =1mol与足量浓盐酸反应,MnO 能完全反应,生成氯气的物质的量1 mol,得到的氯气
M 87g/mol 2
第 9 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
②比①多,故选B。
24. 将100 mL 0.30 mol·L-1的Na SO 溶液和50 mL 0.20 mol·L-1的Al (SO ) 溶液混合后,所得溶液中
2 4 2 4 3
SO2-的物质的量浓度为
4
A. 0.40 mol·L-1 B. 0.25 mol·L-1
C. 0.50 mol·L-1 D. 0.20 mol·L-1
【答案】A
【解析】
【详解】将100 mL 0.30 mol·L-1的Na SO 溶液和50 mL 0.20 mol·L-1的Al (SO ) 溶液混合后,所得溶液
2 4 2 4 3
0.1L0.3mol/L+0.05L0.2mol/L3
中SO2-的物质的量浓度为 0.4mol/L,故选A。
4 0.1L+0.05L
25. 某温度下,将Cl 通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO 的混合溶液,经测定ClO-
2 3
与ClO -的物质的量之比是1∶2,则Cl 与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量
3 2
之比为
A. 2∶3 B. 4∶3 C. 10∶3 D. 11∶3
【答案】D
【解析】
【详解】Cl 生成ClO﹣与ClO -是被氧化的过程,化合价分别由0价升高为+1价和+5价,经测定ClO﹣与ClO -
2 3 3
物质的量之比为 1:2,则可设 ClO﹣为 1mol,ClO -为 2mol,被氧化的氯元素的物质的量为:
3
1mol+2mol=3mol,根据化合价变化可知,反应中失去电子的总物质的量为:1mol×(1-0)+2mol×(5-0)=11mol;
氧化还原反应中得失电子数目一定相等,则该反应中失去电子的物质的量也是11mol;
Cl 生成KCl是被还原的过程,化合价由0价降低为-1价,则被还原的氯元素的物质的量为:
2
11mol
11mol;
10
所以被还原的氯元素和被氧化的氯元素的物质的量之比为11mol:3mol=11:3,答案选D。
二、实验题
26. 化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合如下
实验装置图回答下列问题:
第 10 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(1)实验③的操作名称是_______,操作②中搅拌的作用是_______;
(2)实验时仪器b中冷却水的进水口为_______(填“f或“g”);
(3)从氯化钾溶液中得到氯化钾固体,选择装置_______(填装置图编号,下同);
(4)分离CCl 和水选择装置_______,该操作方法的名称为_______;
4
(5)某同学使用实验⑨中的仪器,从碘水中提取碘,主要操作步骤如图:
①仪器e的名称_______;
②通过仔细观察各步实验操作该同学所采用的萃取剂可能是_______(填编号);
A.酒精 B.苯 C.四氯化碳 D.水
③甲、乙、丙三步实验操作中,不正确的是_______(填“甲”、“乙”或“丙”);
④在乙图的仪器e中,下层液体呈_______色。
【答案】(1) ①. 蒸馏 ②. 加快蒸发速度并防止液体局部过热,发生飞溅
(2)g (3)②
(4) ① ④ ②. 分液
.
(5) ①. 分液漏斗 ②. C ③. 丙 ④. 紫
【解析】
【小问1详解】
实验③中用到的仪器有蒸馏烧瓶、酒精灯、锥形瓶和冷凝管,因此该操作是蒸馏;操作②是蒸发结晶,蒸
发结晶过程中用玻璃棒搅拌可以加快蒸发速度并防止液体局部过热,发生飞溅;
【小问2详解】
仪器b为冷凝管,为了使冷凝更充分,冷却水应从g口进入;
【小问3详解】
第 11 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
从氯化钾溶液中得到氯化钾固体应采用蒸发结晶的方法,因此应选用装置②;
【小问4详解】
CCl 和水互不相溶且分层,应采用分液的方法进行分离,即选择装置④进行分液将两者分离;
4
【小问5详解】
①由图可知,仪器e为分液漏斗;
②萃取剂与水互不相溶,溶质I 在萃取剂中溶解度应比在水中大,且溶质I 与萃取剂不能发生反应,由图
2 2
可知,静置后碘在下层,则萃取剂的密度比水大,在题目已知物质中只有四氯化碳符合要求,故答案选
C;
③分液时为了避免上、下两层液体混合,应将下层液体从下口放出后再将上层液体从上口倒出,且倾倒时
分液漏斗应紧靠烧杯,使液体沿着烧杯内壁流下,由图可知丙操作不合理;
④在乙图的分液漏斗中,下层液体是I 的四氯化碳溶液,呈紫色。
2
三、填空题
27. 已知实验室也可以用氯酸钾与浓盐酸反应制氯气,其反应为:KCl O+6HCl 浓=KCl +3Cl ↑+3HO。
3 2 2
回答下列问题:
(1)反应中的氧化剂是_______,被氧化的元素是_______;
(2)用单线桥法标出电子转移的方向和数目_______;
(3)反应中HCl所表现出来的特性是_______(填序号);
A氧化性B.还原性C.酸性
(4)当反应中转移0.75mol电子时,标准状况下产生的气体体积为_______L(保留两位小数)。
【答案】(1) ① KClO ②. Cl
. 3
(2) (3)BC
(4)10.08
【解析】
【分析】根据反应KCl O+6HCl 浓=KCl +3Cl ↑+3HO可以看出,该氧化还原反应中,若有3molCl 生
3 2 2 2
成,则有lmolKClO 中Cl元素化合价降低为0价,6molHCl中有5mol氯元素化合价升高为0价,
3
1molHCl起酸性作用生成KCl,即作还原剂的浓盐酸为5mol。
【小问1详解】
根据分析,反应中的氧化剂为KClO ,被氧化的元素是HCl中的Cl。
3
第 12 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【小问2详解】
氯酸钾中的氯由+5价降低到0价,氯化氢中的氯由-1价升高到0价,其单线桥为:
;
【小问3详解】
反应中6molHCl中有5mol氯元素化合价升高为0价,1molHCl起酸性作用生成KCl,故表现还原性和酸
性。
【小问4详解】
由反应中每生成3mol氯气转移5mol电子可知,转移0.75mol电子时,生成氯气0.45mol,标准状况下产
生的气体体积为22.4L×0.45mol=10.08L。
28. 现有下列八种物质:①稀硫酸②蔗糖③冰醋酸④氢氧化钡固体⑤氨水⑥汞⑦氯化氢⑧二氧化硫
(1)属于电解质的有_______(填序号);属于非电解质的有_______(填序号);能导电的物质有_______(填
序号);
(2)上述八种物质中有两种物质在水溶液中,可发生离子反应:H OH H O,该离子反应对应的
2
化学方程式为_______。
【答案】(1) ①. ③④⑦ ②. ②⑧ ③. ①⑤⑥
(2)2HCl+Ba(OH) =BaCl +2H O
2 2 2
【解析】
【小问1详解】
①稀硫酸导电,为混合物,既不是电解质也不是非电解质;②蔗糖溶于水和熔融态都不导电,为非电解
质;③冰醋酸溶于水导电,为电解质;④氢氧化钡固体溶于水导电,为电解质;⑤氨水导电,为混合物,
既不是电解质也不是非电解质;⑥汞导电,为单质,既不是电解质也不是非电解质;⑦氯化氢溶于水导
电,为电解质;⑧二氧化硫溶于水导电,但是不是本身电离产生的,为非电解质。故属于电解质的为
③④⑦;属于非电解质的为②⑧;能导电的物质为①⑤⑥。
【小问2详解】
可发生离子反应H OH H O的为强酸和强碱反应生成水和可溶性盐,故符合条件的为
2
2HCl+Ba(OH) =BaCl +2H O。
2 2 2
四、实验题
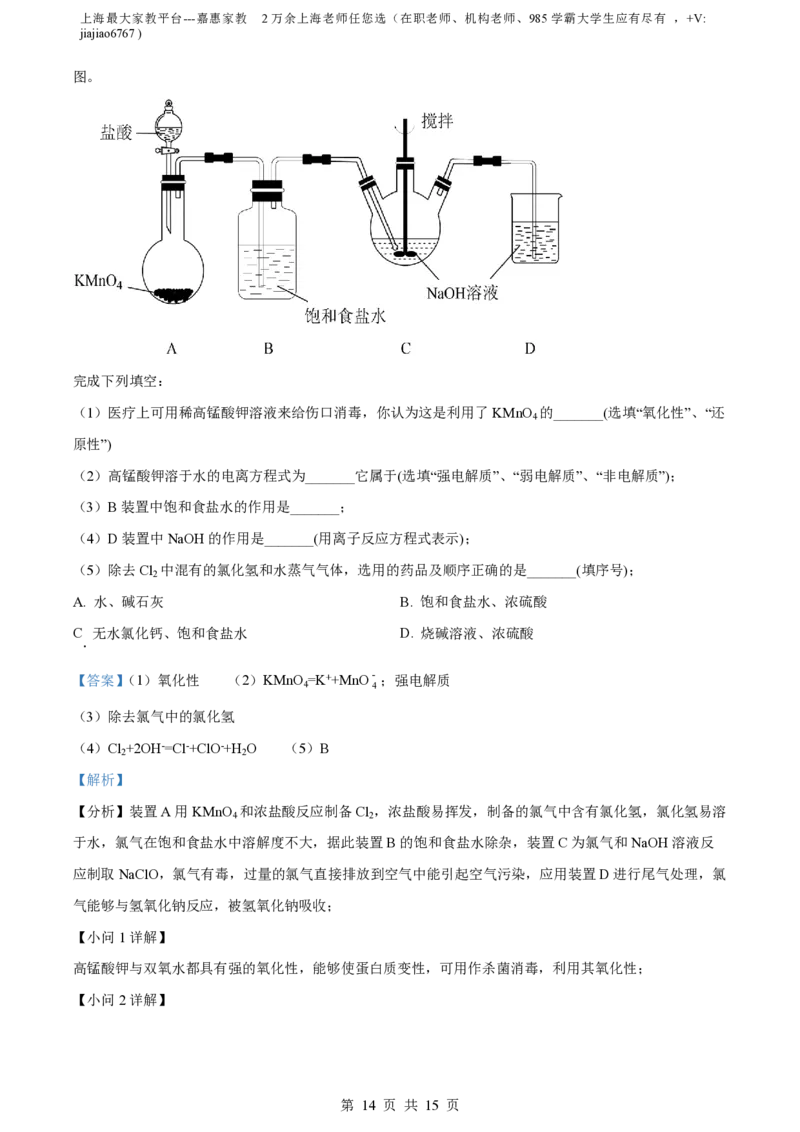
29. KMnO 是一种氧化剂,实验室常用KMnO 和浓盐酸反应制备Cl 。下图是制备 NaClO溶液的装置
4 4 2
第 13 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
图。
完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO 的_______(选填“氧化性”、“还
4
原性”)
(2)高锰酸钾溶于水的电离方程式为_______它属于(选填“强电解质”、“弱电解质”、“非电解质”);
(3)B装置中饱和食盐水的作用是_______;
(4)D装置中NaOH的作用是_______(用离子反应方程式表示);
(5)除去Cl 中混有的氯化氢和水蒸气气体,选用的药品及顺序正确的是_______(填序号);
2
A. 水、碱石灰 B. 饱和食盐水、浓硫酸
C 无水氯化钙、饱和食盐水 D. 烧碱溶液、浓硫酸
.
【答案】(1)氧化性 (2)KMnO =K++MnO- ;强电解质
4 4
(3)除去氯气中的氯化氢
(4)Cl +2OH-=Cl-+ClO-+H O (5)B
2 2
【解析】
【分析】装置A用KMnO 和浓盐酸反应制备Cl ,浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶
4 2
于水,氯气在饱和食盐水中溶解度不大,据此装置B的饱和食盐水除杂,装置C为氯气和NaOH溶液反
应制取NaClO,氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应用装置D进行尾气处理,氯
气能够与氢氧化钠反应,被氢氧化钠吸收;
【小问1详解】
高锰酸钾与双氧水都具有强的氧化性,能够使蛋白质变性,可用作杀菌消毒,利用其氧化性;
【小问2详解】
第 14 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
高锰酸钾属于钾盐,溶于水完全电离,电离方程式为KMnO =K++MnO- ,它属于强电解质;
4 4
【小问3详解】
浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以
用装有饱和食盐水的洗气瓶除去氯气中的氯化氢;
【小问4详解】
氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应进行尾气处理,氯气能够与氢氧化钠反应,
被氢氧化钠吸收,离子反应方程式Cl +2OH-=Cl-+ClO-+H O;
2 2
【小问5详解】
除去Cl 中混有的水蒸气和氯化氢气体,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用
2
装有饱和食盐水的洗气瓶除去氯气中的氯化氢,用浓硫酸吸收水蒸气,选用的药品及顺序正确的是B。
第 15 页 共 15 页