文档内容
绝密★启用前
望城二中高一期中考试化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干
净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
一、单选题:本大题共12小题,共36分。
1.下列关于物质分类的正确组合是( )
碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 硫酸 小苏打 氧化钙 干冰
B 烧碱 盐酸 食盐 氧化钠 一氧化碳
C 石灰水 NaHSO 碳酸钙 氢氧化钠 二氧化碳
4
D N H ⋅H O H NO 明矾 氧化铁 SO
3 2 3 3
A. A B. B C. C D. D
2.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性.制备时将:FeSO 和
4
Fe (SO ) 的溶液等物质的量混合,滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,即可生成黑色的
2 4 3
分散质粒子直径在5.5~36nm的磁流体.下列说法中,正确的是( )
A. 所得的分散系属于溶液
B. 所得的分散系中分散质为Fe O
2 3
C. 当一束强可见光通过该分散系会出现光亮的通路
D. 该分散系不属于介稳体系
3.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 28g N 所含的原子数目为N
2 A
B. 标准状况下,18 g H O所占的体积约为22.4 L
2C. 0.5 mol H SO 含有的原子数目为3.5N
2 4 A
D. 在常温常压下,11.2 L N 含有的原子数为N
2 A
4.下列关于溶液浓度的表述正确的是( )
A. 98%的硫酸溶液物质的量浓度为18.4mol/L,则49%的硫酸溶液物质的量浓度小于9.2mol/L
B. 只含 和 的水溶液中,如果 和 的物质的量浓度相等,则 和 的物质的量浓度
K SO NaCl Na+ SO2− K+ Cl−
2 4 4
一定相等
C. 配制0.4mol/L的NaOH溶液时,可称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至
250mL容量瓶中定容
D. 将100mL20%的NaOH溶液与100mL10%的NaOH的溶液混合,则所得混合溶液的质量分数为
15%
5.已知同温同压下,气体的物质的量之比=气体分子数之比=气体体积之比,一定温度和压强下,用质量相
等的CH 、CO 、O 、SO 四种气体分别吹出四个体积大小不同的气球,下列说法中错误的是( )
4 2 2 2
A. 气球③中装的是O
2
B. 气球①和气球④中气体的密度之比为1:4
C. 气球①和气球②中原子数之比为11:16
D. 气球③和气球④中气体体积之比为1:2
6.油条的做法是将矾、碱、盐按比例加入温水中,再加入面粉搅拌成面团;放置,使面团产生气体,形成
孔洞.放置过程发生反应:
2K Al(SO ) ⋅12H O+3Na CO =2Al(OH) ↓+3Na SO +K SO +3CO ↑+21H O.下列有
4 2 2 2 3 3 2 4 2 4 2 2
关判断正确的是( )
A. 从物质的分类角度来看,油条配方中的“矾、碱、盐”均为盐
B. 放置过程发生的反应为氧化还原反应
C. 放置过程发生的反应中,反应物和生成物均为电解质
D. 反应的离子方程式为
2Al3++3CO2−=2Al(OH) ↓+3CO ↑
3 3 27.下列有关物质分类的说法,不正确的是( )
A. CO、N O 是非金属氧化物,也是酸性氧化物,它们属于电解质
2 5
B. K NO 是钾盐、硝酸盐,也是正盐
3
C. H CO 是含氧酸、二元酸
2 3
D. NaOH是可溶性碱,也是强碱
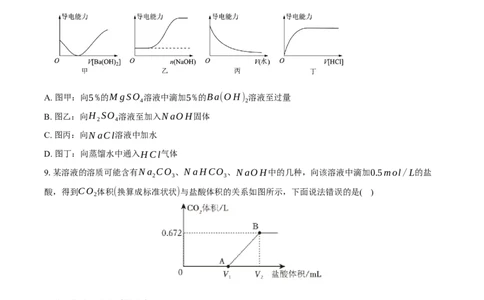
8.溶液的导电能力与溶液中的离子浓度有关。下列图象不正确的是( )
A. 图甲:向5%的MgSO 溶液中滴加5%的Ba(OH) 溶液至过量
4 2
B. 图乙:向H SO 溶液至加入NaOH固体
2 4
C. 图丙:向NaCl溶液中加水
D. 图丁:向蒸馏水中通入HCl气体
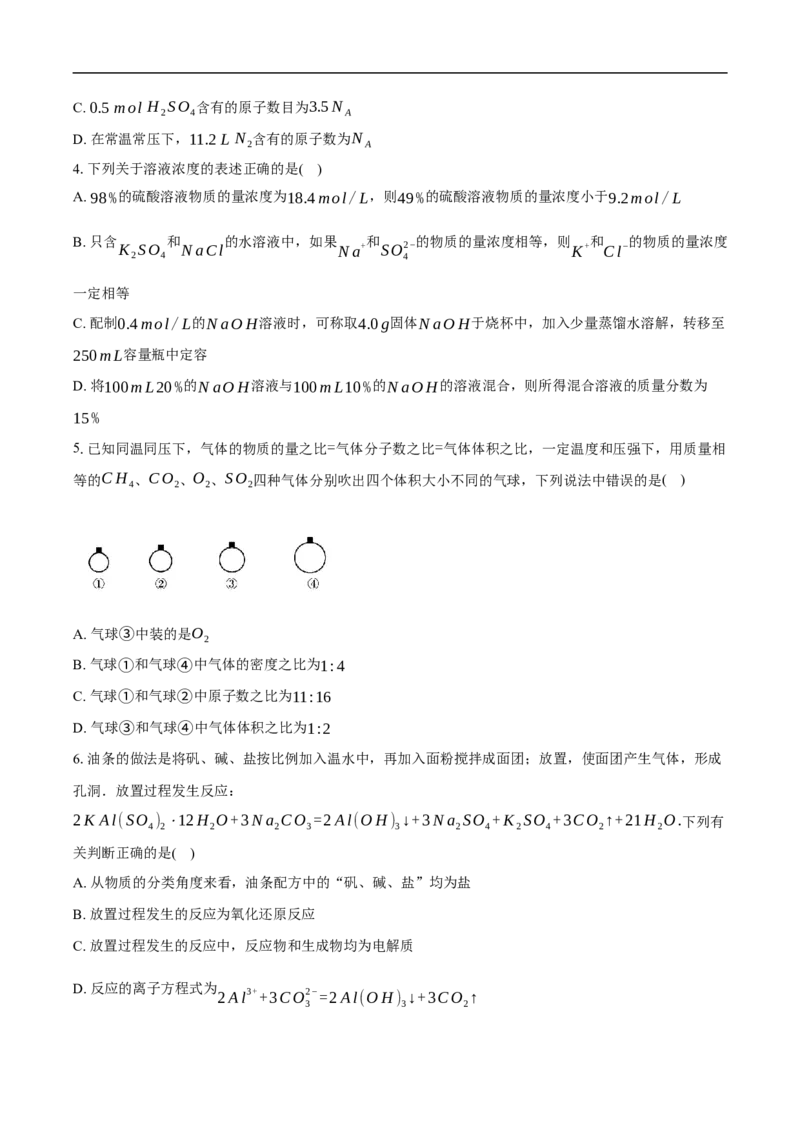
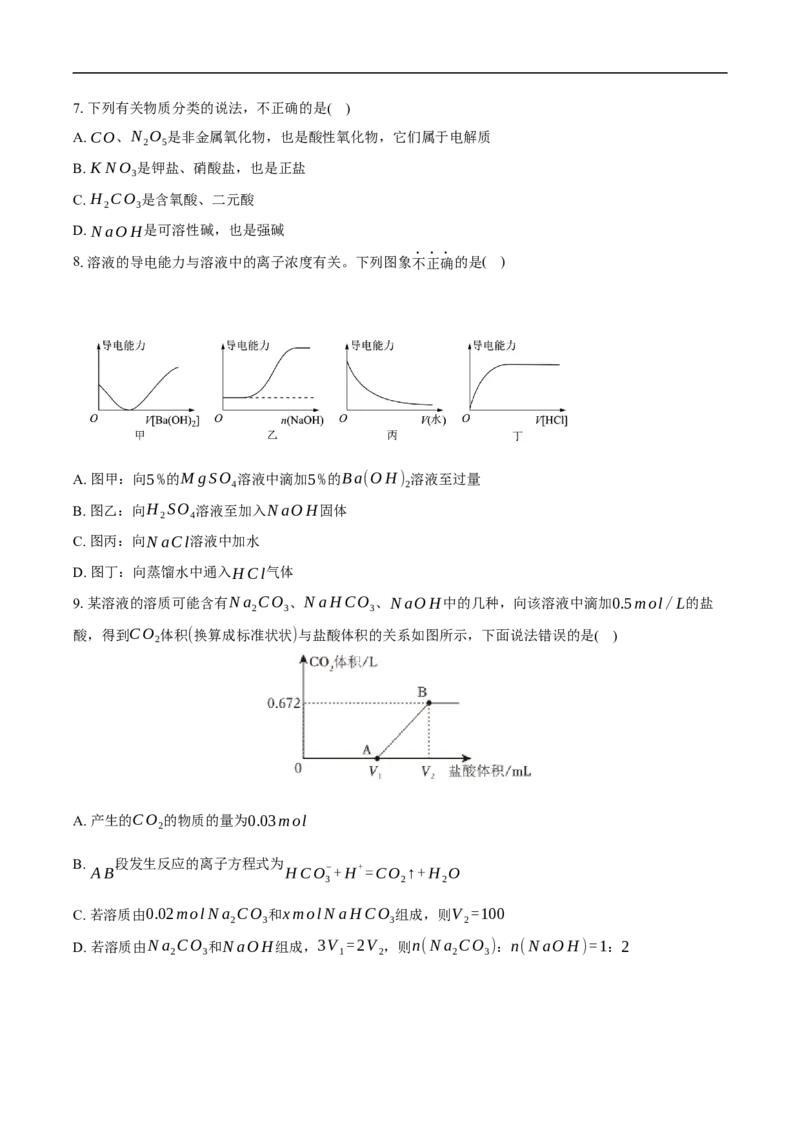
9.某溶液的溶质可能含有Na CO 、NaHCO 、NaOH中的几种,向该溶液中滴加0.5mol/L的盐
2 3 3
酸,得到CO 体积(换算成标准状状)与盐酸体积的关系如图所示,下面说法错误的是( )
2
A. 产生的CO 的物质的量为0.03mol
2
B. 段发生反应的离子方程式为
AB HCO−+H+=CO ↑+H O
3 2 2
C. 若溶质由0.02molNa CO 和xmolNaHCO 组成,则V =100
2 3 3 2
D. 若溶质由Na CO 和NaOH组成,3V =2V ,则n(Na CO ):n(NaOH)=1:2
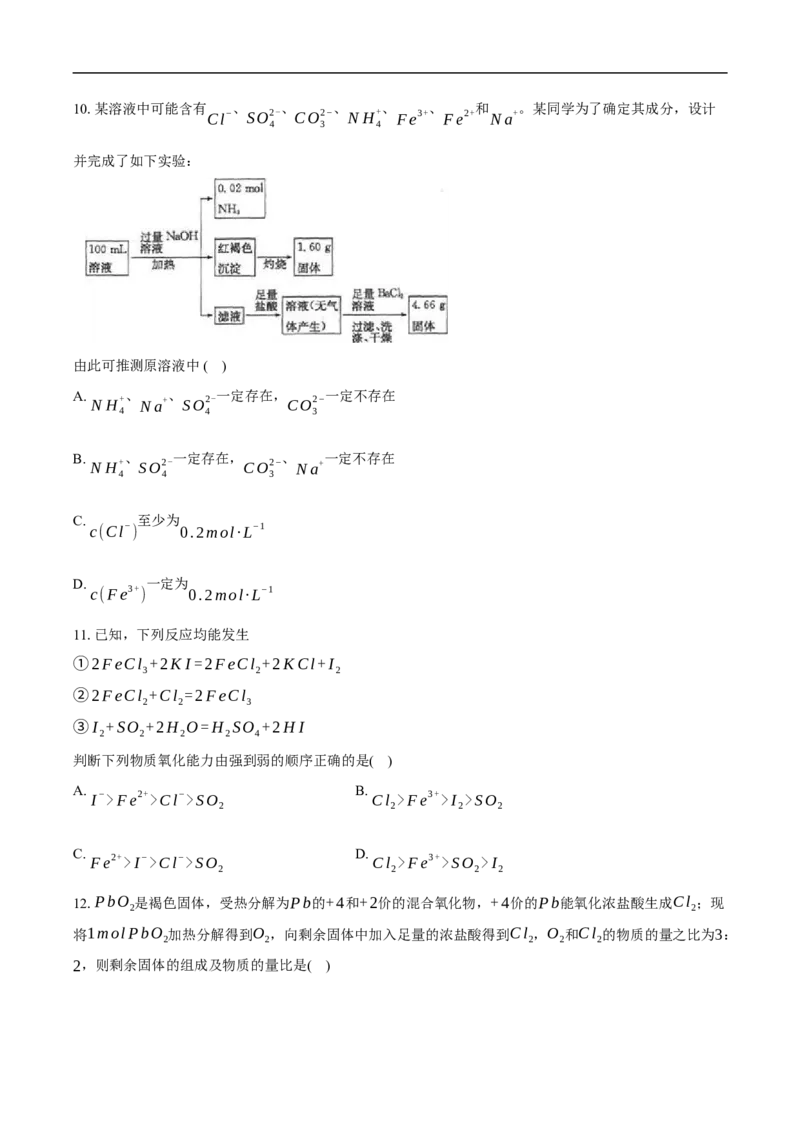
2 3 1 2 2 310.某溶液中可能含有 、 、 、 、 、 和 。某同学为了确定其成分,设计
Cl− SO2- CO2− N H+ Fe3+ Fe2+ Na+
4 3 4
并完成了如下实验:
由此可推测原溶液中 ( )
A. 、 、 一定存在, 一定不存在
N H+ Na+ SO2- CO2−
4 4 3
B. 、 一定存在, 、 一定不存在
N H+ SO2- CO2− Na+
4 4 3
C. 至少为
c(Cl− ) 0.2mol·L−1
D. 一定为
c(Fe3+ ) 0.2mol·L−1
11.已知,下列反应均能发生
①2FeCl +2K I=2FeCl +2KCl+I
3 2 2
②2FeCl +Cl =2FeCl
2 2 3
③I +SO +2H O=H SO +2H I
2 2 2 2 4
判断下列物质氧化能力由强到弱的顺序正确的是( )
A. B.
I−>Fe2+>Cl−>SO Cl >Fe3+>I >SO
2 2 2 2
C. D.
Fe2+>I−>Cl−>SO Cl >Fe3+>SO >I
2 2 2 2
12.PbO 是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl ;现
2 2
将1molPbO 加热分解得到O ,向剩余固体中加入足量的浓盐酸得到Cl ,O 和Cl 的物质的量之比为3:
2 2 2 2 2
2,则剩余固体的组成及物质的量比是( )A. 1:2混合的PbO 、Pb O
2 3 4
B. 1:1混合的Pb O 、PbO
3 4
C. 1:4:1混合的PbO 、Pb O 、PbO
2 3 4
D. 4:1:1混合的PbO 、Pb O 、PbO
2 3 4
二、双选题:本大题共2小题,共8分。
13.能正确表示下列反应的离子反应方程式为( )
A. 溶于过量的浓 溶液中:
N H HCO KOH N H++HCO−+2OH−=CO2−+N H ↑+2H O
4 3 4 3 3 3 2
B. 向明矾溶液中滴加 溶液,恰好使 沉淀完全:
Ba(OH) SO2− 2Al3++3SO2−+3Ba2++6OH
2 4 4
❑ −=2Al(OH) ↓+3BaSO ↓
3 4
C. 向 溶液中通入足量氯气:
FeBr 2Fe2++4Br−+3Cl =2Fe3++2Br +6Cl−
2 2 2
D. 醋酸除去水垢:
2H++CaCO =Ca2++CO ↑+H O
3 2 2
14.下列叙述正确的是( )
A. 同温同压下,相同体积的气体,其分子数一定相等,原子数也一定相等
B. 任何条件下,等物质的量的甲烷(CH )气体和CO气体所含的原子数一定不相等
4
C. 同压同体积的氧气和氮气的分子数相等
D. 同温同压下的CO和N ,若它们体积相同,那么它们的质量也一定相等
2
三、流程题:本大题共1小题,共8分。
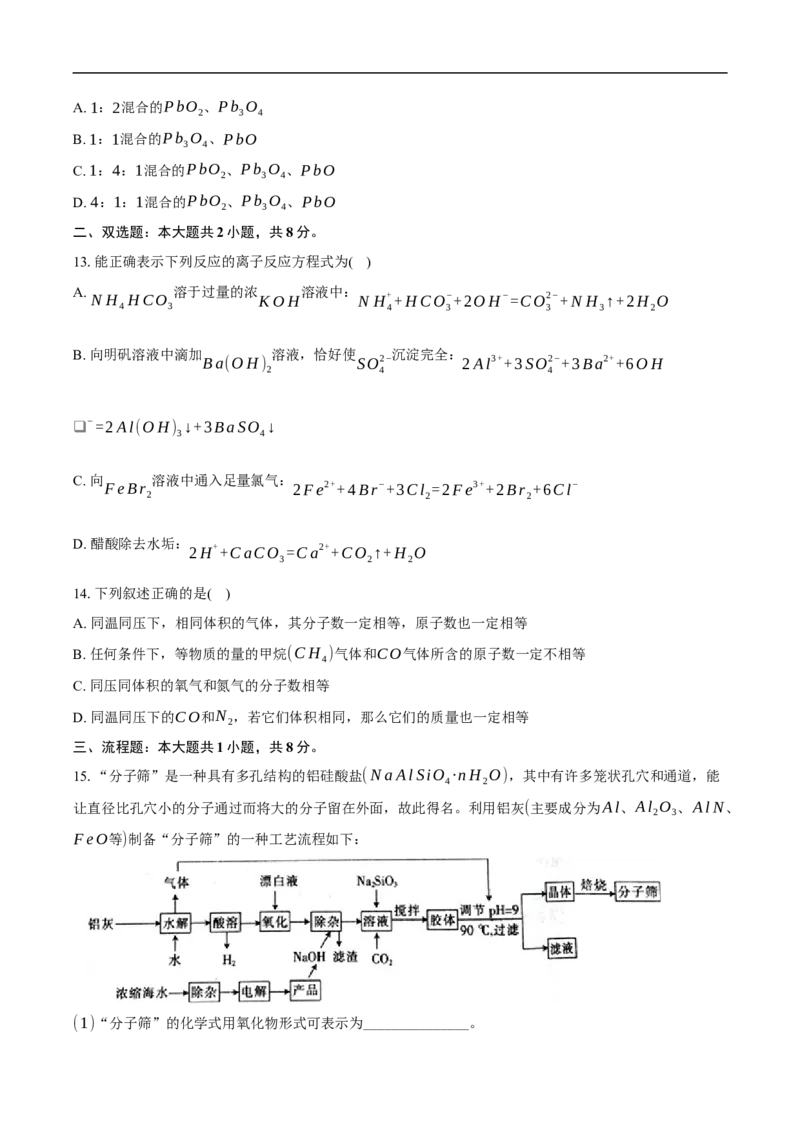
15.“分子筛”是一种具有多孔结构的铝硅酸盐(NaAlSiO ·nH O),其中有许多笼状孔穴和通道,能
4 2
让直径比孔穴小的分子通过而将大的分子留在外面,故此得名。利用铝灰(主要成分为Al、Al O 、AlN、
2 3
FeO等)制备“分子筛”的一种工艺流程如下:
(1)“分子筛”的化学式用氧化物形式可表示为_______________。(2)铝灰水解产生的气体为________(填化学式);“水解”在加热条件下而不在室温下进行的原因是
________________________。
(3)“酸溶”时,发生氧化还原反应的离子方程式为_________________________________。
(4)该工艺中滤渣的颜色为________________________。
某学习小组设计实验模拟从浓缩海水 含 、 、 中提取试剂级 :
(5) ( Ca2+ M g2+ SO2− ) NaCl
4
①实验中若向浓缩海水中加入的是Na CO 浓溶液,则有难溶的M g (OH) CO 生成,同时有气体逸
2 3 2 2 3
出。该反应的离子方程式为______________。
②该学习小组发现上述实验即使BaCl 用量不足,第Ⅲ步沉淀中依然含有少量BaCO 。从平衡角度分析
2 3
其原因:____________________________。
四、实验题:本大题共3小题,共30分。
16.I.据如图所示装置(部分仪器已略去)回答下列有关问题。
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是_______(填“I”或“I I”),试管中发生反应的
化学方程式为: _______________________________________,
通过上述实验,得出的结论是:Na CO 比NaHCO 的热稳定性_______(填“强”或“弱”)
2 3 3
(2)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO 气体通入足量的澄清石灰水中,测得生成
2
沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为___________。
II.某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。(3)装置①中反应的离子方程式是_______________________________________。
(4)过氧化钠跟二氧化碳反应的化学方程式_____________________________________。
(5)钠在空气中燃烧可生成过氧化钠,所需主要实验仪器有:酒精灯、三脚架、泥三角、____。
(6)【进行实验】
步骤1:打开弹簧夹K ,关闭K ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
2 1
步骤2:打开弹簧夹K ,关闭K ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
1 2
下列说法中正确的是:( )
a.装置①中盐酸可换成硫酸
b.装置②中的试剂是饱和Na CO 溶液,装置③中溶液是浓硫酸
2 3
c.步骤1中a处带火星的木条不复燃,步骤2中a处带火星木条复燃
d.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应,要做补充实验
17.二氧化氯(ClO )是一种在水处理等方面有广泛应用的高效安全消毒剂。制备ClO 有下列两种方法:
2 2
方法一:2NaClO +4HCl=2ClO ↑+Cl ↑+2NaCl+2H O
3 2 2 2
方法二:2NaClO +H O +H SO =2ClO ↑+O ↑+Na SO +2H O
3 2 2 2 4 2 2 2 4 2
(1)方法一中氧化剂是______________,氧化产物是______________。
(2)方法一的离子方程式为________________________。
(3)方法二中被氧化的物质是______________,若反应中有0.2mol电子转移,则产生的ClO 气体在标准
2
状况下的体积为____________。
(4)用双线桥法在下面的反应式上标出电子转移的方向与数目。
2NaClO +H O +H SO =2ClO ↑+O ↑+Na SO +2H O
3 2 2 2 4 2 2 2 4 218.回答下列问题。
Ⅰ.某膨松剂的有效成分为碳酸氢钠,测定其中碳酸氢钠含量的操作如下(设该膨松剂中的其他成分不与盐酸
或氢氧化钠反应):
①配制0.20mol/L稀盐酸和0.20mol/LNaOH溶液;
②取0.1g膨松剂研碎,加入蒸馏水;
③加入15.00mL0.20mol/L稀盐酸;
④用0.20mol/LNaOH溶液中和过量的稀盐酸,记录所消耗的NaOH溶液的体积。
(1)如图是实验室某浓盐酸试剂瓶的标签上,用该溶液配制100mL0.20mol/L稀盐酸。
①该浓盐酸的物质的量浓度为________mol·L−1;实验过程中需要的玻璃仪器除了胶头滴管、烧杯、量筒、
玻璃棒,还需要________;应用量筒量取浓盐酸________mL。
②下列操作会导致配制的盐酸浓度偏高的是________(填标号)。
a.未洗涤玻璃棒和烧杯 b.定容时俯视刻度线
c.转移溶液时有少量液体溅出 d.摇匀后发现液面低于刻度线
e.容量瓶中含有少量蒸馏水 f .量取浓盐酸时俯视刻度线
(2)通过3次测定,消耗NaOH溶液的体积平均为13.00mL,膨松剂中碳酸氢钠的质量分数为________。Ⅱ 单位质量膨松剂反应时产生标准状况下气体的体积 是检验膨松剂品质的一项重要指标。用如
. (mL·g−1 )
图装置测定某膨松剂样品产生CO 的质量(装置气密性良好,各装置中气体吸收剂足量),实验前后装置D
2
的质量差即为CO 的质量。回答下列问题:
2
(3)加热前,先对装置A、B和C通入一段时间的氮气,目的是排尽装置中的空气,防止干扰实验,然后再
连接上装置D、E.停止加热后,仍要继续通入一段时间的氮气,目的是
____________________________________________________________________。
(4)装置C中浓硫酸的作用为吸收分解生成的H O,装置E中碱石灰的作用是________。
2
(5)上述实验中,若没有装置E,可能会造成测定结果________(填“偏高”“偏低”或“不变”)。