文档内容
高中化学方程式总结
一、碱金属
第一部分 金属
1.钠 NaOH+H 2 S(足量)=NaHS+H 2 O
Na
2NaOH+H S(少量)=NaS+2HO
2 2 2
4Na+O=2NaO
2 2
3NaOH+AlCl =Al(OH) ↓+3NaCl
点燃 3 3
2Na+O NaO
2 2 2
NaOH+Al(OH) =NaAlO +2H O
点燃 3 2 2
Cl+2Na 2NaCl
2
NaOH+NHCl
△
N aCl+NH ↑+H O
2Na+S=NaS(爆炸) 4 3 2
2 2NaOH+P O=2N aPO +H O
2 5 3 2
2Na+2HO=2NaOH+H ↑
2 2
△ 6NaOH+P 2 O 5 =2Na 3 PO 3 +3H 2 O
2Na+H 2NaH
2 NaAlO
2
2Na+2NH =2NaNH +H 2NaAlO +CO +3H O=2Al(OH) ↓+Na CO
3 2 2 2 2 2 3 2 3
4Na+TiCl (熔融)=4NaCl+Ti 3NaAlO +AlCl +6H O=4Al(OH) ↓
4 2 3 2 3
NaCl、NaClO、NaBr、NaI
Na O
2
△
Na 2 O+H 2 O=2NaOH NaCl+H 2 SO 4 (浓) NaHSO 4 +HCl↑
△
2NaO+O 2NaO
2 2 2 2 HSO (浓)+2NaCl NaSO +2HCl
2 4 2 4
NaO+SO =NaSO
2 3 2 4 2NaI+Cl =2NaCl+I
2 2
NaO+CO=NaCO
2 2 2 3 NaBr+HPO (浓)=NaH PO +HBr
3 4 2 4
NaO+2HCl=2NaCl+H O
2 2 NaI+HPO (浓)=NaH PO +HI
3 4 2 4
NaO+2Na=2NaO(此反应用于制备NaO) Na CO 、NaHCO
2 2 2 2 2 3 3
高温
2NaO+2H O = 4NaOH+O ↑ ( 此 反 应 分 两 步 NaCO+SiO NaSiO+CO
2 2 2 2 2 3 2 2 3 2
NaO+2H O=2NaOH+H O ;2HO =2HO+O↑。
2 2 2 2 2 2 2 2 2 NaCO+HCl=NaHCO +NaCl
HO 的制备可利用类似的反应) 2 3 3
2 2
NaHCO +HCl=NaCl+H O+CO
2NaO+2CO =2NaCO+O 3 2 2
2 2 2 2 3 2
3NaCO+2AlCl +3H O=2Al(OH) ↓+3CO ↑+6NaCl
NaO+H SO (冷、稀)=NaSO +H O 2 3 3 2 3 2
2 2 2 4 2 4 2 2
3NaCO+2FeCl +3H O=2Fe(OH) ↓+3CO ↑+6NaCl
NaH 2 3 3 2 3 2
3NaHCO +AlCl =Al(OH) ↓+3CO ↑
NaH+H O=NaOH+H ↑ 3 3 3 2
2 2
NaOH 3NaHCO +FeCl =Fe(OH) ↓+3CO ↑
3 3 3 2
2NaOH+Si+H 2 O=Na 2 SiO 3 +2H 2 ↑ NaHCO 3 +HCl=NaCl+CO 2 ↑+H 2 O
6NaOH+3S △ 2 N a 2 S+Na 2 SO 3 +3H 2 O 2NaHCO 3 △ N a 2 CO 3 +CO 2 ↑+H 2 O
2NaOH+2Al+2H 2 O=2NaAlO 2 +3H 2 ↑ 3Na 2 CO 3 +2Br 2 +H 2 O =
2NaHCO +2NaBrO+2NaBr+CO ↑
2NaOH(过量)+CO =NaCO+H O 3 2
2 2 3 2
NaHCO +Br =NaBr+HBrO+CO ↑
NaOH+CO (过量)=NaHCO 3 2 2
2 3 NaNO 、NaNO
3 2
2NaOH+SiO =NaSiO+H O(常温下强碱缓慢腐蚀玻
2 2 3 2 △
璃) 2NaNO 2NaNO +O ↑
3 2 2
△
2NaOH+Al 2 O 3 =2NaAlO 2 +H 2 O H 2 SO 4 (浓)+NaNO 3 NaHSO 4 +HNO 3 ↑
2NaOH+Cl 2 =NaCl+NaClO+H 2 O KClO+6HCl=KCl+3Cl ↑+3H O
3 2 2
NaOH+HCl=NaCl+H 2 O NaNO +NHCl=NaCl+N ↑+2H O
2 4 2 2Na PO、NaH PO、Na HPO KHCO +HCl=KCl+CO ↑+H O
3 4 2 4 2 4 3 2 2
△
NaPO +HCl=NaHPO +NaCl 2KHCO KCO+CO ↑+H O
3 4 2 4 3 2 3 2 2
NaHPO +HCl=NaH PO +NaCl KClO
2 4 2 4 3
△
NaH PO +HCl=HPO +NaCl 2KClO 2KCl+3O ↑
2 4 3 4 3 2
Na S、NaHS
2 KClO+6HCl=KCl+3Cl ↑+3H O
3 2 2
NaS+Cl =2NaCl+S↓
2 2 KClO+5KCl+3H SO =3Cl↑+3K SO +3H O
3 2 4 2 2 4 2
3NaS+8HNO (稀)=6NaNO +2NO+3S↓+4H O
2 3 3 2
KI
3NaS+Al (SO )+6H O=2Al(OH) ↓+3H S↑
2 2 4 3 2 3 2 2KI+Cl =2KCl+I
2 2
Na SO 、Na SO 、Na S2O
2 4 2 3 2 3 KI+AgNO=AgI↓+KNO
3 3
3NaSO +2HNO (稀)=3NaSO +2NO↑+H O
2 3 3 2 4 2
KAl(SO )
4 2
2NaSO +O =2NaSO
2 3 2 2 4 2KAl(SO )+6NaOH=KSO +3Na SO +2Al(OH) ↓
4 2 2 4 2 4 3
NaSO+H SO =NaSO +S+SO +H O
2 2 3 2 4 2 4 2 2 2KAl(SO )+3Ba(OH) =KSO +3BaSO ↓+2Al(OH) ↓
NaSO +SO+H O=2NaHSO 4 2 2 2 4 4 3
2 3 2 2 3
△
2NaHSO 3 Na 2 SO 3 +SO 2 ↑+H 2 O KAl(SO 4 ) 2 +2Ba(OH) 2 =KAlO 2 +2BaSO 4 ↓
Na SiO
2 3 KSCN
NaSiO+2HCl=HSiO↓+2NaCl
2 3 2 3
CHONa 3KSCN+FeCl =Fe(SCN) +3KCl
6 5 3 3
C HONa+CO+H O=C HOH+NaHCO
6 5 2 2 6 5 3 KH
2.钾 KH+H O=KOH+H ↑
2 2
K
△
K+O KO
2 2 3.锂
Li
2K+2HO=2KOH+H ↑
2 2
K 2 O、K 2 O 2 Li+O 2 △ L i 2 O
K 2 O+H 2 O=2KOH 2Li+2H 2 O=2LiOH+H 2 ↑
LiO
KO+CO=KCO 2
2 2 2 3
LiO+CO=LiCO
2KO+2CO =KCO+O 2 2 2 3
2 2 2 2 3 2
LiO+HO=2LiOH
2KO+2H O=4KOH+O 2 2
2 2 2 2 LiOH
KOH
2LiOH+CO=LiCO↓+HO
2KOH+CO =KCO+H O 2 2 3 2
2 2 3 2
LiOH+CO=LiHCO
KOH+CO =KHCO 2 3
2 3 LiCO
KCO 2 3
2 3
LiCO+2HCl=2LiCl+CO↑+HO
KCO+2HCl=2KCl+CO ↑+H O 2 3 2 2
2 3 2 2 LiHCO
3
KCO+CaCl =CaCO ↓+2KC
2 3 2 3 LiHCO+HCl=LiCl+CO↑+HO
3 2 2
K
2
CO
3
+2AgNO
3
=Ag
2
CO
3
↓+2KNO
3 2LiHCO
△
L iCO+CO↑+HO
KHCO 3 2 3 2 2
3
二、常见金属
1.镁 Mg+Br =MgBr
2 2
Mg 3Mg+N=MgN
2 3 2
2Mg+O
点燃
2MgO Mg+2HCl=MgCl +H ↑
2 2 2
Mg+2HO=2Mg(OH) ↓+H ↑ Mg+HSO =MgSO +H ↑
2 2 2 2 4 4 2
Mg+Cl
点燃
MgCl 2Mg+TiCl (熔融)=Ti+2MgCl
2 2 4 2
2Mg+CO
点燃
2MgO+C Mg+2RbCl(熔融)=MgCl +2Rb
2 2
Mg+S=MgS MgOMgO+2HCl=MgCl +H O AlCl +3NH·H O=Al(OH) ↓+3NHCl
2 2 3 3 2 3 4
MgO+H O=Mg(OH) ↓ 2AlCl +3Na CO+3H O=2Al(OH) ↓+3CO ↑+6NaCl
2 2 3 2 3 2 3 2
Mg(OH) AlCl +3NaHCO=Al(OH) ↓+3CO ↑
2 3 3 3 2
Mg(OH) +2HCl=MgCl +2H O AlCl +3NaAlO+6H O=4Al(OH) ↓
2 2 2 3 2 2 3
Al (SO )+3Na S+6HO=2Al(OH) ↓+3H S↑
2 4 3 2 2 3 2
MgCO
3 Al C +12H O=4Al(OH) ↓+3CH ↑
4 3 2 3 4
MgCO +2HCl=2MgCl +CO ↑+H O
3 2 2 2
3.铁
△
MgCO +2H O Mg(OH) ↓+CO ↑
3 2 2 2
Fe
△
MgCO CO↑+MgO
3 2 点燃
2Fe+3Cl 2FeCl
2 3
Mg(HCO )
3 2 点燃
3Fe+2O Fe O
2 3 4
Mg(HCO )+2HCl=MgCl +2CO ↑+2H O
3 2 2 2 2 △
Fe+S FeS
△
2Mg(HCO ) Mg(OH) ↓+CO ↑+H O
3 2 2 2 2
2Fe+3Br =2FeBr
2 3
MgSO
4 △
Fe+I FeI
MgSO
4
+Ba(OH)
2
=Mg(OH)
2
↓+BaSO
4
↓ 2 2
△
MgSO +2NaOH=Mg(OH) ↓+Na SO ↓ Fe+S FeS
4 2 2 4
MgN 高温
3 2 3Fe+4H O(g) Fe O+4H
Mg
3
N
2
+8H
2
O=3Mg(OH)
2
+2NH
3
·H
2
O 2 3 4 2
Fe+2HCl=FeCl +H ↑
2 2
2.铝
Fe+CuCl =FeCl +Cu
2 2
Al
Fe+SnCl =FeCl +SnCl
点燃 4 2 2
Al+3O 2Al O
2 2 3
Fe+H S=FeS+H↑
△ 2 2
2Al+3S Al S
2 3
2Fe+6H SO (浓)=Fe (SO )+3SO↑+6H O
△ 2 4 2 4 3 2 2
2Al+3Cl 2AlCl
2 3
Fe+H SO (稀)=FeSO +H ↑
高温 2 4 4 2
4Al+3MnO 2Al O+3Mn
2 2 3
Fe+6HNO =Fe(NO )+3NO↑+3H O
高温 3 3 3 2 2
2Al+Cr O Al O+2Cr
2 3 2 3
Fe+4HNO =Fe(NO )+NO↑+2H O
高温 3 3 3 2
2Al+Fe O Al O+2Fe(铝热反应)
2 3 2 3
8Fe+30HNO =8Fe(NO )+3N O↑+15H O
△ 3 3 3 2 2
2Al+3FeO Al O+3Fe
2 3 10Fe+36HNO =10Fe(NO )+3N ↑+18H O
2Al+6HCl=2AlCl +3H ↑ 3 3 3 2 2
3 2
2Al+3H SO =Al (SO )+3H ↑ 8Fe+30HNO =8Fe(NO )+3NHNO +9H O
2 4 2 4 3 2 3 3 3 4 3 2
△
2Al+6H 2 SO 4 (浓) Al 2 (SO 4 ) 3 +3SO 2 ↑+6H 2 O Fe+(CH 3 COO) 2 Cu=Cu+(CH 3 COO) 2 Fe
Al+4HNO (稀)=Al(NO )+NO↑+2HO(Al、Fe在冷、浓 FeO
3 3 3 2
的H 2 SO 4 、HNO 3 中钝化) 3FeO+2Al △ A l O+3Fe
2Al+2NaOH+2H O=2NaAlO +3H ↑ 2 3
2 2 2
△
6FeO+O 2Fe O
Al O、Al(OH) 2 3 4
2 3 3
FeO+4HNO =Fe(NO )+NO↑+2H O
Al O+3H SO =Al (SO )+3H O(Al O 是两性氧化物) 3 3 3 2 2
2 3 2 4 2 4 3 2 2 3
FeO
Al O+2NaOH=2NaAlO +H O 2 3
2 3 2 2
高温
2Al(OH)
△
A l O+3H O
Fe
2
O
3
+2Al Al
2
O
3
+2Fe
3 2 3 2
△
Fe O+3CO 2Fe+3CO
Al(OH) +3HCl=AlCl +3H O 2 3 2
3 3 2
Fe O+3H =2Fe+3H O(制还原铁粉)
2Al(OH) +3H SO =Al (SO )+6H O 2 3 2 2
3 2 4 2 4 3 2
Fe O+6HCl=2FeCl +3H O
Al(OH) +NaOH=NaAlO +2H O 2 3 3 2
3 2 2
FeO
铝盐 3 4
AlCl +3NaOH=Al(OH) ↓+3NaCl
3 3Fe O+4H △ 3 F e+4H O 2FeCl 3 +3Na 2 CO 3 +3H 2 O=2Fe(OH) 3 ↓+3CO 2 ↑+6NaCl
3 4 2 2
FeCl +3NaHCO=Fe(OH) ↓+3CO ↑
3 3 3 2
△
Fe O+8HCl(浓) FeCl +2FeCl +4H O
3 4 2 3 2 2FeCl +SO+2H O=2FeCl +H SO +2HCl
3 2 2 2 2 4
Fe(OH) 、Fe(OH)
2 3 BaCl +H SO =BaSO↓+2HCl
2 2 4 4
4Fe(OH) 2 +O 2 +2H 2 O=4Fe(OH) 3 FeCl 3 +3KSCN=Fe(SCN) 3 +3KCl
△
2Fe(OH) Fe O+3H O FeS
3 2 3 2
FeCl 2 FeS+2HCl=FeCl 2 +H 2 S↑
2FeCl 2 +Cl 2 =2FeCl 3 FeS+H 2 SO 4 =FeSO 4 +H 2 S↑
FeCl 2 +Mg=Fe+MgCl 2 4FeS 2 +11O 2 =2Fe 2 O 2 +8SO 2
FeCl 3 H 2 FeO 4
4HFeO+2H O=4Fe(OH) +3O ↑
2FeCl +Fe=3FeCl 2 4 2 3 2
3 2
4Na FeO +10H O=4Fe(OH) +3O ↑+8NaOH
2 4 2 3 2
2FeCl +Cu=2FeCl +CuCl (用于雕刻印刷电路板)
3 2 2 2Fe(OH) +3NaClO+4NaOH=2NaFeO+3NaCl+5HO
3 2 4 2
2FeCl +H SO +H O=HSO +2FeCl +2HCl Fe O+3Na O=2NaFeO+Na O
3 2 3 2 2 4 2 2 3 2 2 2 4 2
2FeCl
3
+Zn=2FeCl
2
+ZnCl
2
其它Fe化合物
2FeCl 3 +H 2 S=2FeCl 2 +2HCl+S↓ Fe 2 (SO 4 ) 3 +2Ag=FeSO 4 +Ag 2 SO 4 (较难反应)
2FeCl 3 +2KI=2FeCl 2 +2KCl+I 2 Fe 3 C+22HNO 3 =3Fe(NO 3 ) 3 +CO 2 +13NO 2 +11H 2 O
FeCl +3NH·HO=Fe(OH) ↓+3NHCl
3 3 2 3 4
三、其他金属
△
1.锰 Cu(OH) CuO+HO
2 2
KMnO CuCl +H S=CuS↓+2HCl
4 2 2
△
2KMnO KMnO +MnO+O ↑ CuCl +2NaOH=Cu(OH) ↓+2NaCl
4 2 4 2 2 2 2
2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O CuSO +H S=CuS↓+HSO
4 2 2 2 4 2 2 4
2KMnO +5H O+6HCl=2KCl+2MnCl +5O ↑+8H O CuSO +2NaOH=Cu(OH) ↓+NaSO
4 2 2 2 2 2 4 2 2 4
2KMnO +5KNO +3H SO =2MnSO +K SO +5KNO + CuSO +Ba(OH) =Cu(OH) ↓+BaSO ↓
4 3 2 4 4 2 4 3 4 2 2 4
2HP
2 3.钙
MnO
2 Ca
△ CaO+HO=Ca(OH)
MnO+4HCl(浓) MnCl+Cl↑+2HO 2 2
2 2 2 2
高温
CaO+SiO CaSiO
2 3
2.铜 2Ca(OH)+2Cl=CaCl +Ca(ClO)+2H O
2 2 2 2 2
Cu Ca(OH) +SO=CaSO+H O
2 3 4 2
△
2Cu+O 2CuO CaCO +2HNO =Ca(NO )+H O+CO↑(用HNO 和浓
2 3 3 3 2 2 2 3
2Cu+S △ C u S H 2 SO 4 不能制备H 2 S、HI、HBr、SO 2 等还原性气体)
2
CaCO +SiO
高温
C aSiO +CO ↑
Cu+Cl
2
CuCl
2
3 2 3 2
CaF +H SO (浓)=CaSO+2HF↑
CH+4CuO=4Cu+CO +2H O 2 2 4 4
4 2 2
3CuO+2NH △ 3 C u+N +3H O Ca 3 (PO 4 ) 2 +3H 2 SO 4 (浓)=3CaSO 4 +2H 3 PO 4
3 2 2
Ca (PO )+2H SO (浓)=2CaSO+Ca(HPO )
CuO+2HCl=CuCl+HO 3 4 2 2 4 4 2 4 2
2 2
Ca (PO )+4H PO =3Ca(HPO )(重钙)
CuO+HSO =CuSO +HO 3 4 2 3 4 2 4 2
2 4 4 2
CaH+2H O=Ca(OH) +2H ↑
Cu(OH) +2HCl=CuCl+2HO 2 2 2 2
2 2 2
Cu(OH) +HSO =CuSO +2HO 4.钡
2 2 4 4 2Ba Zn+2NaOH=NaZnO+H↑
2 2 2
Ba(OH) +CO=BaCO ↓+HO Zn+2FeCl =2FeCl +ZnCl
2 2 3 2 3 2 2
Ba(OH) +2CO(过量)=Ba(HCO ) As O+6Zn+12HCl=2AsH ↑+6ZnCl +3H O
2 2 3 2 2 3 3 2 2
ZnO
Ba(OH) +H SO =BaSO↓+2HO
2 2 4 4 2
ZnO+2HCl=ZnCl+HO
3Ba(OH) +2HPO =Ba (PO )↓+6HO 2 2
2 3 3 3 4 2 2
ZnO+2NaOH=NaZnO+H O
BaCl +H SO =BaSO↓+2HCl 2 2 2
2 2 4 4 Zn(OH)
2
BaCl +Na SO =BaSO↓+2NaCl
2 2 4 4 Zn(OH) +2HCl=ZnCl+2HO
2 2 2
BaCO +2HCl=BaCl +CO↑+HO
3 2 2 2 Zn(OH) +2NaOH=NaZnO+2H O
2 2 2 2
BaCO +2HNO=Ba(NO )+CO↑+HO
3 3 3 2 2 2 Zn(OH) +4NH ·HO=Zn(NH )(OH) +4HO
2 3 2 3 4 2 2
BaO+H SO (稀)=BaSO↓+H O) △
2 2 4 4 2 2 Zn(OH) ZnO+HO
2 2
5.铅
7.铍
Pb、PbO
2 Be
Pb+2HCl=PbCl+H↑
2 2 Be+2HCl=BaCl +H↑
2 2
△
PbO+4HCl(浓) PbCl+Cl↑+2H O
2 2 2 2 Be+2NaOH=NaBO+H↑
2 2 2
铅盐
BeCl+2NaOH=Be(OH) ↓+2HO
2 2 2
Pb(NO )+H S=PbS↓+2HNO
3 2 2 3 Be(OH) +2HCl=BeCl+2HO
2 2 2
(CHCOO) Pb+HS=PbS↓+CHCOOH
3 2 2 3 Be(OH) +2NaOH=NaBO+2HO
2 2 2 2
6.锌 8.汞
Zn
Hg
△
Zn+S ZnS 3Hg+8HNO(稀)=3Hg(NO)+2NO ↑+4HO
3 3 2 2 2
Zn+2HCl=ZnCl+H↑ Hg+4HNO(浓)=Hg(NO)+2NO ↑+2H
2 2 3 3 2 2 2
Zn+HSO =ZnSO+H↑
2 4 4 2
一、卤族元素
第二部分 卤族元素、氮族元素
1.氟 5Cl+I +6H O=2HIO +10HCl
2 2 2 3
F
2 Cl+Na S=2NaCl+S↓
F+H=2HF 2 2
2 2
2F 2 +2H 2 O=4HF+O 2 Cl+H S=2HCl+S↓
2 2
HF
4HF+SiO =SiF+2H O Cl+SO+2H O=HSO +2HCl
2 4 2 2 2 2 2 4
Cl+H SO +H O=HSO +2HCl
2.氯 2 2 3 2 2 4
Cl+H O=HCl+HClO
Cl 2 2
2
Cl+H O=2HCl+O
Cl+H =2HCl(光照或点燃) 2 2 2 2
2 2
Cl+2NaOH=NaCl+NaClO+H O
Cl+2Na 2NaCl 2 2
2
2Cl+2Ca(OH)=CaCl +Ca(ClO)+2H O
3Cl+2P 2PCl 2 2 2 2 2
2 3 3Cl+6KOH(热、浓)=5KCl+KClO +3H O
2 3 2
Cl+PCl PCl
2 3 5 HCl
3Cl+2Fe 2FeCl 6HCl+2Al=2AlCl +3H ↑
2 3 3 2
2HCl+Fe=FeCl +H ↑
2 2
Cl 2 +Cu CuCl 2 △
4HCl(浓)+MnO MnCl +Cl+2H O
2 2 2 2
Cl 2 +2FeCl 2 =2FeCl 3 △
4HCl(g)+O 2Cl+2H O
2 2 2
2Cl+2NaBr=2NaCl+Br
2 2 16HCl+2KMnO =2KCl+2MnCl +5Cl+8H O
4 2 2 2
Cl+2KI=2KCl+I
2 2 14HCl+K Cr O=2KCl+2CrCl +3Cl+7H O
2 2 7 3 2 2HCl+NH=NH Cl(白烟) Br +H O=HBr+HBrO
3 4 2 2
2HCl+FeO=FeCl +3H O Br +NaOH=NaBr+NaBrO+HO
2 2 2 2
6HCl+Fe O=2FeCl +3H O Br +SO+2H O=HSO +2HBr
2 3 3 2 2 2 2 2 4
△
8HCl(浓)+Fe O FeCl +2FeCl +4H O Br +H S=S↓+2HBr
3 4 2 3 2 2 2
HCl+Na PO =NaHPO +NaCl 2Br +3Na CO+H O =
3 4 2 4 2 2 3 2
2NaHCO +2NaBrO+2NaBr+CO ↑
HCl+Na HPO =NaH PO +NaCl 3 2
2 4 2 4
HBr
HCl+NaH PO =HPO +NaCl
2 4 3 4
HBr+NaOH=NaBr+HO
HCl+Na CO=NaHCO +NaCl 2
2 3 3
2HBr+Cl=2HCl+Br
HCl+NaHCO =NaCl+H O+CO 2 2
3 2 2
4.碘
HClO
HClO=HCl+O↑
2 I
2
3.溴 I 2 +H 2 2HI
Br 2 I 2 +Fe FeI 2
△ I+2NaOH=NaI+NaIO+HO
Br +H 2HBr 2 2
2 2
Br +Fe=FeBr HI
2 3
△
Br +2FeBr =2FeBr 2HI H+I
2 2 3 2 2
Br +NaI=NaBr+I 2HI+Cl=2HCl+I
2 2 2 2
Br +HI=HBr+I HI+NaOH=NaI+HO
2 2 2
二、氮族元素
1.氮 3As S+28HNO +4H O=6HAsO +9H SO +28NO↑
2 3 3 2 3 4 2 4
△
N 4HNO(浓)+C CO↑+4NO↑+2H O
2 3 2 2 2
催化剂
N+3H 2NH 2HNO+CaCO =Ca(NO )+H O+CO↑
2 2 高 温 、 高 压 3 3 3 3 2 2 2
6HNO+Fe=Fe(NO )+3NO↑+3H O
3 3 3 2 2
4HNO+Fe=Fe(NO )+NO↑+2H O
N+O 2NO 3 3 3 2
2 2
30HNO+8Fe=8Fe(NO )+3N O↑+15H O
N+3Mg
点燃
MgNN+6Na=2NaN
3 3 3 2 2
2 3 2 2 3
36HNO+10Fe=10Fe(NO )+3N ↑+18H O
3 3 3 2 2
NO、NO 2 、N 2 O 5 30HNO+8Fe=8Fe(NO )+3NHNO +9H O
3 3 3 4 3 2
2NO+O =2NO
2 2 FeO+4HNO =Fe(NO )+NO↑+2H O
3 3 3 2 2
NO+NO +2NaOH=2NaNO (用于制硝酸工业中吸收
2 2 3HS+2HNO (稀) 3S↓+2NO+4HO
尾气中的NO和NO ) 2 3 2
2
4HNO=4NO +O +2H O(见光或受热分解)
3 2 2 2
6NO+4NH
催化剂
5 N +6H O
3 2 2 NH +HNO =NH NO(白烟)(用HNO 和浓HSO 不
△ 3 3 4 3 3 2 4
能制备HS、HI、HBr、SO )
NO +2KI+H O=NO+I +2KOH(不能用淀粉KI溶液鉴 2 2
2 2 2
别溴蒸气和NO ) 3NaS+8HNO (稀)=6NaNO +2NO+3S↓+4H O
2 2 3 3 2
4NO +H S=4NO+SO +H O 3NaSO +2HNO (稀)=3NaSO +2NO↑+H O
2 2 3 2 2 3 3 2 4 2
NO +SO=SO +NO 3Cu S+22HNO =6Cu(NO )+10NO↑+3H SO +8H O
2 2 3 2 3 3 2 2 4 2
3NO +H O=2HNO+NO 5HNO(浓)+P=HPO +5NO↑+H O
2 2 3 3 3 4 2 2
NO+H O=2HNO P+20HNO (浓)=4HPO +20NO+4H O
2 5 2 3 4 3 3 4 2 2
HNO S+6HNO (浓)=HSO +6NO↑+2H O
3 3 2 4 2 2
3HNO+Ag PO =HPO +3AgNO 3S+4HNO (稀)=3SO ↑+4NO↑+2H O
3 3 4 3 4 3 3 2 2
Al+4HNO (稀)=Al(NO )+NO↑+2H O S+6HNO (浓)=HSO +6NO↑+2H O
3 3 3 2 3 2 4 2 23As S+28HNO ( 稀 )+4H O = NH NO
2 3 3 2 4 3
6HAsO +9H SO +28NO↑ NH NO +NaOH==NaNO +NH ·HO
3 4 2 4 4 3 3 3 2
△
As S+28HNO (浓)=2HAsO +3H SO +28NO↑+8H O NH NO +NaOH NaNO +NH ↑+H O
2 3 3 3 4 2 4 2 2 4 3 3 3 2
5NH NO 2HNO+4N↑+9HO
4 3 3 2 2
NH
3
2NH +3CuO △ 3 C u+N +3H O (NH 4 ) 2 SO 3 、(NH 4 ) 2 SO 4
3 2 2
(NH )SO +SO+H O=2NH HSO
2NH +3Cl=N+6HCl 4 2 3 2 2 4 3
3 2 2 (NH )SO +2NaOH=NaSO +2NH ·HO
4 2 4 2 4 3 2
8NH 3 +3Cl 2 =N 2 +6NH 4 Cl (NH 4 ) 2 SO 4 +2NaOH
△
N a 2 SO 4 +2NH 3 ↑+2H 2 O
4NH +3O (纯氧)
点燃
2N+6H O
3 2 2 2
2.磷
4NH 3 +5O 2
催化剂
4 N O+6H 2 O P
△
点燃
2P+3Cl 2PCl
4NH +6NO 催化剂 5 N +6HO(用氨清除NO) 2 3
3 2 △
△ PCl +Cl PCl
3 2 5
NH +HCl=NH Cl(白烟) △
3 4 P+6H 4PH
4 2 3
NH
3
+HNO
3
=NH
4
NO
3
(白烟)
4P+5O
点燃
PO (常写成PO)
2 4 10 2 5
2NH +H SO =(NH )SO
3 2 4 4 2 4 P+20HNO (浓)=4HPO +20NO+4H O
4 3 3 4 2 2
NH +NaCl+HO+CO =NaHCO ↓+NHCl(侯氏制碱
3 2 2 3 4 11P+15CuSO+24H O=5Cu P+6HPO +15H SO
法) 4 2 3 3 4 2 4
PH +2O=HPO
3 2 3 4
2NH +SO+H O=(NH )SO
3 2 2 4 2 3 PO、PO、PS
2 3 2 5 4 3
△
NH ·HO NH ↑+H O
3 2 3 2 PO+H O(冷)=2HPO
NH +H O NH ·HO NH ++OH- 2 5 2 3
3 2 3 2 4
PO+3H O(热)=2HPO(PO 极易吸水、可作气体干
NH HCO 、(NH)CO 2 5 2 3 4 2 5
4 3 4 2 3 燥剂)
NH HCO =NH +H O+CO
4 3 3 2 2 PO+3H SO (浓)=2HPO +3SO
2 5 2 4 3 4 3
(NH 4 ) 2 CO 3 =2NH 3 ↑+H 2 O+CO 2 ↑ P 2 O 5 +2NaOH=2NaPO 3 +H 2 O
PO+6NaOH=2NaPO +3H O
2 5 3 3 2
NH Cl PS+38HNO +8H O=9HSO +12H PO +38NO↑
4 4 3 3 2 2 4 3 4
NH Cl=NH +HCl HPO
4 3 3 4
△
2NH Cl+Ca(OH) CaCl +NH ↑+H O 4HPO +Ca (PO )=3Ca(HPO )
4 2 2 3 2 3 4 3 4 2 2 4 2
△
NH Cl+NaOH NaCl+NH ↑+H O HPO (浓)+NaBr=NaH PO +HBr
4 3 2 3 4 2 4
NH Cl+NaOH=NaCl+NH ·HO HPO (浓)+NaI=NaH PO +HI
4 3 2 3 4 2 4
一、碳族元素
第三部分 碳族元素、氧族元素
1.碳 △
C+Si SiC(金刚砂)
C △
C+2S CS
2
C+2F 2 =CF 4 3C+CaO 电炉 C aC +CO↑
2
C+2Cl 2 =CCl 4 3C+SiO 电炉 S iC+2CO↑
2
C
C
C
+
+
+
O
C
O
O
2 (
2
足
( 少
量
△
量
)
)
2
点
C
点
O
燃
燃
C
2
O
C
2
O C
C
+
+
2
4
H
HN
2
S
O
2
O
3
4
(
(
浓
浓
)
)
△
△
C
C
O
O
2
2
↑
↑
+
+
4
2
N
SO
O
2
2
↑
↑
+
+
2
2
H
H
2
2
O
O
2
CO
C+H O
高温
C O+H(生成水煤气)
2 2 点燃
2C+SiO
△
S i +2CO(制得粗硅)
2CO+O
2
2CO
2
2 △
CO+CuO Cu+CO
2△
3CO+Fe O 2Fe+3CO Si
2 3 2
△
Si(粗)+2Cl SiCl
CO+HO
催化剂
C O +H
2 4
2 2 2 △
△ SiCl +2H Si(纯)+4HCl
4 2
CO △
2 Si(粉)+O SiO
2 2
点燃
CO+2Mg 2MgO+C △
2 Si+C SiC(金刚砂)
CO+H O=HCO Si+2NaOH+H O=NaSiO+2H
2 2 2 3 2 2 3 2
SiO
CO+2NaOH(过量)=NaCO+H O 2
2 2 3 2 △
2C+SiO Si+2CO
2
CO(过量)+NaOH=NaHCO
2 3 电炉
3C+SiO SiC+2CO↑
CO+Ca(OH) (过量)=CaCO ↓+H O 2
2 2 3 2 点燃
2Mg+SiO 2MgO+Si
2CO(过量)+Ca(OH) =Ca(HCO ) 2
2 2 3 2
4HF+SiO =SiF+2H O
CO+2NaAlO+3H O=2Al(OH) ↓+Na CO 2 4 2
2 2 2 3 2 3 △
SiO+2H Si+2H O
CO+C HONa+H O=C HOH+NaHCO 2 2 2
2 6 5 2 6 5 3 △
SiO+2Mg 2MgO+Si
CO+Na O=NaCO 2
2 2 2 3 高温
SiO+CaO CaSiO
2CO+2Na O=2NaCO+O 2 3
2 2 2 2 3 2
CO+NH+NaCl+HO=NaHCO ↓+NHCl(侯氏制碱 SiO+2NaOH=NaSiO+H O(常温下强碱缓慢腐蚀玻
2 3 2 3 4 2 2 3 2
法)
璃)
H 2 CO 3 高温
H 2 CO 3 =CO 2 ↑+H 2 O SiO 2 +Na 2 CO 3 Na 2 SiO 3 +CO 2
高温
SiO+CaCO CaSiO +CO
2.硅 2 3 3 2
2NaOH+SiO =NaSiO+H O
2 2 3 2
二、氧族元素
1.氧 △
6FeO+O 2Fe O
2 3 4
O 2HSO +O =2HSO
2 2 3 2 2 4
点燃
O 2 +2H 2 2H 2 O 4Fe(OH) 2 +O 2 +2H 2 O=4Fe(OH) 3
△
O+K KO 2NaSO +O =2NaSO
2 2 2 3 2 2 4
点燃
2O+3Fe Fe O O
2 3 4 3
点燃 2O=3O
O+S SO 3 2
2 2 O
3
+2HI==I
2
+O
2
+H
2
O
O+N 2NO
2 2 HO
2
3O 2O
2 3 2F+2H O=4HF+O
2 2 2
点燃
4P+5O 2PO
2 2 5 Cl
2
+H
2
O=HCl+HClO
点燃
C+O (足量) CO
2 2 2Na+2HO=2NaOH+H ↑
2 2
△
Si+O SiO
2 2 Mg+2HO=Mg(OH)+H ↑
2 2 2
4Na+O 2 =2Na 2 O 3Fe+4H 2 O(g) 高温 F e 3 O 4 +4H 2
△
电解
2Na 2 O+O 2 2Na 2 O 2 2H 2 O 2H 2 ↑+O 2
2Na+O=NaO
2 2 2 SO +H O=HSO
2 2 2 3
点燃
2Mg+O 2MgO
2 SO +H O=HSO
3 2 2 4
点燃
4Al+3O 2 2Al 2 O 3 3NO +H O=2HNO+NO
2 2 3
4NH 3 +5O 2
催化剂
4 N O+6H 2 O NO+H O=2HNO
△ 2 5 2 3
△
2SO +O 2SO PO+H O(冷)=2HPO
2 2 3 2 5 2 3
点燃
2CO+O 2CO PO+3H O(热)=2HPO
2 2 2 5 2 3 4
CO+H O=HCO
2 2 2 3HO SO +Ca(OH) =CaSO+H O
2 2 3 2 4 2
2HO=2HO+O↑ SO +Na O=NaSO
2 2 2 2 3 2 2 4
HO+Cl=2HCl+O SO +2KI=KSO +I
2 2 2 2 3 2 3 2
5HO+2KMnO +6HCl=2MnCl +2KCl+5O↑+8HO HS
2 2 4 2 2 2 2
HS+Cl =2HCl+S↓
2.硫 2 2
HS+Mg=MgS+H
S 2 2
△
S+H 2 H 2 S 2H 2 S+3O 2 (足量)=2SO 2 +2H 2 O
2S+C
△
C S 2 2H 2 S+O 2 (少量)=2S+2H 2 O
△
2HS+SO=3S+2HO
S+Fe FeS 2 2 2
△
HS+HSO (浓)=S↓+SO+2H O
S+2Cu Cu S 2 2 4 2 2
2
△
△ HS H+S
3S+2Al Al
2
S
3
2 2
3HS+2HNO (稀)=3S↓+2NO+4HO
△ 2 3 2
S+Zn ZnS
5HS+2KMnO +3H SO =2MnSO +K SO +5S+8H O
点燃 2 4 2 4 4 2 4 2
S+O SO
2 2 3HS+KCr O+4H SO =Cr (SO )+K SO +3S+7H O
S+6HNO (浓)=HSO +6NO↑+2H O 2 2 2 7 2 4 2 4 3 2 4 2
3 2 4 2 2
HS+4Na O+2H O=NaSO +6NaOH
3S+4HNO (稀)=3SO ↑+4NO↑+2H O 2 2 2 2 2 4
3 2 2
△ HS+Fe=FeS+H↑
3S+6NaOH 2NaS+Na SO +3H O 2 2
2 2 3 2
S+2Na=Na 2 S(爆炸) H 2 S+CuCl 2 =CuS↓+2HCl
S+Mg=MgS
△ H
2
S+2AgNO
3
=Ag
2
S↓+2HNO
3
S+Fe FeS
S+2H 2 SO 4 (浓)=3SO 2 ↑+2H 2 O H 2 S+HgCl 2 =HgS↓+2HCl
HS+Pb(NO )=PbS↓+2HNO
2 3 2 3
SO 2 H 2 S+4NO 2 =4NO+SO 3 +H 2 O
SO +2H S=3S+2HO
2 2 2
△ HSO
2 3
2SO +O 2SO
2 2 3
2SO 2 +O 2 +2H 2 O=2H 2 SO 4 H 2 SO 3 +X 2 +H 2 O=H 2 SO 4 +2HX(X表示Cl 2 、Br 2 、I 2 )
SO 2 +Cl 2 +2H 2 O=H 2 SO 4 +2HCl 2H 2 SO 3 +O 2 =2H 2 SO 4
SO 2 +Br 2 +2H 2 O=H 2 SO 4 +2HBr H 2 SO 3 +H 2 O 2 =H 2 SO 4 +H 2 O
SO 2 +I 2 +2H 2 O=H 2 SO 4 +2HI 5H 2 SO 3 +2KMnO 4 =2MnSO 4 +K 2 SO 4 +2H 2 SO 4 +3H 2 O
SO 2 +NO 2 =SO 3 +NO H 2 SO 3 +2FeCl 3 +H 2 O=H 2 SO 4 +2FeCl 2 +2HCl
SO 2 +2H 2 S=3S+2H 2 O H 2 SO 3 =H 2 O+SO 2 ↑
SO 2 +H 2 O=H 2 SO 3 2H 2 SO 3 +2H 2 S=3S↓+2H 2 O
SO 2 +2NH 3 +H 2 O=(NH 4 ) 2 SO 3 H 2 SO 4
Zn+H SO =ZnSO +H ↑
2 4 4 2
SO 2 +(NH 4 ) 2 SO 3 +H 2 O=2NH 4 HSO 3 Fe+H 2 SO 4 =FeSO 4 +H 2 ↑
Mg+HSO =MgSO +H ↑
SO +Ca(OH) =CaSO↓+H O 2 4 4 2
2 2 3 2 2Al+3H SO =Al (SO )+3H ↑
2 4 2 4 3 2
(不能用澄清石灰水鉴别SO 和CO.可用品红鉴别) △
2 2 2Al+6H SO (浓) Al (SO )+3SO↑+6H O
2 4 2 4 3 2 2
2NaOH+SO 2 (少量)=Na 2 SO 3 +H 2 O 2NH 3 +H 2 SO 4 =(NH 4 ) 2 SO 4
△
NaOH+SO 2 (足量)=NaHSO 3 2Al+6H 2 SO 4 (浓) Al 2 (SO 4 ) 3 +3SO 2 ↑+6H 2 O
Cl+SO+2H O=HSO +2HCl HS+HSO (浓)=S↓+SO+2H O
2 2 2 2 4 2 2 4 2 2
SO 3 P 2 O 5 +3H 2 SO 4 (浓)=2H 3 PO 4 +3SO 3
SO +H O=HSO BaO+H SO (稀)=BaSO+H O)
3 2 2 4 2 2 4 4 2 2
SO +MgO=MgSO NaO+H SO (冷、稀)=NaSO +H O
3 4 2 2 2 4 2 4 2 2MgO+H SO =MgSO +H O △
2 4 4 2 HSO (浓)+2HI SO +I +2H O
2 4 2 2 2
Al O+3H SO =Al (SO )+3H O
2 3 2 4 2 4 3 2 HSO (浓)+CaF =CaSO+2HF↑
△ 2 4 2 4
2HSO (浓)+C CO↑+2SO↑+2H O △
2 4 2 2 2 HSO (浓)+NaCl NaHSO+HCl↑
2 4 4
2HSO (浓)+S=3SO ↑+2H O
2 4 2 2 HSO (浓)+2NaCl NaSO +2HCl
2 4 2 4
6HSO (浓)+2Fe=Fe (SO )+3SO↑+6H O △
2 4 2 4 3 2 2 HSO (浓)+NaNO NaHSO+HNO ↑
2HSO (浓)+Cu
△
C uSO +SO↑+2H O
2 4 3 4 3
2 4 4 2 2
△ 3H 2 SO 4 (浓)+Ca 3 (PO 4 ) 2 =3CaSO 4 +2H 3 PO 4
HSO (浓)+2HBr SO +Br +2H O
2 4 2 2 2
2HSO (浓)+Ca (PO )=2CaSO+Ca(H PO )
2 4 3 4 2 4 2 4 2
第四部分 有机反应
一、烃
1.甲烷
CaO
甲烷的制取:CHCOONa+NaOH NaCO+CH ↑
3 △ 2 3 4
烷烃通式:C H
n 2n-2
(1)氧化反应 点燃
甲烷的燃烧:CH+2O CO+2H O
4 2 2 2
甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应
光
一氯甲烷:CH+Cl CHCl+HCl
4 2 光 3
二氯甲烷:CHCl+Cl CHCl+HCl
3 2 光 2 2
三氯甲烷:CHCl+Cl CHCl +HCl(CHCl 又叫氯仿)
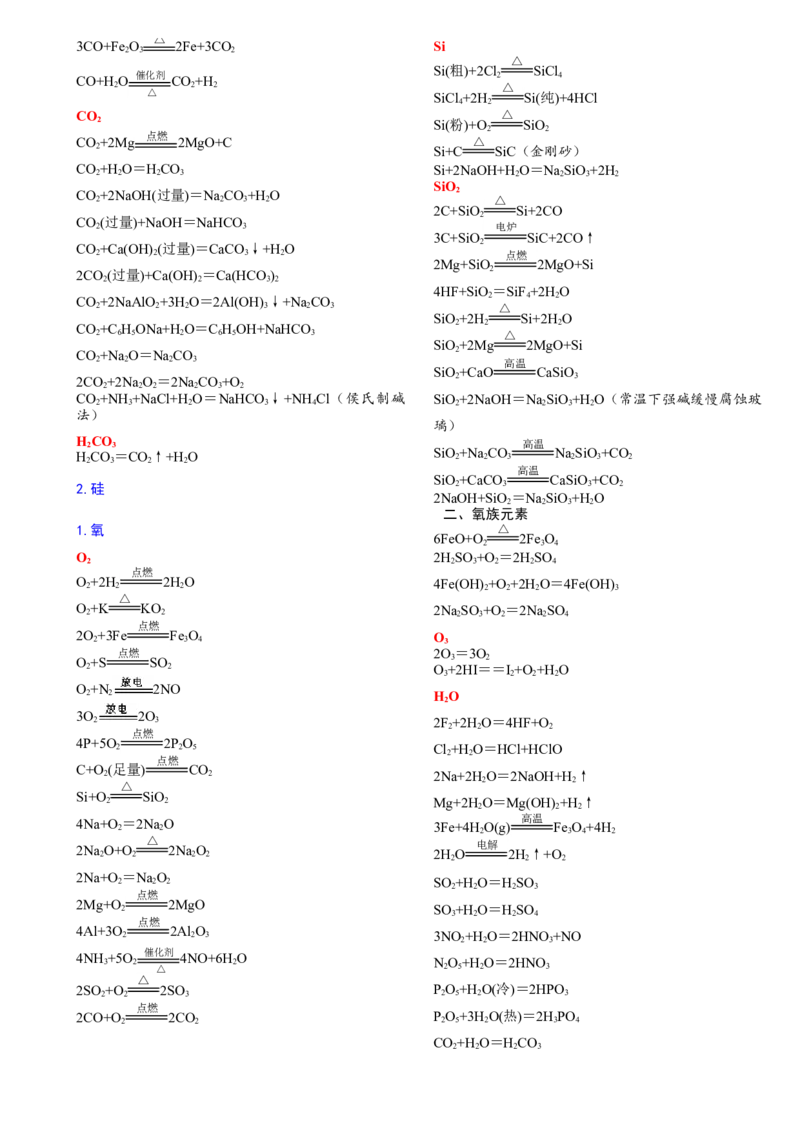
2 2 2 光 3 3 图1 乙烯的制取
四氯化碳:CHCl +Cl CCl +HCl
3 2 4
(3)分解反应
高温
甲烷分解:CH C+2H
4 2
2.乙烯
浓硫酸
乙烯的制取:CH 3 CH 2 OH 1 7 0 ℃ H 2 C=CH 2 ↑+H 2 O
烯烃通式:C H
n 2n
(1)氧化反应
高温
乙烯的燃烧:HC=CH +3O 2CO+2H O
2 2 2 2 2
乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应
与溴水加成:HC=CH +Br CHBr—CHBr
2 2 2 催化剂 2 2
与氢气加成:HC=CH +H CHCH
2 2 2 △ 3 3
与氯化氢加成:HC=CH +HCl CHCHCl
2 2 3 2
与水加成:HC=CH +H O CHCHOH
2 2 2 3 2
(3)聚合反应
一定条件
乙烯加聚,生成聚乙烯:n H 2 C=CH 2 C H 2 - C H n2
3.乙炔
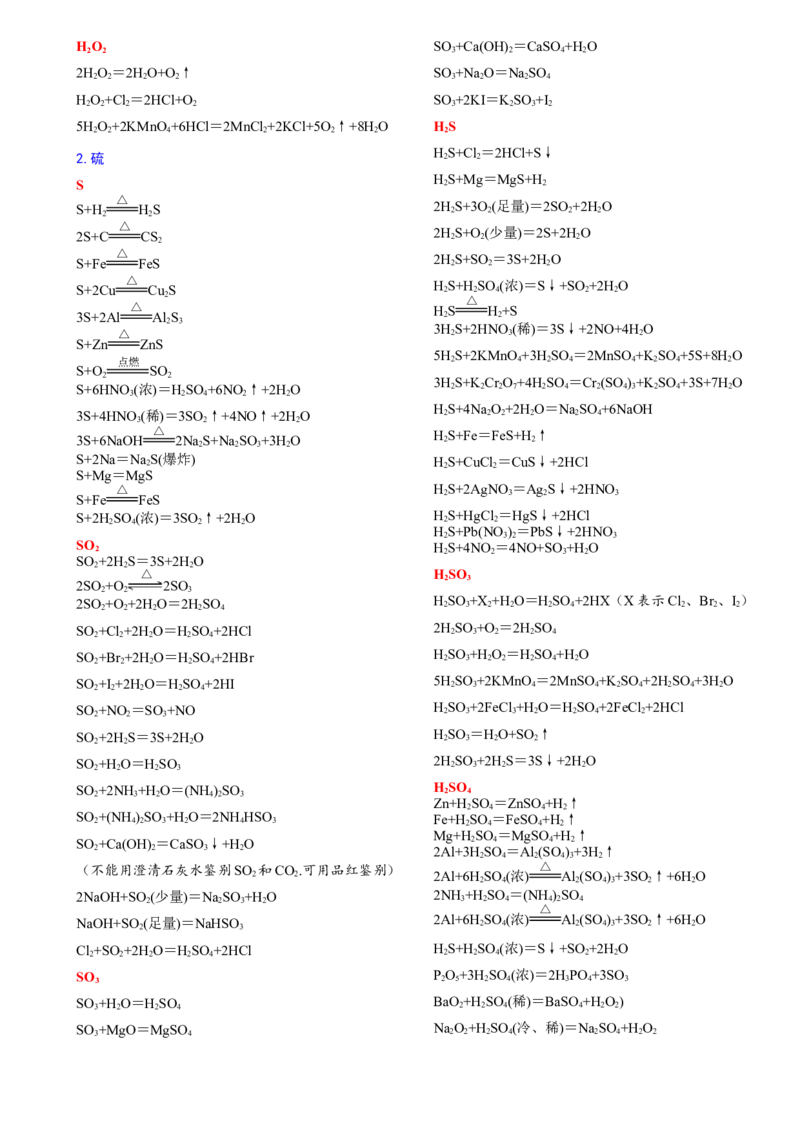
乙炔的制取:CaC +2H O HC≡CH↑+Ca(OH)
2 2 2
炔烃的通式:C H
n 2n-2
图2 乙炔的制取(1)氧化反应
点燃
乙炔的燃烧:HC≡CH+5O 4CO+2H O
2 2 2
乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应
与溴水加成:HC≡CH+Br HC=CH
2
Br Br
CHBr=CHBr+Br CHBr —CHBr
2 2 2
与氢气加成:HC≡CH+H HC=CH
2 2 2
催化剂
与氯化氢加成:HC≡CH+HCl CH=CHCl
△ 2 Cl
(3)聚合反应
一定条件
氯乙烯加聚,得到聚氯乙烯:nCH 2 =CHCl C H 2 — C H n 注意:制取乙烯、乙炔均用排水
乙炔加聚,得到聚乙炔:n HC≡CH 一 定 条 件 C H = C H 法收集;乙烯、乙炔的加成反应
n
一般都需要催化剂(溴除外)。
4.苯
苯的同系物通式:C H
n 2n-6
(1)氧化反应
点燃
苯的燃烧:2C H+15O 12CO+6H O
6 6 2 2 2
苯不能使溴水和酸性高锰酸钾溶液褪色。
(2)取代反应
①苯与溴反应
Fe —Br
+Br +HBr
2
(溴苯)
②硝化反应
浓H 2 SO 4 —NO
+HO—NO 2 6 0 ℃ +H 2 2 O
(硝基苯)
苯硝化反应生成硝基苯,它是一种带有苦杏仁味、无色油状液体,有毒。
③磺化反应
70℃~80℃ —SO H
3
+HO—SO H +H O
3 2
(苯磺酸)
(3)加成反应
催化剂
+3H
2 △
(环己烷)
苯还可以和氯气在紫外光照射下发生加成反应,生成C HCl(剧毒农药)。
6 6 6
5.甲苯
(1)氧化反应
点燃
甲苯的燃烧:C H+9O 7CO+4H O
7 8 2 2 2
甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色。
(2)取代反应
CH CH
3 3
| |
浓硫酸
O N— —NO
+3HNO 2 2 +3H O
3 2
|
NO
2甲苯硝化反应生成2,4,6-三硝基甲苯,简称三硝基甲苯,又叫梯恩梯(TNT),
是一种淡黄色晶体,不溶于水。它是一种烈性炸药,广泛用于国防、开矿等。
CH CH
3 3
| |
+3H SO HO 3 S— —SO 3 H +3H 2 O
2 4
|
SO H
3
注意:甲苯在光照条件下发生侧链的取代,而在催化剂条件下发生苯环上的取代。
(3)加成反应
CH
| 3
催化剂
注意:甲醇、乙醇为可再生能源,
+3H —CH
2 △ 3 甲醇有毒;乙二醇和丙三醇无色、
(甲基环己烷)
粘稠、有甜味、与水和酒精以任
意比互溶,丙三醇(甘油)还有护
肤作用。
二、烃的衍生物
6.溴乙烷
纯净的溴乙烷是无色液体,沸点38.4℃,密度比水大。
(1)取代反应
NaOH
溴乙烷的水解:C H—Br+H O C H—OH+HBr
2 5 2 2 5
(2)消去反应
醇
溴乙烷与NaOH溶液反应:CHCHBr+NaOH CH=CH ↑+NaBr+H O
3 2 △ 2 2 2
注意:检验卤代烃中的卤原子时,需取水解液滴入HNO 酸化,再滴加AgNO
3 3
溶液。一是中和多余的NaOH,二则检验沉淀是否溶于稀硝酸。
7.乙醇
(1)与钠反应
乙醇与钠反应:2CHCHOH+2Na 2CHCHONa+H ↑(乙醇钠)
3 2 3 2 2
(2)氧化反应
乙醇的燃烧:CHCHOH+3O 2CO+3H O
3 2 2 催化剂 2 2
乙醇的催化氧化:2CHCHOH+O 2CHCHO+2H O (乙醛)
3 2 2 △ 3 2
注意:当2-丙醇发生催化氧化时,会生成丙酮,而非丙醛。
OH O
| 催化剂 ||
2CH—CH—CH+O 2CH—C—CH+2H O
3 3 2 △ 3 3 2
(丙酮)
(3)消去反应
乙醇在浓硫酸作催化剂的条件下,加热到170℃生成乙烯。
注意:该反应加热到140℃时,乙醇进行另一种脱水方式,生成乙醚。
浓硫酸
2C HOH C H—O—C H+H O (乙醚)
2 5 140℃ 2 5 2 5 2
(4)取代反应
H+
乙醇与卤化氢取代:CHCHOH+HBr CHCHBr+H O
3 2 3 2 2
注意:乙醇不可以和卤素单质发生取代反应。
8.苯酚
苯酚是无色晶体,露置在空气中会因氧化显粉红色。苯酚具有特殊的气味,熔点43℃,水中溶解度不大,易溶于有机溶剂。苯酚有毒,是一种重要的化工原料。
(1)苯酚的酸性
—OH —ONa
+NaOH +H O
2
(苯酚钠)
苯酚(俗称石炭酸)的电离:
—OH —O -
+H O +H O+
2 3
苯酚钠与CO 反应:
2
注意:凡是含有羟基的有机物,
—ONa —OH 一般均可与钠反应。
+CO +H O +NaHCO 溴水与酚类易取代,不易
2 2 3
加成,且易在苯环邻、对位上取
代。
注意:该反应只能生成NaHCO ,因为 酸性弱于苯酚。
3
(2)取代反应 OH
|
—OH Br— —Br
+3Br ↓+3HBr
2
| (三溴苯酚)
Br
(3)显色反应
苯酚能和FeCl 溶液反应,使溶液呈紫色。
3
9.乙醛
乙醛是无色,具有刺激性气味的液体,沸点20.8℃,密度比水小,易挥发。
(1)加成反应
O
|| 催化剂
乙醛与氢气反应:CH—C—H+H CHCHOH
3 2 △ 3 2
(2)氧化反应
点燃
乙醛的燃烧:2CHCHO+5O 4CO+4H O
3 2 2 2
O
||
催化剂
乙醛的催化氧化:2CH—C—H+O 2CHCOOH (乙酸)
3 2 △ 3
乙醛的银镜反应:
△
CH3CHO +2Ag(NH3)2OH CH3COONH4+2Ag+3NH3+H2O (乙酸铵)
注意:硝酸银与氨水配制而成的银氨溶液中含有Ag(NH)OH(氢氧化二氨合银),
3 2
这是一种弱氧化剂,可以氧化乙醛,生成Ag。有关制备的方程式:
Ag++NH·H O===AgOH↓+
3 2
AgOH+2NH·H O===[Ag(NH)]++OH-+2H O
3 2 3 2 2
△
乙醛还原氢氧化铜:CHCHO+2Cu(OH) CHCOOH+Cu O+2HO
3 2 3 2 2
(3)
一定条件 [ ]
乙醛自身加聚:nCHCHO —CH—O— (聚乙醛)
3
|
n
CH
3 OH
|
催化剂 [ ]
—OH
甲醛与苯酚反应:nHCHO + n △ — — C H 2 — n + 2nH 2 O (酚醛树脂)10.乙酸
(1)乙酸的酸性
乙酸的电离:CHCOOH CHCOO-+H+
3 3
(2)酯化反应
O O
|| 浓硫酸 ||
CH—C—OH+C H—OH CH—C—OC H+H O (乙酸乙酯)
3 2 5 △ 3 2 5 2
注意:酸和醇起作用,生成酯和水的反应叫做酯化反应。
附加:酯化反应简介
(1)反应条件:一般需加热,用浓硫酸作催化剂和吸水剂。
(2)反应物:醇是任意的醇,酸既可以是有机酸,也可以是无机含氧酸。如:
CH —OH CH —ONO
2 2 2
| 催化剂 |
3HO—NO +C H — O H +3HCOH—ONO
3 | △ 2| 2
CH —OH CH —ONO
2 2 2
(3)反应机理:一般是羧酸脱羟基醇脱氢,且羧基与醇羟基数目比为1:1。如:
O=C—OH H —OC H 浓硫酸 O=C—OC H
2 5 2 5
| + |
△ +2H O
O=C—OH H—OC H O=C—OC H 2
2 5 2 5
(乙二醇二乙酯)
(4)反应方式
<1>一元醇与一元羧酸按通式反应;
R—COOH+HO—R’→RCOOR’+H O
2
<2>二元羧酸与二元醇,可以酯化成链,并形成高分子化合物。如:
O O
浓硫酸 [|| || ]
nHO—CH 2 CH 2 —OH+nHOOC— — C O O H △ —C— — C — O C H 2 C H 2 — O — n +2nH 2 O
也可酯化成环状小分子酯。
O O
|| ||
浓硫酸
C—C + CH—CH
| | | 2 | 2 △
OHOH OH OH
<3>羟基羧酸可自身酯化成环状内酯。如:
O
浓硫酸 ||
CH—CH—COOH CH—C + HO
2 2 △ 2 2
| | |
OH CH —
2
也可分子间酯化形成环状小O分子酯或链状高分子化合物(酯),如:
浓硫酸
2CH 3 —CH—COOH △
|
OH
CH 3 CH 3 O
| [ | ||]
nHO—CH—COOH —O—CH—C— n+nH
2
O11.乙酸乙酯
乙酸乙酯是一种带有香味的无色油状液体。
(1)水解反应
无机酸
CHCOOC H+H O CHCOOH+C HOH
3 2 5 2 3 2 5
(2)中和反应
CHCOOC H+NaOH CHCOONa+C HOH
3 2 5 3 2 5
附加:烃的衍生物的转化
水解
酯化
氧化 酯化
卤代烃 水解 醇 醛 氧化 羧酸 酯RCOOR’
还原 水解
R—X R—OH R—CHO RCOOH
加
成 消 加
消 去 成
去
不饱和烃
三、糖类、油脂、蛋白质
12.葡萄糖
结构:CHOH—CHOH—CHOH—CHOH—CHOH—CHO
2
物理性质:白色晶体,易溶于水,有甜味。
化学性质:①具有还原性:能发生银镜反应,能与新制的氢氧化铜反应;②加成
反应:与H 反应;③酯化反应:与羧酸反应;④分解反应:在酒化酶作用下,分
2
解为乙醇和CO;⑤燃烧生成CO 和HO。
2 2 2
葡萄糖的燃烧:C H O+6O →6CO+6H O
6 12 6 2 2 2
葡萄糖的氧化:CHOH(CHOH) CHO+2Ag(NH)OH CHOH(CHOH) COONH+2Ag↓ + 3NH + H O
2 4 3 2 2 4 4 3 2
CHOH(CHOH) CHO+2Cu(OH) CHOH(CHOH) COOH + Cu O↓+ 2H O
2 4 2 2 4 2 2
葡萄糖的还原:CHOH(CHOH) + H CHOH(CHOH) CHOH
2 4 2 2 4 2
葡萄糖的分解:C H O 2CHCHOH + 2CO
6 12 6 3 2 2
13.蔗糖、麦芽糖
催化剂
蔗糖的水解:C H O +H O——→C H O+C H O
12 22 11 2 6 12 6 6 12 6
蔗糖 葡萄糖 果糖
催化剂
麦芽糖的水解:C H O +H O——→2C H O
12 22 11 2 6 12 6
麦芽糖 葡萄糖
注意:蔗糖不含醛基,不可以发生银镜反应;麦芽糖可以发生银镜反应。
14.淀粉、纤维素
催化剂
淀粉的水解:(C H O)+nHO——→nC H O
6 10 5 n 2 6 12 6
淀粉 葡萄糖
催化剂
葡萄糖分解:C H O——→2C HOH+2CO
6 12 6 2 5 2
葡萄糖 乙醇
催化剂
纤维素的水解:(C H O)+nHO——→nC H O
6 10 5 n 2 6 12 6
纤维素 葡萄糖淀粉的酯化反应:
15.油脂
(1)氢化反应
C H COO—CH C H COO—CH
17 33 2 17 35 2
| 催化剂 |
C 17 H 33 COO — | CH+ 3 H 2 加 热 、 加 压 C 17 H 35 COO — | CH
C H COO—CH C H COO—CH
17 3 3 2 17 3 5 2
油酸甘油酯(油) 硬脂酸甘油酯(脂肪)
(2)水解反应
C H COO—CH CH —OH
17 35 2 2
| |
浓硫酸
C H COO — CH + 3H O CH —OH
17 35 2
| |
3C H COOH +
C 1H7 3C5OO—CH CH —OH
17 35 2 2
硬脂酸甘油酯 硬脂酸 甘油
皂化反应:
C H COO—CH CH —OH
17 35 2 2
| |
浓硫酸
C H COO — CH + 3NaOH C H —OH
17 35
| |
3C H COONa +
C 1H7 3C5OO—CH CH —OH
17 35 2 2
硬脂酸甘油酯 硬脂酸钠
16.氨基酸
氨基酸中的—NH 和—COOH发生脱水缩合,生成多肽。
2
+ + HO
2
甘氨酸
+ + HO
2
丙氨酸
+ + HO
2
+ + HO
2
(两种不同的氨基酸进行缩合,可产生4种不同的多肽)第五部分 离子反应 (按字母顺序排列)
Al CHOH(CHOH) COO-+ +2Ag↓+3NH+H O
2 4 3 2
2Al+6H+=2Al3++3H 2 ↑ Ba
2Al+2OH-+2H 2 O=2 +3H 2 ↑ Ba2++ =BaSO↓
4
Al3++3H 2 O Al(OH) 3 +3H+ Ba2++ =BaCO ↓
3
Al3++3OH-=Al(OH)
3
↓
3Ba2++2 =Ba (PO )↓
3 4 2
Al3++4OH-= +2H 2 O Ba2++2OH-+CO =BaCO ↓+H O
2 3 2
3Al3++10OH-错误: 引用源未找到2Al(OH) 3 ↓+ +2H 2 O Ba2++2OH-+2H++ =BaSO↓+2HO(NaHSO 溶液
4 2 4
(当n(AlCl
3
)/n(NaOH)=3:10时)
中加Ba(OH) ,使溶液呈中性)
2
Al3++3NH 3 ·H 2 O=Al(OH) 3 ↓+3 Ba2++OH-+H++ =BaSO↓+H O(NaHSO 溶液中
4 2 4
2Al3++3 +3H O=2Al(OH) ↓+3CO ↑
2 3 2 加Ba(OH) ,使Ba2+全部沉淀)
2
Al3++3 =Al(OH) ↓+3CO ↑
3 2 BaCO+2H+=Ca2++CO ↑+H O
3 2 2
Al3++3HS-+3H O=Al(OH) ↓+3H S↑
2 3 2 Br
2Al3++3S2-+6H 2 O=2Al(OH) 3 ↓+3H 2 S↑ 2Br-+Cl=2Cl-+Br
2 2
Al3++3 +6H O=4Al(OH) ↓
2 3 Br +SO+2H O=2Br-+2H++
2 2 2
2Al3++3 错误: 引用源未找到Al (SiO)↓
2 3 2 4Br-+2Fe2++3Cl 2Fe3++2Br +6Cl-(足量
2错误: 引用源未找到 2
+2H O Al(OH) +OH-
2 3 Cl)
2
+H++H O=Al(OH) ↓
2 3 2Br-+2Fe2++2Cl 2Fe3++Br +4Cl-(当
2错误: 引用源未找到 2
+4H+=Al3++2H O
2 n(FeBr)/n(Cl )=1:1时)
2 2
9 +30H+错误: 引用源未找到2Al(OH) ↓+7Al3++12H O
3 2 10Br-+6Fe2++8Cl 6Fe3++5Br +16Cl-(当
2错误: 引用源未找到 2
(当n(NaAlO )/n(HCl)=3:10时)
2 n(FeBr )/n(Cl )=3:4时)
2 2
3 +Fe3++6H O=Fe(OH) ↓+3Al(OH) ↓
2 3 3 C
+ +H O=Al(OH) ↓+NH↑
2 3 3 +2Ag+错误: 引用源未找到Ag CO↓
2 3
+ +H O=Al(OH) ↓+
2 3 +Ba2+错误: 引用源未找到BaCO↓
3
2 +CO +3HO=2Al(OH) ↓+
2 2 3 +Ca2+错误: 引用源未找到CaCO↓
3
+CO +2HO=Al(OH) ↓+
2 2 3 +2H+错误: 引用源未找到CO↑+HO
2 2
Al 2 O 3 +6H+=2Al3++3H 2 O +H O +OH-
2
Al O+2OH-=2 +H O
2 3 2 3 +2Al3++3H O=2Al(OH) ↓+3CO ↑
2 3 2
Al(OH) +3H+=Al3++2H O
3 2 3 +2Fe3++3H O=2Fe(OH) ↓+3CO ↑
2 3 2
Al(OH) +2OH-= +2H O
3 2 CO+ +3HO=2Al(OH) ↓+
2 2 3
Ag
CO+ +2HO=Al(OH) ↓+
2 2 3
Ag++H O AgOH+H+
2 CO+OH-=
2
Ag++NH 3 ·H 2 O=AgOH↓+ CO+Ba2++2OH-=BaCO ↓+H O
2 3 2
Ag++2NH 3 ·H 2 O= +H 2 O CO+2OH-= +H O
2 2
Ag++Cl-错误: 引用源未找到AgCl↓
3CO+5OH-错误: 引用源未找到2 + +2H O(当
2 2
Ag++Br-错误: 引用源未找到AgBr↓
n(CO)/n(NaOH)=3:5时)
2
Ag++I-错误: 引用源未找到AgI↓
CO+ +2H O=HSiO↓+
2 2 4 4
3Ag++ 错误: 引用源未找到Ag PO ↓
3 4 Ca
2Ag++ 错误: 引用源未找到Ag CO↓
2 3 Ca2++2OH-+CO =CaCO ↓+H O
2 3 2
Ag CO+2H+错误: 引用源未找到2Ag++CO ↑+H O
2 3 2 2 Ca2++2OH-+SO=CaSO↓+H O
2 3 2
Ag PO +3H+错误: 引用源未找到3Ag++H PO
3 4 3 4 Ca2++2ClO-+SO+H O 错 误 : 引 用 源 未 找 到
2 2
2Ag[(NH )]++2OH-+CH CHO CHCOO-+
3 2 3 3 CaSO↓+HClO+H++Cl-(少量
4
+2Ag↓+3NH+H O
3 2 SO )
2
2Ag[(NH 3 ) 2 ]++2OH-+CH 2 OH(CHOH) 4 CHO Ca2++2ClO-+2SO +4HO 错 误 : 引 用 源 未 找 到
2 2CaSO↓+2Cl-+4H++ (足量SO ) +CO ↑+H O
4 2 2 2
Ca2++2ClO-+CO +H O错误: 引用源未找到 CHOH(CHOH) CHO+2Ag[(NH )]++2OH-
2 2 2 4 3 2
CaCO ↓+2HClO CHOH(CHOH) COO-+ +2Ag↓+3NH+H O
3 2 4 3 2
CaCO +2H+=Ca2++CO ↑+H O CHOH(CHOH) CHO+2Cu(OH)
3 2 2 2 4 2
Cl CHOH(CHOH) COOH+Cu O↓+2H O
2 4 2 2
Cl+H O=Cl-+H++HClO 5C H+12 +36H+ 错 误 : 引 用 源 未 找 到 12Mn2+
2 2 2 4
Cl+2OH-=Cl-+ClO-+H O +10CO ↑+28H O
2 2 2 2
Cl+2OH-=Cl-+ClO-+H O 5 +2 +16H+错误: 引用源未找到2Mn2+
2 2
Cl+2I-=2Cl-+I +10CO ↑+8H O
2 2 2 2
Cl+H SO +H O=2Cl-+ +4H+ Fe
2 2 3 2
Cl+H S=2Cl-+2H++S↓ Fe+2H+=Fe2++H↑
2 2 2
Cl+2Fe2+错误: 引用源未找到2Fe3++2Cl-(向FeBr 溶液中少量 Fe+Cu2+=Fe2++Cu
2 2
Cl) Fe+2Fe3+=3Fe2+
2
3Cl+2Fe2++4Br-错误: 引用源未找到2Fe3++2Br +6Cl-(足量 Fe2++2OH-=Fe(OH) ↓
2 2 2
Cl) 2Fe2++Cl=2Fe3++2Cl-
2 2
2Cl+2Fe2++2Br-错误: 引用源未找到2Fe3++Br +4Cl-(当 2Fe2++Br =2Fe3++2Br-
2 2 2
n(FeBr )/n(Cl )=1:1时) 4Fe2++O+4H+=Fe3++2HO
2 2 2 2
8Cl+6Fe2++10Br-错误: 引用源未找到6Fe3++5Br +16Cl-(当 12Fe2++3O+6HO=8Fe3++4Fe(OH) ↓
2 2 2 2 3
n(FeBr )/n(Cl )=3:4时) 2Fe2++H O+2H+=2Fe3++2H O
2 2 2 2 2
Cl+2I-错误: 引用源未找到2Cl-+I 6Fe2++ +14H+=6Fe3++2Cr3++7H O
2 2 2
Cl+2I-错误: 引用源未找到I+2Cl-(向FeI 溶液中通入少量 5Fe2++ +8H+=5Fe3++Mn2+4HO
2 2 2 2
Cl) 3Fe2++ +4H+=3Fe3++NO↑+2H O
2 2
3Cl+2Fe2++4I-错误: 引用源未找到2Fe3++2I +6Cl-(足量Cl) Fe2++S2-=FeS↓
2 2 2
4Cl+2Fe2++6I-错误: 引用源未找到2Fe3++3I+8Cl-(当 2Fe2++Cl 2Fe3++2Cl-(向FeBr 溶液中通入
2 2 2错误: 引用源未找到 2
n(FeI)/n(Cl )=3:4时) 少量Cl)
2 2 2
2Cl-+4H++MnO=Mn2++Cl↑+2H O 2Fe2++4Br-+3Cl 2Fe3++2Br +6Cl-(足量Cl)
2 2 2 2错误: 引用源未找到 2 2
Cl-+Ag+错误: 引用源未找到AgCl↓ 2Fe2++2Br-+2Cl 2Fe3++Br +4Cl-(当
2错误: 引用源未找到 2
ClO-+H+错误: 引用源未找到HClO n(FeBr )/n(Cl )=1:1时)
2 2
ClO-+SO+H O错误: 引用源未找到2H++Cl-+ 6Fe2++10Br-+8Cl 6Fe3++5Br +16Cl-(当
2 2 2错误: 引用源未找到 2
ClO-+H O HClO+OH- n(FeBr )/n(Cl )=3:4时)
2 2 2
Cr 2Fe2++4I-+3Cl 2Fe3++2I +6Cl-(向FeI 溶液
2错误: 引用源未找到 2 2
+6Fe2++14H+=6Fe3++2Cr3++7H O 中足量Cl)
2 2
Cu 2Fe2++6I-+4Cl 2Fe3++3I+8Cl- ( 当
2 错 误 : 引 用 源 未 找 到 2
Cu+2Fe3+=2Fe2++Cu2+ n(FeI)/n(Cl )=3:4时)
2 2
3Cu+2 +8H+=3Cu2++2NO↑+4HO Fe3++3OH-=Fe(OH) ↓
2 3
Cu2++2H O Cu(OH) +2H+ 2Fe3++Cu=2Fe2++Cu2+
2 2
Cu2++2NH·HO=Cu(OH) ↓+2NH+ 2Fe3++Fe=3Fe2+
3 2 2 4
Cu2++2Na+2H O 错 误 : 引 用 源 未 找 到 2Na+ 2Fe3++Zn=2Fe2++Zn2+
2
+Cu(OH) ↓+H ↑ 2Fe3++3Zn=2Fe+3Zn2+
2 2
Cu2++H
2
S错误: 引用源未找到2H++CuS↓ Fe3++3 =Fe(OH)
3
↓+3CO
2
↑
Cu2++Fe错误: 引用源未找到Cu+Fe2+ Fe3++3 +6H
2
O=Fe(OH)
3
↓+3Al(OH)
3
↓
Cu2++2OH-错误: 引用源未找到Cu(OH)
2
↓ 2Fe3++3 +3H
2
O=2Fe(OH)
3
↓+3CO
2
↑
CuO+2H+=Cu2++H O 2Fe3++H S=2Fe2++S↓+2H+
2 2
CHO 2Fe3++S2-=2Fe2++S↓
x y z
C 6 H 5 O-+H 2 O C 6 H 5 OH+OH- 2Fe3++2I-=2Fe2++I 2
C 6 H 5 O-+CO 2 =C 6 H 5 OH+ 2Fe3++SO 2 +2H 2 O=2Fe2++ +4H+
CHCHO+2Ag[(NH )]++2OH- CHCOO-+ Fe3++3SCN-= (红色溶液)
3 3 2 3
+2Ag↓+3NH +H O Fe3++3H O= (胶体)+3H+
3 2 2
CH 3 CHO+2Cu(OH) 2 CH 3 COOH+Cu 2 O↓+2H 2 O FeO+2H+=Fe2++H 2 O
2CH 3 COOH+CaCO 3错误: 引用源未找到 2CH 3 COO-+Ca2+ Fe 2 O 3 +6H+=Fe3++3H 2 OFe O+8H+=Fe2++2Fe3++4H O HS系列
3 4 2 2
FeS+2H+=Fe2++H S↑ HS H++HS-
2 2
HO HS- H++S2-
2
H++OH-=HO H++S2-=HS-
2
2HO+2Na=2Na++2OH-+H↑ H++HS-=HS
2 2 2
2HO+2NaO=4Na++4OH-+O ↑ HO+S2- HS-+
2 2 2 2 2
HO+NaO=2Na++2OH- HS-+H O HS+
2 2 2 2
HO+Cl =Cl-+H++HClO HS+OH-=HS-+HO
2 2 2 2
HO HS-+OH-=S2-+HO
2 2 2
HO+2I-+2H+=I+2HO HS+Cl =2Cl-+2H++S↓
2 2 2 2 2 2
H 2 O 2 +2Fe2++2H+=2Fe3++2H 2 O 2H 2 S+SO 2错误: 引用源未找到 3S↓+2H 2 O
5HO+2 +6H+=2Mn2++5O↑+8HO 2HS+O 2S↓+2H O
2 2 2 2 2 2错误: 引用源未找到 2
HO+Cl=2H++2Cl-+O↑ HS+Cu2+错误: 引用源未找到2H++CuS↓
2 2 2 2 2
HO+SO 2H++ HS+(CH COO) Pb错误: 引用源未找
2 2 2错误: 引用源未找到 2 3 2
HCO 系列 到PbS↓+2CH COOH
2 3 3
HCO H++ HS+2OH-=S2-+2HO
2 3 2 2
H++ 3HS-+Al3++3H O=Al(OH) ↓+3H S↑
2 3 2
HO+ + HSO 系列
2 2 3
+H O HCO+ HSO H++
2 2 3 2 3
+ = +HO H++
2
+H+=CO↑+HO +H O HSO +OH-
2 2 2 2 3
3 +Al3+=Al(OH) ↓+3CO ↑ +OH-= +HO
3 2 2
3 +Fe3+=Fe(OH) ↓+3CO ↑ +H+=SO↑+HO
3 2 2 2
2 +Ca2++2 =CaCO ↓+2HO+ (向 HSO +Cl+H O=2Cl-+ +4H+
3 2 2 3 2 2
NaHCO 溶液中加入少量澄清石灰水) I
3
+Ca2++ =CaCO ↓+H O(足量澄清石灰 2I-+2Fe3+=2Fe2++I
3 2 2
水) 2I-+Cl=2Cl-+I
2 2
+Ca2++ =CaCO ↓+H O(向Ca(HCO ) 2I-+Br =2Br-+I
3 2 3 2 2 2
溶液中加入少量NaOH溶液) I-+Ag+=AgI↓
2 +Ca2++2 =CaCO ↓+2HO+ 2I-+HO+2H+=I+2HO
3 2 2 2 2 2
(Ca(HCO ) 溶液中加入足量NaOH溶液) 5I-+IO-+6H+=3I+3H O
3 2 2 2
+ = +H O(向NH HCO 溶液中加 I+2OH-=I-+IO-+H O
2 4 3 2 2
入少量NaOH溶液) I+5Cl+6H O=12H++10Cl-+2
2 2 2
+ +2 = +H O+NH ·HO(向 Mg
2 3 2
NH HCO 溶液中加入足量NaOH溶液) Mg+2H+=Mg2++H↑
4 3 2
2 +SO
2错误: 引用源未找到
+CO
2
↑+H
2
O Mg2++2OH-=Mg(OH)
2
↓
+ +H O=Al(OH) ↓+ Mg2++ =MgCO ↓
2 3 3
HPO 系列 MgCO+2H+=Mg2++CO↑+HO
3 4 3 2 2
HPO H++ MgO+2H+=Mg2++H O
3 4 2
H++ Mg(OH) +2H+=Mg2++2HO
2 2
H++ Mn
HPO + = +H O MnO +2Cl-+4H+=Mn2++Cl↑+2H O
3 4 2 2 2 2
+ = +H O +5Fe2++8H+=5Fe3++Mn2+4HO
2 2
+ = +HO 2 +5SO+2H O错误: 引用源未找到2Mn2++5
2 2 2
+HO + +4H+
2
+H O + 2 +5HO+6H+错误: 引用源未找到2Mn2++5O ↑+8H O
2 2 2 2 2
+H O HPO + 12 +5C H+36H+ 错 误 : 引 用 源 未 找 到 12Mn2+
2 3 4 2 4
H++ = +10CO ↑+28H O
2 2
H++ = 2 +5 +16H+ 错 误 : 引 用 源 未 找 到 2Mn2+
H++ =HPO +10CO ↑+8H O
3 4 2 2Na PbO+2Cl-+4H+=Pb2++Cl↑+2H O
2 2 2
2Na+2HO=2Na++2OH-+H ↑ (CHCOO) Pb+HS错误: 引用源未找到PbS↓+2CH CO
2 2 3 2 2 3
2Na+Cu2++2H O 错 误 : 引 用 源 未 找 到 2Na+ OH
2
+Cu(OH) ↓+H ↑ S
2 2
NH 系列 3S+6OH-=2S2-+ +3HO
3 2
+H O NH ·HO+H+ S2-+H O HS-+OH-
2 3 2 2
2 + +H O=HSiO↓+2NH↑ 3S2-+2Al3++6H O=2Al(OH) ↓+3H S↑
2 4 4 3 2 3 2
+ +H O=Al(OH) ↓+NH↑ S2-+2Fe3+=2Fe2++S↓
2 3 3
+ +2OH- = +H O+NH ·HO ( 向 SO +Ca2++2ClO-+H O 错 误 : 引 用 源 未 找 到
2 3 2 2 2
NH HCO 溶液中加入足量NaOH溶液) CaSO↓+HClO+H++Cl-(少量SO )
4 3 4 2
NH +H O NH ·HO 2SO +Ca2++2ClO-+4HO 错 误 : 引 用 源 未 找 到
3 2 3 2 2 2
NH ·HO +OH- CaSO↓+2Cl-+4H++ (足量SO )
3 2 4 2
NH ·HO+Ag+=AgOH↓+NH+ SO +2Fe3++2H O=2Fe2++ +4H+
3 2 4 2 2
2AgOH=Ag O+HO(AgNO 溶液中加入少量氨水) SO +2 错误: 引用源未找到 +CO ↑+H O
2 2 3 2 2 2
2NH ·HO+Ag+=[Ag(NH)]++H O(足量氨水) SO +2OH-错误: 引用源未找到 +H O
3 2 3 2 2 2 2
2NH ·HO+Cu2+=Cu(OH) ↓+2 (向CuSO 溶液 SO +OH-=
3 2 2 4 2
中加入少量氨水) SO +Br +2H O=2Br-+2H++
2 2 2
4NH ·HO+Cu2+=[Cu(NH )]2++4H O(足量氨水) SO +I +2H O=2I-+2H++
3 2 3 4 2 2 2 2
2NH 3 ·H 2 O+Zn2+=Zn(OH) 2 ↓+2NH 4 +(向ZnCl 2 溶液中 SO 2 +H 2 O 2错误: 引用源未找到 2H++
加入少量氨水) 3SO +2 +2H O错误: 引用源未找到3 +2NO↑
2 2
4NH ·HO+Zn2+=[Zn(NH )]2++4H O(足量氨水) +4H+
3 2 3 4 2
3NH ·HO+Al3+=Al(OH) ↓+3 SO +ClO-+H O错误: 引用源未找到2H++Cl-+
3 2 3 2 2
SO +2H S错误: 引用源未找到3S↓+2H O
2 2 2
SO +H O HSO
2 2 2 3
2 +2I-+4H+=2NO↑+I 2 +2H 2 O 5SO 2 +2 +2H 2 O错误: 引用源未找到2Mn2++5
5 +2 +6H+=2Mn2++5 +3H O +4H+
2
+3Fe2++4H+=3Fe3++NO↑+2H 2 O +2H+=SO 2 ↑+H 2 O
2 +3SO 2 +2H 2 O错误: 引用源未找到3 +2NO +H 2 O +OH-
↑+4H+ +Ba2+=BaSO 4 ↓
2 +3Cu+8H+=3Cu2++2NO↑+4H 2 O +2H++Ba2++2OH-=BaSO 4 ↓+2H 2 O(NaHSO 4 溶
O 液中加Ba(OH) 2 ,使溶液呈中性)
+H+=H 2 O +H++Ba2++OH-=BaSO 4 ↓+H 2 O(NaHSO 4 溶液中
+CO 2 = 加Ba(OH) 2 ,使Ba2+全部沉淀)
O 2 +2H 2 S错误: 引用源未找到2S↓+2H 2 O +2H+错误: 引用源未找到S↓+SO 2 ↑+H 2 O
O+2S2-+4H+=S↓+2HO Si
2 2
O 2 +2HS-+2H+=S↓+2H 2 O Si+2OH-+H 2 O= +2H 2 ↑
O 2 +4Fe2++4H+=Fe3++2H 2 O SiO 2 +2OH-= +H 2 O
3O 2 +12Fe2++6H 2 O=8Fe3++4Fe(OH) 3 ↓ +2 +H 2 O=H 4 SiO 4 ↓+2NH 3 ↑
O 2 +2 错误: 引用源未找到2 +CO 2 +2H 2 O=H 4 SiO 4 ↓+CO 3 2-
O 3 +2I-+2H+=I 2 +O 2 +H 2 O +2H++H 2 O=H 4 SiO 4 ↓
P 3 +2Fe3+错误: 引用源未找到Fe 2 (SiO 3 ) 2 ↓
+3Ag+=Ag 3 PO 4 ↓ 3 +2Al3+错误: 引用源未找到Al 2 (SiO 3 ) 2 ↓
2 +3Ba2+=Ba(PO )↓ Zn
3 4 2
2 +3Ca2+=Ca 3 (PO 4 ) 2 ↓ Zn+2H+=Zn2++H 2 ↑
2 +3Mg2+=Mg 3 (PO 4 ) 2 ↓ Zn+2OH-= +H 2 ↑
+H+= Zn+2Fe3+=2Fe2++Zn2+(少量Zn片)
+2H+= 3Zn+2Fe3+=2Fe+3Zn2+(过量Zn片)
+3H+=H 3 PO 4 Zn2++2H 2 O Zn(OH) 2 +2H+
Pb2++ =PbSO
4
↓ Zn2++2OH-=Zn(OH)
2
↓
Pb2++S2-=PbS↓ Zn2++2NH
3
·H
2
O=Zn(OH)
2
↓+2 (少量氨水)Zn2++4NH·HO=[Zn(NH )]2++4H O(足量氨水) ZnO+2H+=Zn2++HO
3 2 3 4 2 2
Zn(OH) +2H+=Zn2++2HO ZnO+2OH= +HO
2 2 2
Zn(OH) +2OH= +2HO
2 2
第六部分 电极反应方程式
一、原电池电极反应方程式
1.Cu─HSO ─Zn原电池 正极 (PbO ) :PbO + 2e- + + 4H+ 错误: 引用源
2 4 2 2
正极: 2H+ + 2e- 错误: 引用源未找到 H ↑ 未找到 PbSO↓ + 2H O
2 4 2
负极: Zn—2e- 错误: 引用源未找到 Zn2+ 负极 (Pb) :Pb—2e- + 错误: 引用源未找到
总反应式: Zn + 2H+ == Zn2+ + H ↑ PbSO ↓
2 4
2.Cu─FeCl ─C原电池 总反应式:Pb + PbO + 4H+ + 2 错误: 引用源未
3 2
正极: 2Fe3+ + 2e- 错误: 引用源未找到 2Fe2+ 找到 2PbSO↓ + 2H O
4 2
负极: Cu —2e- 错误: 引用源未找到 Cu2+ 9.Al─NaOH─Mg原电池
总反应式: 2Fe3+ + Cu == 2Fe2+ + Cu2+ 正极:6HO + 6e- 错误: 引用源未找到 3H ↑+ 6OH-
2 2
3.钢铁在潮湿的空气中发生吸氧腐蚀 负极:2Al — 6e- + 8OH- 错误: 引用源未找到 2
正极:O + 2H O + 4e- 错误: 引用源未找到 4OH- + 4H O
2 2 2
负极:2Fe— 4e- 错误: 引用源未找到 2Fe2+ 总反应式:2Al + 2OH- + 2H O 错误: 引用源未找到 2
2
总反应式:2Fe + O + 2H O 错误: 引用源未找到 + 3H ↑
2 2 2
2Fe(OH) ↓ 10.CH 燃料电池(碱性介质)
2 4
4.钢铁在潮湿的空气中发生析氢腐蚀 正极:2O + 4H O + 8e- 错误: 引用源未找到 8OH-
2 2
正极:2H+ +2e- == H↑ 负极:CH —8e- + 10OH- 错误: 引用源未找到 +
2 4
负极:Fe —2e- == Fe2+ 7HO
2
总反应式:Fe +2H+ == Fe2+ +H ↑ 总反应式:CH + 2O + 2OH- 错误: 引用源未找到
2 4 2
5.氢氧燃料电池(中性介质) + 3H O
2
正极:O + 2H O + 4e- 错误: 引用源未找到 4OH- 11.熔融碳酸盐燃料电池
2 2
负极:2H—4e-错误: 引用源未找到 4H+ (LiCO 和NaCO 熔融盐作电解液,CO作燃料):
2 2 3 2 3
总反应式:2H + O 错误: 引用源未找到 2H O 正极:O + 2CO + 4e- 错误: 引用源未找到 2
2 2 2 2 2
6.氢氧燃料电池(酸性介质) (持续补充CO 气体)
2
正极:O + 4H+ + 4e- 错误: 引用源未找到 2H O 负极:2CO + 2 — 4e- 错误: 引用源未找到
2 2
负极:2H — 4e-错误: 引用源未找到 4H+ 4CO
2 2
总反应式:2H + O 错误: 引用源未找到 2H O 总反应式:2CO + O 错误: 引用源未找到 2CO
2 2 2 2 2
7.氢氧燃料电池(碱性介质) 12.银锌纽扣电池(碱性介质)
正极:O + 2H O + 4e- 错误: 引用源未找到 4OH- 正极 (Ag O) :Ag O + HO + 2e- == 2Ag + 2OH-
2 2 2 2 2
负极:2H — 4e- + 4OH- 错误: 引用源未找到 4H O 负极 (Zn) :Zn + 2OH- —2e- == ZnO + H O
2 2 2
总反应式:2H + O 错误: 引用源未找到 2H O 总反应式:Zn + Ag O == ZnO + 2Ag
2 2 2 2
8.铅蓄电池(放电)
二、电解电极反应方程式
1.电解CuCl 溶液 阴极(待镀金属,如Fe):Cu2+ + 2e- 错误: 引用源未
2
阳极:2Cl- — 2e- 错误: 引用源未找到 Cl↑ 找到 Cu
2
阴极:Cu2+ + 2e- 错误: 引用源未找到 Cu 总反应式:无
电解
总反应式:2Cl- + Cu2+ ==== Cl↑ + Cu 4.电解饱和食盐水
2
2.电解精炼铜 阳极:2Cl- —2e- 错误: 引用源未找到 Cl↑
2
阳极(粗铜):Cu —2e- 错误: 引用源未找到 Cu2+ 阴极:2HO + 2e- 错误: 引用源未找到 H ↑ + 2OH-
2 2
电解
阴极 (纯铜) :Cu2+ + 2e- 错误: 引用源未找到 Cu 总反应式:2Cl- + 2H O ==== H ↑+ Cl ↑ + 2OH-
2 2 2
总反应式:无 5.电解HCl溶液
3.电镀铜 阳极:2Cl- - 2e- 错误: 引用源未找到 Cl↑
2
阳极(纯铜):Cu— 2e- 错误: 引用源未找到 Cu2+ 阴极:2H+ + 2e- 错误: 引用源未找到 H ↑
2
电解总反应式:2Cl- + 2H+==== Cl↑ + H ↑ 阴极:2Cu2+ + 4e- 错误: 引用源未找到 2Cu↓
2 2
电解
6.电解NaOH溶液 总反应式:2Cu2+ + 2H O ==== 2Cu↓ + O ↑+ 4H+
2 2
阳极:4OH- —4e- 错误: 引用源未找到 O ↑ + 2H O 10.电解AgNO 溶液
2 2 3
阴极:4HO + 4e- 错误: 引用源未找到 2H ↑ + 4OH- 阳极:2HO— 4e- 错误: 引用源未找到 O ↑ + 4H+
2 2 2 2
电解
总反应式:2HO ==== 2H ↑+ O ↑ 阴极:4Ag+ + 4e- 错误: 引用源未找到 4Ag↓
2 2 2
电解
7.电解HSO 溶液 总反应式:4Ag+ + 2H O ==== 4Ag↓ + O ↑ + 4H+
2 4 2 2
阳极:2HO — 4e- 错误: 引用源未找到 O ↑ + 4H+ 11.铅蓄电池充电
2 2
阴极:4H+ +4e- 错误: 引用源未找到 2H ↑ 阳极:PbSO —2e- + 2H O 错误: 引用源未找到 PbO
2 4 2 2
电解
总反应式:2HO ==== 2H ↑ + O ↑ + + 4H+
2 2 2
8.电解KNO 溶液 阴极:PbSO + 2e- 错误: 引用源未找到 Pb +
3 4
电解
阳极:2HO —4e- 错误: 引用源未找到 O ↑ + 4H+ 总反应式:2PbSO + 2H O ==== Pb + PbO + 4H+ + 2
2 2 4 2 2
阴极:4HO + 4e- 错误: 引用源未找到 2H ↑ + 4OH-
2 2
电解
总反应式:2HO ==== 2H ↑ + O ↑ B H(g) + 3O (g) ==== B O(s) + 3H O(l);ΔH = -
2 2 2 2 6 2 2 3 2
9.电解CuSO 溶液 2165 kJ·mol-1
4
阳极:2HO—4e- 错误: 引用源未找到 O ↑ + 4H+
2 2
第七部分 热反应方程式
C ΔH= -2800kJ·mol -1
C(石墨,s) +O (g) =CO(g);ΔH= -393.5kJ·mol -1 H
2 2
C(金刚石,s) +O
2
(g) =CO
2
(g);ΔH= -395.4kJ·mol -1
H(g) +Cl(g) =2HCl(g);ΔH= -184.6kJ·mol -1
2 2
C(金刚石,s) =C(石墨,s);ΔH= -1.90kJ·mol -1
2H(g) +O (g) =2HO(g);ΔH= -483.6mol·L -1
2 2 2
C(s) +H O(g) =CO(g) +H (g);ΔH= +131.3kJ·mol -1
2 2
H(g) + O(g) =HO(l);ΔH= -241.8kJ·mol -1
2 2 2
C(s) + O (g) =CO(g);ΔH= -110.5kJ·mol -1
2
2H(g) +O (g) =2HO(l);ΔH= -571.6kJ·mol -1
C(s) +O (g) =CO(g);ΔH= -393.5kJ·mol -1
2 2 2
2 2
H(g) + O(g) =HO(l);ΔH= -285.8kJ·mol -1
2 2 2
CO(g) + O(g) =CO(g);ΔH= -283kJ·mol -1
2 2
2HO(g) =2H(g) +O (g);ΔH= +483.6kJ·mol -1
2 2 2
CaC (s) +2HO(l) =C H(g) +Ca(OH) (s);
2 2 2 2 2
ΔH= -127kJ·mol -1 H 2 O(g) =H 2 (g) + O 2 (g);ΔH= +241.8kJ·mol -1
CH(g) +2O (g) =CO(g) +2H O(l);
4 2 2 2 2HO(l) =2H(g) +O (g);ΔH= +571.6kJ·mol -1
2 2 2
ΔH= -890.3kJ·mol -1
C 2 H 4 (g) +3O 2 (g) =2CO 2 (g) +2H 2 O(l); H 2 O(l) =H 2 (g) + O 2 (g);ΔH= +285.8kJ·mol -1
ΔH= -1411kJ·mol -1
HO(l) =HO(g);ΔH= +44kJ·mol -1
2 2
HO(g) =HO(l);ΔH= -44kJ·mol -1
C H(g) + O(g) =2CO(g) +H O(l); 2 2
2 2 2 2 2
HCl(aq) +NaOH(aq) =NaCl(aq) +HO(l);ΔH=
2
ΔH= -1300kJ·mol -1 -57.3kJ·mol -1
H +(aq) +OH-(aq) =HO(l);ΔH= -57.3kJ·mol -1
C 3 H 8 (g) +5 O 2 (g) =3CO 2 (g) +4H 2 O(l); 2
N
ΔH= -2220.0kJ·mol -1
N(g) +O(g)=NO (g);ΔH= +180.7kJ·mol -1
2 2 2
C H (l) + O(g) =8CO(g) +9HO(l);
8 18 2 2 2
催化剂
N(g) +3H (g) 2NH (g);ΔH= -92.4kJ·mol
2 2 3
ΔH= -5518kJ·mol -1 高温、高压
催化剂
-1
CHOH(l) + O(g) =CO(g) +2HO(l); △
3 2 2 2
ΔH= -725.8kJ·mol -1 4NH (g) +5O(g)==== 4NO(g) +6H O(g);ΔH=
3 2 2
C HOH(l) +3O(g) =2CO(g) +3HO(l);
2 5 2 2 2 -907kJ·mol -1
ΔH= -1367kJ·mol -1
2NO(g) +O (g)=2NO (g);ΔH= -113kJ·mol -1
2 2
C H O(s) +6O(g)=6CO(g) +6HO(l);
6 12 6 2 2 23NO (g) +H O(l) = 2HNO(l) +NO(g) ; ΔH=
2 2 3
-136kJ·mol -1.
NH(g) +O (g) =N(g) +2HO(g);ΔH= -534kJ·mol -1
2 4 2 2 2
NH(l) +2HO(l) =N(g) +4HO(g);
2 4 2 2 2 2
ΔH= -641.6kJ·mol -1
2NH(g) +2NO (g) =3N(g) +4HO(g);
2 4 2 2 2
ΔH= -1135.7kJ·mol -1.
P
P(白磷,s) =4P(红磷,s);ΔH= -66.8kJ·mol -1.
4
S
点燃
S(g) +O (g)==== SO (g);ΔH= -297kJ·mol -1
2 2
高温
FeS(s) + O(g)==== Fe O(s) +2SO (g);
2 2 2 3 2
ΔH= -853kJ·mol -1
催化剂
SO(g) + O (g) SO (g);ΔH= -98.3kJ·mol -1
2 2 3
SO(g) +H O(l) =HSO (l);ΔH= -130.3kJ·mol -1
3 2 2 4