文档内容
2021 年北京市普通高中学业水平等级性考试
可能用到的相对原子质量:H1 C12 N14 O16
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一
项。
1. 我国科研人员发现中药成分黄芩素能明显抑制新冠病毒的活性。下列关于黄芩素的说法不正确的是
A. 分子中有3种官能团 B. 能与NaCO 溶液反应
2 3
C. 在空气中可发生氧化反应 D. 能和Br 发生取代反应和加成反应
2
【答案】A
【解析】
【分析】
【详解】A.根据物质结构简式可知:该物质分子中含有酚羟基、醚键、羰基、碳碳双键四种官能团,A
错误;
B.黄芩素分子中含有酚羟基,由于酚的酸性比NaHCO 强,所以黄芩素能与NaCO 溶液反应产生
3 2 3
NaHCO ,B正确;
3
C.酚羟基不稳定,容易被空气中的氧气氧化,C正确;
D.该物质分子中含有酚羟基,由于羟基所连的苯环的邻、对位有H原子,因此可以与浓溴水发生苯环上
的取代反应;分子中含有不饱和的碳碳双键,可以与Br 等发生加成反应,D正确;
2
故合理选项是A。
2. 下列有关放射性核素氚( H)的表述不正确的是
A. H原子核外电子数为1 B. H原子核内中子数为3
C. 与H 化学性质基本相同 D. 具有放射性
2
【答案】B
【解析】
【分析】
第1页 | 共25页【详解】A.放射性核素 H,质量数是3,质子数是1,质子数等于核外电子数,所以核外电子数等于1,
故A正确;
B.放射性核素 H,质量数是3,质子数是1,所以中子数等于3-1=2,故B错误;
C. 与H 的相对分子质量不同,二者的沸点不同,但二者同属于氢气,化学性质基本相同,故C正确;
2
D. H是放射性核素,所以3HO也具有放射性,故D正确;
2
故选B。
3. 下列化学用语或图示表达不正确的是
A. N 的结构式:N≡N B. Na+的结构示意图:
2
C. 溴乙烷的分子模型: D. CO 的电子式:
2
【答案】D
【解析】
【分析】
【详解】A.N 分子中N原子间是三键,结构式:N≡N,正确;
2
B.Na+的结构示意图: ,正确;
C.溴乙烷的分子模型: ,正确;
D.CO 的电子式: ,错误;
2
故选D。
4. 下列性质的比较,不能用元素周期律解释的是
A. 酸性:HClO>HSO >HSiO B. 碱性:KOH>NaOH>LiOH
4 2 3 2 3
C. 热稳定性:HO>HS>PH D. 非金属性:F>O>N
2 2 3
【答案】A
【解析】
【分析】
【详解】A.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,由于 S元素最高价含氧
第2页 | 共25页酸是HSO ,不是HSO ,因此不能根据元素周期律判断酸性:HClO>HSO >HSiO,A错误;
2 4 2 3 4 2 3 2 3
B.同一主族元素的金属性随原子序数的增大而增强。元素的金属性越强,其最高价氧化物对应的水化物
的碱性就越强。元素的金属性:K>Na>Li,所以碱性:KOH>NaOH>LiOH,B正确;
C.同一周期元素的非金属性随原子序数的增大而增强;同一主族元素的非金属性随原子序数的增大而减
弱。元素的非金属性越强,其简单氢化物的稳定性就越强。元素的非金属性:O>S>P,所以氢化物的热
稳定性:HO>HS>PH ,C正确;
2 2 3
D.同一周期元素的非金属性随原子序数的增大而增强,所以元素的非金属性:F>O>N,D正确;
故合理选项是A。
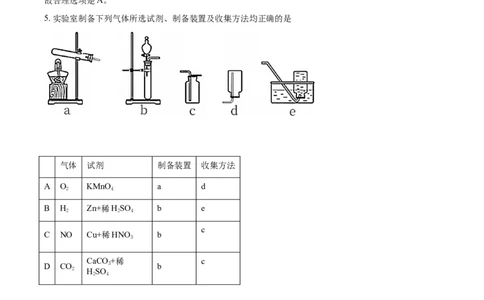
5. 实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法
A O KMnO a d
2 4
B H Zn+稀HSO b e
2 2 4
c
C NO Cu+稀HNO b
3
CaCO +稀 c
D CO 3 b
2 HSO
2 4
A. A B. B C. C D. D
【答案】B
【解析】
【分析】
【详解】A.KMnO 是固体物质,加热分解产生O ,由于O 难溶于水,因此可以用排水方法或向上排空
4 2 2
气的方法收集,故不可以使用a、d装置制取和收集O,A错误;
2
第3页 | 共25页B.Zn与HSO 发生置换反应产生H,块状固体与液体反应制取气体,产生的H 难溶于水,因此可以用排
2 4 2 2
水方法收集,故可以使用装置b、e制取H,B正确;
2
C.Cu与稀HNO 反应产生NO气体,NO能够与O 发生反应产生NO 气体,因此不能使用排空气的方法
3 2 2
收集,C错误;
D.CaCO 与稀硫酸反应产生的CaSO、CO 气体,CaSO 微溶于水,使制取CO 气体不能持续发生,因此
3 4 2 4 2
不能使用该方法制取CO 气体,D错误;
2
故合理选项 是B。
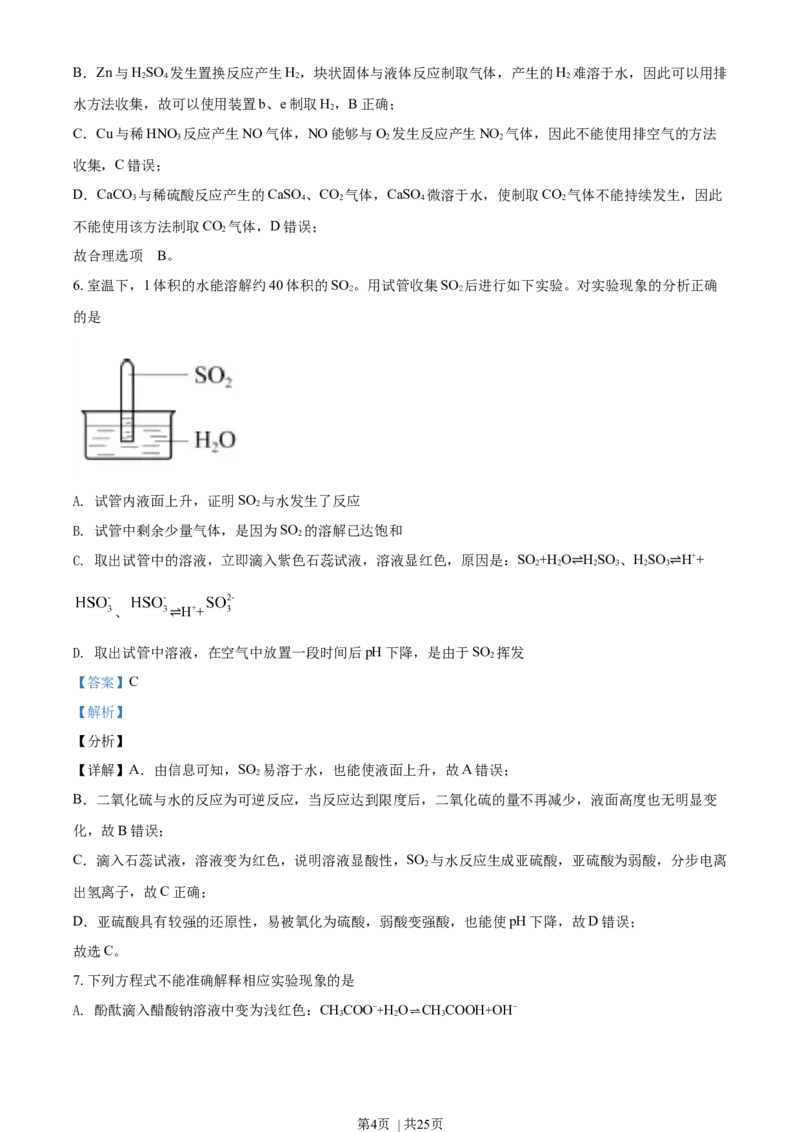
6. 室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实验。对实验现象的分析正确
2 2
的是
A. 试管内液面上升,证明SO 与水发生了反应
2
B. 试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C. 取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +H O HSO 、HSO H++
2 2 2 3 2 3
⇌ ⇌
、 H++
⇌
D. 取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
【答案】C
【解析】
【分析】
【详解】A.由信息可知,SO 易溶于水,也能使液面上升,故A错误;
2
B.二氧化硫与水的反应为可逆反应,当反应达到限度后,二氧化硫的量不再减少,液面高度也无明显变
化,故B错误;
C.滴入石蕊试液,溶液变为红色,说明溶液显酸性,SO 与水反应生成亚硫酸,亚硫酸为弱酸,分步电离
2
出氢离子,故C正确;
D.亚硫酸具有较强的还原性,易被氧化为硫酸,弱酸变强酸,也能使pH下降,故D错误;
故选C。
7. 下列方程式不能准确解释相应实验现象的是
A. 酚酞滴入醋酸钠溶液中变为浅红色:CHCOO-+HO CHCOOH+OH-
3 2 ⇌ 3
第4页 | 共25页B. 金属钠在空气中加热生成淡黄色固体:4Na+O=2NaO
2 2
C. 铝溶于氢氧化钠溶液,有无色气体产生:2Al+2OH-+2HO=2 +3H↑
2 2
D. 将二氧化硫通入氢硫酸中产生黄色沉淀:SO +2HS=3S↓+2HO
2 2 2
【答案】B
【解析】
【分析】
【详解】A.CHCOONa溶液呈碱性是因为发生了CHCOO-的水解:CHCOO-+HO CHCOOH+OH-,A
3 3 3 2 ⇌ 3
正确;
B.金属钠在空气中加热生成淡黄色固体过氧化钠:2Na+O NaO,B错误;
2 2 2
C.铝与NaOH溶液反应生成偏铝酸钠和氢气:2Al+2OH-+2HO=2 +3H↑,C正确;
2 2
D.将SO 通入HS溶液生成S单质和水:SO +2HS=3S↓+2HO,D正确;
2 2 2 2 2
故选B。
8. 使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现“亮→暗(或灭)→亮”现
象的是
选项 A B C D
试剂a CuSO NH HCO HSO CHCOOH
4 4 3 2 4 3
试剂b Ba(OH) Ca(OH) Ba(OH) NH ·H O
2 2 2 3 2
A. A B. B C. C D. D
第5页 | 共25页【答案】D
【解析】
【分析】
【详解】A.Ba(OH) 与CuSO 发生离子反应:Ba2++2OH-+Cu2++ =BaSO ↓+Cu(OH) ↓,随着反应的进
2 4 4 2
行,溶液中自由移动的离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微粒,
灯泡完全熄灭。当CuSO 溶液过量时,其电离产生的Cu2+、 导电,使灯泡逐渐又变亮,A不符合题
4
意;
B.Ca(OH) 与NH HCO 发生离子反应:Ca2++2OH-+ + =CaCO ↓+H O+NH ·H O,随着反应的
2 4 3 3 2 3 2
进行,溶液中自由移动离子浓度减小,灯泡逐渐变暗,当二者恰好反应时,溶液中自由移动的微粒浓度很
小,灯泡很暗。当 NH HCO 溶液过量时,其电离产生的 、 导电,使灯泡逐渐又变亮,B不
4 3
符合题意;
C.Ba(OH) 与HSO 发生离子反应:Ba2++2OH-+2H++ =BaSO ↓+2H O,随着反应的进行,溶液中自由
2 2 4 4 2
移动的离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微粒,灯泡完全熄灭。
当HSO 溶液过量时,其电离产生的H+、 导电,使灯泡逐渐又变亮,C不符合题意;
2 4
D.CHCOOH与氨水发生离子反应:CHCOOH+NH ·H O=CHCOO-+ +H O,反应后自由移动的离子
3 3 3 2 3 2
浓度增大,溶液导电能力增强,灯泡更明亮,不出现亮—灭(或暗)—亮的变化,D符合题意;
故合理选项是D。
9. 用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液除去乙炔中的杂质。反应
2 3 2 4
为:
①CuSO+HS=CuS↓+HSO
4 2 2 4
②11PH +24CuSO +12HO=3HPO +24HSO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是
A. CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、Ca P+6H O=3Ca(OH) +2PH↑
3 2 2 2 2 3 2 2 2 3
B. 不能依据反应①比较硫酸与氢硫酸的酸性强弱
C. 反应②中每24 mol CuSO 氧化11 mol PH
4 3
D. 用酸性KMnO 溶液验证乙炔还原性时,HS、PH 有干扰
4 2 3
第6页 | 共25页【答案】C
【解析】
【分析】
【详解】A.水解过程中元素的化合价不变,根据水解原理结合乙炔中常混有 HS、PH 可知CaS的水解方
2 3
程式为CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式为Ca P+6H O=3Ca(OH) +2PH↑,A项正确;
2 2 2 3 2 3 2 2 2 3
B.该反应能发生是因为有不溶于水也不溶于酸的CuS生成,因此反应①不能说明HS的酸性强于
2
HSO ,事实上硫酸的酸性强于氢硫酸,B项正确;
2 4
C.反应②中Cu元素化合价从+2价降低到+1价,得到1个电子,P元素化合价从-3价升高到+5价,失去8
个电子,则24molCuSO 完全反应时,可氧化PH 的物质的量是24mol÷8=3mol,C项错误;
4 3
D.HS、PH 均被KMnO 酸性溶液氧化,所以会干扰KMnO 酸性溶液对乙炔性质的检验,D项正确;
2 3 4 4
答案选C。
10. NO 和NO 存在平衡:2NO (g)⇌NO(g) △H<0。下列分析正确的是
2 2 4 2 2 4
A. 1 mol平衡混合气体中含1 mol N原子
B. 断裂2 mol NO 中的共价键所需能量小于断裂1 mol N O 中的共价键所需能量
2 2 4
C. 恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的
D. 恒容时,水浴加热,由于平衡正向移动导致气体颜色变浅
【答案】B
【解析】
【分析】
【详解】A.1molNO 含有1molN原子,1molN O 含有2molN原子,现为可逆反应,为NO 和NO 的混
2 2 4 2 2 4
合气体,1 mol平衡混合气体中所含原子大于1 mol N,A项错误;
B.反应2NO (g)⇌NO(g)为放热反应,故完全断开2molNO 分子中的共价键所吸收的热量比完全断开
2 2 4 2
1molN O 分子中的共价键所吸收的热量少,B项正确;
2 4
C.气体体积压缩,颜色变深是因为体积减小,浓度变大引起的,C项错误;
D.放热反应,温度升高,平衡逆向移动,颜色加深,D项错误;
答案选B。
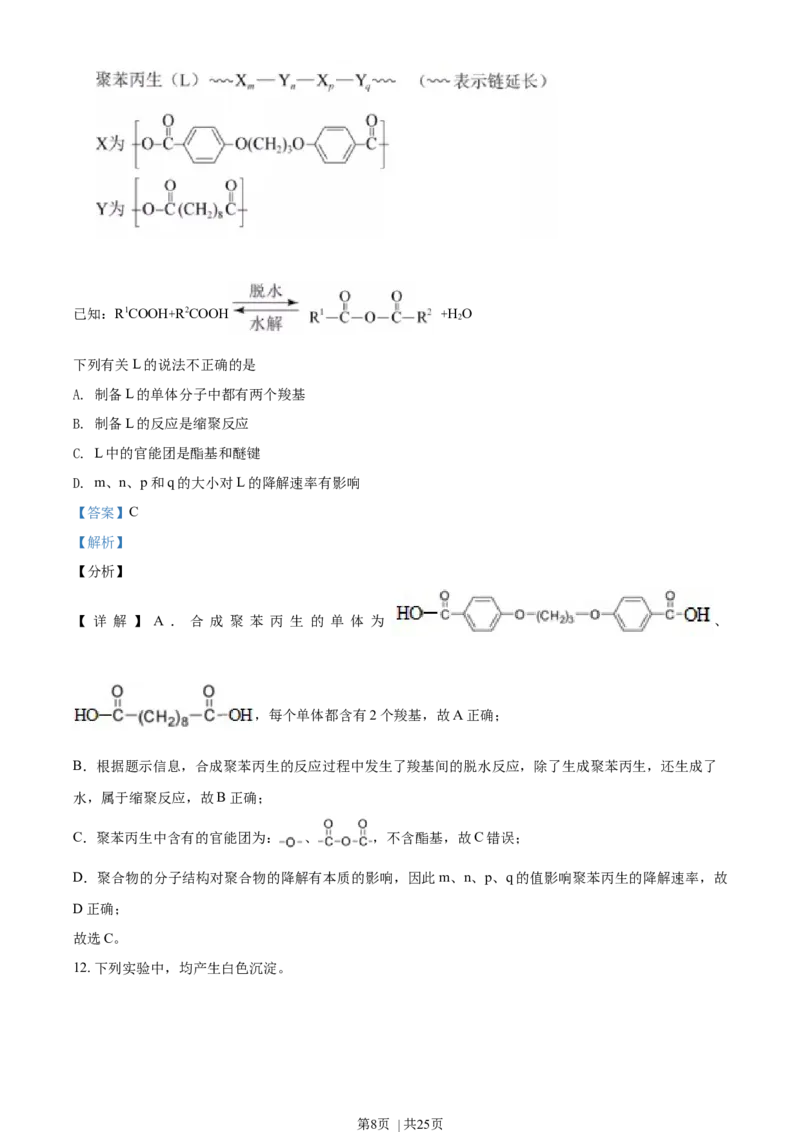
11. 可生物降解的高分子材料聚苯丙生(L)的结构片段如下图。
第7页 | 共25页已知:R1COOH+R2COOH +HO
2
下列有关L的说法不正确的是
A. 制备L的单体分子中都有两个羧基
B. 制备L的反应是缩聚反应
C. L中的官能团是酯基和醚键
D. m、n、p和q的大小对L的降解速率有影响
【答案】C
【解析】
【分析】
【 详 解 】 A . 合 成 聚 苯 丙 生 的 单 体 为 、
,每个单体都含有2个羧基,故A正确;
B.根据题示信息,合成聚苯丙生的反应过程中发生了羧基间的脱水反应,除了生成聚苯丙生,还生成了
水,属于缩聚反应,故B正确;
C.聚苯丙生中含有的官能团为: 、 ,不含酯基,故C错误;
D.聚合物的分子结构对聚合物的降解有本质的影响,因此m、n、p、q的值影响聚苯丙生的降解速率,故
D正确;
故选C。
12. 下列实验中,均产生白色沉淀。
第8页 | 共25页下列分析不正确 的是
A. NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B. CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C. Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D. 4个实验中,溶液滴入后,试管中溶液pH均降低
【答案】B
【解析】
【分析】
【详解】A.NaCO 溶液、NaHCO 溶液均存在Na+、 、 、HCO 、H+、OH-、HO,故含有的
2 3 3 2 3 2
微粒种类相同,A正确;
B. H++ ,加入Ca2+后,Ca2+和 反应生成沉淀,促进 的电离,B错误;
C.Al3+与 、 都能发生互相促进的水解反应,C正确;
D.由题干信息可知形成沉淀时会消耗碳酸根和碳酸氢根,则它们浓度减小,水解产生的氢氧根的浓度会
减小,pH减小,D正确;
故选B。
13. 有科学研究提出:锂电池负极材料(Li)由于生成LH而不利于电池容量的保持。一定温度下,利用足量重
水(D O)与含LiH的Li负极材料反应,通过测定n(D )/n(HD)可以获知 n(Li)/n(LiH)。
2 2
已知:①LiH+H O=LiOH+H ↑
2 2
②2Li(s)+H 2⇌2LiH △H<0
下列说法不正确的是
A. 可用质谱区分D 和HD
2
B. Li与DO的反应:2Li+2DO=2LiOD+D ↑
2 2 2
C. 若n(Li)/n(LiH)越大,则n(D )/n(HD)越小
2
D. 80℃反应所得n(D )/n(HD)比25℃反应所得n(D )/n(HD)大
2 2
【答案】C
第9页 | 共25页【解析】
【分析】
【详解】A.D 和HD的相对分子质量不同,可以用质谱区分,A正确;
2
B.类似于钠和水的反应, Li与DO反应生成LiOD与D,化学方程式是2Li+2DO=2LiOD+D ↑,B正确;
2 2 2 2
C.D 由Li与DO反应生成,HD 通过反应LiH+D O=LiOD+HD , n(D )/n(HD)越大,n(Li)/n(LiH)越大,
2 2 2 2
C不正确;
D.升温,2LiH⇌2Li+H
2
△H>0平衡右移,Li增多LiH 减少,则结合选项C可知:80℃下的n(D
2
)/n(HD)大
于25℃下的n(D )/n(HD) ,D正确;
2
答案为:C。
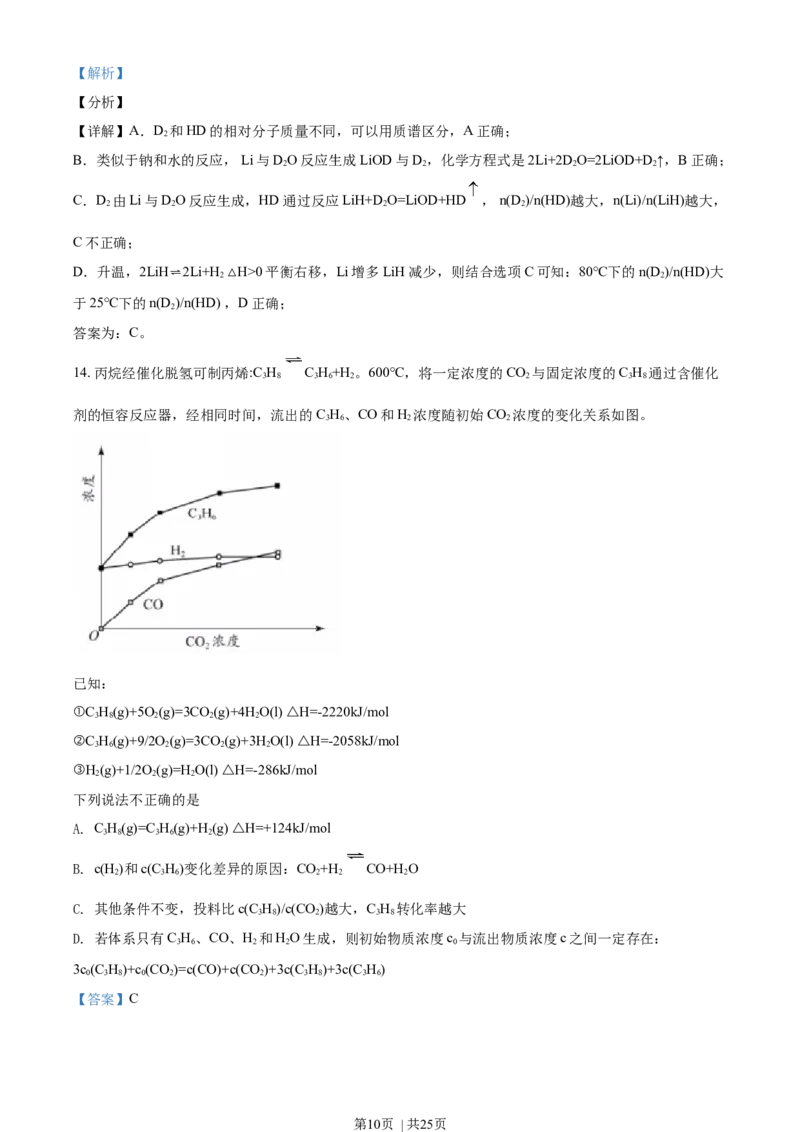
14. 丙烷经催化脱氢可制丙烯:C H C H+H 。600℃,将一定浓度的 CO 与固定浓度的C H 通过含催化
3 8 3 6 2 2 3 8
剂的恒容反应器,经相同时间,流出的 C H、CO和H 浓度随初始 CO 浓度的变化关系如图。
3 6 2 2
已知:
①C H(g)+5O(g)=3CO (g)+4HO(l) △H=-2220kJ/mol
3 8 2 2 2
②C H(g)+9/2O (g)=3CO (g)+3HO(l) △H=-2058kJ/mol
3 6 2 2 2
③H(g)+1/2O (g)=HO(l) △H=-286kJ/mol
2 2 2
下列说法不正确的是
A. C H(g)=C H(g)+H(g) △H=+124kJ/mol
3 8 3 6 2
B. c(H)和c(C H)变化差异的原因:CO+H CO+HO
2 3 6 2 2 2
C. 其他条件不变,投料比c(C H)/c(CO )越大,C H 转化率越大
3 8 2 3 8
D. 若体系只有C H、CO、H 和HO生成,则初始物质浓度c 与流出物质浓度c之间一定存在:
3 6 2 2 0
3c(C H)+c (CO)=c(CO)+c(CO )+3c(C H)+3c(C H)
0 3 8 0 2 2 3 8 3 6
【答案】C
第10页 | 共25页【解析】
【分析】
【详解】A.根据盖斯定律结合题干信息① C H(g)+5O(g)=3CO (g)+4HO(l) △H=-2220kJ/mol②C H(g)
3 8 2 2 2 3 6
+9/2O (g)=3CO (g)+3HO(l) △H=-2058kJ/mol ③H (g)+1/2O (g)=HO(l) △H=-286kJ/mol 可知,可由①-②-③
2 2 2 2 2 2
得到目标反应C H(g)=C H(g)+H(g),该反应的△H= =+124kJ/mol,A正确;
3 8 3 6 2
B.仅按C H(g)=C H(g)+H(g)可知C H、H 的浓度随CO 浓度变化趋势应该是一致的,但是氢气的变化
3 8 3 6 2 3 6 2 2
不明显,反而是CO与C H 的变化趋势是一致的,因此可以推断高温下能够发生反应CO+H
3 6 2 2
CO+HO,从而导致C H、H 的浓度随CO 浓度变化趋势出现这样的差异,B正确;
2 3 6 2 2
C.投料比增大,相当于增大C H 浓度,浓度增大,转化率减小, C错误;
3 8
D.根据质量守恒定律,抓住碳原子守恒即可得出,如果生成物只有C H、CO、HO、H,那么入口各气
3 6 2 2
体的浓度c 和出口各气体的浓度符合3c(C H)+c (CO)=3c(C H)+c(CO)+3c(C H)+c(CO ),D正确;
0 0 3 8 0 2 3 6 3 8 2
答案为:AC。
第二部分
本部分共5题,共58分。
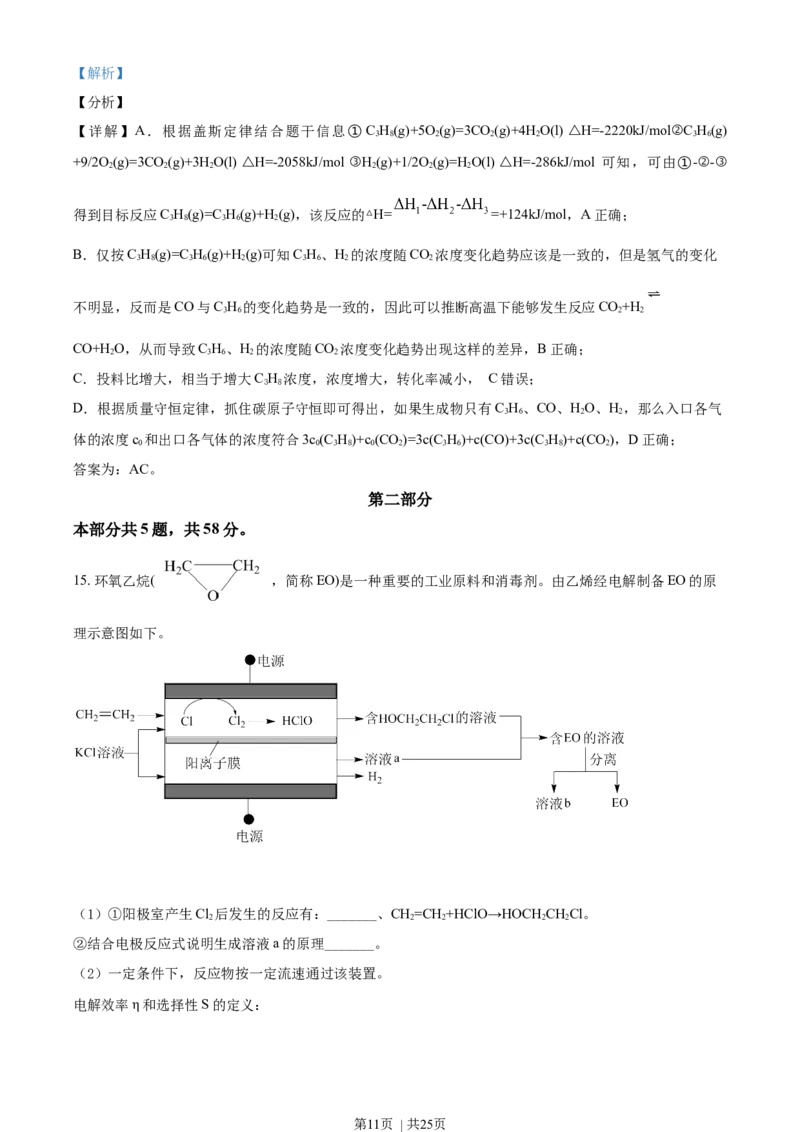
15. 环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原
理示意图如下。
(1)①阳极室产生Cl 后发生的反应有:_______、CH=CH +HClO→HOCH CHCl。
2 2 2 2 2
②结合电极反应式说明生成溶液a的原理_______。
(2)一定条件下,反应物按一定流速通过该装置。
电解效率η和选择性S的定义:
第11页 | 共25页η(B)= ×100%
S(B)= ×100%
①若η(EO)=100%,则溶液b的溶质为_______。
②当乙烯完全消耗时,测得η(EO)≈70%,S(EO)≈97%,推测η(EO)≈70%的原因:
I.阳极有HO放电
2
II.阳极有乙烯放电
III.阳极室流出液中含有Cl 和HClO
2
……
i.检验电解产物,推测I不成立。需要检验的物质是_______。
ii.假设没有生成EO的乙烯全部在阳极放电生成CO,η(CO )≈_______%。经检验阳极放电产物没有CO
2 2 2。
iii.实验证实推测III成立,所用试剂及现象是_______。
可选试剂:AgNO 溶液、KI溶液、淀粉溶液、品红溶液。
3
【答案】(1) ①. Cl +H O= HCl+ HClO ②. 阴极发生反应: 2HO+2e-=H ↑ + 2OH-生成OH-,K+ 通过
2 2 2 2
阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液
(2) ①. KCl ②. O ③. 13 ④. KI 溶液和淀粉溶液,溶液变蓝
2
【解析】
【分析】
【小问1详解】
阳极产生氯气后,可以和水发生反应生成次氯酸其方程式为:Cl +H O= HCl+ HClO;溶液a是阴极的产物,
2 2
在阴极发生反应2HO+2e-=H ↑ + 2OH-,同时阳极的钾离子会向阴极移动和氢氧根结合形成氢氧化钾,故答
2 2
案为:阴极发生反应: 2HO+2e-=H ↑ + 2OH-生成OH-,K+ 通过阳离子交换膜从阳极迁移到阴极,形成
2 2
KOH和KCl的混合溶液;
【小问2详解】
①若η(EO)=100%则说明在电解过程中只有乙烯中的碳化合价发生变化,其他元素化合价没有变,故溶液 b
的溶质为:KCl;
②i.阳极有HO放电时会产生氧气,故需要检验的物质是O;ii. 设EO的物质的量为amol
2 2
则转化的乙烯的物质的量为: ;生成EO转化的电子的物质的量:2amol;此过程转移电子的总物质
第12页 | 共25页的量: ;生成CO 的物质的量: ;生成CO 转移的电子的物质的量:
2 2
,则η(CO )= ≈13%;
2
iii.实验证实推测III成立,则会产生氯气,验证氯气即可,故答案为:KI 溶液和淀粉溶液,溶液变蓝。
16. 某小组实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应并测定其平衡常数。
(1)实验验证
实验I:将0.0100 mol/L Ag SO 溶液与0.0400 mo/L FeSO 溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液
2 4 4
呈黄色。
实验II:向少量Ag粉中加入0.0100 mol/L Fe (SO ) 溶液(pH=1),固体完全溶解。
2 4 3
①取I中沉淀,加入浓硝酸,证实沉淀为Ag。现象是_______。
②II中溶液选用Fe (SO ),不选用Fe(NO ) 的原因是_______。
2 4 3 3 3
综合上述实验,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
③小组同学采用电化学装置从平衡移动角度进行验证。补全电化学装置示意图,写出操作及现象_______。
(2)测定平衡常数
实验Ⅲ:一定温度下,待实验Ⅰ中反应达到平衡状态时,取v mL上层清液,用c mol/L KSCN标准溶液滴
1
定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v mL。
1
资料:Ag++SCN- AgSCN↓(白色) K=1012
Fe3++SCN- FeSCN2+(红色) K=102.3
第13页 | 共25页①滴定过程中Fe3+的作用是_______。
②测得平衡常数K=_______。
(3)思考问题
①取实验I的浊液测定c(Ag+),会使所测K值_______(填“偏高”“偏低”或“不受影响”)。
②不用实验II中清液测定K的原因是_______。
【答案】(1) ①. 灰黑色固体溶解,产生红棕色气体 ②. 防止酸性条件下, 氧化性氧化
Fe2+干扰实验结果 ③. a:铂/石墨电极,b:FeSO 或Fe (SO ) 或二者混合溶液,c:AgNO 溶液;操作
4 2 4 3 3
和现象:闭合开关 K,Ag电极上固体逐渐溶解,指针向左偏转,一段时间后指针归零,再向左侧烧杯中加
入滴加较浓的Fe (SO ) 溶液,与之前的现象相同;或者闭合开关 K,Ag电极上有灰黑色固体析出,指针
2 4 3
向右偏转,一段时间后指针归零,再向左侧烧杯中加入滴加较浓的 Fe (SO ) 溶液,Ag电极上固体逐渐减
2 4 3
少,指针向左偏转
(2) ①. 指示剂 ②.
(3) ①. 偏低 ②. Ag完全反应,无法判断体系是否达到化学平衡状态
【解析】
【分析】
【小问1详解】
①由于Ag能与浓硝酸发生反应:Ag+2HNO (浓)=AgNO +NO↑+H O,故当观察到的现象为灰黑色固体溶
3 3 2 2
解,产生红棕色气体,即可证实灰黑色固体是Ag,故答案为:灰黑色固体溶解,产生红棕色气体。
②由于Fe(NO ) 溶液电离出 将与溶液中的H+结合成由强氧化性的HNO,能氧化Fe2+,而干扰实验,
3 3 3
故实验II使用的是Fe (SO ) 溶液,而不是Fe(NO ) 溶液,故答案为:防止酸性条件下, 氧化性氧化
2 4 3 3 3
Fe2+干扰实验结果。
③由装置图可知,利用原电池原理来证明反应Fe2++Ag+ Ag+Fe3+为可逆反应,两电极反应为:Fe2+-e-
的
Fe3+,Ag++e- Ag,故另一个电极必须是与Fe3+不反应 材料,可用石墨或者铂电极,左侧烧杯中电解质
溶液必须含有Fe3+或者Fe2+,采用FeSO 或Fe (SO ) 或二者混合溶液,右侧烧杯中电解质溶液必须含有
4 2 4 3
Ag+,故用AgNO 溶液,组装好仪器后,加入电解质溶液,闭合开关 K,装置产生电流,电流从哪边流入,
3
第14页 | 共25页指针则向哪个方向偏转,根据b中所加试剂的不同,电流方向可能不同,因此可能观察到的现象为:Ag电
极逐渐溶解,指针向左偏转,一段时间后指针归零,说明此时反应达到平衡,再向左侧烧杯中加入滴加较
浓的Fe (SO ) 溶液,与之前的现象相同,表明平衡发生了移动;另一种现象为:Ag电极上有灰黑色固体
2 4 3
析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡,再向左侧烧杯中加入滴加较浓的
Fe (SO ) 溶液,Ag电极上固体逐渐减少,指针向左偏转,表明平衡发生了移动,故答案为:a:铂/石墨电
2 4 3
极,b:FeSO 或Fe (SO ) 或二者混合溶液,c:AgNO 溶液;操作和现象:闭合开关 K,Ag电极上固体逐
4 2 4 3 3
渐溶解,指针向左偏转,一段时间后指针归零,再向左侧烧杯中加入滴加较浓的Fe (SO ) 溶液,与之前的
2 4 3
现象相同;或者闭合开关 K,Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,再向左
侧烧杯中加入滴加较浓的Fe (SO ) 溶液,Ag电极上固体逐渐减少,指针向左偏转。
2 4 3
【小问2详解】
①Fe3+与SCN-反应生成红色FeSCN2+,因Ag+与SCN-反应相较于Fe3+与SCN-反应更加容易及彻底,当溶液
变为稳定浅红色,说明溶液中的Ag+恰好完全滴定,且溶液中Fe3+浓度不变,说明上述反应答案平衡,故
溶液中Fe3+的作用是滴定反应的指示剂,故答案为:指示剂。
②取I中所得上清液vmL。用cmol/L的KSCN溶液滴定,至溶液变为稳定浅红色时,消耗vmL,已知:
1 1
Ag++SCN- AgSCN,K=1012,说明反应几乎进行完全,故有I中上层清液中Ag+的浓度为:c(Ag+)=
mol/L,根据平衡三段式进行计算如下:
,故反应的平衡常数K=
= ,故答案为:指示剂; 。
【小问3详解】
第15页 | 共25页①若取实验I所得浊液测定Ag+浓度,则浊液中还有Ag,因存在平衡Fe2++Ag+ Ag+Fe3+,且随着反应
Ag++SCN- AgSCN,使得上述平衡逆向移动,则测得平衡体系中的c(Ag+)偏大,即 偏大,故所得到
的K= 偏小,故答案为:偏小。
②由于实验II中Ag完全溶解,故无法判断体系是否达到化学平衡状态,因而不用实验II所得溶液进行测
定并计算K,故答案为:Ag完全反应,无法判断体系是否达到化学平衡状态。
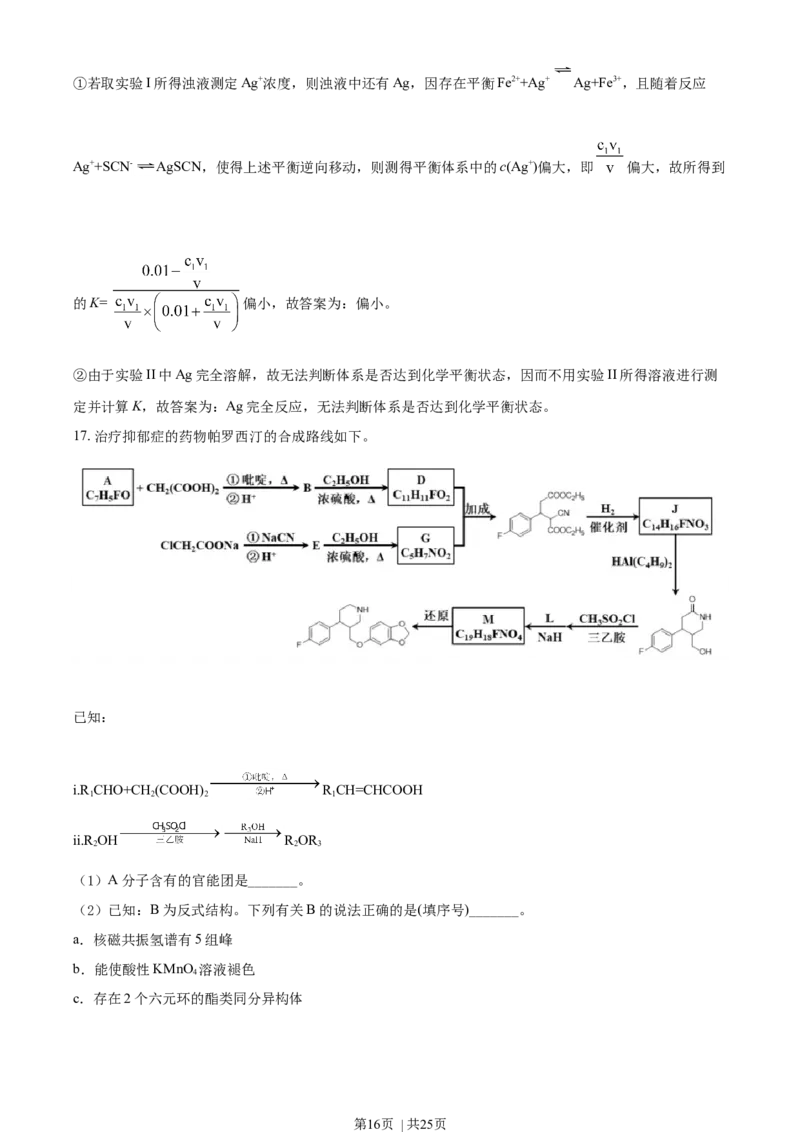
17. 治疗抑郁症的药物帕罗西汀的合成路线如下。
已知:
i.R CHO+CH (COOH) R CH=CHCOOH
1 2 2 1
ii.R OH R OR
2 2 3
(1)A分子含有的官能团是_______。
(2)已知:B为反式结构。下列有关B的说法正确的是(填序号)_______。
a.核磁共振氢谱有5组峰
b.能使酸性KMnO 溶液褪色
4
c.存在2个六元环的酯类同分异构体
第16页 | 共25页d.存在含苯环和碳碳三键的羧酸类同分异构体
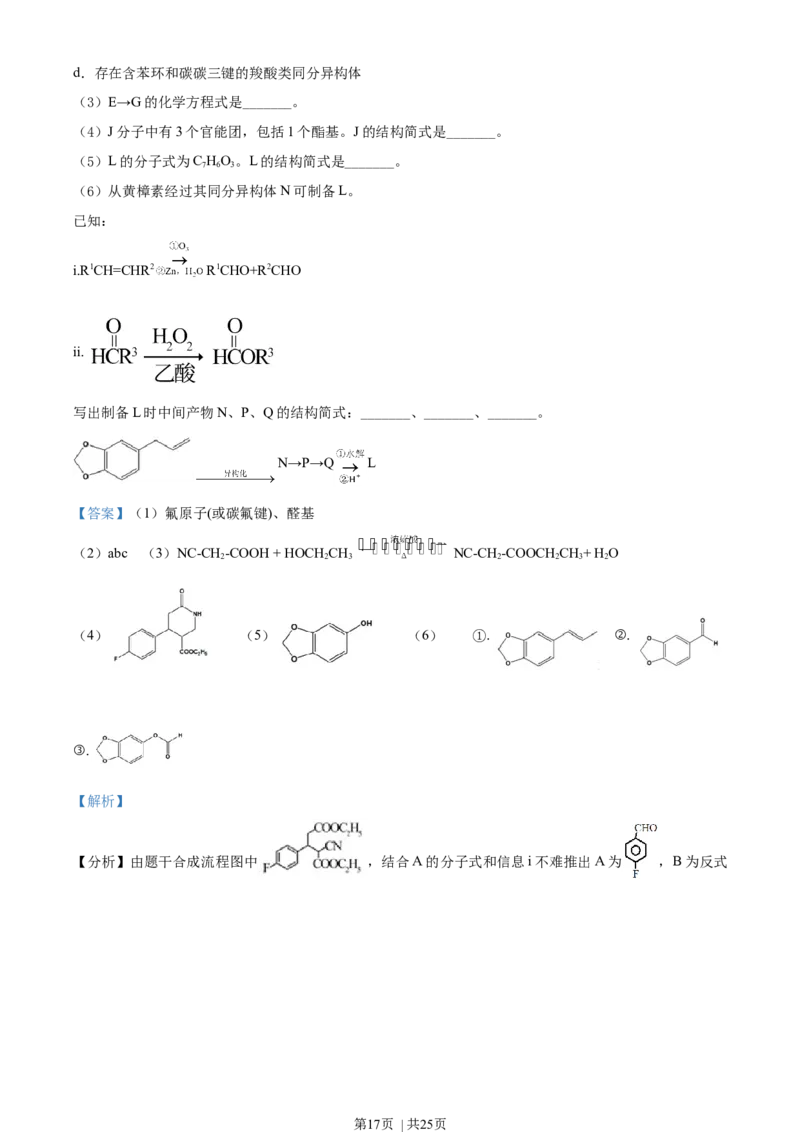
(3)E→G的化学方程式是_______。
(4)J分子中有3个官能团,包括1个酯基。J的结构简式是_______。
(5)L的分子式为C HO。L的结构简式是_______。
7 6 3
(6)从黄樟素经过其同分异构体N可制备L。
已知:
i.R1CH=CHR2 R1CHO+R2CHO
ii.
写出制备L时中间产物N、P、Q的结构简式:_______、_______、_______。
N→P→Q L
【答案】(1)氟原子(或碳氟键)、醛基
(2)abc (3)NC-CH -COOH + HOCH CH NC-CH -COOCH CH+ H O
2 2 3 2 2 3 2
(4) (5) (6) ①. ②.
③.
【解析】
【分析】由题干合成流程图中 ,结合A的分子式和信息i不难推出A为 ,B为反式
第17页 | 共25页结构,进而可以推出B的结构为 ,B与乙醇在浓硫酸共热时发生酯化反应生成D,故D为
,与D的分子式相符;ClCH COONa与NaCN先发生取代反应生成NCCH COONa,
2 2
然后再酸化得到 E,E 为 NCCH COOH,E 再与乙醇、浓硫酸共热发生酯化反应生成 G,G 为
2
NCCH COOCH CH ,D和G发生加成反应生成 ;结合J的分子式,J分子中有3个官能
2 2 3
团,包括1个酯基, 与H 发生反应生成J,可以推出J的结构简式为 ,
2
同时生成乙醇;由物质 结合 M 的分子式和信息 ii,并由(5) L 的分子式为
C HO 可以推出L的结构简式为 ,M的结构简式为 ,据此分析解答。
7 6 3
【小问1详解】
由分析可知,A的结构简式为 ,故A分子含有的官能团是氟原子、醛基,故答案为:氟原子(或碳氟
第18页 | 共25页键)、醛基;
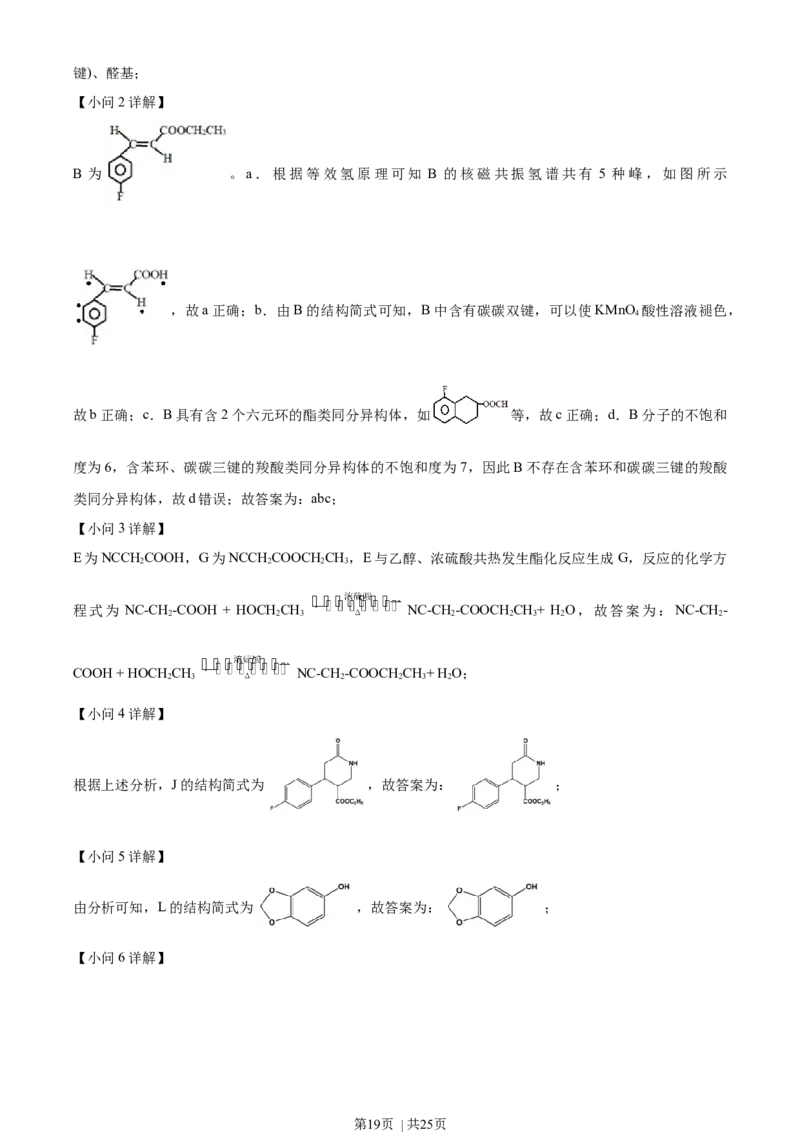
【小问2详解】
B 为 。a.根据等效氢原理可知 B 的核磁共振氢谱共有 5 种峰,如图所示
,故a正确;b.由B的结构简式可知,B中含有碳碳双键,可以使KMnO 酸性溶液褪色,
4
故b正确;c.B具有含2个六元环的酯类同分异构体,如 等,故c正确;d.B分子的不饱和
度为6,含苯环、碳碳三键的羧酸类同分异构体的不饱和度为7,因此B不存在含苯环和碳碳三键的羧酸
类同分异构体,故d错误;故答案为:abc;
【小问3详解】
E为NCCH COOH,G为NCCH COOCH CH,E与乙醇、浓硫酸共热发生酯化反应生成G,反应的化学方
2 2 2 3
程式为 NC-CH -COOH + HOCH CH NC-CH -COOCH CH+ H O,故答案为:NC-CH -
2 2 3 2 2 3 2 2
COOH + HOCH CH NC-CH -COOCH CH+ H O;
2 3 2 2 3 2
【小问4详解】
根据上述分析,J的结构简式为 ,故答案为: ;
【小问5详解】
由分析可知,L的结构简式为 ,故答案为: ;
【小问6详解】
第19页 | 共25页根据 Q 到 L 的转化条件可知 Q 为酯类,结合 L 的结构简式 ,可推知 Q 的结构简式为
,结合信息 i 和信息 ii 可推知 P 到 Q 的转化条件为 HO/HAc,P 的结构简式为
2 2
,由N到P的反应条件为O/Zn,HO且N为黄樟素的同分异构体,可推知N的结构简式为
3 2
,故答案为: ; ; 。
【点睛】本题的难点是题干信息的解读和应用,J的推断较难,要注意 与H 不是发生加
2
成反应生成J;另一个难点是(6),要注意逆推法的应用。
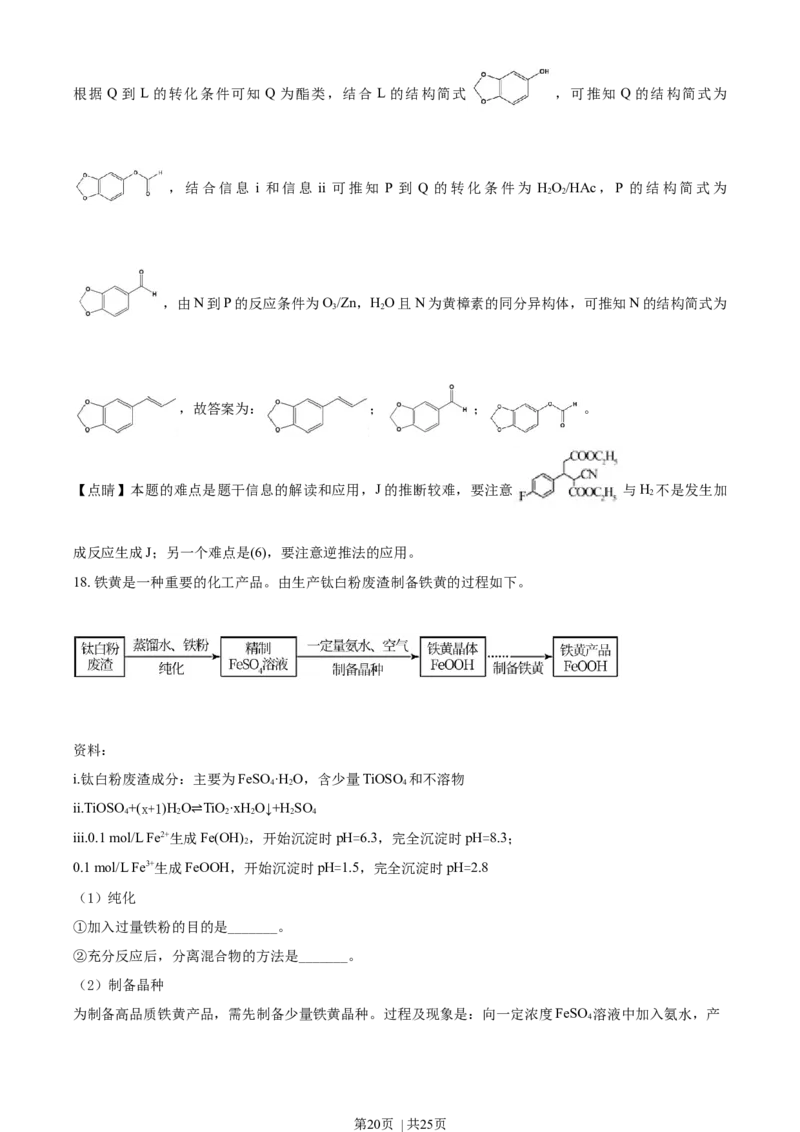
18. 铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
资料:
i.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ii.TiOSO +(x+1)H O TiO·xH O↓+HSO
4 2 2 2 2 4
iii.0.1 mol/L Fe2+生成⇌Fe(OH)
2
,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
0.1 mol/L Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
①加入过量铁粉的目的是_______。
②充分反应后,分离混合物的方法是_______。
(2)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO 溶液中加入氨水,产
4
第20页 | 共25页生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe2+)_______0.1mol/L(填“>”“=”或
“<”)。
③0-t 时段,pH几乎不变;t-t 时段,pH明显降低。结合方程式解释原因:_______。
1 1 2
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增加,
3
且(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄 溶液b 溶液c 滴定
资料:Fe3++3 =Fe(C O) ,Fe(C O) 不与稀碱液反应
2 4 2 4
NaC O 过量,会使测定结果_______(填“偏大”“偏小”或“不受影响”)。
2 2 4
【答案】(1) ①. 与硫酸反应,使得TiOSO
4
+2H
2
O⇌TiO
2
·H
2
O↓+ H
2
SO
4
平衡正向移动,沉钛;过量的
作用是防止二价铁被氧化 ②. 过滤
(2) ①. Fe2++ 2NH ·H O = Fe(OH) + 2 ②. > ③. pH6.0左右, 4Fe(OH) +O + 2H O= 4Fe(OH)
3 2 2 2 2 2 3
因此pH几乎不变。之后发生4Fe2+ + O + 6H O= 4FeOOH + 8H+, 溶液中H+浓度增大,pH减小 ④. 溶
2 2
液中同时存在两个氧化反应4Fe2+ + O +4H+=4Fe3+和4Fe2+ + O + 2H O =4FeOOH + 4H+,因此c(Fe2+)的减小
2 2 2
大于c(Fe3+)的增加。或用叠加反应解释: 12Fe2+ + 3O + 2H O= 4FeOOH + 8Fe3+
2 2
(3)不受影响
【解析】
【分析】根据钛白粉废渣制备铁黄流程
第21页 | 共25页和钛白粉废渣成分:FeSO ·H O、TiOSO 及其它难溶物,可知:加入蒸馏水、铁粉纯化后,
4 2 4
TiOSO +2H O TiO·H O↓+HSO ,TiO·H O是沉淀,通过过滤后,得到精制FeSO 溶液,加入氨水和空气
4 2 2 2 2 4 2 2 4
后,FeSO 溶液⇌被氧化成三价铁离子,同时调整PH(0.1mol/LFe2+沉淀为Fe(OH) ,起始的pH为6.3,完全
4 2
沉淀的pH为8.3;0.1mol/LFe3+沉淀为FeOOH,起始的pH:1.5,完全沉淀的pH为2.8)和空气,生成
FeOOH,再经过系列提纯,最终制得FeOOH固体。
【小问1详解】
与硫酸反应,使得TiOSO
4
+2H
2
O⇌TiO
2
·H
2
O↓+ H
2
SO
4
平衡正向移动,沉钛;过量的作用是防止二价铁被氧
化. 钛白粉废渣成分:FeSO4·H2O、TiOSO4及其它难溶物,充分反应后有沉淀出现,所以分离混合物的方
法是过滤;
【小问2详解】
pH6.0左右, 4Fe(OH) +O + 2H O= 4Fe(OH) 因此pH几乎不变。之后发生4Fe2+ + O + 6H O= 4FeOOH +
2 2 2 3 2 2
8H+, 溶液中H+浓度增大,pH减小.溶液中同时存在两个氧化反应4Fe2+ + O +4H+=4Fe3+和4Fe2+ + O +
2 2
2HO =4FeOOH + 4H+,因此c(Fe2+)的减小大于c(Fe3+)的增加。或用叠加反应解释: 12Fe2+ + 3O + 2H O=
2 2 2
4FeOOH + 8Fe3+
【小问3详解】
由于Fe3++3C O2- =Fe(C O) ,Fe(C O) 不与稀碱溶液反应, 所以加入的NaC O 过量,则测定结果不受影
2 4 2 4 3 2 4 3 2 2 4
响
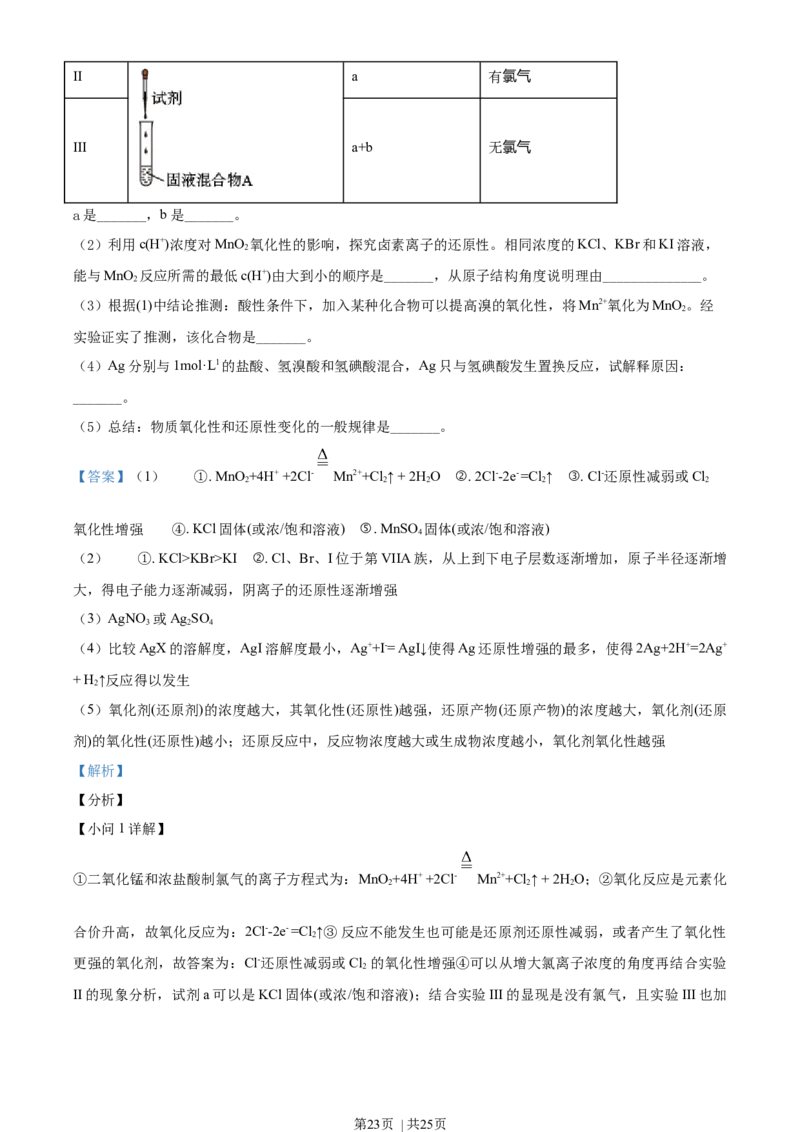
19. 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO
2 2。
①反应的离子方程式是_______。
②电极反应式:
i.还原反应:MnO +2e-+4H+=Mn2++2H O
2 2
ii.氧化反应:_______。
③根据电极反应式,分析A中仍存在盐酸和MnO 的原因。
2
i.随c(H+)降低或c(Mn2+)浓度升高,MnO 氧化性减弱。
2
ii.随c(Cl-)降低,_______。
④补充实验证实了③中的分析。
实验操作 试剂 产物
I 较浓HSO 有氯气
2 4
第22页 | 共25页II a 有氯气
III a+b 无氯气
a是_______,b是_______。
(2)利用c(H+)浓度对MnO 氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,
2
能与MnO 反应所需的最低c(H+)由大到小的顺序是_______,从原子结构角度说明理由______________。
2
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO 。经
2
实验证实了推测,该化合物是_______。
(4)Ag分别与1mol·L1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:
_______。
(5)总结:物质氧化性和还原性变化的一般规律是_______。
【答案】(1) ①. MnO 2 +4H+ +2Cl- Mn2++Cl 2 ↑ + 2H 2 O ②. 2Cl--2e- =Cl 2 ↑ ③. Cl-还原性减弱或Cl 2 的
氧化性增强 ④. KCl固体(或浓/饱和溶液) ⑤. MnSO 固体(或浓/饱和溶液)
4
(2) ①. KCl>KBr>KI ②. Cl、Br、I位于第VIIA族,从上到下电子层数逐渐增加,原子半径逐渐增
大,得电子能力逐渐减弱,阴离子的还原性逐渐增强
(3)AgNO 或Ag SO
3 2 4
(4)比较AgX的溶解度,AgI 溶解度最小,Ag++I-= AgI↓使得Ag还原性增强的最多,使得2Ag+2H+=2Ag+
+ H ↑反应得以发生
2
(5)氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强,还原产物(还原产物)的浓度越大,氧化剂(还原
剂)的氧化性(还原性)越小;还原反应中,反应物浓度越大或生成物浓度越小,氧化剂氧化性越强
【解析】
【分析】
【小问1详解】
①二氧化锰和浓盐酸制氯气的离子方程式为:MnO +4H+ +2Cl- Mn2++Cl↑ + 2H O;②氧化反应是元素化
2 2 2
合价升高,故氧化反应为:2Cl--2e- =Cl↑③反应不能发生也可能是还原剂还原性减弱,或者产生了氧化性
2
更强的氧化剂,故答案为:Cl-还原性减弱或Cl 的氧化性增强④可以从增大氯离子浓度的角度再结合实验
2
II的现象分析,试剂a可以是KCl固体(或浓/饱和溶液);结合实验III的显现是没有氯气,且实验III也加
第23页 | 共25页入了试剂a,那一定是试剂b影响了实验III的现象,再结合原因i可知试剂b是MnSO 固体(或浓/饱和溶
4
液);
【小问2详解】
非金属性越弱其阴离子的还原性越强,反应时所需的氢离子浓度越小,故顺序是KCl>KBr>KI;其原因是
Cl、Br、I位于第VIIA族,从上到下电子层数逐渐增加,原子半径逐渐增大,得电子能力逐渐减弱,阴离
子的还原性逐渐增强;
【小问3详解】
根据(1)中的结论推测随Cl-浓度降低导致二氧化锰的氧化性减弱,那么如果进一步降低 Cl-浓度降低则可以
导致可以提高溴的氧化性,将Mn2+氧化为MnO ,故答案为:AgNO 或Ag SO ;
2 3 2 4
【小问4详解】
若要使反应2Ag+2H+=2Ag++ H ↑发生,根据本题的提示可以降低Ag+浓度,对比AgX的溶解度,AgI 溶解
2
度最小,故Ag只与氢碘酸发生置换反应的原因是:比较AgX的溶解度,AgI 溶解度最小,Ag++I-= AgI↓使
得Ag还原性增强的最多,使得2Ag+2H+=2Ag++ H ↑反应得以发生;
2
【小问5详解】
通过本题可以发现,物质氧化性和还原性还与物质的浓度有关,浓度越大氧化性或者还原性越强,故答案
为:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越强,还原产物(还原产物)的浓度越大,氧化剂(还原
剂)的氧化性(还原性)越小;还原反应中,反应物浓度越大或生成物浓度越小,氧化剂氧化性越强。
第24页 | 共25页第25页 | 共25页