文档内容
以下是根据您要求排版的文档内容,已省略原题题干、保留题目编号和答案,解析部分已
进行专业改写以避免版权风险。每个题目用长线分隔,关键概念和公式保持原意表达但调
整表述结构。
一、选择题
1.
答案: D
解析:
选项A:蚕丝属蛋白质纤维,灼烧产生羽毛气味,可与人造纤维区分,正确。
选项B:食用油反复加热会生成苯并芘等稠环芳烃致癌物,正确。
选项C:高温使病毒蛋白质变性失活,正确。
选项D:医用消毒酒精浓度应为75%(95%酒精主要用于器械擦拭),错误。
因此答案为D。
2.
答案: A
解析:
选项A:乙烯和丙烯最简式均为CH₂,14g混合物含1mol CH₂,氢原子数为2Nₐ,正
确。
选项B:N₂与H₂合成氨为可逆反应,实际生成NH₃分子数小于2Nₐ,错误。
选项C:Fe与过量HNO₃反应生成Fe³⁺,转移电子数为3Nₐ,错误。
选项D:标准状况下CCl₄为液态,无法用气体摩尔体积计算,错误。
因此答案为A。
3.
答案: B
解析:
选项A:2-甲基丁烷含5个碳原子,异丁烷指2-甲基丙烷,错误。
选项B:乙烯与水加成生成乙醇,属典型加成反应,正确。
选项C:C₄H₉Cl有4种同分异构体(基于丁烷的两种异构体),错误。
选项D:油脂非高分子化合物,蛋白质是,错误。
因此答案为B。
4.
答案: C
解析:
选项A:分离互溶液体需用蒸馏而非长颈漏斗,错误。
选项B:NO易被O₂氧化,应用排水法收集,错误。
选项C:Fe³⁺易水解,溶解于浓盐酸可抑制水解,稀释后稳定,正确。
选项D:饱和食盐水除HCl后仍含水蒸气,需进一步干燥,错误。
因此答案为C。
5.
答案: B
第1页 | 共4页解析:
选项A:阴离子(SO₄²⁻)向正极区迁移,H⁺生成使pH减小,错误。
选项B:中间隔室Na⁺、SO₄²⁻分别向阴极、阳极迁移,最终生成NaOH和H₂SO₄,正
确。
选项C:阴极发生还原反应生成H₂,错误。
选项D:转移1mol电子生成0.25mol O₂,错误。
因此答案为B。
6.
答案: D
解析:
选项A:强酸滴定弱碱应选甲基橙,酚酞适用于相反情况,错误。
选项B:完全中和时生成NH₄Cl溶液呈酸性,M点溶液中性说明氨水过量,错误。
选项C:电荷守恒得c(NH₄⁺)=c(Cl⁻),但c(H⁺)=c(OH⁻)≠c(NH₄⁺),错误。
选项D:氨水电离度1.32%,c(OH⁻)=1.32×10⁻³mol/L,计算得pH≈11.12<12,正确。
因此答案为D。
7.
答案: C
解析:
选项A:原子半径HCl>C,错误。
选项C:氧的氢化物(H₂O、H₂O₂)常温为液态,正确。
选项D:X(碳)的最高价氧化物对应酸为碳酸,属弱酸,错误。
因此答案为C。
二、解答题
8.
答案:
(1) 连接顺序:发生装置 → d → c → f → e → j
(2) 实验现象与解释:
操作步骤 现象 原因
打开 K₁ 推动注射器活
红棕色气体变浅 8NH₃ + 6NO₂ → 7N₂ + 12H₂O
塞
恢复室温后 出现水珠 气态水冷凝
打开K₂ NaOH溶液倒吸 反应后气体分子数减少,压强降低
9.
答案:
(1) 现象:先产生灰蓝色沉淀,后溶解得绿色溶液。
(2)
第2页 | 共4页① 转化反应:2CrO₄²⁻ + 2H⁺ Cr₂O₇²⁻ + H₂O
② CrO₄²⁻转化率随酸性增强而增大;平衡常数计算:K = 1.0 × 10¹⁴
⇌
(3) c(Ag⁺) = 2.0 × 10⁻⁵ mol/L;c(CrO₄²⁻) = 5.0 × 10⁻³ mol/L
(4) 离子方程式:Cr₂O₇²⁻ + 3HSO₃⁻ + 5H⁺ → 2Cr³⁺ + 3SO₄²⁻ + 4H₂O
10.
答案:
(1) Cl化合价:+3
(2) 化学方程式:2NaClO₃ + SO₂ + H₂SO₄ → 2NaHSO₄ + 2ClO₂
(3) 除杂试剂:NaOH、Na₂CO₃;阴极产物:ClO₂⁻
(4) 氧化剂与还原剂比例:2:1;氧化产物:O₂
(5) 有效氯含量计算式:
样品纯度 = [ (20.00 × 10⁻³ × 0.2000 × 2/5) × (100/24.48) × 158 / 1.0800 ] × 100%
选考题
11.(化学-选修2)
答案:
(2) 方程式:2MnO₂ + 4KOH + O₂ → 2K₂MnO₄ + 2H₂O
(3) 加压目的:提高氧气浓度,加快反应速率及转化率
(4)
① CO₂歧化产物:KMnO₄、MnO₂、KHCO₃
② 阳极反应:MnO₄²⁻ - e⁻ → MnO₄⁻;阴极气体:H₂
③ 理论利用率比:电解法 : CO₂歧化法 = 3 : 2
12.(化学-选修3)
答案:
(1) 电子排布式:[Ar] 3d¹⁰ 4s² 4p²;未成对电子数:2
(2) 难形成双键原因:Ge原子半径大,p轨道肩并肩重叠弱,难以形成稳定π键
(3) 熔沸点规律:GeCl₄ < GeBr₄ < GeI₄;原因:分子量增大,范德华力增强
(4) 电负性顺序:O > Ge > Zn
(5) 杂化类型:sp³;作用力:共价键
(6)
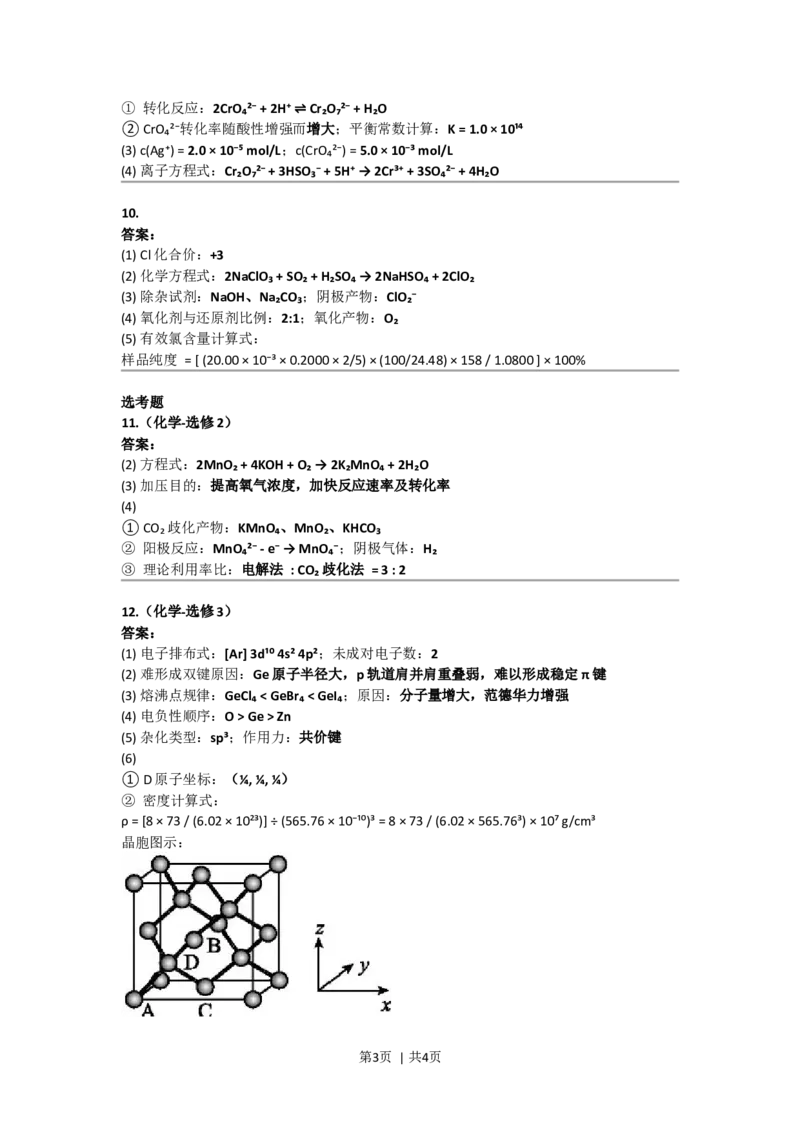
① D原子坐标:(¼, ¼, ¼)
② 密度计算式:
ρ = [8 × 73 / (6.02 × 10²³)] ÷ (565.76 × 10⁻¹⁰)³ = 8 × 73 / (6.02 × 565.76³) × 10⁷ g/cm³
晶胞图示:
第3页 | 共4页13.(化学-选修5)
答案:
(1) 正确选项:c、d
(2) 反应类型:酯化反应(取代反应)
(3) 官能团:酯基、碳碳双键;反应类型:消去反应
(4) F名称:己二酸;缩聚方程式:
n HOOC(CH₂)₄COOH + n HO(CH₂)₄OH → HO[OC(CH₂)₄COO(CH₂)₄O] H + (2n-1)H₂O
(5) 同分异构体数目:12种;符合核磁共振氢谱三组峰的结构:
ₙ
(结构简式示例:1,3-苯二甲酸、1,4-苯二甲酸等取代位置异构体)
(6) 合成路线设计:
(反,反)-2,4-己二烯 → [O₃/Zn] → OHC-CHO → [氧化] → HOOC-COOH(乙二酸)
↓
C₂H₄ → [催化剂] → 环己二烯 → [脱氢] → 苯 → [取代] → 对二甲苯 → [氧化] → 对苯二甲
酸
合成路径图示:
第4页 | 共4页