文档内容
2023年福建省高考化学试卷
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.唐代陆羽《茶经·三之造》中记载茶叶制作过程:“晴采之,蒸之,捣之,拍之,
焙之,穿之,封之,茶之干矣”。以下操作中最不可能引起化学变化的是
A.蒸 B.捣 C.焙 D.封
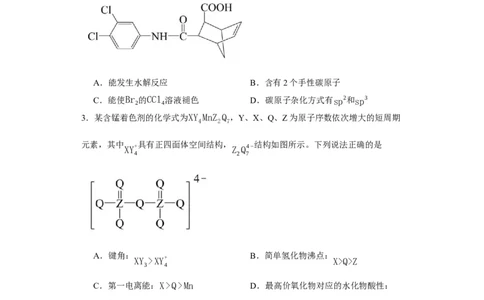
2.抗癌药物CADD522的结构如图。关于该药物的说法错误的是
A.能发生水解反应 B.含有2个手性碳原子
C.能使Br 的CCl 溶液褪色 D.碳原子杂化方式有sp2和sp3
2 4
3.某含锰着色剂的化学式为XY MnZ Q ,Y、X、Q、Z为原子序数依次增大的短周期
4 2 7
元素,其中 具有正四面体空间结构, 结构如图所示。下列说法正确的是
XY+ Z Q4−
4 2 7
A.键角: B.简单氢化物沸点:
XY >XY+ X>Q>Z
3 4
C.第一电离能:X>Q>Mn D.最高价氧化物对应的水化物酸性:
Z>X
4.我国新一代载人飞船使用的绿色推进剂硝酸羟胺 [NH OH) + [NO ) − 在催化剂作用下可
3 3
完全分解为N 、H O和O 。N 为阿伏加德罗常数的值,下列说法正确的是
2 2 2 A
A.
0.1mol[NH OH)
+含有的质子数为
1.5N
3 A
B.48g固态硝酸羟胺含有的离子数为0.5N
A
C.0.5mol硝酸羟胺含有的N−Oσ键数为2N
A
D.硝酸羟胺分解产生11.2LN (已折算为标况)的同时,生成O 分子数为N
2 2 A
第1页 | 共11页5.稀有气体氙的氟化物(XeF )与NaOH溶液反应剧烈,与水反应则较为温和,反应式
n
如下:
与水反应 与NaOH溶液反应
i.
ii.2XeF +4OH−=2Xe↑+O ↑+4F−+2H O
2XeF +2H O=2Xe↑+O ↑+4HF 2 2 2
2 2 2
iii. iv.2XeF +4Na++16OH−=
6
XeF +3H O=XeO +6HF Na XeO ↓+Xe↑+O ↑+12F−+8H O
6 2 3 4 6 2 2
下列说法错误的是
A.XeO 具有平面三角形结构 B.OH−的还原性比H O强
3 2
C.反应i~iv中有3个氧化还原反应 D.反应iv每生成1molO ,转移6mol电
2
子
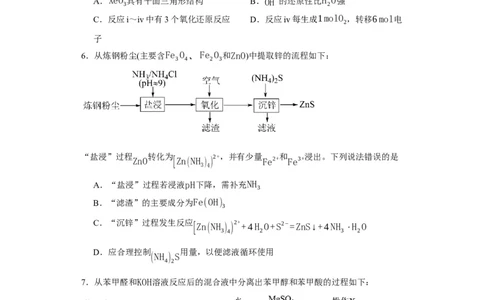
6.从炼钢粉尘(主要含Fe O 、Fe O 和ZnO)中提取锌的流程如下:
3 4 2 3
“盐浸”过程
ZnO
转化为
[Zn(NH ) )
2+,并有少量
Fe2+
和
Fe3+
浸出。下列说法错误的是
3 4
A.“盐浸”过程若浸液pH下降,需补充NH
3
B.“滤渣”的主要成分为Fe(OH)
3
C.“沉锌”过程发生反应 [Zn(NH ) ) 2+ +4H O+S2−=ZnS↓+4NH ⋅H O
3 4 2 3 2
D.应合理控制 用量,以便滤液循环使用
(NH ) S
4 2
7.从苯甲醛和KOH溶液反应后的混合液中分离出苯甲醇和苯甲酸的过程如下:
已知甲基叔丁基醚的密度为 。下列说法错误的是
0.74g⋅cm-3
A.“萃取”过程需振荡、放气、静置分层
B.“有机层”从分液漏斗上口倒出
C.“操作X”为蒸馏,“试剂Y”可选用盐酸
第2页 | 共11页D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
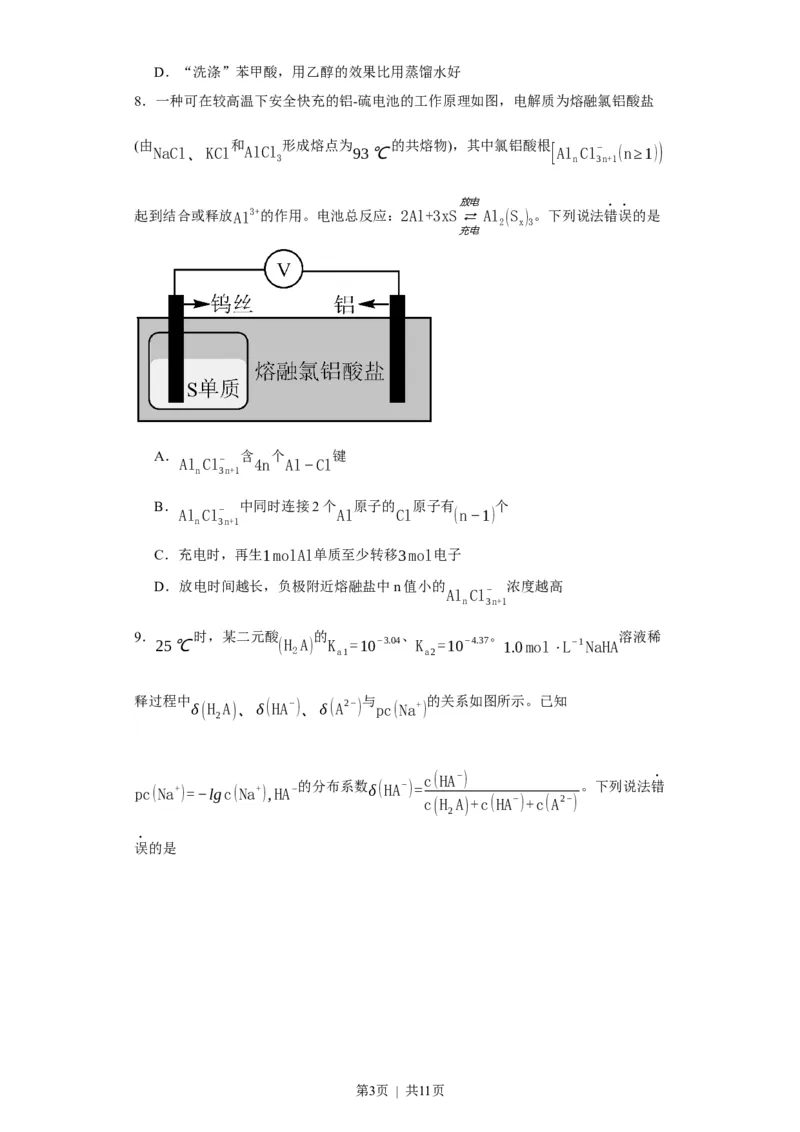
8.一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐
(由
NaCl、KCl
和
AlCl
形成熔点为
93℃
的共熔物),其中氯铝酸根
[Al Cl− (n≥1))
3 n 3n+1
放电
起到结合或释放Al3+的作用。电池总反应:2Al+3xS ⇄ Al (S ) 。下列说法错误的是
2 x 3
充电
A. 含 个 键
Al Cl− 4n Al−Cl
n 3n+1
B. 中同时连接2个 原子的 原子有 个
Al Cl− Al Cl (n−1)
n 3n+1
C.充电时,再生1molAl单质至少转移3mol电子
D.放电时间越长,负极附近熔融盐中n值小的 浓度越高
Al Cl−
n 3n+1
9. 时,某二元酸 的 、 。 溶液稀
25℃ (H A) K =10−3.04 K =10−4.37 1.0mol⋅L−1NaHA
2 a1 a2
释过程中 与 的关系如图所示。已知
δ(H A)、δ(HA−)、δ(A2−) pc(Na+)
2
c(HA−)
pc(Na+)=−lgc(Na+),HA−
的分布系数δ(HA−)= 。下列说法错
c(H A)+c(HA−)+c(A2−)
2
误的是
第3页 | 共11页A.曲线n为 的变化曲线 B.a点:
δ(HA−) pH=4.37
C.b点:
2c(H A)+c(HA−)=c(Na+)
D.c点:
2
c(Na+)+c(H+)=3c(HA−)+c(OH−)
二、工业流程题
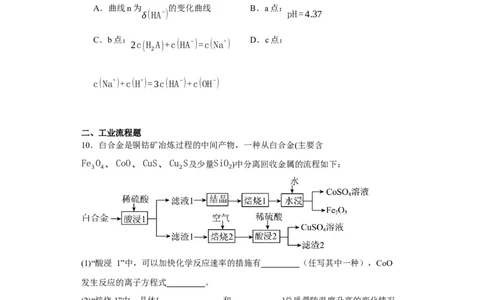
10.白合金是铜钴矿冶炼过程的中间产物,一种从白合金(主要含
Fe O 、CoO、CuS、Cu S及少量SiO )中分离回收金属的流程如下:
3 4 2 2
(1)“酸浸 1”中,可以加快化学反应速率的措施有 (任写其中一种),CoO
发生反应的离子方程式 。
(2)“焙烧1”中,晶体[ 和 ]总质量随温度升高的变化情况
Fe (SO ) ⋅xH O CoSO ⋅yH O
2 4 3 2 4 2
如下:
温度区间/℃ <227 227~566 566~600 600~630
晶体总质量 变小 不变 变小 不变
①升温至227℃过程中,晶体总质量变小的原因是 ;566~600℃发生分解的
物质是 (填化学式)。
②为有效分离铁、钴元素,“焙烧1”的温度应控制为 ℃。
第4页 | 共11页(3) 时, 的 。反应
25℃ K (CuS)=6.3×10−36,H S K =1.1×10−7,K =1.3×10−13
sp 2 a1 a2
CuS(s)+2H+ (aq)=Cu2+ (aq)+H S(aq)
的平衡常数
K=
(列出计算式即可)。经
2
计算可判断CuS难溶于稀硫酸。
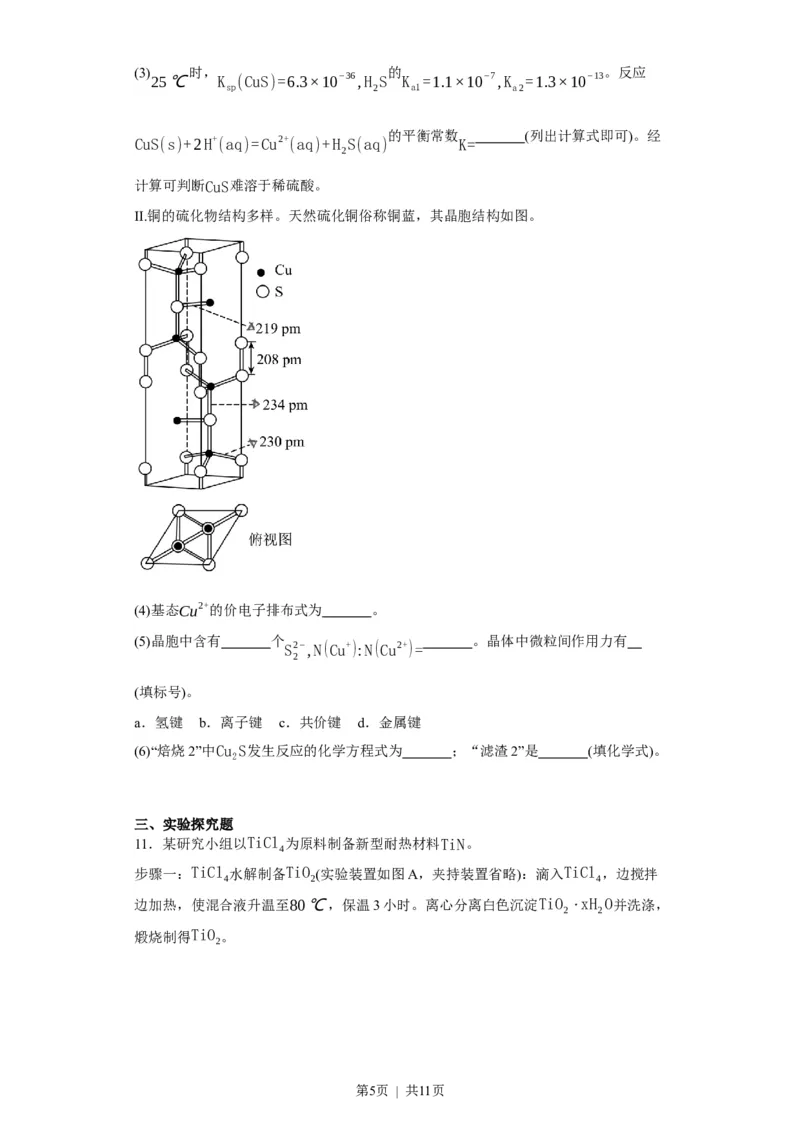
II.铜的硫化物结构多样。天然硫化铜俗称铜蓝,其晶胞结构如图。
(4)基态Cu2+的价电子排布式为 。
(5)晶胞中含有 个 。晶体中微粒间作用力有
S2−,N(Cu+):N(Cu2+)=
2
(填标号)。
a.氢键 b.离子键 c.共价键 d.金属键
(6)“焙烧2”中Cu S发生反应的化学方程式为 ;“滤渣2”是 (填化学式)。
2
三、实验探究题
11.某研究小组以TiCl 为原料制备新型耐热材料TiN。
4
步骤一:TiCl 水解制备TiO (实验装置如图A,夹持装置省略):滴入TiCl ,边搅拌
4 2 4
边加热,使混合液升温至80℃,保温3小时。离心分离白色沉淀TiO ⋅xH O并洗涤,
2 2
煅烧制得TiO 。
2
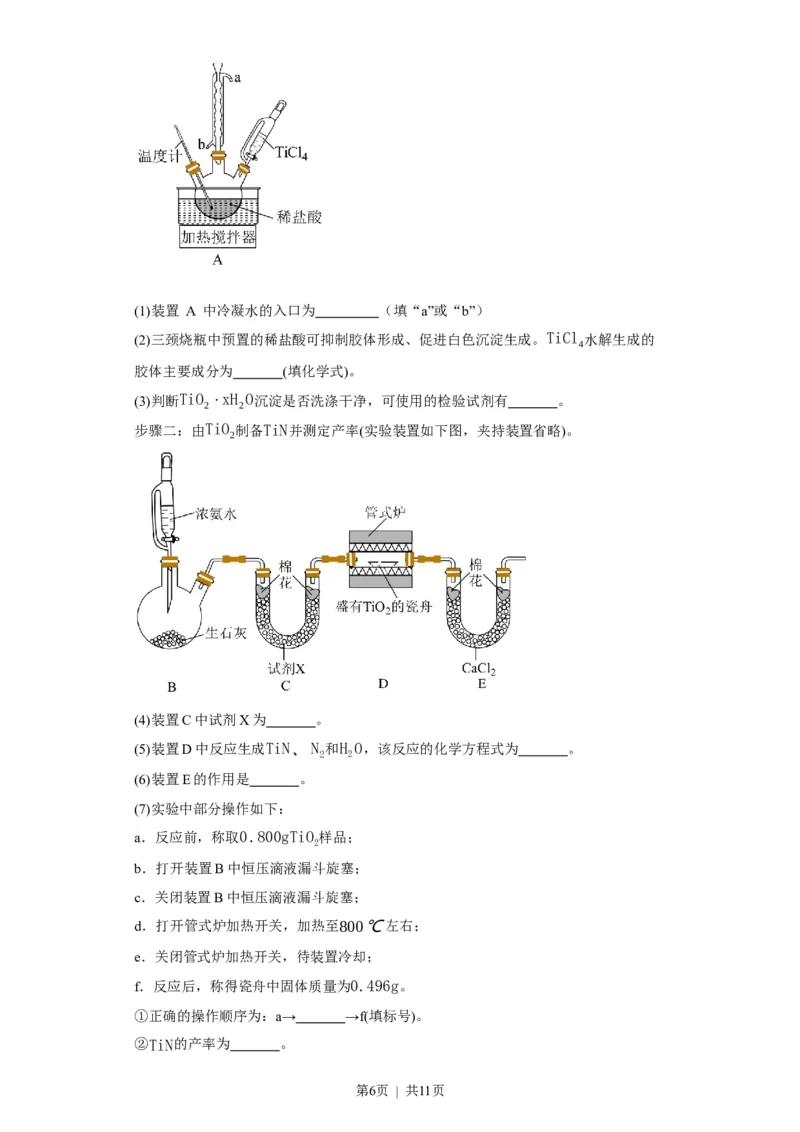
第5页 | 共11页(1)装置 A 中冷凝水的入口为 (填“a”或“b”)
(2)三颈烧瓶中预置的稀盐酸可抑制胶体形成、促进白色沉淀生成。TiCl 水解生成的
4
胶体主要成分为 (填化学式)。
(3)判断TiO ⋅xH O沉淀是否洗涤干净,可使用的检验试剂有 。
2 2
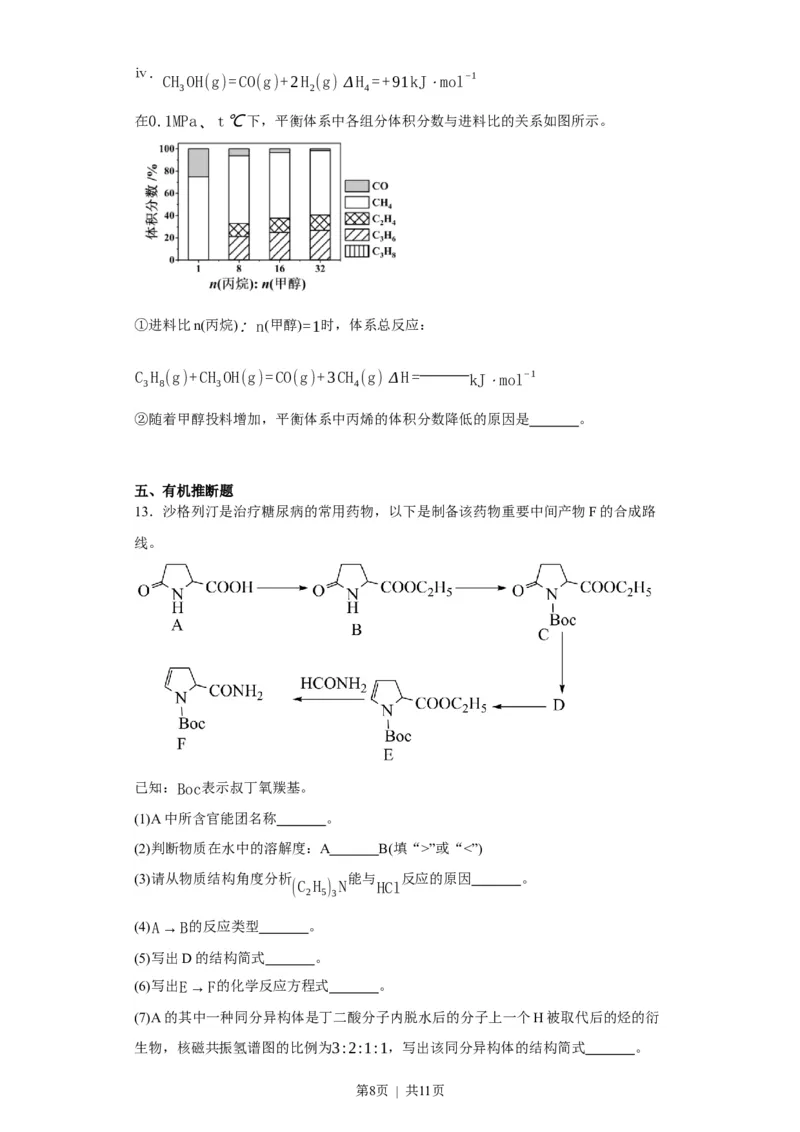
步骤二:由TiO 制备TiN并测定产率(实验装置如下图,夹持装置省略)。
2
(4)装置C中试剂X为 。
(5)装置D中反应生成TiN、N 和H O,该反应的化学方程式为 。
2 2
(6)装置E的作用是 。
(7)实验中部分操作如下:
a.反应前,称取0.800gTiO 样品;
2
b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至800℃左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为0.496g。
①正确的操作顺序为:a→ →f(填标号)。
②TiN的产率为 。
第6页 | 共11页四、原理综合题
12.探究甲醇对丙烷制丙烯的影响。丙烷制烯烃过程主要发生的反应有
ⅰ.
C H (g)=C H (g)+H (g) ΔH =+124kJ⋅mol−1 ΔS =127J⋅K−1 ⋅mol−1 K
3 8 3 6 2 1 1 p1
ⅱ.
C H (g)=C H (g)+CH (g) ΔH =+82kJ⋅mol−1 ΔS =135J⋅K−1 ⋅mol−1 K
3 8 2 4 4 2 2 p2
ⅲ.
C H (g)+2H (g)=3CH (g) ΔH =−120kJ⋅mol−1 ΔS =27.5J⋅K−1 ⋅mol−1 K
3 8 2 4 3 3 p3
已知:K 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在
p
0.1MPa、t℃下,丙烷单独进料时,平衡体系中各组分的体积分数φ见下表。
甲
物质 丙烯 乙烯 丙烷 氢气
烷
体积分数(%) 21 23.7 55.2 0.1 0
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应 ⅰ 反应 ⅱ(填
“>”或“<”)。
(2)①在该温度下,Kp 远大于 Kp ,但φ(C H)和φ(C H)相差不大,说明反应 ⅲ
2 1 3 6 2 4
的正向进行有利于反应 ⅰ 的 反应和反应 ⅱ 的 反应(填“正
向”或“逆向”)。
②从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序
为: 。
③平衡体系中检测不到H ,可认为存在反应:3C H (g)=2C H (g)+3CH (g) K ,
2 3 8 3 6 4 p
下列相关说法正确的是 (填标号)。
a.
K =K2 ⋅K
p p1 p3
b. 0.2102×0.5523×0.12
K = (MPa) 2
p 0.0013
c.使用催化剂,可提高丙烯的平衡产率
d.平衡后再通入少量丙烷,可提高丙烯的体积分数
④由表中数据推算:丙烯选择性 n (丙烯) (列出计算式)。
= 生成 ×100%=
n (丙烷)
转化
(3)丙烷甲醇共进料时,还发生反应:
第7页 | 共11页ⅳ.
CH OH(g)=CO(g)+2H (g) ΔH =+91kJ⋅mol−1
3 2 4
在0.1MPa、t℃下,平衡体系中各组分体积分数与进料比的关系如图所示。
①进料比n(丙烷):n(甲醇)=1时,体系总反应:
C H (g)+CH OH(g)=CO(g)+3CH (g) ΔH= kJ⋅mol−1
3 8 3 4
②随着甲醇投料增加,平衡体系中丙烯的体积分数降低的原因是 。
五、有机推断题
13.沙格列汀是治疗糖尿病的常用药物,以下是制备该药物重要中间产物F的合成路
线。
已知:Boc表示叔丁氧羰基。
(1)A中所含官能团名称 。
(2)判断物质在水中的溶解度:A B(填“>”或“<”)
(3)请从物质结构角度分析 能与 反应的原因 。
(C H ) N HCl
2 5 3
(4)A→B的反应类型 。
(5)写出D的结构简式 。
(6)写出E→F的化学反应方程式 。
(7)A的其中一种同分异构体是丁二酸分子内脱水后的分子上一个H被取代后的烃的衍
生物,核磁共振氢谱图的比例为3:2:1:1,写出该同分异构体的结构简式 。
第8页 | 共11页(只写一种)
第9页 | 共11页第1页 | 共11页