软件设计的PCR引物还跑出二聚体?

大家在做PCR实验的时候会不会突然遇到这种情况:
引物明明是用Primer3、Oligo等专业软件设计的,参数全优、还送公司正规合成,理论上不该有问题,可一跑电泳,清晰的引物二聚体条带就冒出来,轻则干扰结果判读,重则直接导致扩增失败……
明明是最优设计,为啥还会出现二聚体?核心原因可能是软件的理论预测,和真实的PCR反应体系之间,永远存在差距。
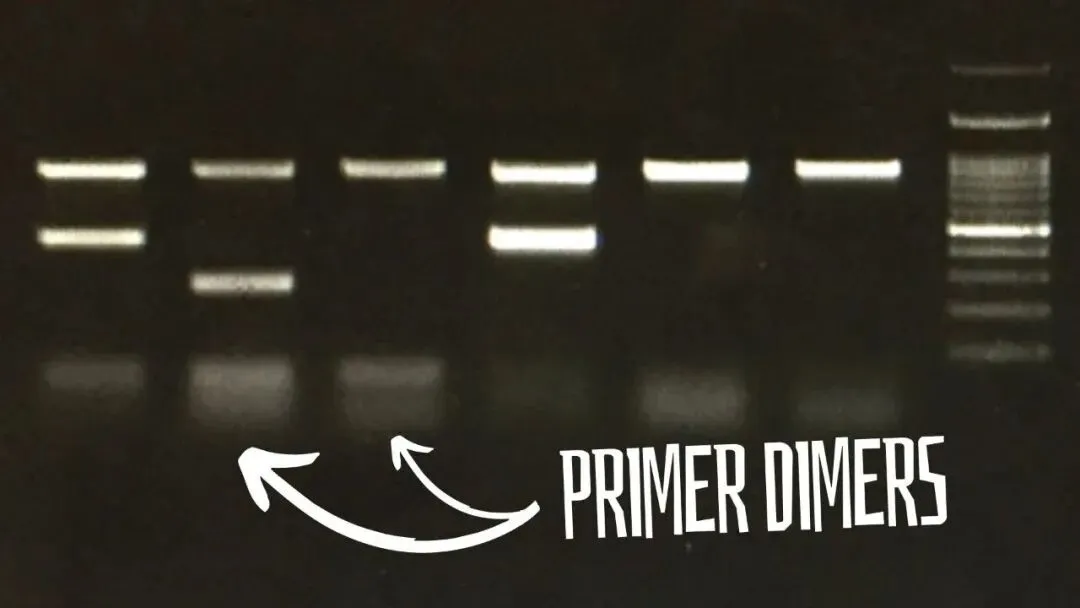
软件再智能,也有先天局限
引物设计软件的算法再完善,都是基于理想反应模型计算的,和实验室的实际条件会存在一定的偏差:
1.默认体系太完美
软件预测时,会默认Mg²⁺、Na⁺等盐离子浓度、dNTP用量、缓冲液环境都是标准理想值,但我们实际配体系时,哪怕是不同批次的试剂、细微的操作误差,都会偏离这个理想状态,二聚体的预测结果自然会失真。
2.二聚体预测能力有限
软件判断二聚体主要靠热力学参数(ΔG吉布斯自由能变),本质是计算机模拟,无法100%还原真实的分子互作。尤其是做多重PCR时,多对引物之间的复杂相互作用,软件更是很难精准预判。
实验操作偏差
理论设计没问题,栽在实验环节的情况占了绝大多数,这几个点最容易踩坑:
1.退火温度(Tm)设置不对
软件给出的Tm值只是理论参考,实际会被缓冲体系、引物浓度、模板复杂度直接影响。退火温度过低→引物错配,轻易形成二聚体;温度过高→引物没法结合模板,游离的引物反而更容易相互配对。
2.模板不给力
模板里存在和引物部分互补的序列,会诱导引物错配形成二聚体;模板浓度太低→引物相对过量,大量未结合模板的引物会互相结合,大幅增加二聚体概率。
3.引物纯度不够
同样是公司合成,纯化方式直接影响引物质量:脱盐、PAGE、HPLC纯化的纯度逐级升高。如果是难度较高的扩增,只用脱盐纯化的引物,短片段杂质多,就特别容易形成二聚体。
还有些易被忽略的细节
-
引物浓度过高:引物过量,反应消耗不完,剩余分子就会抱团形成二聚体;
-
Mg²⁺浓度不当:Mg²⁺是聚合酶辅因子,浓度太高会增强非特异性结合,太低又影响酶活性,都会间接诱发二聚体;
-
其他因素:PCR循环次数太多、酶量加得过量、体系出现轻微污染,也会让二聚体更明显。

手把手优化
引物二聚体没法完全消除,只要把它控制在极淡、不影响目标条带的程度就合格,科研考虑按这个顺序来:
第一步:先优化PCR体系
1.做梯度退火温度
以软件预测的Tm为中心,设置±2~5℃的梯度(每孔间隔1~2℃),跑一次梯度PCR就能找到最佳温度;GC含量>60%的引物,可适当提高退火温度。
2.降低引物浓度
把引物工作液浓度依次试0.1μM、0.05μM,多数情况能明显减少二聚体,注意别太低导致扩增效率下降。
3.梯度调试Mg²⁺浓度
以0.5mM为步进,在1.0~3.0mM区间测试,找到既能保证扩增、又能抑制二聚体的浓度。
第二步:微调引物参数
1.检查3’端互补
用Primer-BLAST核查,保证正反向引物3’端互补碱基不超过2个,3’端是扩增关键,微弱互补都会催生二聚体。
2.规范GC含量与长度
引物GC含量控制在40%~60%,长度18~25bp,避免连续3个以上G/C(如 GGG、CCC)。
3.升级引物纯化
普通PCR用脱盐纯化即可;长引物、难扩增片段,选PAGE或HPLC 纯化,高纯度能减少杂质引发的非特异性结合。
引物溶解后一定要分装保存,绝对避免一管引物反复冻融;同时控制PCR循环数,酶量按说明书规范添加,别盲目多加。
以上就是今天的实验分享,欢迎点赞收藏转发共同学习、共同进步!

关于凯锐医CAREYMED

凯锐医生物是一家专注于基础医学研究服务的高新技术企业。我们致力于为生命科学领域的研究者提供全方位、高质量的实验技术支持,涵盖细胞实验、动物模型构建、生物病理检测等核心服务。让每一次合作都能赋能科研突破,让每一次服务都能加速成果转化,让每一次携手都能守护研究初心,成为您科研路上的坚实后盾。
期待你的
分享
点赞
在看
 夜雨聆风
夜雨聆风




