文档内容
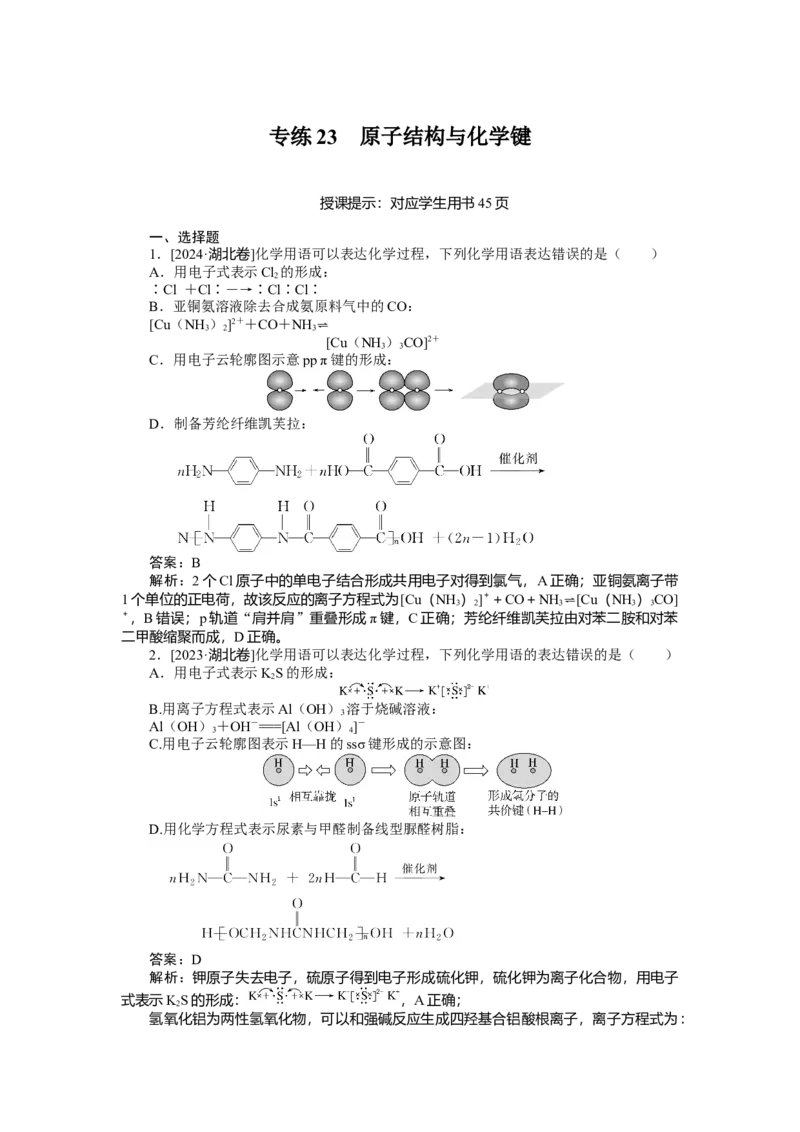
专练 23 原子结构与化学键
授课提示:对应学生用书45页
一、选择题
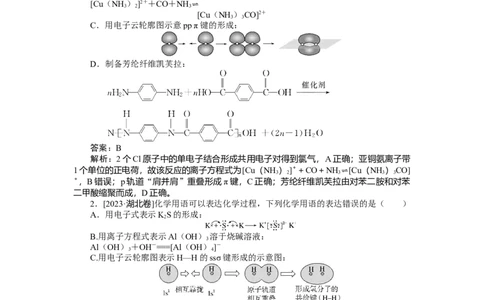
1.[2024·湖北卷]化学用语可以表达化学过程,下列化学用语表达错误的是( )
A.用电子式表示Cl 的形成:
2
∶Cl +Cl∶―→∶Cl∶Cl∶
B.亚铜氨溶液除去合成氨原料气中的CO:
[Cu(NH
3
)
2
]2++CO+NH
3⇌
[Cu(NH )CO]2+
3 3
C.用电子云轮廓图示意pp π键的形成:
D.制备芳纶纤维凯芙拉:
答案:B
解析:2个Cl原子中的单电子结合形成共用电子对得到氯气,A正确;亚铜氨离子带
1个单位的正电荷,故该反应的离子方程式为[Cu(NH
3
)
2
]++CO+NH 3⇌[Cu(NH
3
)
3
CO]
+,B错误;p轨道“肩并肩”重叠形成π键,C正确;芳纶纤维凯芙拉由对苯二胺和对苯
二甲酸缩聚而成,D正确。
2.[2023·湖北卷]化学用语可以表达化学过程,下列化学用语的表达错误的是( )
A.用电子式表示KS的形成:
2
B.用离子方程式表示Al(OH) 溶于烧碱溶液:
3
Al(OH)+OH-===[Al(OH)]-
3 4
C.用电子云轮廓图表示H—H的ssσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
答案:D
解析:钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电子
式表示KS的形成: ,A正确;
2
氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:Al(OH)+OH-===[Al(OH)]-,B正确;
3 4
H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,
形成新的轨道,则用电子云轮廓图表示H—H的ssσ键形成的示意图:
,
C正确;
用化学方程式表示尿素与甲醛制备线型脲醛树脂
D错误;故选D。
3.[2022·北京卷] Sr(锶)的87Sr、86Sr稳定同位素在同一地域土壤中87Sr/86Sr值不变。
38
土壤生物中87Sr/86Sr值与土壤中87Sr/86Sr值有效相关。测定土壤生物中87Sr/86Sr值可进行产
地溯源。下列说法不正确的是( )
A.Sr位于元素周期表中第六周期、第ⅡA族
B.可用质谱法区分87Sr和86Sr
C.87Sr和86Sr含有的中子数分别为49和48
D.同一地域产出的同种土壤生物中87Sr/86Sr值相同
答案:A
解析:Sr和Mg、Ca同主族,位于元素周期表第五周期ⅡA族,A项错误;87Sr和86Sr
的质量数不同,可用质谱法区分,B项正确;Sr的质子数为38,87Sr的中子数为87-38=
49,86Sr的中子数为86-38=48,C项正确;根据题意可知,D项正确。
4.[2023·全国甲卷]W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电
子数之和为19。Y的最外层电子数与其K层电子数相等,WX 是形成酸雨的物质之一。下
2
列说法正确的是( )
A.原子半径:X>W
B.简单氢化物的沸点:XX
B.简单氢化物的沸点:Y>X>Z
C.XY 是导致酸雨的主要物质之一
2
D.基态M原子核外电子有9种运动状态
答案:C
解析:X、Y、Z、M为原子序数依次增大的短周期主族元素,其中基态X原子有3个
未成对电子,则X为氮元素,Y、M位于同一主族,且Y、Z、M原子最外层电子数之和为
13,则Y、M的最外层电子数均为6,Z的最外层电子数为1,则Y为氧元素,M为硫元素,
Z为钠元素。核外电子排布相同的离子,随原子序数递增,离子半径逐渐减小,则简单离
子半径:Na+< N3-,A项错误;NaH常温下为固体,HO常温下为液态,NH 常温下为气
2 3
态,因此简单氢化物的沸点:NH X
eq ¿(H,¿¿4(··))
B.YH的电子式为:[H∶ ∶H]+
Y
C.最高价含氧酸的酸性:Y>X
D.X与Y均能形成多种氢化物
答案:C
解析:由已知核反应可得Z+0=M+1、A+1=R+1,Y可用于测定文物年代,则Y
是C,R=14、M=6、A=14、Z=7,X是N。
同周期主族元素从左到右原子半径逐渐减小,A项正确;C结合3个H失去1个电子
形成CH,B项正确;HNO 的酸性强于HCO,C项错误;N可以形成NH 、NH,C可以
3 2 3 3 2 4
形成多种烃,D项正确。
9.[2024·河北存瑞中学高三质检]W、X、Y是原子序数依次增大的同一短周期元素。
W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层
电子数是核外电子层数的2倍,W与Y可形成化合物WY。下列说法正确的是( )
2
A.Y的低价氧化物与O 漂白的原理相同
3
B.Y的氢化物和WY所含化学键的类型相同
2C.上述三种元素形成的简单离子,X离子半径最小
D.工业上常用电解相应的盐溶液制备W、X的单质
答案:C
解析:由题意可知W、X、Y分别是Na、Al、S。SO 的漂白原理是化合,而臭氧的漂
2
白是氧化性,A不正确;HS中含有共价键,NaS中含有离子键,B错误;S2-核外有3个
2 2
电子层。Na+和Al3+具有2个电子层,离子半径均小于S2-的。在核外电子排布相同的条件
下,微粒半径随原子序数的增大而减小,即Al3+离子半径最小,C正确;工业上电解熔融
氯化钠制取钠,电解熔融氧化铝制取铝,D错误。
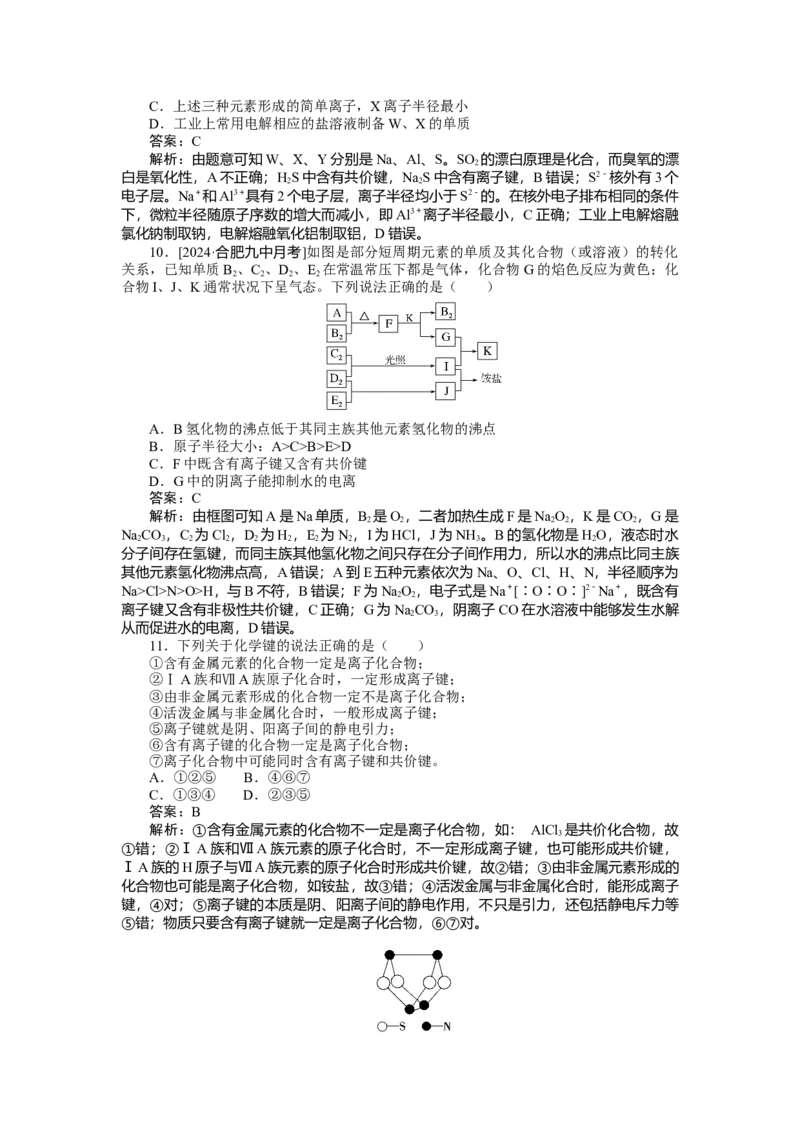
10.[2024·合肥九中月考]如图是部分短周期元素的单质及其化合物(或溶液)的转化
关系,已知单质B 、C 、D 、E 在常温常压下都是气体,化合物G的焰色反应为黄色;化
2 2 2 2
合物I、J、K通常状况下呈气态。下列说法正确的是( )
A.B氢化物的沸点低于其同主族其他元素氢化物的沸点
B.原子半径大小:A>C>B>E>D
C.F中既含有离子键又含有共价键
D.G中的阴离子能抑制水的电离
答案:C
解析:由框图可知A是Na单质,B 是O ,二者加热生成F是NaO ,K是CO ,G是
2 2 2 2 2
NaCO ,C 为Cl ,D 为H ,E 为N ,I为HCl,J为NH 。B的氢化物是HO,液态时水
2 3 2 2 2 2 2 2 3 2
分子间存在氢键,而同主族其他氢化物之间只存在分子间作用力,所以水的沸点比同主族
其他元素氢化物沸点高,A错误;A到E五种元素依次为Na、O、Cl、H、N,半径顺序为
Na>Cl>N>O>H,与B不符,B错误;F为NaO,电子式是Na+[∶O∶O∶]2-Na+,既含有
2 2
离子键又含有非极性共价键,C正确;G为NaCO ,阴离子CO在水溶液中能够发生水解
2 3
从而促进水的电离,D错误。
11.下列关于化学键的说法正确的是( )
①含有金属元素的化合物一定是离子化合物;
②ⅠA族和ⅦA族原子化合时,一定形成离子键;
③由非金属元素形成的化合物一定不是离子化合物;
④活泼金属与非金属化合时,一般形成离子键;
⑤离子键就是阴、阳离子间的静电引力;
⑥含有离子键的化合物一定是离子化合物;
⑦离子化合物中可能同时含有离子键和共价键。
A.①②⑤ B.④⑥⑦
C.①③④ D.②③⑤
答案:B
解析:①含有金属元素的化合物不一定是离子化合物,如: AlCl 是共价化合物,故
3
①错;②ⅠA族和ⅦA族元素的原子化合时,不一定形成离子键,也可能形成共价键,
ⅠA族的H原子与ⅦA族元素的原子化合时形成共价键,故②错;③由非金属元素形成的
化合物也可能是离子化合物,如铵盐,故③错;④活泼金属与非金属化合时,能形成离子
键,④对;⑤离子键的本质是阴、阳离子间的静电作用,不只是引力,还包括静电斥力等
⑤错;物质只要含有离子键就一定是离子化合物,⑥⑦对。12.[素材创新]现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经
合成的最著名的硫氮化合物的分子结构。下列说法不正确的是( )
A.该物质的分子式为SN
4 4
B.该物质各原子最外层都达到8电子稳定结构
C.该物质的分子中既含有极性键又含有非极性键
D.该分子中N的化合价为-3
答案:D
解析:由图可知,该分子的分子式为SN ,因为N的非金属性比S强,N显负价,所
4 4
以N在右边,A正确;因为S原子最外层为6个电子,若形成两个共价单键,则达8电子
稳定结构,N原子最外层为5个电子,若形成3个共价单键,则达8电子稳定结构,据图
可知,B正确;该分子中既含有极性键(N—S键)又含有非极性键(N—N键),C正确;
N—S共用电子对偏向N,N—N共用电子对不偏移,故该分子中N的化合价为-2,D错
误。
二、非选择题
13.城市为保持街道整洁、湿润,在路面或广场上喷洒含化学式为XY 的溶液做保湿
2
剂。X原子的结构示意图为 ,X的阳离子与Y的阴离子的电子层结构相同。元
素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻
且Z、W能形成一种WZ 型分子。
2
(1)m= ,该保湿剂的化学式为 。
(2)Z、W元素的名称为 、 。
(3)下列说法正确的是 (填选项字母)。
A.XY 和WZ 都为离子化合物
2 2
B.XY 中仅含离子键,WZ 中仅含共价键
2 2
C.HZ比HY的稳定性强
2
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是 (填选项字母)。
A.XY 的电子式:X2+[∶Y∶Y∶]2-
2
B.WZ 的结构式:Z===W===Z
2
C.Y元素的单质与HZ水溶液反应的离子方程式为Y+Z2-===2Y-+Z↓
2 2
D.用电子式表示XY 的形成过程为
2
答案:(1)20 CaCl (2)硫 碳 (3)B (4)BD
2
解析:(1)由X原子的结构示意图 不难推知其为 ,该元素为
Ca,根据CaY 可知Y为-1价,又因Y-与Ca2+的电子层结构相同可知Y为Cl。
2
(2)Z、W原子的最外层电子数是其电子层数的2倍,且Z、W能形成一种ZW 型分
2
子,则Z、W是C或S。Z与Y相邻,则Z是S,W是C。
(3)CaCl 是仅含离子键的离子化合物,CS 是共价化合物,仅含有共价键,A项错误,
2 2
B项正确;根据周期律,S的非金属性弱于Cl,则HS的稳定性比HCl弱,C项错误;Ca2
2
+、Cl-具有相同的电子层结构,但Ca2+的核电荷数大,半径小,D项错误。(4)XY 为
2
CaCl ,其电子式为[∶Cl∶]-Ca2+[∶Cl∶]-,HS的水溶液为弱酸,应写成分子式,即Cl
2 2 2
+HS===2H++2Cl-+S↓,A、C两项错误。
2