文档内容
成都市 2009 年高中阶段教育学校统一招生考试试卷
(含成都市初三毕业会考)
化 学
本试卷分第一卷(选择题)和第二卷(非选择题)两部分。全卷满分90分,考试时间60分钟。
第一卷(选择题,共36分)
一、选择题(本题包括12个小题,每小题3分,共36分。每小题只有一个选项符合题意)
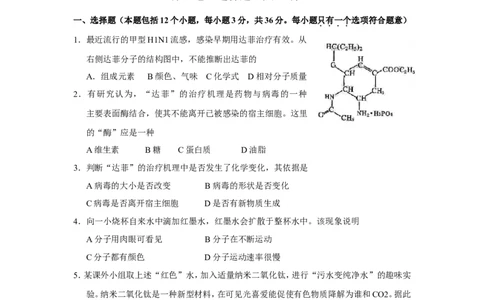
1.最近流行的甲型H1N1流感,感染早期用达菲治疗有效。从
右侧达菲分子的结构图中,不能推断出达菲的
A.组成元素 B颜色、气味 C化学式 D相对分子质量
2.有研究认为,“达菲”的治疗机理是药物与病毒的一种
主要表面酶结合,使其不能离开已被感染的宿主细胞。这里
的“酶”应是一种
A维生素 B糖 C蛋白质 D油脂
3.判断“达菲”的治疗机理中是否发生了化学变化,其依据是
A病毒的大小是否改变 B病毒的形状是否变化
C病毒是否离开宿主细胞 D是否有新物质生成
4.向一小烧杯自来水中滴加红墨水,红墨水会扩散于整杯水中。该现象说明
A分子用肉眼可看见 B分子在不断运动
C分子都有颜色 D分子运动速率很慢
5.某课外小组取上述“红色”水,加入适量纳米二氧化钛,进行“污水变纯净水”的趣味实
验。纳米二氧化钛是一种新型材料,在可见光喜爱能促使有色物质降解为谁和CO2。据此
推测,纳米二氧化钛在污水处理中可作
A吸附剂 B絮凝剂 C消毒剂 D催化剂
6.据统计,成都市因自来水管网老化引起的爆管事故,一年就会损失自来水300多万立方米。
现在常用PVC(聚氯乙烯)等塑料管替代以前使用的镀锌钢管。PVC管的主要优点是
A耐腐蚀,不生锈 B具有一般金属的硬度
C不易燃烧,可回收 D不易造成“白色污染E”
7.右表为元素周期表的一部分,A—E代表五种不同元素。下列说法不正确的是
第 1 页 共 8 页A.原子序数C>B B.核内质子数:A=E
C.B、C同周期 D.A、D同族
8.在大烧杯中导入一定量水,加入适量NH NO ,搅拌,水的温度会急剧降低。说明NH NO
4 3 4 3
溶于水时
A吸收热量 B放出热量 C既不吸热也不放热 D无法判断
9.将少量大都油倒入一个小铁盒中带你然,用坩埚钳把小铁盒放在冰冷的水面上,可观察到
火焰立即熄灭。该实验证明,达到灭火目的的方法之一是
A清除可燃物 B隔绝空气 C降温至着火点以下 D降低着火点
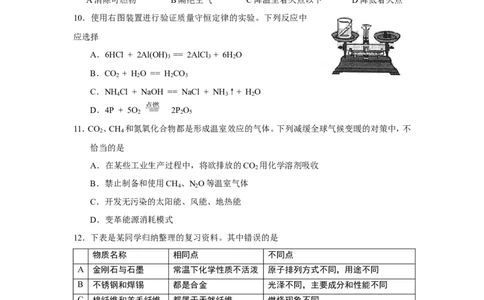
10.使用右图装置进行验证质量守恒定律的实验。下列反应中
应选择
A.6HCl + 2Al(OH)
3
== 2AlCl
3
+ 6H
2
O
B.CO
2
+ H
2
O == H
2
CO
3
C.NH Cl + NaOH == NaCl + NH ↑+ H O
4 3 2
点燃
D.4P + 5O
2
== 2P
2
O
5
11.CO 、CH 和氮氧化合物都是形成温室效应的气体。下列减缓全球气候变暖的对策中,不
2 4
恰当的是
A.在某些工业生产过程中,将欲排放的CO 用化学溶剂吸收
2
B.禁止制备和使用CH 、N O等温室气体
4 2
C.开发无污染的太阳能、风能、地热能
D.变革能源消耗模式
12.下表是某同学归纳整理的复习资料。其中错误的是
物质名称 相同点 不同点
A 金刚石与石墨 常温下化学性质不活泼 原子排列方式不同,用途不同
B 不锈钢和焊锡 都是合金 光泽不同,主要成分和性能不同
C 棉纤维和羊毛纤维 都属于天然纤维 燃烧现象不同
D 纯碱和熟石灰 都是碱 熟石灰能用于中和酸性土壤,纯碱不能
第二卷(非选择题)
二﹑(本题包括2个小题, 共12分)
13. (6分)右表中有六种人体必需的元素.
元 素 钙 钠 钾
(1)表中元素主要以______________的形式存在于人体中(填 名 称 铁 碘 氟
第 2 页 共 8 页“酸”“碱”“或”“无机盐”).
(2)若将表中元素进行简单分类, 则碘、氟属于__________元素(填“金属” “非金属”或
“稀有气体”); 其中碘的元素符号是_________.
(3)钙在人体中主要以羟基磷酸钙【(Ca (PO )(OH) 】的形式存在.其中P的化合价为______.
10 4 6 2
(4)人体缺铁会引起__________;为保证铁的摄入量, 可选择的食物有_____________(填一
种食物名称)
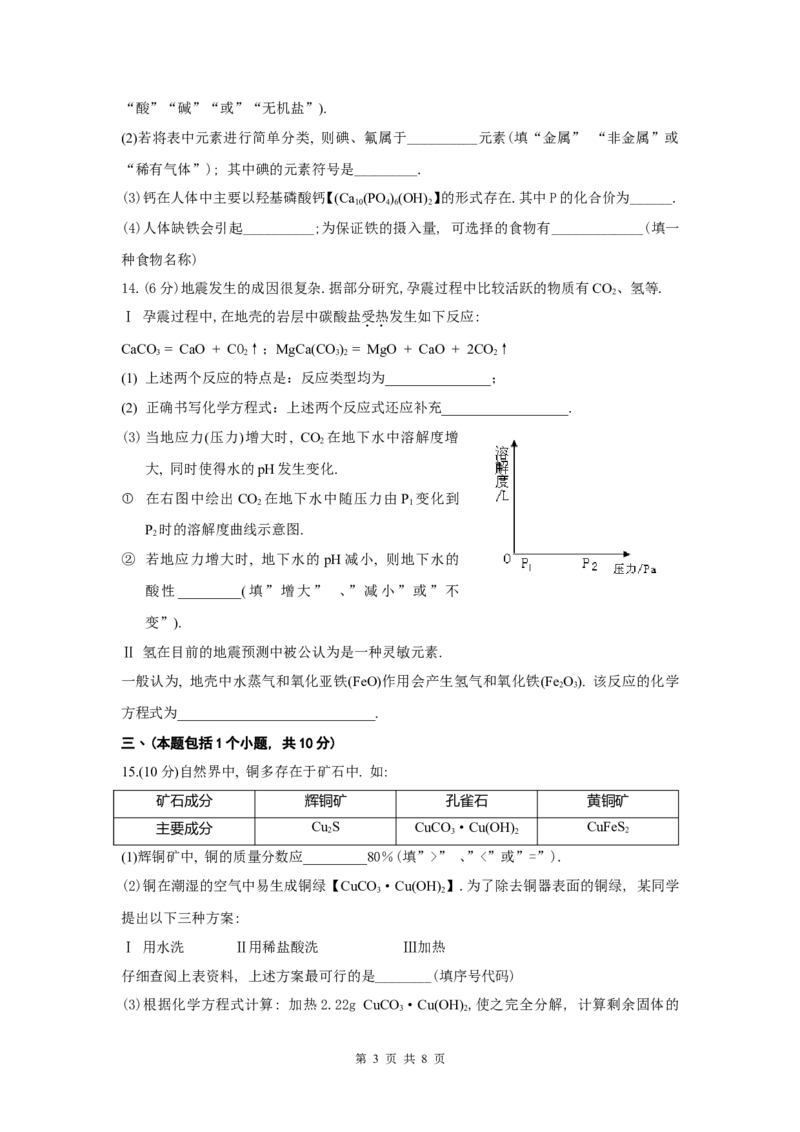
14.(6分)地震发生的成因很复杂.据部分研究,孕震过程中比较活跃的物质有CO、氢等.
2
Ⅰ 孕震过程中,在地壳的岩层中碳酸盐受热发生如下反应:
CaCO = CaO + CO↑;MgCa(CO) = MgO + CaO + 2CO↑
3 2 3 2 2
(1) 上述两个反应的特点是:反应类型均为_______________;
(2) 正确书写化学方程式:上述两个反应式还应补充__________________.
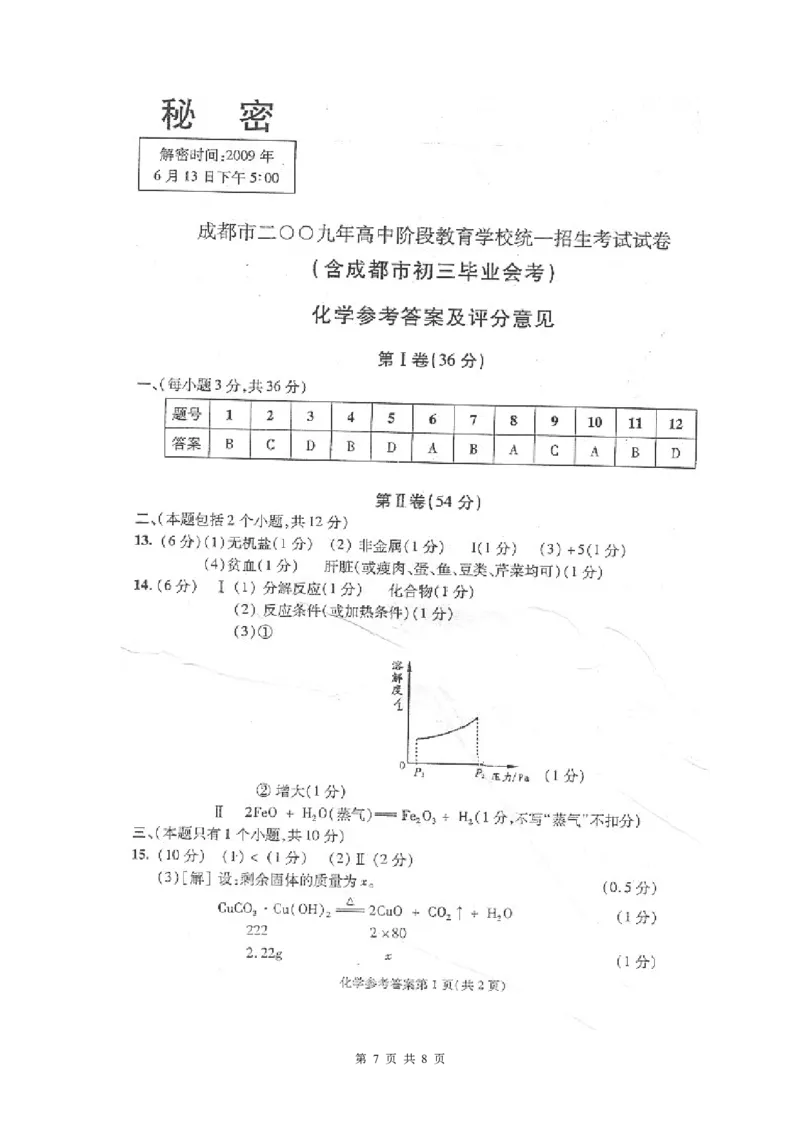
(3)当地应力(压力)增大时, CO 在地下水中溶解度增
2
大, 同时使得水的pH发生变化.
① 在右图中绘出CO 在地下水中随压力由P 变化到
2 1
P 时的溶解度曲线示意图.
2
② 若地应力增大时, 地下水的pH减小, 则地下水的
酸性_________(填”增大” 、”减小”或”不
变”).
Ⅱ 氢在目前的地震预测中被公认为是一种灵敏元素.
一般认为, 地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe O). 该反应的化学
2 3
方程式为____________________________.
三﹑(本题包括1个小题, 共10分)
15.(10分)自然界中, 铜多存在于矿石中. 如:
矿石成分 辉铜矿 孔雀石 黄铜矿
主要成分 Cu 2 S CuCO 3 ·Cu(OH) 2 CuFeS 2
(1)辉铜矿中, 铜的质量分数应_________80%(填”>” 、”<”或”=”).
(2)铜在潮湿的空气中易生成铜绿【CuCO·Cu(OH) 】.为了除去铜器表面的铜绿, 某同学
3 2
提出以下三种方案:
Ⅰ 用水洗 Ⅱ用稀盐酸洗 Ⅲ加热
仔细查阅上表资料, 上述方案最可行的是________(填序号代码)
(3)根据化学方程式计算: 加热2.22g CuCO·Cu(OH) ,使之完全分解, 计算剩余固体的
3 2
第 3 页 共 8 页质量.
(4)工业上以黄铜矿为原料生产铜时会产生SO 尾气. 将SO 直接排放到大气中, 溶于雨水会
2 2
形成__________; 处理该尾气一般是将SO 循环制备成HSO , 用氨水吸收. HSO ,与氨
2 2 4 2 4
水反应生成的铵盐是一种常见氮肥, 该盐是____________(写化学式或名称)
四﹑(本题包括2个小题, 共22分)
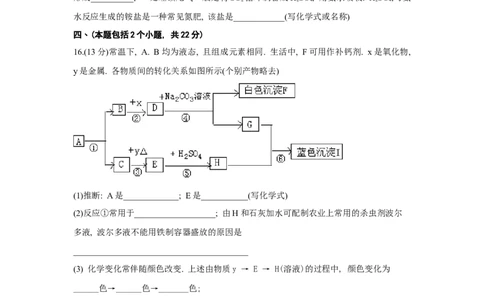
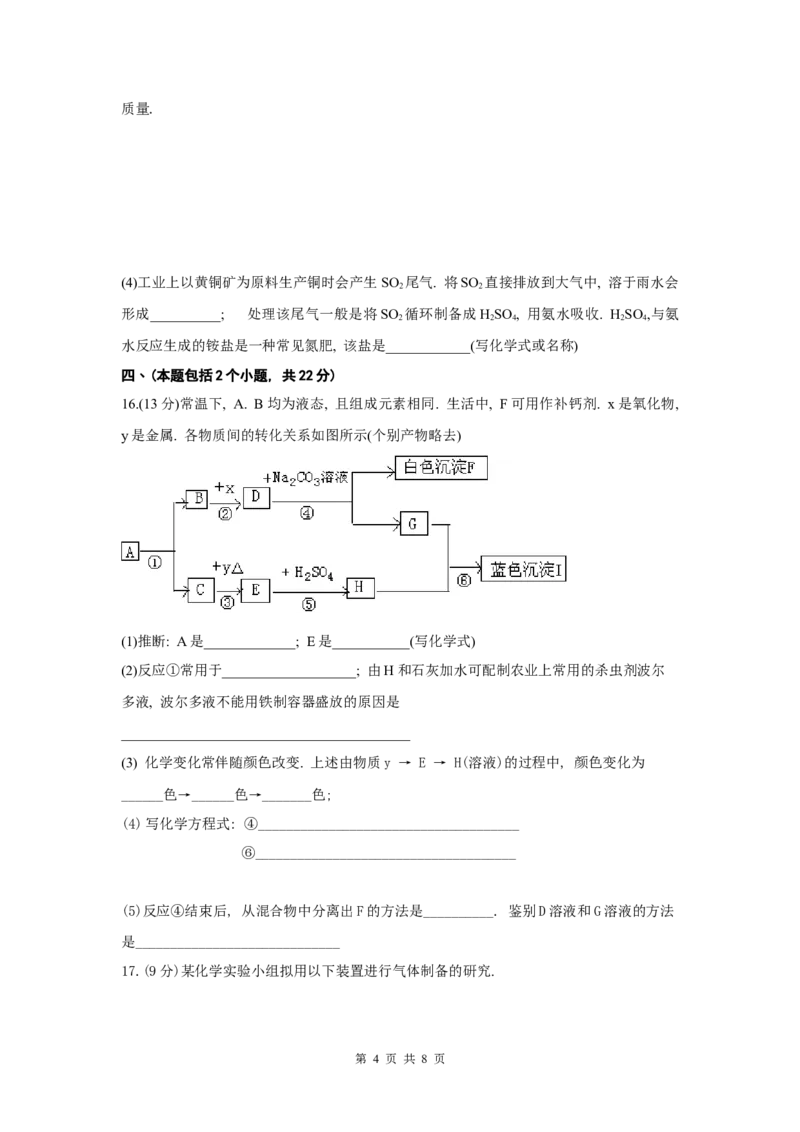
16.(13分)常温下, A. B均为液态, 且组成元素相同. 生活中, F可用作补钙剂. x是氧化物,
y是金属. 各物质间的转化关系如图所示(个别产物略去)
(1)推断: A是_____________; E是___________(写化学式)
(2)反应①常用于___________________; 由H和石灰加水可配制农业上常用的杀虫剂波尔
多液, 波尔多液不能用铁制容器盛放的原因是
_________________________________________
(3) 化学变化常伴随颜色改变. 上述由物质y → E → H(溶液)的过程中, 颜色变化为
______色→______色→_______色;
(4)写化学方程式: ④_____________________________________
⑥_____________________________________
(5)反应④结束后, 从混合物中分离出F的方法是__________. 鉴别D溶液和G溶液的方法
是_____________________________
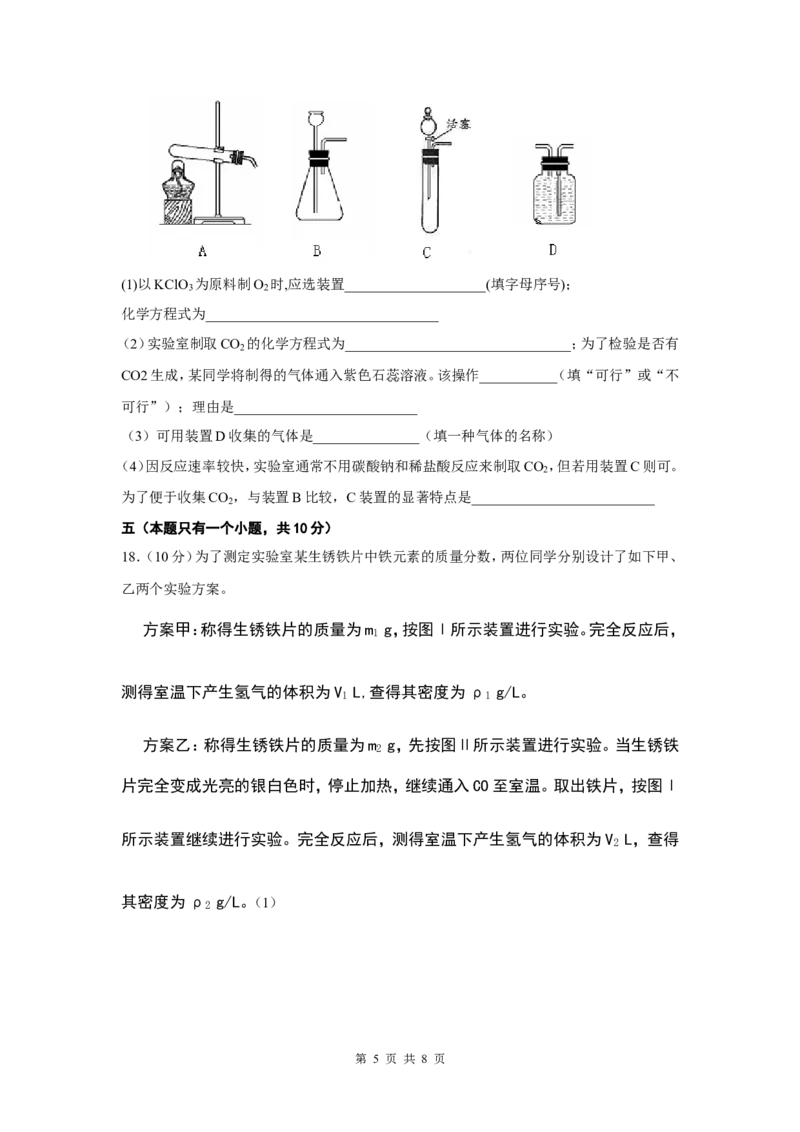
17.(9分)某化学实验小组拟用以下装置进行气体制备的研究.
第 4 页 共 8 页(1)以KClO 为原料制O 时,应选装置____________________(填字母序号);
3 2
化学方程式为_________________________________
(2)实验室制取CO 的化学方程式为________________________________;为了检验是否有
2
CO2生成,某同学将制得的气体通入紫色石蕊溶液。该操作___________(填“可行”或“不
可行”);理由是__________________________
(3)可用装置D收集的气体是_______________(填一种气体的名称)
(4)因反应速率较快,实验室通常不用碳酸钠和稀盐酸反应来制取CO ,但若用装置C则可。
2
为了便于收集CO ,与装置B比较,C装置的显著特点是__________________________
2
五(本题只有一个小题,共10分)
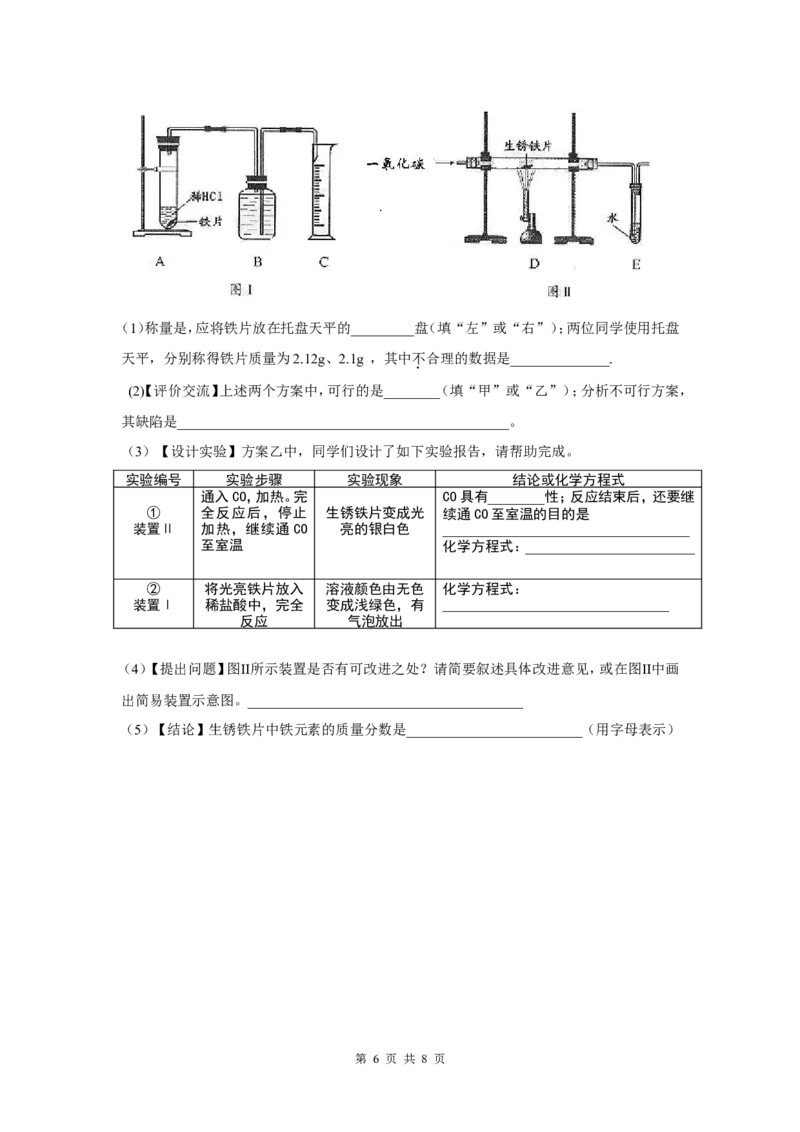
18.(10分)为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、
乙两个实验方案。
方案甲:称得生锈铁片的质量为m g,按图Ⅰ所示装置进行实验。完全反应后,
1
测得室温下产生氢气的体积为V L,查得其密度为ρ g/L。
1 1
方案乙:称得生锈铁片的质量为m g,先按图Ⅱ所示装置进行实验。当生锈铁
2
片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图Ⅰ
所示装置继续进行实验。完全反应后,测得室温下产生氢气的体积为V L,查得
2
其密度为ρ
2
g/L。(1)
第 5 页 共 8 页(1)称量是,应将铁片放在托盘天平的_________盘(填“左”或“右”);两位同学使用托盘
天平,分别称得铁片质量为2.12g、2.1g ,其中不合理的数据是______________.
(2【) 评价交流】上述两个方案中,可行的是________(填“甲”或“乙”);分析不可行方案,
其缺陷是_______________________________________________。
(3)【设计实验】方案乙中,同学们设计了如下实验报告,请帮助完成。
实验编号 实验步骤 实验现象 结论或化学方程式
通入CO,加热。完 CO具有________性;反应结束后,还要继
① 全反应后,停止 生锈铁片变成光 续通CO至室温的目的是
装置Ⅱ 加热,继续通CO 亮的银白色 ___________________________________
至室温 化学方程式:________________________
② 将光亮铁片放入 溶液颜色由无色 化学方程式:
装置Ⅰ 稀盐酸中,完全 变成浅绿色,有 ________________________________
反应 气泡放出
(4)【提出问题】图II所示装置是否有可改进之处?请简要叙述具体改进意见,或在图II中画
出简易装置示意图。_______________________________________
(5)【结论】生锈铁片中铁元素的质量分数是_________________________(用字母表示)
第 6 页 共 8 页第 7 页 共 8 页第 8 页 共 8 页