文档内容
2011 年四川省绵阳市中考化学试卷
一、选择题(共9小题,每小题3分,满分27分)
1.(3分)生活中的下列做法利用了化学反应原理的是( )
A.自制简易净水器净化自来水
B.门锁不易打开时灌入铅笔芯粉末
C.用天然气作燃料煮饭
D.用活性炭除去冰箱中的异味
2.(3分)阳刚同学按教材中的家庭小实验自制汽水,可是家里没有冰箱,为了使自制的汽
水变得冰凉可口,他想到可以从集镇上购买一种商品来产生制冷效果,他应该买的是
( )
A.硝酸铵 B.小苏打 C.生石灰 D.食盐
3.(3分)瘦肉精是一类对人体健康危害极大的化学物质,政府已严禁在猪饲料中添加瘦肉
精。常见的瘦肉精化学式为C H OCl N ,下列有关这种瘦肉精的说法中正确的是( )
12 18 2 2
A.是一种无机化合物
B.分子中碳、氢、氧三种元素的质量比为72:9:8
C.相对分子质量为277g
D.由C H O、Cl 、N 三种分子组成
12 18 2 2
4.(3分)人们常在可燃物建筑材料中添加阻燃剂以防止火灾,Mg(OH) 是一种常见的
2
阻燃剂,它在380℃时分解成水蒸气和耐高温的MgO,并吸收大量的热。下列说法错误
的是( )
A.Mg(OH) 分解吸热能降低可燃物的着火点
2
B.Mg(OH) 分解吸热能降低可燃物的温度
2
C.Mg(OH) 分解的产物能使可燃物与氧气隔绝
2
D.MgCO 比CaCO 易分解,也可作阻燃剂
3 3
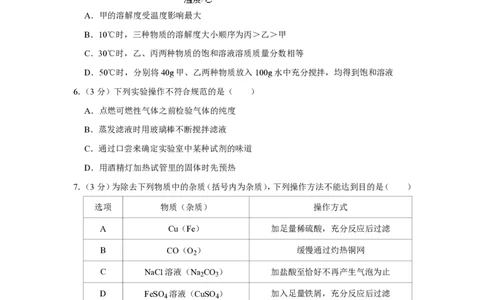
5.(3分)如图是甲、乙、丙三种物质的溶解度曲线,下面说法不正确的是( )
第 1 页 / 共 5 页A.甲的溶解度受温度影响最大
B.10℃时,三种物质的溶解度大小顺序为丙>乙>甲
C.30℃时,乙、丙两种物质的饱和溶液溶质质量分数相等
D.50℃时,分别将40g甲、乙两种物质放入100g水中充分搅拌,均得到饱和溶液
6.(3分)下列实验操作不符合规范的是( )
A.点燃可燃性气体之前检验气体的纯度
B.蒸发滤液时用玻璃棒不断搅拌滤液
C.通过口尝来确定实验室中某种试剂的味道
D.用酒精灯加热试管里的固体时先预热
7.(3分)为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )
选项 物质(杂质) 操作方式
A Cu(Fe) 加足量稀硫酸,充分反应后过滤
B CO(O ) 缓慢通过灼热铜网
2
C NaCl溶液(Na CO ) 加盐酸至恰好不再产生气泡为止
2 3
D FeSO 溶液(CuSO ) 加入足量铁屑,充分反应后过滤
4 4
A.A B.B C.C D.D
8.(3分)镍氢充电电池有着广泛应用,镍(Ni)及其化合物能发生下列反应:
①Ni+2HCl=NiCl +H ↑ ②NiO+2HCl=NiCl +H O ③NiO +4HCl=NiCl +Cl ↑
2 2 2 2 2 2 2
+2H O
2
对上述反应的分析判断错误的是( )
A.镍能与氯化铜溶液发生置换反应
B.NiCl 能与NaOH溶液发生复分解反应
2
第 2 页 / 共 5 页C.反应②和③都是复分解反应
D.反应中①、③中Ni的化合价都发生了变化
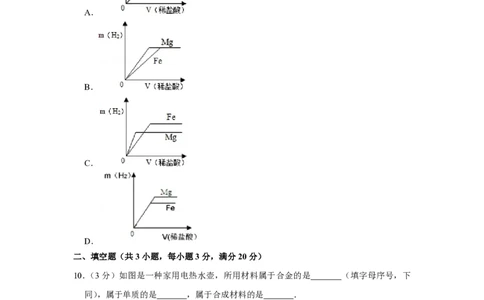
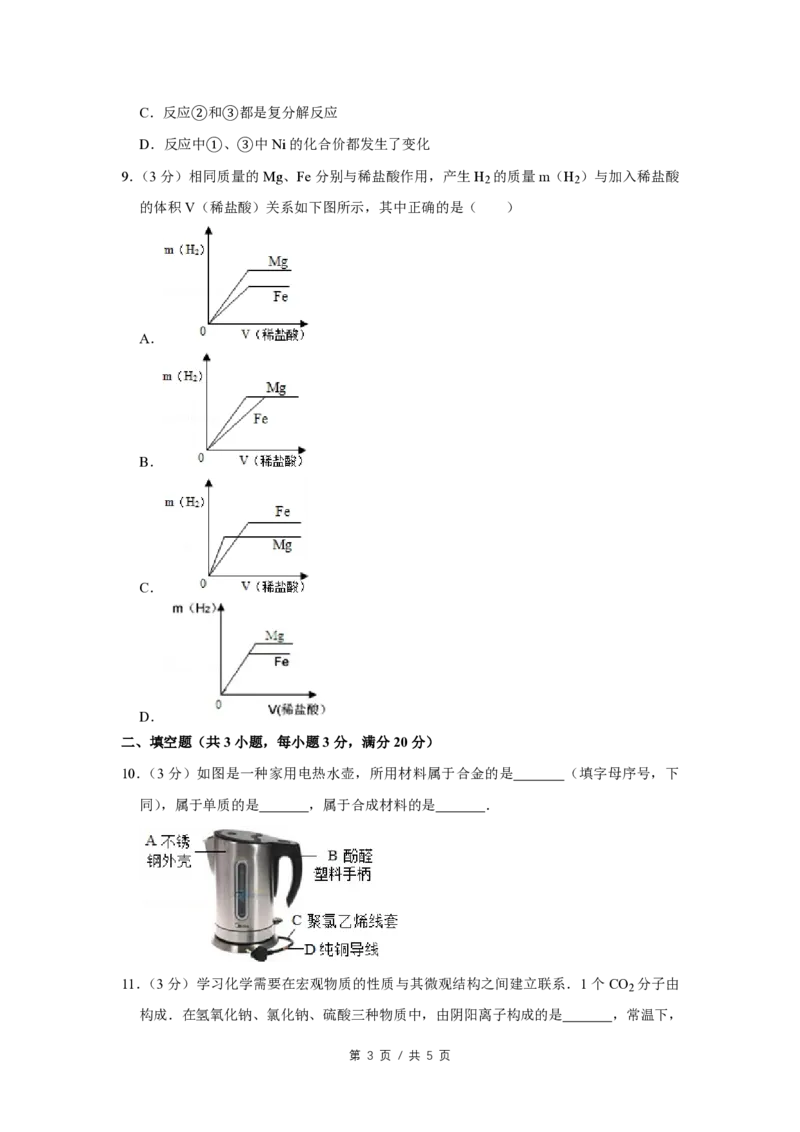
9.(3分)相同质量的Mg、Fe分别与稀盐酸作用,产生H 的质量m(H )与加入稀盐酸
2 2
的体积V(稀盐酸)关系如下图所示,其中正确的是( )
A.
B.
C.
D.
二、填空题(共3小题,每小题3分,满分20分)
10.(3分)如图是一种家用电热水壶,所用材料属于合金的是 (填字母序号,下
同),属于单质的是 ,属于合成材料的是 .
11.(3分)学习化学需要在宏观物质的性质与其微观结构之间建立联系.1个CO 分子由
2
构成.在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是 ,常温下,
第 3 页 / 共 5 页这三种物质的水溶液中pH<7的是 .
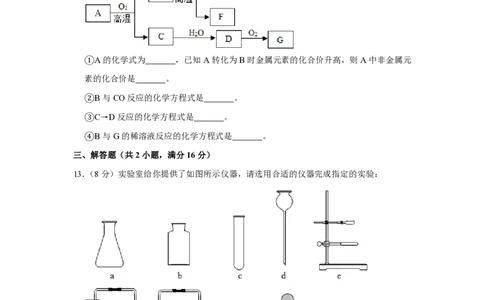
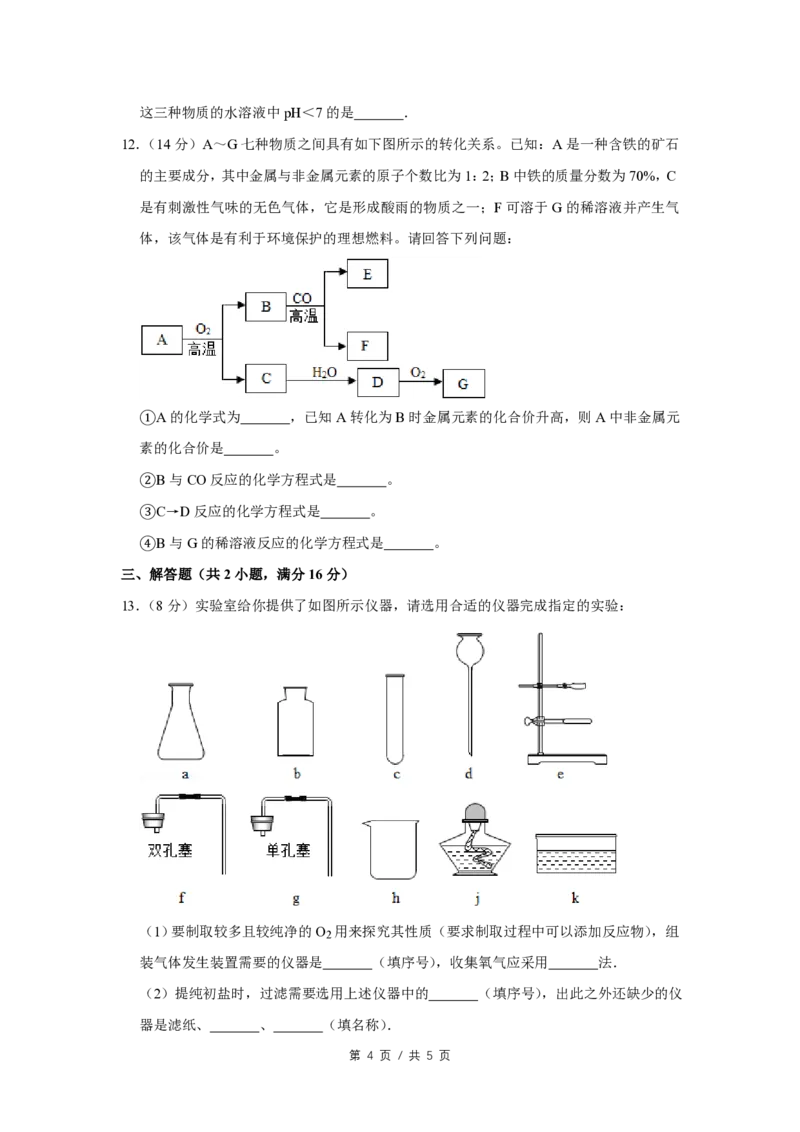
12.(14分)A~G七种物质之间具有如下图所示的转化关系。已知:A是一种含铁的矿石
的主要成分,其中金属与非金属元素的原子个数比为1:2;B中铁的质量分数为70%,C
是有刺激性气味的无色气体,它是形成酸雨的物质之一;F可溶于G的稀溶液并产生气
体,该气体是有利于环境保护的理想燃料。请回答下列问题:
①A的化学式为 ,已知A转化为B时金属元素的化合价升高,则A中非金属元
素的化合价是 。
②B与CO反应的化学方程式是 。
③C→D反应的化学方程式是 。
④B与G的稀溶液反应的化学方程式是 。
三、解答题(共2小题,满分16分)
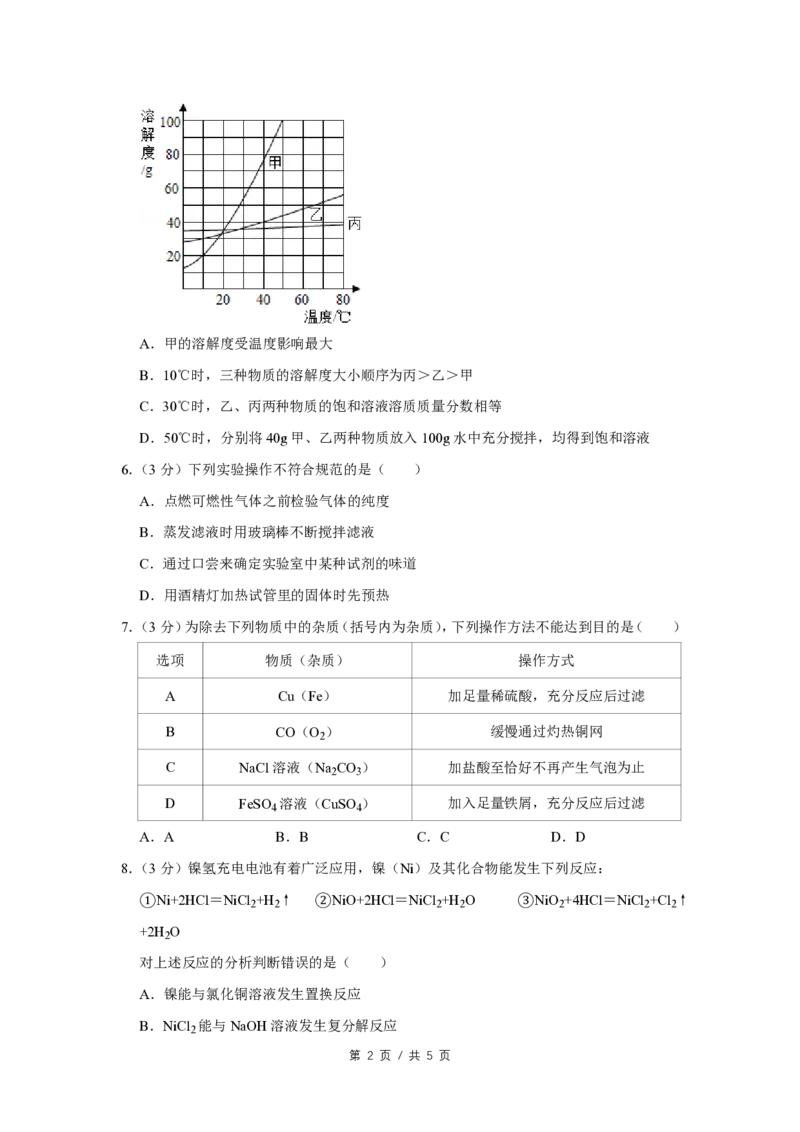
13.(8分)实验室给你提供了如图所示仪器,请选用合适的仪器完成指定的实验:
(1)要制取较多且较纯净的O 用来探究其性质(要求制取过程中可以添加反应物),组
2
装气体发生装置需要的仪器是 (填序号),收集氧气应采用 法.
(2)提纯初盐时,过滤需要选用上述仪器中的 (填序号),出此之外还缺少的仪
器是滤纸、 、 (填名称).
第 4 页 / 共 5 页14.(8分)美羊羊同学在购买回的袋装薯片中发现还有一个小袋,上面标有“成分:CaO、
Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末
有少许是棕红色,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe O ,灰白色粉
2 3
末应该含有CaCO 和Fe,为验证自己的判断,美羊羊同学打算进行实验探究,请你一同
3
参与。
【实验目的】证实灰白色粉末中含有CaCO 和Fe。
3
【实验设计】装置如图所示:
【实验预测与分析】
①若要证实样品中含有CaCO ,观察到的实验现象是 ,B中发生反应的化学方程
3
式为 。
②若要证实样品中含有Fe,E中应该观察到的现象是 ,此时C装置的作用是 。
③看了美羊羊同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请
你写出其中一种物质的化学式 。
四、解答题(共1小题,满分7分)
15.(7分)我市有丰富的石灰石资源,为了测定某地石灰石中碳酸钙的质量分数,取7.5g
样品放入烧杯,加入稀盐酸至恰好不再产生气体时消耗34.7g,放出的气体在常温下体积
为1.1L。
(1)常温下CO 气体的密度为2.0g/L,则上述反应放出气体的质量为 g。
2
(2)若石灰石中的杂质均不溶于水且不与盐酸反应,计算石灰石中CaCO 的质量分数
3
和反应所得溶液中溶质的质量分数(计算最终结果保留1位小数)。
第 5 页 / 共 5 页