文档内容
德州市二○一一年初中学业考试
化 学 试 题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32 Ca-40 Cl-35.5
Fe-56 Zn-65
第I卷(选择题 共 16 分)
一、选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
1.下列叙述中没有化学变化的是
A.小煤窑发生瓦斯(主要成分为甲烷)爆炸 B.涂在墙上的熟石灰逐渐变硬
C.煤燃烧生成的二氧化硫遇水形成酸雨 D.舞台上用干冰制造“云雾”
2.下列实验仪器可直接在火焰上加热的是
溶解度
/g
A B C D
3.化学知识与日常生活关系密切。下列说法错误的是
A.因为煤在燃烧时可能产生一氧化碳,所以冬天用煤取暖时要注意室内通风
B.因为常温下碳的化学性质不活泼,所以用墨书写的文字可以长时间保存
C.因为甲醛具有防腐作用,所以可以用甲醛水溶液浸泡水产品
D.因为儿童缺少钙元素时会得佝偻病,所以应通过进食奶类、豆类加以补充
4.今年年初以来,双汇“瘦肉精”事件引起了社会的广泛关注。人在大量食用喂食“瘦肉精”的猪肉后
会出现手脚发麻、心率加快、呕吐等症状。有一种“瘦肉精”学名叫盐酸克伦特罗,化学式是
C H ClNO。下列对于“瘦肉精”的认识不正确的是
12 18 2 2
A.该物质是由碳、氢、氯、氮和氧五种元素组成的
B.每个盐酸克伦特罗分子中含有18个氢原子
C.盐酸克伦特罗分子中碳、氢两种元素的质量比为12∶18
D.盐酸克伦特罗的相对分子质量为277
5.右图为固体物质X、Y的溶解度曲线。在温度为t℃时分别 把质量为 a g
2
的X、Y放入100 g水中,下表为对溶液状态的判断以及使不饱 和溶液达到饱
和采取的措施。其中正确的是
状态 措施
A X为饱和溶液,Y为不饱和溶液 给Y溶液加热蒸发适量的水
B X为不饱和溶液,Y为饱和溶液 向X溶液加入固体X至有晶体残留
C X、Y都是饱和溶液。
D X、Y都是不饱和溶液。 把X溶液温度降低至t℃,给Y溶液加热蒸发适量的水
16.下列做法正确的是
A.某同学用玻璃棒蘸取食用白醋滴在pH试纸上,测定其pH
B.服用适量的氢氧化钠治疗胃酸过多
C.生活污水不经任何处理.直接排放到河流中
D.为使农作物高产,鼓励农民大量施用化肥和农药
7.某学生为了验证锌、银、铜三种金属的活动性顺序,设计了五个实验:①将Zn、Cu分别放入稀盐酸
中; ②将Ag放入Cu(NO ) 溶液中;③将Cu放入AgNO 溶液中;④将Cu放入ZnSO 溶液中;⑤将Zn
3 2 3 4
放入AgNO 溶液中。下列实验组合不能验证锌、银、铜三种金属活动性顺序的是
3
A.①② B.①③ C.②④ D.①⑤
8.除去下列物质中的少量杂质,所选用的试剂及反应类型均正确的是
选项 物质(括号内为杂质) 试剂 反应类型
A HO(HO) 足量MnO 分解反应
2 2 2 2
B Ca(OH) (CaO) 适量稀盐酸 化合反应
2
C CO (CO) 足量CuO 置换反应
2
D CuO (Cu) 足量O 复分解反应
2
第II卷(非选择题 共 34 分)
注意事项:
1.答第II卷前,考生务必将自已的姓名、座号、准考证号填写在指定的位置,答第II卷时,用蓝、黑
色钢笔(或圆珠笔)直接答在试卷的相应位置。
2.考试结束后,监考人员将本试卷和答题卡一并收回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32 Ca-40 Cl-35.5
Fe-56 Zn-65
得 分 评卷人 二、理解与应用(本题包括5小题,共16分)
1.(4分)乙烯具有促进果实成熟的作用,还是合成纤维、橡胶、 塑 料 的
基本化工原料。乙烯无色,不溶于水,密度比空气小,化学式为 C H ,
2 4
容易燃烧生成二氧化碳和水,与空气混合形成的混合物遇明火有引起 燃 烧 爆
炸的危险。
(l)请根据所给乙烯的化学式,写出其表示意义(写出两点即 乙烯分子立体模型 可):
①
②
(2)写出乙烯燃烧的化学方程式 。(3)根据乙烯的化学性质,在生产、运输、贮存乙烯时应注意 。
2.(3分)阅读文字,在横线上写出相应的化学方程式:
安全火柴的火柴头上主要含有氯酸钾、二氧化锰、硫和玻璃粉等,火柴杆上涂有少量的石蜡,火柴
盒两边的摩擦层是由红磷和玻璃粉调和而成的。火柴着火的主要过程是:
(l)火柴头在火柴盒上划动时,产生的热量使红磷燃烧;
(2)红磷燃烧放出的热量使氯酸钾分解;
(3)氯酸钾分解放出的氧气与硫在点燃条件下反应;
(4)硫与氧气反应放出的热量引燃石蜡,最终使火柴杆着火。
3.(3分) 分类就是按照种类、等级或性质分别归类。依据不同的分类标准,结论也不尽相同。下列
每组中有一种物质具有特殊的组成或性质,而其他两种物质的组成或性质相似。请你利用所学知识将
其区分出来并说明理由。
化学式 被区分的物 理由
质(名称)
CO、CO、HO
2 2
Na、NaOH、NaCO
2 3
HCl、HSO 、HO
2 4 2
4.(4分) 已知:①向水中加入固体氯化钠,溶液的密度增大;②向水中加入乙醇,溶液的密度减小;
③向盐酸中加入碳酸钙,溶液的密度增大。
如下图所示,将鸡蛋放在三种液体中进行实验,最终鸡蛋下沉的是 。(填序号)
导致C中鸡蛋没入溶液的体积发生变化的 原
因是
① ;
② 。
推测:一艘满载货物的轮船由内陆河进入 海
洋时,没入水中的体积将 (填增大 或
减小) 。
5.(2分)用质量相等的锌粉和铁粉,分别与溶质质量分数相同且等质量的稀盐酸充分发生反应,产生
氢气的质量与时间的关系如右图所示。
请回答下列问题:
①表示锌粉与稀盐酸反应的曲线为 (填a或b)
②对于a曲线表示的反应,物质 (填名称) 有剩余。
得 分 评卷人三、实验与探究(本题包括2个小题,共12分)
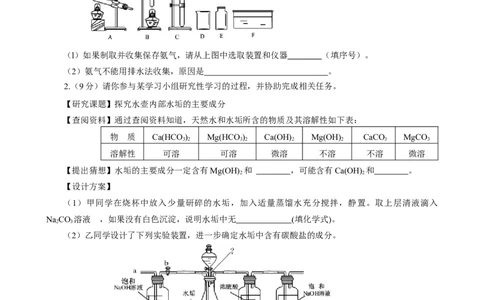
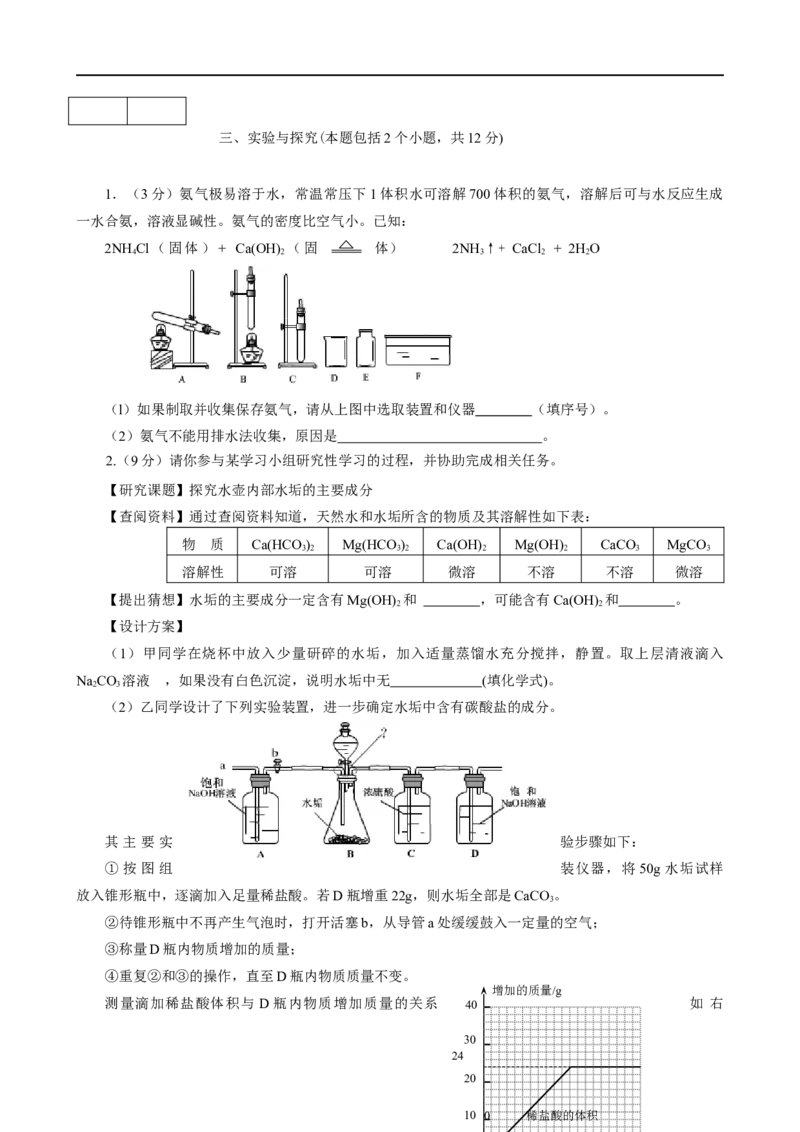
1.(3分)氨气极易溶于水,常温常压下1体积水可溶解700体积的氨气,溶解后可与水反应生成
一水合氨,溶液显碱性。氨气的密度比空气小。已知:
2NH Cl(固体)+ Ca(OH) (固 体) 2NH ↑+ CaCl + 2HO
4 2 3 2 2
(l)如果制取并收集保存氨气,请从上图中选取装置和仪器 (填序号)。
(2)氨气不能用排水法收集,原因是 。
2.(9分)请你参与某学习小组研究性学习的过程,并协助完成相关任务。
【研究课题】探究水壶内部水垢的主要成分
【查阅资料】通过查阅资料知道,天然水和水垢所含的物质及其溶解性如下表:
物 质 Ca(HCO ) Mg(HCO ) Ca(OH) Mg(OH) CaCO MgCO
3 2 3 2 2 2 3 3
溶解性 可溶 可溶 微溶 不溶 不溶 微溶
【提出猜想】水垢的主要成分一定含有Mg(OH) 和 ,可能含有Ca(OH) 和 。
2 2
【设计方案】
(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置。取上层清液滴入
NaCO 溶液 ,如果没有白色沉淀,说明水垢中无 (填化学式)。
2 3
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分。
其主要实 验步骤如下:
①按 图组 装仪器,将 50g水垢试样
放入锥形瓶中,逐滴加入足量稀盐酸。若D瓶增重22g,则水垢全部是CaCO 。
3
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质增加的质量;
④重复②和③的操作,直至D瓶内物质质量不变。
增加的质量/g
测量滴加稀盐酸体积与 D瓶内物质增加质量的关系 40 如 右
30
24
20
10 0 稀盐酸的体积图曲线所示;
【评价】
(1)A瓶中的NaOH溶液起到 作用。若A瓶中无NaOH溶液,D瓶中的质量将
(填“增大”、“不变”或“减小”)。
(2)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两金属的化合价相同、两种盐
的质量相同,则相对分子质量小者放出的气体多。分析曲线图可知:水垢中一定含有
(化学式),理由是 。
(3)装置图中“?”所指处有三根导管同时穿过橡胶塞,已知:导管的直径为 8mm,橡胶塞细段直
径为3cm。从坚固和美观的角度考虑,请你在由图中标出应在哪三点打孔 为好(用圆
圈“○”表示打孔位置)。
以上实验 (填“能够”或“不能”)检测出水垢中含有 Mg(OH) 。
2
得 分 评卷人 四、计算题(本题包括2小题,共6分)
1.(2分)对于化学反应:2A = 2B +C,已知:反应生成B和C的质量比为B∶C = 1∶8。请填空:
物质 A B C
反应前质量/g 100 0 5
反应后质量/g 64
2.(4分)小明同学想测量某赤铁矿样品中氧化铁的纯度(假设其他成分不和酸反应,也不溶于水),进行
如下实验:
称取10g赤铁矿样品,加入到烧杯中,再加入92.5g的稀硫酸,恰好完全反应。过滤得滤渣2.5g。试
计算:
(1)赤铁矿样品中氧化铁的质量分数?
(2)上述反应所得滤液中溶质的质量分数?
德州市二○一一年初中学业考试
化学试题(A 卷)参考答案及评分标准
第Ⅰ卷(选择题 共 16 分)
注:考生给出的答案,只要合理可参照评分标准酌情给分。
一、选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8
答案 D B C C B A D A第Ⅱ卷 (非选择题 共 34 分)
二、理解与应用(本题包括5小题,共16分)
1.(4分)(1)①表示乙烯这种物质;②表示乙烯是由碳、氢两种元素组成的;③表示一个乙烯分
子;④表示乙烯分子是由碳、氢两种原子构成的;⑤表示一个乙烯分子是由2个碳原子和4个氢原子构成
的(1方面意义1分,共2分。以上5方面意义任意答出2方面即可得满分)
(2)C H + 3O 点燃 2CO + 2HO(3)严禁烟火
2 4 2 2 2
点燃
2.(3分)(1)4P+ 5O 2PO
2 2 5
(2)2KClO 2KCl + 3O↑
3 2
点燃
(3)S+ O SO
2 2
3.(3分)
被区分的物质(名
化学式 理由
称)
CO、CO、HO 水 不含碳元素(或含有氢元素)
2 2
Na、NaOH、NaCO 钠 单质
2 3
HCl、HSO 、HO 水 氧化物
2 4 2
物质名称和理由都写对得1分,有一方面错误不得分。
4.(4分)B; ①鸡蛋质量减少;②溶液的密度增大; 减小
5.(2分)① a ②盐酸
三、实验与探究(本题包括2小题,共12分)
1.(共3分)(1)A 、E (2分) (2)氨气极易溶于水(1分)
2.(每空1分,共9分)
【提出猜想】CaCO MgCO
3 3
【设计方案】⑴ Ca(OH)
2
【评价】⑴吸收CO 增大 (2)MgCO 实际生成CO 的质量是24g,大于22g
2 3 2
(3 )(三个孔不在一条直线上即可得分,等边三角形最好)
不能
四、计算题(本题包括2小题,共6分)
1.(2分)4 37
2.(4分),
解:(1)赤铁矿样品中氧化铁的质量分数 为:×100% = 75% ………1分
(2)设反应所得滤液中硫酸铁的质量为x
Fe O + 3H SO Fe (SO ) + 3H O ……………………… 1分
2 3 2 4 2 4 3 2
160 4007.5g x
160:400=7.5g: x x= 18.75g ………………………… 1分
18.75g
10g+92.5g−2.5g
反应所得滤液中溶质的质量分数为: ×100%=18.75% ……1分
答:(略)