文档内容
2013 年河南省初中学业水平暨高级中等学校招生考试试卷
化 学
注意事项:
1.本试卷共4页,满分50分,考试时间50分钟。请用钢笔或圆珠笔直接答在试卷上。
2.答卷前将密封线内的项目填写清楚。
题 号 一 二 三 四 总 分
分 数
相对原子质量 H—1 Li-7 C—12 O—16 Al—27 Na—23 Cl—35.5 Fe—56
一、选择题 (本题包括10个小题,每小题1分,共10分)
下列各题,每题只有一个选项符合题意,请将正确选项的标号填入题后括号内。
1.能源与生活息息相关。下列利用化学反应获得电能的是 【 】
A.风力发电 B.水力发电 C.火力发电 D.太阳能发电
2.下列图标中,属于我国制定的塑料包装制品回收标志的是 【 】
A B C D
3.下列各项中,不属于我国《环境空气质量标准》基本监控项目的是 【 】
A.二氧化硫浓度 B.氮气浓度 C.二氧化氮浓度 D.PM2.5浓度
4.2013年5月在郑州举办的第八届中国中部投资贸易博览会上,河南大枣等果蔬类产
品颇受青睐。下列人体需要的营养素主要由水果、蔬菜提供的是 【 】
A.维生素 B.油脂 C.淀粉 D.蛋白质
5.下列结构示意图表示的粒子中,属于离子的是 【 】
A B C D
6.分类法是化学学习的重要方法。下列说法正确的是 【 】
A.醋酸和干冰都属于有机物 B.不锈钢和金刚石都属于合金
C.尿素和硝酸钾都属于复合肥料 D.锌和碘都属于人体必需的微量元素
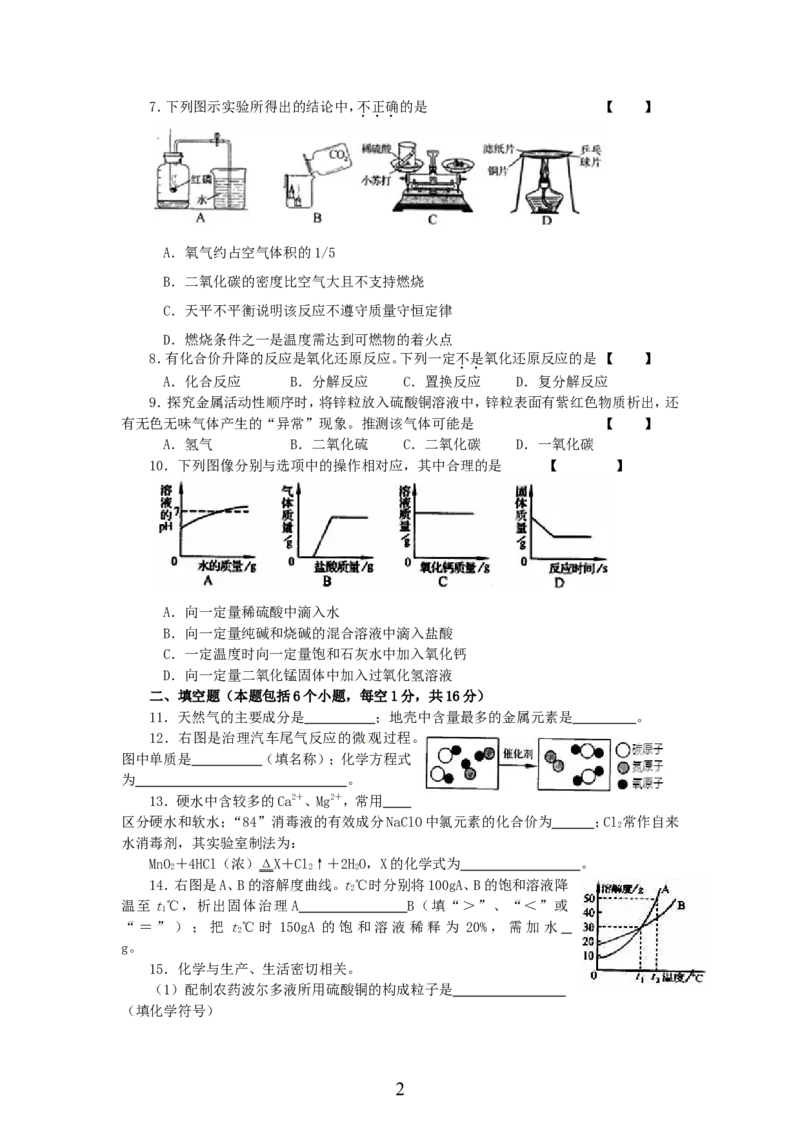
17.下列图示实验所得出的结论中,不正确的是 【 】
A.氧气约占空气体积的1/5
B.二氧化碳的密度比空气大且不支持燃烧
C.天平不平衡说明该反应不遵守质量守恒定律
D.燃烧条件之一是温度需达到可燃物的着火点
8.有化合价升降的反应是氧化还原反应。下列一定不是氧化还原反应的是 【 】
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
9.探究金属活动性顺序时,将锌粒放入硫酸铜溶液中,锌粒表面有紫红色物质析出,还
有无色无味气体产生的“异常”现象。推测该气体可能是 【 】
A.氢气 B.二氧化硫 C.二氧化碳 D.一氧化碳
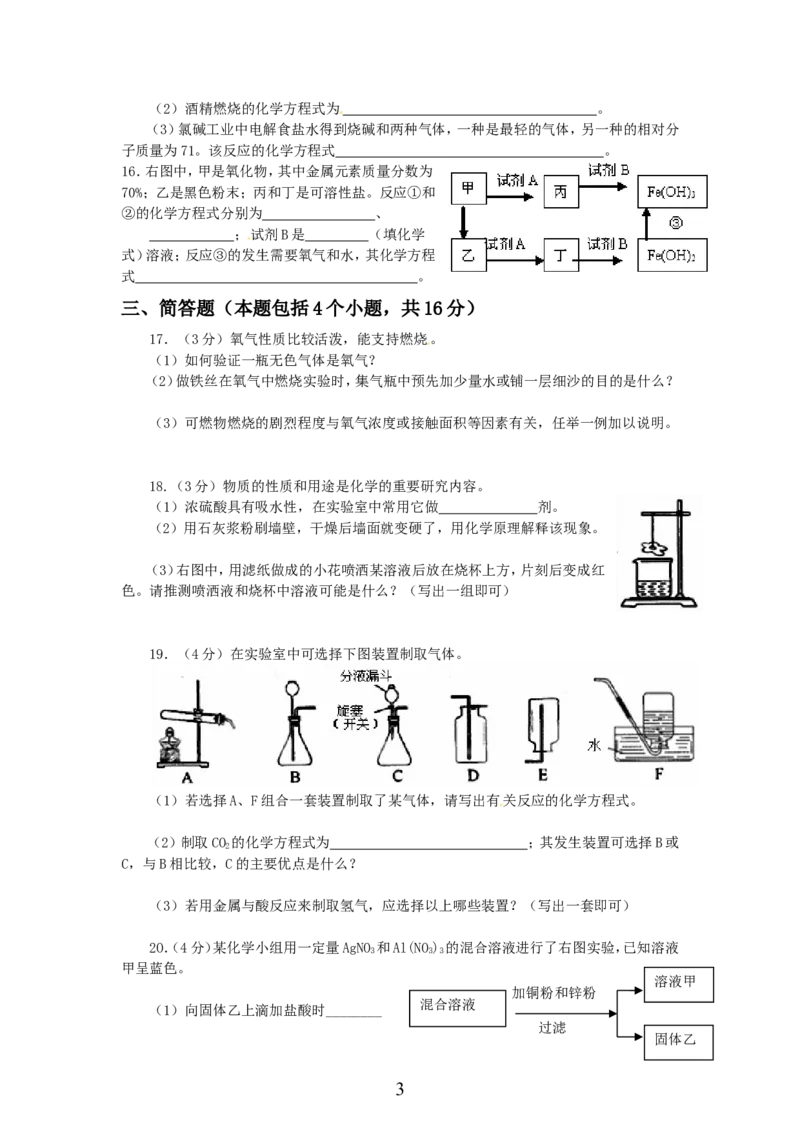
10.下列图像分别与选项中的操作相对应,其中合理的是 【 】
A.向一定量稀硫酸中滴入水
B.向一定量纯碱和烧碱的混合溶液中滴入盐酸
C.一定温度时向一定量饱和石灰水中加入氧化钙
D.向一定量二氧化锰固体中加入过氧化氢溶液
二、填空题(本题包括6个小题,每空1分,共16分)
11.天然气的主要成分是 ;地壳中含量最多的金属元素是 。
12.右图是治理汽车尾气反应的微观过程。
图中单质是 (填名称);化学方程式
为 。
13.硬水中含较多的Ca2+、Mg2+,常用
区分硬水和软水;“84”消毒液的有效成分NaClO中氯元素的化合价为 ;Cl 常作自来
2
水消毒剂,其实验室制法为:
MnO+4HCl(浓)ΔX+Cl↑+2HO,X的化学式为 。
2 2 2
14.右图是A、B的溶解度曲线。t℃时分别将100gA、B的饱和溶液降
2
温至t℃,析出固体治理 A B(填“>”、“<”或
1
“=”);把 t℃时 150gA 的饱和溶液稀释为 20%,需加水
2
g。
15.化学与生产、生活密切相关。
(1)配制农药波尔多液所用硫酸铜的构成粒子是
(填化学符号)
2(2)酒精燃烧的化学方程式为 。
(3)氯碱工业中电解食盐水得到烧碱和两种气体,一种是最轻的气体,另一种的相对分
子质量为71。该反应的化学方程式 。
16.右图中,甲是氧化物,其中金属元素质量分数为
70%;乙是黑色粉末;丙和丁是可溶性盐。反应①和
②的化学方程式分别为 、
;试剂B是 (填化学
式)溶液;反应③的发生需要氧气和水,其化学方程
式 。
三、简答题(本题包括4个小题,共16分)
17.(3分)氧气性质比较活泼,能支持燃烧。
(1)如何验证一瓶无色气体是氧气?
(2)做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是什么?
(3)可燃物燃烧的剧烈程度与氧气浓度或接触面积等因素有关,任举一例加以说明。
18.(3分)物质的性质和用途是化学的重要研究内容。
(1)浓硫酸具有吸水性,在实验室中常用它做 剂。
(2)用石灰浆粉刷墙壁,干燥后墙面就变硬了,用化学原理解释该现象。
(3)右图中,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红
色。请推测喷洒液和烧杯中溶液可能是什么?(写出一组即可)
19.(4分)在实验室中可选择下图装置制取气体。
(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式。
(2)制取CO 的化学方程式为 ;其发生装置可选择B或
2
C,与B相比较,C的主要优点是什么?
(3)若用金属与酸反应来制取氢气,应选择以上哪些装置?(写出一套即可)
2O.(4分)某化学小组用一定量AgNO 和Al(NO) 的混合溶液进行了右图实验,已知溶液
3 3 3
甲呈蓝色。
溶液甲
加铜粉和锌粉
混合溶液
(1)向固体乙上滴加盐酸时________
过滤
固体乙
3(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?
(写化学式)_________________________
(3)请写出该实验过程中所发生反应的化学方程式。
__________________________________________________________________
四、综合应用题(共10分)
21.酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,
实验无明显现象。取反应后的部分溶液加热、蒸干、得到白色固体。
以下是探究白色固体成分的实验,已知CaCl 溶液呈中性。请填写下表:
2
实验操作 测定结果 白色固体成分
用pH试纸测定反应后溶液的酸碱度,操作 pH>7
方法是
CaCl
2
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点。
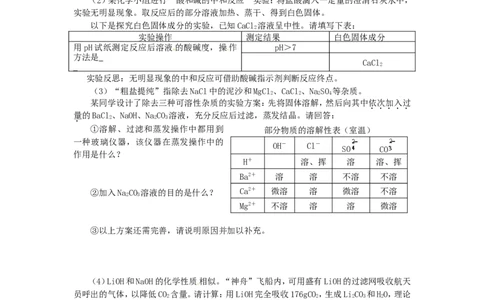
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl、CaCl、NaSO 等杂质。
2 2 2 4
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过
量的BaCl、NaOH、NaCO 溶液,充分反应后过滤,蒸发结晶。请回答:
2 2 3
①溶解、过滤和蒸发操作中都用到 部分物质的溶解性表(室温)
一种玻璃仪器,该仪器在蒸发操作中的
OH- Cl-
SO CO
作用是什么?
H+ 溶、挥 溶 溶、挥
Ba2+ 溶 溶 不溶 不溶
②加入NaCO 溶液的目的是什么? Ca2+ 微溶 溶 微溶 不溶
2 3
Mg2+ 不溶 溶 溶 微溶
③以上方案还需完善,请说明原因并加以补充。
(4)LiOH和NaOH的化学性质相似。“神舟”飞船内,可用盛有LiOH的过滤网吸收航天
员呼出的气体,以降低CO 含量。请计算:用LiOH完全吸收176gCO,生成LiCO 和HO,理论
2 2 2 3 2
上至少需要LiOH的质量是多少?
42013年河南省化学试题参考答案及评分标准
一、选择题(每小题1分,共10分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C B B A C D C D A B
二、填空题(每空1分,共16分)
催化剂
11.甲烷(或CH ) 铝(或A1) 12.氮气 2CO +2NO N +2CO
4 2 2
13.肥皂水 +1 MnCl 14. > 100
2
点燃
15. (l)Cu2+、SO 2— (2)C H OH +3O 2CO +3H O
4 2 5 2 2 2
通电
(3) 2NaCl +2H O 2NaOH +H ↑ + Cl ↑
2 2 2
高温 高温
16.Fe O +3CO 2Fe +3CO (或 2Fe O +3C 4Fe +3CO ↑
2 3 2 2 3 2
等)
Fe O +6HCl = 2FeCl +3H O[或 Fe O +3H SO = Fe (SO ) +3H O
2 3 3 2 2 3 2 4 2 4 3 2
等]
NaOH[或 Ca(OH) 等; 4Fe(OH) +O +2H O = 4Fe(OH)
2 2 2 2 3
三、简答题(共14分)
17.(1)将带火星的木条伸到集气瓶中,木条复燃即可验证。
(2)防止溅落的熔融物炸裂瓶底。
(3)与氧气浓度有关,如硫在氧气里燃烧比在空气里燃烧要剧烈。
(或与接触面积有关,如煤粉比煤块燃烧得更加剧烈。)
18.(3分)(1)干燥 (2)石灰浆中含有Ca(OH) ,干燥过程中与CO
2 2
反应,生成难溶于水的CaCO 。
3
(3)石蕊溶液和浓盐酸。(或酚酞溶液和浓氨水。)
519.(4 分)(1)2KMnO ∆ K MnO + MnO + O ↑
4 2 4 2 2
( 或 2KClO 2KC1 +3O ↑ )
3 2
(2)CaCO + 2HC1 = CaCl + CO ↑ + H O
3 2 2 2
可通过分液漏斗的开关控制液体的滴加速率和滴加量,来控制反应。
(3)发生装置选B(或C),收集装置选E(或F)。
20.(4分)(1)没有 (2)Al( NO ) 、Zn( NO ) 、Cu(NO )
3 3 3 2 3 2
(3)Cu + 2AgNO = Cu (NO ) + 2Ag
3 3 2
Zn +2AgNO = Zn(NO ) +2Ag[或 Zn + Cu(NO ) = Zn(NO ) +Cu]
3 3 2 3 2 3 2
四、综合应用题(共10分}
21.(1)水(或难电离物)(1分)(2)
实验操作 测定结果 白色固体成分
用玻璃棒蘸取溶液滴到pH试纸上,把试 CaCl 、Ca(OH) (1分)
2 2
纸显示的颜色与标准比色卡比较(1分) pH 7(1分)
(3)① 用玻璃棒不断搅拌,防止因局部温度过高造成液滴飞溅。(1
分)
②除去CaCl 杂质和过量的BaCl (1分)
2 2
③过量的NaOH和Na CO 未除去,还应加入适量的盐酸。(1分)
2 3
(4 )解:设理论上至少需要LiOH的质量为x。
2LiOH + CO =Li CO + H O (1 分)
2 2 3 2
48 44
x 176 g
(1分)
6x= = 192 g (1 分)
答:理论上至少需要LiOH的质量为192 g。
7