文档内容
2019 年柳州市初中学业水平考试与高中阶段学校招生考试试卷
化 学
(考试时间90分钟,满分100分)
可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 Mg~24 Al 27 S~32
Cl~35.5 Ca~40 Fe~56 Cu~64 Zn~65 Ba~137
第Ⅰ卷(选择题,共40分)
一、选择题(本大题共40分。每小题只有一个正确答案,每小题2分)
1.常用于登山、潜水、医疗急救的气体是( )
A. 氮气 B. 氧气 C. 二氧化碳 D. 稀有气体
2.下列化学实验基本操作中,正确的是( )
A. 熄灭酒精灯 B. 滴加液体
C. 读取液体体积 D. 闻气体气味
3.下列变化中,一定包含有化学变化的是( )
A. 蜡烛燃烧 B. 水结成冰 C. 汽油挥发 D. 木头做成桌椅
4.下列物质中不属于溶液的是( )
A. 食盐水 B. 糖水 C. 泥土水 D. 澄清石灰水
5.蛋白质是人体必需的重要营养成分之一。下列食物中,富含蛋白质的是 ( )
A. 豆腐 B. 馒头 C. 西红柿 D. 豆油
6.超市中有“高锌高钙”奶粉出售,其中“锌、钙”指的是( )
A. 单质 B. 元素 C. 分子 D. 原子
7.用化学的眼光看世界,能提高人的科学素养。下列对事实的解释错误的是
事 实 解 释
A 每年4月,柳州市紫荆花盛开,花香四溢 分子在不断地运动B 100mL水和100mL酒精混合后的体积小于200mL 分子之间有间隔
金刚石和石墨是由碳元素组成的不同单质,但是金刚石
C 原子的排列方式不同
坚硬,而石墨很软
D 温度计中的水银(汞)热胀冷缩 原子本身的大小发生了改变
A. A B. B C. C D. D
8.化学与人类健康密切相关。下列说法正确的是( )
A. 甜味剂能增加食品的甜度,可在食品中大量使用
B. 可用甲醛浸泡食用水产品
C. 人体摄入过多油脂,容易引发肥胖和心脑血管疾病
D. 霉变大米经淘洗后可供人食用
9.“百里柳江,百里画廊”,保护母亲河,我们在行动。以下符合保护柳江河的做法是( )
A. 在水源地大量网箱养鱼 B. 大量使用化肥、农药
C. 在河边填埋生活垃圾 D. 工业废水经净化处理达标后,方能排放
10.硝酸铵(NH NO )能使农作物枝繁叶茂。硝酸铵属于( )
4 3
A. 钾肥 B. 磷肥 C. 氮肥 D. 复合肥
11.下列物质属于氧化物的是( )
A. CO B. KOH C. AgNO D. HSO
2 3 2 4
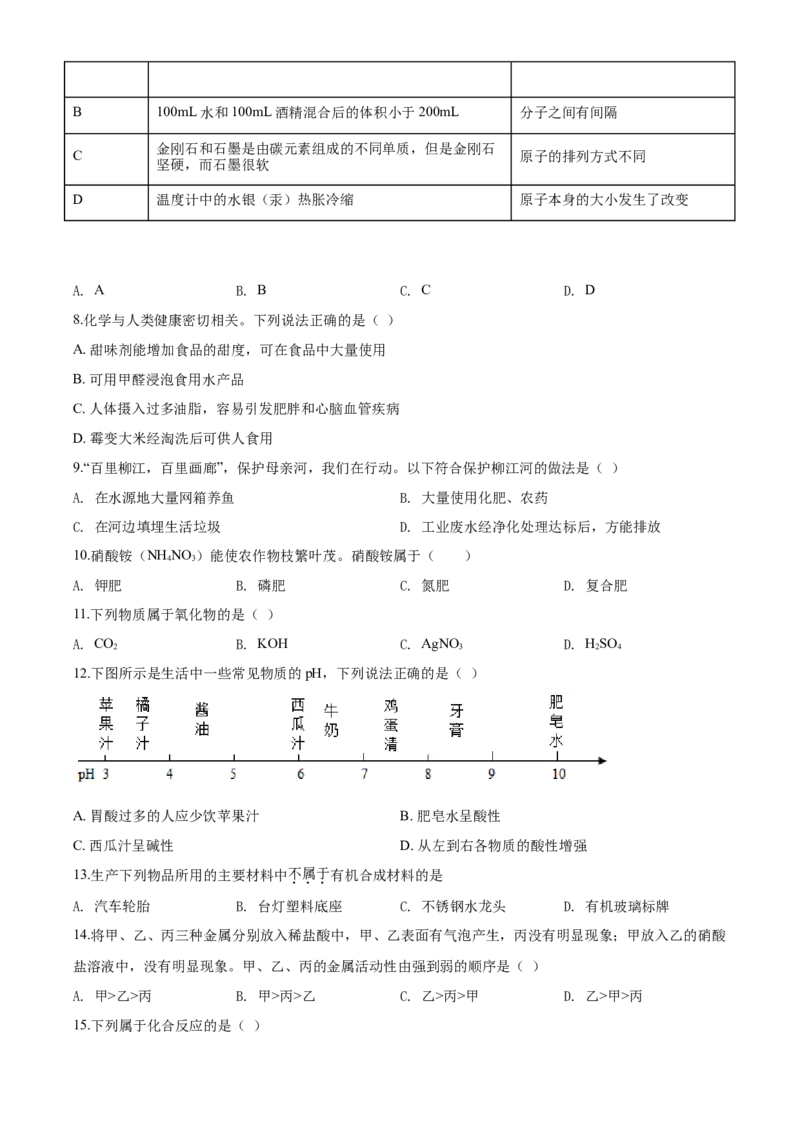
12.下图所示是生活中一些常见物质的pH,下列说法正确的是( )
A. 胃酸过多的人应少饮苹果汁 B. 肥皂水呈酸性
C. 西瓜汁呈碱性 D. 从左到右各物质的酸性增强
13.生产下列物品所用的主要材料中不属于有机合成材料的是
A. 汽车轮胎 B. 台灯塑料底座 C. 不锈钢水龙头 D. 有机玻璃标牌
14.将甲、乙、丙三种金属分别放入稀盐酸中,甲、乙表面有气泡产生,丙没有明显现象;甲放入乙的硝酸
盐溶液中,没有明显现象。甲、乙、丙的金属活动性由强到弱的顺序是( )
A. 甲>乙>丙 B. 甲>丙>乙 C. 乙>丙>甲 D. 乙>甲>丙
15.下列属于化合反应的是( )A. Fe+H SO =FeSO +H ↑ B. BaCl +Na CO =BaCO↓+2NaCl
2 4 4 2 2 2 3 3
C. NH +CO +H O = NH HCO D. CaCO CaO + CO ↑
3 2 2 4 3 3 2
16.下列做法不符合安全要求的是( )
A. 火灾中逃生,弯腰前行 B. 油锅着火时,用锅盖盖灭
C. 用煤火取暖,注意通风 D. 家用电器着火时,马上用水扑灭
17.下列各组离子在pH=13的溶液中能够大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
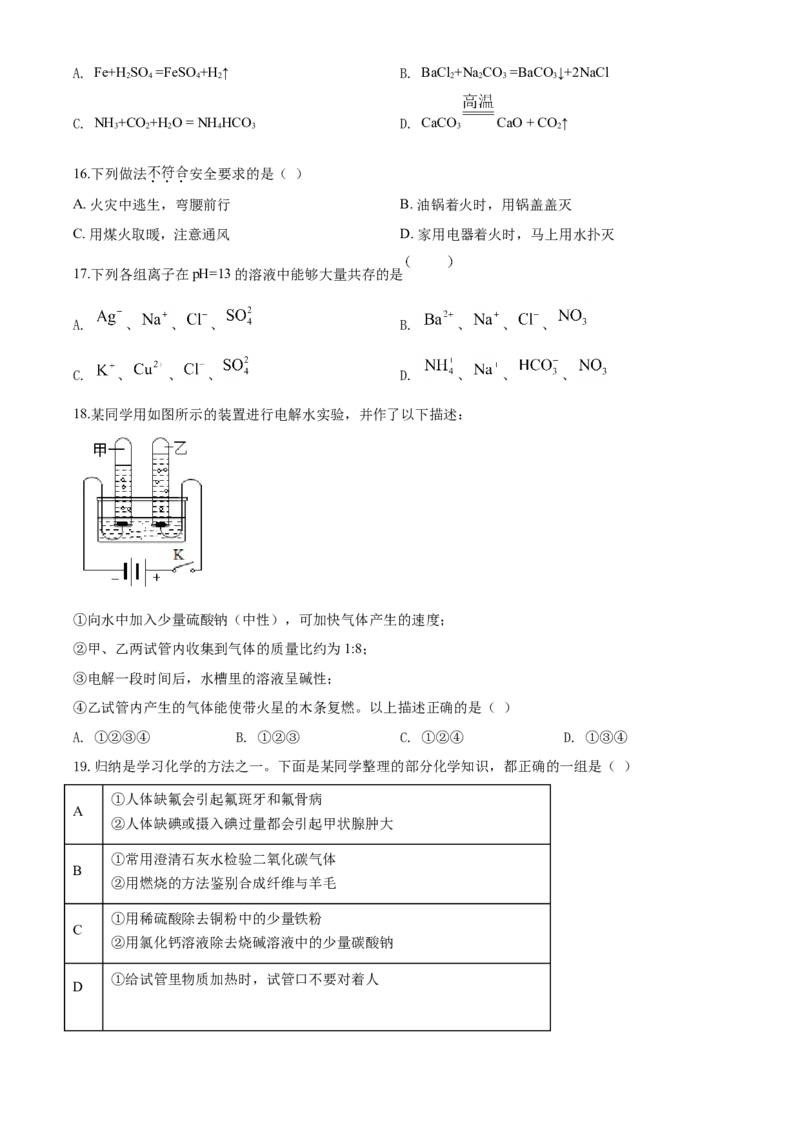
18.某同学用如图所示的装置进行电解水实验,并作了以下描述:
①向水中加入少量硫酸钠(中性),可加快气体产生的速度;
②甲、乙两试管内收集到气体的质量比约为1:8;
③电解一段时间后,水槽里的溶液呈碱性;
④乙试管内产生的气体能使带火星的木条复燃。以上描述正确的是( )
A. ①②③④ B. ①②③ C. ①②④ D. ①③④
19.归纳是学习化学的方法之一。下面是某同学整理的部分化学知识,都正确的一组是( )
①人体缺氟会引起氟斑牙和氟骨病
A
②人体缺碘或摄入碘过量都会引起甲状腺肿大
①常用澄清石灰水检验二氧化碳气体
B
②用燃烧的方法鉴别合成纤维与羊毛
①用稀硫酸除去铜粉中的少量铁粉
C
②用氯化钙溶液除去烧碱溶液中的少量碳酸钠
①给试管里物质加热时,试管口不要对着人
D②强碱不慎沾到皮肤时,应及时用大量水冲洗,然后涂上碳酸氢钠溶
液
A. A B. B C. C D. D
20.将一块铁铝合金(只含Fe、Al)和一块等质量的金属镁分别放入足量的盐酸溶液中,两者产生的氢气
质量相等,则合金中铁元素、铝元素的质量比为( )
A. 7 : 12 B. 28 : 9 C. 3 : 16 D. 56 : 27
第Ⅱ卷(非选择题,共60分)
二、填空题(本大题共26分,每空1分)
21.用化学符号或名称填空。
(1)氢原子____;
(2) ______;
(3)3个钾离子______;
(4)铁元素______;
(5)五氧化二磷__;
(6) _____________。
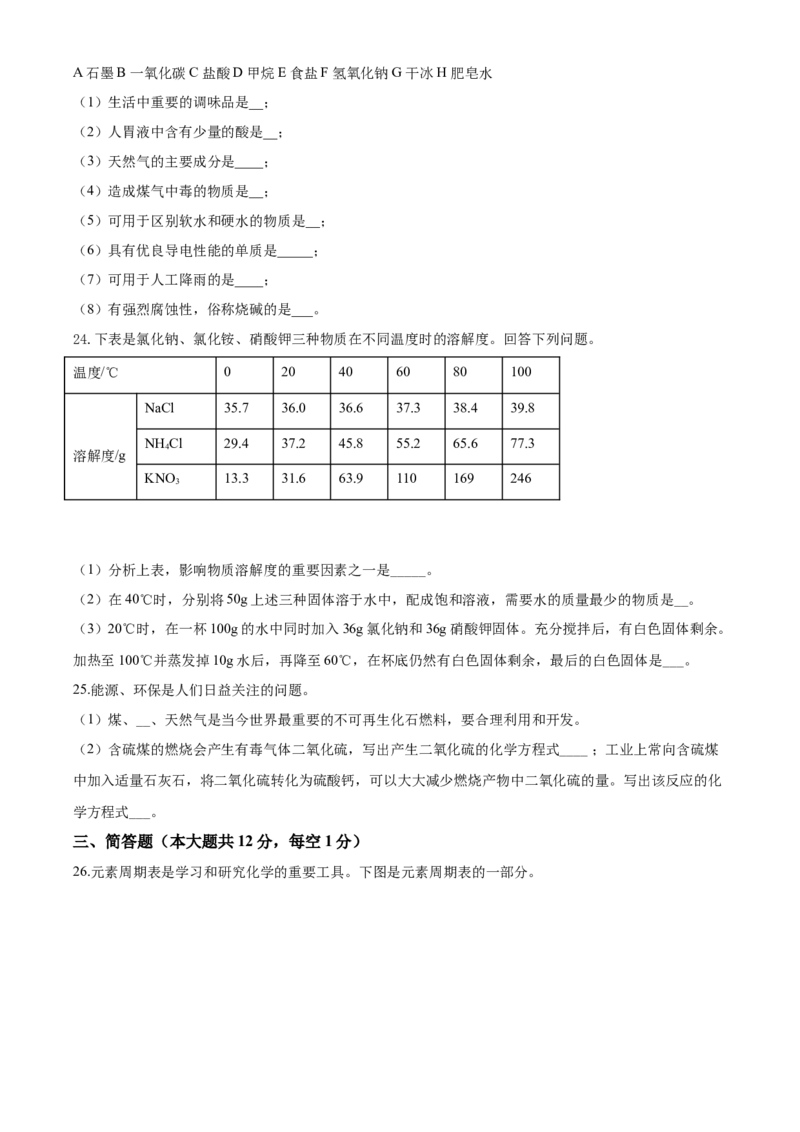
22.在下列图片和各自意义的表述中,找到对应关系,在答题卡上用字母填空。
____, ___, __,
__, ___, __
23.请在A—H八种物质中,选择符合题意的物质,用字母填空。A 石墨B 一氧化碳C 盐酸D 甲烷E 食盐F 氢氧化钠G 干冰 H 肥皂水
(1)生活中重要的调味品是__;
(2)人胃液中含有少量的酸是__;
(3)天然气的主要成分是____;
(4)造成煤气中毒的物质是__;
(5)可用于区别软水和硬水的物质是__;
(6)具有优良导电性能的单质是_____;
(7)可用于人工降雨的是____;
(8)有强烈腐蚀性,俗称烧碱的是___。
24.下表是氯化钠、氯化铵、硝酸钾三种物质在不同温度时的溶解度。回答下列问题。
温度/℃ 0 20 40 60 80 100
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
NH Cl 29.4 37.2 45.8 55.2 65.6 77.3
4
溶解度/g
KNO 13.3 31.6 63.9 110 169 246
3
(1)分析上表,影响物质溶解度的重要因素之一是_____。
(2)在40℃时,分别将50g上述三种固体溶于水中,配成饱和溶液,需要水的质量最少的物质是__。
(3)20℃时,在一杯100g的水中同时加入36g氯化钠和36g硝酸钾固体。充分搅拌后,有白色固体剩余。
加热至100℃并蒸发掉10g水后,再降至60℃,在杯底仍然有白色固体剩余,最后的白色固体是___。
25.能源、环保是人们日益关注的问题。
(1)煤、__、天然气是当今世界最重要的不可再生化石燃料,要合理利用和开发。
(2)含硫煤的燃烧会产生有毒气体二氧化硫,写出产生二氧化硫的化学方程式____ ;工业上常向含硫煤
中加入适量石灰石,将二氧化硫转化为硫酸钙,可以大大减少燃烧产物中二氧化硫的量。写出该反应的化
学方程式___。
三、简答题(本大题共12分,每空1分)
26.元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分。的
(1)同一周期 元素,从左到右,各元素的原子序数依次______,金属性逐渐减弱,非金属性逐渐增强,
则第三周期中氯元素的非金属性比硫元素的非金属性__(填“强”或“弱”)。
(2)同一纵行叫做族,原子序数为4和12的原子为同族元素的原因是_____;画出原子序数为20的阳离
子结构示意图________。
(3)氧原子的核电荷数是_____,氧元素可以和氟元素组成一种分子结构与水分子结构相似的化合物。写
出该化合物的化学式并标出氧元素的化合价_____。
27.硝酸是一种重要的化工原料,工业上常用“氨的催化氧化”制取硝酸,工艺流程图如下:
请回答下列问题:
(1)氨气是一种极易溶于水的气体,氨水溶液呈__(填“酸”、“碱”或“中”)性,氨气与盐酸反应的化学方
程式是______。
(2)完成NO 转化为硝酸的化学方程式:3NO +____=2HNO + NO。生成的NO是一种对空气有污染的气
2 2 3
体,工业上要将它回收,重复利用。上述流程中还有一种物质也可以重复利用,这种物质是____。
28.金属与浓硝酸反应生成的气体是NO ,随着反应的进行,当浓硝酸变为稀硝酸时,生成的气体变成了
2
NO。现有24g镁与溶质质量为189g的浓硝酸恰好完全反应,则反应后溶液中溶质的质量为多少g,生成
气体的总质量为多少g。
四、实验与探究题(本大题共16分,每空1分)
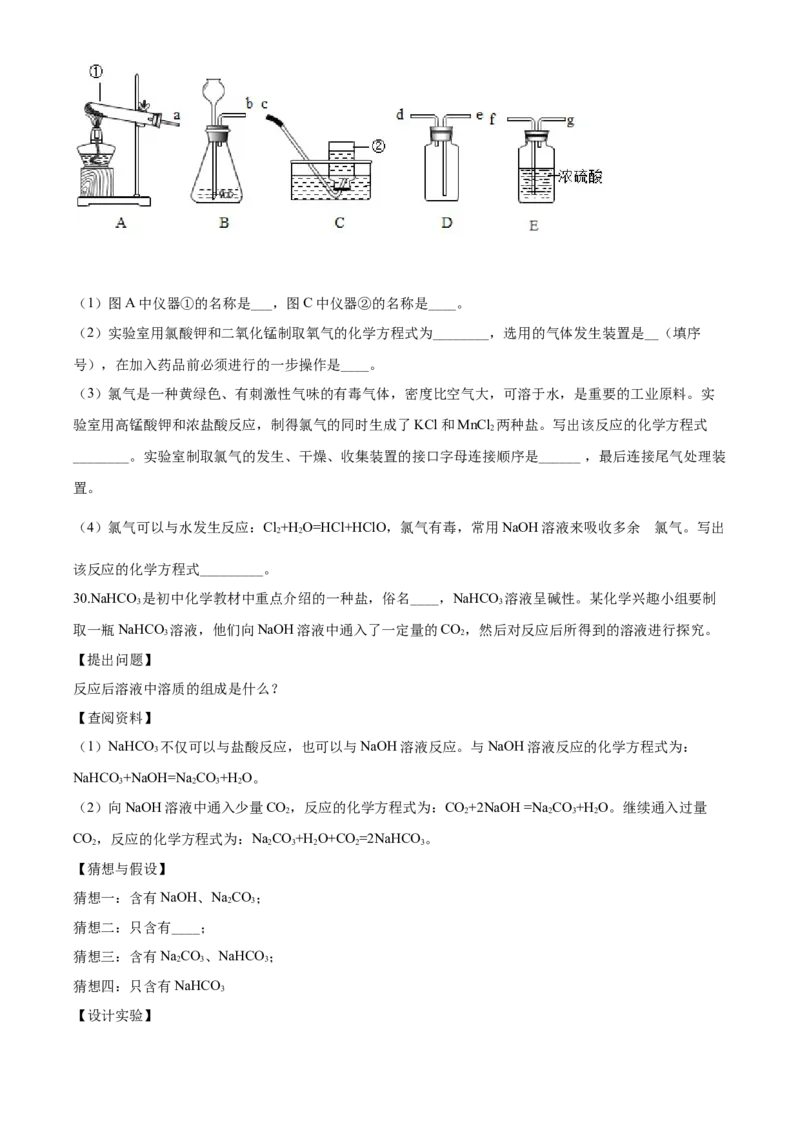
29.根据下列实验装置图,回答问题:(1)图A中仪器①的名称是___,图C中仪器②的名称是____。
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为________,选用的气体发生装置是__(填序
号),在加入药品前必须进行的一步操作是____。
(3)氯气是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,可溶于水,是重要的工业原料。实
验室用高锰酸钾和浓盐酸反应,制得氯气的同时生成了KCl和MnCl 两种盐。写出该反应的化学方程式
2
________。实验室制取氯气的发生、干燥、收集装置的接口字母连接顺序是______ ,最后连接尾气处理装
置。
的
(4)氯气可以与水发生反应:Cl+H O=HCl+HClO,氯气有毒,常用NaOH溶液来吸收多余 氯气。写出
2 2
该反应的化学方程式_________。
30.NaHCO 是初中化学教材中重点介绍的一种盐,俗名____,NaHCO 溶液呈碱性。某化学兴趣小组要制
3 3
取一瓶NaHCO 溶液,他们向NaOH溶液中通入了一定量的CO,然后对反应后所得到的溶液进行探究。
3 2
【提出问题】
反应后溶液中溶质的组成是什么?
【查阅资料】
(1)NaHCO 不仅可以与盐酸反应,也可以与NaOH溶液反应。与NaOH溶液反应的化学方程式为:
3
NaHCO +NaOH=Na CO+H O。
3 2 3 2
(2)向NaOH溶液中通入少量CO,反应的化学方程式为:CO+2NaOH =Na CO+H O。继续通入过量
2 2 2 3 2
CO,反应的化学方程式为:NaCO+H O+CO=2NaHCO。
2 2 3 2 2 3
【猜想与假设】
猜想一:含有NaOH、NaCO;
2 3
猜想二:只含有____;
猜想三:含有NaCO、NaHCO ;
2 3 3
。
猜想四:只含有NaHCO
3
【设计实验】实验步骤 实验现象 解释或结论
①取少量样品于试管中,滴
溶液呈红色。 证明溶液显碱性。
加几滴无色酚酞试液。
②另取少量样品于试管中,
加入BaCl 溶液时观察到 的
加入足量的BaCl 溶液,反 2 证明溶质中有NaCO。
2 2 3
现象_。
应完全后,静置过滤。
有无色无味的气体产生,该
③向实验②所得的滤液中滴 证明实验②所得的滤液
气体能使澄清石灰水变浑
加稀盐酸。 中有__。
浊。
【结论与反思】(1)有同学认为实验①观察到的现象及结论足以证明溶液中有NaOH。你是否同意?请说
出理由_____。
(2)写出实验③中产生气体的化学方程式____。
(3)通过实验①、②、③所观察到的现象及结论,最终得出猜想__是正确的。
【拓展与提升】实验室现有一瓶NaOH溶液和足量CO 气体,要制取一瓶溶质只有NaCO 的溶液,请完
2 2 3
善以下实验方案,仪器可以任意选择。
实验方案:先用量筒将NaOH溶液均匀分成两等份,____。
五、计算题(本大题共6分)
31.我国古代将炉甘石(ZnCO )、赤铜(Cu O)和木炭粉混合后加热到800℃左右,得到二氧化碳气体和一
3 2
种外观似金子的铜锌合金。
(1)Cu O由 元素组成;
2
(2)ZnCO 中C原子与O原子的个数比为多少;
3
(3)CO 的相对分子质量为多少,其中碳元素的质量分数为多少(结果精确到0.1%);
2
(4)将90g铜锌合金(只含Cu、Zn)放入足量稀硫酸中,充分反应,收集到0.8g氢气。计算原混合物中
炉甘石和赤铜的质量比。(要求写出计算过程)