文档内容
普通高中教科书 化学 必修 第一册
上海市中小学(幼儿园)课程改革委员会组织编写
出
版
上海世纪出版(集团)有限公司 上海科学技术出版社
(上海市钦州南路71 号 邮政编码200235)
发 行 上海新华书店
印 刷 上海中华印刷有限公司
版 次 2021 年1 月第1 版
印 次 2021 年7 月第2 次
开 本 890 毫米×1240 毫米 1/16
印 张 9.5
字 数 214 千字
书 号 ISBN 978—7—5478—4897—5/G·978
定 价 11.90 元
版权所有·未经许可不得采用任何方式擅自复制或使用本产品任何部分·违者必究
如发现印装质量问题或对内容有意见建议,请与本社联系。电话:021—64848025,邮箱:jc@sstp.cn
全国物价举报电话:12315
声明 按照《中华人民共和国著作权法》第二十五条有关规定,我们已尽量寻找著作
权人支付报酬。著作权人如有关于支付报酬事宜可及时与出版社联系。
主 编:麻生明 陈 寅
本册主编:麻生明 陈 寅
编写人员: (以姓氏笔画为序)
王 辉 王韻华 占小红 包慧敏
刘瑞婷 李锋云 沈正东 陈雪莹
责任编辑:胡恺岩 孙 伟
美术设计:诸梦婷
1.1
物质的分类 ………………………………………………………… 7
1.2
物质的量 …………………………………………………………… 15
1.3
化学中常用的实验方法 …………………………………………… 22
本章复习 ………………………………………………………………… 34
项目学习活动 如何测定气体摩尔体积 ………………………………… 38
2.1
海水中的氯 ………………………………………………………… 43
2.2
氧化还原反应和离子反应 ………………………………………… 53
2.3
溴和碘的提取 ……………………………………………………… 63
本章复习 …………………………………………………………………69
3.1
硫及其重要化合物 ………………………………………………… 75
3.2
氮及其重要化合物 …………………………………………………84
3.3
硫循环和氮循环 ……………………………………………………91
本章复习 …………………………………………………………………99
项目学习活动 如何测定硫酸铜晶体中结晶水的含量 ……………… 102
4.1
元素周期表和元素周期律 ……………………………………… 107
4.2
原子结构 ………………………………………………………… 119
4.3
核外电子排布 …………………………………………………… 127
目 录
第1 章 化学研究的天地…………………………………………………
5
绪 言�������������������������������
1
第2 章 海洋中的卤素资源… ………………………………………… 41
第3 章 硫、氮及其循环………………………………………………… 73
第4 章 原子结构和化学键… ……………………………………… 105
1
Ⅰ
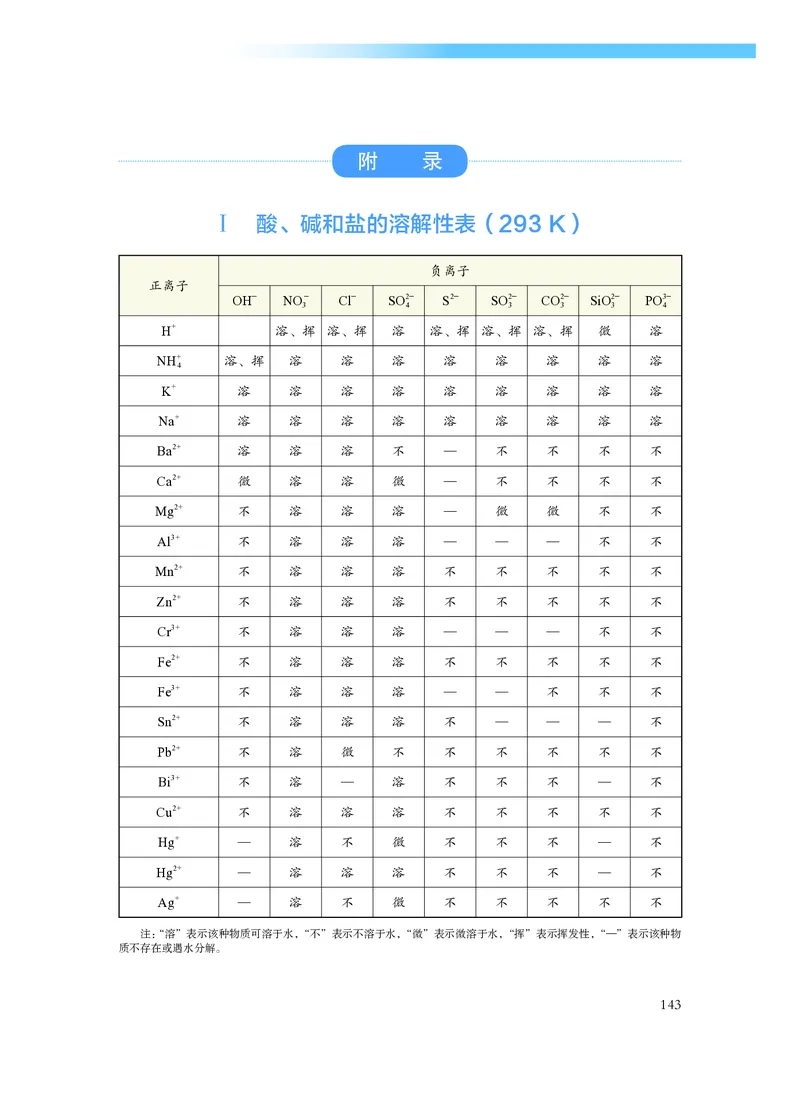
酸、碱和盐的溶解性表(293 K) ……………………………… 143
Ⅱ
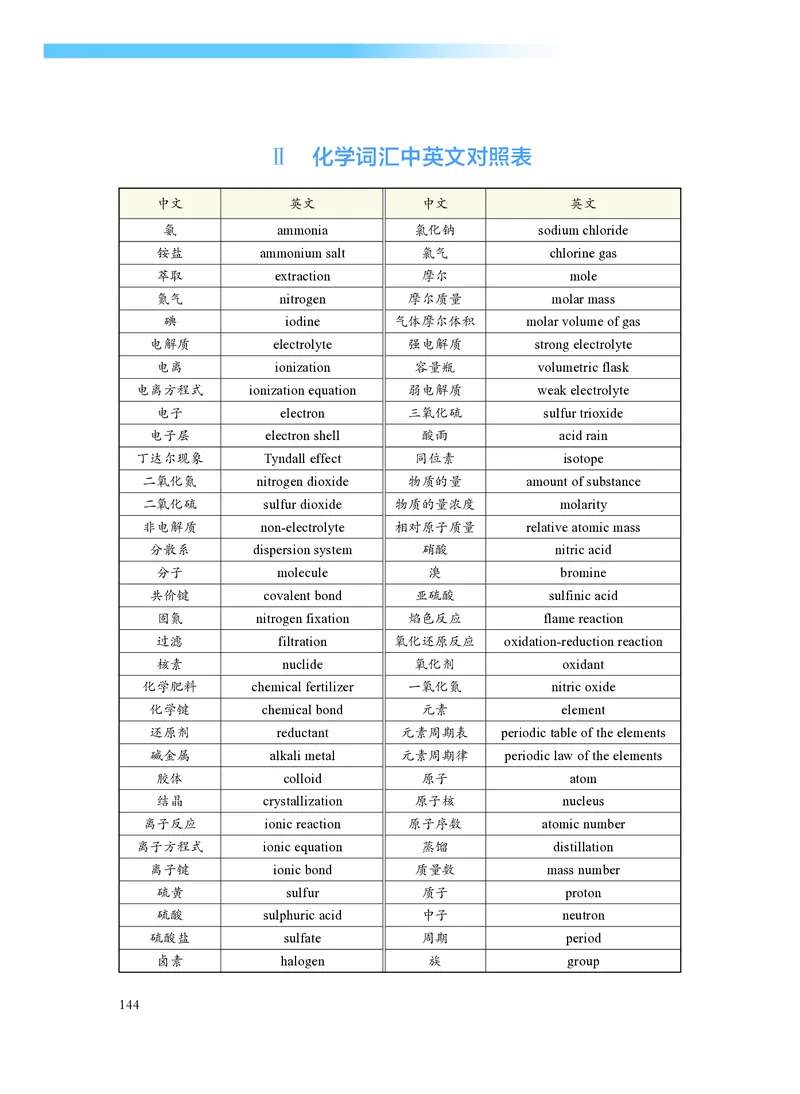
化学词汇中英文对照表 ………………………………………… 144
Ⅲ
学生必做实验索引 ……………………………………………… 145
Ⅳ
元素周期表 ……………………………………………………… 146
附
录
… ………………………………………………………………………… 143
2
4.4
化学键 …………………………………………………………… 133
本章复习 ……………………………………………………………… 139
绪 言
1
化学是人类在认识、探索、利用和保护自然的实践活动中,通过不断总结和完善
而形成的知识体系,具有创造性、实用性和有趣性。化学不仅满足人们日常生活的需
求,提升人们的生活质量,而且不断促进其他领域的科学和技术的进步,已经成为一
门重要的基础和中心学科。
人类早在学会用火起就开始了化学实践活动。古
代先民为满足生活的需求逐步掌握了陶器烧制、金属冶
炼、酒醋酿造、造纸、印染等实用化学工艺。17 世纪开
始,世界范围内的科学研究活动呈现出空前的繁荣,经
过不少化学家的不懈努力,化学被确立为科学。
19 世纪中叶起,随着元素周期律、原子结构模型
的提出和发展,现代化学的雏形初步确立。我国近代化
学的启蒙得从徐寿(1818 — 1884)说起,他从19 世
纪中叶起,先后翻译并出版了《化学鉴原》《化学考质》
《中西化学材料名目表》《化学求数》等十余部化学书籍,
系统地传播了近代化学科学,带动了这一学科在中国的
发展。20 世纪以后,人们对物质认识的层次由宏观进入
微观,创立了许多重要化学理论,研究范围更加宽广,
逐步形成了无机化学、有机化学、分析化学、物理化学、
高分子化学等分支学科。
进入21 世纪,化学与生命、材料、信息、能源、空间科学、环境等学科之间的
关系愈加密切,各学科之间的交叉融合与渗透也越来越普遍。神秘的生命过程中充满
着无数奇妙的化学反应,从分
子水平上认识生命过程,揭示、
探索生命现象的奥秘,仍然需
要化学家与生物学家的不断合
作和探索。在材料科学领域,
科学家以化学、物理等物质科
学为基础,研究和开发具有特
殊光、电、磁以及催化性能的
先进材料,比如非线性光学材
料、高温超导材料、功能高分
子材料、新能源材料等。航天
技术的每一次进步都离不开化
学家开发的安全可靠、高性能、
图1 徐寿创译的元素汉译名
沿用至今(摘自江南制
造局丛书本《化学鉴原》)
图2 我国研制出新型碳纤维复合材料地铁车
2
低成本和高载荷的火箭推进剂,以及高能电池、高敏胶片和碳纤维等耐高温、耐辐射
的特种材料,甚至航天员出舱时所穿航天服及其呼吸所需的供氧剂,都是由化学家主
要通过人工合成提供的。
化学与人类生活的各个方面都有着十分密切的联系。由于化肥、农药、植物生
长调节剂等化学品的使用,农作物的产量大幅提高,人类摆脱饥饿。人类美好的生活
离不开色香味俱佳的食品,在其生产过程中可以合理、合规地使用食品添加剂。防腐
剂、调味剂、食用香料和色素等食品添加剂就是通过从自然界提取或通过合成技术以
及安全性研究而制备的。人们在日常生活中使用的洗涤剂、消毒剂和化妆品等也都是
化学品。
疾病的诊断、治疗和预防是人类提高生活质量、延长寿命的前提,这得益于化
学家不断研制抗病毒、抗肿瘤、抗感染的药物。1972 年,以屠呦呦为代表的我国科
学家从黄花蒿中成功提取得到了青蒿素,测定了其分子结构,并证实其高效抗疟作
用。随后,我国科学家又相继研制成功双氢青蒿素、蒿甲醚、青蒿琥酯等更有效的
药物,被列入世界卫生组织的基本药物目录。青蒿素的发现,挽救了全球特别是发
展中国家数以百万计人的生命。屠呦呦也因此获得共和国勋章、诺贝尔生理学或医
学奖等奖项。
化学对保护人类赖以生存的环境也肩负重要责任。分析、监测环境质量,治理环
境和生态污染,发展环境友好的化学技术,都离不开化学。化学家以绿色化学理念发
展新的化学理论和技术,制造出有利于环境保护的化学品和生活用品,使人类与环境
的互动更加自然和谐,实现社会的可持续发展。
总之,毫不夸张地说,我们生活在一个不断使用化学知识创造的缤纷多彩的世界
里。而化学的奇妙之处,就是基于元素周期表中百余种元素而构建出的如此绚丽多彩
的物质世界。
化学学科核心素养是学生必备的科学素养,也是学生终身学习和发展的重要基础
之一,化学课程则是提升学生发展核心素养的重要载体。《化学
必修
第一册》和
《化学
必修
第二册》是根据“化学科学与实验探究”“常见的无机物及其应用”“物
质结构基础与化学反应规律”“简单的有机化合物及其应用”和“化学与社会发展”
等5 个主题编写的。通过学习必修课程,同学们将认识到化学不但是揭示元素和生命
奥秘的核心力量,而且在促进人类社会可持续发展中发挥着日益重要的作用。必修课
程将在义务教育化学和科学课程的基础上起到巩固与提高的作用,并为学习选择性必
修课程和选修课程做好必要的铺垫。
为了有利于同学们积极主动地投入学习,教材设置了不同功能的栏目,这些栏目
可以归纳为学习准备、概念建构、拓展延伸、巩固提升等部分。
3
想一想
提出与正文相关的问
题,供同学们思考、讨论,
并解决问题。
书写表达
运用化学特有的语言
来表征物质的组成、结构与
变化。
提供教师演示、学生必做实验等内容。
实验探究
概念建构
通过思考讨论、书写表达、实验探究等多样的学习方式,帮助同学们进行概
念建构,有效地掌握知识与技能。
拓展视野
提供与正文内容相关的拓展性知识。
介绍化学家的成就或重要的历史事件。
化学史话
拓展延伸
为了拓展同学们的学习视野并激发学习兴趣,教材选择了一些补充资料,供
同学们进一步了解化学与科学、技术、社会和环境的联系。
学习准备
帮助同学们了解本章节的学习目标,建立新旧知识的关联,有助于知识结构
化和网络化。
梳理在学习本节前需要回顾的知识。
知识回放
明确本节主要的学习目标,包括核心的知识内容和需达到
的学业质量水平等。
学习聚焦
例题导引
提供典型的例题,附以解答过程,呈现解决问题的思维模型。
练习巩固
设计与本章节相关的练习,并检验学习成效。
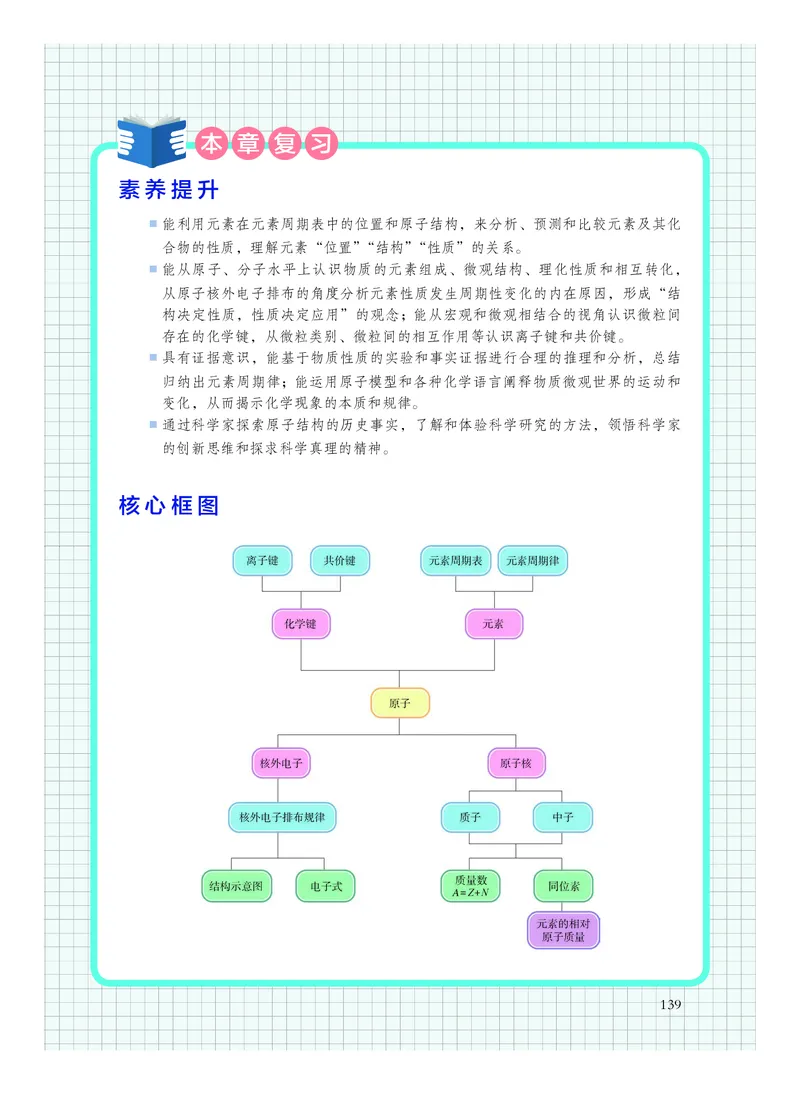
素养提升
从化学学科核心素养的视角对本章的核心概念与技能进行归纳。
核心框图
以概念图形式呈现本章的知识结构。
体验·分享
设计了制作类、课题类的实践任务或实际问题。
巩固提升
在章节的末尾,提供相关的例题、练习和实践活动,并将章节的素养要点进
行提炼,帮助同学们巩固所学内容。
链接学科
链接职业
介绍化学分支领域或跨学科领域,并提供与内容相关的职
业链接。
高中阶段所学的化学知识只是沧海一粟,希望大家通过本课程的学习,打好基
础,爱上化学,用好化学。期望有更多的同学跨入化学科学研究的殿堂,通过大家敏
锐的科学观察和探究能力,发现化学之美,为人类的可持续发展贡献自己的力量!一
个奇妙而有用的化学世界正等待同学们去探索、去开拓!
4
化学研究的天地
设施齐全、整洁有序
的化学实验室,是学习和
研究化学的重要场所。摄
于复旦大学。
第1 章
5
物质的分类
物质的量
化学中常用的实验方法
1.1
1.2
1.3
6
化
学是什么?化学是研究物质的性质、组成、结构、变化和与
之相伴随的能量转变的科学。我们身处丰富多彩的物质世
界,大到日月星辰,小到病毒细菌,无不由物质所组成。尽管物质
的外表形色各异,变化无穷,但都是由基本单元—原子构成的。
人们运用化学科学,从分子、原子水平上研究物质及其变化规
律,针对特定需求来合成新物质、制造新材料、开发新能源,为人
类创造更绿色、更美好的生存环境。在本章中,我们将了解物质
的分类方法,学习如何计量物质和研究物质常用的实验方法。这
些学习经历将帮助我们认识和体验科学家是如何研究物质和创造
新物质的。
物质的分类
7
1.1
身边的有机化合物
第7 章
人类认识和利用大自然中水、火、光、电等手段让物
质发生变化的规律,发展出各种技术,从而提炼出更纯净
的物质、制造新物质,为化学学科的发展奠定了基础。面
对数以亿计的物质,化学家是如何开展研究的?化学的探
索方向又在何处?
列举常见的物质分类方法
掌握溶液、胶体、浊液的区别
和联系
知道丁达尔现象
学习聚焦
知识回放
● 单质和化合物
● 氧化物、酸、碱和盐
● 物质三态的变化
● 溶液和浊液
1.1
物质的分类
化学的研究对象是物质,化学家常根据需要将众多物
质进行分类,从而更好地探索各类物质的性质及其相互转
化的规律。
物质分类的一般原则是将具有相似性质的物质归为同
一类,从不同角度或用不同方法可形成不同的分类。根据
物质的组成,可将物质分为纯净物和混合物;对于纯净物,
可根据物质中所含元素的种类,分为单质和化合物;对于
无机化合物,又可分为酸、碱、盐和氧化物等。此外,还
可以根据物质的导电性、溶解性、聚集状态等进行分类
(图1.1)。
物质的分类
图1.1 物质分类方式列举
在日常生活中,我们常会接触到下列物质:空气、水、
铜、食盐、糖水、碳酸钙、氧气、石墨、乙醇。请你将上
述物质进行分类,并说出分类的依据。
想一想
化学研究的天地
第1 章
8
化学中关于物质的分类远不止以上这些。根据氧化还
原反应理论,可以将物质分为氧化剂和还原剂;根据化合
物在水溶液中或熔融状态下能否导电,可将其分为电解质
和非电解质;根据有机化合物的分子组成中是否含有碳、
氢以外的元素,分为烃和烃的衍生物,烃的衍生物又可分
为含氧衍生物、含氮衍生物等。
生活经验告诉我们:固体有一定的形状;液体没有固
定的形状,但有固定的体积;气体没有固定的形状和体积;
气体容易被压缩,而固体和液体不易被压缩。我们可以根
据物质的聚集状态认识每类物质的宏观和微观状态的性质。
物质在气、液、固三态时的这些特性主要与构成物质的微
粒之间的平均距离、作用力及运动方式等有关(图1.2)。
观察图1.2,分析不同聚集状态物质的宏观和微观性质。
图1.2 物质聚集状态的示意图
聚集状态
宏观性质
微观性质
是否有固定形状
是否有固定体积
微粒间距离的远近
微粒间作用力的强弱
气态
液态
固态
想一想
物质的分类
9
1.1
温度和压强都会对物质微粒之间的平均距离产生影响。
一次性打火机内灌充的燃料是易挥发的有机化合物—丁
烷(常压下沸点为—0.5℃),丁烷气体在打火机内却呈液态,
请解释这一现象。
在一定条件下,物质的三种聚集状态之间可以相互转
化(图1.3)。通常情况下,固体和液体的密度较大,而气
体的密度较小。液体和固体也被称为物质的凝聚态。物质
的体积是由构成物质的微粒数目、微粒大小和微粒之间的
距离等因素决定的。
图1.3 物质的三态变化
拓展视野
当温度达到数千摄氏度时,原子外层电子会具有足够的能量而摆脱原子核的
束缚,成为自由电子,该过程称为电离。由电荷总数相等的正离子和自由电子构
成的电离状态的气体称为等离子体,被视为物质的第四种存在状态,它在自然界
和宇宙中普遍存在。由于等离子体的形成需要10
3 ~10
5 K 的高温,高温促使化
学反应速率大大加快,所以等离子体技术在化工领域应用广泛,如应用于切割、
喷涂和受控热核聚变反应等方面。
物质的第四态—等离子体
图1.4 与等离子体有关的现象
爆炸后的恒星
辉光球
极光
闪电
在日常生活中,我们所接触到的物质大多是混合物。
其中不少混合物是由一种或多种物质分散在另一种物质中
分散系
想一想
化学研究的天地
第1 章
10
生活中我们会接触到不同的分散系,而分散质或分散剂也可以是气、液、固等不同
的聚集状态,它们之间又会有若干组合方式。请举出几种常见的分散系的实例。
溶液中的分散质粒子是小分子或离子,其直径通常小
于1 nm(1 nm =1×10
—9 m),这样的分散系表现出均匀、
稳定的宏观特征,在通常情况下分散质不会自动与分散剂
分离。悬浊液、乳浊液中的分散质粒子是固体小颗粒或小
液滴,直径通常大于100 nm,这样的分散系表现出不均
匀、不稳定等特征,分散质往往会发生沉降或上浮,从而
与分散剂分离(图1.6)。
图1.6 橄榄油和醋形成不太稳定的乳浊液
图1.5 分散系
形成的,如白色硫酸铜粉末分散在水中形成的蓝色溶液,
粉笔灰分散在水中形成的悬浊液,植物油分散在水中形成
的乳浊液等。我们把这些混合体系称为分散系,其中分散
成粒子的物质称为分散质,粒子分散在其中的物质称为分
散剂。根据分散质粒子的大小,可将分散系分为溶液、胶
体、浊液等。
想一想
珍珠
雾
涂料
物质的分类
11
1.1
分散质粒子的直径大小在1 ~100 nm 之间的分散系,
叫做胶体。胶体在一定条件下能稳定存在,并具有一些不
同于溶液和浊液的特性。
实验探究
取一只烧杯,加入约50 mL 蒸馏水,加热至沸腾。将3 mL 饱和FeCl3 溶
液分多次缓慢加入,用玻璃棒轻轻搅拌,继续加热至刚好变成红褐色,停止加
热即得到Fe(OH)3 胶体。
另取两只烧杯,向其中一只烧杯加入50 mL FeCl3 稀溶液,向第二只烧
杯中加入40 mL FeCl3 稀溶液和约10 mL NaOH 溶液,用玻璃棒搅拌后得到
Fe(OH)3 悬浊液。将这三只烧杯置于暗处,分别用红光激光笔水平照射,观察
现象。
将FeCl3 稀溶液、Fe(OH)3 胶体和Fe(OH)3 悬浊液分别进行过滤,观察滤
纸上是否有残留固体。将实验现象填入下表。
胶体的丁达尔现象
问题:根据上述实验现象,思考如何用简便的方法鉴别胶体和溶液?
物质
光束照射时的现象
过滤后的滤纸上是否有残留固体
FeCl3稀溶液
Fe(OH)3胶体
Fe(OH)3悬浊液
半透膜
胶体的分散质粒子比滤
纸孔隙小,很容易透过滤纸。
要除去胶体粒子,可选用半
透膜。半透膜是一种孔径比
滤纸更小的膜,小分子、离
子能透过而胶体粒子不能透
过。常见的半透膜有动物的
肠衣、膀胱膜、羊皮纸、玻
璃纸等。
资料库
图1.7 不同分散质粒子透过滤纸和半透膜时的示意图
化学研究的天地
第1 章
12
图1.8 Fe(OH)3 胶体的丁达尔现象
图1.9 日常生活中的丁达尔现象
胶体粒子有很大的比表面积(单位质量粒子具有的表
面积),具有较好的吸附性,能吸附水中的悬浮颗粒物并使
其沉降,因而常用于水的净化。
丁达尔现象
可见光的波长在400 ~
760 nm 之间。胶体粒子直径
在1 ~ 100 nm 之间,小于可
见光的波长。当光入射胶体
时会发生光的散射,此时每
颗胶体粒子就像一个光源,
向各个方向发射出光线,丁
达尔现象就是胶体粒子对入
射光发生散射的结果。溶液
中分散质粒子直径小于1 nm,
散射作用极其微弱,故光通
过溶液时观察不到这种现象。
资料库
当光通过分散系时,由于分散质粒子对光散射而在
侧面观察到明亮的光线轨迹的现象,称为丁达尔现象(图
1.8)。丁达尔现象是胶体的重要特征,是鉴别胶体和溶液
的常用方法。
丁达尔现象在日常生活中随处可见。例如,清晨在树林
中看到一缕缕光束,阳光通过窗隙射入暗室形成光柱等,都
属于丁达尔现象(图1.9)。这是由于空气中含有微小的尘埃
或液滴,在一定条件下形成云、雾、烟等胶体(又称气溶胶),
因而产生丁达尔现象。在化学分析中,利用丁达尔现象制
成浊度计用以确定胶体中分散质粒子的大小和分布密度。
激光笔
物质的分类
13
1.1
胶体粒子可以选择吸附带相同电荷的微粒,即同种胶
体粒子带上同种电荷,导致胶体粒子彼此相互排斥,在一般
情况下,胶体粒子不容易聚集,因而胶体可以比较稳定地存
在。在外加直流电场作用下,带电的胶体粒子或离子向着与
其电性相反的电极移动,这种现象称为电泳(图1.10)。
当胶体粒子遇到带有相反电荷的离子或其他胶体粒子
时,由于电荷的中和,胶体粒子聚集成为较大的颗粒物,
在重力作用下形成沉淀析出,这种过程叫做聚沉。例如,
向豆浆中加入石膏或盐卤,会引起豆浆里的蛋白质和水等
物质一起聚沉为豆腐。大江大河中含有大量的土壤胶体粒
子,在江河入海口,海水中的盐分使这些胶体粒子发生聚
沉,逐渐形成三角洲、冲积岛等地形地貌。此外,加热、
搅拌也会引起胶体的聚沉。胶体的应用对日常生活、科学
研究、工农业生产以及国防等有着十分重要的意义。在新
材料的研制中,当粒子的大小达到纳米级,即在胶体粒子
直径范围时,材料性能会发生奇特变化,如纳米陶瓷可以
克服陶瓷材料易碎的致命缺点等。因此,纳米材料已成为
新材料研究领域的热点。
拓展视野
有的胶体聚沉后能形成立体网状结构,将大量分散剂包裹其中,形成具有弹
性的半固体,叫做凝胶。果冻、肉冻等是生活中经常见到的凝胶。如果凝胶中包
含的分散剂为气体,则被称为气凝胶,这是一种密度极小的材料,具有很多神奇
的性能,如优异的隔热、隔音、承重性能等。
凝胶
图1.11 气凝胶神奇的性能
具有优异的隔热性能
可支撑较重的物体
气凝胶
气凝胶
图1.10 Fe(OH)3 胶体的电
泳现象
通直流电前
通直流电后
化学研究的天地
第1 章
14
学习指南
练习巩固
1. 下列体系不属于分散系的是( )。
(A) 碘酒
(B) 水
(C) 泥浆
(D) 鸡蛋清
2. 胶体和溶液的本质区别在于( )。
(A) 分散系是否有颜色
(B) 分散系是否均匀
(C) 分散质粒子的直径
(D) 能否发生丁达尔现象
3. 下列对生活中常见现象的正确解释是( )。
(A) 汽化:舞台上常用干冰制作“云雾”效果
(B) 液化:从冰箱里取出的鸡蛋过一会儿会“出汗”
(C) 升华:冰雪消融
(D) 凝固:冬日温暖的车内窗玻璃会变模糊
15
1.2
物质的量
身边的有机化合物
第7 章
1.2
物质的量
物质的量是一个物理量,表示物质中含有一定数目微粒
的集合体。1971 年,第14 届国际计量大会将“物质的量”
确定为国际单位制的7 个基本物理量之一,符号为n。物质
的量的单位是摩尔,用mol 表示。
1 mol 精确包含6.022 140 76×10
23 个基本
单元,该数称为阿伏加德罗常数(NA),以单位
mol
—1 表示。一般来说,NA 取值保留到6.02×10
23
即可。这里指的基本单元可以是原子、分子、
离子、电子、其他任意微粒或微粒的特定组合。
例如:
1 mol C 中约含有6.02×10
23 个碳原子;
1 mol CO2 中约含有6.02×10
23 个二氧化碳
分子;
1 mol NaCl 中约含有6.02×10
23 个钠离子和
6.02×10
23 个氯离子;
1 mol O2 中约含有1.204×10
24 个氧原子。
如果一定量微粒集合体中所含有的微粒数
与阿伏加德罗常数的值相同,我们就说这种微粒
的物质的量为1 mol。
物质的量(n)、阿伏加德罗常数(NA)与微粒数(N)
之间存在以下关系:
N
NA
n =
摩尔成为将微观粒子与宏观物质联系起来的桥梁,并
建立起与其他基本单位之间的定量关系,极大地促进了化
学学科的发展,广泛用于化学、生物等基础科学研究与分
物质的量 阿伏加德罗常数
在描述物品数量时,我们可以根据数量的多少,选择
合适的计量单位。例如,2 只皮鞋是一“双”、12 个鸡蛋是
一“打”、500 张全张纸是一“令”等。物质是由数目巨大、
质量很小、肉眼无法观察到的分子、原子等微粒构成,如
何来计量这些微粒的数量呢?能否建立起微粒数与宏观可
称量的物质质量之间的联系呢?
了解物质的量及其相关物理量
的含义和应用
基于物质的量认识物质组成与
化学变化
运用物质的量、摩尔质量、气
体摩尔体积之间的相互关系进
行简单计算
学习聚焦
知识回放
● 物质的聚集状态
● 化学方程式中化学计量数的
意义
资料库
表1.1 国际单位制(SI)的7 个基本
单位
量的名称
单位
名称
单位
符号
长度
米
m
质量
千克
kg
时间
秒
s
电流
安培
A
热力学温度
开尔文
K
物质的量
摩尔
mol
发光强度
坎德拉
cd
16
化学研究的天地
第1 章
析测试,以及化工、医药等行业的生产实践活动。
在研究化学变化时,采用摩尔进行计量会带来很多方
便。如通过化学反应中反应物与生成物之间原子、分子等
微粒的计量数之比,我们可以直接知道它们之间的物质的
量之比。例如:
通常我们用质量来计量物质的多少,用体积来衡量物
质的大小。那么1 mol 不同物质的质量究竟是多少?它们
的体积又是多大呢?
摩尔质量 气体摩尔体积
表1.2 常压下1 mol 不同物质的质量和体积
物质
状态
相对原子质量或相
对分子质量
质量/g
密度/(g·cm
—3)
体积/cm
3
NaCl
固
58.5
58.5
2.17
Fe
固
56
56
7.86
C2H5OH
液
46
46
0.789
H2SO4
液
98
98
1.84
H2(273 K)
气
2
2
0.000 088
He(273 K)
气
4
4
0.000 176
CH4(273 K)
气
16
16
0.000 716
注: 除标明温度外均为室温下的测量值。
点燃
C + O2
CO2
1 mol 1 mol 1 mol
理论化学是运用理论计算来解释和理解物质世界中的微观化学问题的化学
分支学科。随着理论化学的创立和发展,化学由以实验为基础的科学进入可用理
论计算来认识化学反应的阶段。比如,解释化学反应行为,理解化学反应的现象
和微观本质,预测一些物质的反应活性和设计新的材料等。
理论化学
链接学科
17
1.2
物质的量
由表1.2 可知,对于固态或液态的物质来说,1 mol 不
同物质的体积往往是不相同的,但1 mol 不同气体的体积
在同温同压下却近似相等。
大量的科学实验表明,在273 K 和101 kPa 条件(称
为标准状况
①,简写为STP)下,1 mol 气体的体积约为
22.4 L(图1.12)。
我们把每摩尔气体所具有的体积叫做气体摩尔体积,
用符号Vm 表示,常用的单位为L·mol
—1。一定量气体的
物质的量(n)、体积(V)与气体摩尔体积(Vm)之间存
在以下关系:
V
Vm
n =
每摩尔指定物种(如原子、分子或者某种微粒及其
组合等)所具有的质量称为摩尔质量,符号为M,单位
为g·mol
—1。根据表1.2 可知,物质的摩尔质量在数值上
等于该物质的相对原子质量或相对分子质量。例如:Fe 的
摩尔质量为56 g·mol
—1,乙醇的摩尔质量为46 g·mol
—1,
H2SO4 的摩尔质量为98 g·mol
—1。
物质的质量(m)、摩尔质量(M)和物质的量(n)之
间存在如下关系:
m
M
n =
已知银的相对原子质量为107.9,21.58 g 银所含的银原
子的物质的量是多少?含有银原子的个数是多少?
书写表达
根据表1.2 所给的数据,分析表中1 mol 各物质的质量
在数值上的特点。根据物质的密度计算1 mol 各物质的体积
并填入表中,结合物质聚集状态的特点(图1.2)解释物质
体积数据存在差异的原因。
图1.12 标准状况下1 mol 气
体的体积约为22.4 L
① 标准状况是温度为273.15 K(即0℃,近似值用273 K)和压强为101.325 kPa(近似值用101 kPa)的状况。
想一想
18
化学研究的天地
第1 章
在提到气体体积时,一定要注明温度和压强,这是因
为气体分子之间的平均距离与外界温度和压强有关。温度
升高时,气体分子间平均距离增大;温度降低时,气体分
子间平均距离减小。压强增大时,气体分子间平均距离减
小;压强减小时,气体分子间平均距离增大。各种气体在
相同温度和压强条件下,分子间的平均距离都近似相等,
此时气体体积大小只与分子数目有关。
在相同温度和压强条件下,相同体积的任何气体都含
有相同数目的分子。这个规律最早是由意大利物理学家和化
学家阿伏加德罗(Amedeo Avogadro,1776—1856)提出的,
故被称为阿伏加德罗定律。阿伏加德罗定律也可表述为:在
相同温度和压强条件下,气体的体积与其物质的量成正比。
n1
n2
V1
V2 =
了解气体体积与物质的量之间的关系后,我们在化学
反应中就可以直接用体积来计量气体了。
物质由原子、分子等微粒构成,物质之间发生化学反应
时也是这些微粒以一定的数量关系进行的,化学方程式中的
计量系数表示的就是微粒之间的这种数量关系。例如,表1.4
所示的就是甲烷与氧气的燃烧反应中反应物和生成物之间的
各种定量关系。
表1.3
其他条件下气体摩
尔体积的数值
温度
K
压强
kPa
Vm
(L·mol
—1)
298
101
24.5
300
101
24.6
373
101
30.6
资料库
已知常温常压下,18 g 液态水(假设水分子之间排
列紧密)的体积为18 mL,而相同质量的水蒸气体积为
24.5 L,估算该条件下水蒸气中气体分子之间的平均距
离大概是其分子直径的多少倍?
书写表达
为什么1 mol 任何气体在同温同压时所占的体积都近
似相等呢?这是因为物质的体积主要取决于构成物质的微粒
数目、微粒大小和微粒之间的平均距离。对于固体和液体,
构成物质的微粒间的距离很小,一定量物质的体积主要取
决于它们的微粒大小。对于气体来说,通常情况下,气体
分子之间的平均距离远远大于分子的直径,与气体占有的
总体积相比,气体分子本身的体积可以忽略不计。因此,
一定量气体的体积主要取决于气体分子之间的平均距离。
19
1.2
物质的量
拓展视野
表1.4 甲烷的燃烧反应中各物质间的定量关系
在一定温度和压强下,每消耗10 体积气体A2 与30
体积气体B2,能化合生成20 体积气体X。能否据此推
导出X 的化学式?你在推导过程中运用了什么定律?
中国科学家在国际单位制重新定义中的贡献
摩尔的产生源自近代化学和物理科学研究实践,其含义和内容随着科学的发
展而不断完善。
1971 年第14 届国际计量大会通过决议,“物质的量”成为国际单位制的一个
基本物理量,摩尔是它的单位,并将该单位定义为:摩尔是一系统的物质的量,该
系统中所包含基本单元数与0.012 kg 碳—12 的原子数目相等。摩尔的定义与质量单
位千克直接关联,其质量由保存在国际计量局的千克原器实物基准复现。但是,实
物千克基准不够稳定,容易受到人为或环境因素的影响,质量单位千克原器的不确
定性影响了摩尔的准确度,原有的定义已不能满足精确测量的要求。
2018 年第26 届国际计量大会通过了修订国际单位制的决议,摩尔被重新定义
为:1 mol 精确包含6.022 140 76×10
23 个基本单元,该数为阿伏加德罗常数,阿伏
加德罗常数也是自然科学的重要基本常数之一。摩尔的新定义将物质的量的测量从
质量溯源转变为微粒数量溯源,不再依赖质量单位“千克”而独立存在,新定义真
正实现了基本单位回归到基本常数之上。
阿伏加德罗常数的精确测定成为新定义的关键,科学家通过由高纯度硅—28 制
作的单晶硅的硅球来测量该常数。因此,硅球的质量、体积、硅摩尔质量等都需要
进行精确测量。
中国科学家首次提出并建立了一种基于高分辨质谱的测量方法,很好地消除
了测量过程中产生的干扰离子,实现了浓缩硅摩尔质量的精确测量。中国科学家的
创新研究成果克服了浓缩硅摩尔质量测量方法单一,且不同实验室测量结果存在较
大差异的技术难题,为国际单位制的重新定义做出了实质性贡献。
化学方程式与
各物质状态
CH4 + 2O2
CO2 + 2H2O
气态 气态 气态 液态
分子数目
1 个分子∶2 个分子∶1 个分子∶2 个分子
物质的量
1 mol ∶ 2 mol ∶ 1 mol ∶ 2 mol
质量
16 g + 64 g = 44 g + 36 g
气体体积(STP)
22.4 L ∶ 44.8 L ∶ 22.4 L
点燃
想一想
20
化学研究的天地
第1 章
● 通常情况下,一个三口之家每天做饭约消耗320 g 天然气(全部
以CH4 计)。这些天然气中含有的CH4 个数约是多少?在标准状
况下,这些天然气体积约为多少升?
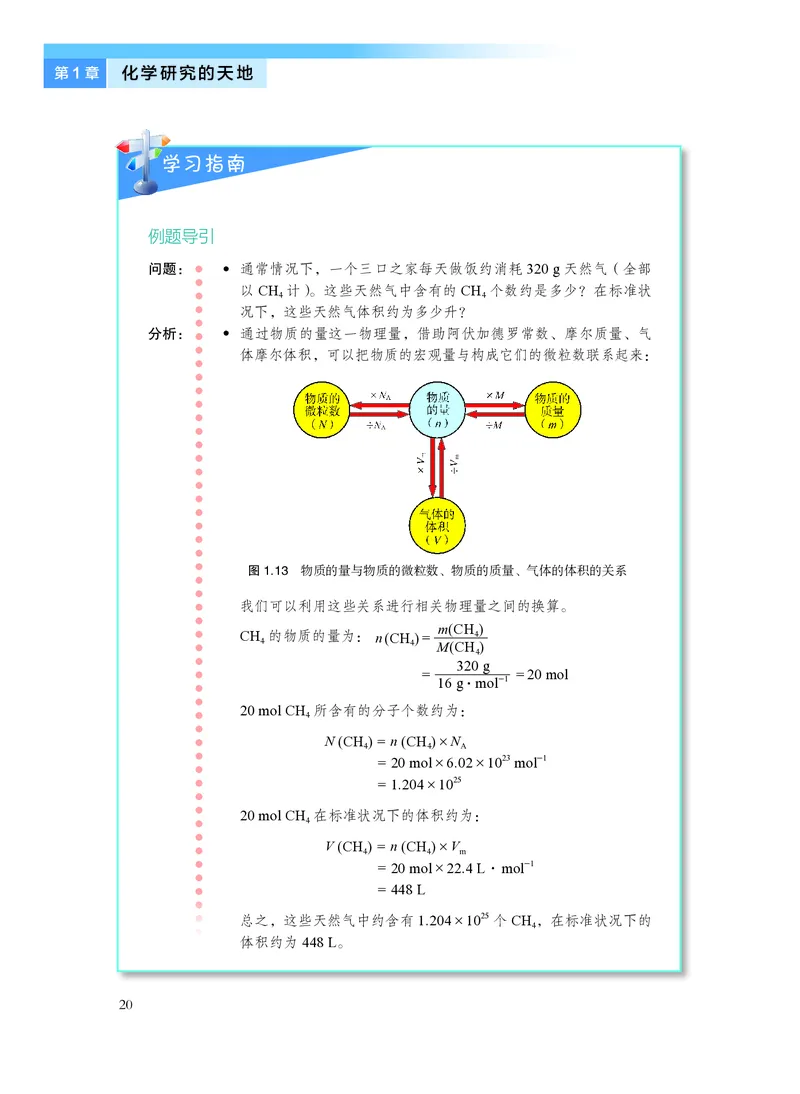
● 通过物质的量这一物理量,借助阿伏加德罗常数、摩尔质量、气
体摩尔体积,可以把物质的宏观量与构成它们的微粒数联系起来:
学习指南
例题导引
问题:
分析:
图1.13 物质的量与物质的微粒数、物质的质量、气体的体积的关系
我们可以利用这些关系进行相关物理量之间的换算。
CH4 的物质的量为:
m(CH4)
M(CH4)
320 g
16 g·mol
—1
n (CH4) =
= 20 mol
=
20 mol CH4 所含有的分子个数约为:
N (CH4) = n (CH4)×NA
= 20 mol×6.02×10
23 mol
—1
= 1.204×10
25
20 mol CH4 在标准状况下的体积约为:
V (CH4) = n (CH4)×Vm
= 20 mol×22.4 L·mol
—1
= 448 L
总之,这些天然气中约含有1.204×10
25 个CH4,在标准状况下的
体积约为448 L。
21
1.2
物质的量
练习巩固
1. 下列关于物质的量的正确说法是( )。
(A) 可以理解为物质的质量
(B) 就是物质的粒子数目
(C) 表示一定数目微粒集合体的物理量
(D) 这一物理量只适用于分子、原子和离子这些微粒的计量
2. 标准状况下,下列物质所占体积最大的是( )。
(A) 360 g H2O
(B) 32 g O2
(C) 1.5 mol H2
(D) 约3.01×10
24 个氮分子
3. 铅笔芯的主要成分是石墨和黏土。假设铅笔芯质量的一半是石墨(其余组
成物质中不含碳),用铅笔写一个汉字消耗的质量约为1 mg,那么这个汉字中含有
的碳原子数约为( )。
(A) 2.5×10
19
(B) 2.5×10
22
(C) 5×10
19
(D) 5×10
22
4. 当温度与压强一定时,气体体积主要取决于以下哪些因素?请在□内
画“√”。
□分子间的平均距离
□分子的数目
□摩尔质量
□密度
□分子自身的大小
5. 填写下表。
物质的量
质量
体积(STP)
分子数
6.72 L N2
约3.01×10
23个氧分子
2 g H2
0.8 mol Cl2
6. 家用天然气中会添加微量的有特殊臭味的泄漏警告剂,其主要成分可以
是四氢噻吩(C4H8S),一般添加量是20 ~50 mg·m
—3。若你家中一年使用的
天然气的量为310 m
3,计算一年所消耗的气态四氢噻吩折算成标准状况下的体
积范围。
22
化学研究的天地
第1 章
身边的有机化合物
第7 章
1.3
化学中常用的实验方法
虽然现代化学的飞速进步已经产生了各种各样新的
研究方法,但时至今日,实验仍然是化学研究不可缺少的
手段。通过实验,我们可以合成新的物质,探究物质的性
质,分离和提纯所需要的物质,确定组成物质的元素与含
量,解析物质的微观结构,揭示化学现象的本质等。可以
说,没有实验,就没有化学。
理解常见物质的制备和分离原
理,掌握相应的实验操作方法
知道焰色反应、显色法、沉淀法、
气体法等鉴别物质的常用方法
能运用物质的量浓度进行简单
计算
学会配制一定物质的量浓度的
溶液
学习聚焦
知识回放
● 实验室制备氧气、二氧化碳
等气体
● 实验室常用的玻璃仪器名称
和用途
● 药品取用、物质加热、过滤、
蒸发等操作方法
日常生活、工农业生产和科学研究都离不开物质的制
备。例如,化工原料的生产、新药的研发、新材料的合成
等。在实验室中,我们也曾有制备O2、CO2 和Fe(OH)3 胶
体等物质的经历。
在进行物质制备等化学实验时,同学们必须遵守实验
规则和安全要求,必须在确保实验安全的前提下,来取得
良好的实验效果。例如,我们要明确实验步骤、注意事项
和操作规范,谨慎处理易燃、易爆、有毒、有腐蚀性的物
质等。
物质的制备
依据实验室制备氧气的实验,思考以下问题:
(1) 制备氧气的实验中,你会选择什么物质作为反
应原料?
(2) 如何设计实验步骤并搭建装置?
(3) 若要得到纯净和干燥的氧气,应如何优化反应
装置?
在制备物质时,常会根据目标产品的组成来选择合适
的原料与确定反应原理,设计反应路径,选择合适的仪器
并搭建实验装置,在一定实验条件下进行制备,最终根据
产品的理化性质将其分离提纯出来。
化学实验安全及相关图形符号
表1.5 化学品安全使用标识
危险
象形图
说明
爆炸物(如具有整体爆
炸危险的物质、混合物
和制品)
易燃类的物质(如易燃
的气体、气溶胶、液体
和固体,自燃的液体和
固体,以及遇水放出易
燃气体的物质和混合物)
氧化性物质(如氧化性
的气体、液体和固体)
加压气体(如压缩气体、
液化气体、溶解气体)
毒性物质(如具有急性
毒性的物质)
警告(如对皮肤、眼具
有刺激的物质,对臭氧
层具有危害的物质)
腐蚀类物质(如金属腐
蚀物)
健康危害(如呼吸道致
敏物、致癌物)
环境危害(如对水生环
境具有危害的物质)
资料库
想一想
23
1.3
化学中常用的实验方法
图1.14 制备物质的一般流程
当原料确定之后,应根据原料性质、设备条件等设计
反应路径。确定反应路径后,反应条件的控制也十分重要,
因为不同的实验条件下,反应的速率和进行程度,以及所
得生成物的状态、性质等也不尽相同。因此,在设计物质
制备的实验方案时,要综合考虑上述流程中的每个环节。
制备物质时一般遵循的原则有:原料易得,原理绿色,条
件温和,装置简单,分离方便等。
实验探究
在实验室中,可用浓盐酸与二氧化锰反应来制备氯气(Cl2)。实验装置如
图1.15 所示,认真观察教师演示的实验过程(必须在教师指导下才能嗅闻氯气
的气味)。涉及实验原理的化学方程式如下:
MnO2 + 4HCl(浓)
MnCl2 + Cl2↑ + 2H2O
Cl2 + 2NaOH
NaCl + NaClO + H2O
实验室制备氯气
现象记录:
。
实验结论:
。
问题:实验室中制备气体的装置通常包括哪些部分?若要制取纯净、干燥
的氯气,你会如何优化上述装置?
图1.15 实验室中制备氯气的装置
△
24
化学研究的天地
第1 章
日常生活中我们见到的物质大部分都属于混合物。在
化学实验中,我们可以运用物理或化学方法,将混合物中
的组分分开,这种操作称为分离;去除杂质得到纯物质的
操作则称为提纯。通过分离和提纯可得到纯净的物质,供
我们进一步研究其组成、结构与性质。初中时,我们就学
过在实验室里可利用过滤、蒸发等操作来分离和提纯物
质。在化工生产中,许多有效的分离技术已成为重要的工
艺过程,通过专用设备来实现。
混合物的分离是根据混合物中各组分性质差异进行的。分离
混合物的常见物理方法有过滤、结晶、蒸馏、萃取和分液等。
物质的分离与提纯
图1.18 工业过滤器和蒸发塔
工业过滤器
热电厂的蒸发塔
我们已学过粗盐提纯,该实验过程中涉及哪些分离操
作?有哪些操作要点?
蒸发操作
图1.17 实验室的过滤与蒸
发操作
过滤操作
药物的制备和新药的研发与人类健康、生活质
量密切相关,长期以来人们一直从天然物质中寻找
和提取药物;化学家与药物学家通力合作,制备各
种新物质用于新药研发;在药物的工业化生产过程
中,化学家创造性地开发绿色环保的高效生产工艺。
化学家通过这些途径为人类的健康做出重要贡献。
药物的研制和绿色生产
链接职业
图1.16 药物研发人员
想一想
25
1.3
化学中常用的实验方法
蒸发结晶与冷却结
晶对被提纯物质的溶
解度有何要求?现有
一混有少量氯化钾的
硝酸钾粉末,请结合
两者的溶解度曲线(图
1.19 ),思考如何提纯
硝酸钾。
图1.19 KCl 和KNO3 的溶解度曲线
将含有少量杂质的晶体溶于水,再重新进
行结晶,利用物质溶解度的差异,使杂质全部
或大部分留在溶液中,这种提纯操作称为重结
晶。经过一次重结晶,若晶体的纯度仍没有达
到要求,可再次进行重结晶。
2. 蒸馏
蒸馏是将液体加热汽化后再冷凝蒸气的操
作。通过蒸馏,可以把溶剂从含有高沸点溶质的
溶液中分离出来,也可以将两种或两种以上沸点
差别较大的液体进行分离。例如,通过蒸馏方法
将海水中的无机盐除去,得到纯净的淡水。
拓展视野
对于沸点相差不大的液体,仅靠一次蒸馏无法实现较好的分离效果。此时可
以采用分馏的方法。分馏装置与蒸馏装置类似,但增加了一根特制的分馏柱,可以
加大蒸气与分馏柱内填充物接触的表面积,通过液体在柱内的反复汽化和冷凝,实
现多次蒸馏效果,使混合物分离更加完全。分馏在工业上应用十分广泛,例如石油
工业中分离汽油、煤油、柴油等燃料;从液态空气中分离氮气和氧气;在酿酒工业
中利用分馏提高酒产品中乙醇的浓度等。
分馏
图1.20 蒸馏装置
1. 结晶
把溶质从溶液中分离出来有两种基本方法:蒸发结晶
与冷却结晶。
想一想
26
化学研究的天地
第1 章
3. 萃取和分液
利用某种溶质在两种互不相溶的溶剂中溶解能力的不
同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中
提取出来的方法,叫做萃取。将两种互不相溶的液体分离
的操作,叫做分液。在实验室中,萃取和分液常常结合在
一起进行。
实验探究
取一只分液漏斗,加入适量水,检查漏斗顶塞与活塞是否漏水。用量筒量
取10 mL 碘水,倒入分液漏斗,然后再注入10 mL 四氯化碳,盖好顶塞,旋紧,
以免漏液。用一手压住分液漏斗顶塞,一手握住活塞(图1.21),把分液漏斗
倒转振荡,使两种液体充分混合,然后旋开活塞放气。反复几次后,将分液漏
斗放在铁架台上静置。
从碘水中萃取碘
在日常生产、生活中,我们也常用溶剂提取固体中
的某些组分,如用水浸取甜菜中的糖类、用乙醇提取中
药里的有效成分等,这些也都属于萃取操作。萃取在天
然香料、精油、药物提取以及核燃料的处理等方面都有着
广泛应用。
图1.22 工业上的萃取设备
待液体分层清晰后,打开分液漏斗顶塞,再将分液漏斗活塞旋开,使下层
液体慢慢沿锥形瓶壁流下。当两种液体的交界面进入活塞孔时,关闭活塞,将
上层液体从上口倒出。
现象记录:
。
实验结论:
。
问题:能用于从碘水中萃取碘的溶剂应具备哪些性质?
图1.21 从碘水中萃取碘
振荡并放气
静置分层
分液
27
1.3
化学中常用的实验方法
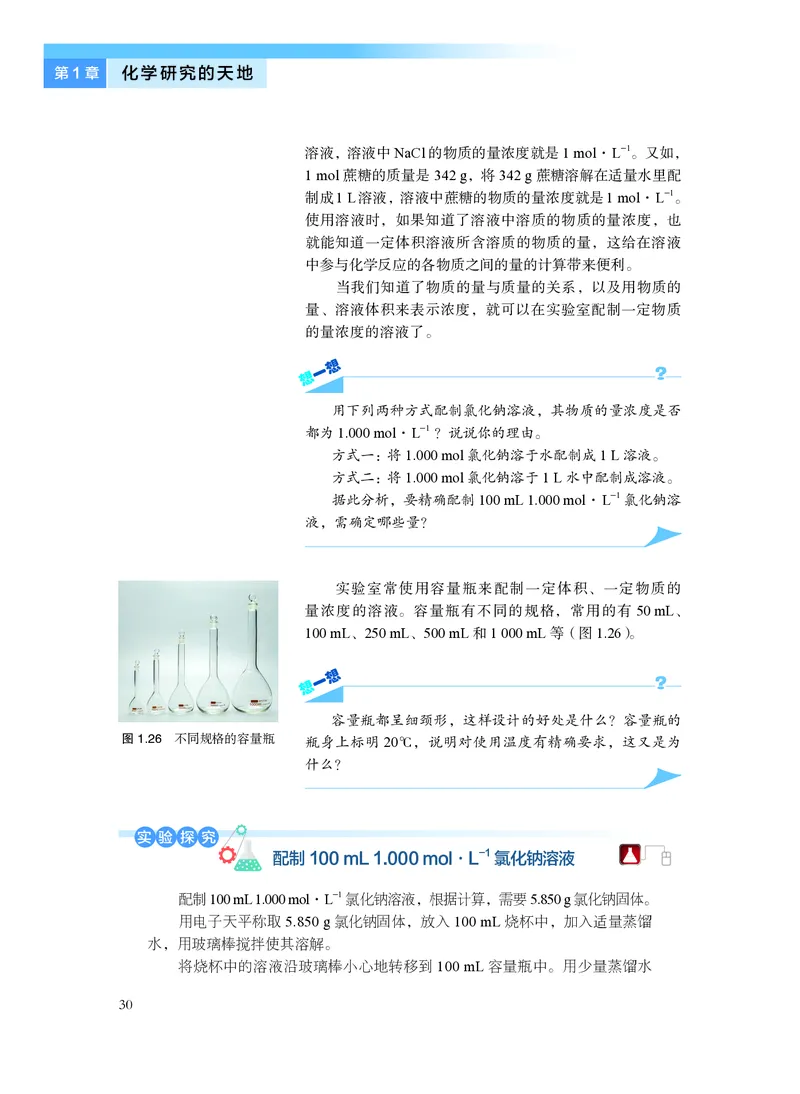
有一份样品,可能是下列物质中的一种或几种:CuSO4、BaSO4、FeCl3、KOH、
NaCl、CaCO3。对该样品进行初步测试后,得出如图1.24 所示的结果。分析该白色粉末
是什么物质。说一说你的理由。
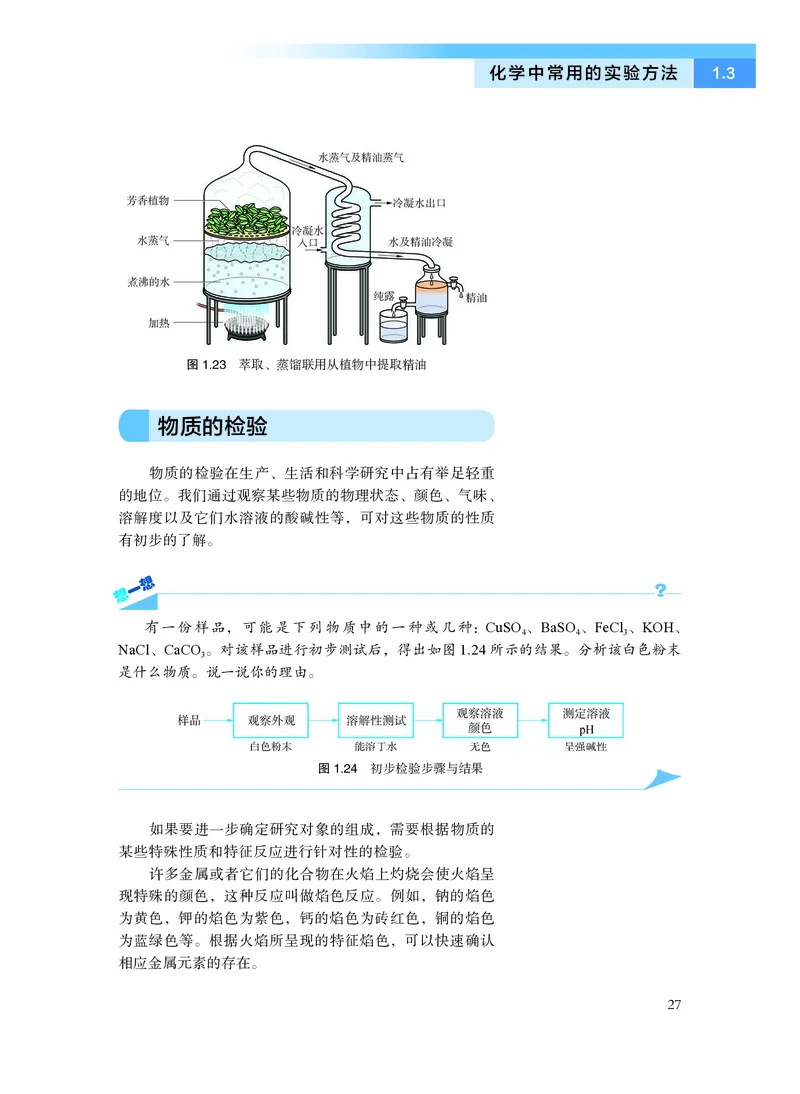
图1.23 萃取、蒸馏联用从植物中提取精油
物质的检验在生产、生活和科学研究中占有举足轻重
的地位。我们通过观察某些物质的物理状态、颜色、气味、
溶解度以及它们水溶液的酸碱性等,可对这些物质的性质
有初步的了解。
物质的检验
图1.24 初步检验步骤与结果
如果要进一步确定研究对象的组成,需要根据物质的
某些特殊性质和特征反应进行针对性的检验。
许多金属或者它们的化合物在火焰上灼烧会使火焰呈
现特殊的颜色,这种反应叫做焰色反应。例如,钠的焰色
为黄色,钾的焰色为紫色,钙的焰色为砖红色,铜的焰色
为蓝绿色等。根据火焰所呈现的特征焰色,可以快速确认
相应金属元素的存在。
想一想
28
化学研究的天地
第1 章
当含钾的物质中同时含有钠元素时,钠的焰色会掩盖
钾的焰色,此时应透过蓝色钴玻璃进行观察,钴玻璃可以
滤去黄光,从而去除钠的干扰。
使特定组分发生化学反应,产生特征颜色,这种方法
称为显色法。例如用酸碱指示剂、pH 试纸等检测溶液的酸
碱性,用淀粉溶液检测碘单质等。
通过加入某种试剂,观察是否有沉淀产生,来判断物
质中所含的组分,这种方法称为沉淀法。例如,向溶液中
加入酸化的硝酸银溶液,观察是否有不溶于稀硝酸的白色
沉淀生成,以检验溶液中的氯离子;向溶液中依次加入稀
盐酸与氯化钡溶液,观察是否有白色沉淀生成,以检验溶
液中的硫酸根离子。
我们也可以通过加入某种试剂,将待测物质转化为易于
鉴别的气体,这种方法称为气体法。例如,向某物质中滴加
盐酸,若产生无色无味并能使澄清石灰水变浑浊的气体,则
可推测该物质中存在碳酸根离子、碳酸氢根离子中的一种或
两种。
图1.25 几种金属元素焰色反应的颜色
以氯化钠、硫酸铵、碳酸钾为例,写出上述检验氯
离子、硫酸根离子以及碳酸根离子时发生反应的化学方
程式。
书写表达
古籍中记载的焰色反应
南北朝时期陶弘景所著
的《本草经集注》中记载“以
火烧之,紫青烟起,云是真
硝石也”。说明人们很早就知
道用焰色反应鉴别硝石(硝
酸钾)。
资料库
鉴别和鉴定有区别吗?有三份纯净样品,分别是KCl、
Na2CO3 和K2SO4,如何设计实验方案进行鉴定?
想一想
Li
Na
K
Ca
Sr
Ba
Cu
29
1.3
化学中常用的实验方法
仪器分析是化学学科的一个重要分支,它是利用某些现代仪器设备,测量
物质的物理或化学性质的参数及其变化来获取物质组成、含量及结构等信息的学
科。仪器分析相较于传统的化学分析,具有灵敏度高、快速、简便等特点。例如,
元素分析仪能够对物质中C、H、N、S 等元素进行定量分析测定;通过核磁共振
分析可以了解特定原子的化学环境、原子个数等;质谱分析技术能够测量化学物
质,特别是某些生物大分子的相对分子质量;色谱及其联用技术能够进行广泛的
高效分离分析测试等。随着科学技术不断进步,仪器分析正朝着智能化、实时跟
踪、微型化、非破坏性检测、遥测等方向迅速发展。
仪器分析
链接学科
化学学科的发展经历了从定性到定量的过程。在实验
室中,有许多计量仪器,如电子天平、量筒、温度计等。
学会正确使用这些计量仪器,是定量分析实验的重要基础。
在生产和科学实验中,我们经常用到一定浓度的溶液。
一般情况下,我们取用溶液时不会去称量它的质量,而是
会量取它的体积。同时,物质在进行化学反应时,反应物
的物质的量之间存在一定的比例关系。所以,知道一定体
积的溶液中所含溶质的物质的量,对于生产和科学实验十
分重要。在化学研究中,物质的量浓度是使用最广泛的一
种表示溶液浓度的方法。
用每升溶液中所含溶质B
①的物质的量表示的浓度称为
溶质B 的物质的量浓度,符号为cB,常用的单位是mol·L
—1。
溶液中溶质B 的物质的量浓度(cB)、溶质B 的物质
的量(nB)与溶液的体积(V)之间存在以下关系:
nB
V
cB =
若1 L 溶液中含有1 mol 溶质B,这种溶液中溶质B
的物质的量浓度就是1 mol·L
—1。如NaCl 的摩尔质量是
58.5 g·mol
—1,将58.5 g NaCl 溶解在适量水里配制成1 L
配制一定物质的量浓度的溶液
① B 表示某种溶质。
30
化学研究的天地
第1 章
用下列两种方式配制氯化钠溶液,其物质的量浓度是否
都为1.000 mol·L
—1 ?说说你的理由。
方式一:将1.000 mol 氯化钠溶于水配制成1 L 溶液。
方式二:将1.000 mol 氯化钠溶于1 L 水中配制成溶液。
据此分析,要精确配制100 mL 1.000 mol·L
—1 氯化钠溶
液,需确定哪些量?
实验室常使用容量瓶来配制一定体积、一定物质的
量浓度的溶液。容量瓶有不同的规格,常用的有50 mL、
100 mL、250 mL、500 mL 和1 000 mL 等(图1.26)。
图1.26 不同规格的容量瓶
容量瓶都呈细颈形,这样设计的好处是什么?容量瓶的
瓶身上标明20℃,说明对使用温度有精确要求,这又是为
什么?
配制100 mL 1.000 mol·L
—1 氯化钠溶液,根据计算,需要5.850 g 氯化钠固体。
用电子天平称取5.850 g 氯化钠固体,放入100 mL 烧杯中,加入适量蒸馏
水,用玻璃棒搅拌使其溶解。
将烧杯中的溶液沿玻璃棒小心地转移到100 mL 容量瓶中。用少量蒸馏水
实验探究
配制100 mL 1.000 mol·L
-1 氯化钠溶液
溶液,溶液中NaCl 的物质的量浓度就是1 mol·L
—1。又如,
1 mol 蔗糖的质量是342 g,将342 g 蔗糖溶解在适量水里配
制成1 L溶液,溶液中蔗糖的物质的量浓度就是1 mol·L
—1。
使用溶液时,如果知道了溶液中溶质的物质的量浓度,也
就能知道一定体积溶液所含溶质的物质的量,这给在溶液
中参与化学反应的各物质之间的量的计算带来便利。
当我们知道了物质的量与质量的关系,以及用物质的
量、溶液体积来表示浓度,就可以在实验室配制一定物质
的量浓度的溶液了。
想一想
想一想
31
1.3
化学中常用的实验方法
根据实验操作步骤,思考下列问题。
(1) 为什么要用蒸馏水洗涤烧杯内壁?为何要将洗涤液
全部转移到容量瓶中?
(2) 用胶头滴管滴加蒸馏水时如果液面超过了刻度线,
所配制溶液的实际浓度比要求浓度高还是低?此时该怎
么办?
图1.27 配制一定物质的量浓度的溶液示意图
除了用固体配制一定浓度的溶液外,在实验室中我们
还常常需要将浓溶液稀释成不同浓度的稀溶液。
在溶液稀释的过程中,虽然溶液的体积发生了变化,
但溶质的物质的量保持不变,因此稀释前后的溶液的物质
的量浓度和体积之间满足以下关系:
c1V1 = c2V2
式中c1、V1 表示稀释前溶液的物质的量浓度和体积;c2、
V2 表示稀释后的物质的量浓度和体积。
洗涤烧杯内壁及玻璃棒2 ~3 次,将洗涤液全部转移到容量瓶中。轻轻摇动容
量瓶,使溶液混合均匀。
然后,将蒸馏水缓慢注入容量瓶,直至液面位于容量瓶颈刻度线下
1 ~2 cm 时,改用胶头滴管滴加蒸馏水至溶液的凹液面底部与刻度线相切。将
容量瓶用瓶塞盖好,上下颠倒几次,摇匀。
这样配制得到的溶液就是100 mL 1.000 mol·L
—1 氯化钠溶液,配制过程
如图1.27 所示。
称量
溶解
转移
定容
摇匀
想一想
32
化学研究的天地
第1 章
● 不同温度下,某固体X 在三种溶剂中的溶解度变化如图1.28 所示。
哪一种溶剂更适宜用冷却结晶来提纯X ?说明理由。
● 若采用冷却结晶的方式使被提纯物质析出,而使杂质留在溶液中,
则被提纯物质在溶剂中的溶解度应随温度有明显变化。即高温时,
溶解度较大,而低温时溶解度较小。从溶解度曲线来看,溶剂A
较为适宜。
学习指南
例题导引
问题:
分析:
图1.28 固体X 在三种溶剂中的溶解度变化曲线
练习巩固
1. 下列混合物可用分液漏斗来分离的是( )。
(A) 泥水
(B) 酒精和水
(C) 植物油和水
(D) 氢氧化铁胶体
2. 能够用于鉴别氯化钡、氯化钠、碳酸钠三种物质的试剂是( )。
(A) 硝酸银溶液
(B) 稀硫酸
(C) 氢氧化钾溶液
(D) 氢氧化钠溶液
3. 瓶装水是我们生活中常见的商品,以下是某500 mL 瓶装水中矿物质成
分表:
(1) 已知该500 mL瓶装水提供的钙(以Ca
2+计)相当于成人每天参考摄
入量的4%,请估算成人每天钙的参考摄入量(以mg 为单位)。
(2) 若用物质的量浓度来表示矿物质的浓度,请重新绘制该瓶装水的成分表。
成分
钙
镁
硅
碳酸氢盐
硫酸盐
氯化物
硝酸盐(以N计)
含量/(mg·L
—1)78
24
14
357
10
4
1
33
1.3
化学中常用的实验方法
物质
NaNO2
NaCl
溶解度(293 K)
[g·(100 g H2O)
—1]
67
36
熔点/℃
271
801
沸点
320℃分解
1 465℃
水溶液的酸碱性
碱性
中性
4. 判断下列分离方法是否正确,正确画“√”,错误画“×”。
(1) 用过滤的方法分离出糖水中的糖
□
(2) 利用分液的方法分离碘酒中的溶质和溶剂
□
(3) 用蒸馏法分离正丁醇(沸点为117.5℃)和乙醚(沸点为34.6℃)
□
(4) 利用重结晶的方法除去硝酸钾中混有的少量氯化钾
□
5. 亚硝酸钠(NaNO2)是一种工业用盐,外观像食盐,具有咸味,却是有
毒物质,误食会给食用者的健康带来极大的危害。根据下表中的信息,并结合
已学知识,设计不同的方法鉴别食盐和亚硝酸钠。
34
化学研究的天地
第1 章
素养提升
■ 根据不同的分类依据,对物质进行分类;从不同视角和层次来认识物质的多样性。
■ 从宏观与微观层面了解物质的量及其相关物理量的含义,基于物质的量理解物质
组成及其化学变化,认识物质的量在定量研究中的重要价值和作用。
■ 根据反应原理等选取实验装置来制备物质;根据物质性质的差异来选择物质分离
的实验方法;根据物质的特征反应等选取适当的试剂进行鉴别或鉴定;观察物质
及其变化的现象,客观地进行记录,对现象作出合理解释,发现和提出有探究价
值的问题;从问题和假设出发,依据探究目的,设计探究方案,运用实验、调查
等方法进行实验探究。
■ 具有安全意识和严谨求实的科学态度;列举事实说明化学对推动社会发展与科学
进步的重要作用;认识化学对创造物质财富和精神财富、满足人们日益增长的美
好生活需要所做的重大贡献。
本章复习
核心框图
34
35
1.3
化学中常用的实验方法
35
35
35
练习巩固
1. 下列关于物质聚集状态的说法正确的是( )。
(A) 气体有固定的形状和体积
(B) 固体、液体不易被压缩的原因是构成的微粒直径太大
(C) 影响物质聚集状态的外界因素主要是温度
(D) 不同聚集状态的物质其内部微粒之间的平均距离、作用力和运动方式各不相同
2. 有相同氧原子数目的Fe3O4 和Fe2O3,它们的物质的量之比为( )。
(A) 3 ∶ 4
(B) 4 ∶ 3
(C) 2 ∶ 3
(D) 2 ∶ 1
3. a L 碳酸钠溶液中,含有b mol 钠离子,则此溶液的物质的量浓度是( )。
(A)
b
a mol·L
—1
(B)
2a
b mol·L
—1
(C) b
2a mol·L
—1
(D)
a
b mol·L
—1
4. 下列混合物中,可用“溶解→过滤→蒸发”操作进行分离的是( )。
(A) 混有泥沙的食盐
(B) 混有水的酒精
(C) 白糖与食盐的混合物
(D) 铁粉与泥沙的混合物
5. 实验室需要配制0.100 0 mol·L
—1 氢氧化钠溶液 100 mL,现有2.000 mol·L
—1
氢氧化钠溶液。计算:
(1)所需2.000 mol·L
—1 氢氧化钠溶液的体积。
(2)完全中和上述配制的溶液,需要1.000 mol·L
—1 盐酸的体积。
6. 脱硫是防治大气中SO2 污染的主要技术措施。一种脱硫措施是在燃煤中加入一定
量的石灰石混烧,最终硫以硫酸钙的形式存在于灰渣中。
(1)若燃煤中硫含量为3.2%(质量分数),采用质量分数为80% 的石灰石处理
1 000 kg 这种煤,可生成CaSO4·2H2O 多少千克?
(2)为保证更好地脱硫,石灰石需过量,常采用钙硫比[n(Ca) / n(S)]为2.2 ∶ 1
的配比,则此时处理上述煤,需质量分数为80% 的石灰石多少千克?
*7. 阅读短文,思考下列问题。
An atom is a body which cannot be cut in two. A molecule is the smallest possible portion
of a particular substance. No one has ever seen or handled a single molecule. Molecular
science, therefore, is one of those branches of study which deal with things invisible and
imperceptible by our senses, and which cannot be subjected to direct experiment.
The mind of man has perplexed itself with many hard questions. Is space infinite, and
if so in what sense? Is the material world infinite in extent, and are all places within that
extent equally full of matter? Do atoms exist, or is matter infinitely divisible?
The discussion of questions of this kind has been going on ever since men began
to reason, and to each of us, as soon as we obtain the use of our faculties, the same old
36
化学研究的天地
第1 章
36
question arise as fresh as ever. They form as essential a part of the science of the nineteenth
century of our era, as of that of the fifth century before it.
Thus far we have been considering molecular science as an inquiry into natural
phenomena. ... The study of molecules has developed a method of its own, and it has also
opened up new views of nature.
(短文取自:Molecules[J]. Nature, 1873, 8: 437 ~441.)
(1)The excerpts above are from “Molecules” by J.C.Maxwell. Do you still hold
the belief that molecular science is one of those branches of study which deal with things
invisible and imperceptible by our senses?
(2)The subject of chemistry deals with study and creation of substances primarily at
a molecular scale. What can you learn from this short passage?
体验· 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和
体会制作成海报、演示文稿,进行分享和交流。
傅鹰(1902—1979)是中国化学家,中国胶体与表面科
学的主要奠基人,他在表面化学吸附理论方面的研究工
作受到国内外学术界的重视。他对化学实验非常重视,
曾说过:“化学是实验的科学,实验是最高法庭。”他还
教导学生手脑并用,仔细观察并分析每一个实验现象。
卢嘉锡(1915—2001)是中国化学家,他提出了固氮
酶活性中心网兜状原子簇结构“福州模型Ⅰ”等,使我
国化学模拟生物固氮及有关原子簇化合物的合成和结构
化学研究跻身世界前列。他曾说过:“化学家的元素组
成应当是C3H3。”这里的C 和H 不是指碳和氢,而是指
Clear Head、Clever Hands、Clean Habit,尤其后两项就
是指做化学实验应具备的基本素质。
请你结合傅鹰和卢嘉锡的观点和自身实验经历,对实验
者的基本素养和态度谈谈你的认识和体会。
纳米科技是21 世纪科技发展的热点领域之一。我们可
开展系列活动:如制备AgI 和Fe(OH)3 溶胶、制取自清
洁剂和多孔铝硅酸盐催化剂、磁珠法提取洋葱细胞中的
DNA 等。通过上述活动,探寻纳米界面的秘密和纳米材
料的性能,体会纳米科技可以造福人类,也辩证地看待
纳米尺度的物质的潜在风险。
图1.30 卢嘉锡
图1.29 傅鹰
37
1.3
化学中常用的实验方法
37
37
37
上海市崇明区位于长江入海口,由崇明、长兴、横沙三岛组成,其中崇明岛是
世界上最大的河口冲积岛。有关资料显示,崇明岛1950 年的面积约为600 km
2,
而现在的面积已扩展至约1 200 km
2。请同学们利用课余时间,查阅相关文献并
走访相关部门,了解并记录崇明岛土地的变化情况,运用所学习的化学、地理
等知识加以解释。
标准状况下的气体摩尔体积约为22.4 L·mol
—1,用纸板等材料搭建一个体积是
22.4 L 的立方体,感受标准状况下1 mol 气体的体积。
我们在做化学实验时,必须遵守一定的规则,在搭建实验装置、投料和拆除实
验装置时同样也要遵守一定的规范,请结合初中阶段的实验,总结搭建实验装
置、投料和拆除实验装置时的注意事项。
注:教材中打“*”号的练习题供有兴趣的同学完成。
38
我们知道,1 mol 气体的质量各不相同,而1 mol 任何气体的体积在同温同压下是大
致相等的,在273 K 和101 kPa 时约为22.4 L。如何来测定一定条件下气体摩尔体积这
一常数呢?
活动目标
(1) 明确测定一定温度和压强下气体摩尔体积的方法。
(2) 学会测定1 mol 气体体积的实验操作。
(3) 知道实验误差的形成和实验相对偏差的计算。
活动指导
(1) 原理分析
镁与稀硫酸反应生成氢气。称取质量为m g 的镁与酸完全反应,通过反应物和生成
物物质的量之间的关系,可以得到氢气的物质的量。
生成的氢气可用排水法收集在有刻度的容器中,并以此来测得其体积V(H2),所以
1 mol 氢气的体积为:
1 mol 氢气的体积=
×M(Mg)
=
=
V(H2)
n(H2)
V(H2)
n(Mg)
V(H2)
m(Mg)
(2) 装置设计
图1.31 是一种对化学反应中产生的气体进行体积测定的装置。该装置由Y 形管、
量气管和水准管组成。量气管和水准管的底部用稍长的橡皮管连接,Y 形管与量气管直
接连接,用水准管来调节液面的高度。
① 按图1.31 所示,装配好化学反应气体体积测定装置,并做如下气密性检查:从
与大气相通的水准管注入水,待水准管和量气管内液体高度相平后,停止注水。连接装
置,将水准管放低,静置一会儿,若两边高度差没有变化,则说明装置的气密性良好。
② 取下Y 形管,将25 mL 的量气管和水准管错开一定高度固定在滴定管夹上,其
中量气管尽量低些,水准管尽量高些。从水准管口注入一定量的水至量气管中水的液面
在0 至1.00 mL 刻度之间。
③ 用量筒量取约5 mL 1 mol·L
—1 硫酸,小心地倒入Y 形管的一个支管中。
④ 用砂纸擦去镁带表面的氧化物,在电子天平上称取0.015 0 ~0.025 0 g 镁带(精
项目学习活动
如何测定气体摩尔体积
39
确至0.000 1 g),将数值准确记录于实验记录表格中。用镊子将已称量的镁带加入另一
支管中。
⑤ 将Y 形管与装置连接,调节水准管使两边液面相平,液面在0 至1.00 mL 刻度
之间,读取量气管内液面刻度数值(精确至0.01 mL),记为初读数V1。
⑥ 倾斜Y 形管,使硫酸全部流入镁带的支管中进行反应。待反应结束后冷却至室温,
调节水准管使两边液面相平,读取量气管内液面刻度数值,记为终读数V2。
重复上述操作进行多次实验,并将每次实验计算所得的氢气体积填入下表。
大气压强:
kPa 实验温度:
K
实验
次数
镁带质量/g
氢气体积
1 mol 氢气
体积/L
初读数V1/mL
终读数V2/mL
ΔV/mL
1
2
3
图1.31 化学反应气体体积测定装置
(3) 确定一定温度和压强条件下1 mol 气体体积的参考值
一定量气体在不同温度、压强下的体积存在如下关系:
p0V0
T0
p1V1
T1
=
我们知道,在标准状况下(273 K,101 kPa),1 mol 任何气体的体积都约为22.4 L,
所以在通常状况下(298 K,101 kPa),1 mol 氢气体积可换算如下:
V (H2) ≈ 24.5(L)
101×22.4
273
101 V(H2)
298
=
镁带
稀硫酸
40
(4) 实验偏差的原因分析
测量过程都会产生一定的误差,误差始终存在于科学实验和测量的结果之中。误
差是测量值与真值之差,通常真值只是一个理想的概念,一般是无法得到的,通常用
一个参考值来代替。所以在化学测量中,我们在分析测量的误差时,对于有限次数的
测量常采用计算偏差的方法来进行。
绝对偏差是指测量值减去它的参考值,参考值往往也可以用测量值的算术平均值来
代替。相对偏差是指绝对偏差在参考值或算术平均值中所占的百分率。
相对偏差=
×100%
测量值 — 参考值
参考值
通过分析可以知道,实验偏差有的来自仪器装置自身或试剂的品质,有的来自操作
的不当。定量测定的偏差允许在一个范围内存在。
我们的测定结果如果与参考值偏差很大,那就应在实验装置、所用试剂的纯度及操
作上寻找原因。例如,装置漏气会造成氢气体积减小,使测定结果偏小。又如反应放热,
氢气的温度高于室温,气体体积增大,使结果偏大。
你的“一定条件下气体摩尔体积的测定”实验结果如何,是否在允许的偏差范围内?
回顾自己的实验过程,分析产生误差的可能原因。
活动要求
完成你的项目活动,并形成一份项目报告。在报告中介绍你的装置、操作步骤,记
录并分析数据,简单分析偏差,思考整个项目活动的心得。
活动反思
(1) 由于实验是在水溶液中进行,而且氢气是通过排水法测量的,因此氢气中会混
有水蒸气,理论上计算氢气体积时应扣除饱和水蒸气的体积,如何消除水的饱和蒸气压
对实验的影响呢?
(2) 根据铝的性质,以“检测铝质易拉罐中金属铝的含量”为课题设计实验方案,
并展开研究。(建议:实验方案中包括实验原理、实验用品、实验步骤、数据记录与处
理等部分)
海洋中的卤素资源
堆放在巨大穹顶式盐
仓里的食盐,是上海氯碱
化工股份有限公司用来生
产烧碱、盐酸,以及聚氯
乙烯等产品的重要原料。
第2 章
41
海水中的氯
氧化还原反应和离子反应
溴和碘的提取
2.1
2.2
2.3
42
离子膜电解法的工业装置
从
太空遥望,地球是一颗蓝色星球,浩瀚的海洋覆盖了70%
以上的地球表面。海洋可谓地球的“聚宝盆”,蕴藏着极为
丰富的化学资源,如海水中就有80 多种元素,氯化物的含量很高。
氯和氟、溴、碘、砹总称为卤族元素,又称卤素。
氯、溴、碘等均可通过开发海洋资源获得。我们将通过学习卤
素单质及其化合物的性质,初步了解元素化学的学习方法,以及氧
化还原反应和离子反应等化学理论。通过学习海洋中卤素资源的开发
利用,了解从自然资源中提取物质的基本思路,感悟化学在合理绿
色地利用自然资源中的重要作用,以及化学与技术、社会、环境之
间的关系。
海水中的氯
43
2.1
身边的有机化合物
第7 章
古代我国的沿海居民就开始了海滩晒盐的生产实践活动,
汉末《说文解字》中有记载:“古者宿沙初作煮海盐。”明末科
学家宋应星(1587—约1666)的《天工开物》中设篇目“海
水盐”,详细记载了海盐的生产过程。把海水引入盐田,利用
日光、风力来蒸发浓缩海水,并进一步使食盐结晶出来,这
种方法叫做盐田法。
粗盐提纯
海水中含有大量的盐,故密度较大、味道咸涩。海水
中所含的盐大部分是氯化钠,氯化钠是生活中和人体内不
可或缺的,也被用来生产氯气以及各种含氯和含钠的制品,
为人们的日常生活和化学工业提供重要的原料。
学会用化学沉淀法进行粗盐
提纯
知道电解饱和食盐水的简单
原理
了解氯气的化学性质及其应用
了解重要含氯化合物的性质及
其应用
学习聚焦
知识回放
● 海水晒盐
● 蒸发结晶
● 电解水
2.1
海水中的氯
通常粗盐中氯化钠含量约为80% ~90%,还有MgCl2、
MgSO4、CaSO4、NaBr 等一些其他的盐以及泥沙等难
溶性物质。粗盐中的难溶性杂质可以通过过滤除去,而
Ca
2+、Mg
2+、SO
2—
4 等可溶性杂质,可通过加入某些化学物
质使其生成沉淀后再过滤除去。除去杂质后的氯化钠纯度
较高,常称为精盐。
图2.1 《天工开物》中制
海盐图①
图2.2 现代盐田的生产场景
机械化收盐
春盐装车
① 上海图书馆藏喜咏轩丛书本。
44
海洋中的卤素资源
第2 章
实验探究
粗盐的提纯
实验探究
电解饱和食盐水
根据附录Ⅰ中列出的部分物质在水中的溶解性,思考加入哪些试剂能除去
粗盐中Ca
2+、Mg
2+、SO
2—
4 等杂质离子?除杂过程中,试剂加入的先后顺序、
每种试剂加入的量是否会影响除杂效果?请根据思考结果,设计出粗盐提纯
的实验方案。
粗盐的提纯
实验目的:通过化学沉淀法去除粗盐中的杂质离子,巩固物质
分离提纯的实验原理和基本操作。
实验原理:
实验用品:
实验步骤:
数据处理与实验结果:
问题与讨论:
从海水晒盐到粗盐提纯,海水中的氯化钠被提取和纯
化了。那么,精盐中的氯又是如何转化为氯单质及含氯化
合物的呢?19 世纪以后,科学家通过电解饱和食盐水制取
了氯气,并实现了工业化生产。
电解饱和食盐水
在图2.3 所示装置中注入饱和食盐水,并在两边各滴入几滴酚酞试液。以
两个石墨棒作电极,分别与电源的正、负极相连。U 形管的阳极(与电源正极
相连)处支管用三通阀分别连接针筒和导气管,导气管出口没入淀粉碘化钾溶
液;U 形管的阴极(与电源负极相连)处支管与针头相连。接通电源后,观察
实验现象。
通电后注意适当抽动注射器调整液面高度,并观察注射器内收集到的气体
颜色。打开阳极连接的阀门,将阳极产生的气体通入淀粉碘化钾溶液;在针尖
处点燃气体。
现象记录:
。
实验结论:
。
海水中的氯
45
2.1
图2.3 电解饱和食盐水装置及电解后实验现象
电解饱和食盐水的化学方程式为:
2NaCl + 2H2O
2NaOH + H2↑ + Cl2↑
通直流电
电解饱和食盐水时,阳极上产生氯气,阴极上产生氢
气,电解后还有氢氧化钠生成。
用电解饱和食盐水的方法制备氯气、氢气和烧碱,并
以它们为原料生产一系列含氯、含钠化工产品的工业称为
氯碱工业。
电解食盐水的电极反应式
阳极的电极反应式:
2Cl
— — 2e
—
Cl2
阴极的电极反应式:
2H2O + 2e
—
H2 + 2OH
—
资料库
吴蕴初和中国氯碱工业
吴蕴初(1891— 1953),原名吴葆元,我国化
工实业家。1923 年吴蕴初出任上海天厨味精厂厂长,
该厂所产佛手牌味精大获成功,由此他成为闻名遐迩
的“味精大王”。当时国内生产味精所需的主要化工
原料—盐酸,一直依赖进口。吴蕴初带领技术人员
经过艰难探索,研发了通过电解食盐水生产盐酸、烧
碱和漂白粉的工艺,并创办了天原电化厂,后改名为
天原化工厂。随着天原的成功,吴蕴初又先后开办了
天盛陶器、天利氮气等天字号化工企业,为振兴民族
工业做出了卓越贡献。
化学史话
图2.4 吴蕴初
46
海洋中的卤素资源
第2 章
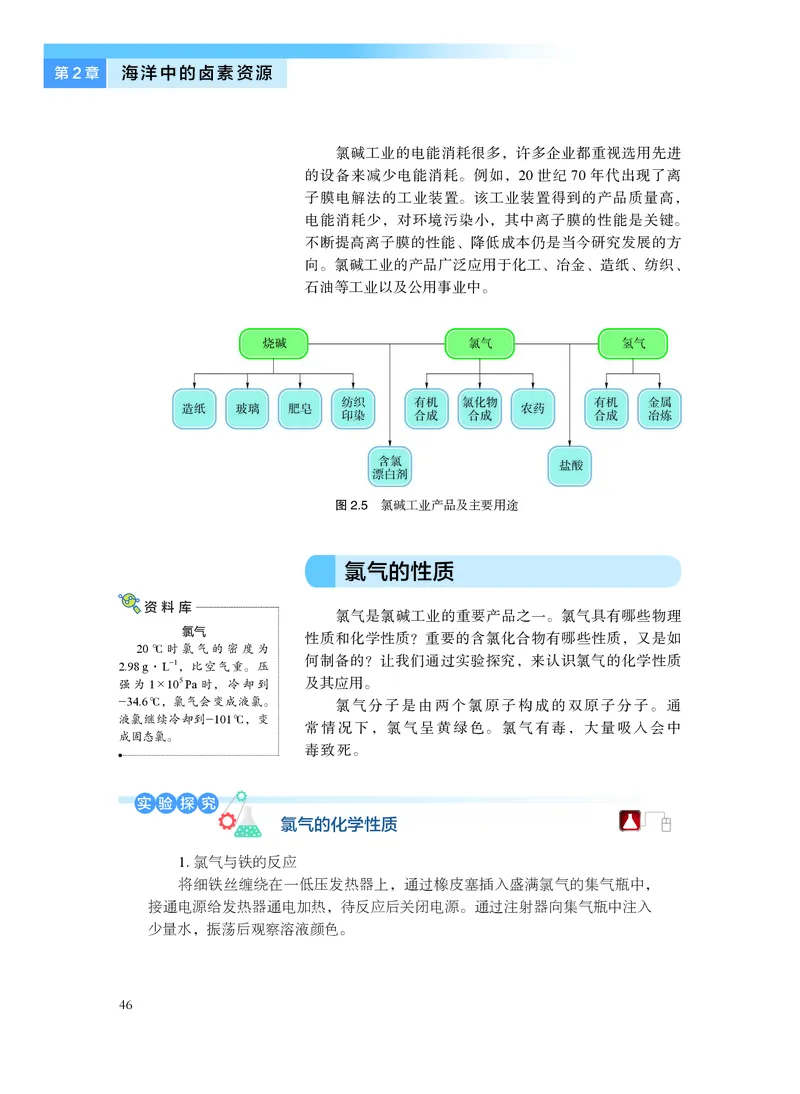
氯碱工业的电能消耗很多,许多企业都重视选用先进
的设备来减少电能消耗。例如,20 世纪70 年代出现了离
子膜电解法的工业装置。该工业装置得到的产品质量高,
电能消耗少,对环境污染小,其中离子膜的性能是关键。
不断提高离子膜的性能、降低成本仍是当今研究发展的方
向。氯碱工业的产品广泛应用于化工、冶金、造纸、纺织、
石油等工业以及公用事业中。
图2.5 氯碱工业产品及主要用途
氯气是氯碱工业的重要产品之一。氯气具有哪些物理
性质和化学性质?重要的含氯化合物有哪些性质,又是如
何制备的?让我们通过实验探究,来认识氯气的化学性质
及其应用。
氯气分子是由两个氯原子构成的双原子分子。通
常情况下,氯气呈黄绿色。氯气有毒,大量吸入会中
毒致死。
氯气的性质
实验探究
氯气的化学性质
1. 氯气与铁的反应
将细铁丝缠绕在一低压发热器上,通过橡皮塞插入盛满氯气的集气瓶中,
接通电源给发热器通电加热,待反应后关闭电源。通过注射器向集气瓶中注入
少量水,振荡后观察溶液颜色。
氯气
20 ℃时氯气的密度为
2.98 g·L
—1,比空气重。压
强为1×10
5 Pa 时,冷却到
—34.6℃,氯气会变成液氯。
液氯继续冷却到—101℃,变
成固态氯。
资料库
海水中的氯
47
2.1
图2.6 铁丝在氯气中燃烧
图2.7 氢气在氯气中燃烧
氢气在氯气中燃烧
滴入紫色石蕊试液
2. 氯气与氢气的反应
实验室制备氢气,验纯后点燃纯净的氢气,然后将导管伸入盛满氯气的集
气瓶中,观察现象。片刻后熄灭火焰,向集气瓶内注入少量蒸馏水,再滴入几
滴紫色石蕊试液后观察现象。
3. 氯气与水的反应
用50 mL 注射器收集40 mL 氯气,注射器通过阀门与针头连接。打开阀
门吸入10 mL 蒸馏水后关闭,充分振荡后静置,观察现象。在试管中加入约
2 mL 紫色石蕊试液,将注射器内溶液小心地注射到试管中,观察现象。
图2.8 氯气的溶解性及氯水的酸性
石蕊试液变红
40 mL 氯气
20 mL 氯气溶于水
氯气与铁丝
铁丝在氯气中燃烧
反应后加入水
48
海洋中的卤素资源
第2 章
4. 氯气与氢氧化钠的反应
用50 mL 注射器收集40 mL 氯气,注射器通过阀门与针头连接。打开阀
门吸入10 mL 氢氧化钠溶液后关闭,充分振荡后静置,观察现象。
编号
现象记录
现象分析
1
2
3
4
实验表明,氯气的化学性质很活泼,可以与许多物质
发生反应。
氯气除了与铁反应生成氯化铁之外,还能与大多数金属
单质直接化合,生成金属氯化物。例如,金属钠、铜等都能
在氯气中燃烧。
氯气也能与许多非金属单质化合。例如,氢气在氯气中
燃烧生成氯化氢;氯气和氢气的混合气体受到强光照射,两者
迅速化合,放出大量的热,发生爆炸,也生成氯化氢气体。
氯化氢是有刺激性气味的无色气体,极易溶于水。工
业上常用氯气在氢气中燃烧(图2.9)来制备氯化氢,氯化
氢溶于水后得到的溶液就是盐酸。
2Fe + 3Cl2
2FeCl3
2Na + Cl2
2NaCl
Cu + Cl2
CuCl2
点燃
点燃
点燃
点燃或光照
H2 + Cl2
2HCl
实验探究
探究氯气与水反应
取两个集气瓶,用排气法收集干燥的氯气至满。向两个集气瓶中分别放入
干燥的有色纸条和湿润的有色纸条(或有色布条),观察现象并推断结论。
图2.9
工业上氯气在氢气中
燃烧时火焰呈苍白色
海水中的氯
49
2.1
图2.10 氯气与水反应生成漂白性物质
氯气使湿润的红纸条褪色
氯气不能使干燥的红纸条褪色
现象记录:____________________________________________________。
实验结论:____________________________________________________。
实验表明,氯气不能使干燥的有色纸条褪色,但可以
使湿润的有色纸条褪色,说明使有色纸条褪色的应该是氯
气与水反应后产生的新物质,这种物质就是次氯酸。
氯气可以溶解在水中,所得溶液称为氯水。常温下,
1 体积水能溶解约2 体积氯气,氯水中的部分氯气能与水
发生反应,生成盐酸和次氯酸(HClO)。
Cl2 + H2O
HCl + HClO
Cl2 + 2NaOH
NaCl + NaClO + H2O
氯气可与氢氧化钠溶液发生反应,生成氯化钠、次氯
酸钠和水。
可逆反应
通常人们把朝生成物方
向进行的反应叫做正反应,
朝反应物方向进行的反应叫
做逆反应。常温时,氯气与水
发生正反应的同时还有逆反
应发生,这种反应叫做可逆
反应。在化学方程式里,用
“
”代替“
”来表
示可逆反应。
资料库
实验室里,为避免使用氯气时存在的安全隐患,在处
理尾气中的剩余氯气时应采用什么安全措施?
次氯酸和次氯酸盐
次氯酸和次氯酸盐都是重要的含氯化合物。
次氯酸是一种很弱的酸,具有强氧化性,能杀死水中
想一想
50
海洋中的卤素资源
第2 章
次氯酸盐一般是用氯气与碱反应得到的。由于次氯酸盐
比次氯酸稳定,因此更容易保存。工业中,用氯气与氢氧化
钠生产次氯酸钠,用氯气与消石灰制成漂白粉,这些制品常
用作漂白剂和消毒剂。
光照
2HClO
2HCl + O2↑
2Cl2 + 2Ca(OH)2
CaCl2 + Ca(ClO)2 + 2H2O
漂白粉是次氯酸钙、氯化钙、氢氧化钙等所组成的混
合物(有效成分是次氯酸钙),被广泛地用作饮用水、污
水、排泄物及环境的消毒剂,也可用于游泳池等公共场所
的消毒。如果漂白粉遇酸性溶液或露置在空气中,其中的
次氯酸钙会与酸或与水蒸气和二氧化碳发生反应,生成稳
定性差的次氯酸,从而使漂白粉失效,因此漂白粉应密封
保存。
Ca(ClO)2 + 2HCl
CaCl2 + 2HClO
Ca(ClO)2 + CO2 + H2O
CaCO3 + 2HClO
拓展视野
用氯气进行饮用水消毒时,水中的有机化合物会与氯气发生反应,生成含氯
有机化合物,这种有机化合物中的氯会在人体内积留产生慢性累积中毒,还会诱发
癌症。因此,人们研究并开发了新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。
二氧化氯是一种有刺激性气味的黄绿色气体,1 L 水中约能溶解2.9 g 二氧
化氯。它在水中的杀菌消毒能力强,持效久,受水体pH 变化的影响小,一般无
副作用。除用于杀菌消毒之外,还用于环保、灭藻、漂白、保鲜、除臭等。世界
卫生组织和联合国粮食及农业组织将二氧化氯列为安全高效消毒剂。
新一代绿色消毒剂——二氧化氯
有效氯
漂白粉的效能是以有效
氯的含量来衡量的。有效氯
是指漂白粉与浓盐酸反应生
成氯气的质量与漂白粉质量
之比。工业生产的漂白粉,
有效氯一般约为35%。漂粉
精是用氯气与氢氧化钙溶液
反应得到的,其有效氯可高
达70%。
资料库
的细菌,起到消毒作用。次氯酸能使染料和有机色质褪色,
可用作棉、麻和纸张等的漂白剂。次氯酸不稳定,易分解
生成氧气,故一般只存在于稀溶液中。在阳光的照射下,
次氯酸的分解速度加快。
海水中的氯
51
2.1
● 海水晒盐可得粗盐,除去粗盐中的杂质后得到精盐,电解精制的饱
和食盐水又进一步得到氯气、氢气和烧碱等一系列工业产品。
(1) 实验室里除去粗盐中Ca
2+、Mg
2+、SO
2—
4 等可溶性杂质离子,用
到的化学试剂有氯化钡溶液、氢氧化钠溶液、碳酸钠溶液以及
盐酸等,思考这些试剂加入的先后顺序。
(2) 电解精制的饱和食盐水时消耗了117 g 氯化钠。计算理论上得
到的氯气体积(标准状况下)。
● (1) 选择沉淀剂时应先考虑加入的试剂能将杂质离子沉淀,同时不引
入新的杂质离子,或者引入的离子在后续操作中容易除去。其次要
考虑沉淀剂加入的顺序。
本例中,用过量的碳酸钠、氢氧化钠、氯化钡可分别沉淀除去
Ca
2+、Mg
2+ 和SO
2—
4,沉淀完全后过滤,在滤液中加入盐酸调节
溶液呈中性。但应注意过量的试剂要在后续过程中能够除去,
且不影响后续反应。
综上所述,下列几组试剂可供选择(含试剂及其加入顺序):
① 氯化钡、氢氧化钠、碳酸钠、盐酸;② 氢氧化钠、氯化钡、
碳酸钠、盐酸;③ 氯化钡、碳酸钠、氢氧化钠、盐酸。
学习指南
例题导引
问题:
分析:
(2) n(NaCl) = = 2 mol
117 g
58.5 g·mol
—1
2 mol
22.4 L
2 mol
V(Cl2)
2NaCl + 2H2O
2NaOH + H2↑ + Cl2↑
通直流电
总之,理论上得到氯气22.4 L(标准状况下)。
2 mol×22.4 L
2 mol
V(Cl2) = = 22.4 L
练习巩固
1. 液氯储存在钢瓶中,你认为液氯钢瓶上应贴的标签是( )。
(D)
(A)
(B)
(C)
52
海洋中的卤素资源
第2 章
2. 为了防止储存氯气的钢瓶被腐蚀,钢瓶在装入氯气前必须( )。
(A) 充入稀有气体
(B) 用盐酸彻底清洗
(C) 彻底干燥内壁
(D) 除去表面的铁锈
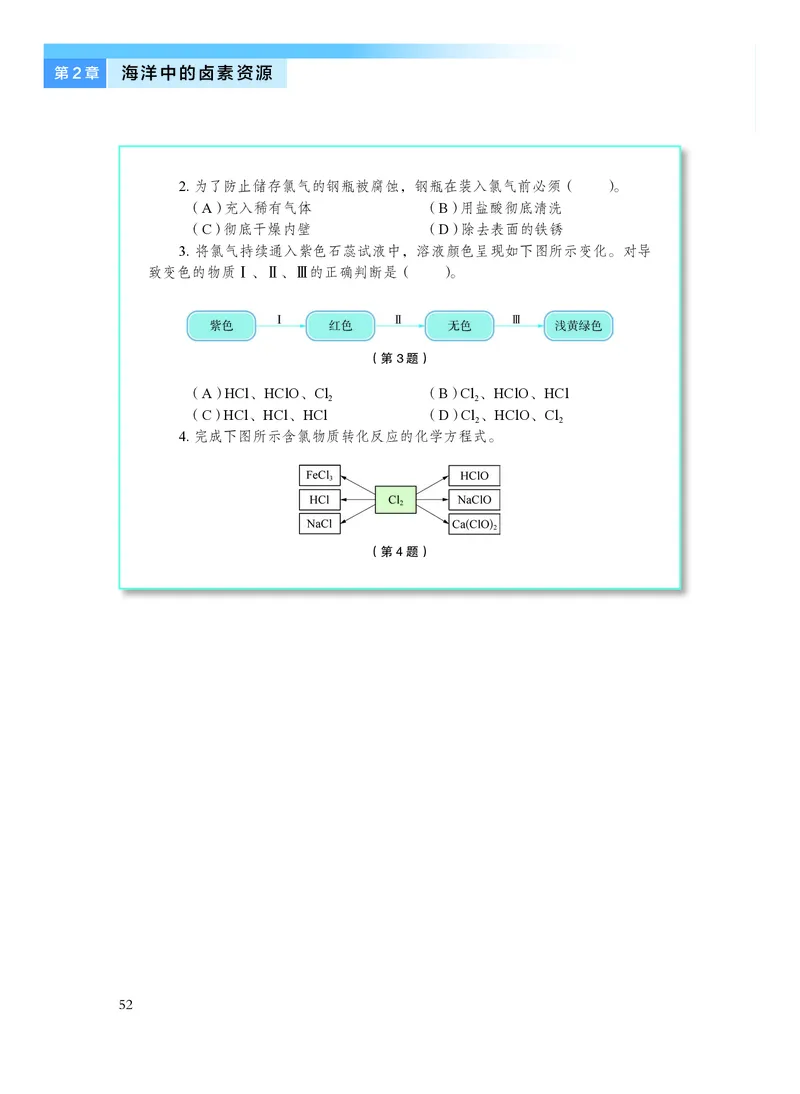
3. 将氯气持续通入紫色石蕊试液中,溶液颜色呈现如下图所示变化。对导
致变色的物质Ⅰ、Ⅱ、Ⅲ的正确判断是( )。
(A) HCl、HClO、Cl2
(B) Cl2、HClO、HCl
(C) HCl、HCl、HCl
(D) Cl2、HClO、Cl2
4. 完成下图所示含氯物质转化反应的化学方程式。
(第3 题)
(第4 题)
53
2.2
氧化还原反应和离子反应
身边的有机化合物
第7 章
2.2
氧化还原反应和离子反应
上一节的内容中涉及了氯及其重要化合物性质的反应。
在这些类型不同而且多变的化学反应中蕴藏着一定的规律,
氧化还原反应、离子反应都是从内在规律上认识这些化学
反应的重要视角。本节中我们将初步学习这两类化学反应
的基本原理。
了解氧化还原反应及其本质
知道常见的氧化剂和还原剂
认识电解质及电离过程
认识离子反应及其发生条件
学习聚焦
知识回放
● 化学反应的基本类型
● 氧化反应和还原反应
● 物质的分类和分散系
● 复分解反应及其发生条件
上述两个反应都有元素化合价的升降,反应前后元素
化合价的变化是氧化还原反应的重要特征。
凡有元素化合价升降的化学反应就是氧化还原反应。
物质所含元素化合价升高的反应是氧化反应,物质所含元
素化合价降低的反应是还原反应。
请用元素化合价的升降来分析下列氧化还原反应:
(1)
点燃
2Fe + 3Cl2
2FeCl3
(2)
点燃或光照
H2 + Cl2
2HCl
(3) Cl2 + 2NaOH
NaCl + NaClO + H2O
书写表达
初中时,我们已经从得氧和失氧的角度初步认识了氧化
反应和还原反应。氧化反应和还原反应总是同时发生、相互
依存在一个氧化还原反应中。在学习氯及其重要化合物的性质
中,我们也接触了许多氧化还原反应,学习时会发现,有些化
学反应并没有氧原子的得失,如氯气与钠的反应中就没有氧原
子的参与,那么这个反应为什么也是氧化还原反应呢?
让我们从元素的化合价入手,进一步来认识氧化还原
反应。
氧化还原反应
CuO + H2
Cu + H2O
△
+2
0
0
0
0
+1
—1
+1
化合价升高,被氧化
化合价升高,被氧化
化合价降低,被还原
化合价降低,被还原
2Na + Cl2
2NaCl
点燃
海洋中的卤素资源
54
第2 章
点燃
2Na + Cl2
2NaCl
2e
—
在氧化还原反应中,有原子失去电子,必然有原子
同时得到电子,而且失去电子的总数必定等于得到电子
的总数。因此,从本质上看,氧化还原反应是有电子转移
(得失或偏移)的反应。
我们知道原子是由原子核和核外电子构成的,元素化
合价的升降与电子的得失或偏移有密切的关系。在钠与氯
气的反应中,一个钠原子失去1 个电子变为Na
+,化合价
由0 升高到+1;一个氯原子得到1 个电子变为Cl
—,化合
价由0 降低到—1。可以用箭头表示反应物中不同元素间电
子转移的情况。
在氧化还原反应中得到电子的物质称为氧化剂,具有
氧化性,能氧化其他物质而自身被还原,化合价降低而发
生还原反应。失去电子的物质称为还原剂,具有还原性,
能还原其他物质而自身被氧化,化合价升高而发生氧化
反应。
根据物质中所含元素的化合价,可推测该物质在某
个氧化还原反应中是氧化剂还是还原剂。例如,高锰酸钾
(KMnO4)中锰元素显+7 价,是锰元素的最高正化合价,
因此高锰酸钾可做氧化剂。常用的氧化剂除高锰酸钾外,
还有氧气、氯气、硝酸和浓硫酸等。
碘化钾(KI)中碘元素显—1 价,是碘元素的最低负化
合价,所以碘化钾可做还原剂。常用的还原剂还有碳、氢
气、一氧化碳,以及钠、钙等金属单质。
有些具有中间价态的化合物既可做氧化剂,又可做
还原剂。例如,过氧化氢(H2O2)做氧化剂时,它被还
原为水;当遇到比它更强的氧化剂时,可做还原剂,被氧
化为氧气。一般来说,过氧化氢主要用作氧化剂,在氧化
还原反应中被还原为水,故有绿色氧化剂之称。过氧化氢
可用于工业生产和生活废水处理等,也可取代氯气用作漂
白剂。
氧化剂和还原剂
55
2.2
氧化还原反应和离子反应
图2.11 广泛存在的氧化还原反应
不同的氧化剂或还原剂,因其得失电子的能力不同,
氧化性或还原性的强弱会有所不同。
氧化还原反应是一类重要的化学反应,广泛存在于工
农业生产、科学技术和日常生活中,如酿造、金属的冶炼、
燃料的燃烧、生物的呼吸等。但是,并非所有的氧化还原
反应都能造福人类,有些氧化还原反应会带来危害,如食
品变质、钢铁锈蚀等。我们运用化学知识,可以趋利避害,
为科学技术的发展和人类生活质量的提高服务。
在化学实验室中,常利用氧化还原反应制取O2、H2、
NaClO 等物质。请写出制备这些物质的化学方程式,并指
出反应中的氧化剂和还原剂。
书写表达
海洋中的卤素资源
56
第2 章
实验表明,有一类化合物,如氯化钠、氢氧化钠和氯
化氢的水溶液能导电,硝酸钾固体加热至熔融时也能导电,
这类能在水溶液中或熔融状态下导电的化合物叫做电解质。
另有一类化合物,如蔗糖、酒精等,在水溶液中和熔融状
态下均不能导电,这类化合物叫做非电解质。常见的酸、
碱、盐大多数都是电解质,蔗糖、酒精等有机化合物大多
数都是非电解质。
物质导电的必要条件是什么?为什么氯化钠水溶液和盐
酸能导电,而氯化钠固体和气态氯化氢却不能导电呢?
实验探究
物质的导电性
1. 按图2.12 装置,在容器中,可以分别放入
以下物质:氯化钠固体和氯化钠水溶液、氢氧化
钠固体和氢氧化钠水溶液、硝酸钾固体和硝酸钾
水溶液、蔗糖固体和蔗糖水溶液、无水酒精和酒
精水溶液、盐酸。接通
电源,观察实验现象并
做好记录。
2. 按图2.13 装置,在V 形玻璃管里装入少量硝
酸钾固体,加热玻璃管,待固体熔化时,再插入电极,
观察实验现象并做好记录。
图2.13 熔融固体的导电性
实验装置示意图
现象
固体
溶液
熔融状态
灯泡发亮
灯泡不亮
图2.12 物质导电实验装置
电解质的电离
硝酸钾固体
硝酸钾
水溶液
想一想
57
2.2
氧化还原反应和离子反应
电解质的水溶液或熔融状态之所以能够导电,是因为
在水溶液中或熔融状态下,产生了可以自由移动的离子,
与外接电源形成闭合通路时,就产生了电流。例如,氯化
钠溶于水时,在水分子的作用下,钠离子和氯离子脱离氯
化钠固体表面进入水中,与水分子结合形成能够自由移动
的水合钠离子和水合氯离子。氯化钠熔融时也能产生自由
移动的钠离子和氯离子。
图2.14 氯化钠电离过程的示意图
电解质在水溶液中或熔融状态下,形成可以自由移动
离子的过程称为电离。这一过程可用电离方程式表示如下
(为了书写简便,用离子符号表示水合离子):
NaCl
Na
+ + Cl
—
HCl
H
+ + Cl
—
NaOH
Na
+ + OH
—
写出下列电解质的电离方程式。
Ba(OH) 2:____________________________________。
Na2SO4:____________________________________。
BaCl2:______________________________________。
书写表达
海洋中的卤素资源
58
第2 章
像氯化钠、氯化氢、氢氧化钠等在水溶液中能够全部
电离为自由移动离子的电解质称为强电解质。像醋酸、一
水合氨(NH3·H2O)等在水溶液中仅有部分分子能电离出
自由移动离子的电解质称为弱电解质。弱电解质的电离是
一个可逆过程,因此电离方程式中用“
”来表示。醋
酸、一水合氨的电离方程式可表示为:
强酸、强碱和大多数盐都是强电解质,弱酸、弱碱等
是弱电解质,水则是极弱的电解质。
图2.15 水分子电离过程的示意图
阿伦尼乌斯(Svante August Arrhenius,1859— 1927)是瑞典物理化学家,他
在化学上的主要贡献是建立电离学说。他在探索电解质溶液的导电性时,借鉴了物
理学的研究成果,1887 年他在《关于溶质在水中的离解》一文中阐述了电离学说
的基本观点:
(1) 由于溶剂的作用,电解质在水中自动离解成带相反电荷的正、负离子。
(2) 在水溶液中每一种电解质都是由已离解的分子和未离解的分子构成,
溶液稀释时未离解的分子继续离解,以致在无限稀释的溶液中只有已离解的分
子存在。
阿伦尼乌斯的观点当时被认为是离经叛道之说,遭到多数人的排斥。因为当
时电离理论的研究尚处于定性描述阶段,并没有关注和吸纳物理等其他学科的成
果。化学界对此展开了近20 年的争论,最终电离理论被广泛认可,阿伦尼乌斯也
化学史话
电离学说
水分子会发生非常微弱的电离(图2.15),写出水的电
离方程式(用简单离子符号来表示)。
CH3COOH
H
+ + CH3COO
—
NH3·H2O
NH
+
4 + OH
—
书写表达
59
2.2
氧化还原反应和离子反应
离子反应
实验探究
溶液中的离子反应
在试管中完成下列两组反应:(1) 硫酸钠溶液与氯化钡溶液反应;(2) 硫酸
铜溶液与氯化钡溶液反应。
硫酸钠、氯化钡、硫酸铜是盐,在溶液中均电离产生自由移动的离子,如
Na
+、Ba
2+、Cu
2+ 和SO
2—
4 等。根据实验现象,将相关变化情况填入下表。
反应物
生成物
反应前溶液中浓
度较大的离子
反应后溶液中浓
度较大的离子
反应前后溶液中
浓度有明显变化
的离子
硫酸钠溶液与
氯化钡溶液
硫酸铜溶液与
氯化钡溶液
因此荣获1903 年诺贝尔化学奖。
科学的发展启示我们:很多理论建立和问题的攻克单靠一门学科是难以完成的,
必须学会用跨学科、多维度的知识或思维去探究。
问题:通过本实验,你认为是否所有的离子均参与了相应的反应?
两组溶液反应后均产生了白色硫酸钡沉淀。反应后,第
一组溶液中还存在大量的Na
+ 和Cl
— ;第二组溶液中还存在
大量的Cu
2+ 和Cl
—,显然两组溶液实质上发生变化的都是
Ba
2+ 和SO
2—
4 结合生成硫酸钡沉淀,而其他离子并未参与反应。
化学上把有离子参加或生成的反应叫做离子反应。酸、
碱、盐在溶液中反应的实质就是离子之间的反应。上述两
组离子反应的实质都可以表示为:
Ba
2+ + SO
2—
4
BaSO4↓
海洋中的卤素资源
60
第2 章
组别
能否发生离子反应
(在“□”中画“√”)
离子方程式
① 硫酸与氢氧化钾
□ 能 □ 否
② 碳酸钾与硝酸
□ 能 □ 否
③ 硫酸铜与氢氧化钠
□ 能 □ 否
判断下列各组溶液之间能否发生离子反应?若能发生反应,请写出相应的离子方程式。
我们以碳酸钙与盐酸的反应为例,说明离子方程式的
书写步骤。
离子方程式的书写
书写表达
这种用实际参加反应的离子符号来表示反应的方程式
叫做离子方程式。可见,离子方程式能更好地表示出上述
两组化学反应属于同一类离子反应的本质。
图2.16 离子方程式的书写步骤示例
写出发生反应的化学方程式
把易溶于水的强电解质写成离
子形式,难溶电解质、气体以
及弱电解质等仍以化学式表示
省略化学方程式中两边不参
加反应的离子
检查离子方程式是否正确,如
离子方程式两边各元素的原子
数目、电荷数是否相等
CaCO3 + 2HCl
CaCl2 + CO2 ↑ + H2O
CaCO3 + 2H
+ + 2Cl
—
Ca
2+ + 2Cl
— + CO2↑ + H2O
CaCO3 + 2H
+
Ca
2+ + CO2↑ + H2O
CaCO3 + 2H
+ + 2Cl
—
Ca
2+ + 2Cl
— + CO2↑ + H2O
第一步
第二步
第三步
第四步
61
2.2
氧化还原反应和离子反应
电解质溶液中发生的氧化还原反应也可用离子方程式
表示。例如:
化学方程式:Fe + CuSO4
FeSO4 + Cu
离子方程式:Fe + Cu
2+
Fe
2+ + Cu
归纳酸、碱、盐在溶液中能够发生离子反应的条件。
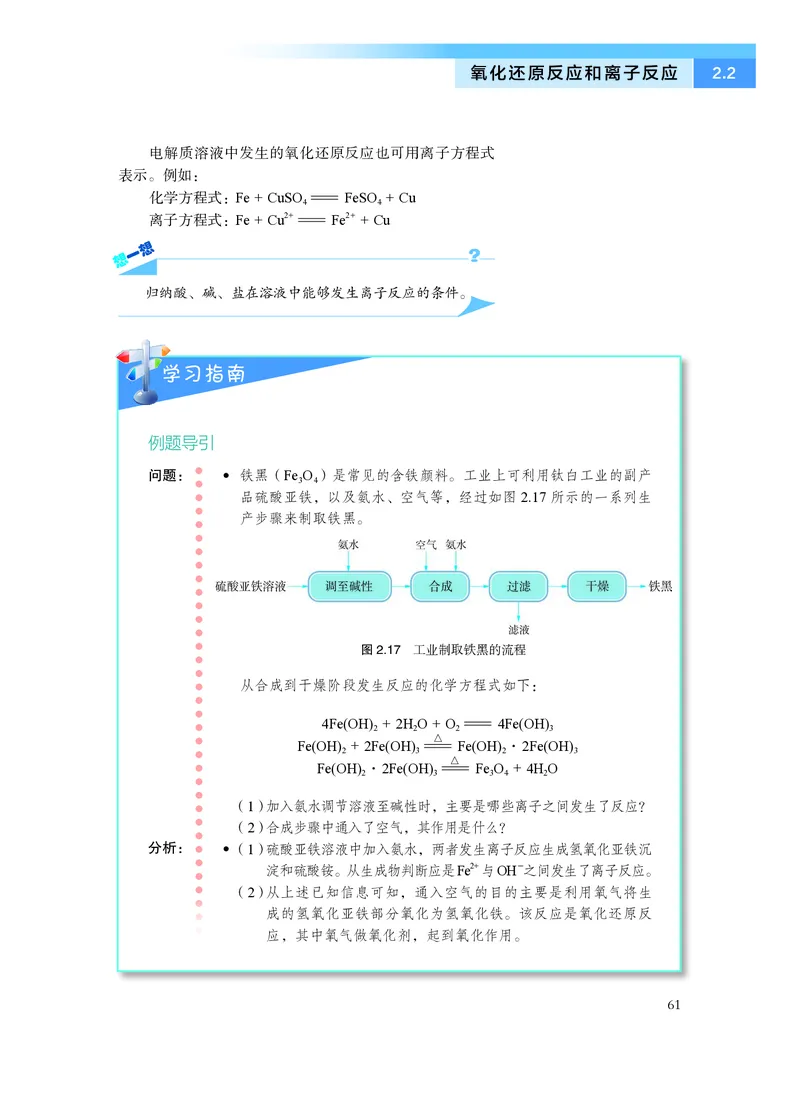
● 铁黑(Fe3O4)是常见的含铁颜料。工业上可利用钛白工业的副产
品硫酸亚铁,以及氨水、空气等,经过如图2.17 所示的一系列生
产步骤来制取铁黑。
从合成到干燥阶段发生反应的化学方程式如下:
学习指南
例题导引
问题:
图2.17 工业制取铁黑的流程
(1) 加入氨水调节溶液至碱性时,主要是哪些离子之间发生了反应?
(2) 合成步骤中通入了空气,其作用是什么?
● (1) 硫酸亚铁溶液中加入氨水,两者发生离子反应生成氢氧化亚铁沉
淀和硫酸铵。从生成物判断应是Fe
2+与OH
—之间发生了离子反应。
(2) 从上述已知信息可知,通入空气的目的主要是利用氧气将生
成的氢氧化亚铁部分氧化为氢氧化铁。该反应是氧化还原反
应,其中氧气做氧化剂,起到氧化作用。
4Fe(OH)2 + 2H2O + O2
4Fe(OH)3
Fe(OH)2 + 2Fe(OH)3
Fe(OH)2·2Fe(OH)3
Fe(OH)2·2Fe(OH)3
Fe3O4 + 4H2O
△
△
分析:
想一想
海洋中的卤素资源
62
第2 章
练习巩固
1. 下列变化中,金属元素被还原的是( )。
(A) Cu 变成Cu
2+
(B) Sn
4+ 变成Sn
2+
(C) Fe
2+ 变成Fe
3+
(D) Ag 变成Ag
+
2. 厨房中有很多化学物质,下列物质中属于强电解质的是( )。
(A) 醋酸
(B) 白糖
(C) 小苏打
(D) 淀粉
3. 下列反应中,能用离子方程式H
+ + OH
—
H2O 表示的是( )。
(A)
点燃
2H2 + O2
2H2O
(B) HCl + NaOH
NaCl + H2O
(C) 2HCl + Cu(OH)2
CuCl2 + 2H2O
(D) Ba(OH)2 + H2SO4
BaSO4↓ + 2H2O
4. 写出符合下列离子方程式的化学方程式(各一个)。
(1) Cu
2+ + 2OH
—
Cu(OH)2↓
(2) H
++OH
—
H2O
(3) MgCO3 + 2H
+
Mg
2+ + CO2↑ + H2O
(4) ZnO + 2H
+
Zn
2+ + H2O
(5) Cu
2+ + Fe
Cu + Fe
2+
5. 下表列出了几种常见的氧化剂,写出每种氧化剂的一个用途,并用化学方
程式表示。模仿下表制作一个常见还原剂的表格。
物质
用途
化学方程式
O2
Cl2
H2O2
Ca(ClO)2
63
2.2
氧化还原反应和离子反应
身边的有机化合物
第7 章
2.3
溴和碘的提取
氯、溴、碘元素的单质都是双原子分子,随着相对分
子质量的增大,它们的物理性质呈现规律性的变化。
常温常压下,溴是深棕红色液体,密度比水大,容
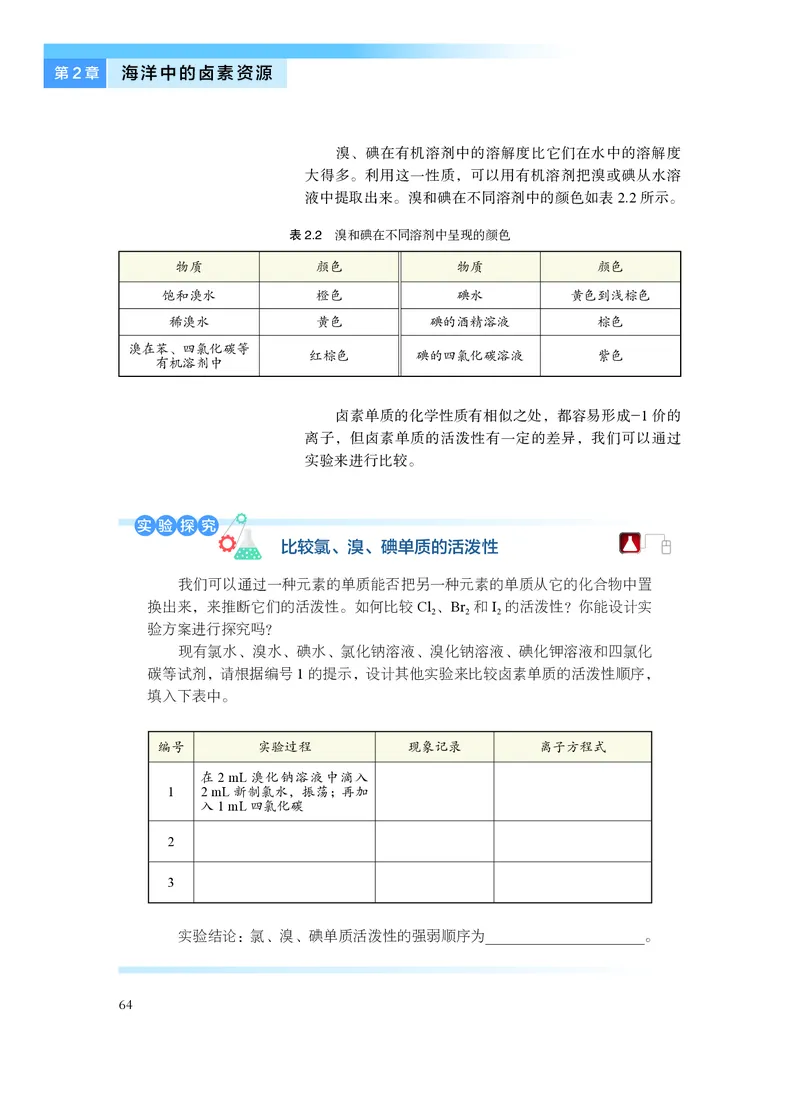
易挥发,具有强烈的腐蚀性,所以把溴存放在试剂瓶里
时应密封保存,同时需要在瓶中加一些水覆盖,以减少
溴的挥发。
常温常压下,碘是紫黑色固体,几乎不溶于水,但能
溶于酒精,形成碘酒。常压下固体碘受热易升华,蒸气遇
冷,重新凝聚成固体。碘还能使淀粉溶液变蓝色,这一特
征反应常用于检验碘单质。
卤素单质的性质
从海水中不仅可以获得氯碱工业的原料—氯化钠,
还可提取溴、碘、镁、钾等多种物质。其中,溴和碘在陆
地上的含量较少,主要是从海洋中提取。我们在掌握了氧
化还原反应和离子反应的知识后,将继续学习从海洋中提
取溴、碘单质等资源的一般方法和主要步骤,进而理解卤
素单质活泼性的递变规律以及卤素离子的检验方法等,对
以氯为代表的卤族元素的性质形成较为全面的认识。
了解卤素单质的性质及其应用
了解从海洋中提溴和提碘的主
要原理
了解Cl
—、Br
—、I
—的检验方法
学习聚焦
知识回放
● 氯及其重要化合物的性质
● 氧化还原反应
● 离子反应及其发生条件
图2.18 氯、溴、碘的单质
表2.1 氯、溴、碘单质的物理性质
卤素
单质
常温下
状态
颜色
密度
熔点
℃
沸点
℃
溶解度
Cl2
气体
黄绿色
2.98 g·L
—1
(293 K)
—101.5
—34.0
199 cm
3·(100 g H2O)
—1
(298 K)
Br2
液体
深棕红色
3.10 g·cm
—3
(298 K)
—7.2
58.8
3.4 g·(100 g H2O)
—1
(293 K)
I2
固体
紫黑色
4.63 g·cm
—3
(298 K)
113.6
185.2
0.029 g·(100 g H2O)
—1
(293 K)
根据表2.1 中的信息,归纳Cl2、Br2 和I2 在常温下的状
态、颜色等物理性质的变化规律。
氯气
液溴
碘
想一想
海洋中的卤素资源
64
第2 章
编号
实验过程
现象记录
离子方程式
1
在2 mL 溴化钠溶液中滴入
2 mL 新制氯水,振荡;再加
入1 mL 四氯化碳
2
3
卤素单质的化学性质有相似之处,都容易形成—1 价的
离子,但卤素单质的活泼性有一定的差异,我们可以通过
实验来进行比较。
实验探究
我们可以通过一种元素的单质能否把另一种元素的单质从它的化合物中置
换出来,来推断它们的活泼性。如何比较Cl2、Br2 和I2 的活泼性?你能设计实
验方案进行探究吗?
现有氯水、溴水、碘水、氯化钠溶液、溴化钠溶液、碘化钾溶液和四氯化
碳等试剂,请根据编号1 的提示,设计其他实验来比较卤素单质的活泼性顺序,
填入下表中。
比较氯、溴、碘单质的活泼性
实验结论:氯、溴、碘单质活泼性的强弱顺序为
。
表2.2 溴和碘在不同溶剂中呈现的颜色
物质
颜色
物质
颜色
饱和溴水
橙色
碘水
黄色到浅棕色
稀溴水
黄色
碘的酒精溶液
棕色
溴在苯、四氯化碳等
有机溶剂中
红棕色
碘的四氯化碳溶液
紫色
溴、碘在有机溶剂中的溶解度比它们在水中的溶解度
大得多。利用这一性质,可以用有机溶剂把溴或碘从水溶
液中提取出来。溴和碘在不同溶剂中的颜色如表2.2 所示。
65
2.3
溴和碘的提取
目前,从海洋中提取的两类物质有:一类是海水中
含量较高,提取成本相对较低的物质,如镁、钾等;另
一类是陆地上含量极少,只能从海洋中提取的物质,如溴、
碘等。
地球上99%的溴元素分布在海洋中。从海水中提取溴,
一般要经过浓缩、氧化和提取三个步骤。
苦卤(海水提盐后的母液)是海水制盐工业的副产
物,其中溴离子的含量较海水而言已提高很多,可直接用
作提取溴的原料。要将海水中的溴离子氧化成溴单质,常
用的氧化剂是氯气。氯气通入苦卤中,将溴离子转化为溴
单质。
溴和碘的提取
反应生成的溴仍然溶解在苦卤中,怎样才能将溴提取
出来呢?根据溴的沸点比水低的性质,可以向溶液中鼓入
热空气或水蒸气,使溴和水蒸气一起挥发出来,冷凝后得
到含有杂质的粗溴,其主要流程如图2.19 所示。再将粗溴
精制,就可以得到高纯度的溴单质。
Cl2 + 2Br
—
2Cl
— + Br2
图2.19 从海水中提取粗溴的主要流程
在工业上,大量的溴被用来制造燃料的抗爆剂;在农
业生产中,含溴元素的杀虫剂被广泛使用;在医药方面,
溴化钠、溴化钾常被用作镇静剂;此外,溴化银见光容易
分解,可被用作感光材料。
虽然海洋中碘的总量不少,但由于海水中碘的浓度
很低,工业上一般不直接从海水中提取碘。海洋中的海
带等海藻类植物具有富集碘的能力,海带或海带灰在水
中浸泡时,所含的I
—进入水中,然后再用氯气氧化得到
碘单质。这是工业上获取碘的重要途径,其主要流程如
图2.20 所示。
海洋中的卤素资源
66
第2 章
拓展视野
除卤素之外,海洋中还蕴藏着多种金属元素的资源。例如,海水中镁的含
量仅次于氯和钠,位居第三,总储量约为1.8×10
15 t。从海水中提取镁的流程是:
先将石灰乳加入海水沉淀池中,生成氢氧化镁沉淀,以此达到富集镁离子的目
的;然后用盐酸将沉淀溶解,得到氯化镁溶液,通过蒸发浓缩,可获得六水合氯
化镁晶体(MgCl2·6H2O);再将六水合氯化镁在一定条件下加热脱水,生成无
水氯化镁;电解熔融的氯化镁便可得到金属镁。
海水中镁的提取
目前工业上从海带中提取碘时,选用离子交换法处理
含碘离子的溶液,这样能提高碘的提取效率。
图2.20 从海带中提取碘的主要流程
写出海带浸泡液中通入氯气后发生反应的离子方程式。
卤素离子的检验
实验探究
把少量硝酸银溶液分别滴入盛有氯化钠溶液、溴化钠溶液和碘化钾溶液的
3 支试管中,再向3 支试管中各加入少量稀硝酸,观察实验现象。
现象记录:____________________________________________________。
实验结论:____________________________________________________。
卤素离子与银离子反应
在上述反应中,3 支试管里的氯化钠、溴化钠、碘化
钾分别与硝酸银反应,生成了相应的卤化银沉淀。卤化银
书写表达
67
2.3
溴和碘的提取
Ag
+ + Cl
—
AgCl↓
Ag
+ + Br
—
AgBr↓
Ag
+ + I
—
AgI↓
1. 如何检验烧杯中的水是蒸馏水还是自来水?
2. 归纳检验卤素离子的实验步骤和实验现象。
Ag
+ 与CO
2—
3 的反应
Ag
+ 离子与CO
2—
3 离子
也会反应生成Ag 2CO 3
沉淀:2Ag
+ + CO
2—
3
Ag2CO3↓。但Ag2CO3 溶
于稀硝酸:Ag 2CO 3 +
2H
+
2Ag
+ + H2O +
CO2↑。
资料库
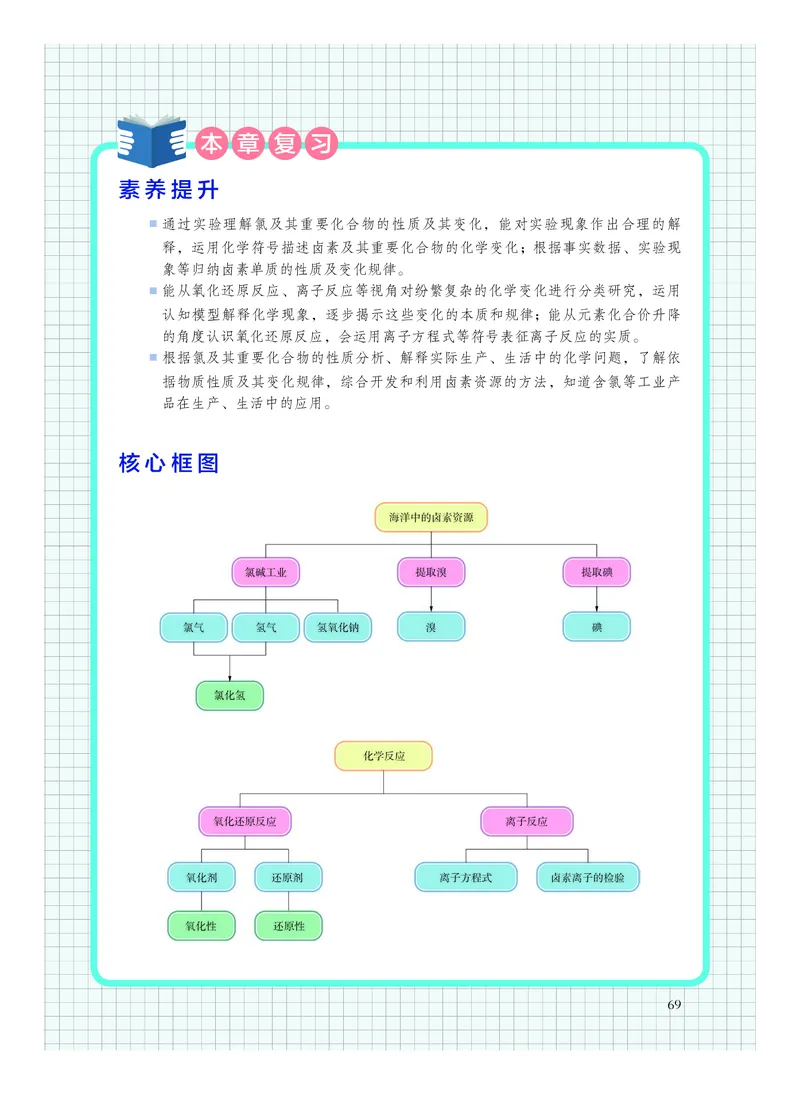
● 海洋中化学资源的综合利用包含许多方面。图2.21 所示的是从海
水中提取粗盐和溴的一种流程。
(1) 利用蒸馏法淡化海水,处理后得到的A 和B 分别是什么物质?
(2) 经过步骤Ⅰ后已经获得了粗溴,步骤Ⅱ、Ⅲ又将起到什么作用?
(3) 步骤Ⅱ用SO2 水溶液吸收Br2,吸收率可以达到95%。在该反
应中,SO2 起到什么作用?
● (1) 蒸馏法淡化海水后,产物除了淡水还有结晶产生的粗盐和苦卤。
A 通过化学反应生成Cl2,因此可判断A 为粗盐,B 为苦卤。
学习指南
例题导引
问题:
分析:
图2.21 海水中提取粗盐和溴的过程
的颜色分别为白色、浅黄色、黄色,且均不溶于稀硝酸。
利用上述反应现象,可以鉴别卤素离子。
想一想
海洋中的卤素资源
68
第2 章
(2) 虽然步骤Ⅰ已得到粗溴,但此时Br2 的浓度较低,需要富集处
理,通过步骤Ⅱ、Ⅲ可以得到高纯度的溴单质。
(3) 在步骤Ⅱ中,Br2 转化为HBr。溴元素的化合价由0 降低为—1
价,可判断Br2 为氧化剂,则SO2 为还原剂,起到还原作用。
练习巩固
1. 淀粉溶液与下列物质分别混合后,溶液呈现蓝色的是( )。
(A) 碘化钾溶液
(B) 碘单质
(C) 氯水
(D) 硫酸
2. 向溴化钠、碘化钠的混合溶液中通入足量氯气之后加热,将溶液蒸干,
并灼烧片刻,最后残留的物质是( )。
(A) 氯化钠
(B) 氯化钠、溴化钠、碘化钠
(C) 溴化钠、碘化钠
(D) 氯化钠、碘单质
3. 某种黄色溶液可能是碘水,试用两种方法加以验证。
4. 三瓶失去标签的试剂瓶中,分别盛有氯化钠、溴化钠和碘化钠溶液,试
用两种不同的实验方法来鉴别,并写出有关反应的离子方程式。
69
2.3
溴和碘的提取
素养提升
■ 通过实验理解氯及其重要化合物的性质及其变化,能对实验现象作出合理的解
释,运用化学符号描述卤素及其重要化合物的化学变化;根据事实数据、实验现
象等归纳卤素单质的性质及变化规律。
■ 能从氧化还原反应、离子反应等视角对纷繁复杂的化学变化进行分类研究,运用
认知模型解释化学现象,逐步揭示这些变化的本质和规律;能从元素化合价升降
的角度认识氧化还原反应,会运用离子方程式等符号表征离子反应的实质。
■ 根据氯及其重要化合物的性质分析、解释实际生产、生活中的化学问题,了解依
据物质性质及其变化规律,综合开发和利用卤素资源的方法,知道含氯等工业产
品在生产、生活中的应用。
本章复习
核心框图
69
海洋中的卤素资源
70
第2 章
70
练习巩固
1. 下列不能通过单质间直接化合制得的氯化物是( )。
(A) FeCl2
(B) FeCl3
(C) CuCl2
(D) NaCl
2. 检验氯化氢气体中是否混有氯气,可采用的方法是( )。
(A) 用干燥的蓝色石蕊试纸
(B) 用干燥的有色布条
(C) 将气体通入硝酸银溶液
(D) 用湿润的淀粉碘化钾试纸
3. 氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验
现象和结论一致的是( )。
(A) 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2 存在
(B) 溶液呈黄绿色且有刺激性气味,说明有HClO 存在
(C) 加入硝酸酸化的硝酸银溶液有白色沉淀,说明有Cl
—存在
(D) 加入氢氧化钠溶液,黄绿色消失,说明有HClO 存在
4. 以油类为溶剂的防锈漆称为油基防锈漆,由于环保要求,目前正推广使用水基防
锈漆。但水基漆较易溶解氧气,在干燥之前易导致金属表面产生锈斑。为此需要在水基
漆中加入缓蚀剂。下列物质可作为缓蚀剂的是( )。
(A) KMnO4
(B) NaNO2
(C) NaCl
(D) H2SO4
5. 下列离子方程式书写正确的是( )。
(A) 盐酸与氢氧化镁反应:H
+ + OH
—
H2O
(B) 溴与碘化钾溶液反应:Br2 + I
—
Br
— + I2
(C) 溴化钠与硝酸银溶液反应:NaBr + AgNO3
AgBr↓ + NaNO3
(D) 氯气与氢氧化钠溶液反应:Cl2 + 2OH
—
Cl
— + ClO
— + H2O
6. 现有① KMnO4、② H2、③ O2、④ Cl2、⑤ CO、⑥ Al 六种物质,可从氧化性、
还原性的角度进行分类。
(1) 常见的氧化剂有__________ ;常见的还原剂有__________ 。(填序号)
(2) 由
Ⅰ
Fe
Fe3O4,
Ⅱ
Fe2O3
Fe 可知,欲实现转化Ⅰ应从___________(填“氧
化剂”或“还原剂”,下同)中找物质,欲实现转化Ⅱ应从___________中找物质。
(3) NO 是制硝酸的中间产物,生成NO 的化学方程式为:
高温
4X + 5O2
4NO + 6H2O
催化剂
,
则X 的化学式为___________。
7. 海水中含有丰富的氯元素。下图是以海水为原料生产许多重要的含氯化工产品
的示意图。请完成填空。
(1) 步骤①在实验室中的操作名称是__________ ;步骤②的反应条件是__________ 。
(2) 将氯气通入氢氧化钠溶液中可以得到家用消毒液。这是一种无色、有漂白作用
的液体,其有效成分是__________。消毒液在使用时加入少量白醋,可以提高消毒效果,
原因是__________。
71
2.3
溴和碘的提取
71
71
(第7 题)
(3) 从苦卤中可提取溴。请在图中补画出提溴的流程,并回答下列问题。
① 氧化苦卤中的溴离子,需要在酸性条件下进行,原因是什么?
② 氧化后生成的溴单质为什么可用热空气吹出,阐述理由。
*8. 将硫酸酸化的过氧化氢溶液滴入无色的碘化钾溶液中,溶液变成浅棕色。这是什
么物质的颜色?用离子方程式解释变色的原因。
*9. 阅读短文,思考下列问题。
Some chemiluminescent redox reactions occur naturally in the atmosphere as a result
of lightning. When lightning is produced by an electrical discharge in the atmosphere,
electrons in molecules of O2 and N2 gases are excited to higher energy levels. Energy from
the electricity breaks the O2 and N2 molecules into atoms. When the atoms recombine to
form other molecules and the electrons return to lower energy levels, light energy is released
through chemiluminescence.
Other chemiluminescent reactions involve luminol, an organic compound that emits
cool blue-green light when it is oxidized. Luminol is a crystalline solid that is white to pale
yellow in color, and soluble in water. Luminol reactions are utilized by forensic chemists
to analyze evidence in crime investigations. They spray luminol onto a location where the
presence of blood is suspected. If blood is present, the iron(II) ions in the hemoglobin of
red blood cells oxidize the luminol to form a chemiluminescent compound that glows in the
dark. The iron is reduced by the luminol and the luminol is oxidized.
(短文取自:John S. Phillips, Victor S. Strozak, Cheryl Wistrom, et al. Chemistry:
Concepts and Applications[M]. The McGraw-Hill Companies, 2009: 573.)
(1) Luminol is also known as luminescent ammonia. Do you know why luminol
produces blue-green light when it comes into contact with iron(II) ions?
(2) Do you understand the principle of chemiluminescence? What reactions in the
chemical reactions you have learned are accompanied by the release of light energy?
海洋中的卤素资源
72
第2 章
72
体验 · 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制作成海报、演示
文稿,进行分享和交流。
中华人民共和国国家标准《氯气安全规程》(GB11984—2008)中关于氯气使用
安全的部分内容摘录如图2.22 所示。
查阅相关资料后解释:(1) 充装及输送液氯时,使用压
缩空气干燥的原因;(2) 在使用氯气的过程中应注意哪
些安全问题。
日常生活中使用的某消毒液的主要成分为次氯酸钠。请
利用电解饱和食盐水原理,在教师指导下设计一个安全、
简易的制备少量次氯酸钠消毒液的实验装置。在实验室
里,利用设计的装置,完成自制消毒水的实验,并检验
消毒效果。(提示:氯气有毒,注意实验安全,同时还应
避免氯气造成的环境污染)
200 多年前,人们就发现给长途航行的水兵吃柠檬可以
预防坏血病。维生素C 泡腾片是人们用来增强抵抗力、预防和治疗坏血病等的
家庭常备药品。维生素C 是重要的抗氧化剂,能保护人体细胞免遭氧化性物质
的破坏。阅读药品说明书,了解维生素C 泡腾片成分中电解质或非电解质的功
效、维生素C 的结构等,运用氧化还原反应知识解释维生素C 具备抗氧化作用
的原理。
加入适量碘的食盐简称碘盐,食用碘盐有利于防治缺碘引起的疾病。请查询资
料了解碘盐的组成,并设计实验方案,选用生活中的物品,检测所购食盐是否
为碘盐。
图2.23 家用消毒液
图2.22 《氯气安全规程》及部分内容摘录
5.2.7 罐车上卸液氯用的压缩空气,应
经过干燥处理,保证干燥后空气含水量低于
0.01%。
5.3.1 充装液氯贮罐时,应先缓慢打开
贮罐的通气阀,确认进入罐车内的干燥压缩
空气或气化氯的压力高于贮罐内的压力时,
方可充装。
硫、氮及其循环
第3 章
烟花的成分中通常含
有硫、氮的化合物。节日
中,骤然绽放在夜空中绚
丽璀璨的烟花,照亮了浦
江两岸。
73
硫及其重要化合物
氮及其重要化合物
硫循环和氮循环
3.1
3.2
3.3
74
硫
和氮是人们熟悉的元素,含硫、含氮的物质与人们的生活密
切相关。中国古代四大发明之一的黑火药中就含有硫元素和
氮元素,硫和氮也是生命物质的组成元素,现代工业、农业、国防、
航天、医药和日常生活都离不开这两种元素。
自然界中硫、氮的循环是维持生态平衡的重要物质基础, 含硫、
含氮物质的使用在为人类带来益处的同时,也给人们带来了一些
困扰。通过本章的学习,我们可以运用已有知识和方法,综合分
析化学给自然界带来的各种影响,从而形成全面客观地看待问题
的思维习惯。
硫及其重要化合物
75
3.1
身边的有机化合物
第7 章
据记载,我国古代炼丹家在长期炼丹的过程中,发现硝
石、硫和木炭混合后加热会燃烧甚至发生爆炸,由此得到了
黑火药。黑火药后来传入欧洲,影响了世界历史发展的进程。
纯净的硫是一种黄色或淡黄色的固体,俗称硫黄。硫很脆,
容易研磨成粉末,不溶于水,微溶于酒精,易溶于二硫化碳。
硫的化学性质比较活泼,与氧气相似,容易与金属、
其他非金属发生反应。
黑火药中的硫黄
硫是重要的非金属元素,也是人类较早认识的化学元
素之一。自然界中的硫元素主要以单质硫、硫化物和硫酸
盐等形式存在。人们对硫元素的利用,其本质就是通过各
种化学反应,实现含硫元素的物质之间的转化。这种转化
既可在含不同价态硫元素的物质之间进行,也可在含相同
价态硫元素的物质之间实现。
了解硫的化学性质
理解二氧化硫的化学性质
理解浓硫酸的特性
学习聚焦
知识回放
● 硫与氧气反应
● 酸性氧化物
● 酸的通性
● 氧化还原反应
3.1
硫及其重要化合物
实验探究
将4 g 铁粉与2.5 g 硫粉在研钵中充分混合,然后装入干燥的石英试管中。
在试管口塞上带长导管的橡皮塞,并在导管末端放入一小团蘸有氢氧化钠溶液
的棉花。加热试管,待混合物开始出现红热现象后,立即移开热源,观察现象。
硫与铁的反应
硫
密度:1.92 g·cm
—3
熔点:106.8℃
沸点:444.7℃
资料库
现象记录:
。
实验结论:
。
图3.1 硫与铁的反应
硫、氮及其循环
第3 章
76
通过之前的学习,我们知道氯气也能与铁、铜等金属反
应,从反应条件、生成物中金属元素的价态等角度,比较
硫和氯气的化学性质。
硫元素有—2、+4、+6 等几种常见的价态,有些硫的
化合物有着十分重要的应用。
1. 硫的氧化物
二氧化硫(SO2)和三氧化硫(SO3)是硫的常见氧化物。
硫的重要化合物
实验探究
1. 将集满二氧化硫气体的试管倒立于水槽中,在水下打开试管口的橡皮
塞,观察现象。在水下塞上橡皮塞,将试管移出水面,从试管中取出少量液体,
并滴加紫色石蕊试液。
二氧化硫的性质
图3.2 二氧化硫溶于水实验
硫在一定条件下与金属反应生成硫化物,如硫与铁粉
混合加热生成硫化亚铁,铜在硫蒸气中燃烧生成硫化亚铜,
常温下硫与汞反应生成硫化汞。硫在空气中燃烧会生成二
氧化硫,与氢气加热生成硫化氢。
S + Fe
FeS
S + 2Cu
Cu2S
S + Hg
HgS
S + O2
SO2
S + H2
H2S
△
△
点燃
△
想一想
硫及其重要化合物
77
3.1
2. 封管中封闭了少许溶有二氧化硫的品红试液,将封管加热至试液变红
后,停止加热(封管实验加热时间不宜过长),上下颠倒几下封管,冷却后观
察试液颜色变化。
图3.3 溶有二氧化硫的品红试液加热后再冷却
编号
现象记录
二氧化硫的性质
1
2
二氧化硫是无色、有刺激性气味的有毒气体,密度比
空气大,易溶于水,通常情况下,1 体积的水可溶解40 体
积的二氧化硫。溶于水的二氧化硫与水反应生成亚硫酸。
亚硫酸是一种不稳定的弱酸,易分解成二氧化硫和水。这
个可逆反应可表示为:
SO2 + H2O
H2SO3
我们还发现,二氧化硫有漂白作用,能漂白品红等某
些有色物质。这是由于它能与这些有色物质反应生成不稳
定的无色物质,这种无色物质受热后容易分解,从而使有
色物质恢复至原来的颜色。
二氧化硫的漂白作用和氯水相比有何不同?为什么?
冷却后
溶有二氧化硫的品红试液封管
加热后
想一想
硫、氮及其循环
第3 章
78
拓展视野
二氧化硫具有杀菌防腐和漂白作用,故可用作食品加工的防腐剂和漂白剂。
当然使用时必须严格遵守国家相关规定和使用标准,否则会影响健康。例如,我
国规定二氧化硫可用于葡萄酒和果酒的生产,最大使用量为0.25 g·kg
—1,残留
量不得超过0.05 g·kg
—1。
工业上常用二氧化硫来漂白纸浆、毛、丝、草编制品等,但时间久了,纸
张、草帽又会发黄,这就是因为二氧化硫漂白后的生成物不稳定,加热或经过一
段时间后又会恢复原色。
二氧化硫的用途
二氧化硫中的硫为+4 价,它既有氧化性,又有还原
性。当二氧化硫遇到还原性较强的硫化氢时会表现出氧化
性,生成单质硫和水。
SO2 + 2H2S
3S + 2H2O
在一定温度并有催化剂存在的条件下,二氧化硫可以
被氧气氧化成三氧化硫。
2SO2 + O2
2SO3
催化剂
△
三氧化硫也是一种酸性氧化物,它易与水反应生成硫酸。
SO3 + H2O
H2SO4
2. 硫酸
硫酸是一种用途很广的无机强酸。纯硫酸是一种难挥
实验探究
取一支试管,向其中加入5 mL 二氧化硫水溶液,滴加氯化钡溶液和
0.5 mL 3% 的过氧化氢溶液。振荡,静置片刻后,滴加稀盐酸,观察实验现象。
二氧化硫的还原性
现象记录:____________________________________________________。
实验结论:____________________________________________________。
硫及其重要化合物
79
3.1
取15 g 蔗糖放入100 mL 烧杯中,加入1 mL 水后,再加入约15 mL 浓硫
酸并迅速用玻璃棒搅拌后静置。观察并记录实验现象。
实验探究
浓硫酸使蔗糖脱水
现象记录:____________________________________________________。
实验结论:____________________________________________________。
图3.4 浓硫酸与蔗糖的反应
我们知道稀硫酸不能与铜、木炭等发生反应,那么浓
硫酸遇到这些物质会发生什么变化呢?
发的无色油状液体,可与水以任意比例混合,并释放出大
量热。市售硫酸的质量分数有92.5% 和98% 两种。
浓硫酸有强烈的吸水性,常被用来干燥不与它起反应
的气体。由于浓硫酸也会吸收空气中的水分,使酸的浓度
下降,因此使用浓硫酸后需将瓶盖拧紧。
浓硫酸具有脱水性,能把棉花、纸屑、蔗糖等有机化
合物中的氢、氧元素按水的组成脱去,使其发生炭化。
实验探究
按图3.5 搭好装置,关闭双连球上的活塞,在从左至右的第1 支试管中加
入约2 ~ 3 mL 浓硫酸,第2 支试管中加入3 mL 0.1% 品红试液,第3 支试管
中加入约3 mL 酸性高锰酸钾稀溶液,烧杯中加入约50 mL 氢氧化钠稀溶液。
将插在橡皮塞上的粗铜丝缓慢旋入浓硫酸中,加热试管。反应后,将铜丝慢慢
旋出液体,打开双连球上的活塞,用双连球将装置内残留的气体吹入氢氧化钠
溶液,随后打开橡皮塞,用长滴管吸取第1 支试管中的悬浊液,小心注入另一
支盛有少量水的试管中,观察溶液颜色。
浓硫酸与铜的反应
硫、氮及其循环
第3 章
80
图3.5 浓硫酸与铜的反应
浓硫酸具有强氧化性,它可以将金属铜氧化成+2
价的铜离子,而浓硫酸中的硫元素被还原为+4 价,生
成二氧化硫。
与铜一样,在加热条件下,多数金属(除铂、金外)
可以与浓硫酸反应,生成相应的硫酸盐、二氧化硫和水。
常温下,浓硫酸还可以“钝化”铁、铝等金属,在这些金
属的表面形成一层致密氧化物,从而阻止金属内部继续与
浓硫酸反应。利用“钝化”现象,冷的浓硫酸可用铁或铝
制的容器进行贮存。
在加热条件下,浓硫酸还可以氧化一些非金属。例如,
将烧红的木炭加入热的浓硫酸中,会发生剧烈反应。
C + 2H2SO4( 浓 )
CO2↑+ 2SO2↑+ 2H2O
△
3. 硫酸盐
三氧化硫、硫酸与碱性氧化物、碱反应都可以生成硫
酸盐。硫酸盐的种类很多,重晶石、石膏、明矾和胆矾等
都是常见的硫酸盐。
写出浓硫酸与铜反应的化学方程式,并指出反应中的
氧化剂和还原剂。
书写表达
现象记录:____________________________________________________。
实验结论:____________________________________________________。
反应中
反应后
硫及其重要化合物
81
3.1
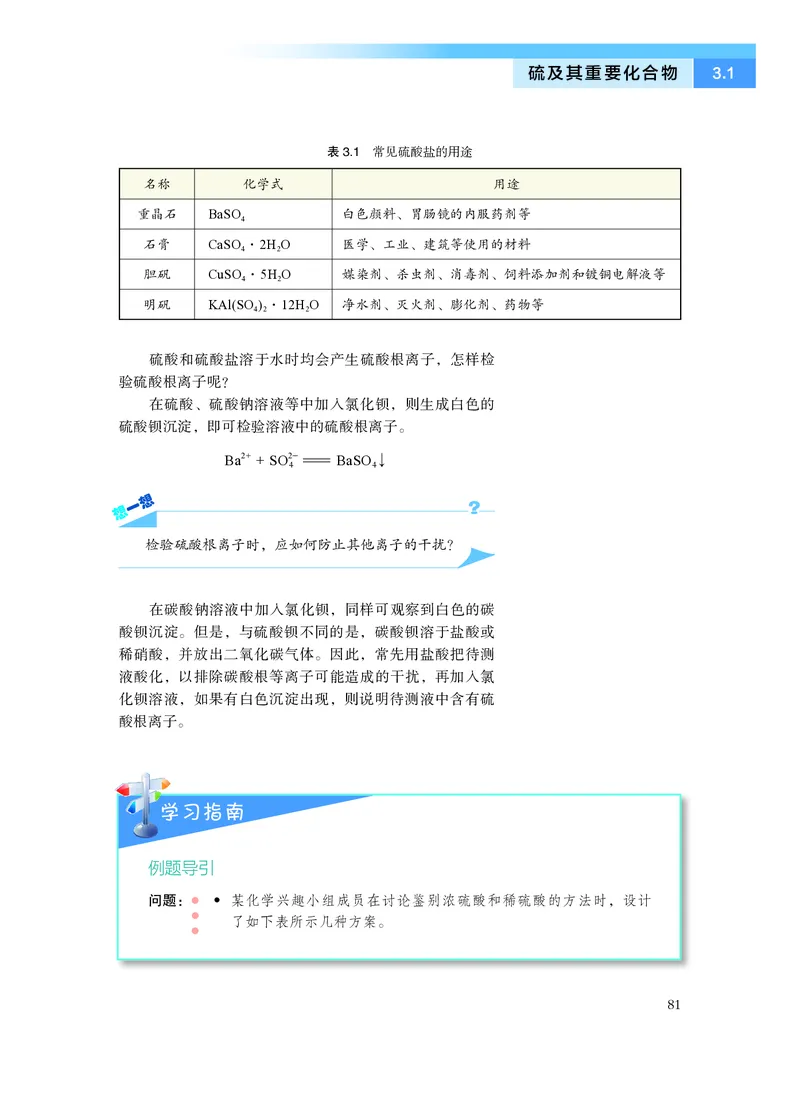
表3.1 常见硫酸盐的用途
名称
化学式
用途
重晶石
BaSO4
白色颜料、胃肠镜的内服药剂等
石膏
CaSO4·2H2O
医学、工业、建筑等使用的材料
胆矾
CuSO4·5H2O
媒染剂、杀虫剂、消毒剂、饲料添加剂和镀铜电解液等
明矾
KAl(SO4)2·12H2O
净水剂、灭火剂、膨化剂、药物等
硫酸和硫酸盐溶于水时均会产生硫酸根离子,怎样检
验硫酸根离子呢?
在硫酸、硫酸钠溶液等中加入氯化钡,则生成白色的
硫酸钡沉淀,即可检验溶液中的硫酸根离子。
Ba
2+ + SO
2—
4
BaSO4↓
检验硫酸根离子时,应如何防止其他离子的干扰?
在碳酸钠溶液中加入氯化钡,同样可观察到白色的碳
酸钡沉淀。但是,与硫酸钡不同的是,碳酸钡溶于盐酸或
稀硝酸,并放出二氧化碳气体。因此,常先用盐酸把待测
液酸化,以排除碳酸根等离子可能造成的干扰,再加入氯
化钡溶液,如果有白色沉淀出现,则说明待测液中含有硫
酸根离子。
● 某化学兴趣小组成员在讨论鉴别浓硫酸和稀硫酸的方法时,设计
了如下表所示几种方案。
学习指南
例题导引
问题:
想一想
硫、氮及其循环
第3 章
82
(1) 评价甲、乙、丙、丁四组方法的可行性。
(2) 请再给出两种鉴别方法。
分析:
● (1) 我们需要了解稀硫酸和浓硫酸在性质上的差异,才能找到鉴别
的方法。甲方案利用的是浓硫酸的脱水性;丙方案利用的是浓
硫酸遇水放热的特点。乙方案想要利用浓硫酸的强氧化性来生
成二氧化硫,但没有考虑到铝在浓硫酸中会钝化;丁方案想要利
用挥发性来鉴别酸性气体,但硫酸沸点高,不具有挥发性。所以,
乙、丁方案不可行。
(2) 我们可以利用浓硫酸的一些特殊性质,如密度大、黏稠等物理
性质或与铜、碳反应等化学特性进行鉴别,例如:
编号
操作
结论
①
取等体积样品,称取质量
质量小者为稀硫酸
②
加入碳粒(或铜片),加热
产生刺激性气味者为浓硫酸
③
分别加到胆矾晶体中
晶体变白者为浓硫酸
练习巩固
1. 下图为元素周期表的一部分。从A、B、C、D 中找出其单质能氧化硫
的元素。
(第1 题)
组别
操作
结论
甲
分别滴在火柴梗上
变黑者为浓硫酸
乙
分别加入金属铝片
产生刺激性气味者为浓硫酸
丙
分别加入盛水的试管中
剧烈放热者为浓硫酸
丁
用湿润的蓝色石蕊试纸靠近
装酸的瓶口
快速变红者为浓硫酸
硫及其重要化合物
83
3.1
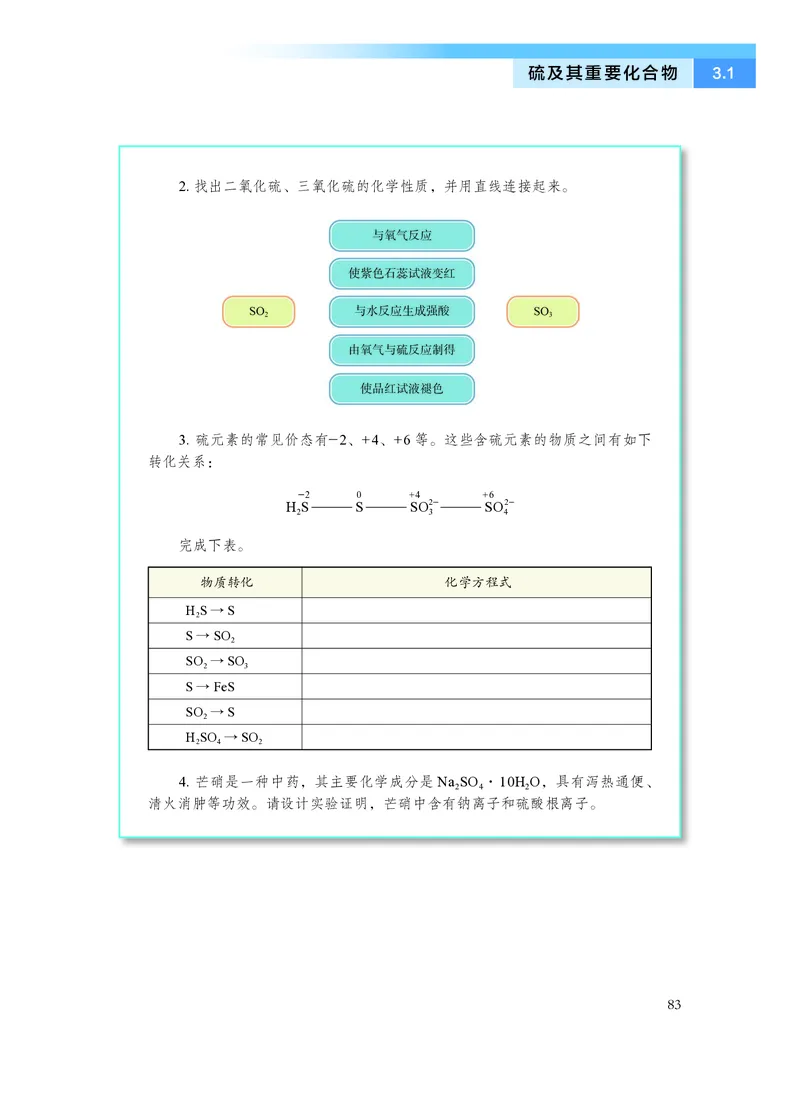
2. 找出二氧化硫、三氧化硫的化学性质,并用直线连接起来。
3. 硫元素的常见价态有—2、+4、+6 等。这些含硫元素的物质之间有如下
转化关系:
完成下表。
物质转化
化学方程式
H2S →S
S →SO2
SO2 →SO3
S →FeS
SO2 →S
H2SO4 →SO2
H2S
S
SO3
2—
SO4
2—
—2
+4
+6
0
4. 芒硝是一种中药,其主要化学成分是Na2SO4·10H2O,具有泻热通便、
清火消肿等功效。请设计实验证明,芒硝中含有钠离子和硫酸根离子。
硫、氮及其循环
第3 章
84
身边的有机化合物
第7 章
自然界中的氮元素以氮气、氮氧化物和硝酸盐等形式
存在,人类对氮元素的利用,就是实现氮元素在不同物质
之间的转化。氮肥是化学肥料中使用量很大的一类,为世
界粮食增产做出了重大贡献。工业上生产氮肥的原理是什
么?有哪些供农业使用的常见氮肥?让我们带着这些问题,
先来认识氮及其重要化合物的性质吧。
知道氮的固定
知道氮气的性质
了解一氧化氮、二氧化氮的化
学性质
理解氨的化学性质
了解铵盐、硝酸的化学性质
学习聚焦
知识回放
● 空气的组成
● 常见的化肥
氮及其重要化合物
3.2
纯净的氮气是一种无色、无味的气体。氮气在
101 kPa、—195.8℃时变成无色的液体。液氮不活泼,常被
用作低温实验的冷冻剂。
大部分氮元素以游离态存在于空气中。游离态的氮气
很难被植物吸收,而植物通常是从含氮化合物中获得氮元
素的。采用天然或人工的方式,将空气中的游离态氮转化
为化合态氮的过程称为固氮,固氮对植物生长尤为重要。
天然固氮有两种方式。一种是生物固氮,氮气在豆科
植物的根瘤菌体内所含的固氮酶作用下还原为氨。另一种
是大气固氮,在放电或高温下,空气中的氮气与氧气直接
化合,生成无色的一氧化氮。一氧化氮难溶于水,在常温
下很容易与空气中的氧气化合,生成红棕色并有刺激性气
味的二氧化氮。二氧化氮有毒,易溶于水,溶于水后生成
硝酸和一氧化氮。发生雷电时,大气中的氮转化为氮的氧
化物,经降水生成极稀的硝态氮肥—硝酸,渗入土壤被
植物根系吸收。
放电
N2 + O2
2NO
2NO + O2
2NO2
3NO2 + H2O
2HNO3 + NO
人工固氮目前主要通过工业合成氨来实现。氮气
和氢气在高温、高压并有催化剂的条件下,直接化合
生成氨。
固氮
图3.6 液氮
图3.7 根瘤菌固氮
N2 + 3H2
2NH3
高温、高压
催化剂
85
3.2
氮及其重要化合物
图3.8 合成氨工厂
化学仿生学是一门横跨化学与分子生物学领
域的交叉科学,模拟生物体内的化学反应过程、
模拟生物体内的物质输送过程,以及模拟生物体
内的能量转换等是其主要研究内容。化学仿生学
的关键技术就是模拟,以生物为原型,模拟其行
为以制备某种物质或者模拟某种行为来满足实际
需要。例如,科学家研发了一种“人工树叶”来
模拟自然界的光合作用、合成药物。
氮气和氢气在化工厂合成氨,须在约400 ~
500℃的高温、2×10
4 ~5×10
4 kPa 的高压以及催化剂等条件下完成。但是,豆
科植物的根瘤菌具有特殊的固氮本领,科学家根据根瘤菌的固氮机理,用化学方
法模拟生物固氮,实现在常温、常压的温和条件下固定空气中的氮。近年来,功
能高分子材料、人工膜技术、活性酶催化剂的研发取得了许多成果,其中仿蛛丝
纤维、生物陶瓷、人工肌肉等已被广泛应用。化学仿生学是在分子水平上模拟生
物的功能,也是人们打开科学的奇思妙想之门的钥匙。
化学仿生学
链接学科
图3.9 科学家研发“人工树叶”
来生产药物
氮肥对农作物生长起着非常重要的作用,施用氮肥能
提高农产品的产量。工业上生产氮肥的主要原料就是人工
固氮获得的氨。
氮肥
86
硫、氮及其循环
第3 章
实验探究
用干燥的圆底烧瓶集满氨,立即倒置烧瓶,将带
有玻璃管(连有活塞)和胶头滴管(预先吸入水)的
塞子塞紧瓶口,使玻璃管插入盛有水的烧杯里(水中
预先加入少量酚酞试液)。如图3.11 所示,安装好装
置,挤压滴管的胶头,使少量水进入烧瓶后,打开活
塞。观察并记录实验现象。
现象记录:
。
实验结论:
。
问题:从上述实验中,可得出氨具有哪些性质?
氨的“喷泉”实验
图3.11 氨的“喷泉”实验
阅读图3.10,找出粮食产量和化肥施用量之间的关联。
图3.10 我国粮食产量和化肥施用量
1. 氨和氨水
氨(NH3)是氮的氢化物,一般是无色、有刺激性气
味的气体。氨冷却或加压后易被液化,液氨汽化时要吸
收大量的热,使周围的温度急剧下降,所以液氨常用作
制冷剂。
氨
密度:0.771 g·L
—1(STP)
熔点:—77.75℃
沸点:—33.35℃
资料库
想一想
87
3.2
氮及其重要化合物
氨极易溶于水,在常温常压下,1 体积水约可溶解
700 体积的氨。氨的水溶液叫做氨水。氨水能使酚酞试液
变红色,说明氨水显碱性。
氨溶于水中,大部分与水结合成一水合氨。一水合氨
不稳定,受热后容易分解成氨和水。
NH3 + H2O
NH3·H2O
NH3·H2O
NH3↑+ H2O
△
一水合氨是弱电解质,可少部分电离出铵根离子
(NH
+
4)和氢氧根离子(OH
—),使溶液显弱碱性。
NH3·H2O
NH
+
4 + OH
—
2. 铵态氮肥
氨水可以作为氮肥,但不便于运输和使用,所以,人
们常将氨水制成铵盐来获得铵态氮肥。
实验探究
向容积约500 mL 的塑料瓶中滴入几滴浓氨水,在
瓶盖内侧贴一小张滤纸,向滤纸上滴几滴浓盐酸后,立
即将瓶盖拧上,观察现象。
现象记录:_____________________________________
___________________________________________________。
实验结论:_____________________________________
___________________________________________________。
氨与氯化氢的反应
图3.12 氨与氯化氢反应的
实验现象
氨与浓盐酸挥发出来的氯化氢气体反应,生成白色氯
化铵固体。氨同样能与其他的酸反应生成铵盐,如把氨通
入硫酸或硝酸中,就会生成硫酸铵或硝酸铵。铵盐都是晶
体,能溶于水,受热容易分解,分解时一般放出氨。
NH3 + HCl
NH4Cl
2NH3 + H2SO4
(NH4)2SO4
NH3 + HNO3
NH4NO3
88
硫、氮及其循环
第3 章
实验探究
1. 如图3.13 所示,在封管内一端盛有少量白色
氯化铵晶体,小火加热封管内晶体,观察现象。
2. 取氯化铵、硝酸铵和硫酸铵晶体各约1 g,分
别放在三支试管里,各加入2 mL 1 mol·L
—1 氢氧化钠
溶液。加热试管,并将湿润的红色石蕊试纸靠近试管
口上方,观察试纸的颜色变化。
铵盐的性质
编号
现象记录
铵盐的性质
化学方程式或离子方程式
1
2
图3.13 氯化铵受热分解
氯化铵晶体受热时会分解出氨和氯化氢,冷却时,它
们又重新结合生成氯化铵。铵盐能与碱起反应放出氨,实
验室常利用铵盐的这一性质来制备氨和检验NH
+
4 的存在。
氯化铵、硫酸铵(俗称硫铵)、硝酸铵(俗称硝铵)等
都是重要的铵态氮肥,易被植物吸收。
3. 硝态氮肥和硝酸
硝态氮肥是以硝酸盐为主要成分的氮肥,常见的有硝
酸铵、硝酸钠、硝酸钙等。硝态氮肥的水溶性好,肥效快,
但土壤对其吸收能力弱,容易随水流失。
硝酸除了可制取硝态氮肥之外,也是制造炸药、染料、
塑料、硝酸盐等化工产品的重要原料。硝酸是一种很强的
氧化剂,不论稀硝酸还是浓硝酸都有强氧化性,能与几乎
所有的金属(除金、铂等少数金属外)或部分非金属发生
氧化还原反应。
89
3.2
氮及其重要化合物
● 含氮量是衡量氮肥肥效的指标之一。现有三种氮肥:CO (NH2) 2、
NH4NO3 和(NH4) 2SO4。
(1) 通过计算指出哪种氮肥的肥效最高。
(2) 目前CO (NH2) 2(尿素)是使用量最多的氮肥之一;与上述三种
氮肥相比,氨的含氮量更高,然而氨却很少直接施用在土壤中
作为肥料。通过查阅资料,分析上述事实的原因。
● (1) 我们可以通过比较含氮量来确定氮肥肥效的高低。
CO (NH2) 2 的含氮量:
2M (N)
2×14 g·mol
—1
M[CO (NH2) 2]
60 g·mol
—1
=
=0.467
NH4NO3 的含氮量:
2M (N)
2×14 g·mol
—1
M(NH4NO3)
80 g·mol
—1
=
=0.350
(NH4) 2SO4 的含氮量:
2M (N)
2×14 g·mol
—1
M[(NH4)2SO4]
132 g·mol
—1
=
=0.212
从以上数值分析得出,CO(NH2)2 的含氮量最高,其肥效应最好。
(2) 尿素是使用量最多的氮肥之一,主要是由于:尿素的含氮量较其
他氮肥高,肥效也高;尿素在土壤中会与水缓慢反应,生成物可
被作物吸收利用,肥效较其他氮肥持久;尿素属于中性肥料,与
其他氮肥相比,对土壤一般无不良影响;等等。
在土壤中通常很少直接施用氨水的原因,可从以下方面思考:氨
水具有碱性;氨水的挥发性很强,容易造成氮元素的损失;氨具
有刺激性气味;氨极易溶于水,雨水也很容易使氨流失;氨水为
液态,储存、运输和使用均不如固态氮肥方便;等等。
学习指南
例题导引
问题:
分析:
Cu + 4HNO3( 浓 )
Cu(NO3)2 + 2NO2↑ + 2H2O
3Cu + 8HNO3( 稀 )
3Cu(NO3)2 + 2NO↑ + 4H2O
4. 尿素
尿素是一种重要的有机氮肥,为白色结晶,易溶于水,
水溶液呈中性。尿素与水反应的生成物NH4
+ 和HCO3
—均可
被作物吸收利用,施用后对土壤一般无不良影响。尿素还
可作为反刍动物的蛋白质补充饲料,尿素中的氮在反刍动
物胃中,经微生物酶作用转化成氨基酸等,最后形成组织
蛋白和奶蛋白等。
90
硫、氮及其循环
第3 章
1. 发射卫星的运载火箭,其推进剂引燃后发生剧烈反应,产生大量高温气体
从火箭尾部喷出。引燃后产生的高温气体主要有CO2、H2O、N2、NO 等,这些
气体均为无色,但在卫星发射现场却可看到火箭尾部喷出大量红色气体,产生红
色气体的原因是( )。
(A) 高温下N2 遇空气生成NO2
(B) NO 遇空气生成NO2
(C) CO2 与NO 反应生成CO 与NO2 (D) NO 和H2O 反应生成H2 和NO2
2. 某些含氮物质之间的转化关系如下所示:
NH3
N2
NO
NO2
HNO3
—3
+2
+4
+5
0
(1) 请圈画出属于氮的固定的转化关系。
(2) 写出N2 转化为NH3 的化学方程式。
(3) 上述转化关系中哪些物质可作为氮肥?
(4)在上述转化关系中用箭头再标注至少一种转化关系,并补全反应条件和
反应物。
3. 阅读下图,回答下列问题。
(第3 题)
(1) 说出20 世纪以来世界人口增长与耕地面积分别呈现的变化趋势。
(2) 为满足生存需求,在现有的耕地上人类采取哪些措施来养活更多的人?
请查阅资料,分析这些做法的利与弊。
练习巩固
91
3.3
硫循环和氮循环
身边的有机化合物
第7 章
3.3
人类的文明历程与自然环境的变化密切相关。自然界
中,陆地、海洋、大气中的硫元素和氮元素,通过各种循环
建立起生态平衡。工业革命以来,过度的资源开发和利用,
打破了自然界的平衡。生态危机是人类生存与发展的最大威
胁,人类必须探索新的发展道路。下面我们就通过认识自然界
中硫、氮的循环,探讨人与自然和谐共处的出路和前景。
知道酸雨的成因、主要危害及
其防治措施
知道人类活动对硫循环和氮循
环的影响
感悟化学对促进人与自然和谐
相处的意义
认识物质及其转化在促进社会
文明进步、自然资源综合利用
和环境保护中的重要价值
学习聚焦
知识回放
● 二氧化硫的化学性质
● 一氧化氮、二氧化氮的化学
性质
硫循环和氮循环
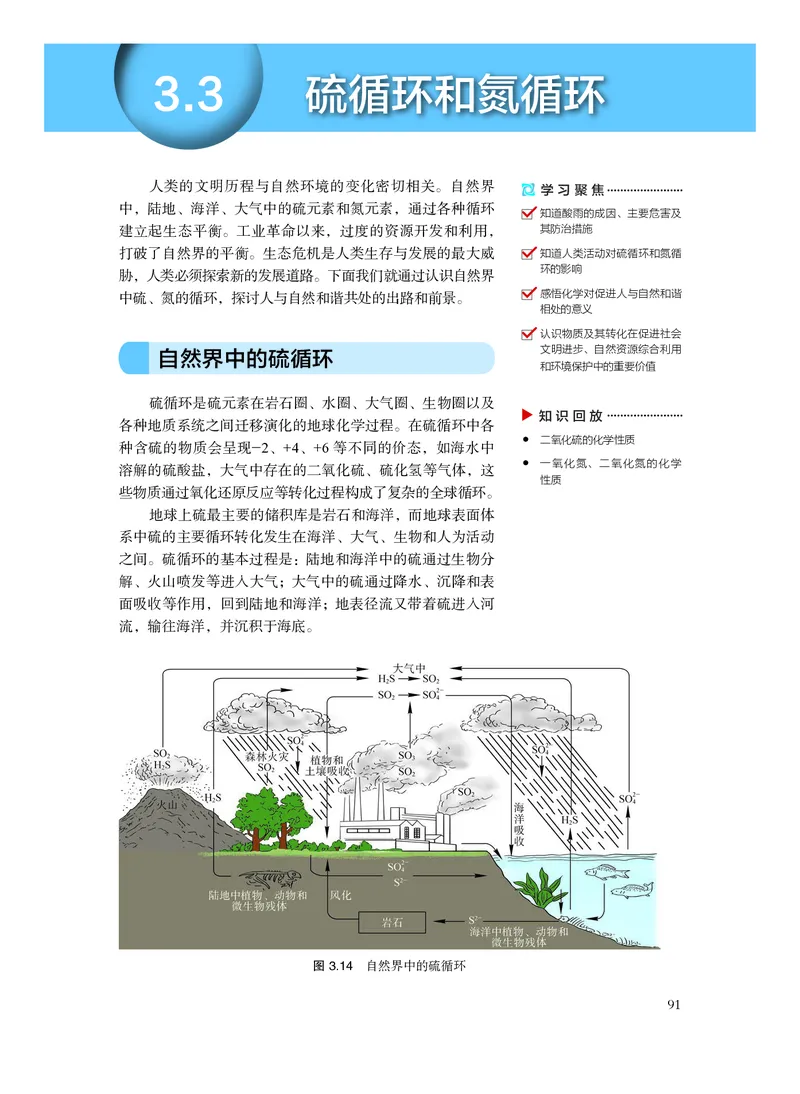
硫循环是硫元素在岩石圈、水圈、大气圈、生物圈以及
各种地质系统之间迁移演化的地球化学过程。在硫循环中各
种含硫的物质会呈现—2、+4、+6 等不同的价态,如海水中
溶解的硫酸盐,大气中存在的二氧化硫、硫化氢等气体,这
些物质通过氧化还原反应等转化过程构成了复杂的全球循环。
地球上硫最主要的储积库是岩石和海洋,而地球表面体
系中硫的主要循环转化发生在海洋、大气、生物和人为活动
之间。硫循环的基本过程是:陆地和海洋中的硫通过生物分
解、火山喷发等进入大气;大气中的硫通过降水、沉降和表
面吸收等作用,回到陆地和海洋;地表径流又带着硫进入河
流,输往海洋,并沉积于海底。
自然界中的硫循环
图3.14 自然界中的硫循环
92
硫、氮及其循环
第3 章
氮循环是自然界中又一种重要的物质循环方式,其主
要的化学过程如下:
空气中的氮气与氧气在放电条件下反应,使游离态的
氮转化为化合态的氮。
自然界中,通过这种固氮所形成
的含氮化合物很少,大部分是来自生
物固氮。生物固氮酶将空气中的氮气
还原为氨,氨溶于水后产生铵根离子,
被植物吸收。
铵根离子经土壤中细菌的作用转
化为硝酸根离子,这种氧化过程称为
硝化作用。硝酸根离子是可被植物吸
收的另一种形态。
自然界中的氮循环
(硝酸盐)
N2
0
NO
+2
NO2
+4
HNO3
+5
NO
—
3
+5
图3.15 自然界中的氮循环
陆地火山喷发,使地壳和岩浆中的硫以二氧化硫、硫化
氢、硫酸盐等形式排入大气;陆地和海洋中的一些动植物腐
败后,其机体中的硫经微生物的厌氧活动还原产生硫化氢,
并向大气释放;海水中硫酸盐也会随着波浪翻涌进入大气。
大气中的二氧化硫、硫化氢被氧化成硫酸根离子,随
降水落到陆地和海洋;大气中的二氧化硫、硫酸根离子还
可经自然沉降被土壤、植物或海水吸收,或随大气运动参
与海陆间循环。
人类的工农业活动对硫循环有重要影响。燃烧、冶炼
含硫矿物而排入大气的二氧化硫远高于因风化作用进入大气
圈和水圈的硫,城市和工矿区的大气二氧化硫污染和酸雨灾
害引起了各国的普遍关注。
N2
0
NH3
—3
NH
+
4
—3
固氮酶
H2O
NH
+
4
—3
NO
—
2
+3
NO
—
3
+5
土壤中的细菌
土壤中的细菌
93
3.3
硫循环和氮循环
在氧气不足的条件下,土壤中的细菌又将硝酸根转化
为氮气,且从土壤中释放出来。这是硝酸根在土壤中的细
菌作用下被还原的过程,称为反硝化作用。
拓展视野
汽车尾气对城市大气环境的污染引起了广泛的关注,尾气中的氮氧化物主
要指一氧化氮(NO)、二氧化氮(NO2)。一氧化氮很容易被氧化成有刺激性气
味的二氧化氮。对儿童来说,氮氧化物可能会造成肺部发育受损。研究指出,长
期吸入氮氧化物可导致肺部构造改变。二氧化氮受日光照射,光解产生原子氧
(
光
NO2
NO + O),原子氧与氧气结合生成臭氧(O2 + O
O3),氧与臭
氧将烃类物质氧化成醛、酮等刺激性很强的物质,光化学烟雾就是这些气体的
混合物。
1943 年美国洛杉矶的光化学烟雾事件,持续数十天之久,这种烟雾使人眼
睛发红、咽喉疼痛、呼吸憋闷、头昏、头痛,不少老人因呼吸衰竭而死亡。光化
学烟雾还使远离城市100 km 以外的海拔2 km 高山上的大片松林枯死,柑橘减
产。这是世界上的第一次光化学污染事件。此后,日本、英国、加拿大、澳大利
亚等国的城市曾出现过光化学烟雾。
目前,国际上减少汽车尾气污染的措施主要有以下三种:用甲醇、液化气代
替汽油;安装汽车尾气净
化器,将氮氧化物转化
为中性的、无污染的氮
气,排向大气;使用高效
燃料电池的汽车替代燃气
汽车。
汽车尾气与氮氧化物
总之,氮循环是大气中的氮气经微生物等作用进入土
壤与海洋,为动植物所利用,最终又在微生物的参与下返
回大气,如此反复循环,建立起的平衡。氮循环为动植物
的生长提供所需的营养物质,对生物和人类活动具有重要
意义。
图3.16 氢燃料电池汽车结构示意图
NO
—
3
+5
NO
+2
N2O
+1
N2
0
土壤中的细菌
土壤中的细菌
土壤中的细菌
94
硫、氮及其循环
第3 章
1. 在硫循环和氮循环中涉及自然界中的众多物质,从
氧化还原反应等视角分析,硫、氮元素能够形成循环的奥
秘有哪些?
2. 碳循环是自然界另一重要的元素循环,该循环对地球
自然环境产生了哪些重要影响?
大量的二氧化硫散发到大气中,被雨水吸收就会形成
对自然界危害较大的酸雨。
未污染的大气降水的pH 一般小于7,大于5.6,这是
由于溶解了二氧化碳气体的缘故。如果其他酸性污染物也
溶于降水中,其pH 会明显变小。当大气降水的pH 小于5.6
时,我们就称之为酸雨。
酸雨的成因很复杂。化学分析表明,酸雨中含有硫酸、
硝酸和有机酸,多数情况下以硫酸为主。硫酸和硝酸是由
人为排放的二氧化硫和氮氧化物(主要指一氧化氮和二氧
化氮)转化而成的。
空气中的二氧化硫溶于水生成亚硫酸,亚硫酸被氧化生
成硫酸。空气中少量的二氧化硫在催化剂(烟尘中的金属氧
化物)作用下,被氧化成三氧化硫,三氧化硫溶于水也形成
硫酸。空气中的二氧化硫主要来自含硫的煤和石油的燃烧。
酸雨
图3.17 酸雨形成示意图
SO2
H2SO3
H2SO4
NO
NO2
HNO3
H2O
H2O
O2
O2
pH
pH 是表示水溶液酸碱
性的一种标度,其定义为:
pH = —lg c(H
+)。在水溶液中,
H
+ 的浓度越大,pH 越小,
酸性越强。
资料库
想一想
95
3.3
硫循环和氮循环
酸雨中存在硝酸,主要是因为高温燃烧生成的一氧
化氮,排入大气后转化成二氧化氮,遇水则生成硝酸和
亚硝酸。
硫和氮是营养元素,弱酸性降水可溶解地壳中的矿物
质,供动植物吸收,可一旦酸性过强,土壤中的营养成分溶
解后流失,就会对动植物生长产生危害。此外,湖泊、河流
酸化后,鱼的繁殖和发育会受到严重影响;土壤酸化后,植
物生长所必需的细菌大多无法存活,致使农业减产;酸雨还
会伤害植物的新生芽叶或树叶,从而影响其发育生长。
酸雨容易腐蚀建筑材料、金属结构等,使大理石雕像
受损、钢铁表面生锈、古建筑物被破坏。作为水源的湖泊
和地下水酸化后,由于金属的溶出,可能对饮用者的健康
产生有害影响。
如何防治酸雨?减少酸雨的生成,必须控制空气中二
氧化硫、氮氧化物等气体的含量。目前世界上减少二氧化
硫排放量的措施主要有:优先使用低硫燃料,如含硫量较
低的煤和天然气等;对煤和石油进行脱硫,或对它们燃烧
后形成的烟气在排放之前除去硫的氧化物等。
SO2 + H2O
H2SO3
2H2SO3 + O2
2H2SO4
2SO2 + O2
2SO3
SO3 + H2O
H2SO4
催化剂
△
图3.18 酸雨致使树木凋零
酸雨的发现
近代工业革命后,蒸汽机广泛应用于生活中,通过锅炉烧煤产生蒸汽推动机
器。火力电厂星罗棋布,燃煤数量日益增加。由于煤炭中含硫,在燃烧过程中会
产生二氧化硫气体,进而形成酸雨。17 世纪英国作家约翰·伊夫林(John Evelyn,
1620—1706)首次注意到大理石被酸性大气腐蚀的现象。
1852 年,英国化学家罗伯特· 安格斯· 史密斯(Robert Angus Smith,
1817— 1884)分析了工业城市曼彻斯特的酸雨和大气污染之间的关联。他对酸雨
进行了20 多年持续研究,发现了酸雨对金属的腐蚀、城市雨水中含硫酸和酸性较
强的硫酸盐等,并在《空气和降雨:化学气候学的开端》一书中首次提出了“酸
雨”的概念。
化学史话
96
硫、氮及其循环
第3 章
1. 氮氧化物是造成酸雨的原因之一,说出天然和人为排
放氮氧化物的主要途径。
2. 阅读酸雨对金属和大理石危害的资料,讨论如何减少
酸雨对室外建筑的侵蚀。
挪威科学家还发现英国酸雨长距离转移到挪威的过程,这种转移使酸雨逐渐
扩展到北美和亚洲,进而成为全球性的环境问题。1979 年,30 多个国家共同签署
了《远程越界空气污染公约》,自此各国都加大了对酸雨的预防与监测规模。20 世
纪80 年代以来,我国在全国开展了大规模的酸雨调查与监测,酸雨被列入气象观
测项目。
生态兴则文明兴,生态衰则文明衰。古今中外,这
方面的事例很多,你能举出一些实例吗?
自然界中,陆地、海洋、大气中的硫、氮、碳等元素,
建立起各自的循环和平衡。随着社会的发展,过度开采、
消耗资源,破坏了自然界的平衡,从而出现了气候变暖、
资源减少、臭氧层破坏、生物多样性减少、土地荒漠化等
现象,使生态系统不断遭受破坏。很明显,不受限制的增
长方式是不可持续的,因此人类开始开发新能源和新技术,
尽可能减少人为的二氧化硫和氮氧化物大量排放,建立人
与自然和谐共处的生态文明。
生态文明是人类社会进步的重大成果,是实现人与自然
和谐共生的必然要求。人与自然的关系是人类社会最基本的
关系。自然界是人类社会产生、存在和发展的基础和前提,
人类社会可以通过社会实践活动有目的地利用、改造自然,
但人类的行为方式必须符合自然规律。
建立人与自然的和谐共生
图3.19 浙江湖州桑基鱼塘
系统体现人与自然和
谐发展
想一想
想一想
97
3.3
硫循环和氮循环
环境化学是在化学科学的传统理论和方法基础上发展起来的,以化学物质在
环境中出现而引起的环境问题为研究对象,以解决环境问题为目标而兴起的一门
综合性、基础性的新型学科。环境化学主要应用化学的基本原理和方法,研究大
气、水、土壤等环境介质中化学物质的特性、存在状态、化学转化过程及其变化
规律、化学行为与化学效应及其控制的科学。它是环境科学的核心组成部分,也
是化学科学的一个新的重要分支。
环境化学
链接学科
● 阅读图3.15 后,回答下列问题。
(1) 大气中的氮以什么形式存在?图3.15 中显示了哪些氮的固定
途径?
(2) 土壤中的硝酸盐会被细菌分解。有一种脱氮硫杆菌能够利用土
壤中的硫化物来分解硝酸盐,其主要化学反应原理如下:
5K2S + 8KNO3 + 4H2O
4N2↑ + 5K2SO4 + 8KOH
脱氮硫杆菌
上述过程的发生改变了土壤的成分,从而对农业生产带来一定
的不利影响,请选择某一角度进行简要说明。
● (1) 大气中的氮以游离态N2 的形式存在,图3.15 主要展示了天然
固氮、人工固氮等两类氮的固定途径。
(2) 土壤中的硝酸盐被脱氮硫杆菌与硫化物分解成N2,使得土壤中氮
元素流失,肥力下降。同时土壤中的硝酸盐与硫化物在脱氮硫杆菌
的作用下发生反应,生成KOH,使得土壤pH 增大,易盐碱化。
学习指南
例题导引
问题:
分析:
练习巩固
1. 在生产、生活中,与NO2 的大量排放有关的环境问题是( )。
(A) 酸雨
(B) PM2.5
(C) 温室效应
(D) 白色污染
98
硫、氮及其循环
第3 章
编号
比较
氮循环
硫循环
①
异
氮元素会进入大气
硫元素不会进入大气
②
氮元素可以有机化合物形式参与循环
硫元素都以无机物形式参与循环
③
同
人类活动对氮循环和硫循环都造成了巨大影响
④
氮循环和硫循环对环境的影响都能导致温室效应
4. 二氧化硫在空气中经过一系列的化学反应最终形成硫酸。许多硫酸分子
先聚集在一起形成微滴,然后许多硫酸微滴结合在一起形成较大微滴,并进一
步形成气溶胶。这些酸性气溶胶在空气中会与碱性物质反应产生硫酸盐气
溶胶。
(1) 请分别写出硫酸与氨(少量或过量)反应的化学方程式。
(2) 请简述环境检测部门通过测定硫酸根离子的浓度,而不是测定pH 来
反映最初产生硫酸的量的原因。
2. 阅读短文,将方框中合适的微粒符号填入横线上。
火山爆发、化石燃料的燃烧等会产生________。在大气中,这种物质一部
分被植物吸收,一部分与大气中的水反应,最终形成________,随大气降水落
入土壤或水体中,以________ 的形式被植物的根系吸收,转变成蛋白质等有机
化合物,进而被各级消费者所利用,动植物的遗体被微生物分解后,又能将硫
元素释放到土壤或大气中,这样就形成较为完整的元素循环。此外,微生物的
分解也会产生另一种含硫物质进入大气,该物质是________。
S H2S SO2 SO3 H2SO4 SO
2—
4 H2SO3
3. 氮循环和硫循环是自然界中两种重要的元素循环过程。请选出关于这两
种循环的正确评价。
99
3.3
硫循环和氮循环
素养提升
■ 借助实验理解硫、氮及其重要化合物的性质及其变化,能对相关实验现象作出合
理的解释,运用化学符号描述硫、氮及其重要化合物的化学变化。
■ 根据硫、氮及其重要化合物的性质,了解硫循环、氮循环的基本过程,解释酸雨
形成的原因,分析酸雨的防治方法。
■ 运用所学知识探讨人类活动给社会可持续发展带来的双重影响,建立人与自然和
谐共生的观念;能依据实际条件并运用所学的化学知识与方法解决生产、生活中
的化学问题。
本章复习
99
核心框图
练习巩固
1. 不能由单质之间直接化合得到的化合物是( )。
(A) FeS
(B) H2S
(C) SO3
(D) FeCl3
2. 在氧化还原反应中,所含硫元素只能表现出还原性的物质是( )。
(A) H2S
(B) SO2
(C) H2SO3
(D) H2SO4
3. 在检验SO
2—
4 的过程中,下列操作中正确的是( )。
(A) 先加入稀硝酸,然后再加硝酸钡,产生白色沉淀,证明有SO
2—
4
(B) 先加入硝酸钡,然后再加稀硝酸,沉淀不溶解,证明有SO
2—
4
(C) 先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO
2—
4
(D) 先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO
2—
4
100
硫、氮及其循环
第3 章
100
100
4. 下列关于铜与硝酸反应的叙述中,正确的是( )。
(A) 若为稀硝酸,反应不进行
(B) 氮元素全部被还原
(C) 若为浓硝酸,还原产物为NO
(D) Cu(NO3)2 是氧化产物
5. 随着汽车销量的增加,空气受到了污染。汽车尾气
装置里,气体在催化剂表面吸附与解吸作用的过程如图所
示。下列说法中,正确的是( )。
(A) 反应中NO 为氧化剂
(B) 汽车尾气的主要污染成分包括CO、NO 和N2
(C) NO 和O2 必须在催化剂表面才能反应
(D) 催化转化总化学方程式为
催化剂
2NO + O2 + 4CO
4CO2 + N2
6. 以前,某地使用的柴油中含约2%(质量分数)的硫。现在,该地使用的柴油都
是超低硫柴油(ULSD),含有不到50 ppm(ppm 是比率的表示,1 ppm 即百万分之一)
的硫。
(1) 柴油含有C12H26(一种烃),写出C12H26 燃烧释放二氧化碳和水的化学方程式。
(2) 含硫柴油燃烧会污染空气,写出有关的化学方程式。
(3) 用质量分数表示50 ppm,ULSD 比原有柴油中硫含量降低了多少倍?
(4) 按照可持续发展理念,你认为可以如何进一步调整柴油的成分。
7. 某工厂运输氨的管道出现小孔导致氨泄漏,技术人员常常用一种挥发性液体进行
检查,该液体最有可能是( )。
(A) 浓盐酸
(B) 烧碱
(C) 浓硫酸
(D) 碳酸钠溶液
8. 下图显示了酸雨形成的两种主要途径。
(1) X 是空气的主要成分之一,请推断A 的化学式。
(2) 写出反应④的化学方程式。
9. 随着工业的发展,酸雨已经成为全球性的环境问题。
(1) 说出检验某次降雨是否为酸雨的方法。
(2) 某酸雨样品放置一段时间后,酸性略有增强,请分析其原因。
(3) 二氧化硫、氮氧化物等是造成酸雨的主要原因,了解我国采取了哪些措施来减
排这些气体。
(第8 题)
(第5 题)
101
4.4
化 学 键
101
*10. 阅读短文,思考下列问题。
Volatile sulphur compounds are emitted both by terrestrial and marine biota. The
marine emissions are almost exclusively in the form of DMS, whereas the emissions from
land are in a variety of chemical species, including H2S, DMS, methanethiol, CS2, COS
and others. This difference is related to the biological processes which are responsible
for the production of the sulphur volatiles. Most sulphur at the Earth’s surface is present
as sulphate, which is the thermodynamically stable form of sulphur in the presence of
oxygen. Sulphate is reduced by organisms through two mechanisms, “assimilatory” and
“dissimilatory” sulphate reduction. The dissimilatory pathway is restricted to sulphate-
reducing bacteria in anaerobic environments; due to physical and microbial restrictions
only a small fraction of the H2S produced by this process can escape to the atmosphere.
The products of the assimilatory pathway are a variety of organosulphur compounds, the
largest fraction being the amino acids cysteine and methionine, which are incorporated into
proteins.
(短文取自:Robert J. Charlson, James E. Lovelock, Meinrat O. Andreae, et al. Oceanic
phytoplankton, atmospheric sulphur, cloud albedo and climate[J]. Nature, 1987, 326:
655 ~ 661.)
(1) What are the major sulfur compounds emitted by land and sea life?
(2) What is the main form of sulfur on the earth’s surface?
体验 · 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制作成海报、演示
文稿,进行分享和交流。
我们在研究、治理大气污染的同时,也应重视室内的空气质量。动手制作空气
净化器中的过滤、吸附、光催化等模块,并进行相关效果的检测,了解改善室
内空气质量的方法和途径。
二氧化硫是一种大气污染物,因此属于空气质量预报的项目。请查询本地空气
质量报告,记录每日二氧化硫的浓度变化并绘制曲线。对数据进行如下分析:
一周内二氧化硫浓度日平均值之间的波动、本地6 月与12 月二氧化硫浓度月平
均值之间的差异及其成因等。
硝酸是一种重要的基础化工原料。在硝酸工业的发展过程中,先后出现多种工
业制法。例如,早在17 世纪就用钠硝石与浓硫酸共热制得硝酸;或用电弧使空
气中氮气与氧气直接化合生成一氧化氮,一氧化氮与氧气化合生成二氧化氮,
最后用水吸收而得硝酸。请搜集资料,通过对比分析,比较上述方法的优缺点。
102
硫、氮及其循环
第3 章
102
测定物质的组成,确定其化学式是化学研究的重要内容,用化学方法测定物质化学
组成是确定其化学式的一种常用方法。
活动目标
(1) 理解结晶水合物中结晶水含量测定的基本方法。
(2) 学会灼烧、在干燥器中进行冷却等实验操作。
(3) 了解恒重操作。
(4) 知道实验误差的形成和实验相对偏差的计算。
活动指导
(1) 原理分析
我们知道,硫酸铜晶体是一种蓝色的硫酸盐,其组成中含一定量的结晶水。许
多结晶水合物受热会失去结晶水,硫酸铜晶体(因结晶水含量待测定,设化学式为
CuSO4·xH2O)失水的化学方程式为:
CuSO4·xH2O
CuSO4 + xH2O
1 mol
x mol
△
称取一定质量的硫酸铜晶体,将其加热失去全部结晶水后再进行称量,就可以知道
硫酸铜晶体中硫酸铜的质量和结晶水的质量,然后根据硫酸铜和水的摩尔质量,计算出
1 mol 硫酸铜晶体中含结晶水的物质的量:
m(CuSO4)
M(CuSO4)
m(H2O)
M(H2O) =1 ∶ x
∶
(2) 完全失水的确定
虽然硫酸铜晶体加热失去结晶水后,晶体会由蓝色变成白色,但用肉眼来观察,
以蓝色的晶体全部变成白色作依据,误差太大。化学实验中,通过恒重操作(图3.20),
以确保硫酸铜晶体中结晶水全部失去。即我们在完成第一次加热、冷却、称量后,再
进行第二次加热、冷却、称量;如果第二次的质量仍在减小,还要再进行第三次加热、
冷却、称量,直到连续两次称量的结果差值不超过实验所规定的偏差为止。根据本实
验称量仪器的精度,达到本实验恒重的要求为两次称量的结果相差不得超过0.001 g。
如何测定硫酸铜晶体中结晶水的含量
项目学习活动
103
(3) 实验步骤
① 用研钵轻轻研磨少量硫酸铜晶体备用。
② 准确称量瓷坩埚的质量,记为m0 g。(精确至0.001 g,下同)
③ 在瓷坩埚中称量约2 g 硫酸铜晶体,记为m1 g。
④ 用坩埚钳把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变
白,迅速把瓷坩埚移至干燥器中冷却到室温,再称量。
⑤ 重复步骤④操作,直至前后两次称量结果相差不超过0.001 g 为止,记录最后一
次称量的质量为m2 g。
⑥ 另取硫酸铜晶体,重复上述②~⑤的操作,进行数次实验。
图3.20 恒重操作
名称
质量/g
第一次
第二次
第三次
瓷坩埚质量(m0)
瓷坩埚和硫酸铜晶体质量(m1)
瓷坩埚和无水硫酸铜质量(m2)
硫酸铜晶体质量(m1—m0)
无水硫酸铜质量(m2—m0)
结晶水质量(m1—m2)
数据处理和结论:
设1 mol 硫酸铜晶体中有x mol 结晶水。用表格数据计算x 值:第一次
,
104
第二次
,第三次
。1 mol 硫酸铜晶体中含有
mol 水
(平均值精确至0.01)。
(4) 实验偏差的原因分析
1 mol 硫酸铜晶体中含结晶水5 mol,这是一个参考值。固体试样的读数可精确到
0.001 g,考虑到硫酸铜和水的摩尔质量的精确度(严格地说,铜和氢的摩尔质量应使用
63.55 g·mol
—1 和1.008 g·mol
—1),假如实验结果测得1 mol 硫酸铜晶体的结晶水含量
在4.90 ~5.10 mol 范围内,仍可认为是合理的结果。
如果测定结果与参考值偏差很大,那就应寻找原因。反思自己的实验过程,找到造
成偏差的具体原因。
活动要求
完成你的项目活动并形成一份项目报告。在报告中介绍你的操作步骤,记录并分析
数据,简单分析误差,思考整个项目活动的心得。
活动反思
(1) 很多物质受热能分解,比如碳酸氢钠。食用小苏打中含有碳酸氢钠,你能否在
经历本项目活动后,设计方案并完成食用小苏打中碳酸氢钠含量测定的活动。
(2) 热重分析法也是研究晶体组成的一种仪器分析方法。查阅资料,研究热重分析
法,并向同学介绍这种方法的应用。
原子结构和化学键
存放有元素单质及化合
物实物样品的元素周期表,
将您带入化学元素的世界。
摄于华东师范大学。
第4 章
105
元素周期表和元素周期律
原子结构
核外电子排布
化学键
4.1
4.2
4.3
4.4
106
人
类赖以生存的大千世界是由众多物质组成的,而数量如此庞大
的物质却仅由百余种化学元素组成。这些元素的性质是否具
有一定的规律性?元素的原子之间是如何结合成种类繁多、性能各异
的物质?物质的化学性质又与原子的核外电子排布存在什么关系?……
在本章中,我们将探索元素性质的周期性递变规律,揭开原子
微观结构的奥秘和发现原子核外电子排布的规律,理解原子是如何
通过相互作用构建物质的。只有充分认识这些问题并掌握规律,才
能创造出更多、更好的物质为人类服务。
元素周期表和元素周期律
107
4.1
身边的有机化合物
第7 章
4.1
元素周期表和元素周期律
19 世纪初,许多新的元素被相继发现,化学家开始
关注这些元素在化学性质和物理性质上的相似性和递变
性。1869 年,俄国化学家门捷列夫(Dmitry Ivanovich
Mendeleyev,1834— 1907)在当时已知的63 种元素的性
质和原子量
①相互关系的基础上,编制了一份元素周期表。
随着不断地研究和修正,现代的元素周期表逐渐发展为图
4.1 和附录Ⅳ所示的这种常见形式。
① 现在也称相对原子质量。
元素周期表
当你走进图书馆,你会发现书籍是分类摆放的。想象
一下,如果图书馆里的书籍都是混乱排列的,你要从中挑
选需要的图书将会何等困难。百余种不同的元素,是构成
大千世界中所有物质的“基石”。那么,科学家们是如何设
计元素周期表对元素进行编排的?元素的性质又会遵循怎
样的变化规律?
知道元素周期表的结构
结合有关数据和实验事实,认
识同周期和同主族元素性质的
递变规律
感悟元素周期表在学习元素及
其化合物知识与科学研究中的
重要作用
学习聚焦
知识回放
● 元素
● 硫的化学性质
● 氯气的化学性质
● 卤素单质的活泼性
图4.1 国际纯粹与应用化学联合会(IUPAC)推荐使用的元素周期表
发布时间:
2018 年12 月
原子结构和化学键
第4 章
108
化学史话
元素周期表的发展
元素周期表
早在1829 年,当时已发现54 种元素,德国化学
家德贝莱纳(Johann Wolfgang Döbereiner,1780—
1849)把其中15 种元素按3 种元素为一组,编成5 组。
他发现每3 种元素的化学性质很相似,称为“三
素组”。后来,德国化学家迈尔(Julius Lothar Meyer,
1830— 1895)又发表了“六元素表”。
八音律
英国化学家纽兰
兹(John Newlands,
1837—1898)将所有已
知的元素,按照原子
量的递增次序,形成
垂直的7 族,和音符
的八度相似。他发现
每一族中第八种元素
的物理性质与化学性质
和第一种元素相似,这
是科学家首次发现元素
的性质规律,但仍未揭
示元素分类的本质。
俄国化学家门捷列夫把当时已知的元素都制成类似
纸牌的卡片,每张卡片上列出元素符号、化学性质和物理
性质,然后按原子量的递增次序进行排列。1869 年,他
编制了一份元素周期表,即根据元素
的原子量及其相似的化学性质所制定
的元素系统表,表中化学性质相似的
元素排成同一横行。他还在表中为若
干尚未发现的元素预留了空位。1871
年,他把竖排的表格改为横列,突出
了元素族和周期的规律性;划分了主
族和副族,使之基本具备了现代元素
周期表的形式。
Li
Ca
P
S
Cl
Na
Sr
As
Se
Br
K
Ba
Sb
Te
I
图4.3 门捷列夫编制的元素周
期表
三素组
1869 年
1865 年
1829 年
图4.2 门捷列夫
元素周期表和元素周期律
109
4.1
美国核化学家西博格(Glenn Theodore
Seaborg,1912—1999)等人发现了95 ~
102 号和106 号的超铀元素,于是他对元
素周期表做了修改,并把这些超铀元素放
置在元素周期表的底部。
从20 世纪中后期至21 世纪前期,
科学家合成出的新元素已经将第7 周
期填满,元素周期表的边界也已推至
118 号元素。下一种新元素将是……
0 族元素的发现
超铀元素
新元素的发现
莫塞莱定律
1894 年,英国物理学家瑞利(Third
Baron Rayleigh,1842—1919)和英国化
学家拉姆齐(William Ramsay,1852—
1916)从空气中
分离出氩。后来,
拉姆齐又发现了
氦、氖和氪这些稀
有气体,因而在
元素周期表中建
立了一个新的族。
英国物理学家莫塞莱(Henry
Moseley,1887—1915)由X 射
线实验结果提出原子序数的概
念,他依据原子序数的递增来排
列元素,而不再根据原子量排序,
解决了原来按原子量增大顺序排
列出现的元素倒置的困惑。这种
排列方法称为莫塞莱定律。
20 世纪
中后期
20 世纪
中期
1914 年
1894 年
随着量子力学理论的创立和发展,人们逐渐认识到元素周期律的实质是与原子
核外电子排布密切相关的,特别是最外层电子排布。
图4.4 瑞利
原子结构和化学键
第4 章
110
元素在元素周期表中排列的序号,我们称为原子序数。
在元素周期表中,原子序数从左到右、从上到下都是依次
递增的。元素周期表中的横行称为周期,纵列称为族。
元素周期表中共有7 个周期,其中第1、2、3 周期称为短
周期,第4、5、6、7 周期称为长周期。周期表中有18 个纵列,
依次为1 ~18 族。其中,第1、2、13 ~17 族,即ⅠA ~ⅦA
族,为主族元素;第11、12、3 ~7 族,即ⅠB ~ⅦB 族,为
副族元素;第8、9、10 族,为第Ⅷ族;第18 族为0 族。
① 稀有气体元素的原子半径测定和相邻非金属元素的依据不同,数据作为参考但不具可比性,故无需绘出。
1. 随着原子序数的递增,依次列出第2、3 周期主族元素的主要化合价(指最高正化
合价和最低负化合价),找出其中变化的规律。
2. 原子半径是描述原子大小的参数,根据表4.1 中数据,在图4.5 中画出随着原子序数
的递增,3 ~9 号、11 ~17 号元素的原子半径变化的折线图,分析原子半径变化的规律。
对原子序数为1 ~18 的元素进行研究,有助于我们认
识更多种元素之间的关联和元素性质变化的规律性。
元素周期律
表4.1 原子序数为1 ~ 18 的元素的原子半径①
原子序数
元素名称
元素符号
原子半径
pm
原子序数
元素名称
元素符号
原子半径
pm
1
氢
H
37
10
氖
Ne
154
2
氦
He
140
11
钠
Na
186
3
锂
Li
152
12
镁
Mg
160
4
铍
Be
89
13
铝
Al
143
5
硼
B
82
14
硅
Si
117
6
碳
C
77
15
磷
P
110
7
氮
N
75
16
硫
S
102
8
氧
O
74
17
氯
Cl
99
9
氟
F
71
18
氩
Ar
192
阅读元素周期表(图4.1 或附录Ⅳ)。
(1) 指出钠、硫、氯、铁等元素在周期表中的位置。
(2) 第2、3 周期中典型金属元素和典型非金属元素的出现是否有规律可循?
主族的别名
主族元素中,ⅠA ~ⅦA
族也分别称作碱金属、碱土
金属、硼族、碳族、氮族、
氧族和卤族。
资料库
书写表达
想一想
元素周期表和元素周期律
111
4.1
图4.5 第2、3 周期主族元素的原子半径随原子序数的变化
举例说明氯气和硫的氧化性哪一个更强。预测氯元素和
硫元素的非金属性的相对强弱。
1. 同周期元素性质的递变规律
通过上述讨论我们知道,同周期元素(除稀有气体元
素外),从左向右,随着原子序数的递增,原子半径依次减
小,呈现周期性的变化。那么元素的化学性质是否也有类
似的周期性变化规律呢?
实验探究
1. 取一小块绿豆大小的金属钠,用滤纸吸干其表面的煤油,将其投入滴有
2 滴酚酞试液的盛有100 mL 水的烧杯中;另取一小段镁带和铝条,用砂纸打磨
除去它们表面的氧化膜,分别放入两支试管中,各加入2 mL 水,再滴入2 滴
酚酞试液,加热、观察并记录实验现象。
2. 取一小段镁带和铝条,用砂纸打磨除去它们表面的氧化膜,分别放入两
支试管中,再向试管中各加入2 mL 2 mol·L
—1 盐酸,观察并记录实验现象。
3. 在试管中加入2 mL 0.5 mol·L
—1 Al2(SO4)3 溶液,然后滴加氨水,直至
不再产生白色Al(OH)3 沉淀为止。将所得沉淀分装在两支试管中,向一支试管
钠、镁、铝元素性质的递变
我们可以发现,随着原子序数的递增,元素的主要化
合价、原子半径均呈现出周期性变化。
金属性和非金属性的
相对强弱
通常,元素非金属性越
强,元素原子得电子能力越
强,元素的单质越容易与氢
气化合,生成的气态氢化物
越稳定,元素最高价氧化物
对应水化物的酸性越强。元
素金属性越强,元素原子失
电子能力越强,元素的单质
与水(或酸)反应越容易置
换出氢气,元素最高价氧化
物对应水化物的碱性越强。
资料库
想一想
原子结构和化学键
第4 章
112
中滴加1 mol·L
—1 硫酸,向另一支试管中滴加2 mol·L
—1 NaOH 溶液。边滴
边振荡,观察实验现象。用2 mL 1 mol·L
—1 MgSO4 溶液代替Al2(SO4)3 溶液做
上述实验,观察现象,并进行比较。
实验表明(图4.6):金属钠与冷水发生剧烈反
应,烧杯内溶液变红;金属镁与冷水反应缓慢,加
热后镁带表面有少量气泡,试管内溶液变红;金属
铝加热后与水的反应也不明显,滴入酚酞试液后溶
液几乎不呈红色。镁与盐酸的反应比铝与盐酸的反
应剧烈得多(图4.7)。
图4.6 钠、镁、铝与水反应的现象
图4.7 镁、铝与盐酸反应的现象
镁
铝
钠
镁
铝
问题:通过实验推断钠、镁、铝元素性质的递变规律。
编号
现象记录
化学方程式或离子方程式
1
2
3
氢氧化铝的两性
氢氧化铝溶于强酸生成相应的铝
盐,也能溶于强碱生成四羟基合铝酸
盐,因此它是一种两性氢氧化物。
2Al(OH)3+3H2SO4
Al2(SO4)3+6H2O
Al(OH)3+NaOH
Na[Al(OH)4]
资料库
元素周期表和元素周期律
113
4.1
表4.2 硅、磷、硫和氯元素的性质比较
元素
Si
P
S
Cl
单质与氢气的化合
高温下反应
磷蒸气与氢气
能反应
加热时反应
光照或点燃时
反应
气态氢化物及其热稳定性
SiH4
很不稳定
PH3
不稳定
H2S
较稳定
HCl
稳定
最高价氧化物对应水化物
的酸性强弱
H2SiO3
弱酸
H3PO4
中强酸
H2SO4
强酸
HClO4
最强酸
利用表4.2 中的信息,分析硅、磷、硫、氯等元素非金属性的相对强弱。
通过对第3 周期元素性质的比较可知:随着原子序数
的递增,同周期元素(除稀有气体元素外),从左到右,元
素的金属性逐渐减弱,非金属性逐渐增强。
2. 同主族元素性质的递变规律
碱金属元素指元素周期表中第1 族(或ⅠA 族)除氢
以外的元素,包括锂、钠、钾、铷、铯和钫。
从图4.9 的实验现象比较锂、钠、钾与水反应的难易程
度。预测锂、钠、钾的最高价氧化物对应水化物碱性的强弱,
你会用什么实验或事实加以验证?
图4.8 第3 周期元素的单质
钠
镁
铝
硅
磷
硫
氯
氩
想一想
想一想
原子结构和化学键
第4 章
114
人们发现碱金属元素的化学性质相似,其单质都能
与氧气、水等发生反应,而最高价氧化物对应水化物一
般都具有很强的碱性。不过,从锂到铯,最高价氧化物
对应水化物的碱性逐渐增强,元素的金属性逐渐增强。
与水发生反应时,铷、铯的反应要比钾、钠的反应更
加剧烈。
碱金属在物理性质上也表现出一定的相似性和递变性,
例如,它们都比较柔软、熔点较低等。
表4.3 碱金属单质的物理常数
碱金属单质
熔点/℃
沸点/℃
密度/ (g · cm
—3 )
Li
180.5
1 341
0.534(293 K)
Na
97.8
881.4
0.968(293 K)
K
63.4
759
0.89(298 K)
Rb
39.3
691
1.532(298 K)
Cs
28.4
668.2
1.878(288 K)
卤族元素是元素周期表中第17 族(或ⅦA 族)元素
的总称,包括氟、氯、溴、碘和砹。在第2 章“海洋中的
卤素资源”我们知道Cl2 可将Br
—、I
—氧化成Br2 和I2,Br2
可将I
—氧化成I2。
完成下表,推测氯、溴、碘三种元素非金属性的相
对强弱。
图4.9 锂、钠、钾与水反应的现象
钠
钾
锂
书写表达
元素周期表和元素周期律
115
4.1
卤族元素单质的化学性质表现出相似性和递变性。从
氟到碘,其气态氢化物的热稳定性逐渐减弱(表4.4),其
最高价氧化物对应水化物的酸性也逐渐减弱。总体而言,
随着原子序数的递增,卤族元素的非金属性逐渐减弱。
对其他主族元素的化学性质进行探讨,也会得到类似
的结论。总之,在同主族元素中,随着原子序数的递增,
元素的金属性逐渐增强,非金属性逐渐减弱。
化学反应
Cl2 与KBr
反应
Cl2 与KI
反应
Br2 与KI
反应
化学方程式
Cl2、Br2 和I2 氧化
性的强弱顺序
氯、溴、碘元素非
金属性的强弱顺序
表4.4 卤族元素单质与氢气的反应及气态氢化物的热稳定性
元素
F
Cl
Br
I
单质与氢气的
化合
冷暗处能
剧烈化合
并发生
爆炸
光照或点
燃时发生
化合
加热时
反应
加热时才能缓
慢反应,同时
生成的碘化氢
又分解
气态氢化物及
其热稳定性
HF
很稳定
HCl
稳定
HBr
较稳定
HI
较不稳定
图4.10 主族元素金属性和非金属性的递变规律
周期
族
1 2 13 14 15 16 17 18
1
2
3
4
5
6
7
非
金
属
性
逐
渐
增
强
金属性逐渐增强
非金属性逐渐增强
金
属
性
逐
渐
增
强
原子结构和化学键
第4 章
116
元素周期表是元素周期律的具体表现,是学习和研究
化学的一种重要工具。我们可以利用元素的性质、在周期
表中的位置和原子结构三者之间的密切关系,来指导我们
对化学的学习和研究。
门捷列夫曾用周期律预言未知元素并得到了证实。现
在人们可以借助元素周期律和元素周期表,来寻找具有特
定性质的新物质和新材料。例如,通常用来合成农药的元
素,如氟、磷、硫、氯、砷等元素在周期表处于一定的区
域,对这个区域里的元素进行充分的研究,有助于创造出
新品种的农药。再如,我们可以在含过渡元素的物质中寻
找催化剂和耐高温、耐腐蚀的合金材料等。
元素周期表的应用
根据图4.11,讨论下列问题。
(1) 分别指出金属性和非金属性最强的元素。在图中适
当位置写出其名称和元素符号。
(2) 在图中红色分界处能找到有何种用途的材料?
图4.11 元素性质的递变
在大量科学研究的基础上,人们归纳出这样一条规律:
元素的性质随着原子序数的递增而呈周期性的变化,这个
规律就称为元素周期律。
元素周期律建立的意义在于它把自然界的元素视为具
有内在联系的统一体,表明元素性质的变化是一个由量变
到质变的过程。元素周期律对于20 世纪原子结构模型的建
立也有重要的启示作用,促进了化学和物理学共同深入研
究原子、分子的结构和性质。
想一想
元素周期表和元素周期律
117
4.1
● 元素①~④是周期表中第2、3 周期的四种元素,表中列出其原
子半径及主要化合价。阅读表中信息后,推测并写出其元素名称
和符号。
● 阅读表中提供的信息,根据元素的主要化合价可以判断,
①和③的最高价均为+1 价,应属于第1 族;②和④的最低价均
为—1 价,且②的最高价为+7,故应在第17 族。根据同主族元
素的原子半径随原子序数的递增而增大的规律可知:③的原子序
数大于①,②的原子序数大于④。在元素周期表第2、3 周期范
围内,①为锂(Li),②为氯(Cl),③为钠(Na),④为氟(F)。
学习指南
例题导引
问题:
分析:
练习巩固
1. 1913 年,英国物理学家莫塞莱提出了莫塞莱定律。该定律要点是元素
若按原子序数大小排列,其性质能更清晰地呈现周期性变化。某元素X 的原子
序数是9,下列原子序数代表的元素中,与X 具有相似化学性质的是( )。
(A) 1
(B) 8
(C) 17
(D)18
2. 你认为下列哪些描述可说明随着核电荷数增加,同主族元素性质的递变
规律?请在□内画“√”。
□原子半径逐渐增大
□金属性逐渐增强
□非金属性逐渐增强
□最高价氧化物对应水化物的碱性逐渐增强
□最高价氧化物对应水化物的酸性逐渐增强
□气态氢化物的热稳定性逐渐减弱
元素
原子半径/pm
最高正化合价
最低负化合价
①
152
+1
②
99
+7
—1
③
186
+1
④
71
—1
原子结构和化学键
第4 章
118
4. 根据元素周期律,请比较:
(1) H3PO4、H2SO4、HClO4 的酸性强弱。
(2) O、Al、S 的原子半径大小。
(3) N、O、F 的非金属性强弱。
(第3 题)
( )
( )
( )
( )
3. 下图是某种形式的元素周期表中氧元素的一格,请你写出这些信息各自
表示的含义。
119
4.2
原子结构
身边的有机化合物
第7 章
4.2
原子结构
按照现代原子结构理论,原子是由位于原子中心的原
子核和核外电子构成的。原子很小,原子核更小。原子核
是由带正电荷的质子和不带电荷的中子构成,每个质子
带1 个单位正电荷,所以原子核的电荷数等于其核内的
质子数。
原子整体显电中性,原子核所带正电荷的电量一定等
于核外电子所带负电荷的总电量。因此,对一个原子而言:
原子序数= 核电荷数= 质子数= 核外电子数
电子的质量很小,相对于质子、中子的质量而言,可以
忽略不计,因此原子的质量主要集中在原子核上。原子核中质
子数(Z)和中子数(N)之和,称为质量数,用符号A 表示。
质量数(A)= 质子数(Z) + 中子数(N)
原子的构成
人类很早就开始观察、利用和改造自然界中形形色色的
物质,也在不断探究物质的性质并尝试寻找其变化规律。随着
科技的发展和进步,人们开始深入思索物质是怎样构成的。历
史上,形成了不少有关物质构成的观点和理论。在本节中,我
们将会了解先哲的观点,体验一段探索物质结构奥秘的历程。
图4.12 构成碳原子的微粒及其性质
了解构成原子的微粒
理解构成原子的微粒数之间的
关系
知道元素、核素、同位素的
含义
理解元素的相对原子质量
学习聚焦
知识回放
● 分子和原子
● 元素
● 摩尔质量
图4.13 化学符号各种角
标的意义
资料库
原子结构和化学键
第4 章
120
化学史话
原子结构的探索历程
发现电子
葡萄干面包模型
古希腊哲学家德谟克利特(Democritus,
约公元前460—公元前370)是原子唯物论的
创立者之一,他认为物质是由极小的、不可分
割的被称为“原子”的微粒构成。中国战国初
墨家创始人墨子(约公元
前468—公元前376)认
为物质被分割是有条件
的,“ 非半弗斫则不动,
说在端”,这种“端”就
是不能再被分割的部分。
然而,古代思想家没能用
任何科学证据去证明这些
观点。
道尔顿原子论
19 世纪初,英国化学
家和物理学家道尔顿(John
Dalton,1766—1844)根据实
验结果,提出了原子论。其主
要内容包括:
(1) 元素是由不可再分的
极小微粒构成,这种微粒称为
原子。原子在一切化学变化中
均保持其不可再分性。
(2) 同一元素的原子在质
量和性质上都相同,不同元素
的原子在质量和性质上都不同。
(3) 不同元素化合时,这
些元素的原子按简单整数比
结合。
英国物理学家汤姆孙(Sir Joseph
John Thomson,1856—1940)通过阴
极射线实验发现原子内有微小而带负
电的粒子存在,他称之为“电子”,
电子也是第一种被确认的粒子。
根据原子是电中性的事实,促使
汤姆孙提出了葡萄干面包原子模型。
他认为原子中的正电荷是均匀地分布
在整个原子的球体内,电子则均匀地
嵌在其中。该原子模型说明原子是有
结构的,打破了原子不可再分的论点。
古代思想家关于物质构成的观点
图4.15 阴极射线管的简化结构图
图4.16 葡萄干面包模型
约公元前
400 年
1803 年
1897 年
1903 年
图4.14 墨子
121
4.2
原子结构
有核模型
英国物理学家E. 卢瑟福(Ernest Rutherford,1871—1937)领导的科研小组
在用α 粒子(
4
2He
2+)轰击金箔时,发现一个奇怪的现象:绝大多数的α 粒子都直
线穿过金箔,但有极少数α 粒子发生偏转,有个别α 粒子甚至被直接反弹回去。
在实验结果基础上,卢瑟福提出了原子结构的有核模型:原子是由体积极微
小、质量很集中的、带正电荷的原子核,以及在原子核周围空间做高速运动的带
负电荷的电子构成的。
有核模型的提出,标志着对原子结构的认识进入了新阶段,为以后原子结构
的现代模型奠定了基础,但很快又被新的理论和模型取代。
玻尔模型
丹麦物理学家玻尔(Niels Bohr,
1885—1962)对原子的结构进行了更
深入的研究和描述,他认为电子是在
一个特定的距离围绕原子核运动,而
且有着特定的轨道。
发现质子
E. 卢瑟福用α 粒子轰击氮反
应时射出的一种带正电荷的亚原
子粒子,并称它为“质子”。
发现中子
现代原子结构理论在新的实验基础
上保留了玻尔模型的合理部分,并赋予其
新的内容。随着科技迅速发展,新的发现
将继续解开原子更深层次结构的奥秘。
图4.17 α 粒子轰击金箔示意图
图4.19 玻尔原子结构模型
图4.18 玻尔
英国实验物理学家查德威克
(Sir James Chadwick,1891—1974)
发现原子核内另一种亚原子粒子,由
于它是电中性的,故称之为“中子”。
1911 年
1913 年
1932 年
1919 年
原子结构和化学键
第4 章
122
我们知道,元素是具有相同核电荷数的原子的总称。
也就是说,同种元素原子的质子数相同,那么其中子数是
否也相同呢?
科学家发现自然界中有三种不同的氢原子,这三种氢
原子都含有1 个质子,但它们所含的中子数都不相同。
人们把具有一定数目质子和一定数目中子的一种原子
称为核素,例如,
1
1H、
2
1H 和
3
1H 就各为一种核素。质子数相
同而中子数不同的同种元素的不同核素互称为同位素,例
如,
1
1H、
2
1H 和
3
1H 互为同位素。许多元素都有同位素。例
如,碳元素有
12
6C、
13
6C 和
14
6C 等核素;氧元素有
16
8O、
17
8O 和
18
8O 等核素;铁元素有
54
26Fe、
56
26Fe、
57
26Fe 和
58
26Fe 等核素;铀
元素有
234
92U、
235
92U 和
238
92U 等核素。
核素
表4.5 氢元素的三种不同氢原子
原子符号
原子名称
(俗称)
原子核
发现年代
质子数
中子数
1
1H 或H
氕
1
0
1766 年,英国物理学家和化学家卡文迪什
(Henry Cavendish,1731—1810)制得氢气
2
1H 或D
氘(重氢)
1
1
1931 年,美国化学家和天体化学家尤里
(Harold Clayton Urey,1893— 1981)利用
光谱检测的方法发现了氘
3
1H 或T
氚(超重氢)
1
2
1934 年,E. 卢瑟福等人通过核反应发现人
工氚,随后科学家又证实了重水中天然氚
的存在
原子序数是元素分类的依据
拓展视野
门捷列夫设计的元素周期表是将元素按其原子量的大小依次排序,但会出现
某些元素被归入不同性质元素一族的情况。例如,碲(原子序数为52)的原子
量为128,而碘(原子序数为53)的原子量为127。若按原子量的大小排序,碲
应该排到碘的后面,但是与氯性质相似的是碘元素。尽管门捷列夫在元素周期表
中还是将碘排在了碲之后,并且坚信自己的判断,但这种原子量倒置的现象却让
123
4.2
原子结构
门捷列夫十分不解和苦恼。
直至科学家揭开原子结构的奥秘,人们才知道元素的本质区别在于核电荷数
或质子数,而非原子量。
同位素分为稳定同位素和放射性同位素。放射性同位素
在工农业生产、科学研究、医学等领域有着重要的应用。例
如,放射性同位素放射出的射线,可用于金属制品缺陷探测、
食物保鲜、辐射育种、肿瘤诊断治疗和探究反应机理等方面。
图4.20 断层放射治疗机
核素的丰度
核素的丰度指某特定核
素的原子数与该元素的总原
子数之比。
资料库
放射化学是研究放射性物质、与原子核转变过程相关的化学问题的化学分支
学科,它的研究对象本身会含有放射性物质,或是进行研究而人为加入放射性物
质。放射化学具有以下特点:很高的灵敏度,可测几百个乃至几个原子的质量,
如10
—23 kg;利用放射性示踪研究化学反应的历程等。放射化学诞生于19 世纪末
法国科学家居里夫妇发现钋、镭的年代,随着1942 年第一座核反应堆的建成,
它与原子核物理一起走进人类合理利用核能的时代。放射化学也为我国研制原子
弹、建设核电站等做出了重大贡献。
放射化学
链接学科
同一元素的各种核素虽然质量数不同,但它们的化学
性质几乎完全相同。在天然存在的某种元素里,不论是游
离态还是化合态,各种核素所占的丰度一般是不变的。
原子结构和化学键
第4 章
124
由于原子的实际质量非常小,如果用“千克”作单位来
描述原子的质量,所得的数值极小,会给使用带来不便。在
化学中,我们常用相对原子质量进行描述。相对原子质量是指
以一个
12
6C 原子质量的1
12作为标准,任何一个原子的真实
质量与这个标准之间的比值,称为该原子的相对原子质量。
例如,一个
12
6C 的质量约为1.993×10
—26 kg,一个
16
8O 的质
量约为2.656×10
—26 kg,则该氧原子的相对原子质量是:
2.656×10
—26 kg
1.993×10
—26 kg× 1
12
≈ 15.992
元素的相对原子质量,就是它的各种核素的相对原子
质量,按各种核素的丰度而取的平均值。元素周期表中列
出的就是元素的相对原子质量。
A = A1·a1% + A2·a2% + …… + An·an%
式中,A 表示元素的相对原子质量,A1、 A2、……、 An
表示该元素各种核素的相对原子质量,a1%、 a2%、……、
an% 表示各种核素的丰度。根据核素的质量数,也可以算
出元素的近似相对原子质量。
相对原子质量
相对分子质量是分子式中各种原子的个数与相对原子质
量乘积的代数和。你能说出O2 的相对分子质量和摩尔质量的
区别与联系吗?
● 氯元素有
35
17Cl 和
37
17Cl 两种核素,它们的相对原子质量及丰度如表
所示。
学习指南
例题导引
问题:
想一想
125
4.2
原子结构
(1) 说出氯元素的两种核素
35
17Cl、
37
17Cl 互为何种关系。
(2) 列式计算氯元素的相对原子质量。
● (1) 核素
35
17Cl 和
37
17Cl 的质子数都是17,只是它们的中子数不同,
分别为18 和20,所以
35
17Cl 和
37
17Cl 互称同位素。
(2) 根据元素相对原子质量的定义,可知氯元素的相对原子质量
应为
35
17Cl、
37
17Cl 两种核素的相对原子质量按其丰度而得的加权
平均值,即:
氯元素的相对原子质量= 34.969×75.77%+36.966×24.23%
= 35.453
分析:
练习巩固
1. 下列叙述中,符合现代原子结构理论的是( )。
(A) 原子核显电中性
(B) 原子核一般由质子和中子构成
(C) 原子核内中子数与核外电子数相等
(D) 原子的质量主要由质子和电子决定
2. 化学符号“
35
17Cl”左上角的数字“35”表示( )。
(A) 质子数
(B) 中子数
(C) 电子数
(D) 质量数
3. 完成下表。
核素符号
相对原子质量
丰度(%)
35
17Cl
34.969
75.77
37
17Cl
36.966
24.23
核素符号
核电荷数
质子数
中子数
18
8O
10
12
23
11Na
11
原子结构和化学键
第4 章
126
4. 下图所示的两种碳原子之间的关系是什么?试说明它们在结构上的相同点
与不同点。
5. 目前已发现和合成的元素有118 种。试解
释为何原子的种类要远多于元素的种类。
6. 1910 年,英国化学家索迪(Frederick
Soddy,1877—1956)提出了化学元素中存在同
位素的观点。若金属元素M 的三种核素分别是
189M、
190M 和
192M,这三种核素的丰度如图所示,
试确定元素M 的近似相对原子质量。
( 第4 题)
(第6 题)
127
4.3
核外电子排布
身边的有机化合物
第7 章
4.3
核外电子排布
电子在原子核外空间做高速运动。20 世纪以来,科学
家主要运用量子力学等方法来研究核外电子的运动规律。
科学研究表明,通常在离核较近的区域内运动的电子
能量较低,在离核较远的区域内运动的电子能量较高。在
含有多个电子的原子中,电子在原子核外离核由近及远、
能量由低到高的不同电子层上分层排布。通常用n 来表示
电子层。把离核最近、能量最低的电子层称为第一电子层
(n=1),用符号K 表示;其余由里往外依次类推,分别为
第二、三、四、五、六、七电子层,依次用符号L、M、N、
O、P、Q 表示。每一层上最多可以容纳的电子数也各不
相同。
核外电子排布的规律
电子带负电荷,质量仅为9.109×10
—31 kg,而原子内
部大部分是空的,那么电子在原子内“广阔”的空间里是
怎样运动的呢?
了解核外电子运动的特点
理解核外电子排布的规律
学会书写原子和离子的结构示
意图和电子式
运用原子结构解释元素性质的
递变规律
学习聚焦
知识回放
● 构成原子的微粒
● 离子
● 元素周期律
表4.6 核电荷数为1 ~20 的元素原子的电子层排布
核电
荷数
元素
名称
元素
符号
各电子层的电子数
核电
荷数
元素
名称
元素
符号
各电子层的电子数
K
L
M
N
K
L
M
N
1
氢
H
1
11
钠
Na
2
8
1
2
氦
He
2
12
镁
Mg
2
8
2
3
锂
Li
2
1
13
铝
Al
2
8
3
4
铍
Be
2
2
14
硅
Si
2
8
4
5
硼
B
2
3
15
磷
P
2
8
5
6
碳
C
2
4
16
硫
S
2
8
6
7
氮
N
2
5
17
氯
Cl
2
8
7
8
氧
O
2
6
18
氩
Ar
2
8
8
9
氟
F
2
7
19
钾
K
2
8
8
1
10
氖
Ne
2
8
20
钙
Ca
2
8
8
2
原子结构和化学键
第4 章
128
表4.7 第18 族部分元素原子的电子层排布
核电荷数
元素名称
(元素符号)
各电子层的电子数
K
L
M
N
O
P
2
氦(He)
2
10
氖(Ne)
2
8
18
氩(Ar)
2
8
8
36
氪(Kr)
2
8
18
8
54
氙(Xe)
2
8
18
18
8
86
氡(Rn)
2
8
18
32
18
8
依据表4.6、表4.7 中元素原子的电子层排布,你能归纳
出核外电子排布的规律吗?
多电子原子核外电子的排布主要遵循如下规律:
1. 各电子层最多可容纳的电子数为2n2(n 代表电子层
数),例如,K 层(n=1)最多容纳2×1
2=2 个电子,M 层
(n=3)最多容纳2×3
2=18 个电子。
2. 最外层电子数不超过8 个(K 层为最外层时则不超
过2 个)。当最外层电子数达到8(K 层为2)时,就达到
第18 族(稀有气体元素)的稳定结构。
3. 次外层电子数不超过18,倒数第三层电子数不超过32。
试分别写出图4.21 中两种元素Z 和X 的原子的电
子层数,以及最外层上的电子数。
图4.21 元素Z 和X 在
元素周期表中
的位置
书写表达
想一想
129
4.3
核外电子排布
许多事实表明,元素的化学性质与原子的最外层电子
排布密切相关。例如,金属元素原子最外层电子数较少,
在化学反应中容易失去这些电子,使次外层变为最外层,
达到稳定结构;反之,非金属元素原子最外层电子数比较
多,反应时容易得到电子,使最外层达到8 个电子的稳定
结构;稀有气体元素原子最外层已达稳定结构,它们既不
易得电子,也不易失电子,所以化学性质稳定。
原子的核外电子排布可以用原子结构示意图(图4.22)
简明地表示。
我们常在元素符号周围用小黑点(或×)来表示元素
原子的最外层上的电子,这种图式称为电子式。
结构示意图和电子式
图4.22 碳原子的结构
示意图
图4.23 第3 周期元素原子的电子式
我们知道,离子是原子得到或失去电子后形成的微粒,
故也可用结构示意图和电子式来表示,如图4.24 所示。
图4.24 氧离子、钠离子的结构示意图和电子式
O
[ ]
2—
Na
+
电子式
氧离子
钠离子
结构示意图
填写下表。
名称
化学符号
结构示意图
电子式
氮原子
硫离子
书写表达
原子结构和化学键
第4 章
130
现在让我们回到前面的问题,为什么元素的性质会随
着原子序数的递增呈现周期性变化呢?
随着原子序数的递增,各元素原子的最外层电子数增
加,且每隔一定数目的元素,电子层数也在增加。也就是
说,元素原子核外电子排布的周期性变化引起了元素性质
的周期性变化。元素周期表中,元素就是按核电荷数和原
子核外电子排布的周期性变化进行排列的。
同周期元素的原子半径随原子序数的递增依次减小,
同主族元素的原子半径随原子序数的递增依次增大。这是
因为同周期元素原子的电子层数相同,随着原子序数增大,
原子的核电荷数增多,主要表现在原子核对最外层电子的
吸引力增大,因而原子半径逐渐减小。同主族元素的原子
半径主要取决于电子层数,从上到下,原子的电子层数逐
渐增多,原子核对最外层电子的吸引力减弱,因而原子半
径逐渐增大。
通过比较第3 周期元素单质和化合物的性质,以及
碱金属元素、卤族元素的性质变化,我们已经知道同
周期和同主族元素的金属性和非金属性的递变规律。
同周期元素,随着原子序数的递增,原子半径逐渐减小,
失电子能力逐渐减弱,得电子能力逐渐增强,因而元素
的金属性减弱,非金属性增强。同主族元素,随着原子
序数的递增,原子半径逐渐增大,失电子能力逐渐增强,
得电子能力逐渐减弱,因而元素的金属性增强,非金属性
减弱。
核外电子排布与元素周期律
● 元素周期表中第17 族元素如图4.25 所示。
(1) 简述该族元素原子的核外电子排布的特点。
(2) 比较碘和氯分别与金属铁反应的难易程度。
学习指南
例题导引
问题:
131
4.3
核外电子排布
图4.25 元素周期表中第17 族元素
● (1) 该族元素原子的最外层电子数均为7,从氟到砹,原子的电
子层数逐渐增多。
(2) 随着原子序数的递增,同主族元素的非金属性逐渐减弱,即
得电子能力逐渐减弱,因此氯的非金属性强于碘,也会更容
易与金属铁发生反应。
分析:
练习巩固
1. 某元素原子的最外层电子数为4,则其核电荷数可能为( )。
(A) 4 (B) 8 (C) 14 (D) 18
2. 下列微粒的结构示意图或电子式书写正确吗?如有错,请改正。
3. A
+和B
3—两种离子的核外电子排布与氖原子相同,则A
+的结构示意图为
_________,B
3—的电子式为_________。
4. 请在左右两栏相关联的内容之间进行连线。
氟原子: _______________
氧原子: _______________
硫离子: _______________
氯离子: _______________
O
[ ]
2—
Cl×
原子结构和化学键
第4 章
132
5. 完成下表。
微粒
符号
核内
质子数
核外
电子数
结构
示意图
电子式
是否达到
稳定结构
C
K
+
Br
—
Ar
133
4.3
核外电子排布
元素周期表中的百余种元素是如何构成数量惊人的物
质世界的?为何外观相似的盐和糖的性质会完全不同?我
们将在原子结构的基础上,进一步认识原子在构成物质时
不同的相互作用,并认识它们与物质性质之间的关联。
身边的有机化合物
4.4
化 学 键
通常我们把物质中近邻的原子或离子之间存在的强相
互作用称为化学键。
我们知道金属钠在氯气中燃烧生成氯化钠,现在可用
学过的原子结构和元素性质的相关知识,来分析氯化钠的
形成。
钠原子容易失去一个电子,而氯原子容易接受一个电
子。当金属钠与氯气反应时,钠原子将电子给了氯原子,
形成带一个正电荷的钠离子,最外层达到8 电子稳定结构;
氯原子接受一个电子,形成了带一个负电荷的氯离子,最
外层也达到8 电子稳定结构。于是带相反电荷的钠离子和
氯离子通过静电作用结合在一起。这种正、负离子之间由
于静电作用所形成的化学键称为离子键。
以离子键结合的化合物叫做离子化合物,通常第1、2
族的活泼金属和第16、17 族的活泼非金属间易形成离子化
合物。像氯化钠这样的离子化合物在室温下是以晶体形式
存在的,晶体中正、负离子按一定的规律在空间排列,并
通过离子键结合在一起,其结构如图4.26 所示。
离子键
知道化学键的含义
理解离子键和共价键的形成
学会用电子式和结构式表示分
子和离子
知道分子存在一定的空间结构
学习聚焦
知识回放
● 原子核外电子排布的规律
● 元素周期表
● 元素周期律
图4.26 氯化钠的晶体结构示意图
134
原子结构和化学键
第4 章
离子化合物的形成过程可用电子式来表示,例如,氯
化钠的形成过程为:
在离子化合物中存在离子键,像氯化钠这样的离子化
合物有较高的熔点和沸点,硬度也较大。高温下,由于离
子键被破坏,离子可以自由运动,故离子化合物受热熔化
时可以导电。当离子化合物溶于水后,由于水分子作用,
离子键也被破坏而形成自由移动的离子,故离子化合物溶
于水也能导电。
离子半径
拓展视野
离子半径是描述离子大小的参数,取决于离子所带电荷、电子分布和晶体结
构类型。当原子失去电子并形成正离子时,半径一般会变小;当原子获得电子并
形成负离子时,半径一般会增大。
图4.27 Na 和Na
+、Cl 和Cl
—的原子半径和离子半径
我们知道,两个氢原子可以结合成一个氢分子,两个
氯原子可以结合成一个氯分子,一个氯原子和一个氢原子
可以结合成一个氯化氢分子。那么,这些非金属元素原子
之间又是怎样结合的呢?
共价键
尝试用学过的知识,解释氢原子和氯原子为何能结合成氯
化氢分子,结合时原子的个数比例是不是任意的。
Na + Cl
Na
+
—
Cl
[ ]
×
×
想一想
135
4.4
化 学 键
氢和氯都属于非金属元素,氢原子最外层有1 个电子,
氯原子的最外层有7 个电子。氢原子和氯原子分别要达到稳
定的2 电子和8 电子稳定结构,都需要获得1 个电子。由于
氢原子、氯原子之间难以发生电子得失,唯有各自提供1
个电子形成共用电子对使氢原子和氯原子都达到稳定结构。
像氯化氢分子这样,原子间通过共用电子对所形成的
化学键,叫做共价键。仅由共价键构成的化合物叫做共价
化合物,例如,水、乙醇(C2H6O)、蔗糖(C12H22O11)等
都是共价化合物。
共价化合物的形成过程也可以用电子式表示,氯化氢
的形成过程可表示为:
试用电子式表示N2 的形成过程。
一般来说,一个原子中有几个可以共用的未成对电子,
就可以形成几个共价键。例如,一个氧原子、氮原子和碳
原子可以分别形成二、三、四个共价键,它们分别和氢原
子结合成水分子、氨分子、甲烷分子等共价分子。
在化学上常用一条短线来表示一对共用电子,因此,
氯化氢分子也可以表示为:H—Cl,这种式子叫做结构式。
表4.8 给出了几种常见分子的电子式和结构式。
分子式
H2
Cl2
H2O
NH3
CH4
电子式
H H
Cl Cl
O
H
H
×
×
N
H
H
H
×
×
×
C
H
H
H
H
×
××
×
结构式
H—H
Cl—Cl
H—O—H
H—N—H
H
—
H— C— H
H
H
—
—
表4.8 几种分子的电子式和结构式
书写表达
H
H
Cl
Cl
+
×
×
136
原子结构和化学键
第4 章
离子键和共价键的提出
1916 年,德国物理学家柯塞尔(W. Kossel,1888— 1956)根据稀有气体元素
原子的电子层结构具有高度稳定性的事实提出了离子键理论。他指出原子失去或获
得电子变成正、负离子时,都使得原子结构中的电子处于最稳定状态,与原子序数
相近的稀有气体元素原子具有相同的核外电子排布;它们之间靠离子键结合在一起
而生成离子化合物。
1916 年,美国物理化学家路易斯(Gilbert Newton Lewis,1875— 1946)提出
共价键理论,指出原子间的价键可以通过原子间共享一对或多对电子来形成,每个
原子外层的电子结构应和相近稀有气体元素原子所具有的最稳定电子层结构相同。
化学史话
原子在结合形成共价键时,每个原子都有一个最大的
成键数,结合原子的数目不是任意的。共价化合物分子中
各原子间有一定的连接方式,共价键具有空间指向,所以
共价键之间有夹角,因而分子有空间结构,常用球棍模型
和空间填充模型来表示。例如,一个碳原子可以和四个氢
原子结合形成甲烷分子,该分子具有正四面体结构,其球
棍模型和空间填充模型如图4.28 所示。
图4.28 甲烷分子的球棍模
型和空间填充模型
分子中近邻的原子之间存在着强相互作用—共价键,那
么在分子和分子之间是否也存在相互作用?试举例说明。
空间填充模型
拓展视野
许多事实证明分子间存在将分子聚集在一起的作用力,这种作用力叫做分子
间作用力。分子间作用力比化学键弱得多,它主要影响由分子所构成的物质的熔
点、沸点和溶解性等。水的三态变化中的能量变化,就是因为水分子之间存在着
分子间的相互作用力。
分子间作用力
球棍模型
想一想
137
4.4
化 学 键
● 在NH3、H2O、NaOH、KCl 中,哪些物质只含有离子键?哪些物
质既含有离子键,又含有共价键?
● 非金属元素的原子之间形成的化学键通常是共价键,如Cl2、HF、
H2O 等。活泼的金属元素与活泼的非金属元素的原子之间易形成
离子键,如NaF、NaCl、CaBr2 等是典型的离子化合物。NaOH
也是离子化合物,因为它的原子团内部虽是共价键,但Na
+ 与
OH
—之间的相互作用是离子键。
NH3、H2O 中H 分别与N、O 以共价键结合。NaOH 中Na
+ 与
OH
—以离子键结合,OH
—中H 与O 以共价键结合。KCl 中K、
Cl 分别是活泼的金属元素和非金属元素,K
+ 与Cl
—之间应以离
子键结合。所以,KCl 中只含有离子键,而NaOH 中既含有离子
键,又含有共价键。
学习指南
例题导引
问题:
分析:
练习巩固
1. 化学键是一种强相互作用,它存在于( )。
(A) 分子或原子团中的所有原子之间
(B) 构成物质的所有微粒之间
(C) 物质中近邻的原子或离子之间
(D) 分子之间
2. 下列物质的电子式中,正确的是( )。
(A)
Mg
2+
—
—
Cl
[ ]
Cl
[ ]
×
×
(B)
×
C
Cl
Cl
Cl
Cl
××
×
(C) K Cl
×
(D)
—
Cl
[ ]
H
+ ×
3. 下列化合物中存在哪一种或哪两种化学键?在表格中画“√”表示下列化
合物中存在的化学键。
化合物
离子键
共价键
HBr
KI
KOH
MgO
CO2
138
原子结构和化学键
第4 章
4. 下图是局部的元素周期表(其中部分元素用字母表示),在这些元素的原子
中哪些能以离子键两两相互结合?写出结合成离子化合物的化学式。
5. 比较离子键和共价键的特点,将相关内容填入下表。
(第4 题)
化学键
离子键
共价键
成键微粒
组成元素
代表物质
139
4.4
化 学 键
素养提升
■ 能利用元素在元素周期表中的位置和原子结构,来分析、预测和比较元素及其化
合物的性质,理解元素“位置”“结构”“性质”的关系。
■ 能从原子、分子水平上认识物质的元素组成、微观结构、理化性质和相互转化,
从原子核外电子排布的角度分析元素性质发生周期性变化的内在原因,形成“结
构决定性质,性质决定应用”的观念;能从宏观和微观相结合的视角认识微粒间
存在的化学键,从微粒类别、微粒间的相互作用等认识离子键和共价键。
■ 具有证据意识,能基于物质性质的实验和事实证据进行合理的推理和分析,总结
归纳出元素周期律;能运用原子模型和各种化学语言阐释物质微观世界的运动和
变化,从而揭示化学现象的本质和规律。
■ 通过科学家探索原子结构的历史事实,了解和体验科学研究的方法,领悟科学家
的创新思维和探求科学真理的精神。
本章复习
139
核心框图
140
原子结构和化学键
第4 章
练习巩固
1. 元素X 的原子序数为17。下列叙述中,正确的是( )。
(A) X 位于第4 周期
(B) X 的电子式为X
(C) X 为副族元素
(D)
可表示X 所形成离子的结构示意图
2. A、B 和C 是三种不同的元素,在元素周期表中A 与C 属于同一周期,B 与C
属于同一族,且A
2+、B
—和氩原子具有相同的电子排布。推断元素C 是( )。
(A) Mg
(B) Cl
(C) Ca
(D) Br
3. 核电荷数为16 的元素和核电荷数为4 的元素的原子相比较,前者的下列数据是
后者的4 倍的是( )。
(A) 电子数
(B) 最外层电子数
(C)电子层数
(D) 原子半径
4. 将图中物质按要求分类。
5. 铂、钯、铑用于车载三元催化剂。
(1) 每种金属的元素符号是什么?
(2) 这些金属位于元素周期表的什么位置?
(3) 根据该用途并结合相关资料,你能了解这些金属具有何种性质吗?
6. 下表列出了一些卤素单质的熔点和沸点。
卤素单质
熔点/℃
沸点/℃
Cl2
—101.5
—34.0
Br2
—7.2
58.8
I2
113.6
185.2
140
(第4 题)
141
4.4
化 学 键
根据上表,某学生对砹元素的性质进行了一些预测,请你对此做出判断。你认为砹
元素还可能具有哪些性质?填入下表。
预测
判断
砹元素位于周期表第5 周期
砹单质熔点高于114℃
砹原子的最外层电子数为7
砹单质沸点比碘单质低
其他性质:
141
*7. 阅读短文,思考下列问题。
In a letter to this journal last week, Mr. Soddy has discussed the bearing of my theory of the
nucleus atom on radio-active phenomena, and seems to be under the impression of fact, I hold the
view that the nucleus must consist entirely of positive electricity. ...
The original suggestion of van der Broek that the charge on the nucleus is equal to the
atomic number and not to half the atomic weight seems to me very promising. This idea has
already been used by Bohr in his theory of the constitution of atoms. The strongest and most
convincing evidence in support of this hypothesis will be found in a paper by Moseley in the
Philosophical Magazine of this month. He there shows that the frequency of the X radiations
from a number of elements can be simply explained if the number of unit charges on the nucleus
is equal to the atomic number. It would appear that the charge on the nucleus is the fundamental
constant which determines the physical and chemical properties of the atom, while the atomic
weight, although it approximately follows the order of the nucleus charge, is probably a
complicated function of the latter depending on the detailed structure of the nucleus.
(短文取自: E. Rutherford. The structure of the atom[J]. Nature, 1913, 92: 423.)
(1) The essay titled “The Structure of the Atom” was written by Ernest Rutherford. Do you
know the famous Atom Model put forward by him?
(2) There are also some famous scientists mentioned in the essay, such as Soddy, Bohr,
Moseley. Do you have any idea about their great achievements?
(3) Can you infer when this essay was published? At that time, what particles that compose
the atom weren’t discovered?
142
原子结构和化学键
第4 章
体验 · 分享
在下列选题中,开展文献、调查、实验等研究,并将成果和体会制作成海报、演示
文稿,进行分享和交流。
收集日常生活和工农业生产中安全、易得的样品,制作一张短周期的实物元素
周期表。
利用橡皮泥、火柴棍、塑料球等生活中常见的材料,搭出HCl、Cl2、H2O、CH4
等分子的球棍模型。查阅资料后,判断你所搭建的分子模型是否准确。
科学实验(仪器)对揭示原子结构的奥秘起着重要作用。请你收集、查阅和分
析不同文献和资料,罗列出阴极射线管、α 粒子散射实验等科学实验(仪器)。
通过这些信息,思考和阐述科学实验(仪器)对科学研究的意义。
相对原子质量的测定在化学发展进程中,具有十分重
要的地位。如果没有可靠的相对原子质量,也就不可
能有可靠的分子式。现在,科学家已能通过完善和精
密的方法测定其精确的数值,国际纯粹与应用化学联
合会(IUPAC)也会每隔几年公布一次相对原子质量
的新值。张青莲(1908— 2006)是中国无机化学与同
位素化学家。1991 年,他用同位素质谱法测得铟元素
的相对原子质量114.818±0.003 被国际采用作为标准
数据。了解张青莲的主要事迹和成就,以及测定相对
原子质量的现代手段,感悟相对原子质量的测定为何
对化学研究而言意义重大。
142
图4.29 张青莲
143
4.4
化 学 键
Ⅰ 酸、碱和盐的溶解性表(293 K)
正离子
负离子
OH
—
NO3
—
Cl
—
SO
2—
4
S
2—
SO
2—
3
CO
2—
3
SiO3
2—
PO
3—
4
H
+
溶、挥
溶、挥
溶
溶、挥
溶、挥
溶、挥
微
溶
NH
+
4
溶、挥
溶
溶
溶
溶
溶
溶
溶
溶
K
+
溶
溶
溶
溶
溶
溶
溶
溶
溶
Na
+
溶
溶
溶
溶
溶
溶
溶
溶
溶
Ba
2+
溶
溶
溶
不
—
不
不
不
不
Ca
2+
微
溶
溶
微
—
不
不
不
不
Mg
2+
不
溶
溶
溶
—
微
微
不
不
Al
3+
不
溶
溶
溶
—
—
—
不
不
Mn
2+
不
溶
溶
溶
不
不
不
不
不
Zn
2+
不
溶
溶
溶
不
不
不
不
不
Cr
3+
不
溶
溶
溶
—
—
—
不
不
Fe
2+
不
溶
溶
溶
不
不
不
不
不
Fe
3+
不
溶
溶
溶
—
—
不
不
不
Sn
2+
不
溶
溶
溶
不
—
—
—
不
Pb
2+
不
溶
微
不
不
不
不
不
不
Bi
3+
不
溶
—
溶
不
不
不
—
不
Cu
2+
不
溶
溶
溶
不
不
不
不
不
Hg
+
—
溶
不
微
不
不
不
—
不
Hg
2+
—
溶
溶
溶
不
不
不
—
不
Ag
+
—
溶
不
微
不
不
不
不
不
注:“溶”表示该种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“—”表示该种物
质不存在或遇水分解。
附 录
144
原子结构和化学键
第4 章
Ⅱ 化学词汇中英文对照表
中文
英文
中文
英文
氨
ammonia
氯化钠
sodium chloride
铵盐
ammonium salt
氯气
chlorine gas
萃取
extraction
摩尔
mole
氮气
nitrogen
摩尔质量
molar mass
碘
iodine
气体摩尔体积
molar volume of gas
电解质
electrolyte
强电解质
strong electrolyte
电离
ionization
容量瓶
volumetric flask
电离方程式
ionization equation
弱电解质
weak electrolyte
电子
electron
三氧化硫
sulfur trioxide
电子层
electron shell
酸雨
acid rain
丁达尔现象
Tyndall effect
同位素
isotope
二氧化氮
nitrogen dioxide
物质的量
amount of substance
二氧化硫
sulfur dioxide
物质的量浓度
molarity
非电解质
non-electrolyte
相对原子质量
relative atomic mass
分散系
dispersion system
硝酸
nitric acid
分子
molecule
溴
bromine
共价键
covalent bond
亚硫酸
sulfinic acid
固氮
nitrogen fixation
焰色反应
flame reaction
过滤
filtration
氧化还原反应
oxidation-reduction reaction
核素
nuclide
氧化剂
oxidant
化学肥料
chemical fertilizer
一氧化氮
nitric oxide
化学键
chemical bond
元素
element
还原剂
reductant
元素周期表
periodic table of the elements
碱金属
alkali metal
元素周期律
periodic law of the elements
胶体
colloid
原子
atom
结晶
crystallization
原子核
nucleus
离子反应
ionic reaction
原子序数
atomic number
离子方程式
ionic equation
蒸馏
distillation
离子键
ionic bond
质量数
mass number
硫黄
sulfur
质子
proton
硫酸
sulphuric acid
中子
neutron
硫酸盐
sulfate
周期
period
卤素
halogen
族
group
145
4.4
化 学 键
学生必做实验
实验名称
页码
配制一定物质的量浓度的溶液
配制100 mL 1.000 mol·L
—1 氯化钠溶液
30
用化学沉淀法去除粗盐中的杂质离子
粗盐的提纯
44
不同价态含硫物质的转化
二氧化硫的性质
76
二氧化硫的还原性
78
浓硫酸与铜的反应
79
同周期、同主族元素性质的递变
比较氯、溴、碘单质的活泼性
64
钠、镁、铝元素性质的递变
111
Ⅲ 学生必做实验索引
146
原子结构和化学键
第4 章
Ⅳ 元素周期表
147
4.4
化 学 键
后 记
本册教材根据教育部颁布的《普通高中化学课程标准(2017 年版2020 年修订)》编
写并经国家教材委员会专家委员会审核通过。
编写过程中,上海市中小学(幼儿园)课程改革委员会专家工作委员会,上海市教
育委员会教学研究室,上海市课程方案教育教学研究基地、上海市心理教育教学研究基
地、上海市基础教育教材建设研究基地及基地所在单位华东师范大学,上海市化学教育
教学研究基地(上海高校“立德树人”人文社会科学重点研究基地)及基地所在单位复
旦大学给予了大力支持。复旦大学化学实验教学示范中心为本册教材中化学实验的验证
和拍摄提供支持。许多专家和社会各界朋友十分关心并提出很多意见和建议。在此一并
表示诚挚的敬意!
本册教材出版之前,我们就教材中使用的照片、图片等选用作品,通过多种途径与
作者进行了联系,得到了他们的大力支持,在此表示衷心的感谢!对于未联系到的作者,
我们也希望作者能及时联系出版社,以便出版社支付相应的稿酬。
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见,我们将不断修订,
使教材趋于完善。
2020 年5 月
148
原子结构和化学键
第4 章
本册教材图片提供信息:
本册教材中的图片由视觉中国、IC photo、中国全球图片总汇(图1.29、图1.30、
图2.2、图3.19)等提供。