文档内容
2025-2026 学年度高三上学期期中考试
高三化学答案、解析及评分标准
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
B A C C A D C D C C B D B B C
1、【答案】B
【解析】A.硬水中含有较多的钙、镁化合物(如碳酸氢钙、碳酸氢镁等)。加热煮沸时,这些化合物会
发生反应,如碳酸氢钙受热分解为碳酸钙(沉淀)、水和二氧化碳,碳酸氢镁也会发生类似反应生成氢氧
化镁(沉淀)等新物质。有新物质生成,涉及化学变化。
B.硅电池用于光伏发电,是利用半导体的光电效应,将太阳能直接转化为电能,这个过程中没有新物质
生成,不涉及化学变化。
C.用CO 人工合成淀粉,CO 是无机物,淀粉是有机物,有新物质(淀粉)生成,涉及化学变化。
2 2
D.ClO 用于自来水消毒,是利用ClO 的强氧化性,使细菌、病毒等的蛋白质变性,有新物质生成,涉及
2 2
化学变化。故选B。
2、【答案】A
【解析】A.HClO分子空间结构为V形,且是极性分子。
B.CCl 分子中,中心原子C的sp3杂化轨道分别与4个Cl原子的3p轨道形成4个sp3-pσ键。
4
C.由于O的电负性较大,H O分子中的共用电子对更偏向O,使H O的H几乎成为一个裸露质子,更易
2 2
与NH 中N原子的孤电子对形成氢键。
3
D.一般来说,Na+带正电,常与H O中带负电的O靠近;Cl-带负电,常与H O中带正电的H靠近。
2 2
3、【答案】C
【解析】A.石膏的主要成分为硫酸钙,能使豆浆中的蛋白质聚沉,可以用作制豆腐时的凝固剂,A正确;
B.加热条件下铜与浓硫酸发生氧化还原反应,H SO 被还原生成SO ,B正确;
2 4 2
C.小火加热下乙醇与乙酸发生酯化反应生成乙酸乙酯为可逆反应,不可能完全反应,C错误;
D.阿司匹林具有解热镇痛作用,它在人体内产生的水杨酸会刺激胃黏膜,长期大量服用可能会导致胃疼
等不适症状,D正确;故选C。
4、【答案】C
【解析】A.制备氢氧化铁胶体的正确方法是:向沸水中逐滴加入FeCl 饱和溶液,继续煮沸至液体呈红
3
褐色,停止加热。而该实验示意图中用的是Fe (SO ) 饱和溶液,Fe (SO ) 溶液与沸水作用不能制备出氢
2 4 3 2 4 3
氧化铁胶体,A不符合题意;
B.要比较Cl、C、Si的非金属性,需通过比较它们最高价氧化物对应水化物的酸性强弱来判断(非金属
性越强,最高价氧化物对应水化物的酸性越强),稀盐酸不是Cl的最高价氧化物对应水化物(Cl的最高
价氧化物对应水化物是HClO )且盐酸具有挥发性,挥发出的HCl会与Na SiO 溶液反应生成沉淀,干扰
4 2 3
CO 与Na SiO 溶液的反应,无法准确比较C和Si的非金属性,B不符合题意;
2 2 3
C.在中性或弱酸性条件下,铁发生吸氧腐蚀。实验中用食盐水(呈中性)浸润铁丝网,铁丝网发生吸氧
腐蚀,消耗装置内的氧气,使试管内压强减小,外界大气压将红墨水压入试管,能观察到红墨水上升的现
象,可验证铁的吸氧腐蚀,C符合题意;
D.萃取振荡时放气,应将分液漏斗倒置,打开活塞放气,而实验示意图中是正立放气,操作错误,D不
符合题意;故选C。
5、【答案】A
【解析】A.由天然油脂得到的油酸和亚油酸一般具有顺式结构,A错误;
B.气态物质在高温或者在外加电场激发下,分子发生分解,产生由电子、阳离子和中性粒子形成等离子
体,B正确;
高三化学答案(共 6 页)第 1 页
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}C.引入有机基团可使离子的体积增大,使离子化合物的熔点降低至或稍高于室温而呈液态,C正确;
D.模型在科学认识中具有描述、解释和预测等功能,是理论发展的一种重要方式,D正确;故选A。
6、【答案】D
【分析】X、Y、Z、W均为短周期元素且原子序数依次增大,Z的价电子层p轨道差1个电子填满,X形
成3个共价键,X是N元素,Y、W均能形成2个共价键,Y与W同主族,Y是O、W是S元素,Z形
成1个共价键,Z是F元素。
【详解】A.O、S杂化方式均为sp3杂化,O、S均有两对孤电子对,但电负性O>S,所以键角H O>H S,
2 2
A正确;
B.电子层数越多半径越大,电子层数相同,质子数越多半径越小,离子半径S2->N3->O2->F-,故B正确;
C.同周期元素从左到右,第一电离能有增大趋势,N原子2p能级半充满,结构稳定,第一电离能大于同
周期相邻元素,第一电离能F>N>O,故C正确;
D.圆圈内结构为平面六元环,C、N均采用sp2杂化,氮原子的孤对电子占据一条杂化轨道,未参加杂化
的p轨道上有一个单电子形成大π键,D错误;
选D。
7、【答案】C
【详解】A.四氯化碳能萃取溴水中的溴,丙酮不能,并非是氢键的因素,四氯化碳是非极性分子,不溶
于水,丙酮是极性分子与水互溶,结构因素错误,A错误;
B.Cl 溶解度高于CO并非因极性(Cl 非极性,CO极性),而是Cl 与水反应,结构因素错误,B错误
2 2 2
C.氯乙烷、氯乙烯、氯乙炔三种分子中形成CCl键的原子相同,键长取决于碳原子杂化轨道中s成分的
多少,s的成分越多,碳氯键越强,键长越短,同时也取决于氯原子参与形成大π键的数目,形成的大π键
越多,碳氯键越短,键越强,C正确;
D.邻羟基苯甲酸形成分子内氢键如图: ,D错误;
故选C。
8、【答案】D
【解析】由焊接和切割金属可联想到乙炔氧焰,因此可确定F为氧气,E为乙炔,H为二氧化碳,B为水;
联系乙炔的制法可知,D为氢氧化钙,A为碳化钙;与水反应生成氧气的通常是过氧化钠,且C的焰色试
验显黄色,所以可据此确定C为过氧化钠,G为氢氧化钠,推出I为碳酸钠或碳酸氢钠;
A.反应①为实验室制乙炔。碳化钙与水反应是剧烈的放热反应,实验时一定要防热烫, A正确;
B.I为碳酸钠或碳酸氢钠,可用作食用碱或工业用碱。B正确;
C.若消耗1molNa O ,则转移电子数目为N ,C正确;
2 2 A
D.E为乙炔,发生加聚反应形成的导电高分子聚乙炔中共轭大π键表示为:π2n,D错误。
2n
9、【答案】C
【解析】A.该晶胞中,O原子8个位于顶点(4个被6个晶胞共用,4个被12个晶胞共用),1个晶胞
1 1
中所含O原子数为4 4 1,Ni原子8个位于棱(均被4个晶胞共用)、6个位于面(均被2个晶
6 12
1 1
胞共用),1个位于体内,Ni原子数为18 6 6 ,因此该物质的化学式为Ni O,A正确;
6
4 2
3
B.该晶胞的体积为 abc,B正确;
2
C.由于a=b≠c,每个O原子周围与其等距且紧邻的O原子有4个,C错误;
D.基态氧原子有2个自旋平行的2p电子,D正确。
高三化学答案(共 6 页)第 2 页
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}10、【答案】C
【解析】A.它的单体是乳酸,都含有手性碳原子;
B.它有三种官能团:羟基、酯基和羧基;
C.聚乳酸它是有良好的生物相容性和生物可吸收性,作为手术固定材料,不需要取出来;
D乳酸在一定条件下通过缩聚反应制备聚乳酸;答案选C。
11、【答案】B
【解析】A.选必3教材138页,聚乙烯分子拉直后除去外力又恢复卷曲状态,是因为这个聚乙烯分子碳
碳单键可以发生旋转;
B.选必3教材145页,天然橡胶和杜仲橡胶分别是顺式聚异戊二烯和反式聚异戊二烯。杜肿橡胶硬而弹
性差,实质是它们的结构决定的;
C.选必3教材151面,第八题的第4问该材料应具有良好的亲水性,是结构中含有羟基;
D.选必3教材141页,有关实验的解释:在碱催化下,苯酚与过量的甲醛反应生成多羟甲基苯酚,后继
续发生缩聚反应,可生成网状结构的酚醛树脂。
12、【答案】D
【详解】A.向某溶液中加入氢氧化钠溶液并加热,若溶液中存在 NH ,会发生反应
4
。氨气是碱性气体,能使湿润的红色石蕊试纸变蓝。通过观察产生的气体
能否使红色石蕊试纸变色,可判断溶液中是否存在NH,因此该方案不能达到探究目的。
4
B.Fe2+与H O 反应时,Fe2+会被氧化为Fe3+,Fe3+对H O 的分解有催化作用。所以仅通过向H O 溶液中
2 2 2 2 2 2
滴加FeSO 溶液观察气泡,无法确定是Fe2+还是其氧化产物Fe3+起到了催化作用,该方案不能达到探究目
4
的。
C.NaClO溶液具有强氧化性,会漂白pH试纸,导致无法用试纸准确测定其pH,也就不能通过测定NaClO
溶液和CH COONa溶液的pH来比较HClO和CH COOH酸性强弱,且两溶液的浓度也未说明,故该方案
3 3
不能达到探究目的。
D.酸性KMnO 溶液与H C O 溶液反应的离子方程式为 。
4 2 2 4
计算可知两种浓度的H C O 溶液都足量,KMnO 溶液均能完全褪色,可通过观察褪色情况探究浓度对化
2 2 4 4
学反应速率的影响,该方案能达到探究目的。
综上所述,答案选D。
13、【答案】B
【解析】A.CO₂为分子晶体,微粒间以分子间作用力结合,沸点低;SiO₂为共价晶体,微粒间以共价键结
合,沸点高,解释正确,A不符合题意;
B.该反应能发生,主要是因为CO为气体,生成后脱离反应体系,使平衡正向移动,并非碳的还原性强
于硅(硅的还原性比碳强),解释错误,B符合题意;
C.中心原子电负性:C>Si,H CO 中H-O键受C的吸电子作用,极性更大,更易电离出H⁺,故酸性H CO
2 3 2 3
>H SiO ,解释正确,C不符合题意;
2 3
D.Si的价层电子排布为3s²3p²,有3d空轨道可参与杂化形成SiF2;C的价层电子排布为2s²2p²,无2d
6
轨道,难形成CF2,解释正确,D不符合题意;故选B。
6
14、【答案】B
【解析】A.H L2+的 K =c(H+)×c(H L+)/c(H L2+),滴定曲线上当 V(NaOH)=10mL 时,pH=1.82,此时
3 a1 2 3
c(H L2+)≈c(H L+),K ≈c(H+)=10-1.82,数量级为10-2,A正确;
3 2 a1
B.pH=7时,组氨酸主要以H L+和HL形式存在,且Cl-不参与电离水解,浓度最大,结合滴定过程中离
2
子生成顺序,c(Cl-)>c(HL)>c(H L+)>c(H L2+),B错误;
2 3
高三化学答案(共 6 页)第 3 页
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}C.组氨酸pK =6.0、pK =9.17,pH=9.0介于pK 和pK 之间,主要存在形式为HL,C正确;
a2 a3 a2 a3
D.根据电荷守恒,溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数,且 pH=1.82 时
c(H L2+)=c(H L+)电荷守恒式为c(H+)+2c(H L2+)+c(H L+)+c(Na+)=c(Cl-)+c(OH-)+c(L-),D正确;故选B。
3 2 3 2
15、【答案】C
A.由图可知通CO 的一极得电子生成了甲酸根离子,为阴极,和电源的负极相连;通CH OH失电子生
2 3
成甲酸的一极做阳极,和电源的正极相连。所以图中直流电源a为负极;
B.电解过程中CH OH参与的电极反应式为:CH OH4e H OHCOOH4H;
3 3 2
C.当有 1molH+通过质子交换膜时,电路中转移1mol 电子,根据两极反应CO 2e H HCOO-和
2
CH OH4e H OHCOOH4H可知装置中生成0.5molHCOO和0.25molHCOOH共计0.75mol;
3 2
D.由电解时甲醇难在电极上直接放电可知,电解时加入氯化钠溶液的目的是氯离子在阳极放电生成氯气,
氯气将甲醇氧化为甲酸。
16.【答案】(每空2分,共14分)
(1)4d105s1
(2)CuS+2O 细菌 CuSO 条件温和;能耗低(或对设备要求低等合理答案)
2 4
(3)增强Au的还原性,促进Au溶解 130
(4)AgCl
(5)[Ag(NH ) ]++e−=Ag+2NH ↑
3 2 3
【解析】
(1)Cu的价层电子排布式为 3d104s1 ,Cu和Ag 在周期表中位于同族且相邻,Ag位于第五周期ⅠB族,
基态Ag 原子价层电子排布式是4d105s1。
(2)“细菌氧化”时,CuS 与空气、H SO 反应生成胆水(CuSO 溶液),化学方程式为
2 4 4
CuS+2O 细菌 CuSO 。“焙烧氧化”需要高温条件,相比之下,“细菌氧化” 的优势为条件温和;能耗
2 4
低(或对设备要求低等合理答案)。
(3)“浸取”步骤中,Au转化为一元强酸 H[AuCl ] ,Au 的化合价升高,被氧化, Cl-与Au3+结合形成
4
配离子[AuCl ]− ,增强Au的还原性,使Au的溶解反应正向进行,所以Cl−的作用为增强Au的还原性,
4
促进Au溶解。沉金时发生反应2H[AuCl ]+4Zn=2Au+4ZnCl +H ↑,由化学计量数可知,生成1mol金,
4 2 2
消耗2.0molZn,消耗Zn的质量为2.0mol×65g/mol=130.0g 。
(4)“浸取”步骤中,Ag被氧化, Cl−与Ag+结合形成AgCl。
(5)“电沉积”步骤中,阴极发生还原反应,[Ag(NH ) ]+得到电子生成Ag,电极反应式为
3 2
[Ag(NH ) ]++e−=Ag+2NH ↑。
3 2 3
17、【答案】(每空2分,共14分)
(1)对溴苯甲酸(4-溴苯甲酸)
(2)A中含有羧基(−COOH),NH NH (肼)具有碱性,羧基会与肼发生酸碱中和反应,所以不能直
2 2
接用A与NH NH 反应制取C。(其他合理答案也给分,如从结构上或共价键的断裂难易程度角度解释)
2 2
(3)AC
(4)
高三化学答案(共 6 页)第 4 页
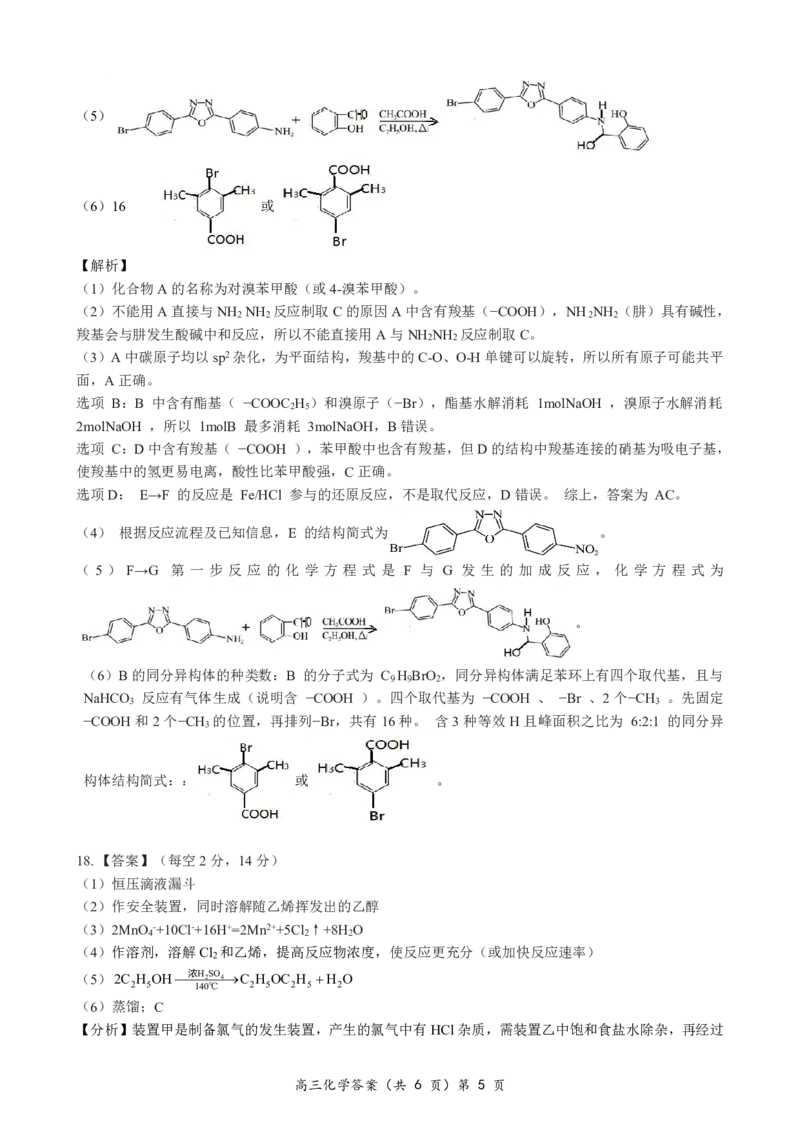
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}(5)
(6)16 或
【解析】
(1)化合物A的名称为对溴苯甲酸(或4-溴苯甲酸)。
(2)不能用A直接与NH NH 反应制取C的原因A中含有羧基(−COOH),NH NH (肼)具有碱性,
2 2 2 2
羧基会与肼发生酸碱中和反应,所以不能直接用A与NH NH 反应制取C。
2 2
(3)A中碳原子均以sp2杂化,为平面结构,羧基中的C-O、O-H单键可以旋转,所以所有原子可能共平
面,A正确。
选项 B:B 中含有酯基( −COOC H )和溴原子(−Br),酯基水解消耗 1molNaOH ,溴原子水解消耗
2 5
2molNaOH ,所以 1molB 最多消耗 3molNaOH,B错误。
选项 C:D中含有羧基( −COOH ),苯甲酸中也含有羧基,但D的结构中羧基连接的硝基为吸电子基,
使羧基中的氢更易电离,酸性比苯甲酸强,C正确。
选项D: E→F 的反应是 Fe/HCl 参与的还原反应,不是取代反应,D错误。 综上,答案为 AC。
(4) 根据反应流程及已知信息,E 的结构简式为 。
( 5 ) F→G 第 一 步 反 应 的 化 学 方 程 式 是 F 与 G 发 生 的 加 成 反 应 , 化 学 方 程 式 为
。
(6)B的同分异构体的种类数:B 的分子式为 C H BrO ,同分异构体满足苯环上有四个取代基,且与
9 9 2
NaHCO 反应有气体生成(说明含 −COOH )。四个取代基为 −COOH 、 −Br 、2个−CH 。先固定
3 3
−COOH和2个−CH 的位置,再排列−Br,共有16种。 含3种等效H且峰面积之比为 6:2:1 的同分异
3
构体结构简式:: 或 。
18.【答案】(每空2分,14分)
(1)恒压滴液漏斗
(2)作安全装置,同时溶解随乙烯挥发出的乙醇
(3)2MnO -+10Cl-+16H+=2Mn2++5Cl ↑+8H O
4 2 2
(4)作溶剂,溶解Cl 和乙烯,提高反应物浓度,使反应更充分(或加快反应速率)
2
(5)2C H OH浓H2 SO4C H OC H H O
2 5 140℃ 2 5 2 5 2
(6)蒸馏;C
【分析】装置甲是制备氯气的发生装置,产生的氯气中有HCl杂质,需装置乙中饱和食盐水除杂,再经过
高三化学答案(共 6 页)第 5 页
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}装置丙中浓硫酸干燥;装置庚是制备乙烯的发生装置,产生的乙烯中有乙醇,需装置己中水除杂,再经过
装置戊中浓硫酸干燥;最后氯气和乙烯通入装置丁,发生乙烯的加成反应制备1,2-二氯乙烷。
【解析】(1)由图可知,仪器a的名称为恒压滴液漏斗。(2)装置己中盛放的是水,其作用是作安全瓶,
同时吸收随乙烯挥发出的乙醇。(3)装置甲中是高锰酸钾和浓盐酸反应制取氯气,其离子方程式为
2MnO -+10Cl-+16H+=2Mn2++5Cl ↑+8H O。(4)丁中先加入少量1,2-二氯乙烷液体,作溶剂,可使Cl 和
4 2 2 2
乙烯更好溶解,提高反应物浓度加快反应的进行。(5)当温度为140℃时乙醇可发生副反应,分子间脱
水生成乙醚,化学方程式为2C H OH浓H2 SO4C H OC H H O 。(6)由以上反应可知,1,2-二氯乙
2 5 140℃ 2 5 2 5 2
烷中有少量的乙醚,两者沸点不同,可采用蒸馏的方法除去。蒸馏需要用到蒸馏烧瓶、温度计、直形冷凝
管、尾接管等仪器,不会用到球形冷凝管(C)。
19. 【答案】(13分)
(1)高温 (2分)
(2)+497.9(2分)
(3)反应 i 生成固态炭,会覆盖在催化剂表面,影响催化剂的活性(2分)
(4)1400(2分) 此条件下,苯的生成速率最大,积炭的收率最低(2分)
1
(5)①kr= (2分) ②反应i(1分)
p
6
反应i、反应ii 均为吸热反应,且∆H₁<∆H₂,温度升高,反应i的平衡常数随温度升高的增加量小于反应
ii的(2分)
【命题立意】本题考查反应原理分析,考查考生思维方法的学科素养。
【解析】
(1)反应i的∆H>0,∆S>0,能自发进行则需要∆H-T∆S<0,则高温时,有利于反应i自发进行。
(2)由题给燃烧热数据可得出以下热化学方程式:
③CH (g)+2O (g)=CO (g)+2H O(l) ΔH=akJ·mol-1
4 2 2 2
④C H (l)+7.5O (g)=6CO (g)+3H O(l) ΔH=bkJ·mol-1
6 6 2 2 2
⑤H (g)+0.5O (g)=H O(l) ΔH=ckJ·mol-1
2 2 2
依据盖斯定律,将反应③×6 -④ - ⑤×9 得反应ⅱ,故反应ⅱ的∆H =(6a-b-9c) kJ·mol-1,代入数据算得
2
∆H =+497.9kJ·mol-1。
2
(3)反应i、ii均为吸热反应,升高温度均有利于平衡正向移动,CH₄的转化率增大,但是温度较高,生
成积炭的速率也较快,反应i生成的固态炭会覆盖在催化剂表面,影响催化剂的活性,使反应ii生成苯的
速率下降。
(4)由图可知,同一条件下,相同时间内,反应空速为1400mL·g-1·h-1时苯的生成速率最大,积炭的收率
最低,故最佳空速为1400mL·g-1·h-1。
p H
2
2 200kPa25% 2
(5)①kr= p 0 = 100kPa = 1 ;
p p CH 200kPa75% 6
4
p 100kPa
0
②反应i 、反应ii 均为吸热反应,且∆H₁<∆H₂,温度升高,反应 i 的平衡常数随温度升高的增加量较小,
1
所以L 是反应i的Inkr随 变化的曲线。
2 p
T
高三化学答案(共 6 页)第 6 页
{#{QQABQQIs5wCQgpRACK66AUH2CgqYsIKSLCgORVAQuAQKwQNIBCA=}#}