文档内容
化学
一、选择题
1. 下列具有达州特色的农副产品的加工过程,主要发生化学变化的是
A. 酿“苞谷烧”酒 B. 编制竹蒌
C. 采摘“巴山雀舌”茶 D. 包装“灯影牛肉”
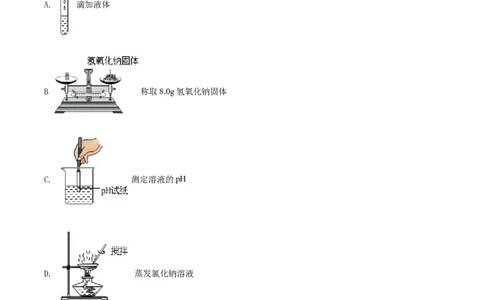
2. 正确的实验操作是化学实验成功的重要保证。下列实验操作正确的是
A. 滴加液体
B 称取8.0g氢氧化钠固体
.
C. 测定溶液的pH
D. 蒸发氯化钠溶液
3. 蓝莓富含花青素(C H O)。花青素是一种水溶性色素,颜色与细胞液的酸碱性有关,酸性时为红色,
15 11 6
碱性时为蓝色。下列有关说法正确的是
A. 花青素是有机物
B. 花青素中碳、氢、氧的质量比为15:11:6
C. 花青素由碳原子、氢原子、氧原子构成在
D. 氢氧化钠溶液中滴入蓝莓汁液,溶液呈红色
4. 化学与我们的生产生活息息相关。下列说法不正确的是
A. 碘是人体所需要的一种微量元素,缺碘会导致甲状腺肿大
B. 纸箱着火用水浇灭,降低了可燃物的着火点
C. 洗涤剂具有乳化作用,能用于清洗油污
D. 鉴别聚酯纤维和羊毛可用灼烧闻气味的方法
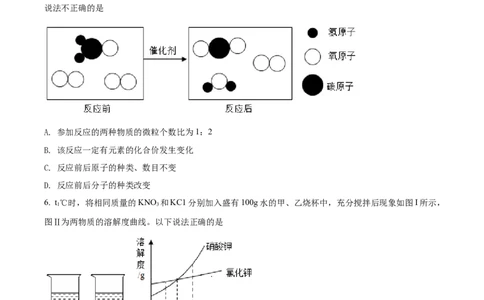
5. 甲醛(CHO)是一种有毒气体,房屋装修时部分建材释放出的甲醛严重影响人体健康。科学家们研究发现,
2
使用特殊的催化剂可高效地促进甲醛的转化,从而降低甲醛的危害。其反应过程的微观示意图如下,下列
说法不正确的是
A. 参加反应的两种物质的微粒个数比为1:2
B. 该反应一定有元素的化合价发生变化
C. 反应前后原子的种类、数目不变
D. 反应前后分子的种类改变
6. t℃时,将相同质量的KNO 和KC1分别加入盛有100g水的甲、乙烧杯中,充分搅拌后现象如图I所示,
1 3
图Ⅱ为两物质的溶解度曲线。以下说法正确的是
A. 甲烧杯中的溶质为KNO
3
B. 将温度升高到t℃时,乙烧杯中仍然有固体剩余
2
C. 若KNO 中混有少量KCl,可采用蒸发结晶的方法提纯KNO
3 3
D. 若取t℃时KNO 和KC1的饱和溶液各100g,降温至t℃时,析出晶体较多的是KNO
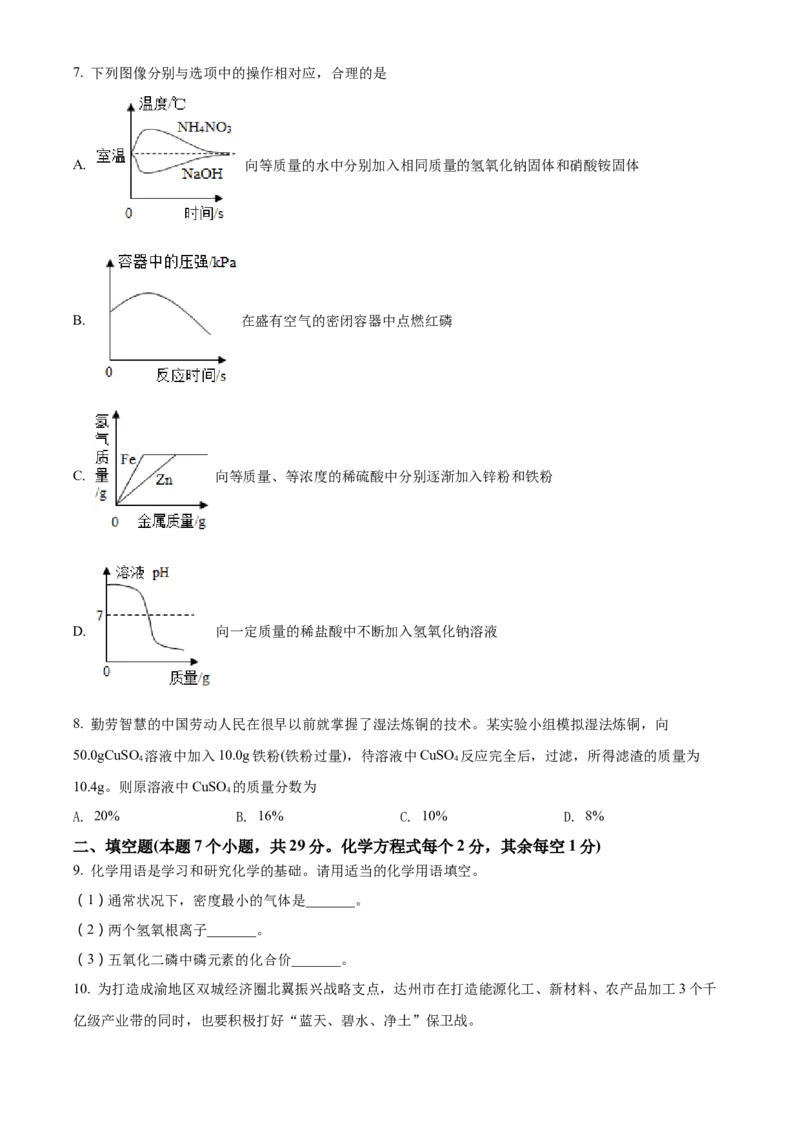
3 3 2 37. 下列图像分别与选项中的操作相对应,合理的是
A. 向等质量的水中分别加入相同质量的氢氧化钠固体和硝酸铵固体
B. 在盛有空气的密闭容器中点燃红磷
C. 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D. 向一定质量的稀盐酸中不断加入氢氧化钠溶液
8. 勤劳智慧的中国劳动人民在很早以前就掌握了湿法炼铜的技术。某实验小组模拟湿法炼铜,向
50.0gCuSO 溶液中加入10.0g铁粉(铁粉过量),待溶液中CuSO 反应完全后,过滤,所得滤渣的质量为
4 4
10.4g。则原溶液中CuSO 的质量分数为
4
A. 20% B. 16% C. 10% D. 8%
二、填空题(本题7个小题,共29分。化学方程式每个2分,其余每空1分)
9. 化学用语是学习和研究化学的基础。请用适当的化学用语填空。
(1)通常状况下,密度最小的气体是_______。
(2)两个氢氧根离子_______。
(3)五氧化二磷中磷元素的化合价_______。
10. 为打造成渝地区双城经济圈北翼振兴战略支点,达州市在打造能源化工、新材料、农产品加工3个千
亿级产业带的同时,也要积极打好“蓝天、碧水、净土”保卫战。(1)为建成全国性综合交通枢纽城市,达州市大力实施“经济发展、交通先行”战略,在基础设施建设
中选择应用新材料。达州新建机场一金垭机场使用了大量玻璃钢材料,玻璃钢是一种 (填字母序号)。
A. 复合材料 B. 无机非金属材料 C. 合成材料
(2)自2013年以来,达州以水稻、油菜、玉米、薯类等为重点,建设“川渝粮仓”,粮食总产量连续9
年保持在六十亿斤以上,稳居全省第一、
①大米、玉米、薯类中主要富含的营养素是____(填字母序号)。
A.蛋白质 B.油脂 C.糖类 D.维生素
②抓三农促振兴,坚定建设农业强市。2022年,我市规划大豆种植须达到53.5万亩。正所谓:“庄稼一枝
花,全靠肥当家”。大豆等农作物生长期间常需施加一些肥料。下列属于复合肥料的是____(填字母序号)。
A.CO(NH ) B.NH HPO C.K SO
2 2 4 2 4 2 4
(3)2021年3月金国两会期间提出,2030年“碳达峰”,2060年“碳中和”。实现“碳达峰”“碳中
和”需控制二氧化碳的排放量。请写出一条生活中践行“低碳”生活的具体做法:_______。
的
(4)“碧水”就得保护好水资源。下列关于水资源保护 做法正确的是 (填字母序号)。
A. 为了改善水质,向其中加入大量的净水剂和消毒剂
B. 为保护好水资源,禁止使用化肥和农药
C. 大量开采利用地下水
D. 工业废水处理达标后再排放
11. 化学是在原子、分子水平上研究物质及其变化规律的一门基础学科。
(1)图I是五种微粒的结构示意图。
①上述微粒共表示_______种元素。
②上述五种微粒中,化学性质相似的两种原子是_______(填字母序号)。
(2)元素周期表是学习化学的重要工具。由图Ⅱ知,氯元素的相对原子质量为_______。
12. 在实验操作考试中,小明的考试题目是配制50g溶质质量分数为6%的NaC1溶液(已知p =lg/mL),请
水
回答下列问题:
(1)小明应称取NaCl固体_______g。在称量的过程中,发现托盘天平的指针向左偏转,此时小明应该
_______(填字母序号)。A 增加适量NaCl B.减少适量NaCl
C.增加砝码 D.调节天平平衡螺母
的
(2)量取蒸馏水时,小明应选择_______(填“20mL”或“50mL”或“100mL”) 量筒。
(3)下列因素会造成小明所配溶液溶质质量分数偏小的是 (填字母序号)。
A. 量取蒸馏水时仰视读数
B. 量取蒸馏水时俯视读数
C. 将称量好的NaCl固体转移至烧杯时,NaCl洒落
D. 配好的溶液转移到试剂瓶时,部分溶液溅出
13. 已知A、B、C、D、E为初中化学中常见的五种不同类别的物质,B为红棕色粉末,C由两种元素组成,
D广泛应用于治金、造纸、纺织、印染和洗涤剂生产等领域,五种物质的转化关系如图所示(“-”表示相
连的两种物质能发生反应,“→”表示相连物质能向箭头所指一方转化)。部分反应物、生成物及反应条件
已省略。请回答下列问题:
(1)B物质的化学式为_______。
(2)A和C反应的化学方程式为_______。
(3)C和E反应的实质为_______。
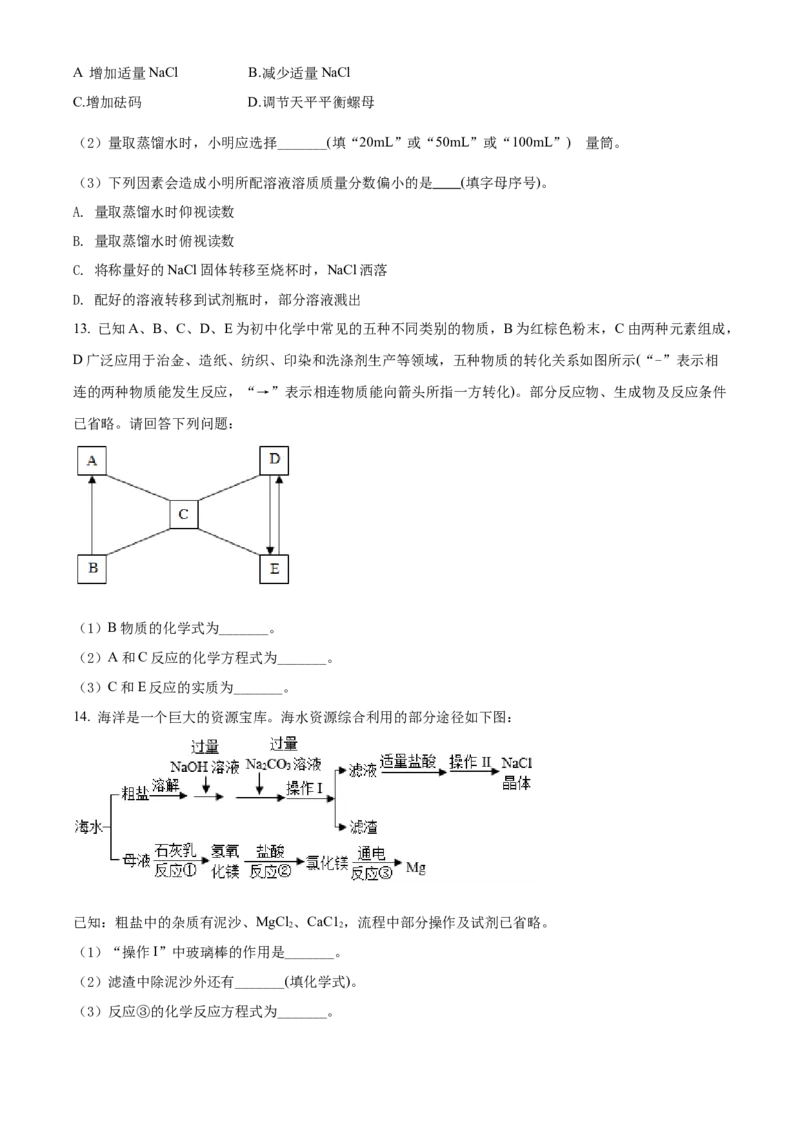
14. 海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如下图:
已知:粗盐中的杂质有泥沙、MgCl 、CaC1 ,流程中部分操作及试剂已省略。
2 2
(1)“操作I”中玻璃棒的作用是_______。
(2)滤渣中除泥沙外还有_______(填化学式)。
(3)反应③的化学反应方程式为_______。(4)海水中本身就有氯化镁,请分析反应①、②转化过程的目的_______。
15. 钢铁是应用最普遍的金属材料,也是最容易发生锈蚀的金属材料之一、人类为金属的锈蚀付出了巨大
的代价,所以金属的防腐和废旧金属的回收有着十分重要的意义。
(1)工业上用赤铁矿(主要成分Fe O)炼铁的原理:_______(用化学方程式表示)。
2 3
(2)钢铁生锈是铁与空气中_______发生化学反应的结果。
(3)处理某废旧金属后的溶液中含有Cu(NO ) 和AgNO 两种溶质,为回收其中的金属,向该溶液中加入
3 2 3
一定量的铁粉,充分反应后过滤,再向滤渣中加入稀盐酸,无气泡产生。则滤液中一定含有的金属离子是
_______;滤渣中可能含有_______。
三、实验探究题(本题2个小题,共16分。化学方程式每个2分,其余每空1分)
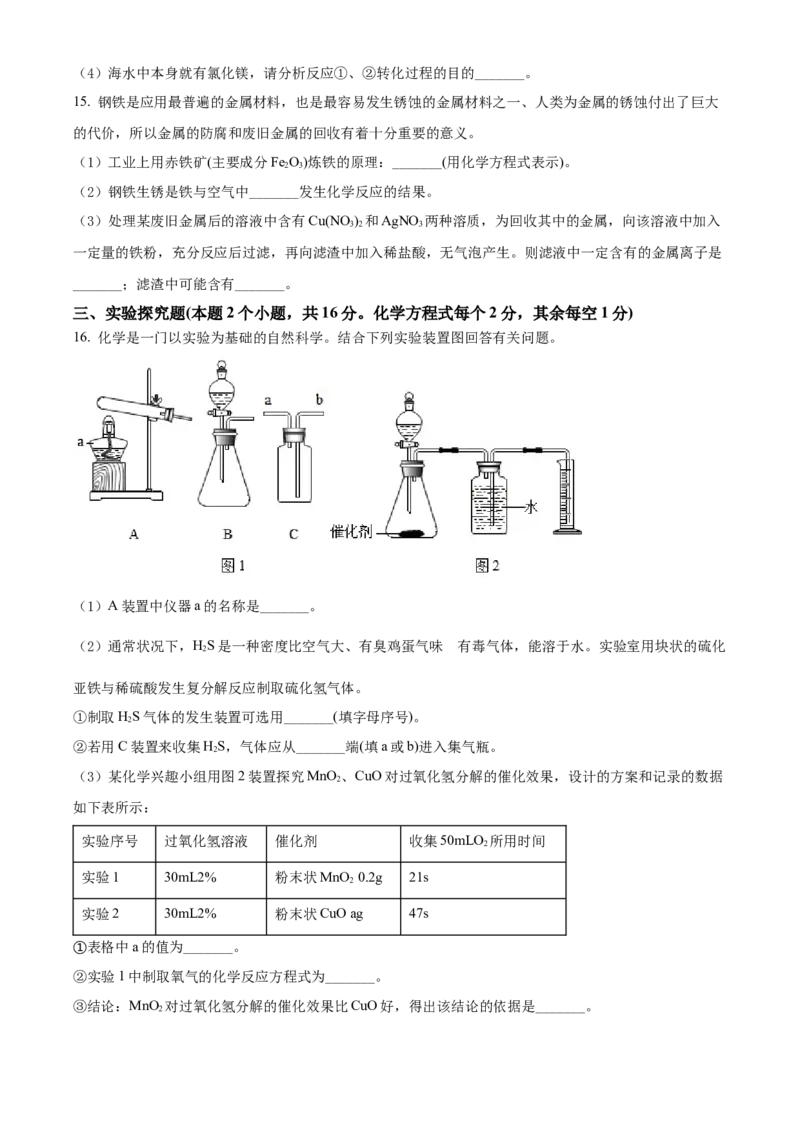
16. 化学是一门以实验为基础的自然科学。结合下列实验装置图回答有关问题。
(1)A装置中仪器a的名称是_______。
的
(2)通常状况下,HS是一种密度比空气大、有臭鸡蛋气味 有毒气体,能溶于水。实验室用块状的硫化
2
亚铁与稀硫酸发生复分解反应制取硫化氢气体。
①制取HS气体的发生装置可选用_______(填字母序号)。
2
②若用C装置来收集HS,气体应从_______端(填a或b)进入集气瓶。
2
(3)某化学兴趣小组用图2装置探究MnO 、CuO对过氧化氢分解的催化效果,设计的方案和记录的数据
2
如下表所示:
实验序号 过氧化氢溶液 催化剂 收集50mLO 所用时间
2
实验1 30mL2% 粉末状MnO 0.2g 21s
2
实验2 30mL2% 粉末状CuO ag 47s
①表格中a的值为_______。
②实验1中制取氧气的化学反应方程式为_______。
③结论:MnO 对过氧化氢分解的催化效果比CuO好,得出该结论的依据是_______。
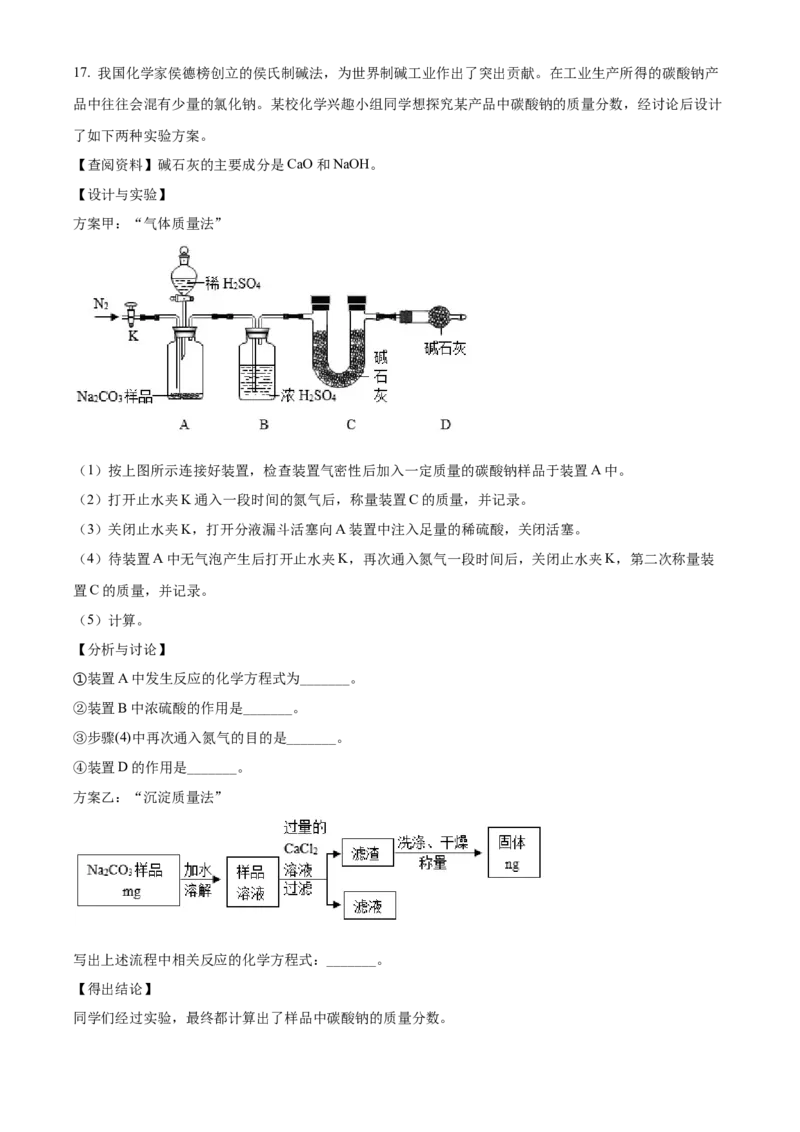
217. 我国化学家侯德榜创立的侯氏制碱法,为世界制碱工业作出了突出贡献。在工业生产所得的碳酸钠产
品中往往会混有少量的氯化钠。某校化学兴趣小组同学想探究某产品中碳酸钠的质量分数,经讨论后设计
了如下两种实验方案。
【查阅资料】碱石灰的主要成分是CaO和NaOH。
【设计与实验】
方案甲:“气体质量法”
(1)按上图所示连接好装置,检查装置气密性后加入一定质量的碳酸钠样品于装置A中。
(2)打开止水夹K通入一段时间的氮气后,称量装置C的质量,并记录。
(3)关闭止水夹K,打开分液漏斗活塞向A装置中注入足量的稀硫酸,关闭活塞。
(4)待装置A中无气泡产生后打开止水夹K,再次通入氮气一段时间后,关闭止水夹K,第二次称量装
置C的质量,并记录。
(5)计算。
【分析与讨论】
①装置A中发生反应的化学方程式为_______。
②装置B中浓硫酸的作用是_______。
③步骤(4)中再次通入氮气的目的是_______。
④装置D的作用是_______。
方案乙:“沉淀质量法”
写出上述流程中相关反应的化学方程式:_______。
【得出结论】
同学们经过实验,最终都计算出了样品中碳酸钠的质量分数。请你根据方案乙中测定的相关数据,求出样品中碳酸钠的质量分数为_______×100%(用含有m、n的代数
式表示)。
【反思与交流】
同学们经过讨论认为方案乙优于方案甲,理由主要是_______(填字母序号)。
A.节约能源 B.操作简便 C.保护环境
四、计算题(本大题只有一个小题,共6分)
18. 某厂生产的NaC1样品中含有少量MgCl 杂质。该厂质检员称取20g该样品,完全溶解在100g蒸馏水
2
中,向所得溶液中加入氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液的质量关系如图所示,请回答:
(1)样品中MgCl 的质量为_______g。
2
(2)计算恰好完全反应时,溶液中溶质的质量分数_____。(写出计算过程)