文档内容
乌鲁木齐市实验学校 2023-2024学年高三上学期1月月考
化学试题
总分100分 考试时间90分钟
一、单项选择题(共16小题,每题3分共48分)
1.分类思想是研究化学的常用方法。下列物质的分类正确的是
A.纯净物:石灰石、干冰、液氯、水银
B.电解质:BaSO、熔融NaCl、盐酸、CO
4 2
C.酸性氧化物:MnO、SO 、CO、CO
2 7 3 2
D.盐:NaHSO、CHCOONH、NaSO 、KClO
4 3 4 2 3
2.下列表达方式正确的是
A.Cr的外围电子排布式:3d44s2
B.NaHCO 在水中的电离方程式:NaHCO =Na++H++CO 2-
3 3 3
C.基态碳原子的价电子排布图为:
D.二氧化硅的分子式为SiO
2
3.三星堆,菁华荟萃的文物宝库,神秘梦幻的艺术殿堂,充溢着中华古代文明的无穷
魅力,闪烁着人类文化遗产的璀璨光彩。下列说法错误的是
文物
名称 青铜人头像 金面具 陶鸟头把勺 象牙
A.青铜是一种合金
B.金面具的金元素是不活泼金属,与任何物质均不反应
C.陶鸟头把勺是无机非金属材料D.象牙中含有的14C常用来考古断代,其中子数是8
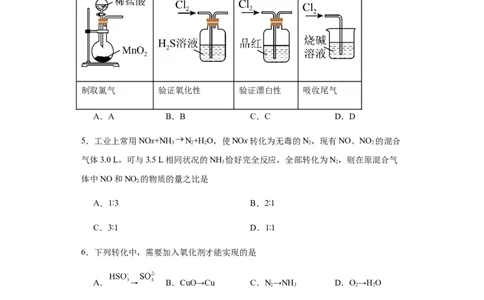
4.氯气及其化合物在生产、生活中应用广泛。实验室常用浓盐酸与 共热[或用
(s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达
到相应实验目的的是
A B C D
制取氯气 验证氧化性 验证漂白性 吸收尾气
A.A B.B C.C D.D
5.工业上常用NOx+NH N+H O,使NOx转化为无毒的N,现有NO、NO 的混合
3 2 2 2 2
气体3.0 L,可与3.5 L相同状况的NH 恰好完全反应,全部转化为N,则在原混合气
3 2
体中NO和NO 的物质的量之比是
2
A.1∶3 B.2∶1
C.3∶1 D.1∶1
6.下列转化中,需要加入氧化剂才能实现的是
A. → B.CuO→Cu C.N→NH D.O→HO
2 3 2 2
7.下列有关方程式书写均正确的是
A. 水溶液显碱性:
B.硫酸氢钠熔融状态下可发生电离:
C.泡沫灭火器的制作原理:D.加入氨水除去氯化铵溶液中少去氯化铁杂质:
8.新冠病毒(如图)由蛋白质和核酸组成,核酸由核苷酸组成。核苷酸的单体由戊糖、
磷酸基和含氮碱基构成。下列说法错误的是
A.蛋白质和核酸均是高分子
B.蛋白质中含C、H、O、N等元素
C.戊糖(C H O)与葡萄糖互为同系物
5 10 5
D.组成RNA的戊糖和碱基与DNA的不完全相同
9.某有机物的结构简式如图所示。下列关于该有机物的说法正确的是
A.该有机物能发生酯化、加成、氧化、水解等反应
B.该有机物中所有碳原子不可能处于同一平面上
C.与该有机物具有相同官能团的同分异构体有3种
D.1mol该有机物最多与4molH 反应
2
10.下列叙述不正确的是( )
A.原子半径:
B.热稳定性:
C.N、O、F元素的非金属性依次减弱
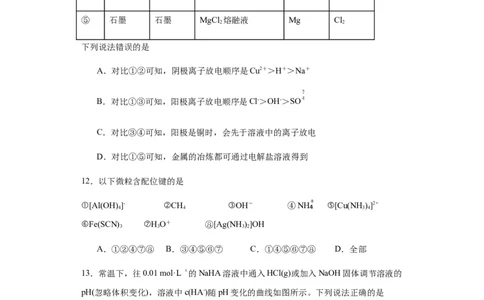
D.P、S、 元素最高价氧化物对应的水化物酸性依次增强11.为探究电解的离子放电规律,进行如下实验:
序号 阳极材料 阴极材料 电解质 阳极产物 阴极产物
① 石墨 石墨 0.1 mol/L CuCl 溶液 Cl Cu
2 2
② 石墨 石墨 0.1 mol/L NaCl溶液 Cl H
2 2
③ 石墨 石墨 0.2 mol/L CuSO 溶液 O Cu
4 2
④ 铜 石墨 0.2 mol/L CuSO 溶液 Cu2+ Cu
4
⑤ 石墨 石墨 MgCl 熔融液 Mg Cl
2 2
下列说法错误的是
A.对比①②可知,阴极离子放电顺序是Cu2+>H+>Na+
B.对比①③可知,阳极离子放电顺序是Cl->OH->SO
C.对比③④可知,阳极是铜时,会先于溶液中的离子放电
D.对比①⑤可知,金属的冶炼都可通过电解盐溶液得到
12.以下微粒含配位键的是
①[Al(OH) ]- ②CH ③OH- ④NH ⑤[Cu(NH )]2+
4 4 3 4
⑥Fe(SCN) ⑦H O+ ⑧[Ag(NH)]OH
3 3 3 2
A.①②④⑦⑧ B.③④⑤⑥⑦ C.①④⑤⑥⑦⑧ D.全部
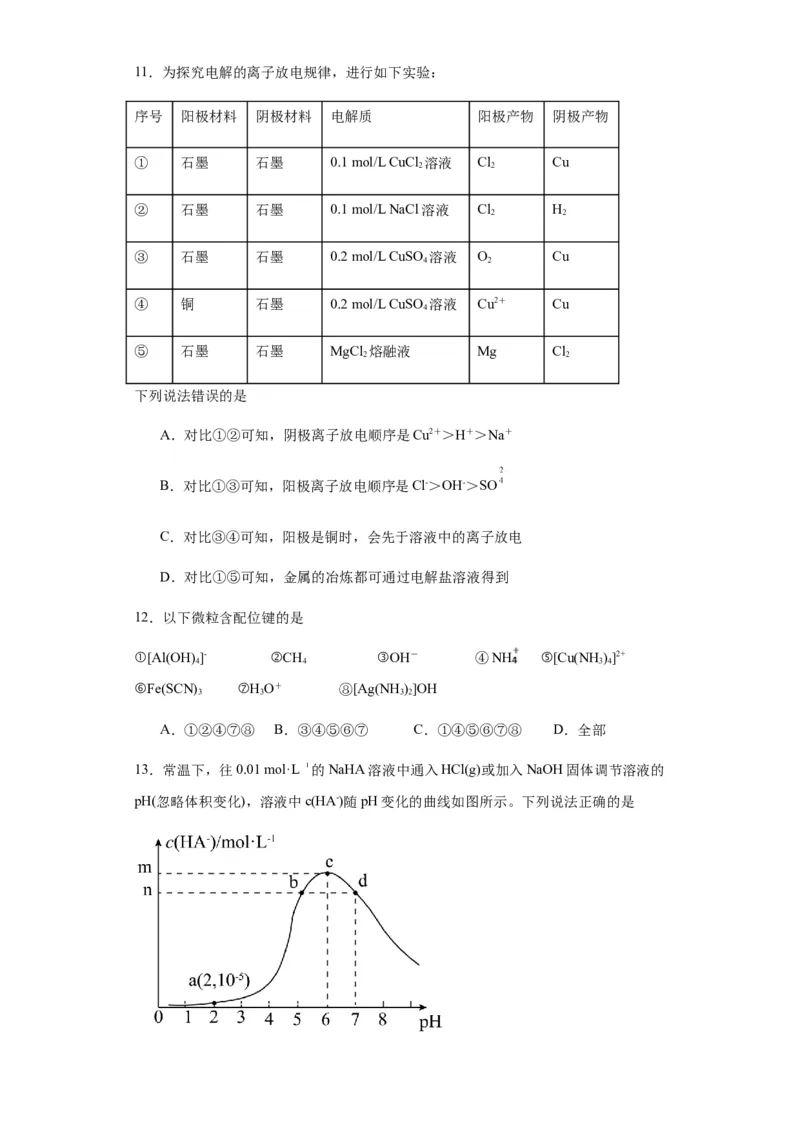
13.常温下,往0.01 mol·L 的NaHA溶液中通入HCl(g)或加入NaOH固体调节溶液的
pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图所示。下列说法正确的是A.水的电离程度:c>b=d>a
B.c点溶液中存在:
C.d点溶液中存在:
D.
14.科学家研究了钒系 催化剂催化脱硝机理,部分反应机理如下图所示。有关该
过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)
A. 是反应中间体 B.反应过程中V的成键数目发生变化
C.反应过程中 被还原 D.脱硝反应为:
15.化学中常用AG表示溶液的酸度(AG=lg )。室温下,向20.00 mL0.1000
mol·L-1的某一元碱MOH溶液中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度
AG随加入稀硫酸体积的变化如图所示。下列说法正确的是A.室温下MOH的电离常数K=1.0×10-6
b
B.当AG=0时,溶液中存在c(SO )>c(M+)>c(H+)=c(OH-)
C.a点对应的溶液中:c(M+)+c(MOH)=8c(SO )
D.b、c、d三点对应的溶液中,水的电离程度大小关系:c>b=d
16.生活因化学更加美丽,世界因化学更加精彩。下列与化学有关的说法正确的是
A.漂白精不可用作游泳池和环境消毒剂
B.腌制咸鸭蛋利用了半透膜的渗析原理
C.泡沫灭火器能用于电器起火时的灭火
D.95%的医用酒精消毒液效果比75%的好
二、综合题(本题共5小题,共52分。请根据答题卡题号及分值在各题目
的答题区域内作答,超出答题区域的答案无效。)
17.X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在地壳中含量
最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J
形成离子化合物,且J+的半径大于X—的半径,Y的氧化物是形成酸雨的主要物质之一。
请回答:
(1)Q元素在周期表中的位置 ;
(2)这五种元素原子半径从大到小的顺序为(填元素符号)。
(3)元素的非金属性Z Q(填“>”或“<”),下列各项中,不能说明这一结
论的事实有 (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)Q的氢化物与Z的氢化物反应的化学方程式为
。
(5)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,
写出A的电子式 ;B的水溶液不呈中性的原因
(用离子方程式表示)。
(6)液态A类似XZ,也能微弱电离且产生电子数相同的两种离子,则液态A的电离
2
方程式为 ;
(7)若使A按下列途径完全转化为F:
①F的化学式为 ;
②参加反应的A与整个过程中消耗D的物质的量之比为 。
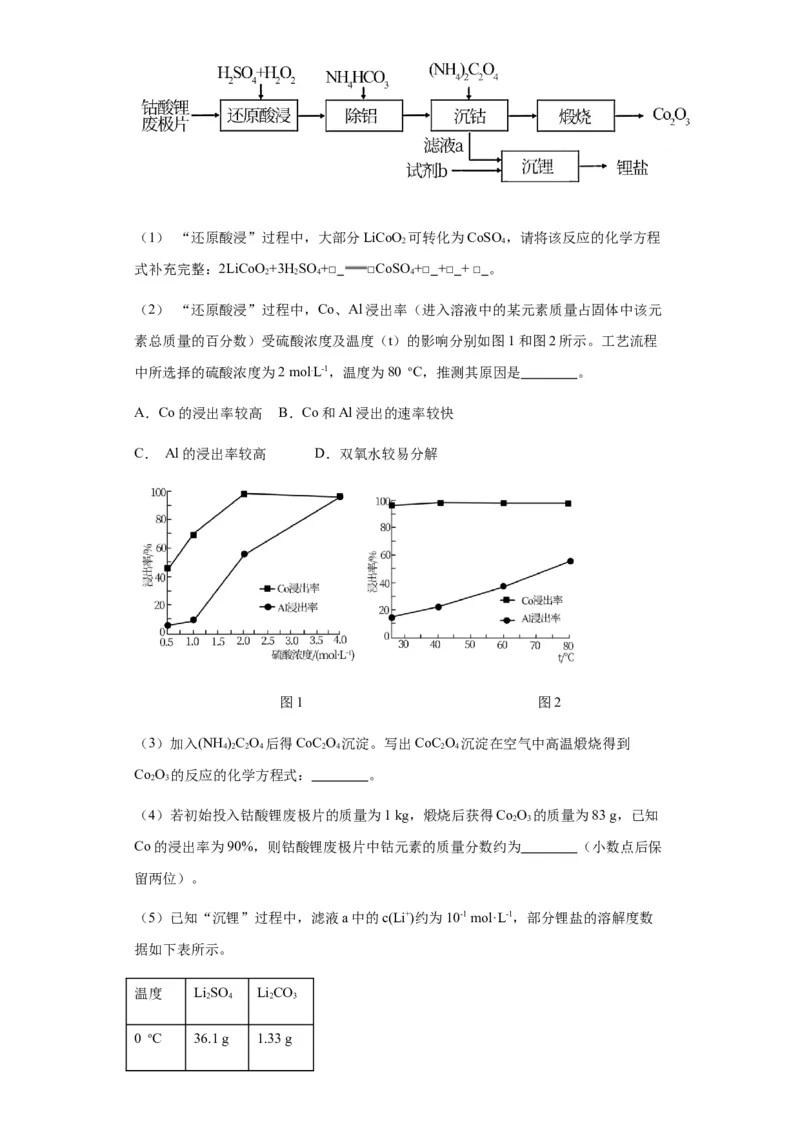
18.钴酸锂废极片中钴回收的某种工艺流程如下图所示,其中废极片的主要成分为钴
酸锂(LiCoO )和金属铝,最终可得到Co O 及锂盐。
2 2 3(1) “还原酸浸”过程中,大部分LiCoO 可转化为CoSO ,请将该反应的化学方程
2 4
式补充完整:2LiCoO +3H SO +□ □CoSO +□ +□ + □ 。
2 2 4 4
(2) “还原酸浸”过程中,Co、Al浸出率(进入溶液中的某元素质量占固体中该元
素总质量的百分数)受硫酸浓度及温度(t)的影响分别如图1和图2所示。工艺流程
中所选择的硫酸浓度为2 mol.L-1,温度为80 oC,推测其原因是 。
A.Co的浸出率较高 B.Co和Al浸出的速率较快
C. Al的浸出率较高 D.双氧水较易分解
图1 图2
(3)加入(NH )C O 后得CoC O 沉淀。写出CoC O 沉淀在空气中高温煅烧得到
4 2 2 4 2 4 2 4
Co O 的反应的化学方程式: 。
2 3
(4)若初始投入钴酸锂废极片的质量为1 kg,煅烧后获得Co O 的质量为83 g,已知
2 3
Co的浸出率为90%,则钴酸锂废极片中钴元素的质量分数约为 (小数点后保
留两位)。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10-1 mol·L-1,部分锂盐的溶解度数
据如下表所示。
温度 LiSO LiCO
2 4 2 3
0 oC 36.1 g 1.33 g100 oC 24.0 g 0.72 g
结合数据分析,沉锂过程所用的试剂b是 (写化学式),相应的操作方法:
向滤液a中加入略过量的试剂b,搅拌, ,洗涤干燥。
19.二硫化钼(MoS )被誉为“固体润滑剂之王”,利用低品质的辉钼矿(含MoS 、SiO
2 2 2
以及CuFeS 等杂质)制备高纯二硫化钼的一种生产工艺如下:
2
回答下列问题:
(1)钼酸铵的化学式为(NH )MoO ,其中Mo的化合价为 。
4 2 4
(2)利用联合浸出除杂时,氢氟酸可除去的杂质化学式为 ,如改用FeCl 溶液氧
3
化浸出,CuFeS 杂质的浸出效果更好,写出氧化浸出时发生的化学反应方程式 。
2
(3)加入NaS后,钼酸铵转化为硫代钼酸铵[(NH )MoS ],写出(NH )MoS 与盐酸生成
2 4 2 4 4 2 4
MoS 沉淀的离子反应方程式 。
3
(4)由下图分析产生三硫化钼沉淀的流程中应选择的最优温度和时间是 。
利用化学平衡移动原理分析低于或高于最优温度时,MoS 的产率均下降的原因:
3
。
(5)MoO ·H O作为高能非水体系电池的正极材料优于一般新型材料,某电池反应为:
3 2
MoO ·H O+xA=AxMoO ·H O(某文献记载:式中0c(SO ) >c(H+)=c(OH-),故B错
误;
C.a点时,消耗硫酸5mL,根据2MOH~H SO 可知:消耗MOH的量2×0.05×5×10-3mol;
2 4
剩余MOH的量为20.00×10-3×0.1000 -2×0.05×5×10-3=1.5×10-3mol,生成MSO 的量为
2 4
0.05×5×10-3mol,即混合液中n(MOH):n(M SO )=1.5:0.25=6:1;根据物料守恒可知,c(M+)
2 4
+c(MOH)=8c(SO ),故C正确;
D.c点为酸碱恰好完全反应的点,生成了强酸弱碱盐,促进了水解,从c点以后,硫酸过
学科网(北京)股份有限公司量,酸抑制水电离,硫酸属于强酸,对水的电离平衡抑制程度大,因此水的电离程度:
c>b>d,故D错误;
故选C。
16.B
【解析】A.漂白精的主要成分是Ca(ClO) 和CaCl ,具有强氧化性,能杀菌消毒,可用作
2 2
游泳池和环境消毒剂,A不正确;
B.鸭蛋的蛋液与蛋壳之间有一层膜,此膜能让食盐透过,但不能让蛋清透过,所以腌制
咸鸭蛋时利用了半透膜的渗析原理,B正确;
C.电器起火时,不能使用泡沫灭火器灭火,否则会造成火势蔓延,C不正确;
D.95%的医用酒精消毒液效果比75%的差,因为它能使细菌表面蛋白质迅速变性,形成硬
壳保护膜,阻止酒精与细菌表面蛋白质的进一步作用,不能杀死细菌,D不正确;
故选B。
17. 第三周期第ⅥA族 Na>S>N>O>H > C H S+HO=
2 2 2
2HO+S↓ NH ++H O NH ·H O+H+ 2NH NH ++NH-
2 4 2 3 2 3 4 2
HNO 1:2
3
【解析】试题分析:X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在
地壳中含量最高,则Z是氧元素;J元素的焰色反应呈黄色,所以j是钠元素;Q的最外层
电子数与其电子总数比为3:8,且Q的原子序数大于钠元素,因此Q是S元素。X能与J形
成离子化合物,且J+的半径大于X—的半径,所以X是氢元素。Y的氧化物是形成酸雨的主
要物质之一,原子序数小于氧元素,则Y是氮元素。
(1)S的原子序数是16,S元素在周期表中的位置第三周期第ⅥA族;
(2)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,因此这五种
元素原子半径从大到小的顺序为Na>S>N>O>H。
(3)同主族自上而下非金属性逐渐减弱,则元素的非金属性O>S。A. S的氢化物的水溶液放置在空气中会变浑浊,这说明HS被氧气氧化为S,因此可以说明氧元素的 非金属性
2
强于S,A正确;B. Z与Q之间形成的化合物中S元素显正价,则说明共用电子对偏离S,
所以氧元素的非金属性强于S,B正确;C.非金属性强弱与单质所处的状态没有关系,C错
误;D.根据元素在周期表中的相对位置也判断元素的非金属性强弱,D正确,答案选C。
(4)Q的氢化物双氧水与Z的氢化物HS反应的化学方程式为HS+HO=2HO+S↓。
2 2 2 2 2
(5)H与N可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,则
A是氨气,B是铵根。氨气是共价化合物,电子式为 ;铵根水解,溶液显酸性,
离子方程式为NH ++HO NH ·H O+H+。
4 2 3 2
(6)液态氨气类似HO,也能微弱电离且产生电子数相同的两种离子,则根据水的电离方
2
程式可知液态氨气的电离方程式为2NH NH ++NH-;
3 4 2
(7)①根据氨气能与D连续反应说明D是氧气,E是NO,C是NO ,F是硝酸,则F的
2
化学式为HNO;
3
②根据方程式NH +2O =HNO+H O可知参加反应的A与整个过程中消耗D的物质的量之
3 2 3 2
比为1:2。
考点:考查元素推断的有关应用与判断
18. 2LiCoO + 3H SO + H O 2CoSO + LiSO + O ↑+ 4H O A B
2 2 4 2 2 4 2 4 2 2
4CoC O + 3O 2Co O + 8CO 6.56 % NaCO 加热浓缩,趁热过滤
2 4 2 2 3 2 2 3
【解析】(1). “还原酸浸”过程中,大部分LiCoO 可转化为CoSO ,Co元素的化合价从+3
2 4
价降低到+2价,则HO 中O元素的化合价从-1价升高到0价,根据得失电子守恒和原子
2 2
守恒,该反应的化学方程式为:2LiCoO + 3H SO + H O=2CoSO + LiSO + O ↑+
2 2 4 2 2 4 2 4 2
4HO,故答案为2LiCoO + 3H SO + H O=2CoSO + LiSO + O ↑+ 4H O;
2 2 2 4 2 2 4 2 4 2 2
(2). 由图1可知,当硫酸浓度为2 mol.L-1时,Co的浸出率较高,由图2可知,当温度为
80℃,Co和Al浸出的速率较快,故答案选:AB;
(3). CoC O 沉淀在空气中高温煅烧,CoC O 被氧气氧化得到Co O,反应的化学方程式为:
2 4 2 4 2 3
4CoC O + 3O =2Co O + 8CO,故答案为4CoC O + 3O =2Co O + 8CO;
2 4 2 2 3 2 2 4 2 2 3 2
学科网(北京)股份有限公司(4). 煅烧后获得Co O 的质量为83 g,则Co原子的质量为:83× =59g,Co的浸出率为
2 3
90%,则1 kg钴酸锂废极片中钴元素的质量分数约为 ×100%=6.56 %,故答案为
6.56 %;
(5). 由表中数据可知,在相同温度下,LiCO 的溶解度更小,且温度越高,LiCO 的溶解
2 3 2 3
度越小,则沉锂过程所用的试剂b是NaCO,相应的操作方法:向滤液a中加入略过量的
2 3
NaCO,搅拌,加热浓缩,趁热过滤,洗涤干燥,故答案为NaCO;加热浓缩,趁热过滤。
2 3 2 3
19.(1)+6
(2) SiO 4FeCl +CuFeS =5FeCl +CuCl +2S↓
2 3 2 2 2
(3)MoS +2H+=MoS↓+H S↑
3 2
(4) 40℃,30min 温度太低不利于HS逸出;温度太高,盐酸挥发,溶液c(H+)下
2
降,都不利于反应正向进行
(5)Li MoO ·H O-xe-=xLi++MoO·H O
x 3 2 3 2
(6)3.6×102
【分析】本流程欲利用辉钼矿制备高纯二硫化钼,将辉钼矿溶解在盐酸-氢氟酸中,此时矿
石中的SiO、CuFeS 溶解,得到的固体是粗MoS ,随后将得到是粗MoS 洗净干燥、经氧
2 2 2 2
化焙烧后得到MoS 固体,将MoS 溶解在氨水中得到钼酸铵溶液,随后向钼酸铵溶液中加
3 3
入NaS溶液,钼酸铵转化为硫代钼酸铵[(NH )MoS ],硫代钼酸铵[(NH )MoS ]与盐酸反应
2 4 2 4 4 2 4
生成纯净的MoS ,MoS 在氢气中还原得到MoS 。
3 3 2
【解析】(1)根据化合价原则,钼酸铵[(NH )MoO ]中Mo元素的化合价为+6价。
4 2 4
(2)氢氟酸可与酸性氧化物SiO 反应,所以联合浸出除杂时,用氢氟酸除去的是SiO 杂
2 2
质;Fe3+具有较强的氧化性,可氧化杂质CuFeS 中的-2价的S,反应的化学方程式为
2
4FeCl +CuFeS =5FeCl +CuCl +2S↓。
3 2 2 2(3)根据题目所述,(NH )MoS 属于铵盐,易溶于水,所以与盐酸生成MoS 沉淀的离子
4 2 4 3
方程式为MoS +2H+=MoS↓+H S↑。
3 2
(4)由图象分析可知,在40℃时产率比其它温度下都高,反应进行到30min时产率达到
最大值,所以产生三硫化钼沉淀的最优温度和时间是40℃、30min;如果温度太低不利于
HS逸出,不利于沉淀的生成;温度太高,盐酸挥发,使溶液中c(H+)下降,都不利于反应
2
正向进行。
(5)该电池以金属锂为负极,则负极反应式为xLi-xe-=xLi+,正极反应式可由总反应式—
负极反应式得到,即MoO ·H O+xLi++xe-=LixMoO ·H O,根据充放电原则,当对该电池充
3 2 3 2
电时,阳极反应则为原电池的正极反应的逆反应,所以阳极反应式为LiMoO ·H O-xe-=xLi+
x 3 2
+MoO·H O。
3 2
(6)已知BaSO 和BaMoO 的组成比相同,结合其溶度积大小,当BaMo0 开始沉淀时,
4 4 4
c(MoO )= ,而此时溶液中c(SO )= ,所以c(MoO )/c(SO
)=4.0×10-8/1.1×10-10=3.6×102。
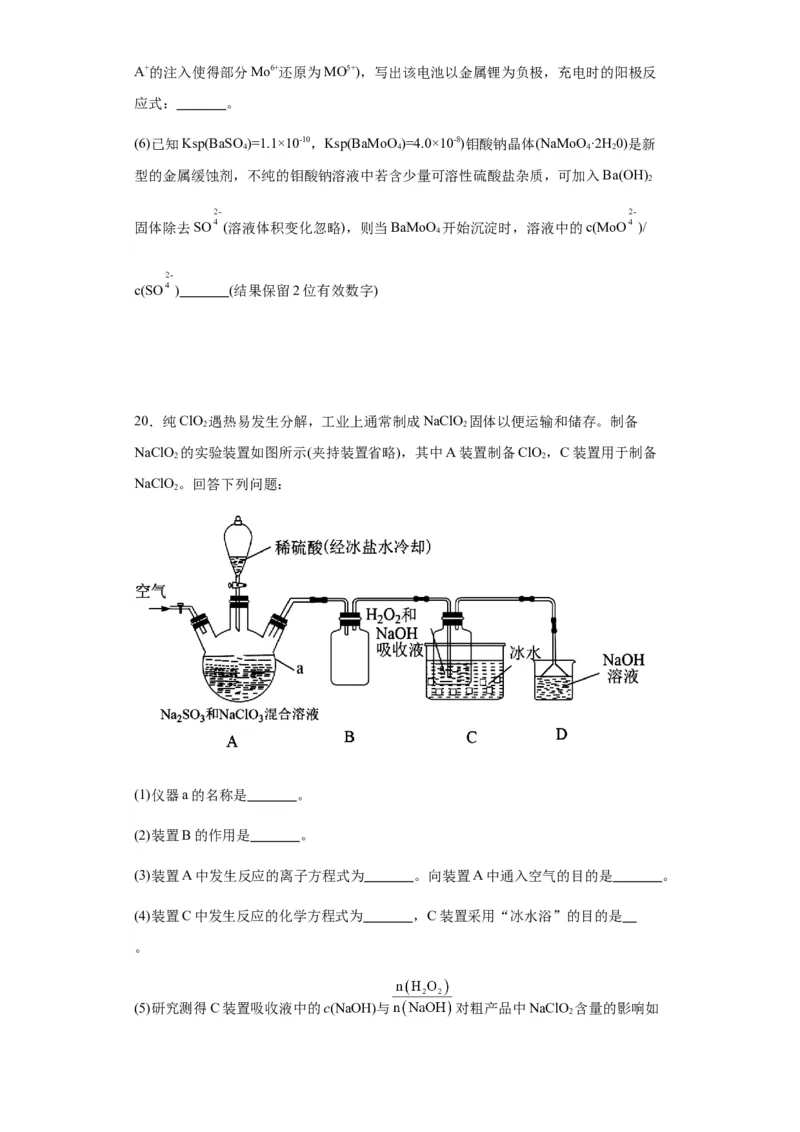
20.(1)三颈烧瓶
(2)安全瓶,防止倒吸
(3) +2 +2H+= +2ClO ↑+H O 赶出ClO 气体,使其进入装置C则发
2 2 2
生反应制取NaClO;
2
(4) 2ClO +2NaOH+HO=2NaClO +2H O+O 防止温度过高,NaClO 分解为
2 2 2 2 2 2 2
NaClO 和NaCl,同时可减少由于温度过高导致HO 分解。
3 2 2
(5) 4 0.8
(6)72.4%
【分析】在装置A中NaSO 、NaClO 与硫酸发生氧化还原反应产生ClO ,在装置C中发
2 3 3 2
学科网(北京)股份有限公司生反应:2ClO +2NaOH+HO=2NaClO +2H O+O,以制取NaClO,装置B的作用是安全
2 2 2 2 2 2 2
瓶,防止由于装置C降温使装置气体压强减少,而使装置A中液体倒吸,装置D的NaOH
可以吸收ClO ,防止大气污染。根据物质反应转化关系,由反应消耗NaSO 的物质的量
2 2 2 3
计算NaClO 的物质的量及质量,最后结合样品总质量计算其中NaClO 的含量。
2 2
【解析】(1)根据装置图可知:仪器a的名称是三颈烧瓶;
(2)装置B的作用是安全瓶,防止倒吸现象的发生;
(3)在装置A中NaSO 、NaClO 与硫酸发生氧化还原反应产生ClO 、NaSO 、HO,反
2 3 3 2 2 4 2
应的化学方程式为:NaSO +2NaClO +H SO =2Na SO +2ClO +H O,该反应的离子方程式
2 3 3 2 4 2 4 2 2
为: +2 +2H+= +2ClO ↑+H O;
2 2
向装置A中通入空气的目的是赶出ClO 气体,然后通过装置B到装置C中发生反应;
2
(4)在装置C中,ClO 与NaOH及HO 发生氧化还原反应产生NaClO,根据电子守恒、
2 2 2 2
原子守恒,可得发生反应的化学方程式为:2ClO +2NaOH+HO=2NaClO +2H O+O;
2 2 2 2 2 2
NaClO 的溶解度随温度升高而增大,过氧化氢高温易分解,所以冰水浴冷却的目的是:降
2
低NaClO 的溶解度、减少HO 的分解;由于纯ClO 遇热易发生分解,且ClO 的沸点较低,
2 2 2 2 2
所以冰水浴还可以避免ClO 分解,使其变为液态,方便使用;
2
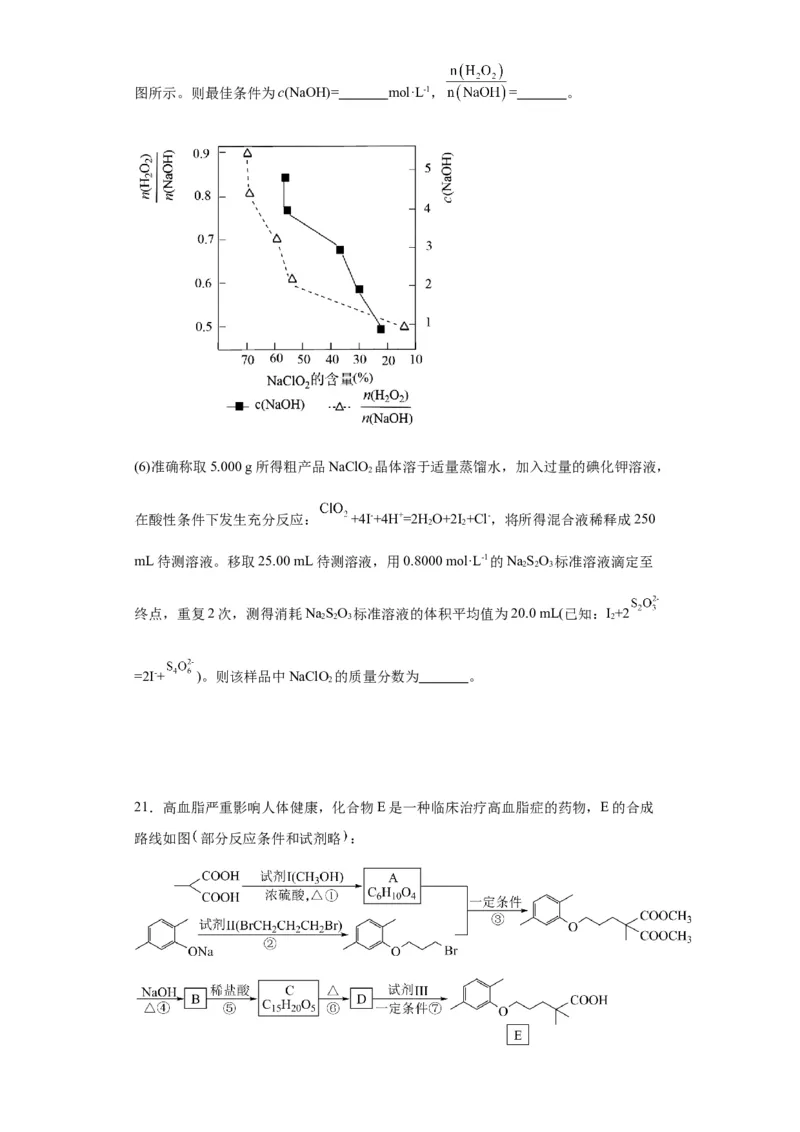
(5)根据图示可知:当c(NaOH)=4 mol/L时, =0.8时粗产品中NaClO 含量最高,
2
再进一步提高浓度和比值,对产量并没有提高,浪费原料。故最佳最佳条件为c(NaOH)= 4
mol/L, =0.8;
(6)根据反应方程式 +4I-+4H+=2H O+2I +Cl-、I+2 =2I-+ ,可得关系式:
2 2 2
ClO ~2I~4 ,20.00 mL0.8000 mol·L-1的NaSO 标准溶液中含有溶质的物质的量
2 2 2 2 3
n(Na SO)=c·V=0.8000 mol/L×0.02 L=0.016 mol,则根据关系式可知其反应消耗NaClO 的
2 2 3 2物质的量n(NaClO)= n(Na SO)=0.004 mol,则5.000 g样品中含有NaClO 的物质的量
2 2 2 3 2
n(NaClO)= 0.004 mol× =0.04 mol,m(NaClO)=0.04 mol×90.5 g/mol=3.62 g,所以该
2 2
样品中NaClO 的质量分数为 。
2
21. 甲醇 溴原子 取代反应 CHCH(COOH) +2CH OH
3 2 3
CHCH(COOCH )+2H O
3 3 2 2
n + n
→ +(2n-1)HO
2
【解析】(1)试剂Ⅰ的结构简式为CHOH,名称为甲醇;试剂Ⅱ的结构简式为
3
BrCHCHCHBr,所含官能团的名称为溴原子;根据 和
2 2 2
的结构及试剂Ⅱ判断第②步的反应类型为取代反应;
(2)根据题给转化关系知第①步反应为CHCH(COOH) 和CHOH在浓硫酸、加热的条件
3 2 3
学科网(北京)股份有限公司下发生酯化反应生成CHCH(COOCH ) 和水,化学方程式为CHCH(COOH) +2CH OH
3 3 2 3 2 3
CHCH(COOCH )+2H O ;
3 3 2 2
(3)根据题给转化关系推断C为 ,结合题给信息反应知
在加热条件下反应生成
,化学方程式为
;
(4)试剂Ⅲ为单碘代烷烃,根据 和
的结构推断,试剂Ⅲ的结构简式是CHI;
3
(5)C的分子式为C H O,其同分异构体在酸性条件下水解,含有酯基,生成X、Y和
15 20 5
CH(CH)OH,生成物X含有羧基和苯环,且X和Y的核磁共振氢谱均只有两种类型的吸
3 2 4
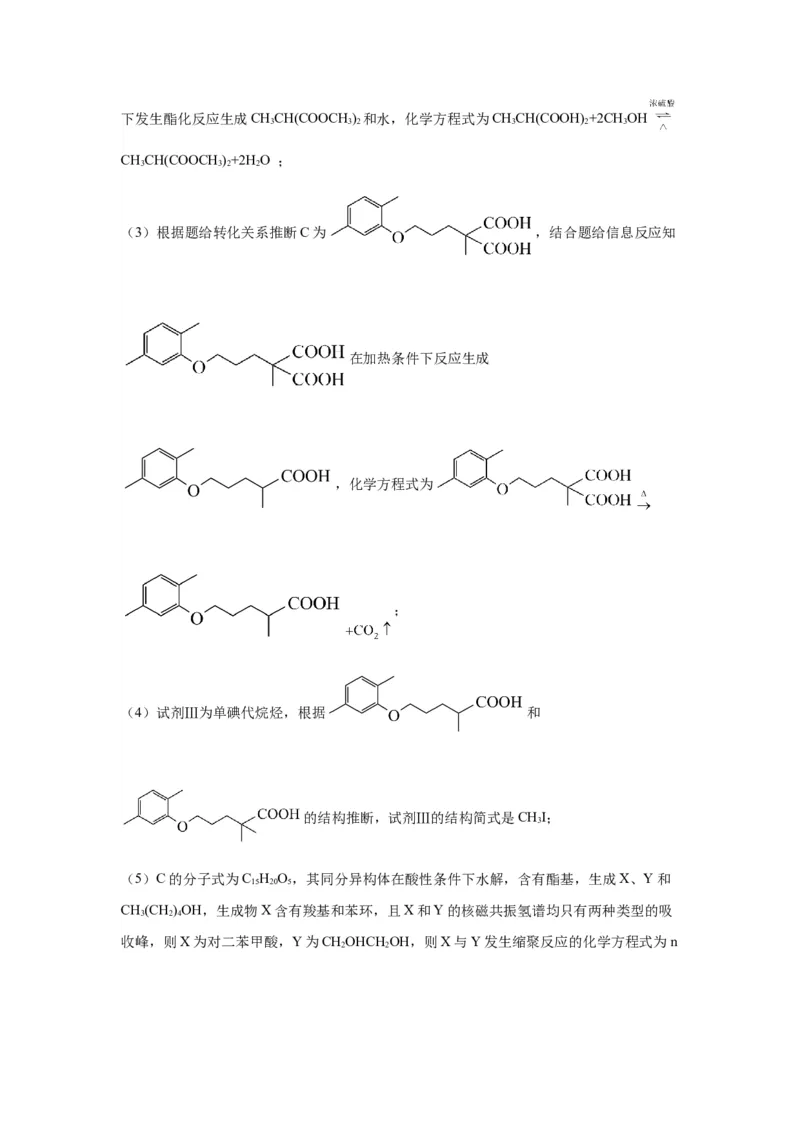
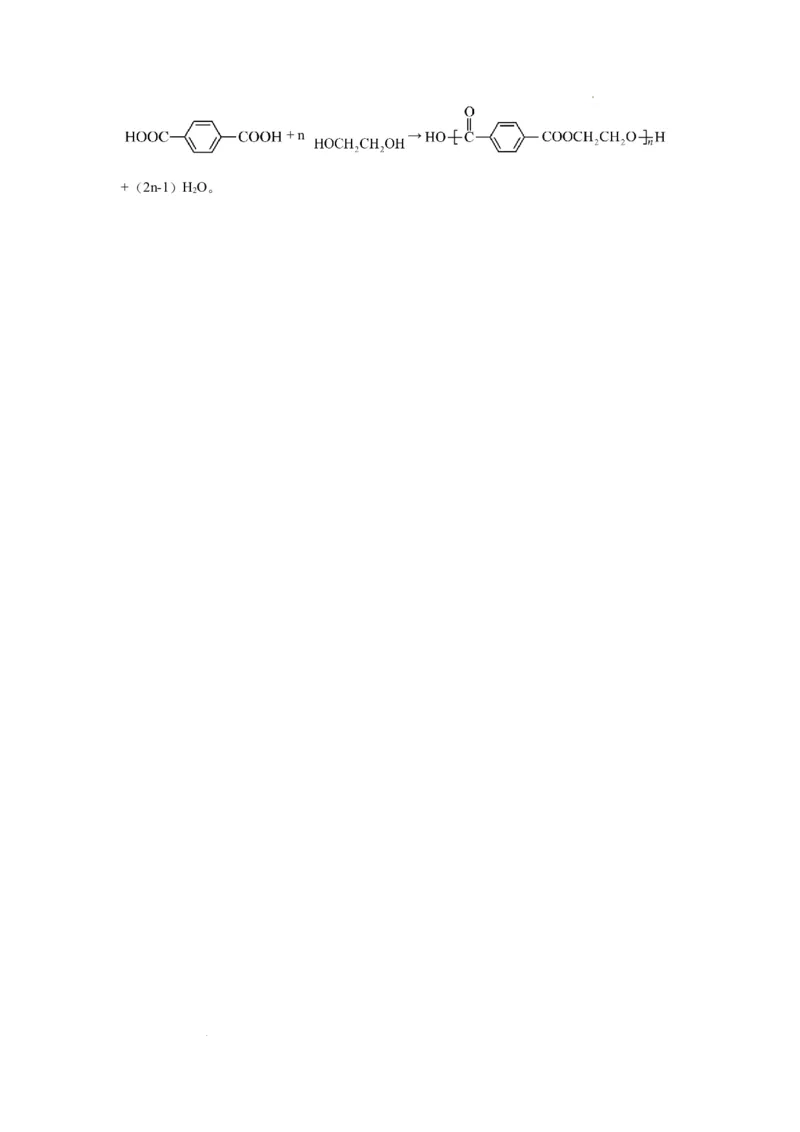
收峰,则X为对二苯甲酸,Y为CHOHCH OH,则X与Y发生缩聚反应的化学方程式为n
2 2+ n →
+(2n-1)HO。
2
学科网(北京)股份有限公司