文档内容
江阴市三校 2025-2026 学年度第一学期 12 月联合考试
化学试卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Mo 96
一、单项选择题:共13小题,每题3分,共39分。每题只有一个选项最符合题意。
1. 化学与生产生活、科技密切相关。下列应用中所用到的主要物质属于无机非金属材料的是
A. 亚冬会冰壶所用花岗岩 B. 制造飞机材料所用的硬铝
C. 制造医用材料所用的聚乳酸 D. 潜艇降噪所用的橡胶消声瓦
2. 探索自然界奥秘的一个重要方面是研究物质的微观结构。下列化学用语不正确的是
A. 的电子式: B. 溶液中的水合离子:
C. 键形成的轨道重叠示意图: D. 分子的球棍模型为:
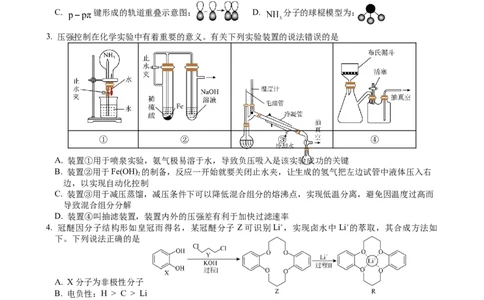
3. 压强控制在化学实验中有着重要的意义。有关下列实验装置的说法错误的是
① ② ③ ④
A. 装置①用于喷泉实验,氨气极易溶于水,导致负压吸入是该实验成功的关键
B. 装置②用于Fe(OH) 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右
2
边,以实现自动化控制
C. 装置③用于减压蒸馏,减压条件下可以降低混合组分的熔沸点,实现低温分离,避免因温度过高而
导致混合组分分解
D. 装置④叫抽滤装置,装置内外的压强差有利于加快过滤速率
4. 冠醚因分子结构形如皇冠而得名,某冠醚分子 Z可识别Li+,实现卤水中Li+的萃取,其合成方法如
下。下列说法正确的是
A. X分子为非极性分子
B. 电负性:H > C > Li
C. Li+与Z通过弱配位键相结合
D. Z可以识别Li+、Na+、K+、Cs+等碱金属离子,形成类似于R的结构
阅读下列材料,完成下列几个问题:
氮及其化合物在生产生活中有重要应用。氮元素是典型变价非金属元素,其氧化物和氢化物种类较多,
氢化物有NH 、NH(联氨,又名肼)、HN (叠氮酸)等。人工固氮技术是20世纪人类最伟大的成就之一,
3 2 4 3
为人类解决粮食短缺问题作出了巨大的贡献。氨易液化,液氨能与钠反应。NH 中的一个H原子被-OH
3
取代可形成羟胺(NH OH),被-NH 取代可形成肼(N H),肼的燃烧热为622kJ·mol-1。将尿素、NaClO和
2 2 2 4
NaOH溶液混合,在一定条件下反应可制得肼。
5. 下列有关含氮物质的性质与用途对应关系正确的是
A. NH 具有较强的还原性,可用作火箭升空的燃料
2 4
B. NO为无色气体,在人 的生命活动中作为一种信息分子
C. NH Cl受热易分解,实验室可用NH Cl和Ca(OH) 共热制NH
4 4 2 3D. 浓硝酸有强酸性,常温下可用铁槽车运输浓硝酸
6. 下列化学反应的表示正确的是
A. 尿素、NaClO、NaOH溶液制取肼的离子方程式:CO(NH)+ClO-=CO ↑+N H+Cl-
2 2 2 2 4
B. 过量氨水和SO 反应:SO +2NH·H O=(NH )SO +H O
2 2 3 2 4 2 3 2
C. 金属钠和液氨反应:NH +Na=NaNH+H ↑
3 2 2
D. 肼燃烧的热化学方程式:NH(l)+O (g)=N(g)+2HO(g) ΔH =-622kJ·mol-1
2 4 2 2 2
7. 已知:-OH的吸电子能力比-NH 的强。下列说法正确的是
2
A. NH OH中N结合H+的能力比NH 弱 B. NH 的键角比HO小
2 2 4 3 2
C. NH OH难溶于水 D. NH 、HN 、NH Cl形成的晶体都是分子晶体
2 3 3 4
8. 在给定条件下,下列制备过程涉及 的物质转化均可实现的是
.
A 制备金属钛:熔融NaCl――→Na――→Ti
B. 制镁工业: 海水――→Mg(OH) ――→MgO――→Mg
2
C. 提取碘:I(CCl )――――→NaI和NaIO ――→I
2 4 3 2
D. 制备Fe(OH) 胶体:Fe O――→FeCl――→Fe(OH) 胶体
3 2 3 3 3
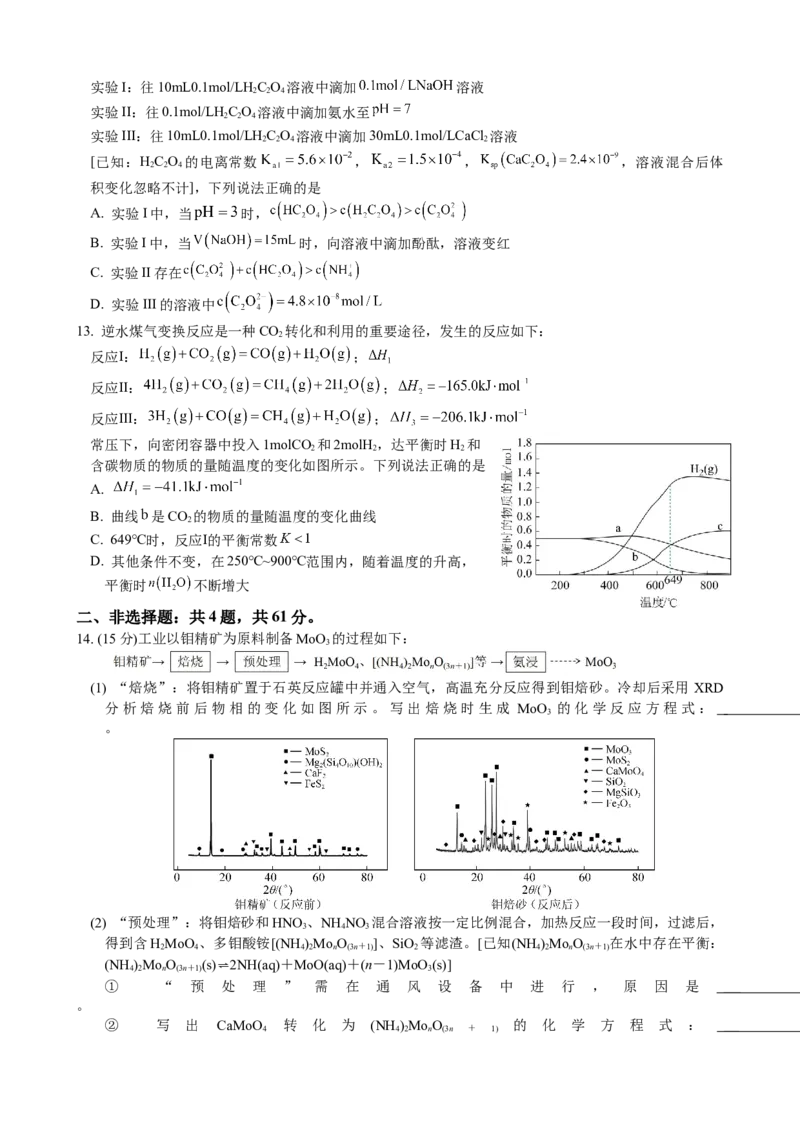
9. 在 水溶液中,电化学方法合成高能物质 时,伴随少量 生成,
电解原理如图所示,下列说法正确的是
A. 生成 的电极反应:
B. 电解时, 向 电极移动
C. 每生成 的同时,生成
D. 电解一段时间后,溶液 降低
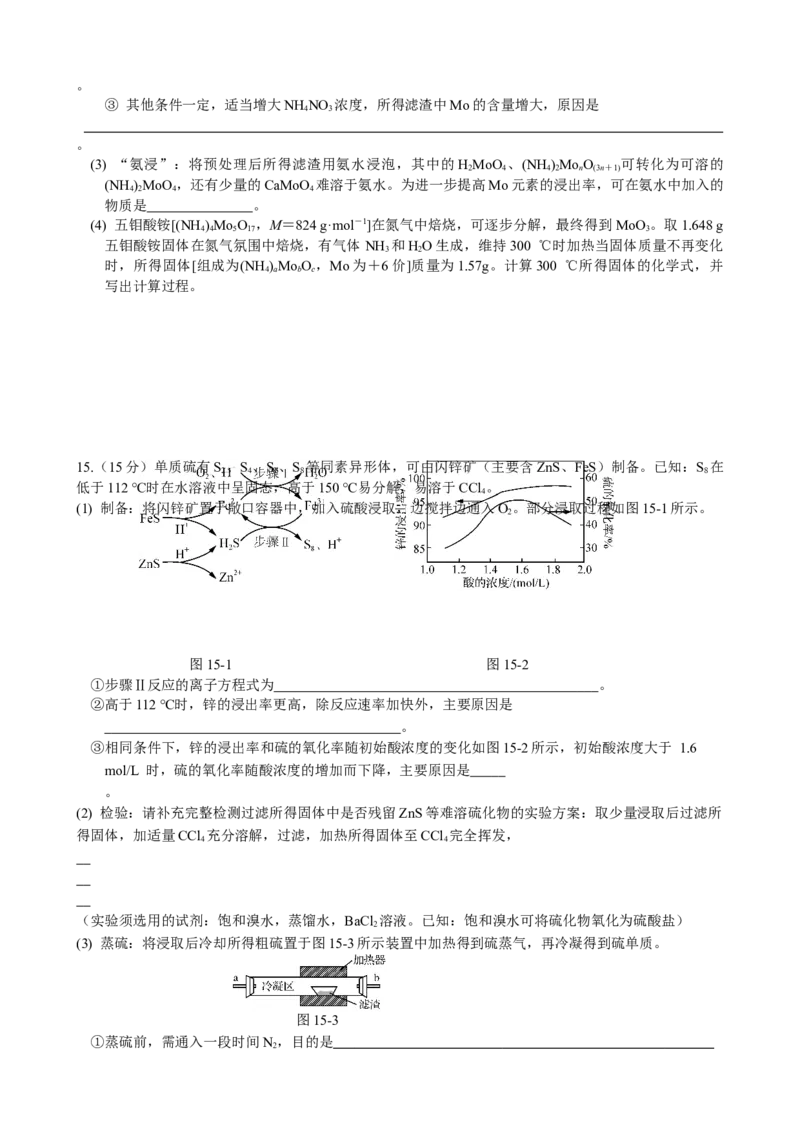
10. 工业利用钒渣(主要成分为FeVO,杂质为Al O)制备VO 的工艺流程如下:
2 4 2 3 2 5
已知:“焙烧”的产物之一为NaVO 。下列说法不正确的是( )
3
A. “焙烧”时,n(氧化剂)∶n(还原剂)=4∶5
B. “调pH”的目的是将溶液中的铝元素转化为Al(OH) 而除去
3
C. 不选用HCl“调pH”的原因可能与VO的氧化性较强有关
D. “沉钒”后的溶液中c(VO)·c(NH)=K (NH VO )
sp 4 3
11. 下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
用pH试纸分别测 溶液和 证明 的酸性强
A
溶液的pH 于
将可能含有Fe2+的氯化铁溶液滴入酸性KMnO 溶液中, 氯化铁溶液中是否含有
B 4
溶液紫红色是否褪去 Fe2+
向等物质的量浓度的 、 混合溶液中滴加 证明:
C
溶液,先生成 白色沉淀
向含酚酞的 溶液中加入少量 固体,观察溶液颜色 证明 溶液中存在
D
变化 水解平衡
12. 草酸(HC O)是二元弱酸。某小组做如下三组实验:
2 2 4实验I:往10mL0.1mol/LHC O 溶液中滴加 溶液
2 2 4
实验II:往0.1mol/LHC O 溶液中滴加氨水至
2 2 4
实验III:往10mL0.1mol/LHC O 溶液中滴加30mL0.1mol/LCaCl 溶液
2 2 4 2
[已知:HC O 的电离常数 , , ,溶液混合后体
2 2 4
积变化忽略不计],下列说法正确的是
A. 实验I中,当 时,
B. 实验I中,当 时,向溶液中滴加酚酞,溶液变红
C. 实验II存在
D. 实验III的溶液中
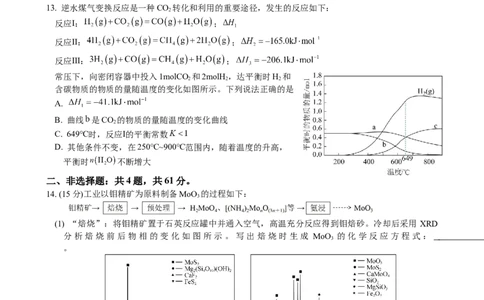
13. 逆水煤气变换反应是一种CO 转化和利用的重要途径,发生的反应如下:
2
反应Ⅰ: ;
反应Ⅱ: ;
反应Ⅲ: ;
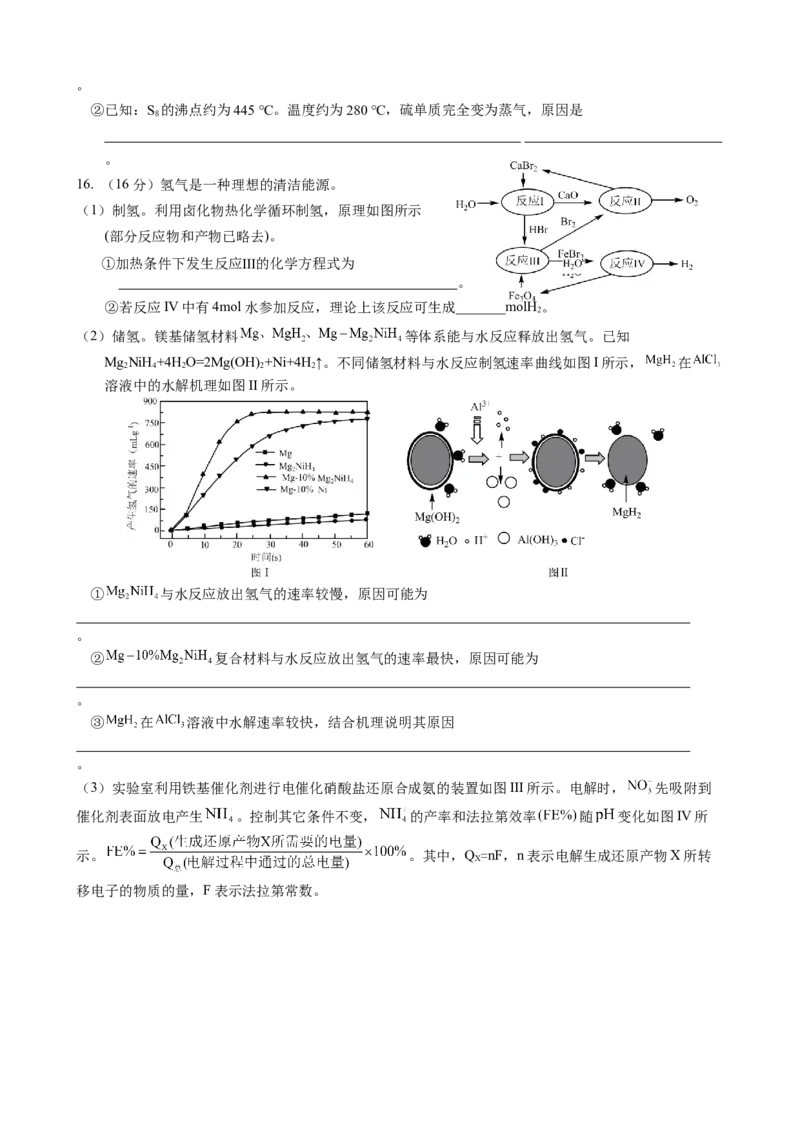
常压下,向密闭容器中投入1molCO 和2molH ,达平衡时H 和
2 2 2
含碳物质的物质的量随温度的变化如图所示。下列说法正确的是
A.
B. 曲线 是CO 的物质的量随温度的变化曲线
2
C. 649℃时,反应Ⅰ的平衡常数
D. 其他条件不变,在250℃~900℃范围内,随着温度的升高,
平衡时 不断增大
二、非选择题:共4题,共61分。
14. (15分)工业以钼精矿为原料制备MoO 的过程如下:
3
(1) “焙烧”:将钼精矿置于石英反应罐中并通入空气,高温充分反应得到钼焙砂。冷却后采用 XRD
分析焙烧前后物相的变化如图所示。写出焙烧时生成 MoO 的化学反应方程式:
3
。
(2) “预处理”:将钼焙砂和HNO、NH NO 混合溶液按一定比例混合,加热反应一段时间,过滤后,
3 4 3
得到含HMoO 、多钼酸铵[(NH )MoO ]、SiO 等滤渣。[已知(NH )MoO 在水中存在平衡:
2 4 4 2 n (3n+1) 2 4 2 n (3n+1)
(NH
4
)
2
Mo
n
O
(3n+1)
(s)⇌2NH(aq)+MoO(aq)+(n-1)MoO
3
(s)]
① “ 预 处 理 ” 需 在 通 风 设 备 中 进 行 , 原 因 是
。
② 写 出 CaMoO 转 化 为 (NH )MoO 的 化 学 方 程 式 :
4 4 2 n (3n + 1)。
③ 其他条件一定,适当增大NH NO 浓度,所得滤渣中Mo的含量增大,原因是
4 3
。
(3) “氨浸”:将预处理后所得滤渣用氨水浸泡,其中的HMoO 、(NH )MoO 可转化为可溶的
2 4 4 2 n (3n+1)
(NH )MoO ,还有少量的CaMoO 难溶于氨水。为进一步提高Mo元素的浸出率,可在氨水中加入的
4 2 4 4
物质是 。
(4) 五钼酸铵[(NH )MoO ,M=824 g·mol-1]在氮气中焙烧,可逐步分解,最终得到MoO 。取1.648 g
4 4 5 17 3
五钼酸铵固体在氮气氛围中焙烧,有气体NH 和HO生成,维持300 ℃时加热当固体质量不再变化
3 2
时,所得固体[组成为(NH )MoO,Mo为+6价]质量为1.57g。计算300 ℃所得固体的化学式,并
4 a b c
写出计算过程。
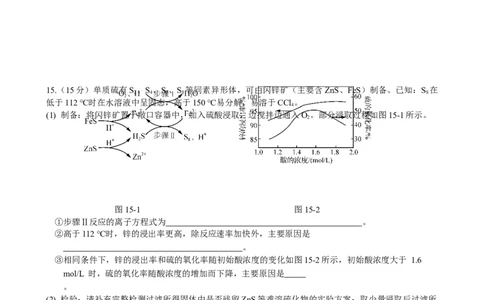
15.(15分)单质硫有S 、S 、S 、S 等同素异形体,可由闪锌矿(主要含ZnS、FeS)制备。已知:S 在
2 4 6 8 8
低于112 ℃时在水溶液中呈固态,高于150 ℃易分解,易溶于CCl 。
4
(1) 制备:将闪锌矿置于敞口容器中,加入硫酸浸取,边搅拌边通入O。部分浸取过程如图15-1所示。
2
图15-1 图15-2
①步骤Ⅱ反应的离子方程式为 。
②高于112 ℃时,锌的浸出率更高,除反应速率加快外,主要原因是
。
③相同条件下,锌的浸出率和硫的氧化率随初始酸浓度的变化如图15-2所示,初始酸浓度大于 1.6
mol/L 时,硫的氧化率随酸浓度的增加而下降,主要原因是
。
(2) 检验:请补充完整检测过滤所得固体中是否残留ZnS等难溶硫化物的实验方案:取少量浸取后过滤所
得固体,加适量CCl 充分溶解,过滤,加热所得固体至CCl 完全挥发,
4 4
(实验须选用的试剂:饱和溴水,蒸馏水,BaCl 溶液。已知:饱和溴水可将硫化物氧化为硫酸盐)
2
(3) 蒸硫:将浸取后冷却所得粗硫置于图15-3所示装置中加热得到硫蒸气,再冷凝得到硫单质。
图15-3
①蒸硫前,需通入一段时间N,目的是
2。
②已知:S 的沸点约为445 ℃。温度约为280 ℃,硫单质完全变为蒸气,原因是
8
。
16. (16分)氢气是一种理想的清洁能源。
(1)制氢。利用卤化物热化学循环制氢,原理如图所示
(部分反应物和产物已略去)。
①加热条件下发生反应Ⅲ的化学方程式为
。
②若反应IV中有4mol水参加反应,理论上该反应可生成_______molH。
2
(2)储氢。镁基储氢材料 等体系能与水反应释放出氢气。已知
MgNiH+4H O=2Mg(OH)+Ni+4H ↑。不同储氢材料与水反应制氢速率曲线如图I所示, 在
2 4 2 2 2
溶液中的水解机理如图II所示。
① 与水反应放出氢气的速率较慢,原因可能为
。
② 复合材料与水反应放出氢气的速率最快,原因可能为
。
③ 在 溶液中水解速率较快,结合机理说明其原因
。
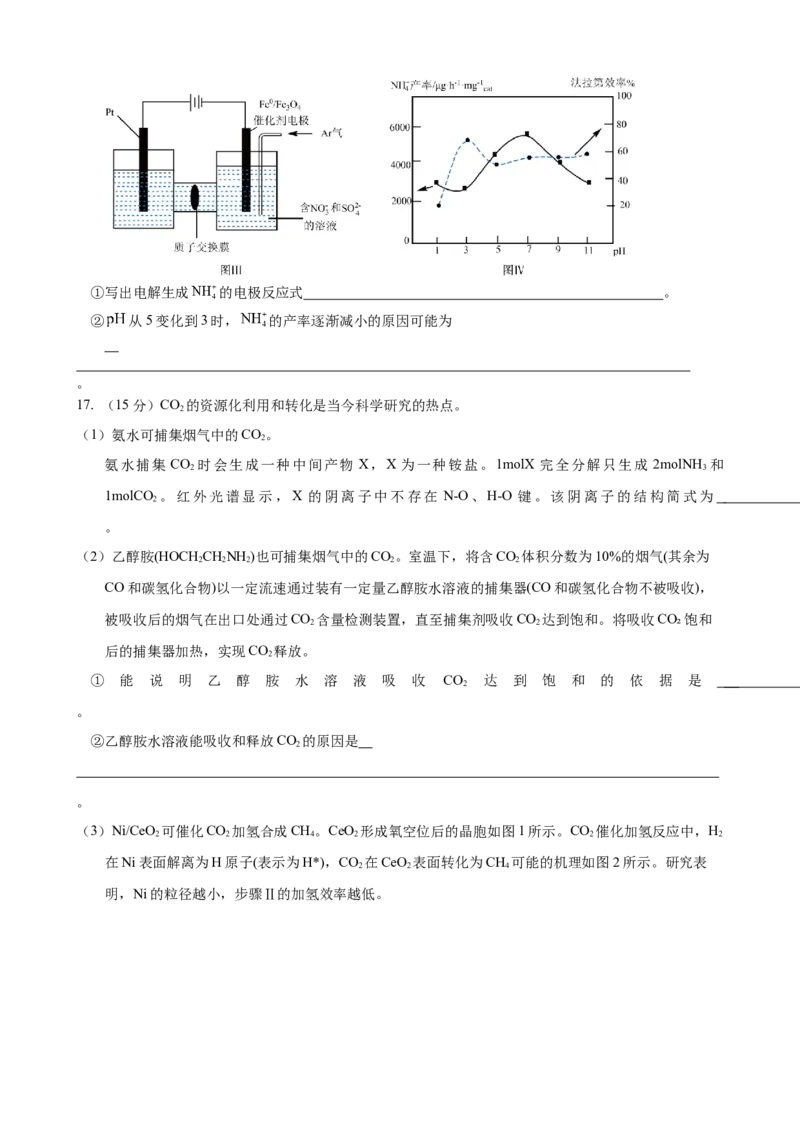
(3)实验室利用铁基催化剂进行电催化硝酸盐还原合成氨的装置如图III所示。电解时, 先吸附到
催化剂表面放电产生 。控制其它条件不变, 的产率和法拉第效率 随 变化如图IV所
示。 。其中,Q =nF,n表示电解生成还原产物X所转
X
移电子的物质的量,F表示法拉第常数。①写出电解生成 的电极反应式 。
② 从5变化到3时, 的产率逐渐减小的原因可能为
。
17. (15分)CO 的资源化利用和转化是当今科学研究的热点。
2
(1)氨水可捕集烟气中的CO。
2
氨水捕集 CO 时会生成一种中间产物 X,X 为一种铵盐。1molX 完全分解只生成 2molNH 和
2 3
1molCO 。红外光谱显示,X 的阴离子中不存在 N-O、H-O 键。该阴离子的结构简式为
2
。
(2)乙醇胺(HOCHCHNH )也可捕集烟气中的CO。室温下,将含CO 体积分数为10%的烟气(其余为
2 2 2 2 2
CO和碳氢化合物)以一定流速通过装有一定量乙醇胺水溶液的捕集器(CO和碳氢化合物不被吸收),
被吸收后的烟气在出口处通过CO 含量检测装置,直至捕集剂吸收CO 达到饱和。将吸收CO₂饱和
2 2
后的捕集器加热,实现CO 释放。
2
① 能 说 明 乙 醇 胺 水 溶 液 吸 收 CO 达 到 饱 和 的 依 据 是
2
。
②乙醇胺水溶液能吸收和释放CO 的原因是
2
。
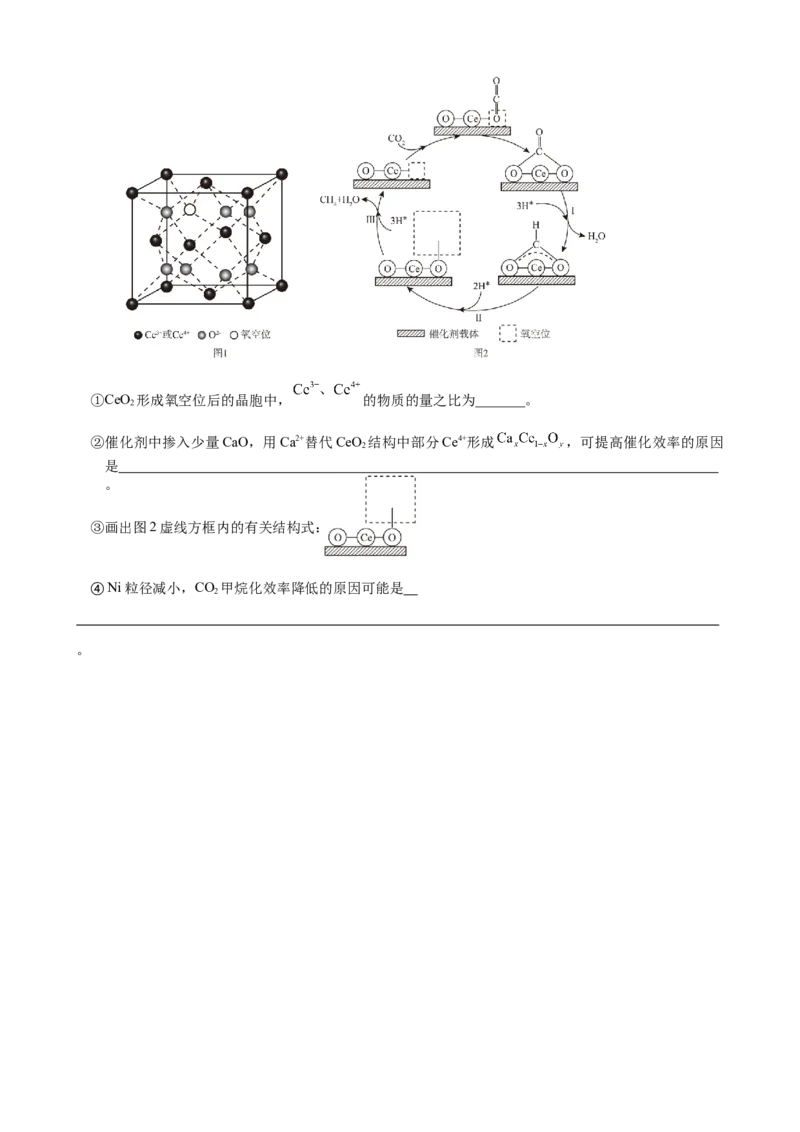
(3)Ni/CeO 可催化CO 加氢合成CH。CeO 形成氧空位后的晶胞如图1所示。CO 催化加氢反应中,H
2 2 4 2 2 2
在Ni表面解离为H原子(表示为H*),CO 在CeO 表面转化为CH 可能的机理如图2所示。研究表
2 2 4
明,Ni的粒径越小,步骤Ⅱ的加氢效率越低。①CeO 形成氧空位后的晶胞中, 的物质的量之比为_______。
2
②催化剂中掺入少量CaO,用Ca2+替代CeO 结构中部分Ce4+形成 ,可提高催化效率的原因
2
是
。
③画出图2虚线方框内的有关结构式:
④Ni粒径减小,CO 甲烷化效率降低的原因可能是
2
。