文档内容
专题 08 元素周期表与元素周期律
内容概览
考点01 元素周期表及其应用
考点02 元素周期律及其应用
考点03 有关元素周期表和周期律的综合考查
考点01 元素周期表及其应用
1.(23-24高一上·河南省开封市联考·期末)元素周期表中某区域的一些元素多用于制造半导体材料,它
们是
A.左下方区域的金属元素
B.右上方区域的非金属元素
C.金属元素和非金属元素分界线附近的元素
D.稀有气体元素
【答案】C
【解析】A.元素周期表中有金属元素和非金属元素,其中金属元素位于元素周期表的左边,可以用来做
导体材料,A项错误;
B.非金属元素一般位于元素周期表的右边,氢元素除外,非金属元素一般不导电,是绝缘体材料,B项
错误;
C.在金属与非金属元素交界处的元素大多数可用于制作半导体材料,C项正确;
D.稀有气体元素属于非金属元素,它们的性质更稳定,一般不用来做半导体材料,D项错误;
答案选:C。
2.(23-24高一上·新疆乌鲁木齐市六校联考·期末)铼可用于制造航空发动机的核心部件。铼元素在周期
表中的信息如图所示。下列有关该元素说法错误的是
A.属于金属元素 B.元素符号为Re
C.质子数为75 D.相对原子质量为186.2g
【答案】D
【解析】A.Re属于金属元素,故A正确;
B.Re为元素符号,故B正确;
C.75为元素的质子数,故C正确;
学科网(北京)股份有限公司D.Re的相对原子质量为186.2,故D错误;
故选D。
3.(23-24高一上·天津市重点校·期末)根据元素周期律和周期表,下列推断不合理的是
A.第83号元素的最高化合价是+5价
B.在周期表中金属与非金属的分界处可以找到半导体材料
C.某元素原子最外电子层上只有两个电子,该元素一定是第Ⅱ 族元素
D.元素周期表中第3列的元素种类数最多
【答案】C
【解析】A.第83号元素为铋元素,其位于元素周期表第六周期第ⅤA族,最高化合价是+5价,A合理;
B.在周期表中金属与非金属的分界处可以找到半导体材料,如:Si,B合理;
C.某元素原子最外电子层上只有两个电子,该元素可能是第ⅡA族元素,也可能是0族元素(氦)或过渡金
属,C不合理;
D.元素周期表中第3列的元素,包括镧系元素和锕系元素,元素的种类数最多,D合理;
故选C。
4.(23-24高一上·广东省广州市·期末)元素周期表的建立是化学发展史上的重要里程碑之一,下表列出
了A~G7种元素在周期表中的位置:
请回答下列问题:
(1)画出A的原子结构示意图 ,写出化合物 的电子式 。
(2)到目前为止,元素周期表的第七周期已经被填满,如果发现第119号元素,则它的性质与表中
(填字母,从A~G中选择)元素的性质最相似。
(3)写出D的单质与B的氢氧化物的水溶液反应的化学方程式 ,若反应中产生6.72L气体(标
准状况),则消耗D的质量为 g。
(4)F、G元素氢化物的稳定性由大到小的顺序是 (写化学式),它们含有的化学键为
(填“非极性键”或“极性键”)。
(5)比较B、C的金属性大小: (填元素符号),请设计实验进行证明。
实验方案 预期现象
学科网(北京)股份有限公司【答案】(1)
(2)B
(3) 5.4
(4) 极性键
(5)Na>Mg 对比金属钠和镁分别与水(等体积、等浓度稀 盐酸)反应置换氢气的难易程度 金属
钠与水的反应比镁的剧烈
【分析】根据元素周期表可知,A为Li,B为Na,C为Mg,D为Al,E为O,F为Cl,G为Br,据此回
答。
【解析】(1)
①由分析可知,A为Li,原子结构示意图为: ,故答案为: ;
②化合物AE为LiO,其电子式为: ,故答案为: ;
2 2
(2)元素周期表的第七周期已经被填满,如果发现第119号元素,则它的性质与表中Na的化学性质相
似,故答案为:B;
(3)①D的单质为Al, B的氢氧化物的水溶液为NaOH溶液,反应的化学方程式为:
,故答案为:
;
②若反应中产生6.72L气体(标准状况),即生成0.3molH,根据关系式:2Al~3H,则消耗Al的质量为
2 2
0.3mol× ×27g/mol=5.4g,故答案为:5.4g;
(4)①氢化物的稳定性主要取决于非金属性,同主族元素从上到下,非金属性逐渐减弱,则F、G的非金
属性:Cl>Br,氢化物的稳定性由大到小的顺序:HCl>HBr,故答案为:HCl>HBr;
②HCl、HBr是由不同种元素形成的共价键,则含有的化学键为极性共价键,故答案为:极性;
(5)①同周期元素从左到右金属性逐渐减弱,则金属性:Na>Mg,故答案为:Na>Mg;
②设计实验证明金属性:Na>Mg,可对比金属钠和镁分别与水(等体积、等浓度稀 盐酸)反应置换氢气的难
易程度,若金属钠与水的反应比镁的剧烈,则证明金属性:Na>Mg,故答案为:对比金属钠和镁分别与水
(等体积、等浓度稀 盐酸)反应置换氢气的难易程度;
③实验现象为:金属钠与水的反应比镁的剧烈,故答案为:金属钠与水的反应比镁的剧烈。
考点02 元素周期律及其应用
5.(23-24高一上·北京市东城区·期末)下列元素中,原子半径最大的是
学科网(北京)股份有限公司A. B. C. D.
【答案】B
【解析】同周期主族元素从左向右原子半径减小,同主族从上到下原子半径增大,则原子半径为K>Na>
Si>N,原子半径最大的是K;
答案选B。
6.(23-24高一上·北京市朝阳区·期末)下列物质性质的比较中,不正确的是
A.酸性:HSO >HPO B.还原性: HCl>HBr
2 4 3 4
C.碱性:NaOH>Mg(OH) D.稳定性:HO>HS
2 2 2
【答案】B
【解析】A.同周期元素从左到右非金属性增强,最高价含氧酸的酸性增强,酸性:HSO >HPO ,故A
2 4 3 4
正确;
B.同主族元素从上到下,气态氢化物还原性增强,还原性: HClMg>Al,则碱性:Al(OH)
3
学科网(北京)股份有限公司<Mg(OH) <NaOH,能用元素周期律解释,B不符合题意;
2
C.I、Br、Cl属于同一主族元素,从上到下原子半径逐渐增大,得电子能力逐渐减弱,元素的非金属性逐
渐减弱,其形成的简单氢化物的稳定性逐渐减弱,即非金属性:I<Br<Cl,则简单氢化物的稳定性:HI<
HBr<HCl,能用元素周期律解释,C不符合题意;
D.因HSO 、HClO不是S、Cl元素的最高价氧化物对应的水化物,因此不能根据元素的非金属性来判断
2 3
物质的酸性:HSO >HCO>HClO,故不能用元素周期律来解释,D符合题意;
2 3 2 3
故选D。
9.(23-24高一上·吉林省部分名校·期末)下列关于元素金属性和非金属性强弱比较的说法错误的是
A.Fe投入 溶液中,能置换出Cu,说明Fe的金属性比Cu的强
B. 的酸性强于HF的酸性,说明Cl的非金属性强于F
C.Na与冷水反应剧烈,而Mg与冷水反应缓慢,说明Na的金属性强于Mg
D.Si与 化合所需温度远高于S与 化合所需温度,说明S的非金属性强于Si
【答案】B
【解析】A.较活泼的金属可将较不活泼的金属从它的盐溶液中置换出来,A正确;
B. HCl不是氯元素的最高价氧化物对应的水化物,虽然HCl的酸性比HF的强,但不能作为Cl、F非金
属性强弱的判断依据,B错误;
C.单质与水越易反应生成碱和氢气,其金属性越强,C正确;
D.单质与氢气越易化合,元素的非金属性越强,D正确;
答案选B。
10.(23-24高一上·福建省福州市·期末)元素周期表和元素周期律可以指导人们进行规律性的推测和判
断。下列说法错误的是
A.若 和 白的核外电子层结构相同,则原子序数:X>Y
B.硫、硒为同主族元素,因此硒的主要化合价有-2、+4、+6
C. 和 分别位于第六周期IA和IIA族,碱性:
D.常温下,形状和大小相同的 、 与浓度相同的盐酸反应, 更剧烈
【答案】C
【解析】A.X+和Y2-的核外电子层结构相同,则X的原子序数-1=Y的原子序数+2,故原子序数X>Y,故
A正确;
B.硫为第ⅥA族元素,最高价为+6价,最低价为-2价,还有可能为+4,,硒与硫为同主族元素,因此硒的
主要化合价有-2、+4、+6,故B正确;
C.同周期从左向右金属性减弱,同主族从上往下金属性逐渐增强,金属性越强,对应碱的碱性越强,Cs
和Ba分别位于第六周期IA和IIA族,Cs的金属性强于Ba,则碱性:CsOH>Ba(OH),故C错误;
2
D.镁的金属活动性强于铝,常温下,形状和大小相同的镁和铝与同浓度盐酸反应,镁条反应更剧烈,故
D正确;
答案选C。
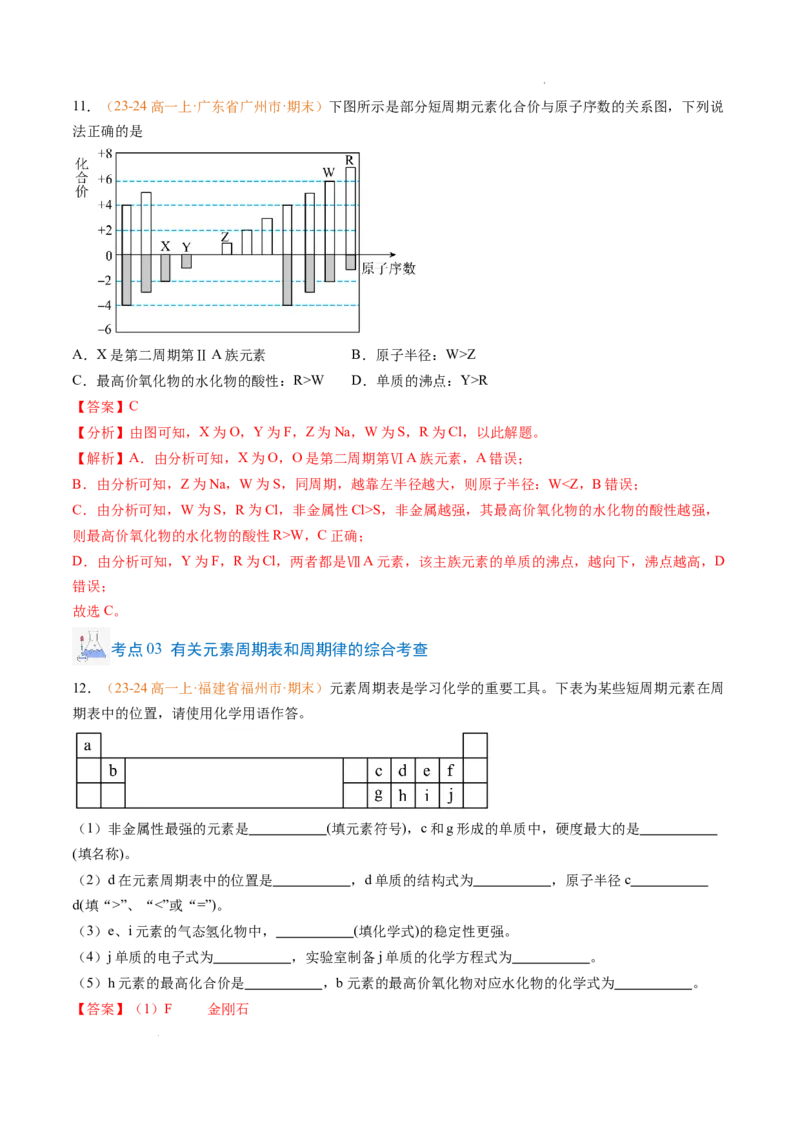
学科网(北京)股份有限公司11.(23-24高一上·广东省广州市·期末)下图所示是部分短周期元素化合价与原子序数的关系图,下列说
法正确的是
A.X是第二周期第ⅡA族元素 B.原子半径:W>Z
C.最高价氧化物的水化物的酸性:R>W D.单质的沸点:Y>R
【答案】C
【分析】由图可知,X为O,Y为F,Z为Na,W为S,R为Cl,以此解题。
【解析】A.由分析可知,X为O,O是第二周期第ⅥA族元素,A错误;
B.由分析可知,Z为Na,W为S,同周期,越靠左半径越大,则原子半径:WS,非金属越强,其最高价氧化物的水化物的酸性越强,
则最高价氧化物的水化物的酸性R>W,C正确;
D.由分析可知,Y为F,R为Cl,两者都是ⅦA元素,该主族元素的单质的沸点,越向下,沸点越高,D
错误;
故选C。
考点03 有关元素周期表和周期律的综合考查
12.(23-24高一上·福建省福州市·期末)元素周期表是学习化学的重要工具。下表为某些短周期元素在周
期表中的位置,请使用化学用语作答。
(1)非金属性最强的元素是 (填元素符号),c和g形成的单质中,硬度最大的是
(填名称)。
(2)d在元素周期表中的位置是 ,d单质的结构式为 ,原子半径c
d(填“>”、“<”或“=”)。
(3)e、i元素的气态氢化物中, (填化学式)的稳定性更强。
(4)j单质的电子式为 ,实验室制备j单质的化学方程式为 。
(5)h元素的最高化合价是 ,b元素的最高价氧化物对应水化物的化学式为 。
【答案】(1)F 金刚石
学科网(北京)股份有限公司(2)第二周期VA族 >
(3)
(4)
(5)+5
【分析】根据元素在周期表中的位置,a是H元素、b是Be元素、c是C元素、d是N元素、e是O元素、
f是F元素、g是Si元素、h是P元素、i是S元素、j是Cl元素。
【解析】(1)同周期元素从左到右非金属性增强,同主族元素从上到下非金属性减弱,非金属性最强的
元素是F;C和Si形成的单质金刚石、晶体硅是共价晶体,原子半径越小,共价键键能越大,硬度最大的
是金刚石。
(2)d是N元素,在周期表中的位置是第二周期VA族,d单质是N,存在氮氮三键,结构式为 ;
2
同周期元素从左到右原子半径依次减小,原子半径C>N。
(3)同主族元素从上到下非金属性减弱,气态氢化物稳定性减弱,e、i元素的气态氢化物中,HO的稳定
2
性更强。
(4)
j单质是Cl,电子式为 ,实验室用二氧化锰和浓盐酸在加热条件下反应制备Cl,反应的化学方
2 2
程式为 。
(5)h是P元素,最外层有5个电子,最高化合价是+5,b是Be元素,b元素的最高价氧化物对应水化物
的化学式为 。
13.(23-24高一上·河南省开封市联考·期末)某同学为探究元素周期表中元素性质的递变规律,设计了如
下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是 ;分别向新
制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是 氢氧化
物,其中 与氢氧化钠溶液反应的离子方程式为 。
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
①图中仪器a的名称是 ,圆底烧瓶中发生反应的离子方程式为 。
学科网(北京)股份有限公司②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ,该实验能证明非金属性强
弱,依据的原理是 。
【答案】(1)钠 两性
(2)分液漏斗 一段时间后烧杯中产生白色胶状沉淀 元素非金
属性越强,其最高价氧化物对应水化物的酸性越强
【分析】该实验的实验目的是探究同周期元素的金属性强弱,以及元素的非金属性强弱。
【解析】(1)同周期元素,从左到右金属性依次增强,与水反应的剧烈程度依次增强,则将大小相同的
钠、镁、铝(除去氧化膜)分别投入到冷水中,金属钠钠与冷水反应最剧烈;向氢氧化铝沉淀中滴加稀盐酸
和氢氧化钠溶液,沉淀都溶解说明氢氧化铝即能与强酸溶液反应生成盐和水,也能与强碱溶液反应生成盐
和水,则氢氧化铝我两性氢氧化物;氢氧化铝与氢氧化钠溶液反应生成四羟基合铝酸钠,反应的离子方程
式为 ,故答案为:Na;两性; ;
(2)①由实验装置图可知,仪器a为分液漏斗;圆底烧瓶中发生的反应为碳酸钠与稀硫酸反应生成硫酸
钠、二氧化碳和水,反应的离子方程式为 ,故答案为:
;
②圆底烧瓶中反应生成的二氧化碳与烧杯中二氧化碳反应生成硅酸沉淀和碳酸氢钠,则一段时间后烧杯中
产生白色胶状沉淀说明碳酸的酸性强于硅酸,碳元素的非金属性强于硅元素非金属性;元素的非金属性越
强,最高价氧化物对应水化物的酸性越强,则该实验能证明非金属性强弱依据的原理是元素非金属性越
强,其最高价氧化物对应水化物的酸性越强,故答案为:一段时间后烧杯中产生白色胶状沉淀;元素非金
属性越强,其最高价氧化物对应水化物的酸性越强。
14.(23-24高一上·湖北省A9高中联盟·期末)元素周期表是学习化学的重要工具,它隐含着许多信息和
规律。下表列出了七种短周期主族元素在元素周期表中的相对位置,回答下列问题:
A
B C D
E F G
(1)C 元素在周期表中的位置是 。
(2)元素E比元素F金属性强,下列表述中能证明这一事实的是 (填字母序号)。
a. E的最高价氧化物对应的水化物的碱性比F的强
b. E的化合价比F的低
c. 常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水缓慢反应
(3)比较沸点:HC HG (填“>”或“<”),原因是 。
2 2
(4)元素C与元素E以原子个数比1∶1形成一种淡黄色固体Y,Y中存在的化学键有 。
(5)C、D、E形成的简单离子半径由大到小的顺序是 。(用离子符号表示)。
(6)肼B A 常用作火箭燃料,分子中B、A两种原子的最外层均达到稳定结构,写出肼的电子式:
2 4
学科网(北京)股份有限公司。
【答案】(1)第二周期第ⅥA族
(2)ac
(3)> H O分子间存在氢键,而HS分子间不存在氢键
2 2
(4)离子键、共价键
(5)O2- > F- > Na+
(6)
【分析】根据元素周期表中元素的信息可知,A为H元素,B为N元素,C为O元素,D为F元素,E为
Na元素,F为Al元素,G为S元素;
【解析】(1)C 为O元素,氧元素的位置为第二周期第ⅥA族;
(2)根据最高价氧化物的水化物的碱性、金属与水反应的难易可以比较金属性的强弱,答案选ac;
(3)氢键比范德华力强,分子间存在氢键,物质沸点升高,故沸点HO>HS;
2 2
(4)元素C与元素E以原子个数比1∶1形成一种淡黄色固体Y,则Y为NaO,NaO 存在离子键、共价
2 2 2 2
键;
(5)离子的电子排布相同,核电荷数大的离子半径小,离子半径:O2- > F- > Na+;
(6)
NH 的电子式为 。
2 4
15.(23-24高一上·安徽省芜湖市·期末)下表是元素周期表的一部分,参照元素在表中的位置,回答下列
问题。
(1)写出元素②的一种同素异形体的名称: 。
(2)④、⑤、⑥三种元素中,原子半径最大的是 (填元素符号)。
(3)⑦和⑧的最高价含氧酸的酸性较强的是 (填最高价含氧酸的化学式)。
(4)写出②和⑧形成的最简单的化合物的结构式: ,化学键的类型是 。
(5)用电子式表示④、⑧形成化合物的过程: 。
(6)①、③两种元素按原子个数比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反
应的离子方程式: 。
【答案】(1)金刚石、石墨等(填一种即可)
学科网(北京)股份有限公司(2)Na
(3)HClO
4
(4) 极性共价键(或共价键)
(5)
(6)2Fe2++H O+2H+=2Fe3++2H O
2 2 2
【分析】由图中信息可以得出,①、②、③、④、⑤、⑥、⑦、⑧分别为H、C、O、Na、Mg、Al、S、
Cl。
【解析】(1)由分析可知,②为碳元素,它的一种同素异形体的名称:金刚石、石墨等(填一种即可)。
(2)④、⑤、⑥三种元素分别为Na、Mg、Al,三者为同一周期的相邻元素,同周期元素从左到右,原子
半径依次减小,所以原子半径最大的是Na。
(3)⑦和⑧分别为S、Cl,二者的非金属性S<Cl,非金属性越强,其最高价氧化物的水化物的酸性越
强,所以最高价含氧酸的酸性较强的是HClO。
4
(4)②和⑧形成的最简单的化合物为CCl ,结构式: ,化学键的类型是极性共价键(或共价
4
键)。
(5)④、⑧形成化合物为NaCl,用电子式表示④、⑧形成化合物的过程:
。
(6)①、③两种元素按原子个数比为1:1组成的常见液态化合物为HO,在酸性溶液中能将Fe2+氧化为
2 2
Fe3+,该反应的离子方程式:2Fe2++H O+2H+=2Fe3++2H O。
2 2 2
【点睛】对于电子层结构相同的离子来说,随着原子序数的递增,离子半径依次减小。
16.(23-24高一上·河南省开封市联考·期末)下图是短周期元素 在元素周期表中的位置。
(1) 在周期表中的位置是第 周期第 族。
(2)b、c、e三种元素原子半径由大到小的顺序是 (填元素符号)。
(3)非金属性:e f(填“ ”或“ ”),从原子结构角度解释其原因是 。
(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈 色;用电子式
表示a、f形成化合物的过程 。
【答案】(1)三 VIA
学科网(北京)股份有限公司(2)
(3)> 随着核电荷数增加,同主族元素从上到下电子层数依次增多,原子半径逐渐增大,原子核对
最外层电子的吸引力减弱,得电子能力逐渐减弱。所以非金属性逐渐减弱
(4)黄
【分析】根据元素周期表的位置可知,a为H、b为Na、c为Mg、d为S、e为F、f为Cl,据此分析解题。
【解析】(1) 为S,为第16号元素,在周期表中的位置是第三周期第VIA族。
(2)同周期原子半径从左到右逐渐减小,同主族原子半径从上到下逐渐增大,b、c、e三种元素原子半径
由大到小的顺序是 。
(3)非金属性:e>f,从原子结构角度解释其原因是:随着核电荷数增加,同主族元素从上到下电子层数
依次增多,原子半径逐渐增大,原子核对最外层电子的吸引力减弱,得电子能力逐渐减弱。所以非金属性
逐渐减弱。
(4)
b、f两种元素形成的化合物(NaCl)有重要的用途,高温灼烧该化合物时,火焰呈黄色,因为钠的焰色反应
显黄色;用电子式表示a、f形成化合物(HCl)的过程: 。
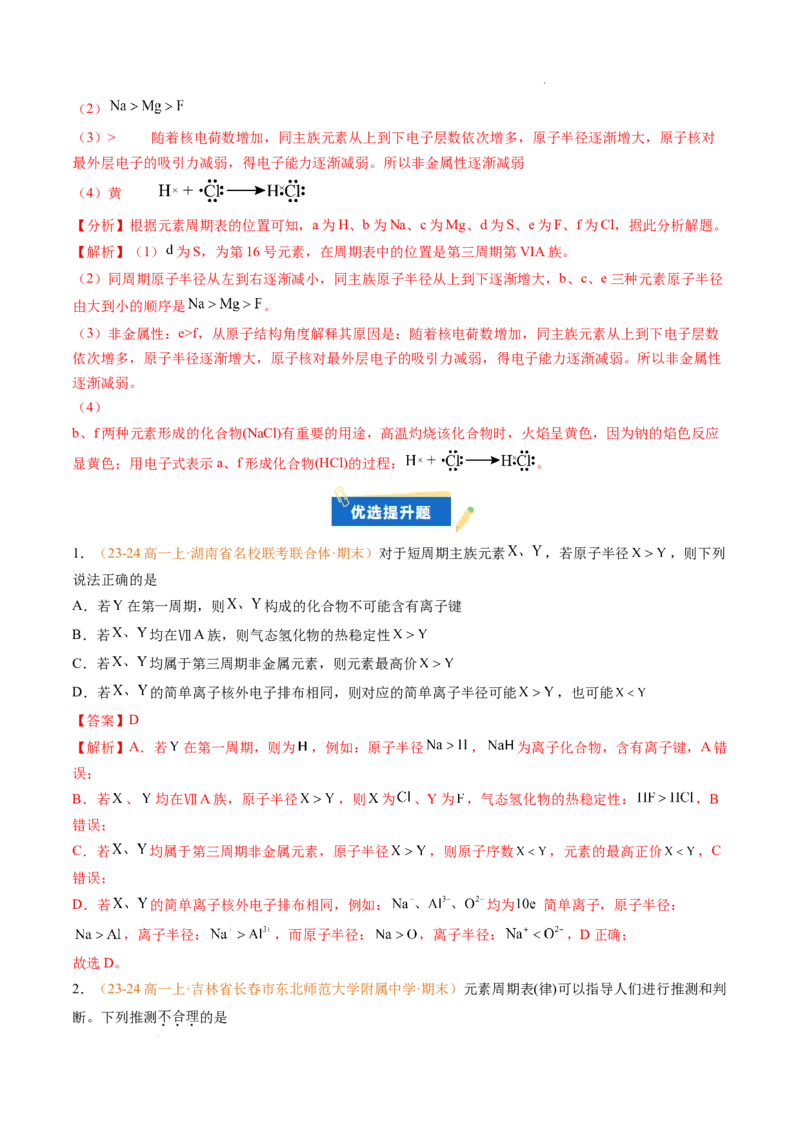
1.(23-24高一上·湖南省名校联考联合体·期末)对于短周期主族元素 ,若原子半径 ,则下列
说法正确的是
A.若 在第一周期,则 构成的化合物不可能含有离子键
B.若 均在ⅦA族,则气态氢化物的热稳定性
C.若 均属于第三周期非金属元素,则元素最高价
D.若 的简单离子核外电子排布相同,则对应的简单离子半径可能 ,也可能
【答案】D
【解析】A.若 在第一周期,则为 ,例如:原子半径 , 为离子化合物,含有离子键,A错
误;
B.若 、 均在ⅦA族,原子半径 ,则 为 、Y为 ,气态氢化物的热稳定性: ,B
错误;
C.若 均属于第三周期非金属元素,原子半径 ,则原子序数 ,元素的最高正价 ,C
错误;
D.若 的简单离子核外电子排布相同,例如: 均为 简单离子,原子半径:
,离子半径: ,而原子半径: ,离子半径: ,D正确;
故选D。
2.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)元素周期表(律)可以指导人们进行推测和判
断。下列推测不合理的是
学科网(北京)股份有限公司A.若X+和Y2−的核外电子层结构相同,则原子序数:X>Y
B.由水溶液的酸性:HCl>HS,可推断元素的非金属性:Cl>S
2
C.Cs和Ba分别位于第六周期第IA和IIA族,则碱性:CsOH>Ba(OH)
2
D.IIA族元素依次为Be、Mg、Ca、Sr、Ba;MgSO4易溶于水,CaSO 微溶于水,则SrSO 可能难溶于水
4 4
【答案】B
【解析】A.若X+和Y2−的核外电子层结构相同,根据“阴上阳下”即阴离子再上一周期右边,阳离子在
下一周期左边,则原子序数:X>Y,推断合理,故A不符合题意;
B.推断元素的非金属性:Cl>S,是根据最高价氧化物对应水化物的强弱推断,不能根据水溶液的酸性:
HCl>HS来判断,故B符合题意;
2
C.根据同周期从左到右金属性减弱,则最高价氧化物对应水化物碱性减弱,Cs和Ba分别位于第六周期第
IA和IIA族,则碱性:CsOH>Ba(OH) ,推断合理,故C不符合题意;
2
D.IIA族元素依次为Be、Mg、Ca、Sr、Ba;MgSO 易溶于水,CaSO 微溶于水,根据递变性,则SrSO
4 4 4
可能难溶于水,推断合理,故D不符合题意。
综上所述,答案为B。
3.(23-24高一上·广东省茂名市·期末)主族元素W、X、Y和Z在周期表中的相对位置如图所示,其中
元素X为Si,下列说法错误的是
W
X Y
Z
A.X的最高价氧化物与水反应生成强酸
B.W、Y两种元素的最简单氢化物之间能反应
C.可用单质Y、氢气、水为原料制取盐酸
D.Z原子的核外最外层电子数为6
【答案】A
【分析】X为Si元素,W为N,Y为Cl元素,Z为Se元素,据此解答。
【解析】A.X的最高价氧化物为SiO,不与水反应,A项错误;
2
B.W的最简单氢化物为NH ,Y的最简单氢化物为HCl,两者反应生成NH Cl,B项正确;
3 4
C.单质Y为Cl,工业上常采用氢气和氯气燃烧制取HCl,HCl溶于水得到盐酸,C项正确;
2
D.Z为Se元素,处于ⅥA族,核外最外层电子数为6,D项正确;
故选:A。
4.(23-24高一上·广东省东莞市·期末)一种医药分子结构如下图所示。已知X、Y、Z、W、E的原子序
数依次增大,X是原子半径最小的元素,Y的最高正价与最低负价绝对值相等,Z的L层电子数是K层的
3倍,W、E的半径同周期最小(不考虑稀有气体原子)。下列说法正确的是
学科网(北京)股份有限公司A.原子半径:Y<Z B. 含有非极性键
C.非金属性:W>Z D.该分子中所有原子的最外层都满足8电子结构
【答案】C
【分析】根据题意,X是 H元素,Y是 C元素,Z是O元素,由于原子序数依次增大,且W、E是同周
期内半径最小,分别为F和Cl,据此分析选项;
【解析】A.根据分析,Y、Z分别为C、O元素,属于第二周期,同一周期内,原子半径从左到右逐渐减
小,则Y>Z,A错误;
B.根据分析,X、Z分别为H、O元素,XZ为水分子,不含非极性键,B错误;
2
C.根据分析,W、Z分别为F、O元素,同一周期内,非金属性从左到右逐渐增强,即W>Z,C正确;
D.题目所给分子结构图中,X为H原子,H原子最外层只能容纳2电子,D错误;
答案选C。
5.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)短周期主族元素W、X、Y、Z的原子序数
依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和
相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所
示。下列叙述正确的是
A.元素非金属性强弱的顺序为
B.离子半径关系
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.化合物M中W不都满足8电子稳定结构
【答案】B
【分析】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大
的,则X为Na;由W、X、Y三种元素形成的化合物M的结构可知,Y形成四个共价键,说明Y为Si;Y
的原子序数是Z的最外层电子数的2倍,即Z的最外层电子数为7,则Z为Cl;W的核外电子数与X、Z
的最外层电子数之和相等,即W的核外电子数为8,则W为O,且X为Na、Y为Si、Z为Cl,据此解
答。
【解析】A.W为O、Y为Si、Z为Cl,同周期元素,从左到右非金属性依次增强,则氯元素的非金属性
强于硅元素,则非金属性:W>Z>Y,A错误;
B.W为O,X为Na、Z为Cl,其简单离子分别为O2-、Na+、Cl-,则离子半径关系:r(Z)>r(W)>r(X),B正
确;
学科网(北京)股份有限公司C.W为O、Y为Si,非金属性:W>Y,则W的简单氢化物稳定性比Y的简单氢化物稳定性高,C错误;
D.W为O,化合物M中O都满足8电子稳定结构,D错误;
故选B。
6.(23-24高一上·北京市东城区·期末)元素周期表与元素周期律在学习、研究和生产实践中有很重要的
作用。下表列出了5种元素在周期表中的位置,其中①~④代表4种元素。
ⅠA ⅡA ⅢA ⅣA ⅤA ⅦA 0
3 ① ② ③
4 ④
(1)③的元素符号是 。
(2)下列能说明①比②失电子能力强的事实是 (填字母)。
a.单质①的密度比单质②的密度小
b.单质①比单质②更容易与水反应置换出氢气
c.最高价氧化物对应的水化物的碱性:①强于②
(3)依据元素周期律推测:
Ⅰ. 属于 (填“金属”或“非金属”)元素。
Ⅱ. 的最高价氧化物对应的水化物的化学式是 。
Ⅲ.气态氢化物的热稳定性: (填“强于”或“弱于”) 。
(4)某元素的原子结构示意图为 。下列关于该元素的说法正确的是 (填字
母)。
a.位于周期表中第五周期第ⅡA族 b.属于非金属元素
c.单质能与水反应 d.其碳酸盐难溶于水
【答案】(1)
(2)bc
(3)非金属 弱于
(4)acd
【分析】依据元素在周期表中的相对位置可知①是Na、②是Mg、③是Al、④是Se,据此解答。
【解析】(1)元素③位于第三周期第 族,为 元素。
答案为: 。
(2)a.金属元素的单质得失电子的能力与单质的密度无关,则单质钠的密度比单质镁的密度小不能说明
钠比镁失电子能力强,a错误;
学科网(北京)股份有限公司b.同周期元素,从左到右元素的金属性依次减弱,与水反应的剧烈程度减弱,则单质钠比单质镁更容易
与水反应置换出氢能说明钠比镁失电子能力强,b正确;
c.同周期元素,从左到右元素的金属性依次减弱,最高价氧化物对应的水化物的碱性依次减弱,则氢氧
化钠的碱性强于氢氧化镁能说明钠比镁失电子能力强,c正确。
答案为:bc。
(3) 的原子序数为34,是位于第四周期第 族的非金属元素。
答案为:非金属。
根据 元素在元素周期表中的位置可知其最高化合价为+6,其最高价氧化物对应水化物的化学式为
。
答案为: 。
同主元素随着原子序数的增大,元素的非金属性逐渐减弱, 、 为同主族元素,非金属性:
。同周期元素随着原子序数的增大,元素的非金属性逐渐减弱, 、 同周期且后者原子序数大,非金属
性: ,因此 的非金属性强于 ,表现为气态氢化物的热稳定性: 。
答案为:弱于。
(4)a.该元素原子核外电子层数为5,则其所在周期数为5;最外层电子数为2,则其族序数为2,因此
该元素位于第五周期第 族,a正确;
b.该元素符号为 ,元素名称为锶,为金属元素,b错误;
c. 与 位于同一主族,化学性质相似。 单质能与水反应,则 单质也能与水反应,c正确;
d. 、 、 位于同一主族, 、 难溶于水,则 也难溶于水,d正确。
答案为:acd。
7.(23-24高一上·广东省东莞市·期末)元素周期律和元素周期表,反映了元素性质与原子结构的关系,
在自然科学、生产实践等各方面都有重要意义。下图为部分短周期元素化合价与原子序数的关系图。
(1)b在元素周期表中的位置为 。
(2)f在半导体领域中有着重要应用,其原子结构示意图为 。
(3)h、g的气态氢化物稳定性由强到弱的顺序为 (填化学式)。
(4)c、d、e简单离子的半径从大到小为 (用化学式表示)。
(5)c与d形成的淡黄色化合物的电子式为 。
(6)X射线衍射法可以测定某些分子的结构,下列分子的结构模型正确是_______(填字母)。
学科网(北京)股份有限公司选项 A B C D
分子
平面正方形
直线形 直线形
直线形
结构
模型
(7)a、h的最高价氧化物的水化物酸性由强到弱的顺序为 (填化学式)。
(8)写出一条仅含a、b、c元素的氧化还原反应方程式 。
【答案】(1)第二周期第VA族
(2)
(3)
(4)
(5)
(6)AC
(7)
(8)
【分析】根据图像横纵坐标可推知,图像中元素从左到右分别为碳、氮、氧、氟、钠、镁、铝、硅、磷、
硫、氯,据此回答问题。
【解析】(1)根据推断,b为氮,在元素周期表第二周期第VA族,故答案为第二周期第VA族。
(2)
根据推断,f为硅,其原子结构示意图为 ,故答案为 。
(3)根据推断h、g分别是氯和硫,气态氢化物稳定性与非金属性成正比,非金属性氯大于硫,故气态氢
化物稳定性由强到弱的顺序为 ,故答案为 。
(4)这三个简单离子的核外电子排布相同,此时该比较核电荷数,核电荷数越大,对核外电子的吸引能
力越强,半径越小,故c、d、e简单离子的半径从大到小为 ,故答案为
。
学科网(北京)股份有限公司(5)c与d形成的淡黄色化合物为过氧化钠,电子式为 ,故答案为
。
(6)A.氯化氢为直线形分子,故A正确;
B.水分子为V形,故B错误;
C.二氧化碳为直线形分子,故C正确;
D.甲烷为正四面体,故D错误;
故选AC。
(7)最高价氧化物的水化物酸性与非金属性成正比,氯的非金属性比碳强,故酸性 ,故
答案为 。
(8)仅含碳氮氧三种元素的氧化还原方程式可以为 ,故答案为
。
8.(23-24高一上·广东省茂名市·期末)元素周期律和周期表是我们研究、预测物质性质的重要工具。下
表是元素周期表中前四周期的5种元素的相关信息。
元
元素性质或原子结构
素
A
B B能形成多种单质,其中一种单质是硬度最大的物质
C 地壳中含量最高的金属元素,其合金可用于制造飞机外壳
D D的单质是一种黄绿色气体
E 用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃片)
回答下列问题:
(1)D在元素周期表中的位置是第 周期第 族。
(2) (元素B的氢化物)的分子结构模型为正四面体, (元素B的气态氢化物)的稳定性
HD(元素D的气态氢化物)的稳定性(填写“大于”“小于”或“等于”)。
(3)少量E的单质加入水中剧烈反应,反应的化学方程式是 ;元素A、E的最高价氧化物对
应的水化物中,碱性更强的物质是 (填写化学式)。
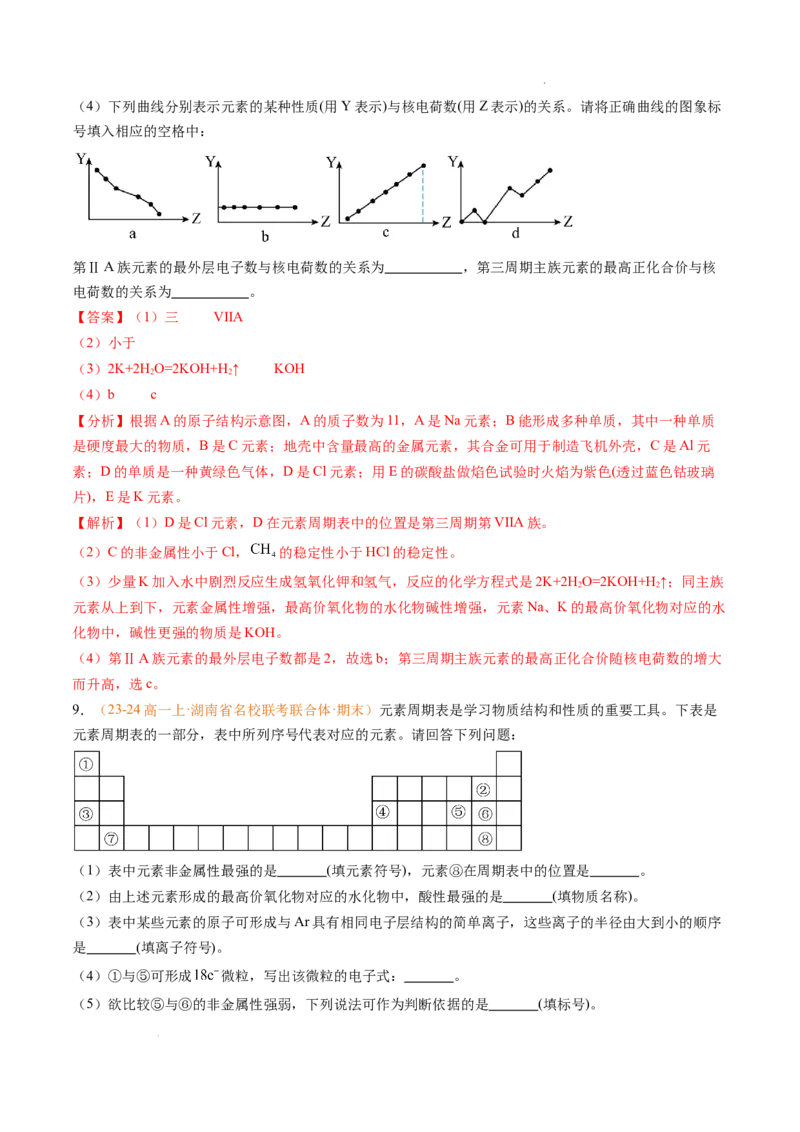
学科网(北京)股份有限公司(4)下列曲线分别表示元素的某种性质(用Y表示)与核电荷数(用Z表示)的关系。请将正确曲线的图象标
号填入相应的空格中:
第ⅡA族元素的最外层电子数与核电荷数的关系为 ,第三周期主族元素的最高正化合价与核
电荷数的关系为 。
【答案】(1)三 VIIA
(2)小于
(3)2K+2HO=2KOH+H ↑ KOH
2 2
(4)b c
【分析】根据A的原子结构示意图,A的质子数为11,A是Na元素;B能形成多种单质,其中一种单质
是硬度最大的物质,B是C元素;地壳中含量最高的金属元素,其合金可用于制造飞机外壳,C是Al元
素;D的单质是一种黄绿色气体,D是Cl元素;用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃
片),E是K元素。
【解析】(1)D是Cl元素,D在元素周期表中的位置是第三周期第VIIA族。
(2)C的非金属性小于Cl, 的稳定性小于HCl的稳定性。
(3)少量K加入水中剧烈反应生成氢氧化钾和氢气,反应的化学方程式是2K+2HO=2KOH+H ↑;同主族
2 2
元素从上到下,元素金属性增强,最高价氧化物的水化物碱性增强,元素Na、K的最高价氧化物对应的水
化物中,碱性更强的物质是KOH。
(4)第ⅡA族元素的最外层电子数都是2,故选b;第三周期主族元素的最高正化合价随核电荷数的增大
而升高,选c。
9.(23-24高一上·湖南省名校联考联合体·期末)元素周期表是学习物质结构和性质的重要工具。下表是
元素周期表的一部分,表中所列序号代表对应的元素。请回答下列问题:
(1)表中元素非金属性最强的是 (填元素符号),元素⑧在周期表中的位置是 。
(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是 (填物质名称)。
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序
是 (填离子符号)。
(4)①与⑤可形成 微粒,写出该微粒的电子式: 。
(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是 (填标号)。
学科网(北京)股份有限公司a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与 化合的难易程度
c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③ ④(填“>”或“<”),元素④的单质可与元素③的最高价氧化物的水
化物反应,写出该反应的化学方程式: 。
【答案】(1) 第四周期第ⅦA族
(2)高氯酸
(3)
(4)
(5)bc
(6)>
【分析】由元素在周期表中的位置可知①为H,②为F,③为Na,④为Al,⑤为S,⑥为Cl,⑦为Ca,⑧
为Br,据此解答。
【解析】(1)同一周期从左到右非金属性增大,同一主族从上到下非金属性减小,故表中元素非金属性
最强的是F,元素⑧为Br,在周期表中的位置是第四周期第VIIA族;
(2)元素非金属性越强,最高价氧化物的水化物酸性越强,F没有最高价氧化物水化物,剩余元素非金属
性最强的是氯,故上述元素形成的最高价氧化物对应的水化物中,酸性最强的是高氯酸;
(3)可形成与Ar具有相同电子层结构的简单离子的原子为Ar同周期的非金属元素和下一周期的金属元
素,有S2-、Cl-、Ca2+,这些离子核外电子排布相同,核电荷数越大,离子半径越小,故这些离子的半径由
大到小的顺序是S2−>Cl−>Ca2+;
(4)氢元素与硫元素形成的18电子微粒为HS,电子式为 ;
2
(5)a.⑤、⑥两种元素单质的沸点高低与单质形态、分子间作用力等因素有关,与非金属性强弱无关,a
不选;
b.非金属元素单质越易与H 化合,非金属性越强,故可以通过比较⑤、⑥两种元素单质与H 化合的难易
2 2
程度比较非金属性强弱,b选;
c.非金属元素气态氢化物越稳定,非金属性越强,故可以通过比较⑤、⑥两种元素气态氢化物的稳定性
比较非金属性强弱,c选;
d.非金属元素非金属性越强,最高价氧化物水化物酸性越强,选项没有说明是最高价氧化物的水化物,
故d不选;
故选bc;
(6)同一周期,从左到右,元素金属性减弱,故金属性:③>④,铝是两性金属,可以与钠最高价氧化物
的水化物氢氧化钠反应,生成偏铝酸钠(四羟基合铝酸钠)和氢气,反应的化学方程式为
2Al+2NaOH+6H O=2Na[Al(OH) ]+3H ↑。
2 4 2
10.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)结合元素周期表,回答下列问题:
学科网(北京)股份有限公司族周
ⅠA 0
期
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨
(1)①、③、⑨按照原子个数比 构成化合物的结构式 。
(2)写出含有③、⑤元素且既具有离子键又具有非极性共价键化合物的电子式 。
(3)①②③⑤形成化合物在水溶液中的电离方程式 。
(4)下列事实能用元素周期律解释并正确的是 (填字母序号)。
a.对应阴离子还原性由强到弱的顺序为⑧>⑨>④
b.⑨的气态氢化物的稳定性大于④的氢化物
c.原子序数为35的元素最高价氧化物的水化的酸性比⑨最高价氧化物的水化的酸性强
d.③的简单氢化物的沸点高于⑧的氢化物
e.原子半径由小到大的顺序为③<⑧<⑥<⑤
(5)②和⑦按照原子个数比 构成的固体化合物,易与水反应生成可燃性气体和白色沉淀。在相同条件
下,此气体密度是 密度的8倍。化合物与水反应的化学方程式为 。
(6)W是第Ⅷ族中原子序数最小的元素。W的单质可用于处理酸性废水中的 ,使其转换为 ,同
时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为 。
【答案】(1)H-O-Cl
(2)
(3) ;
(4)ae
(5)
(6)
【分析】根据元素在周期表中的位置可知,①为H,②为C,③为O,④为F,⑤为Na,⑥为Mg,⑦为
Al,⑧为S,⑨为Cl,以此解题。
【解析】(1)由分析可知,①为H,③为O,⑨为Cl,则①、③、⑨按照原子个数比 构成化合物为
HClO,其结构式为:H-O-Cl;
(2)由分析可知,③为O,⑤为Na,两者形成的既具有离子键又具有非极性共价键化合物为过氧化钠,
其电子式为: ;
(3)由分析可知,①为H,②为C,③为O,⑤为Na,这四种元素形成的化合物为碳酸氢钠,其在水溶
学科网(北京)股份有限公司液中的电离方程式为: ; ;
(4)由分析可知,③为O,④为F,⑧为S,⑨为Cl,a.非金属性F>Cl>S,则对应阴离子还原性由强到
弱的顺序为S2->Cl->F-,a正确;
b.非金属性F>Cl,则⑨的气态氢化物的稳定性小于④的氢化物,b错误;
c.原子序数为35的元素为Br,其非金属性小于Cl,则其最高价氧化物的水化的酸性比⑨最高价氧化物的
水化的酸性弱,c错误;
d.水分子之间存在氢键,沸点较高,则③的简单氢化物的沸点高于⑧的氢化物,d正确;
e.同周期越靠左半径越大,同主族越靠下半径越大,则原子半径由小到大的顺序为③<⑧<⑥<⑤,e正确;
故选ade;
(5)由分析可知,②为C,⑦为Al,按照原子个数比 构成的固体化合物为Al C ,其和水反应生成的
4 3
气体密度是 密度的8倍,则其分子量为16,根据元素守恒可知,该气体为甲烷,则化合物与水反应的
化学方程式为: ;
(6)W是第Ⅷ族中原子序数最小的元素,则W是Fe,有磁性的W的氧化物X为Fe O,根据题意可知,
3 4
上述反应的离子方程式为 。
学科网(北京)股份有限公司