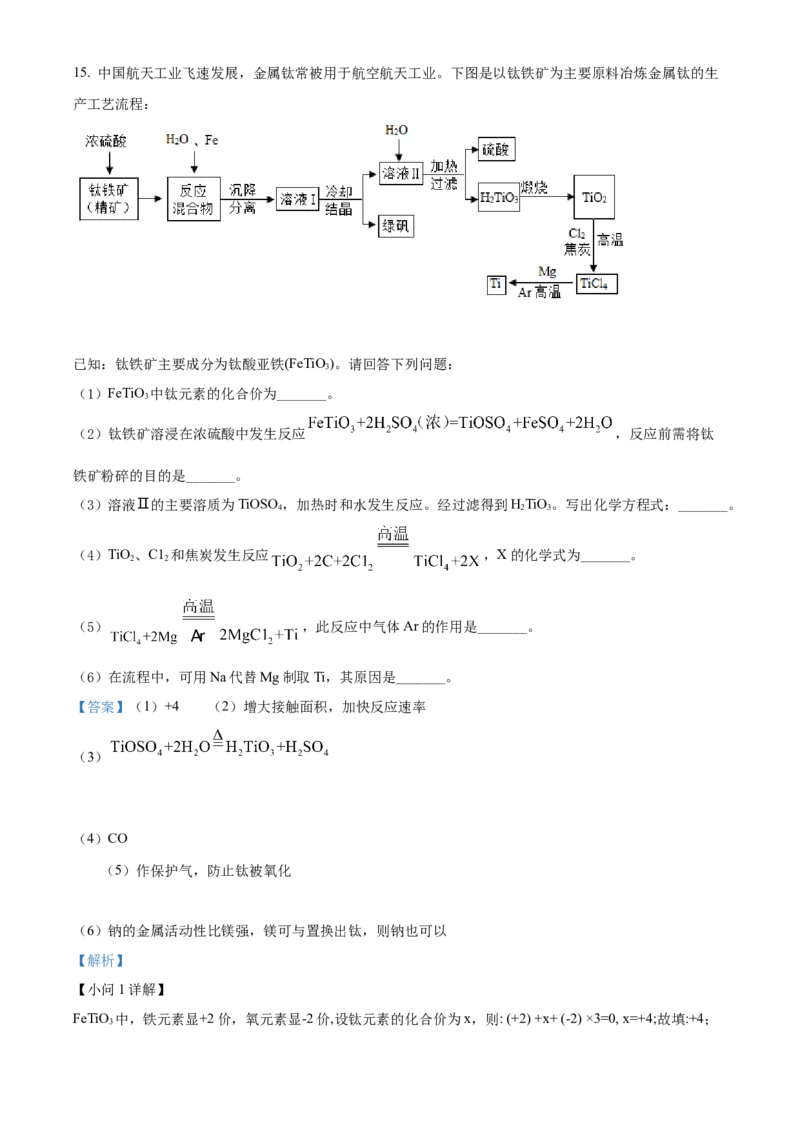
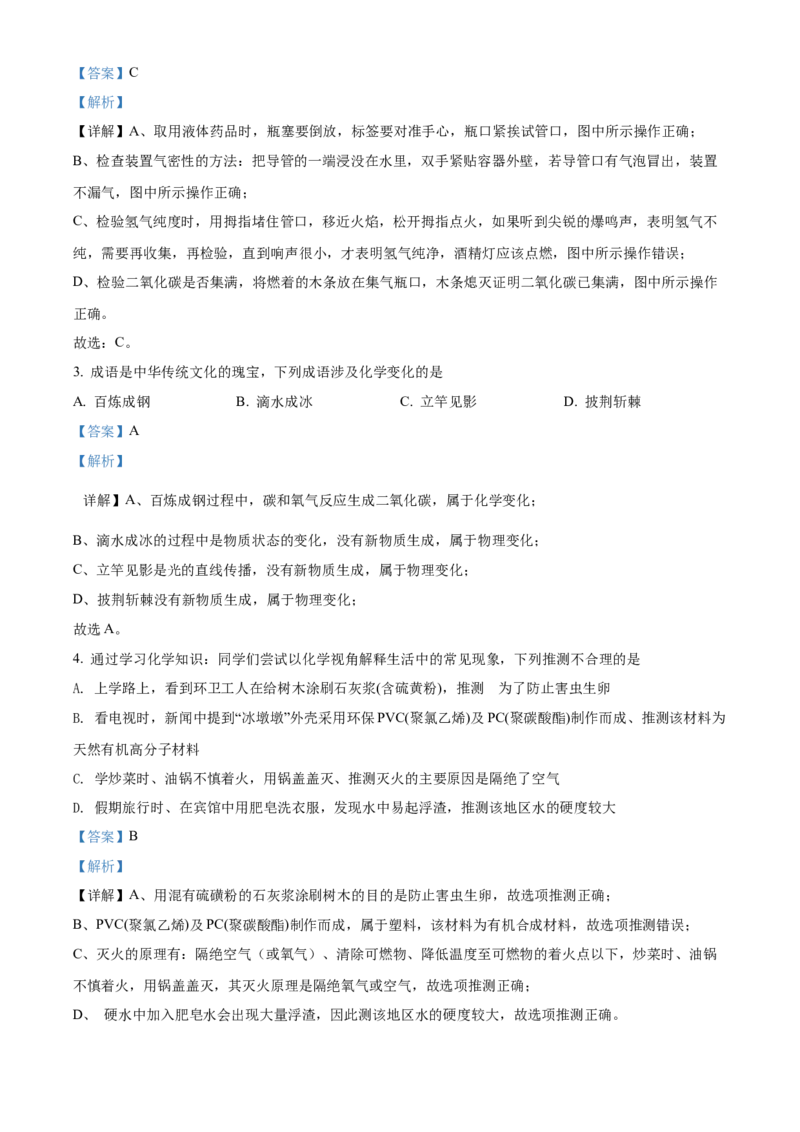文档内容
2022 年大庆市初中升学考试
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Cl-35.5
K-39 Ca-40 Cu-64 Zn-65 Ag-108
一、选择题(本大题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一
项符合要求)
1. 我国提出争取在2030年前实现碳达峰,2060年实现碳中和,碳中和是指CO 的排放总量和减少总量相
2
当。下列做法不利于实现此目标的是
A. 太阳能、风能等清洁能源代替化石燃料的使用
B. 为了实现CO 的零排放,大规模开采可燃冰作为新能源
2
C. 大力植树造林,严禁乱砍滥伐森林
D. 在日常生活中,倡导“低碳”生活
【答案】B
【解析】
【详解】A、太阳能、风能等清洁能源代替化石燃料的使用,可以减少CO 的排放,做法利于实现此目标;
2
B、为了实现CO 的零排放,要合理开采可燃冰作为新能源,大量开采会造成资源浪费,做法不利于实现
2
此目标;
C、大力植树造林,严禁乱砍滥伐森林,植物光合作用吸收二氧化碳,做法利于实现此目标;
D、在日常生活中,倡导“低碳”生活,可以减少CO 的排放,做法利于实现此目标;
2
故选B。
2. 下列图示实验操作错误的是
A. 液体的倾倒 B. 检查装置气密性
C. 检验H 的纯度 D. 证明CO 是否集满
2 2【答案】C
【解析】
【详解】A、取用液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口,图中所示操作正确;
B、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置
不漏气,图中所示操作正确;
C、检验氢气纯度时,用拇指堵住管口,移近火焰,松开拇指点火,如果听到尖锐的爆鸣声,表明氢气不
纯,需要再收集,再检验,直到响声很小,才表明氢气纯净,酒精灯应该点燃,图中所示操作错误;
D、检验二氧化碳是否集满,将燃着的木条放在集气瓶口,木条熄灭证明二氧化碳已集满,图中所示操作
正确。
故选:C。
3. 成语是中华传统文化的瑰宝,下列成语涉及化学变化的是
A. 百炼成钢 B. 滴水成冰 C. 立竿见影 D. 披荆斩棘
【答案】A
【解析】
【
详解】A、百炼成钢过程中,碳和氧气反应生成二氧化碳,属于化学变化;
B、滴水成冰的过程中是物质状态的变化,没有新物质生成,属于物理变化;
C、立竿见影是光的直线传播,没有新物质生成,属于物理变化;
D、披荆斩棘没有新物质生成,属于物理变化;
故选A。
4. 通过学习化学知识:同学们尝试以化学视角解释生活中的常见现象,下列推测不合理的是
A. 上学路上,看到环卫工人在给树木涂刷石灰浆(含硫黄粉),推测 是为了防止害虫生卵
B. 看电视时,新闻中提到“冰墩墩”外壳采用环保PVC(聚氯乙烯)及PC(聚碳酸酯)制作而成、推测该材料为
天然有机高分子材料
C. 学炒菜时、油锅不慎着火,用锅盖盖灭、推测灭火的主要原因是隔绝了空气
D. 假期旅行时、在宾馆中用肥皂洗衣服,发现水中易起浮渣,推测该地区水的硬度较大
【答案】B
【解析】
【详解】A、用混有硫磺粉的石灰浆涂刷树木的目的是防止害虫生卵,故选项推测正确;
B、PVC(聚氯乙烯)及PC(聚碳酸酯)制作而成,属于塑料,该材料为有机合成材料,故选项推测错误;
C、灭火的原理有:隔绝空气(或氧气)、清除可燃物、降低温度至可燃物的着火点以下,炒菜时、油锅
不慎着火,用锅盖盖灭,其灭火原理是隔绝氧气或空气,故选项推测正确;
D、 硬水中加入肥皂水会出现大量浮渣,因此测该地区水的硬度较大,故选项推测正确。故选:B。
5. 化学的世界五彩缤纷,在化学变化中感受化学之美。下列反应的现象或化学方程式错误的是
A. 铝丝浸入硫酸铜溶液中,铝丝上附着红色固体,溶液蓝色变浅:
B. 向黄色的FeCl 溶液中加入NaOH溶液,产生红褐色沉淀:
3
C. 紫红色的铜丝浸入稀硫酸中,产生无色气泡,溶液变为蓝色:
D. 黑色的氧化亚铁溶于稀盐酸中,溶液变为浅绿色:
【答案】C
【解析】
【详解】A、铝丝浸入硫酸铜溶液中,铝和硫酸铜反应生成硫酸铝和铜,铝丝上附着红色固体,溶液蓝色
变浅,该反应的化学方程式为: ,不符合题意;
B、向黄色的氯化铁溶液中加入氢氧化钠溶液,氢氧化钠和氯化铁反应生成氢氧化铁和氯化钠,产生红褐
色沉淀,该反应的化学方程式为: ,不符合题意;
C、紫红色的铜丝浸入稀硫酸中,铜位于金属活动性顺序表氢的后面,不和稀硫酸不反应,无明显现象,
符合题意;
D、黑色的氧化亚铁和稀盐酸反应生成氯化亚铁和水,现象为:黑色固体逐渐溶解,溶液变为浅绿色,该
反应的化学方程式为: ,不符合题意。
故选C。
6. 为达到下列实验目的,相应的实验操作合理的是
选项 实验目的 实验操作
A 除去KCl溶液中少量CaC1 杂质 向溶液中通入过量的CO 气体,过滤
2 2
用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色
B 测定质量分数为98%的浓硫酸的pH
与标准比色卡对照
取少量两种化肥分别置于研钵中,各加入少量熟石灰粉
C 鉴别尿素和碳铵两种化肥
末,混合、研磨,闻气味
用托盘天平称量2.88gNaCl倒入烧杯中,用量
D 配制48g质量分数为6%的NaCl溶液
筒量取所需水于烧杯中,用玻璃棒搅拌A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、二氧化碳和杂质不反应,无法除去杂质,A错,不符合题意;
B、浓硫酸具有腐蚀性,会腐蚀滤纸,B错,不符合题意;
C、尿素中不含铵根离子,碳铵中含有铵根;加熟石灰研磨,尿素没反应,碳铵有强烈的氨味,可以鉴别
出,C对,符合题意;
D、托盘天平的精确值是0.1g无法准确测出2.88g质量,D错,不符合题意。
故选C。
7. 下列图象能正确反映对应变化关系的是
A. 在盛有不同固体的三个密闭容器中,分别加入等量质量分数为10%的盐酸
B. 在密闭容器中用红磷测定空气中氧气的含量
C. 向质量均为6.0g的MgO、Mg(OH) 固体中,分别加入100g质量分数为
2
20%的盐酸
D. 将锌粉加入到Cu(NO ) 和AgNO 的混合溶液中,溶液最终变为无色
3 2 3【答案】C
【解析】
【详解】A、在盛有不同固体的三个密闭容器中,分别加入等量质量分数为10%的盐酸,氧化钙和盐酸反
应生成氯化钙和水,放出大量的热,装置内气体受热膨胀,压强增大,待完全反应后,逐渐冷却至室温,
压强恢复至原来的压强,氢氧化钙和盐酸反应生成氯化钙和水,放出热量,装置内气体受热膨胀,压强增
大,待完全反应后,逐渐冷却至室温,压强恢复至原来的压强,碳酸钙和稀盐酸反应生成氯化钙、二氧化
碳和水,反应生成了气体,装置内压强增大,待完全反应后,由于二氧化碳溶于水,且压强增大,二氧化
碳的溶解度增大,故压强逐渐减小,待二氧化碳的水溶液达到饱和后,不再变化,不符合题意;
B、在密闭容器中用红磷测定空气中氧气的含量,红磷燃烧,放出大量的热,装置内气体受热膨胀,压强
增大,待完全反应后,逐渐冷却至室温,由于消耗了氧气,装置内压强减小,但是最后压强低于原来的压
强,不符合题意;
C、向质量均为6.0g的MgO、Mg(OH)2固体中,分别加入100g质量分数为20%的盐酸,氧化镁和稀盐酸
反应: ,氢氧化镁和稀盐酸反应: ,
由化学方程式可知,这两个反应中,最后盐酸均过量,一开始盐酸不足,生成氯化镁的质量相同,最后盐
酸过量,氧化镁生成氯化镁的质量大,符合题意;
D、将锌粉加入到硝酸铜和硝酸银的混合溶液中,锌先与硝酸银反应: ,
65份质量的锌置换出216份质量的银,固体质量增加,溶液质量减小,待硝酸银完全反应后,锌和硝酸铜
反应: ,65份质量的锌置换出64份质量的铜,固体质量减小,溶液质量
增加,最终溶液变为无色,说明硝酸铜已经完全反应,故溶液质量先减小后增加,待完全反应后,不再变
化,不符合题意。
故选C。
8. 碘元素被称为“智力元素”。是人体必需的微量元素之一、下列叙述正确的是的
A. 碘原子核内有53个质子,一个碘原子 质量是126.9g
B. 碘原子核内质子的总质量等于核外电子的总质量
C. 食用碘盐可预防碘缺乏病,人体摄入碘越多越有利于健康
D. 碘离子(I-)核外有5个电子层、最外层有8个电子
【答案】D
【解析】
【详解】A.由图知,碘的相对原子质量为126.9,实际质量很小,故说法错误;
B.电子的质量很小,所以碘原子核内质子的质量远大于核外电子的质量,故说法错误;
C.碘摄入过多或过少都会引发疾病,故说法错误;
D.由碘原子结构示意图可知,碘原子有5个电子层,当碘原子得到1个电子后,变成碘离子,最外层达到
8个电子的稳定结构,电子层仍是5层,故说法正确。故选D。
9. 甲、乙两个烧杯中各盛有100.0g水,T℃时,分别加入质量均为ag的KNO 或KC1固体,充分溶解后,
2 3
甲烧杯中现象如图1所示,再将两个烧杯同时降温至T℃、乙烧杯中现象如图2所示。
1
KNO 和KC1在不同温度时的溶解度表
3
温度/℃ 0 T 20 T 40 60 80 100
1 2
KNO 13.3 25.0 31.6 35.1 63.9 110 169 246
3
溶解
度/g
KC1 27.6 31.8 34.0 35.1 40.0 45.5 51.1 56.7
下列说法正确的是( )
A. 乙烧杯中加入的固体一定是KNO
3
B. 图1中溶液可能是该溶质的饱和溶液,图2中上层清液一定是该溶质的饱和溶液
C. 若从T℃重新升高到T℃,甲、乙两溶液中的溶质质量分数一定不相等
1 2
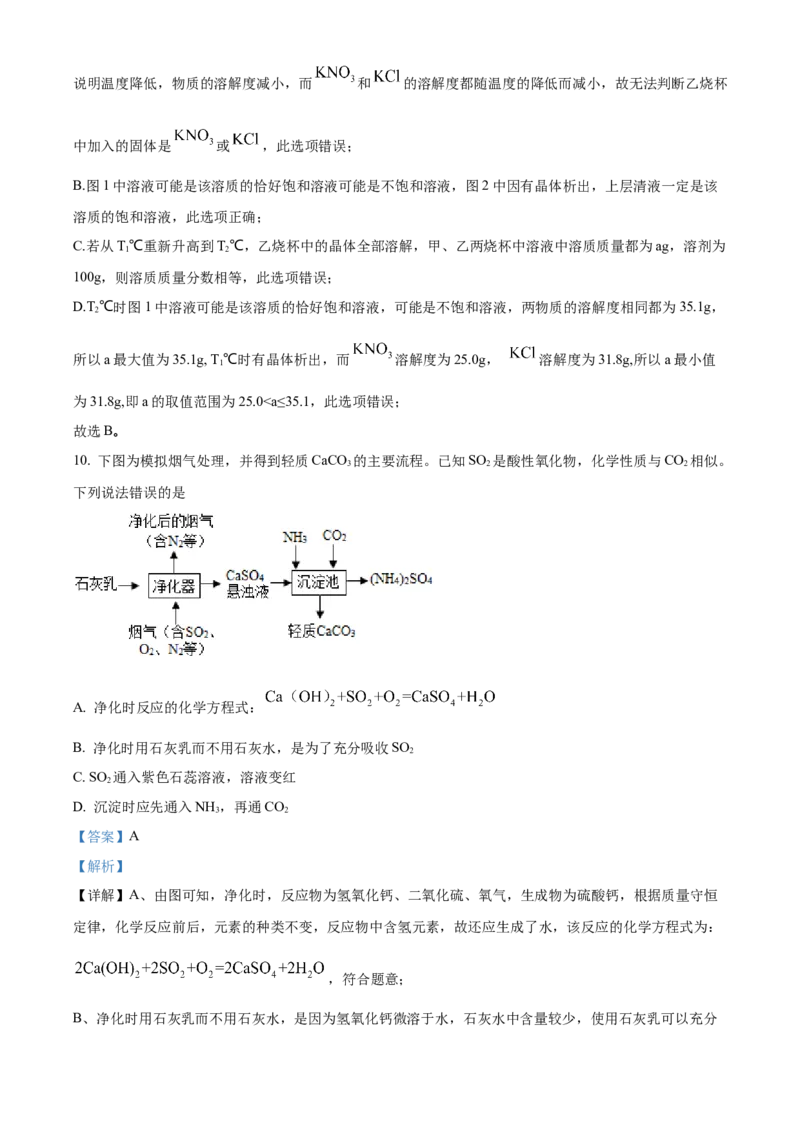
D. a的取值范围为31.8”、“<”或
2 4 2 4 2 4 2 4
“=”)。
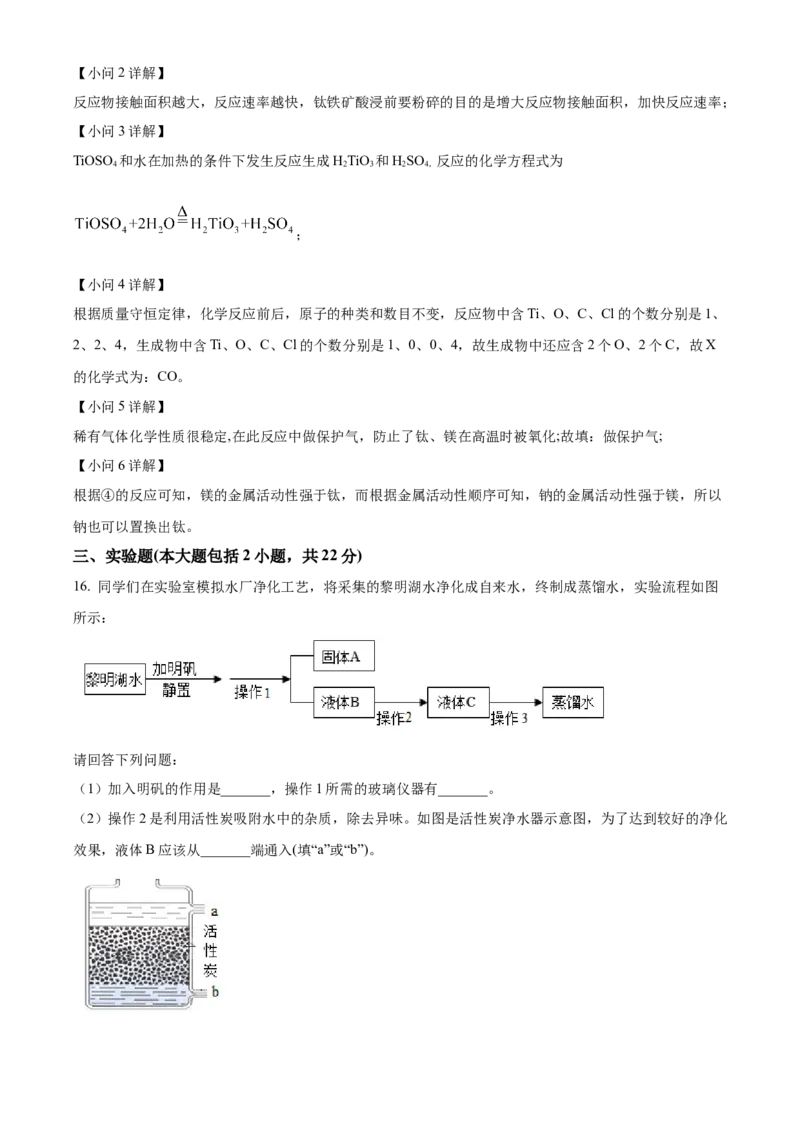
【答案】(1) ①. 吸附水中悬浮颗粒,加速沉降 ②. 玻璃棒、烧杯和漏斗 (2)b
(3) ①. 蒸馏 ②. 碎瓷片
③. 防止液体暴沸
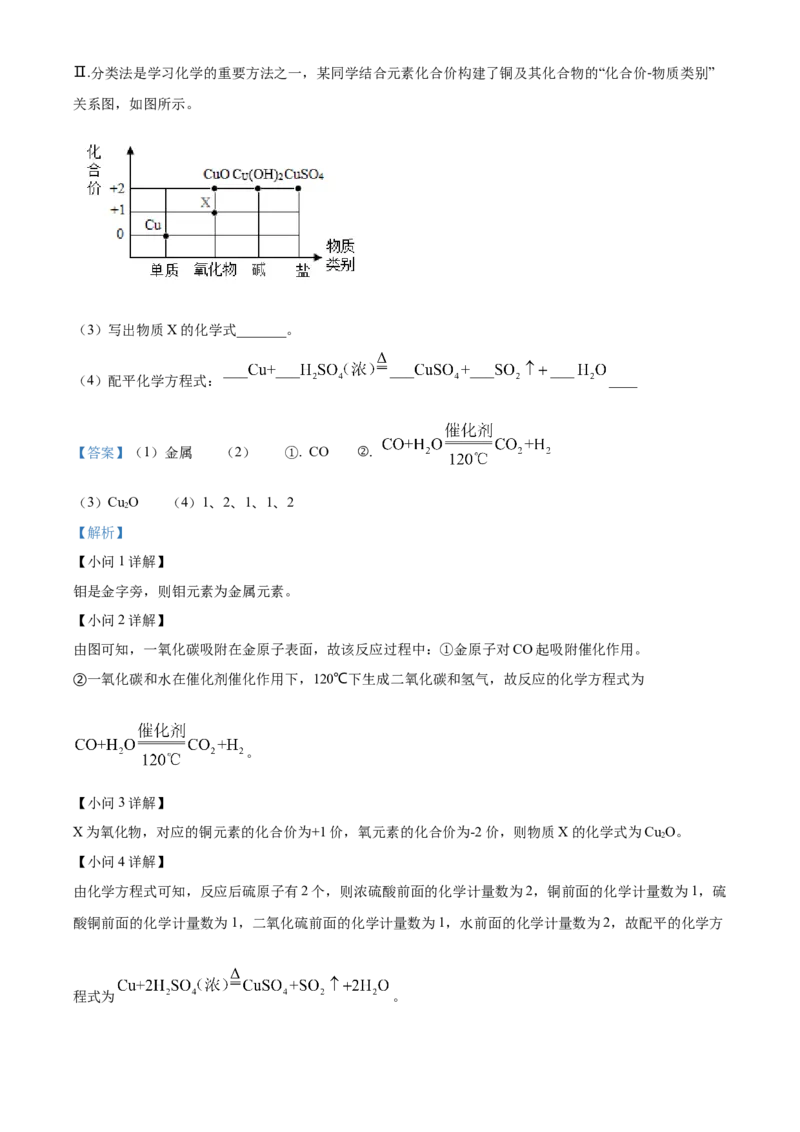
(4) ①.
②. >
【解析】
【小问1详解】
明矾溶于水形成具有吸附性的物质,能加速除去水中的不溶性固体杂质,故加入明矾的作用是吸附固体,
加速沉降;操作1得到的是固体和液体,该操作的名称是过滤,所需的玻璃仪器有玻璃棒、烧杯和漏斗;
【小问2详解】
利用如图所示的装置进行操作2,可以利用活性炭的吸附性,除去色素和异味,待处理的水应该从b端通
入,水与活性炭充分接触,净化效果更好;
【小问3详解】
①通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是蒸馏;
②蒸馏操作时时,除了向烧瓶中加入液体C,还需要加入少量的碎瓷片,其作用是防止液体暴沸;
【小问4详解】
①高铁酸钾与水反应生成氢氧化钾、氢氧化铁和氧气,反应的化学方程式为:
;
②根据化学反应方程式可知,NaFeO 可以反应生成KFeO,因此可以推断出NaFeO 的溶解度大于
2 4 2 4 2 4
KFeO 的溶解度。
2 417. 春晚节目《只此青绿》取材于宋朝王希孟的《千里江山图》,画中主要用了石绿、石青两种矿物质颜
料。
I.石绿,又称孔雀石,主要成分的化学式为Cu (OH) CO,我国古代曾用孔雀石炼铜,涉及两步反应。
2 2 3
(1)请写出第一步反应的化学方程式:_______。
Ⅱ.石青。又称蓝铜矿。主要成分的化学式为xCu(OH) ·yCuCO,某学习小组设计实验对其组成进行探究(假
2 3
设矿石中其它杂质受热不分解,不溶于水且不与稀硫酸反应。
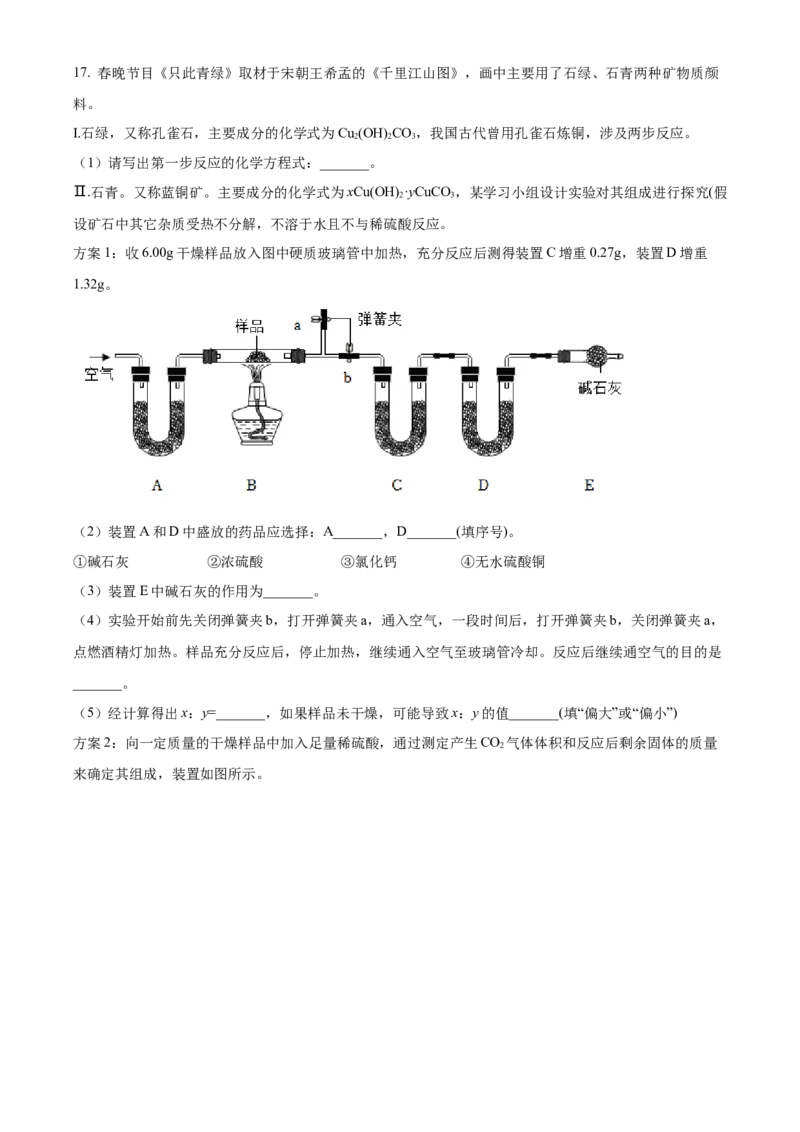
方案1:收6.00g干燥样品放入图中硬质玻璃管中加热,充分反应后测得装置C增重0.27g,装置D增重
1.32g。
(2)装置A和D中盛放的药品应选择:A_______,D_______(填序号)。
①碱石灰 ②浓硫酸 ③氯化钙 ④无水硫酸铜
(3)装置E中碱石灰的作用为_______。
(4)实验开始前先关闭弹簧夹b,打开弹簧夹a,通入空气,一段时间后,打开弹簧夹b,关闭弹簧夹a,
点燃酒精灯加热。样品充分反应后,停止加热,继续通入空气至玻璃管冷却。反应后继续通空气的目的是
_______。
(5)经计算得出x:y=_______,如果样品未干燥,可能导致x:y的值_______(填“偏大”或“偏小”)
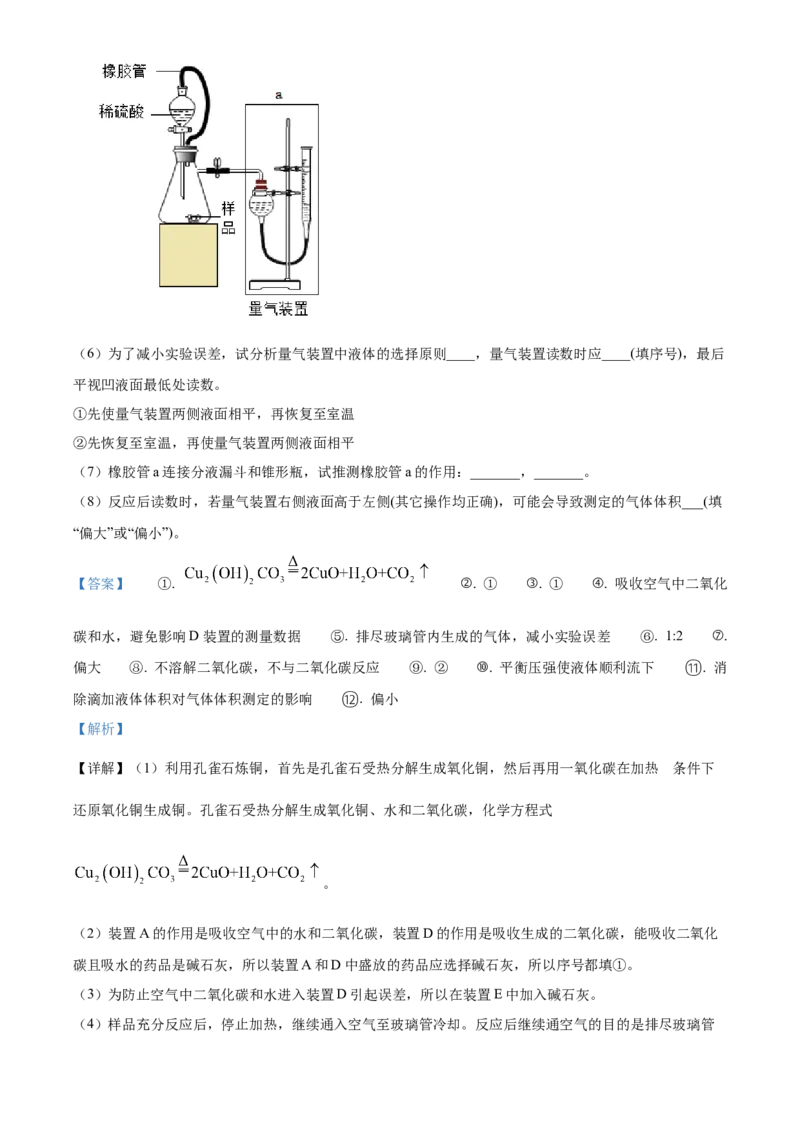
方案2:向一定质量的干燥样品中加入足量稀硫酸,通过测定产生CO 气体体积和反应后剩余固体的质量
2
来确定其组成,装置如图所示。(6)为了减小实验误差,试分析量气装置中液体的选择原则____,量气装置读数时应____(填序号),最后
平视凹液面最低处读数。
①先使量气装置两侧液面相平,再恢复至室温
②先恢复至室温,再使量气装置两侧液面相平
(7)橡胶管a连接分液漏斗和锥形瓶,试推测橡胶管a的作用:_______,_______。
(8)反应后读数时,若量气装置右侧液面高于左侧(其它操作均正确),可能会导致测定的气体体积___(填
“偏大”或“偏小”)。
【答案】 ①. ②. ① ③. ① ④. 吸收空气中二氧化
碳和水,避免影响D装置的测量数据 ⑤. 排尽玻璃管内生成的气体,减小实验误差 ⑥. 1:2 ⑦.
偏大 ⑧. 不溶解二氧化碳,不与二氧化碳反应 ⑨. ② ⑩. 平衡压强使液体顺利流下 ⑪. 消
除滴加液体体积对气体体积测定的影响 ⑫. 偏小
【解析】
的
【详解】(1)利用孔雀石炼铜,首先是孔雀石受热分解生成氧化铜,然后再用一氧化碳在加热 条件下
还原氧化铜生成铜。孔雀石受热分解生成氧化铜、水和二氧化碳,化学方程式
。
(2)装置A的作用是吸收空气中的水和二氧化碳,装置D的作用是吸收生成的二氧化碳,能吸收二氧化
碳且吸水的药品是碱石灰,所以装置A和D中盛放的药品应选择碱石灰,所以序号都填①。
(3)为防止空气中二氧化碳和水进入装置D引起误差,所以在装置E中加入碱石灰。
(4)样品充分反应后,停止加热,继续通入空气至玻璃管冷却。反应后继续通空气的目的是排尽玻璃管内生成的气体,减小实验误差。
(5)
如果样品未干燥,装置C增重会吸收样品中的水,增重偏大,根据上述计算过程可知,会导致x:y的值
偏大。
(6)为了减小实验误差,量气装置中液体的选择原则是不溶解二氧化碳,不与二氧化碳反应。量气装置
读数时应先恢复至室温,再使量气装置两侧液面相平。
(7)橡胶管a连接分液漏斗和锥形瓶,作用是:平衡压强使液体顺利流下;消除滴加液体体积对气体体积
测定的影响。
(8)反应后读数时,若量气装置右侧液面高于左侧,则左侧气体受到右侧液体的压强被压缩,会导致测
定的气体体积偏小。
四、计算题(共8分)
18. 含氯消毒液是家庭常用的消毒用品,有效成分为次氯酸钠(NaClO)。工业制备原理为
。现向质量分数为8.0%的NaOH溶液中通入氯气,制得质量分数为
5.0%的NaClO消毒液(溶质为NaCl、NaClO和NaOH)2980g,请回答下列问题:
(1)NaClO中氯元素的化合价为_______。
(2)已知质量分数为0.05%的NaClO消毒液用于家居消毒效果较好。现用10g质量分数为5.0%的NaClO
消毒液,配制质量分数为0.05%的NaClO消毒液,需加入水的质量为_______g。
(3)请计算质量分数为5.0%的NaClO消毒液中NaOH的质量分数是___?(写出计算过程,计算结果精确
至0.1%)。
【答案】(1)+1 (2)990
(3)解:质量分数为5.0%的NaClO消毒液中NaClO的质量为:2980g×5.0%=149g
设参加反应的氯气的质量为x,参加反应的氢氧化钠的质量为yx=142g
y=160g
根据质量守恒定律,化学反应前后,物质的总质量不变,氢氧化钠溶液的质量为:2980g-142g=2838g
故剩余氢氧化钠的质量为:2838g×8.0%-160g=67.04g
故质量分数为5.0%的NaClO消毒液中NaOH的质量分数是:
答:质量分数为5.0%的NaC1O消毒液中NaOH的质量分数是2.2%。
【解析】
【小问1详解】
NaClO中钠元素显+1价,氧元素显-2价,设氯元素的化合价为x,根据化合物中,正、负化合价的代数和
为零,可得:(+1)+x+(-2)=0,x=+1;
【小问2详解】
解:设需加水的质量为x,根据稀释前后,溶质的质量不变,可得:10g×5.0%=(10g+x)×0.05%,
x=990g;
【小问3详解】
见答案。