文档内容
化学试题 河南专版 参考答案 第1
页 共6页
2025届高三部分重点中学3月联合测评
化学试题参考答案及多维细目表
题号
1
2
3
4
5
6
7
答案
D
B
C
B
A
C
D
题号
8
9
10
11
12
13
14
答案
D
A
D
C
D
B
C
1.【答案】D
【解析】甘油作冷却剂与吸水性无关,A 项错误;
光敏材料见光易分解,聚四氟乙烯性质稳定,不
能用作光敏胶片,B 项错误;激发氧气发光是物
理变化,C项错误;氮化镓为新型无机非金属材
料,D 项正确.
2.【答案】B
【解析】图中表示基态氮原子的轨道表示式,A 项
错误;3,3G二甲基戊烷的键线式为
,B项正确;
HF分子间形成氢键时,显负电性的氟原子在一
条直线上时排斥力最小, 可表示为
,C 项错误;图中表示
丙烷的球棍模型,D 项错误.
3.【答案】C
【解析】SO2转化为SO3,再用浓硫酸吸收,可制
得硫酸,A 不符合题意;铁强化酱油可以给人补
铁,B不符合题意;硅用作半导体材料,C 符合题
意;氯气与自来水中有机物反应生成的有机氯化
物对人体有害,D 不符合题意.
4.【答案】B
【解析】P4(
)在氧气中充分燃烧生成P4O10,
1molP4断裂P-P 键的数目为6N A,A 项错
误;SO
2-
4
中σ键个数是4,无孤电子对,即价层
电子对数是4,B 项正确;Fe与水蒸气反应生成
Fe3O4,1molFe反应转移的电子数是8
3N A,C
项错误;没有给出溶液的体积,无法确定Na
+的
数目,D 项错误.
5.【答案】A
【解析】OF2和SF2都是V 形分子,由于S-F键
的极性强于O-F键,故SF2分子的极性比OF2
的大,A 符合题意;O 的原子半径比S小,O-H
键的键长较短,故O-H 键键能较大,H2O 的稳
定性较强,B不符合题意;氧原子的电负性比硫
原子的大,导致H2O 中σ键电子对更靠近中心
原子,σ键电子对间的排斥力更大,从而使H2O
的键角更大,C不符合题意;分子间作用力越小,
物质沸点越低,H2O 分子间存在氢键,导致其分
子间作用力更大,沸点更高,D 不符合题意.
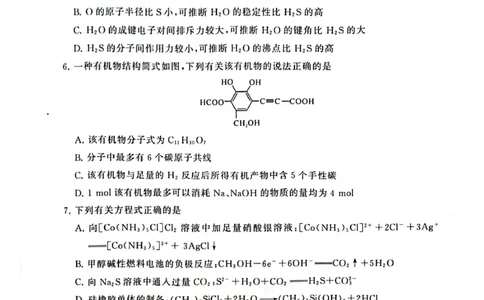
6.【答案】C
【解析】分子式为C11H8O7,A 项错误;分子中共
线的碳原子最多有
5
个, 如图:
,B 项错误;与足
量的H2反应后所得有机物的结构简式中的手
性
碳
原
子
如
图
所
示:
,C项正确;1mol
该有机物最多可以消耗NaOH 的物质的量为5
mol,D 项错误.
7.【答案】D
【解析】配合物内界的氯离子不易电离出来,反应
的离子方程式为Cl
-+Ag
+AgCl↓,A 项错
误;碱性溶液中甲醇转化为CO
2-
3,负极反应为
CH3OH-6e
-+8OH
-CO
2-
3+6H2O,B 项
错误;CO2过量时,CO
2-
3
转化为HCO
-
3,C 项错
误;硅橡胶单体的制备正确,D 项正确.
8.【答案】D
【解析】氯气与水发生反应:Cl
2+H2O
HCl
+HClO,碳酸钙消耗盐酸,使平衡向生成HClO
的方向移动,制得较高浓度的次氯酸溶液,A 不
符合题意;MnO2可以催化过氧化氢分解,加快
化学试题 河南专版 参考答案 第2
页 共6页
生成氧气的速率,B 不符合题意;饱和碳酸钠溶
液可与乙酸反应,且可降低乙酸乙酯的溶解度,C
不符合题意;固体NaOH 溶于水放热,需要冷却
至室温后再转移到容量瓶中,且洗涤烧杯和玻璃
棒的洗涤液也转入容量瓶,再加水定容,D 符合
题意.
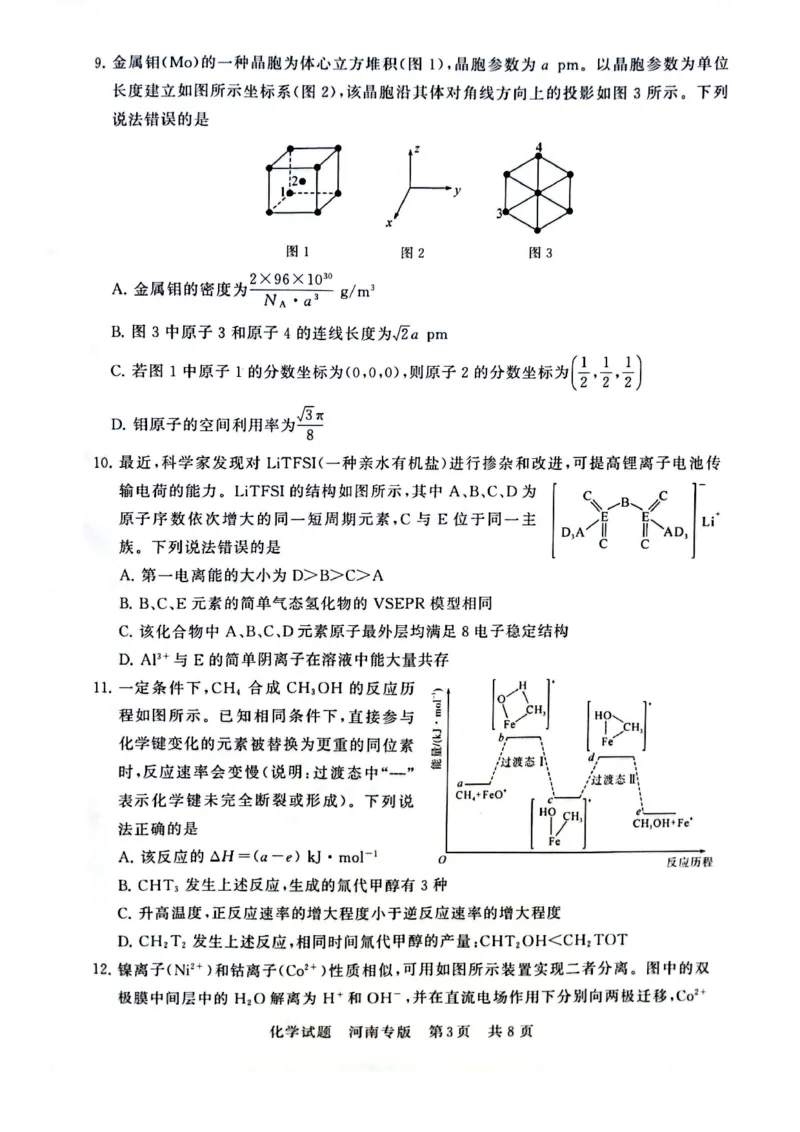
9.【答案】A
【解析】由图1知晶胞所含Mo的个数为1
8×8+
1=2,所以有ρ(a×10
-12m)
3=96×2
N A g,可得ρ
=2×96×10
36
a
3N A
g/m
3,A 符合题意;原子3和原
子4处于面对角线的关系,其连线长度是2a
pm,B不符合题意;原子2位于晶胞的体心,其分
数坐标是(1
2,1
2,1
2),C 不符合题意;晶胞体对
角线上的3个钼原子相切,3a=4r,钼原子的
空间利用率=
4
3πr
3×2
a
3
,将a=4r
3
代入,可得空
间利用率为3π
8,D 不符合题意.
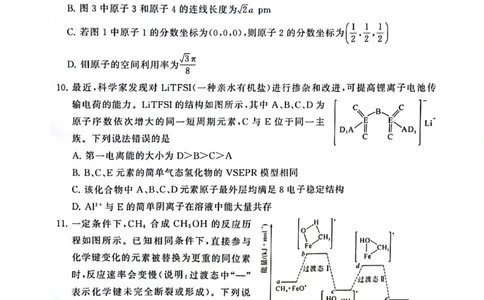
10.【答案】D
【解析】由结构简式可推知,A、B、C、D、E分别是
C、N、O、F、S.第一电离能:F>N>O>C,A
不符合题意;NH3、H2O、H2S 分子的VSEPR
模型都是四面体形,B 不符合题意;该化合物中
C、N、O、F元素原子最外层都是8个电子,C 不
符合题意;Al
3+与S
2-在溶液中发生相互促进
的水解反应,生成Al(OH)
3和H2S,D 符合
题意.
11.【答案】C
【解析】反应:CH4+FeO
+
CH3OH+Fe
+的
ΔH =(e-a)kJmol
-1,A 项错误;CHT3发
生上述反应,生成的氚代甲醇有CT3OH、
CHT2OT 两种,B 项错误;该反应放热,升高温
度平衡逆向移动,即正反应速率的增大程度小
于逆反应速率的增大程度,C 项正确;
转化为
过程中,若用
CH2T2代替CH4,由于H-C 键比T-C 键更
易断开,导致生成
更快,相同时间氚
代甲醇的产量:CHT2OH >CH2TOT,D 项
错误.
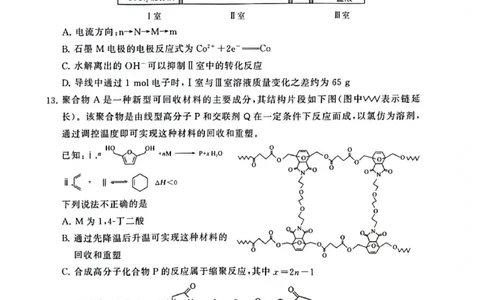
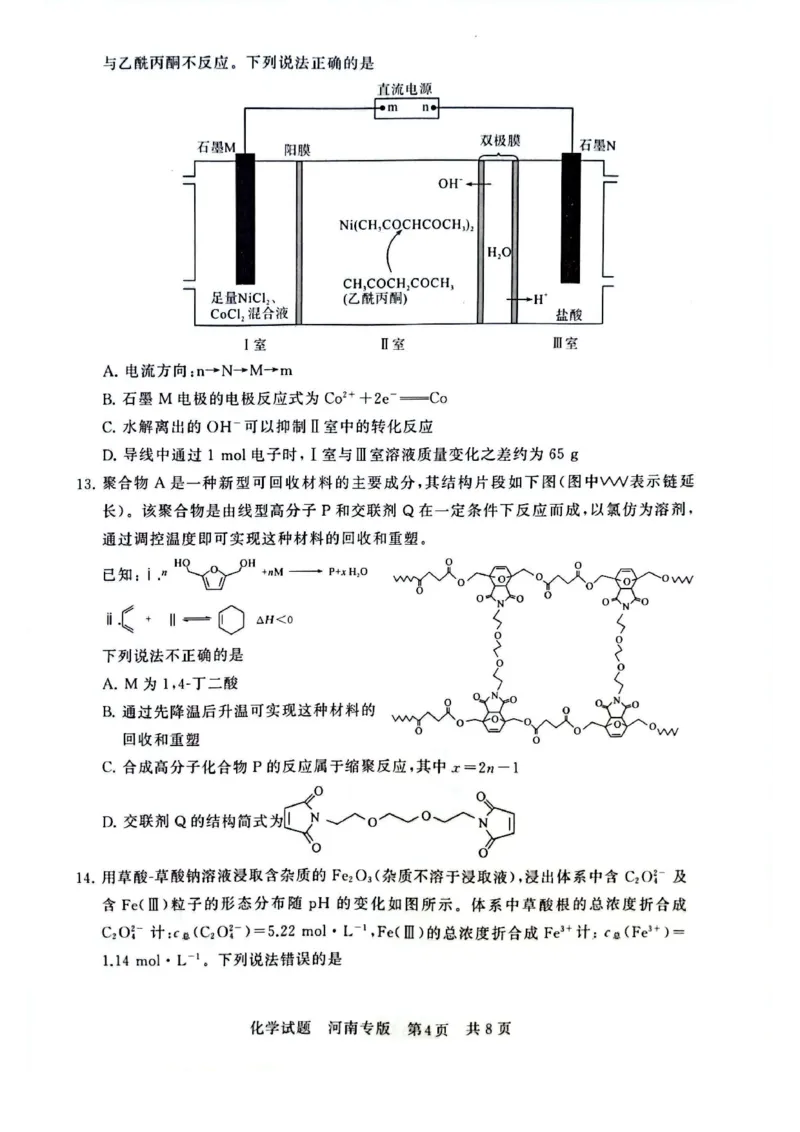
12.【答案】D
【解析】根据双极膜中H2O 解离生成的H
+、
OH
-的迁移方向,可以判断石墨M 是阳极、石
墨N 是阴极,电流方向:m→M→N→n,A 项错
误;石墨M 的电极反应式:2Cl
--2e
-Cl
2↑,
B项错误;Ⅱ
室中发生转化: Ni
2+
+
2CH3COCH2COCH3
Ni(CH3COCHCOCH3)
2
+2H
+,水解离出的OH
-与H
+反应,促进
Ni
2+的转化,C项错误;导线中通过1mol电子
时,Ⅰ室中有1molCl
-转化为Cl
2,同时0.
5
molNi
2+和Co
2+穿过阳膜进入Ⅱ室,减少的质
量约为35.
5g+59
2g=65g;Ⅲ室中1molH
+转
化为H2,同时有1molH
+进入Ⅲ室,Ⅲ室溶液
质量不变;因此,两室溶液质量变化之差约为
65g,D 项正确.
13.【答案】B
【解析】由聚合物A 的结构片段可推知,M 为
、
P
为
, M
的名称为1,4G丁二酸,A 不符合题意;聚合物A
通过先升温使化学键断开形成单体,再在低温
时单体重新聚合形成新的聚合物,实现回收和
重塑,B 符合题意;缩聚反应生成P 的同时,生
成(2n-1)个H2O,C不符合题意;交联剂Q 与
P发生DA 反应,故交联剂Q 的结构简式为
,D 不符
合题意.
化学试题 河南专版 参考答案 第3
页 共6页
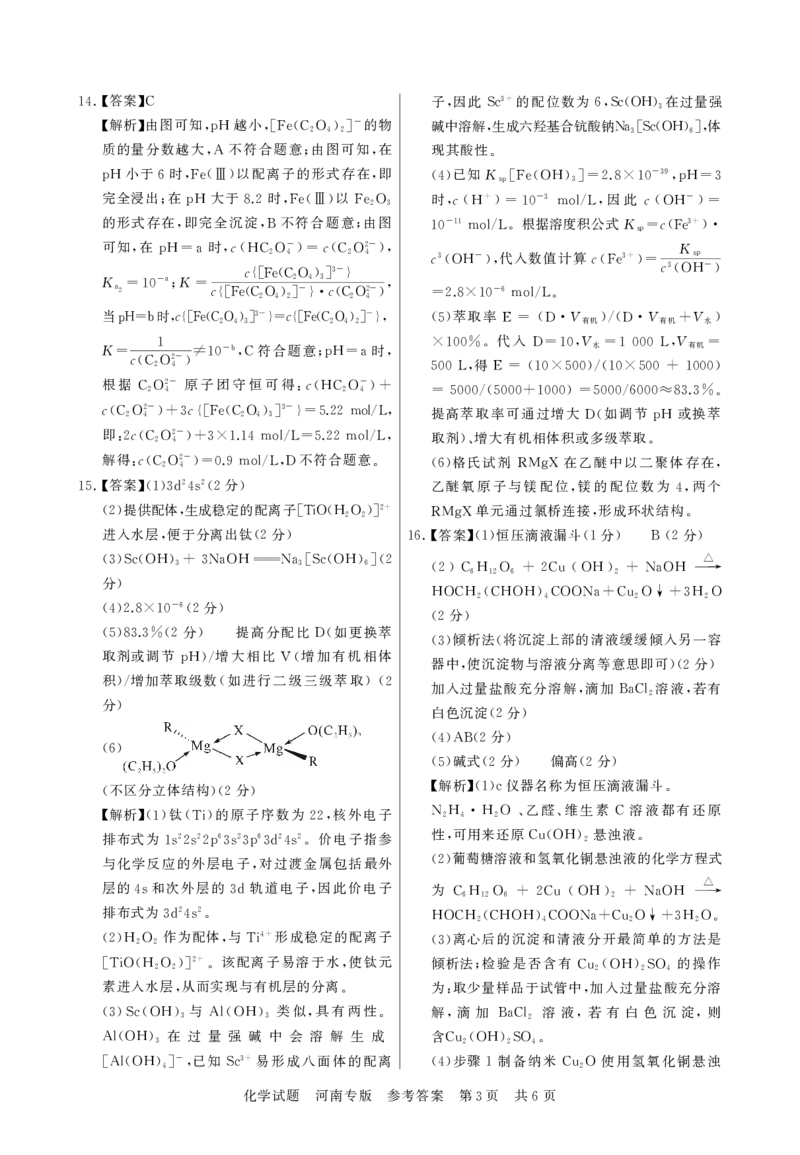
14.【答案】C
【解析】由图可知,pH 越小,[Fe(C2O4)
2]
-的物
质的量分数越大,A 不符合题意;由图可知,在
pH 小于6时,Fe(Ⅲ)以配离子的形式存在,即
完全浸出;在pH 大于8.
2时,Fe(Ⅲ)以Fe2O3
的形式存在,即完全沉淀,B 不符合题意;由图
可知,在pH=a时,c(HC2O
-
4)=c(C2O
2-
4),
Ka2=10
-a;K =
c{[Fe(C2O4)
3]
3-}
c{[Fe(C2O4)
2]
-}c(C2O
2-
4),
当pH=b时,
c{[Fe(C2O4)
3]
3-}=c{[Fe(C2O4)
2]
-},
K=
1
c(C2O
2-
4)≠10
-b,C 符合题意;pH=a时,
根据C2O
2-
4
原子团守恒可得:c(HC2O
-
4)+
c(C2O
2-
4)+3c{[Fe(C2O4)
3]
3-}=5.
22mol/L,
即:2c(C2O
2-
4)+3×1.
14mol/L=5.
22mol/L,
解得:
c(C2O
2-
4)=0.
9mol/L,D 不符合题意.
15.【答案】(1)3d
24s
2(2分)
(2)提供配体,生成稳定的配离子[TiO(H2O2)]
2+
进入水层,便于分离出钛(2分)
(3)Sc(OH)
3+3NaOH Na3[Sc(OH)
6](2
分)
(4)2.
8×10
-6(2分)
(5)83.
3%(2分) 提高分配比D(如更换萃
取剂或调节pH)/增大相比V(增加有机相体
积)/增加萃取级数(如进行二级三级萃取)(2
分)
(6)
(不区分立体结构)(2分)
【解析】(1)钛(Ti)的原子序数为22,核外电子
排布式为1s
22s
22p
63s
23p
63d
24s
2.价电子指参
与化学反应的外层电子,对过渡金属包括最外
层的4s和次外层的3d轨道电子,因此价电子
排布式为3d
24s
2.
(2)H2O2作为配体,与Ti
4+形成稳定的配离子
[TiO(H2O2)]
2+.该配离子易溶于水,使钛元
素进入水层,从而实现与有机层的分离.
(3)Sc(OH)
3与Al(OH)
3类似,具有两性.
Al(OH)
3在过量强碱中会溶解生成
[Al(OH)
4]
-,已知Sc
3+易形成八面体的配离
子,因此Sc
3+的配位数为6,Sc(OH)
3在过量强
碱中溶解,生成六羟基合钪酸钠Na
3[Sc(OH)
6],体
现其酸性.
(4)已知Ksp[Fe(OH)
3]=2.
8×10
-39,pH=3
时,
c(H
+)=10
-3mol/L,因此c(OH
-)=
10
-11mol/L.根据溶度积公式Ksp=c(Fe
3+)
c
3(OH
-),代入数值计算c(Fe
3+)=
Ksp
c
3(OH
-)
=2.
8×10
-6mol/L.
(5)萃取率E =(DV有机)/(DV有机+V水)
×100%.代入D=10,V水=1000L,V有机=
500L,得E =(10×500)/(10×500+1000)
=5000/(5000+1000)=5000/6000≈83.
3%.
提高萃取率可通过增大D(如调节pH 或换萃
取剂)、增大有机相体积或多级萃取.
(6)格氏试剂RMgX 在乙醚中以二聚体存在,
乙醚氧原子与镁配位,镁的配位数为4,两个
RMgX 单元通过氯桥连接,形成环状结构.
16.【答案】(1)恒压滴液漏斗(1分) B (2分)
(2)C6H12O6+2Cu (OH)
2+NaOH
△
→
HOCH2(CHOH)
4COONa+Cu2O↓+3H2O
(2分)
(3)倾析法(将沉淀上部的清液缓缓倾入另一容
器中,使沉淀物与溶液分离等意思即可)(2分)
加入过量盐酸充分溶解,滴加BaCl
2溶液,若有
白色沉淀(2分)
(4)AB(2分)
(5)碱式(2分) 偏高(2分)
【解析】(1)c仪器名称为恒压滴液漏斗.
N2H4H2O 、乙醛、维生素C 溶液都有还原
性,可用来还原Cu(OH)
2悬浊液.
(2)葡萄糖溶液和氢氧化铜悬浊液的化学方程式
为C6H12O6+2Cu (OH )
2+NaOH
△
→
HOCH2(CHOH)
4COONa+Cu2O↓+3H2O.
(3)离心后的沉淀和清液分开最简单的方法是
倾析法;检验是否含有Cu2(OH)
2SO4的操作
为:取少量样品于试管中,加入过量盐酸充分溶
解,滴加BaCl
2溶液,若有白色沉淀,则
含Cu2(OH)
2SO4.
(4)步骤1制备纳米Cu2O 使用氢氧化铜悬浊
化学试题 河南专版 参考答案 第4
页 共6页
液代替硫酸铜溶液可能的原因是氢氧化铜悬浊
液中Cu
2+浓度小,反应速率慢,Cu
2+在碱性条件
下比酸性条件下氧化性弱,A、B正确;Cu(OH)
2
不能循环使用,原子利用率低,C错误.
(5)①Na2S2O3标准液应使用碱式滴定管.
②若水样中含有Fe
3+,则会氧化I
— 为I
2,消耗
Na2S2O3溶液变多,则测定水样中含氧量会
偏高.
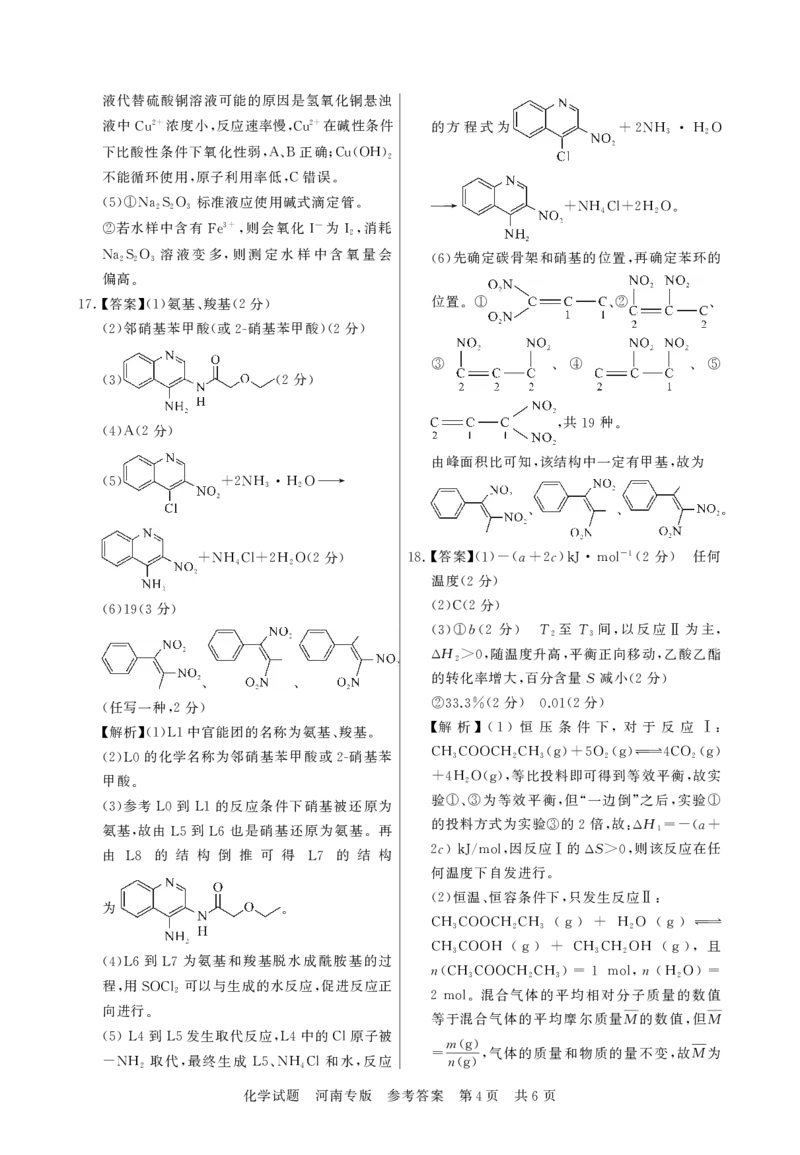
17.【答案】(1)氨基、羧基(2分)
(2)邻硝基苯甲酸(或2G硝基苯甲酸)(2分)
(3)
(2分)
(4)A(2分)
(5)
+2NH3H2O
→
+NH4Cl+2H2O(2分)
(6)19(3分)
、
、
(任写一种,2分)
【解析】(1)L1中官能团的名称为氨基、羧基.
(2)L0的化学名称为邻硝基苯甲酸或2G硝基苯
甲酸.
(3)参考L0到L1的反应条件下硝基被还原为
氨基,故由L5到L6也是硝基还原为氨基.再
由L8的结构倒推可得
L7的结构
为
.
(4)L6到L7为氨基和羧基脱水成酰胺基的过
程,用SOCl
2可以与生成的水反应,促进反应正
向进行.
(5)L4到L5发生取代反应,L4中的Cl原子被
-NH2取代,最终生成L5、NH4Cl和水,反应
的方程式为
+2NH3H2O
→
+NH4Cl+2H2O.
(6)先确定碳骨架和硝基的位置,再确定苯环的
位置.①
、②
、
③
、④
、⑤
,共19种.
由峰面积比可知,该结构中一定有甲基,故为
、
、
.
18.【答案】(1)-(a+2c)kJmol
-1(2分) 任何
温度(2分)
(2)C(2分)
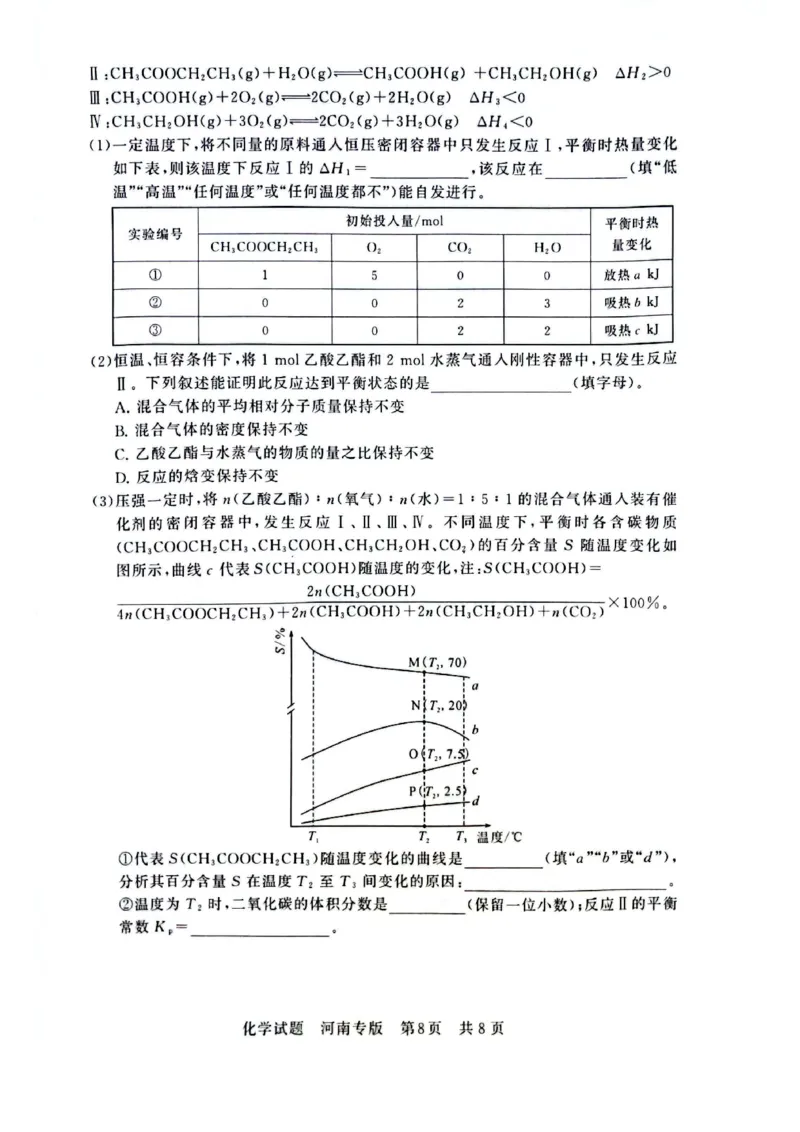
(3)①b(2分) T2至T3间,以反应Ⅱ为主,
ΔH2>0,随温度升高,平衡正向移动,乙酸乙酯
的转化率增大,百分含量S 减小(2分)
②33.
3%(2分) 0.
01(2分)
【解析】(1)恒压条件下,对于反应Ⅰ:
CH3COOCH2CH3(g)+5O2(g)
4CO2(g)
+4H2O(g),等比投料即可得到等效平衡,故实
验①、③为等效平衡,但“一边倒”之后,实验①
的投料方式为实验③的2倍,故:ΔH1=-(a+
2c)kJ/mol,因反应Ⅰ的ΔS>0,则该反应在任
何温度下自发进行.
(2)恒温、恒容条件下,只发生反应Ⅱ:
CH3COOCH2CH3(g) +H2O (g)
CH3COOH (g) +CH3CH2OH (g), 且
n(CH3COOCH2CH3)=1mol,n (H2O)=
2mol.混合气体的平均相对分子质量的数值
等于混合气体的平均摩尔质量M 的数值,但M
=m(g)
n(g),气体的质量和物质的量不变,故M 为
化学试题 河南专版 参考答案 第5
页 共6页
恒量,不能说明反应达平衡状态,A 错误;混合
气体的密度ρ=m(g)
V(g),气体的质量和体积不变,
故ρ 为恒量,不能说明反应达平衡状态,B 错
误;乙酸乙酯、水蒸气初始量为1mol、2mol,而
两物质以1∶1反应,故乙酸乙酯与水蒸气的物
质的量之比保持不变,能说明反应已达平衡状
态,C正确;反应的焓变与是否平衡无关,故不
能说明反应已达平衡状态,D 错误.
(3)①反应Ⅰ的ΔH1<0,反应Ⅱ的ΔH2>0,温度升
高,反应Ⅰ的平衡逆移,S(CH3COOCH2CH3)减小,
反应Ⅱ的平衡正移,S(CH3COOCH2CH3)增
大,故S(CH3COOCH2CH3)受两个反应共同
影响,故代表S(CH3COOCH2CH3)随温度的
变化曲线为b,且其百分含量S 在温度T2至
T3间变化的原因为:T2至T3,以反应Ⅱ为主,
ΔH2>0,随温度升高,平衡正向移动,乙酸乙酯
的转化率增大,S 减小.
②温度为T2时,a 代表S(CO2)随温度的变化
曲线,设投入了1mol乙酸乙酯,故
n(CO2)=4×1×70%
1
=2.
8mol,
n(CH2COOCH2CH3)=4×1×20%
4
=0.
2mol,
n(CH3COOH)=4×1×7.
5%
2
=0.
15mol,
n(C2H5OH)=4×1×2.
5%
2
=0.
05mol.
由三段式法可得:
CH3COOCH2CH3(g)+H2O(g)
CH3COOH(g)+C2H5OH(g)
始 1 1 O O
Δn 0.
8 0.
8 0.
8 0.
8
平 0.
2 3.
75 0.
15 0.
05
CH3COOH(g)+2O2(g)
2CO2(g)+2H2O(g)
始 0 5 0 1
Δn 0.
65 1.
3 1.
3 1.
3
平 0.
15 1.
45 2.
8 3.
75
CH3CH2OH(g)+3O2(g)
2CO2(g)+3H2O(g)
始 0 5 0 1
Δn 0.
75 2.
25 1.
5 2.
25
平 0.
05 1.
45 2.
8 3.
75
n(总)=0.
2+3.
75+0.
15+0.
05+1.
45+2.
8=
8.
4mol,
CO2的体积分数是2.
8
8.
4×100%≈33.
3%;
反应Ⅱ的平衡常数Kp=0.
15×0.
05
0.
2×3.
75=0.
01.
化学试题 河南专版 参考答案 第6
页 共6页
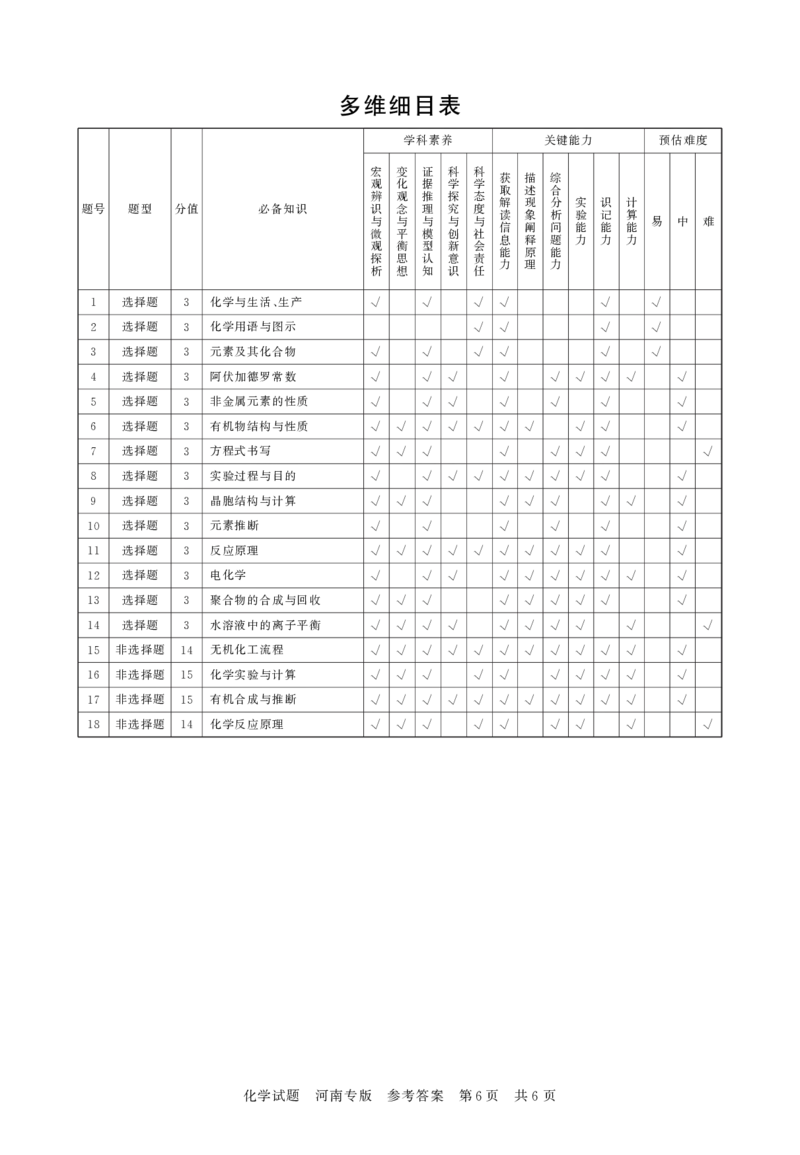
多维细目表
题号
题型
分值
必备知识
学科素养
关键能力
预估难度
宏
观
辨
识
与
微
观
探
析
变
化
观
念
与
平
衡
思
想
证
据
推
理
与
模
型
认
知
科
学
探
究
与
创
新
意
识
科
学
态
度
与
社
会
责
任
获
取
解
读
信
息
能
力
描
述
现
象
阐
释
原
理
综
合
分
析
问
题
能
力
实
验
能
力
识
记
能
力
计
算
能
力
易
中
难
1
选择题
3
化学与生活、生产
√
√
√
√
√
√
2
选择题
3
化学用语与图示
√
√
√
√
3
选择题
3
元素及其化合物
√
√
√
√
√
√
4
选择题
3
阿伏加德罗常数
√
√
√
√
√
√
√
√
√
5
选择题
3
非金属元素的性质
√
√
√
√
√
√
√
6
选择题
3
有机物结构与性质
√
√
√
√
√
√
√
√
√
√
7
选择题
3
方程式书写
√
√
√
√
√
√
√
√
8
选择题
3
实验过程与目的
√
√
√
√
√
√
√
√
√
√
9
选择题
3
晶胞结构与计算
√
√
√
√
√
√
√
√
√
10
选择题
3
元素推断
√
√
√
√
√
√
11
选择题
3
反应原理
√
√
√
√
√
√
√
√
√
√
√
12
选择题
3
电化学
√
√
√
√
√
√
√
√
√
√
13
选择题
3
聚合物的合成与回收
√
√
√
√
√
√
√
√
√
14
选择题
3
水溶液中的离子平衡
√
√
√
√
√
√
√
√
√
√
15
非选择题
14
无机化工流程
√
√
√
√
√
√
√
√
√
√
√
√
16
非选择题
15
化学实验与计算
√
√
√
√
√
√
√
√
√
√
17
非选择题
15
有机合成与推断
√
√
√
√
√
√
√
√
√
√
√
√
18
非选择题
14
化学反应原理
√
√
√
√
√
√
√
√
√