文档内容
让更多的孩子得到更好的教育
中考总复习:混合物的去杂分离提纯物质制备解题技巧(基础)
撰稿:李伟 审稿:熊亚军
【考纲要求】
1.了解混合物提纯的基本原理,能根据物质的物理、化学性质确定分离方法。
2.掌握过滤、蒸发等方法对混合物进行分离;了解粗盐提纯等固体混合物分离的方法和过程。
3.了解气体混合物的净化、干燥、收集、尾气处理的流程。
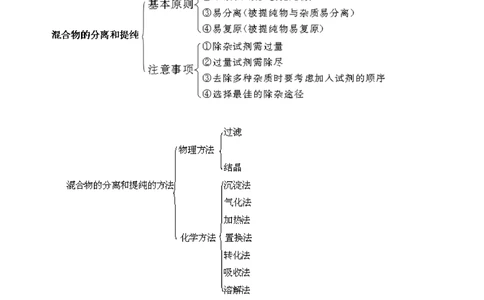
【知识网络】
【考点梳理】
考点一、物质分离和提纯的方法(高清课堂《物质的检验、分离和提纯》一)
1.物理方法:
方法 适用范围或原理 举例
①固体与液体混合物的分离 粗盐的提纯
过滤法
②可溶性固体与不溶性固体混合物的分离
物
理 ①分离溶质与溶剂 从含有 HCl 的 NaCl 溶液中
方 结 蒸发 ②除去易挥发的杂质 分离出固体NaCl
晶
法
法 降低温度 可溶性固体溶质溶解度受温度影响变化大 分离NaCl与KNO 3 的混合物
小不同
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共8页让更多的孩子得到更好的教育
(1)过滤:把不溶性的固体与液体分开的一种方法叫过滤。
①过滤器的准备(如图甲):取一张圆形滤纸,对折两次,然后打开,使滤纸成为圆锥形(一边是一层滤纸,
另一边是三层滤纸),放入漏斗内,使之紧帖漏斗壁,用少量水润湿滤纸使滤纸和漏斗壁之间不要留有气
泡。
甲 乙
②安装过滤器(如图乙):使漏斗的下端管口紧靠烧杯内壁。
③过滤操作:将浑浊的液体混合均匀后,沿玻璃棒慢慢倒入漏斗内进行过滤。
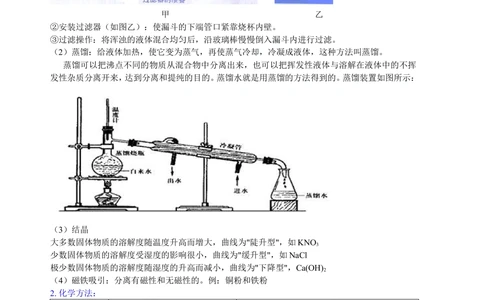
(2)蒸馏:给液体加热,使它变为蒸气,再使蒸气冷却,冷凝成液体,这种方法叫蒸馏。
蒸馏可以把沸点不同的物质从混合物中分离出来,也可以把挥发性液体与溶解在液体中的不挥
发性杂质分离开来,达到分离和提纯的目的。蒸馏水就是用蒸馏的方法得到的。蒸馏装置如图所示:
(3)结晶
大多数固体物质的溶解度随温度升高而增大,曲线为"陡升型",如KNO
3
少数固体物质的溶解度受湿度的影响很小,曲线为"缓升型",如NaCl
极少数固体物质的溶解度随湿度的升高而减小,曲线为"下降型",Ca(OH)
2
(4)磁铁吸引:分离有磁性和无磁性的。例:铜粉和铁粉
2. 化学方法:
方法 适用范围或原理 举例
除 NaSO 中 NaCO ,可加适量稀 HSO :
化气法 与杂质反应生成气体而除去 2 4 2 3 2 4
NaCO+ H SO =NaSO + CO↑+ H O
2 3 2 4 2 4 2 2
除去NaCl中的NaSO ,可加适量的 BaCl :
沉淀法 将杂质转化为沉淀过滤除去 2 4 2
NaSO + BaCl ==BaSO ↓+2NaCl
化 2 4 2 4
学 置换法 将杂质通过置换反应而除去 除FeSO 4 中的CuSO 4 ,可加过量的铁粉,再过
方 滤:CuSO +Fe==Cu+Fe SO
4 4
法 除C粉中的CuO粉,可加适量稀硫酸,再过滤:
溶解法 将杂质溶于某种试剂而除去
CuO+ H SO ==CuSO + H O
2 4 4 2
杂质受热易分解,通过加热将杂 除CaO中的CaCO 3 可加热:
加热法
质除去 CaCO CaO+ CO ↑
3 2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共8页让更多的孩子得到更好的教育
将杂质通过化学反应转化为主 除CO 2 中的CO,可将气体通过灼热的CuO:
转化法
要成分 CO+CuO Cu+CO
2
【要点诠释】
1. 过滤的操作要点是“一贴,二低,三靠”:
一贴:制作过滤器时,滤纸要紧贴漏斗内壁(中间不要留有气泡,否则会影响过滤速度)。
二低:(1)滤纸边缘低于漏斗边缘;(2)过滤器中液面低于滤纸边缘(否则,液体就会从滤纸和漏斗壁之间
流下,达不到过滤的目的)。
三靠:(1)盛待过滤液的烧杯口要紧靠玻璃棒,使液体沿玻璃棒流入过滤器;(2)玻璃棒下端轻轻斜靠在
三层滤纸的一边,以免弄破滤纸;(3)漏斗下端要紧靠在下面烧杯的内壁,使滤液沿烧杯壁流下(否则滤
液会向四周飞溅,而且影响过滤的速度)。
2.粗盐的提纯
(1)粗盐是含有较多杂质的氯化钠晶体。通过晾晒海水或煮盐井水、盐湖水而得到的粗盐中含有较多的可
溶性杂质(氯化镁、氯化钙、硫酸镁等)和不溶性杂质(泥沙等)。可以通过溶解、过滤、蒸发、结晶等步骤来
制取精盐。
(2)粗盐提纯的步骤:
①溶解:用托盘天平称取5.0g粗盐,用量筒量取10mL水,用药匙将粗盐逐渐加入盛有10mL水的烧杯里,
边加边用玻璃棒搅拌,加到不再溶解为止。
②过滤:过滤食盐水。
③蒸发:将澄清的滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多的固体时停止加热,利用
蒸发皿的余热使滤液蒸干。
④计算产率:用玻璃棒把氯化钠固体转移到纸上,称量,计算产率。
考点二、气体的净化与干燥
1.气体净化的几种方法
(1)吸收法:用吸收剂将杂质气体吸收除去。如,除去CO中混有的少量CO,可先用浓NaOH溶液吸收
2
CO,再用浓硫酸等干燥剂除去水蒸气。
2
常见气体吸收剂见下表:
吸收剂 吸收的气体杂质 吸收剂 吸收的气体杂质
水 可溶性气体:HCl、NH 等 NaOH固体 CO、HCl、HO
3 2 2
无水CuSO HO 碱石灰 CO、HCl、HO
4 2 2 2
灼热的铜网 O NaOH溶液 CO、HCl
2 2
灼热的CuO H、CO 浓硫酸 HO
2 2
(2)转化法:通过化学反应,将杂质气体转化为所要得到的气体。如,除去CO 中的少量CO,可将混合气
2
体通过足量的灼热CuO,CO + CuO Cu + CO 。
2
2.气体的干燥
气体的干燥是通过干燥剂来实现的,选择干燥要根据气体的性质,一般原则是:酸性干燥剂不能用来
干燥碱性气体,碱性干燥剂不能用来干燥酸性气体,干燥装置由干燥剂状态决定。
(1)常见的干燥剂
干燥剂 干燥
可干燥气体 不可干燥气体
名称或化学式 酸碱性 状态 装置
H、N、O、CO、
浓HSO 酸性 液态 2 2 2 2 NH A
2 4 HCl、CH、CO等 3
4
固体NaOH H、O、N、CH、
碱性 固态 2 2 2 4 CO、SO 、HCl B或C
生石灰 CO、NH 等 2 2
3
无水CaCl 中性 固态 除NH 外所有气体 NH B或C
2 3 3
(2)常用干燥装置如下:
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共8页让更多的孩子得到更好的教育
【要点诠释】
选择吸收装置时,要注意进、出气体导管的连接方法,若用“洗气瓶”,要注意“长进短出”,若用干燥
管要注意“大进小出”。先除去气体中含有的其他杂质,干燥除去水蒸气的操作放在最后。
【典型例题】
类型一、考查物质的分离、除杂和提纯
1. (2012广东)选择一种试剂(适量)除去下列括号中的杂质(填化学式):
(1)铜粉(锌粉)_______________;
(2)二氧化碳(一氧化碳)_______________;
(3)盐酸(硫酸)_______________;
(4)硝酸亚铁(硝酸银)_______________。
【思路点拨】一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;
②反应时不能引入新的杂质。
【答案】 (1)HCl或HSO (2)灼热的CuO
2 4
(3)BaCl (4)Fe
2
【解析】(1)铜粉与稀盐酸或稀硫酸不反应,锌粉与稀盐酸或稀硫酸反应,过滤即可;(2)二氧化碳(一氧
化碳)中的杂质一氧化碳可以用加热的氧化铜除去,二氧化碳与氧化铜不反应;(3)盐酸(硫酸)中的杂质
硫酸可以用氯化钡除去,硫酸与氯化钡反应生成硫酸钡白色沉淀和盐酸,过滤即可;(4)硝酸亚铁(硝酸
银)中的杂质硝酸银可以用铁粉除去,铁和硝酸银反应生成硝酸亚铁和银,过滤即可。
【总结升华】加强记忆除去常用离子的方法和物质的溶解性是解答本题的关键。
2.下列做法正确的是(
)
A.加入适量的氢氧化钡溶液以除去NaCl溶液中的少量NaSO
2 4
B.加入适量的碳酸钙粉末以除去CaCl 溶液中的少量盐酸
2
C.用点燃的方法除去CO 中混有的少量CO
2
D.用氢氧化钠(或氢氧化钙等)
溶液处理硫在氧气中燃烧产生的气体
【思路点拨】碳酸根离子会与氢离子反应生成水和二氧化碳;二氧化碳不具有可燃性、助燃性;硫燃烧会生
成二氧化硫。
【答案】 B
【解析】氢氧化钡和硫酸钠反应生成了硫酸钡沉淀和氢氧化钠,过滤可以将硫酸钡除去,但是氢氧化钠对
于氯化钠也是杂质;盐酸和碳酸钙反应会生成氯化钙、水和二氧化碳;一氧化碳和二氧化碳是均匀的分布
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共8页让更多的孩子得到更好的教育
在一起的,一氧化碳的周围有二氧化碳,不能被点燃;硫在氧气中燃烧产生的二氧化硫属于酸性氧化物,
要用碱液进行吸收。
【总结升华】在对物质进行除杂质时,首先分析杂质和物质的性质,然后选择合适的试剂(只与杂质反应,
且还不会引入新的难以分离的杂质)。
3. (2012淄博)除去下列物质中混有的少量杂质,所选用的试剂及操作方法正确的是( )
序号 物 质 杂质(少量) 试剂和操作方法
A Fe O Fe 加入足量稀盐酸
2 3
B NaOH溶液 NaCO 溶液、 加入适量澄清的石灰水,过滤
2 3
C CaCO CaO 高温煅烧
3
D Cu(NO ) 溶液 AgNO 溶液 加入足量铁粉,过滤
3 2 3
【思路点拨】除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后
不能引入新的难以分离的杂质。
【答案】 B
【解析】A中Fe和Fe O 均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则; B
2 3
中NaCO 溶液能与石灰水反应生成碳酸钙沉淀和氢氧化钠,再过滤除去不溶物,能除去杂质且没有引入
2 3
新的杂质,符合除杂原则;C中碳酸钙高温下分解生成氧化钙和二氧化碳,高温下煅烧反而会把原物质除
去,不符合除杂原则;D中Cu(NO )溶液和AgNO 溶液均能与铁粉反应,不但能把杂质除去,也会把原
3 2 3
物质除去,不符合除杂原则。
【总结升华】记住常用的物质分离、除杂的方法,根据物质的性质选择合适的反应。
4. (2012遵义)要除去下列四种物质中的少量杂质(括号内的物质为杂质)
甲:CaCO (KCl) 乙:NaSO (CuSO ) 丙:KCl(KOH) 丁:碳粉(CuO)
3 2 4 4
可选用的试剂及操作方法有:①加适量水,搅拌,过滤;②加过量稀HSO ,过滤;③溶解后加适量KOH溶
2 4
液,过滤;④溶解后加适量盐酸,蒸发;⑤加热(或高温灼烧)。下列组合中正确的是( )
A.甲-⑤ B.乙-③ C.丙-④ D.丁-①
【思路点拨】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,
同时被提纯物质不得改变。
【答案】 C
【解析】甲:KCl易溶于水,CaCO 难溶于水,可采取加水溶解、过滤的方法进行分离除杂;乙:除去NaSO
3 2 4
中的CuSO ,为除去杂质且没有引入新的杂质,可选用适量的氢氧化钠溶液,再过滤除去沉淀,若选用
4
KOH溶液会引入新的杂质硫酸钾;丙:KOH能与盐酸反应生成氯化钾和水,再蒸发,能除去杂质且没有
引入新的杂质;丁:CuO能与稀硫酸反应生成硫酸铜和水,碳粉不与稀硫酸反应,再过滤即可得到碳粉,
能除去杂质且没有引入新的杂质。
【总结升华】解决除杂问题时,抓住除杂质的必需条件:加入的试剂只与杂质反应,反应后不能引入新的杂
质。
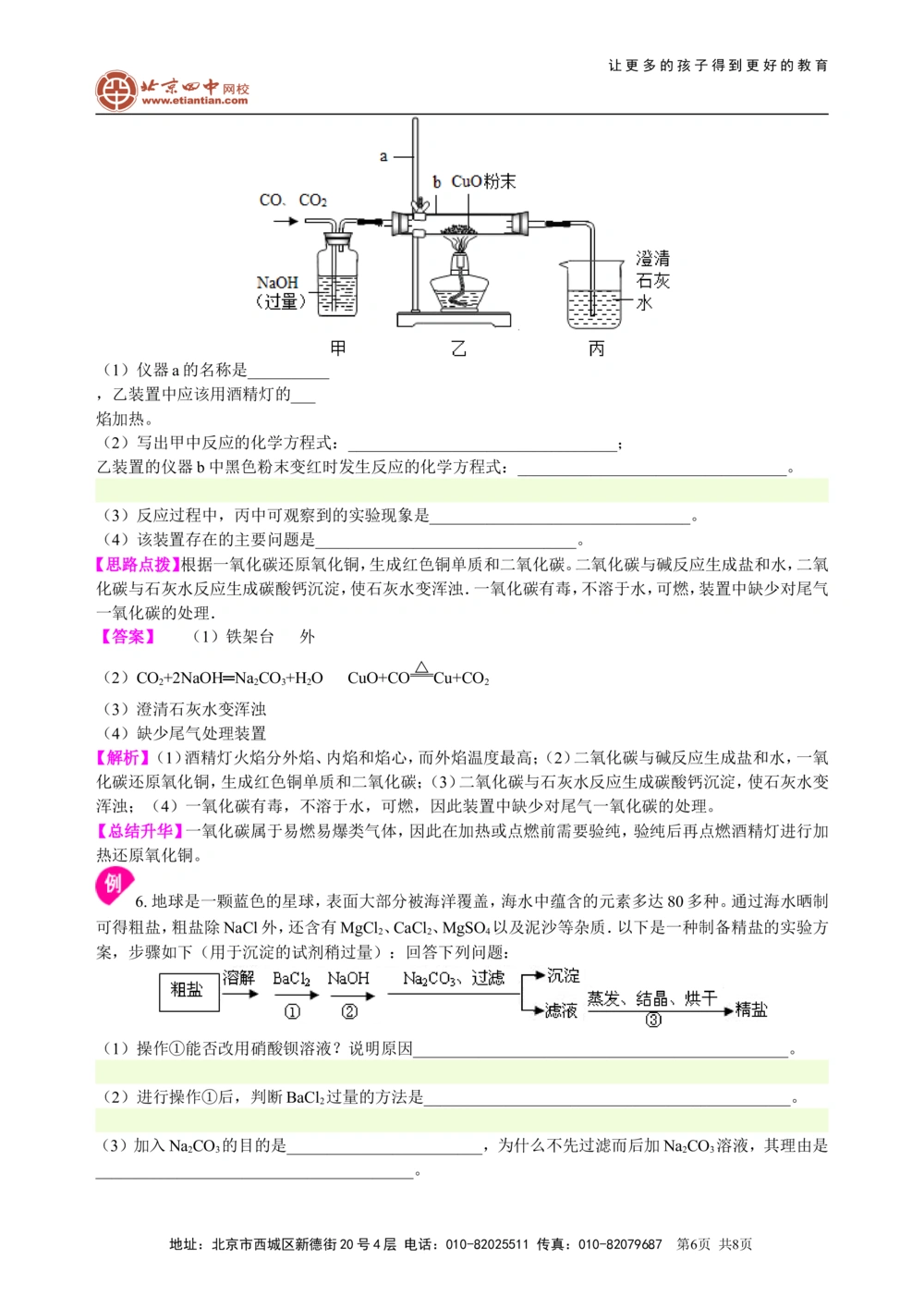
5. 如图是利用CO、CO 混合气体中的CO还原CuO的实验示意图。
2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共8页让更多的孩子得到更好的教育
(1)仪器a的名称是__________
,乙装置中应该用酒精灯的___
焰加热。
(2)写出甲中反应的化学方程式:_________________________________;
乙装置的仪器b中黑色粉末变红时发生反应的化学方程式:_________________________________。
(3)反应过程中,丙中可观察到的实验现象是________________________________。
(4)该装置存在的主要问题是________________________________。
【思路点拨】根据一氧化碳还原氧化铜,生成红色铜单质和二氧化碳。二氧化碳与碱反应生成盐和水,二氧
化碳与石灰水反应生成碳酸钙沉淀,使石灰水变浑浊.一氧化碳有毒,不溶于水,可燃,装置中缺少对尾气
一氧化碳的处理.
【答案】 (1)铁架台 外
△
(2)CO+2NaOH═Na CO+H O CuO+CO Cu+CO
2 2 3 2 2
(3)澄清石灰水变浑浊
(4)缺少尾气处理装置
【解析】(1)酒精灯火焰分外焰、内焰和焰心,而外焰温度最高;(2)二氧化碳与碱反应生成盐和水,一氧
化碳还原氧化铜,生成红色铜单质和二氧化碳;(3)二氧化碳与石灰水反应生成碳酸钙沉淀,使石灰水变
浑浊;(4)一氧化碳有毒,不溶于水,可燃,因此装置中缺少对尾气一氧化碳的处理。
【总结升华】一氧化碳属于易燃易爆类气体,因此在加热或点燃前需要验纯,验纯后再点燃酒精灯进行加
热还原氧化铜。
6. 地球是一颗蓝色的星球,表面大部分被海洋覆盖,海水中蕴含的元素多达80多种。通过海水晒制
可得粗盐,粗盐除NaCl外,还含有MgCl 、CaCl 、MgSO 以及泥沙等杂质.以下是一种制备精盐的实验方
2 2 4
案,步骤如下(用于沉淀的试剂稍过量):回答下列问题:
(1)操作①能否改用硝酸钡溶液?说明原因______________________________________________。
(2)进行操作①后,判断BaCl 过量的方法是_____________________________________________。
2
(3)加入NaCO 的目的是________________________,为什么不先过滤而后加NaCO 溶液,其理由是
2 3 2 3
_______________________________________。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共8页让更多的孩子得到更好的教育
(4)滤液的主要成分有_______________________
,实验方案尚需完善,具体步骤是___________________________________________________。
【思路点拨】可以根据物质的性质方面进行分析、判断,从而得出正确的结论。例如最后的滤液中含有
NaCl、NaOH、NaCO 等物质,需要把氢氧化钠和碳酸钠除去,可以向溶液中加入适量的稀盐酸。
2 3
【答案】 (1)否 因为引入新的杂质离子NO -
3
(2)取少量上层清液,滴加NaSO 溶液,如有白色沉淀出现则说明BaCl 过量
2 4 2
(3)除去Ca2+、Ba2+ 一次过滤,简化实验步骤
(4)NaCl、NaOH、NaCO 向滤液中加入适量的稀盐酸以除去氢氧化钠和碳酸钠
2 3
【解析】(1)不能改用硝酸钡溶液,因为硝酸根会进入溶液中,从而引入了新的杂质。(2)判断BaCl 过量
2
的方法是:取少量上层清液,滴加NaSO 溶液,若有白色沉淀出现则说明BaCl 过量。(3)加入NaCO 的
2 4 2 2 3
目的是除去Ca2+、Ba2+,因为碳酸根能和钙离子、钡离子结合生成碳酸钙和碳酸钡两种沉淀;不先过滤而后
加NaCO 溶液,其理由是:一次过滤,简化实验步骤。(4)除杂试剂需过量,因此滤液中的主要成分有:
2 3
NaCl、NaOH、NaCO,最后向滤液中加入适量的稀盐酸来除去氢氧化钠和碳酸钠。【总结升华】充分理解
2 3
各种物质的性质,只有这样才能对问题组成正确的判断。
举一反三:
【变式1】除去氯化钠溶液中混有的少量碳酸钠,应选用适量的试剂是( )
A.稀硫酸 B.稀盐酸 C.澄清石灰水 D.硝酸银溶液
【答案】 B
【解析】A中硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,硫酸钠对于氯化钠也是杂质;B中盐酸和碳酸
钠反应生成氯化钠、水和二氧化碳,蒸发后就只是氯化钠固体了;C中澄清石灰水和碳酸钠反应生成碳酸
钙沉淀和氢氧化钠,过滤可以将碳酸钙沉淀除去,但是氢氧化钠对于氯化钠也是杂质;D中硝酸银和氯化
钠、碳酸钠都会反应,这样杂质除去了,主要物质也除去了。
【变式2】要除掉粗盐中含有的氯化镁、硫酸镁等杂质。现设计一个除杂质的方案:把粗盐溶于水,过滤得
澄清溶液,再进行下列各步骤:①加入过量氯化钡溶液至沉淀完全;②用盐酸调节pH至溶液呈微酸性;③
加入过量NaOH溶液至沉淀完全;④过滤;⑤加入过量碳酸钠溶液至沉淀完全;最后蒸发浓缩使NaCl晶
体析出,则对上述各处理步骤的顺序安排合理的是( )
A.③①⑤④② B. ①②③④⑤
C. ②①③④⑤ D. ②③⑤④①
【答案】 A
【解析】首先加入NaOH溶液至沉淀(生成氢氧化镁而除去镁离子)完全;然后加入氯化钡溶液至沉淀(生
成硫酸钡而除去硫酸根离子)完全;接着加入碳酸钠溶液至沉淀(生成碳酸钡而除去钡离子)完全,过滤后
用盐酸调节pH至溶液呈微酸性(在此过程中同时也将过量的氢氧化钠和碳酸钠溶液均反应掉并转化为
了氯化钠),最后蒸发浓缩使NaCl晶体析出。
【变式3】除去下列物质中混入的少量杂质(括号中的物质为杂质)所设计的实验方案或操作中,合理的是
( )
A.KNO 晶体(NaCl):将固体溶于水配制成热的饱和溶液,采用降温结晶的方法
3
B.CO 气体(HCl):将气体通过装有NaOH溶液的洗气瓶
2
C.BaCl 溶液[Ba(OH)]:加入适量的稀硫酸,过滤
2 2
D.O(N):将混合气体通过炽热的铜网
2 2
【答案】 A
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共8页让更多的孩子得到更好的教育
【解析】A中用冷却热播和溶液的方法可以除去KNO 晶体中的NaCl,因为硝酸钾的溶解度受温度影响大,
3
氯化钠的溶解度受温度影响小; B中CO 气体(HCl):将气体通过装有NaOH溶液的洗气瓶会把二氧化
2
碳也除去; C中氯化钡和氢氧化钡都能和稀硫酸反应,会把原物质除去; D中将混合气体通过炽热的铜
网,氧气和铜反应,会把原物质除去。
【变式4】氮气中混有少量氢气、二氧化碳和水蒸气,欲获得干燥纯净的氮气,可采用下列操作:①通过浓
硫酸;②通过填充氧化铜的加热管;③通过氢氧化钠溶液;④通过浓盐酸。最好的组合顺序是( )
A.①→②→③ B.③→②→④ C.③→②→① D.④→②→③
【答案】 C
【解析】气体的除杂一般把干燥装置放在最后。①是干燥作用②是除去氢气③是除去二氧化碳。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第8页 共8页