文档内容
让更多的孩子得到更好的教育
中考总复习:混合物的去杂分离提纯物质制备解题技巧(基础)
撰稿:李伟 审稿:熊亚军
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
1.下列各混合物能通过过滤的方法将两种物质分离的是( )
A. 牛奶和水 B. 酱油和水
C. 食盐晶体和饱和食盐水 D. 盐酸和硫酸
2.下列仪器可用于分离物质的有( )
①托盘天平;②干燥管;③集气瓶;④漏斗;⑤洗气瓶;⑥U形管;⑦胶头滴管;⑧水槽;⑨量筒。
A.②④⑤⑥ B. ①②④⑤⑧
C. ①③④⑧ D. ②④⑤⑦⑨
3.能用重结晶法分离的一组混合物是( )
A. NaCl和KNO B. KCl和MnO
3 2
C. BaCO 和BaSO D. KCl和AgCl
3 4
4.要除去下列物质中混有的少量杂质(括号内为杂质),所用的试剂和主要操作都正确的是( )
A.KC(l KClO) 加少量MnO 粉末,加热
3 2
B.Fe粉(Cu粉) 加足量CuSO 溶液,过滤
4
C.NaC(l NaCO) 加适量稀硫酸,蒸发结晶
2 3
D.稀HNO(HSO ) 加适量Ba(NO ) 溶液,过滤
3 2 4 3 2
5.除去下列物质中的杂质,所用的试剂和方法不正确的是( )
A.除去二氧化碳中混有的一氧化碳可以用点燃的方法
B.除去氯化钾中混有的二氧化锰可以用溶解、过滤、蒸发的方法
C.除去铜粉中混有的锌粉可以用加入过量的稀盐酸、过滤、洗涤、烘干的方法
D.除去生石灰中混有的碳酸钙可以用高温煅烧的方法
6.(2012梧州)除去下列物质中所含少量杂质(括号内为杂质)的方法正确的是( )
A.NaCl(泥沙)——溶解、过滤、蒸发
B.FeCl 溶液(CuCl )——加入金属锌,过滤
2 2
C.CaO(CaCO )——加入足量的稀盐酸,过滤
3
D.Fe粉(Cu粉)——加入足量的稀硫酸,过滤
7.除去下列物质中所含杂质,括号内的除杂剂不正确的是( )
A.KOH溶液中混有KCO(稀盐酸)
2 3
B.NaNO 溶液中混有AgNO(适量NaCl溶液)
3 3
C.Cu粉中混有铁粉(稀硫酸)
D.氧气中混有水蒸气(生石灰)
8.下列各组括号内除杂质的方法或试剂错误的是( )
A. CaO中混有CaCO (稀盐酸) B. NaNO 溶液中混有NaCl(AgNO 溶液)
3 3 3
C. C粉中混有CuO(稀硫酸) D. Cu粉中混有铁粉(用磁铁吸引)
9.某溶液中含有Ba2+、Cu2+、Ag+,可用①NaSO 溶液、②NaOH溶液、③盐酸三种试剂将它们一一沉淀加
2 4
以分离。则加入试剂的正确顺序为( )
A. ①②③ B. ②①③
C. ②③① D. ③①②
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共5页让更多的孩子得到更好的教育
10. 下列除去杂质的方法正确的是( )
A.除去CaO中的少量CaCO :加入足量的稀盐酸,充分反应
3
B.除去Cu(NO ) 溶液中的少量AgNO:加入足量铜粉,充分反应后过滤
3 2 3
C.除去KCl溶液中的少量MgCl :加入适量NaOH溶液,过滤
2
D.除去N 中的少量O:通过灼热的CuO粉末,收集气体
2 2
11.分离下列混合物时所采用的操作方法对应正确的是( )
①从食盐水中分离出NaCl;②从NaCO 和CaCO 的混合物中分离出CaCO ;③从KCl和MnO 的混合物
2 3 3 3 2
中分离出KCl;④从KNO 和NaCl的混合物中分离出KNO。
3 3
a.溶解过滤 b.加热分解 c.蒸发结晶 d.降温结晶
A. c a a d B. c b a c C. a c a c D. a b c d
二、填空题
12.除去盐酸中混有的少量硫酸,应加入适量的_______
溶液。能将Ca(OH)、NaOH、稀HSO 三种溶液一次鉴别开来的试剂是________
2 2 4
,用稀硫酸除铁锈的化学方程式是_______________________。
13. 除去下列物质中的杂质,请把操作方法的序号填写在相应的空格内:
A、加适量水溶解、冷却、过滤; B、加水溶解、过滤、洗涤、干燥;
C、加适量盐酸、蒸发结晶; D、加适量水、过滤、蒸发结晶;
E、加适量稀盐酸、过滤; F、加适量水溶解、蒸发结晶、趁热过滤。
①碳酸钙中混有少量硝酸钾________
;②氯化钠中混有少量碳酸钠________
;③白糖中混有少量砂粒________
;④氯化钠中混有少量的硝酸钾________
;⑤硝酸钾中混有少量的氯化钠________
;⑥铜粉中混有铁粉________。
三、实验题
14.为除去氢氧化钠溶液中混有的少量碳酸钠,某化学兴趣小组设计了两个实验方案。
(1)方案一:往溶液中滴加稀盐酸至不再产生气体为止,所得溶液即为氢氧化钠溶液。该方案是否合理?
_______
,理由是_____________________________________。
(2)方案二:往溶液中滴加氯化钙溶液至不再产生沉淀为止,过滤,所得滤液即为氢氧化钠溶液。写出该
方案所涉及反应的化学方程式_______________________________。分析该方案是否合理?______
,理由是_____________________________________。
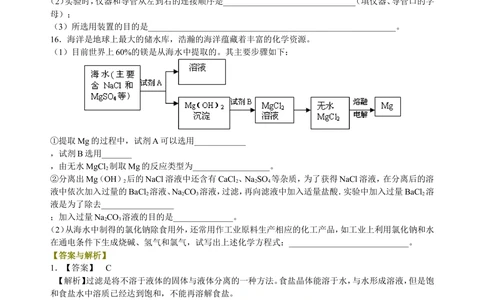
15.为了有效地除去二氧化碳气体中少量的水蒸气、氯化氢等气体杂质,制得干燥、纯净的二氧化碳气体,
请根据下图所示的装置、药品,回答下列问题:
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共5页让更多的孩子得到更好的教育
(1)写出实验室制备二氧化碳气体的化学方程式________________________________
;
(2)实验时,仪器和导管从左到右的连接顺序是_______________________________(填仪器、导管口的字
母);
(3)所选用装置的目的是__________________________________________________________。
16.海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源。
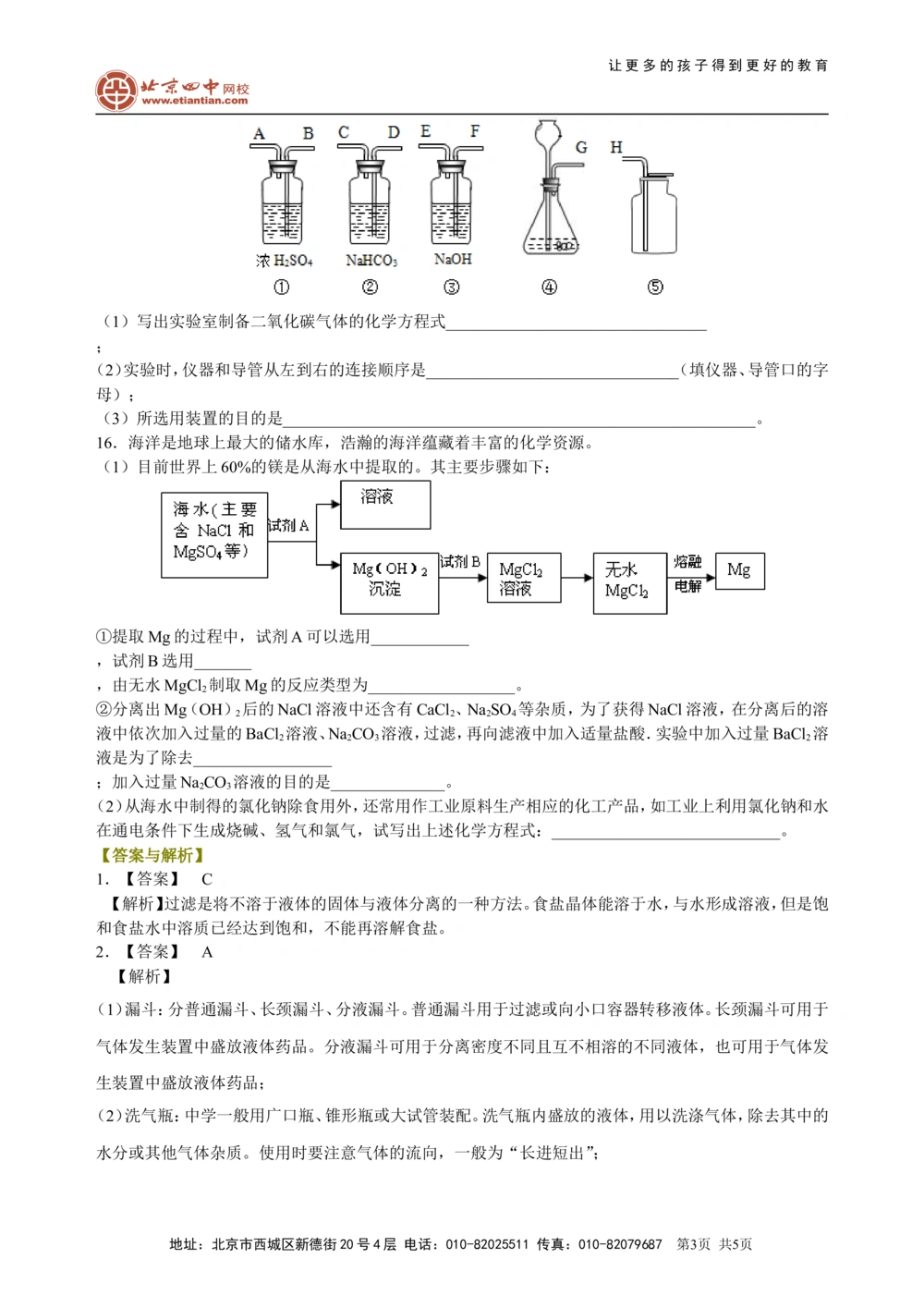
(1)目前世界上60%的镁是从海水中提取的。其主要步骤如下:
①提取Mg的过程中,试剂A可以选用____________
,试剂B选用_______
,由无水MgCl 制取Mg的反应类型为__________________。
2
②分离出Mg(OH)后的NaCl溶液中还含有CaCl 、NaSO 等杂质,为了获得NaCl溶液,在分离后的溶
2 2 2 4
液中依次加入过量的BaCl 溶液、NaCO 溶液,过滤,再向滤液中加入适量盐酸.实验中加入过量BaCl 溶
2 2 3 2
液是为了除去_________________
;加入过量NaCO 溶液的目的是______________。
2 3
(2)从海水中制得的氯化钠除食用外,还常用作工业原料生产相应的化工产品,如工业上利用氯化钠和水
在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:____________________________。
【答案与解析】
1.【答案】 C
【解析】过滤是将不溶于液体的固体与液体分离的一种方法。食盐晶体能溶于水,与水形成溶液,但是饱
和食盐水中溶质已经达到饱和,不能再溶解食盐。
2.【答案】 A
【解析】
(1)漏斗:分普通漏斗、长颈漏斗、分液漏斗。普通漏斗用于过滤或向小口容器转移液体。长颈漏斗可用于
气体发生装置中盛放液体药品。分液漏斗可用于分离密度不同且互不相溶的不同液体,也可用于气体发
生装置中盛放液体药品;
(2)洗气瓶:中学一般用广口瓶、锥形瓶或大试管装配。洗气瓶内盛放的液体,用以洗涤气体,除去其中的
水分或其他气体杂质。使用时要注意气体的流向,一般为“长进短出”;
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共5页让更多的孩子得到更好的教育
(3)干燥管:干燥管内盛放的固体,用以洗涤气体,除去其中的水分或其他气体杂质,也可以使用U型管。
3.【答案】 A
【解析】KNO 的溶解度随温度的变化较大,而NaCl的溶解度却随温度的变化较小,故可利用多次结晶
3
(即重结晶)的方法来提纯KNO。
3
4.【答案】 D
【解析】A中KC(l KClO),加少量MnO 粉末能除去氯酸钾杂质,但会引入二氧化锰杂质,操作中还应
3 2
加入溶解,过滤步骤;B中Fe粉(Cu粉),加足量CuSO 溶液后,铁粉能与硫酸铜反应,会把原物质除去;
4
C中NaCl(NaCO),稀硫酸和碳酸钠反应生成硫酸钠,硫酸钠对应氯化钠来说是新的杂质; D中稀
2 3
HNO(HSO ),加适量Ba(NO )溶液后生成硫酸钡沉淀和稀硝酸,过滤后得到硝酸,不会带入新的杂质。
3 2 4 3 2
5.【答案】 A
【解析】A中二氧化碳不能支持燃烧,所以在大量的二氧化碳中一氧化碳是不能燃烧的,所以难以通过
此方法除去一氧化碳;B中二氧化锰不溶于水,而氯化钾能够溶于水,所以可以通过溶解、过滤和蒸发的
方法来将氯化钾中的二氧化锰除去;C中铜不和盐酸反应但是锌可以和盐酸反应,所以通过用加入过量
的稀盐酸、过滤、洗涤、烘干的方法来除去铜粉中的锌粉; D中高温煅烧可以使碳酸钙分解产生氧化钙和
二氧化碳,二氧化碳是气体逸出,剩余的固体为氧化钙。
6.【答案】 A
【解析】A中氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂;B中金属
锌与FeCl 、CuCl 溶液均能发生反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则; C中
2 2
CaCO 、CaO均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则; D中Fe粉能
3
与稀硫酸反应,铜粉不能与稀硫酸反应,选用稀硫酸反而会把原物质除去,不符合除杂原则。
7.【答案】 A
【解析】A中KOH溶液中混有KCO,加入稀盐酸后,氢氧化钾和碳酸钾都会和盐酸发生反应,把主要
2 3
物质也除出去了;B中NaNO 溶液中混有AgNO,加入适量NaCl溶液能和硝酸银生成氯化银沉淀和硝酸
3 3
钠,不会带入新的杂质,方法正确;C中Cu粉中混有铁粉,加入稀硫酸能和铁粉反应,不和铜粉反应;D中
氧气中混有水蒸气,通过生石灰,生石灰能吸收水蒸气,不和氧气反应。
8.【答案】 A
【解析】除杂需遵循的原则:一、除去杂质;二、不能大量消耗被提纯物;三、不能产生其他不可分离的杂
质。题中所给盐酸与CaO和CaCO 都能反应,因此不符合。
3
9.【答案】 D
【解析】注意既然要将它们一一沉淀加以分离,那么所加试剂不能产生两种沉淀。因此先加盐酸使Ag+
生成氯化银沉淀;然后分别加硫酸钠和氢氧化钠除去钡离子、铜离子。
10.【答案】 B
【解析】N 和O 均不与CuO反应;CaO和CaCO 均与稀盐酸反应;MgCl 与NaOH反应生成了可溶性
2 2 3 2
的NaCl,引入了新的杂质。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共5页让更多的孩子得到更好的教育
11.【答案】 A
【解析】从题目所给定的几种物质中,NaCO、KCl、KNO、NaCl均可溶,而CaCO 和MnO 不溶于水,
2 3 3 3 2
因此分离NaCO 与CaCO 、KCl与MnO 时均可采用过滤方法;由于KNO 和NaCl均可溶,但它们的溶
2 3 3 2 3
解度受温度变化的影响不相同,故可用降温结晶的方法进行分离。
12.【答案】BaCl Na CO Fe O+3H SO ═Fe (SO )+3H O
2 2 3 2 3 2 4 2 4 3 2
【解析】杂质为硫酸,只有硫酸根离子是杂质,可以用钡离子除去,盐酸中有氯离子,因此要用氯化钡;
当加入碳酸钠时,有沉淀生成的是氢氧化钙,有气体生成的是硫酸,无明显现象的是氢氧化钠。
13.【答案】①B ②C ③D ④F ⑤A ⑥E
【解析】①碳酸钙不溶于水,硝酸钾易溶于水;②碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
③白糖易溶于水,沙粒不溶于水.可以通过过滤除去;④氯化钠的溶解度受温度变化影响小,硝酸钾的溶
解度受温度变化影响大;⑤氯化钠的溶解度受温度变化影响小,硝酸钾的溶解度受温度变化影响大;⑥铁
能和稀盐酸反应,铜不能和稀盐酸反应。
14.【答案】 (1)不合理 氢氧化钠也会与稀盐酸反应(或所得溶液为氯化钠溶液)
(2)CaCl +Na CO═CaCO↓+2NaCl 不合理 反应生成的NaCl是新的杂质
2 2 3 3
【解析】(1)方案一:稀盐酸与氢氧化钠、碳酸钠均能发生化学反应,不但能把杂质除去,也会把原物
质除去,不符合除杂原则。
(2)方案二:氯化钙溶液能与碳酸钠反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为
CaCl +Na CO═CaCO↓+2NaCl;该反应能除去杂质但引入了新的杂质氯化钠,不符合除杂原则。
2 2 3 3
15.【答案】 (1)CaCO +2HCl=CaCl +CO ↑+H O (2)G→D→C→B→A→H
3 2 2 2
(3)④是二氧化碳的制取装置 ②是除HCl的装置
①是除水蒸气的装置 ⑤是收集二氧化碳的装置
【解析】结合题目要求和所给装置,可以看出整个操作流程是:④装置用来制取CO;装置②来吸收
2
HCl气体;装置①来干燥CO;装置⑤来收集纯净、干燥的CO。
2 2
16.【答案】 (1)①氢氧化钙溶液 稀盐酸 分解反应
②NaSO 除去CaCl 和BaCl
2 4 2 2
(2)2NaCl+2H O 2NaOH+H ↑+Cl↑
2 2 2
【解析】(1)①氢氧化钙溶都能把镁离子转化成沉淀,稀盐酸和氢氧化镁反应生成氯化镁和水,由无水
MgCl 制取Mg的方法是电解熔化的氯化镁生成镁和氯气,属于分解反应;②加入过量BaCl 溶液是为了
2 2
除去硫酸钠,加入过量NaCO 溶液的目的是除去氯化钙和氯化钡;(2)氯化钠和水在通电条件下生成烧
2 3
碱、氢气和氯气,注意要配平及书写气体符号。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共5页