文档内容
姓名 准考证号
干冰晶体和冰晶体的晶胞结构相同
秘密 启用前 C.
★
1s 2s 2p
基态 原子的电子轨道表示式 违背了洪特规则
D. C
化学实验必须树立安全意识。下列说法错误的是
化 学 3.
金属钠着火时,应使用干燥的沙土扑灭
A.
能相互反应产生有毒气体的废液,不得倒入同一收集桶中
B.
若不慎将苯酚沾到皮肤上,应立即用 溶液清洗
C. NaOH
注意事项:
体积分数为 的酒精免洗消毒喷雾存放处应张贴 警示标识
答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。 D. 75%
1.
设N 为阿伏加德罗常数的值。下列说法正确的是
全部答案在答题卡上完成,答在本试题上无效。 4. A
2.
标准状况下, 和 在密闭容器中混合,容器内气体分子数为N
回答选择题时,选出每小题答案后,用 铅笔把答题卡上对应题目的答案标号 A. 22.4LNO 11.2LO2 A
3. 2B
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用 ( )与 ( )的混合物中所含共价键数为 N
B.32gS8 S6 2 A
黑色笔迹签字笔写在答题卡上。 标准状况下, 通入水中,溶液中氯离子数为 N
0.5mm C. 11.2LCl2 0.5 A
考试结束后,将本试题和答题卡一并交回。 和 充分反应,反应后 键的数目为 N
4. D.1molC2H6 1molCl2 σ 8 A
可能用到的相对原子质量: 劳动人民的发明创造是中华优秀传统文化的组成部分。下列劳动项目对应的化学知
H1 C12 O16 F19 P31 S32 Ti48 Zn65 Co59 5.
识描述错误的是
选项 劳动项目 化学知识
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只有一 用明矾净水 明矾具有强氧化性,能杀菌消毒
14 3 42 A
项是符合题目要求的。 制豆腐用石膏点浆 石膏能使蛋白质发生聚沉
B
用白醋清洗水壶中的水垢 醋酸的酸性比碳酸强
《黑神话·悟空》作为国产第一部 游戏,以中国经典文学著作《西游记》为蓝本,对山
C
1. 3A
使用天然磁石制作出勺形的司南 磁石主要成分为四氧化三铁
西多处名胜古迹进行实景扫描,游戏中形态各异的佛像,反映了古代匠人高超的技艺 D
电解质在溶液中的反应与离子有关。下列各组离子能大量共存的是
水平。雕塑的主要成分为硅酸盐及铁合金等,下列说法错误的是
6.
在 溶液中: 、 、 、
硅酸盐雕塑佛像历经千年依然身形完好,这是由硅酸盐材料中硅氧四面体的特殊 A. 0.1mol/LKMnO4 Fe 2+ Cl − Ca 2+ H +
A.
在 硝酸银溶液中: 、 、、
+ + − 2−
结构决定的 B. 0.1mol/L K Na I SO4
在 氨水中: 、 、 、
2− + 2+ +
铁佛寺雕塑主要成分为铁合金,合金的熔点一般比各成分金属低 C. 0.1mol/L SO4 NH4 Cu Na
B. 在 盐酸中: 、 、 、
2− + − +
雕塑彩绘颜料都是以天然的矿物质手工加工而成,历经千年仍然色彩艳丽,其中
D. 0.1mol/L SO4 K Br H
C. 实验是化学学科的特征之一。用如图所示装置及药品进行实验,下列能达到实验目
7.
用到的红色矿物颜料成分主要是硫化汞,常温下容易被空气中的氧气氧化
的的是
玻璃、陶瓷、水泥等硅酸盐材料属于传统无机非金属材料
D.
50mL0.5mol/L
化
2
“
.
侯氏制碱法”誉满全球,反应原理之一为:
NaCl + CO2 + NH3 + H2O
====
NaHCO3↓ +
H2SO4 溶液 温度计
镀件
。下列表达正确的是 Cu 玻璃搅拌器
NH4Cl H2(g)+I2(g) 2HI(g)
、、 的第一电离能由大到小的顺序为
A.C N O O > N>C
硫酸铜溶液 50mL溶1.0液mol/L
NaOH
碎纸屑
关注微信公众号 的 模型为 图 图 图 图
获得答案详解及更多资讯 B.NH3 VSEPR 1 2 3 4
化学试题 第 页(共 页) 化学试题 第 页(共 页)
1 8 2 8姓名 准考证号
干冰晶体和冰晶体的晶胞结构相同
秘密 启用前 C.
★
1s 2s 2p
基态 原子的电子轨道表示式 违背了洪特规则
D. C
化学实验必须树立安全意识。下列说法错误的是
化 学 3.
金属钠着火时,应使用干燥的沙土扑灭
A.
能相互反应产生有毒气体的废液,不得倒入同一收集桶中
B.
若不慎将苯酚沾到皮肤上,应立即用 溶液清洗
C. NaOH
注意事项:
体积分数为 的酒精免洗消毒喷雾存放处应张贴 警示标识
答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。 D. 75%
1.
设N 为阿伏加德罗常数的值。下列说法正确的是
全部答案在答题卡上完成,答在本试题上无效。 4. A
2.
标准状况下, 和 在密闭容器中混合,容器内气体分子数为N
回答选择题时,选出每小题答案后,用 铅笔把答题卡上对应题目的答案标号 A. 22.4LNO 11.2LO2 A
3. 2B
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用 ( )与 ( )的混合物中所含共价键数为 N
B.32gS8 S6 2 A
黑色笔迹签字笔写在答题卡上。 标准状况下, 通入水中,溶液中氯离子数为 N
0.5mm C. 11.2LCl2 0.5 A
考试结束后,将本试题和答题卡一并交回。 和 充分反应,反应后 键的数目为 N
4. D.1molC2H6 1molCl2 σ 8 A
可能用到的相对原子质量: 劳动人民的发明创造是中华优秀传统文化的组成部分。下列劳动项目对应的化学知
H1 C12 O16 F19 P31 S32 Ti48 Zn65 Co59 5.
识描述错误的是
选项 劳动项目 化学知识
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只有一 用明矾净水 明矾具有强氧化性,能杀菌消毒
14 3 42 A
项是符合题目要求的。 制豆腐用石膏点浆 石膏能使蛋白质发生聚沉
B
用白醋清洗水壶中的水垢 醋酸的酸性比碳酸强
《黑神话·悟空》作为国产第一部 游戏,以中国经典文学著作《西游记》为蓝本,对山
C
1. 3A
使用天然磁石制作出勺形的司南 磁石主要成分为四氧化三铁
西多处名胜古迹进行实景扫描,游戏中形态各异的佛像,反映了古代匠人高超的技艺 D
电解质在溶液中的反应与离子有关。下列各组离子能大量共存的是
水平。雕塑的主要成分为硅酸盐及铁合金等,下列说法错误的是
6.
在 溶液中: 、 、 、
硅酸盐雕塑佛像历经千年依然身形完好,这是由硅酸盐材料中硅氧四面体的特殊 A. 0.1mol/LKMnO4 Fe 2+ Cl − Ca 2+ H +
A.
在 硝酸银溶液中: 、 、、
+ + − 2−
结构决定的 B. 0.1mol/L K Na I SO4
在 氨水中: 、 、 、
2− + 2+ +
铁佛寺雕塑主要成分为铁合金,合金的熔点一般比各成分金属低 C. 0.1mol/L SO4 NH4 Cu Na
B. 在 盐酸中: 、 、 、
2− + − +
雕塑彩绘颜料都是以天然的矿物质手工加工而成,历经千年仍然色彩艳丽,其中
D. 0.1mol/L SO4 K Br H
C. 实验是化学学科的特征之一。用如图所示装置及药品进行实验,下列能达到实验目
7.
用到的红色矿物颜料成分主要是硫化汞,常温下容易被空气中的氧气氧化
的的是
玻璃、陶瓷、水泥等硅酸盐材料属于传统无机非金属材料
D.
50mL0.5mol/L
化
2
“
.
侯氏制碱法”誉满全球,反应原理之一为:
NaCl + CO2 + NH3 + H2O
====
NaHCO3↓ +
H2SO4 溶液 温度计
镀件
。下列表达正确的是 Cu 玻璃搅拌器
NH4Cl H2(g)+I2(g) 2HI(g)
、、 的第一电离能由大到小的顺序为
A.C N O O > N>C
硫酸铜溶液 50mL溶1.0液mol/L
NaOH
碎纸屑
关注微信公众号 的 模型为 图 图 图 图
获得答案详解及更多资讯 B.NH3 VSEPR 1 2 3 4
化学试题 第 页(共 页) 化学试题 第 页(共 页)
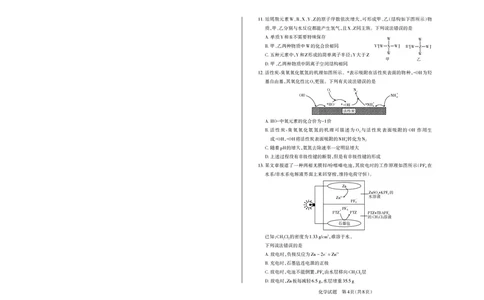
1 8 2 8图 :为镀件镀铜 短周期元素 、、、、的原子序数依次增大,可形成甲、乙(结构如下图所示)物
A. 1 11. W R X Y Z
图 :测定中和反应的反应热 质,甲、乙分别与水反应都能产生氢气,且 、同主族。下列说法错误的是
B. 2 X Z
图 :缩小容器容积,气体颜色加深,() () ()平衡逆向移动 单质 和 不需要特殊保存
C. 3 H2 g +I2 g 2HI g A. Y R
W W
D. 图 4 :用于尾气处理,防倒吸 B. 甲、乙两种物质中 W 的化合价相同 Y + [W X W] - R + [W Z W] -
“宏观辨识与微观探析”是化学学科核心素养之一。下列有关宏观辨识与微观探析的
五种元素中, 和 形成的简单离子半径: 大于
8. C. Y Z Y Z 甲 W 乙 W
说法,错误的是
甲、乙两种物质中阴离子空间结构相同
D.
选项 宏观辨识 微观探析 活性炭 臭氧氧化氨氮的机理如图所示。 表示吸附在活性炭表面的物种,· 为羟
12. * OH
溶解度( ): ( )大于 ( ) 阴离子电荷不同 基自由基,其氧化性比 更强。下列有关说法错误的是
A 20℃ Na2CO3 29g NaHCO3 8g O3
在水中的溶解度大于 是极性分子, 是非极性分子
B O3 O2 O3 O2 O3 N2
- +
石墨的导电性只能沿石墨平面的方向 石墨晶体中相邻碳原子平面之间相隔较远 OH NH4
C
- +
在标准状况下呈液态 分子之间存在氢键 一一一一一*H一一O 一一*·一一OH一一一一一一*N一一H4 一一一一一一一
D HF HF 活性炭
一一一一一一一一一一一一一一一一一一一一一一一一一一
物质类别和核心元素的价态是我们学习元素及其化合物性质的两个重要认识视角。
9. ·中氧元素的化合价一为一一一一价一一一一一一一一一一一一一一一一一一一一一
A.HO -1
以下是硫元素形成物质的“价 类”二维图及含硫物质相互转化的部分信息。下列说
- 活性炭 臭氧氧化氨氮的机理可描述为 与活性炭表面吸附的 作用生
-
法不正确的是 B. O3 OH
成· ,· 将活性炭表面吸附的 转化为
+
实验室制备 可以用启普发生器 硫元素 OH OH NH4 N2
A. A 化合价 随着 的增大,氨氮去除速率一定明显增大
硫元素在自然界以游离态和化合态的形式 +6 D E H C. pH
B.
上述过程没有非极性键的断裂,但是有非极性键的形成
存在 +4 C F G D.
某文章报道了一种两相无膜锌 吩噻嗪电池,其放电时的工作原理如图所示( 在
-
中阴离子的检验试剂为稀硝酸和氯化钡 13. / PF6
C.H
水系 非水系电解液界面上来回穿梭,维持电荷守恒)。
溶液 0 B /
食品中加入适量的 可起到漂白、防腐、抗 -2 A
氢 单 氧 酸 盐 物质类别
D. C Zn
氧化等作用 化 质 化 的
物 物 Z水n溶SO液4+KPF6
2+
内酯 可由 通过电解合成,并在一定条件下转化为 ,转化路线如下: Zn -
10. Y X Z
PF6
-
O O O OC 2 H 5 PTZ + PF6 PTZ 的PTZ+TBA溶PF液6
C
OH
电解 C
O
C
催
2H
化
5O
剂
H C OH
石墨毡
CH₂Cl₂
已知: 的密度为 ,难溶于水。
3
X Y Z
CH2Cl2 1.33g/cm
下列说法错误的是
下列说法正确的是
的核磁共振氢谱有 组峰 放电时,负极反应为 - 2+
A.X 7 A. Zn-2e =Zn
、、中所有原子一定处于同一平面 充电时,石墨毡连电源的正极
B.X Y Z B.
相同物质的量的 、、与 反应,消耗 的物质的量相同 放电时,电池不能倒置, - 由水层移向 层
C. X Y Z NaOH NaOH C. PF6 CH2Cl2
通过分子结构可以推测, 在水中溶解度较小 放电时, 板每减轻 ,水层增重
D. Y D. Zn 6.5g 35.5g
化学试题 第 页(共 页) 化学试题 第 页(共 页)
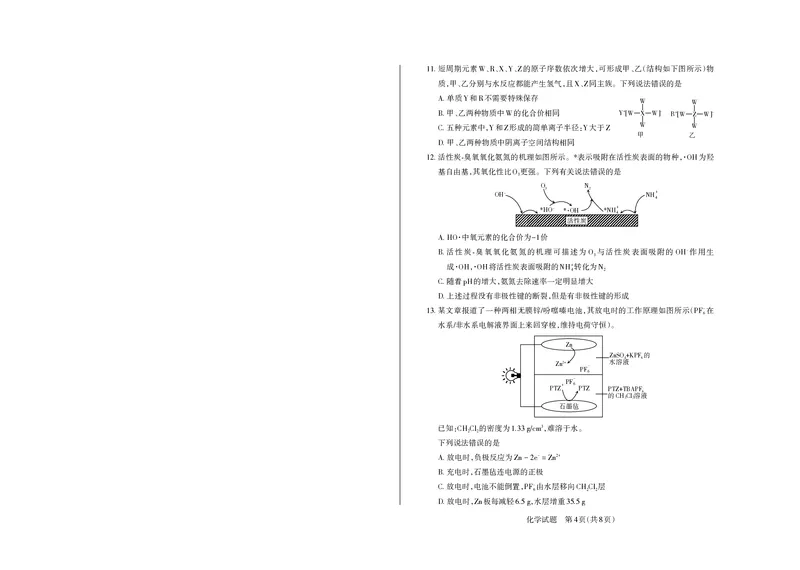
3 8 4 8图 :为镀件镀铜 短周期元素 、、、、的原子序数依次增大,可形成甲、乙(结构如下图所示)物
A. 1 11. W R X Y Z
图 :测定中和反应的反应热 质,甲、乙分别与水反应都能产生氢气,且 、同主族。下列说法错误的是
B. 2 X Z
图 :缩小容器容积,气体颜色加深,() () ()平衡逆向移动 单质 和 不需要特殊保存
C. 3 H2 g +I2 g 2HI g A. Y R
W W
D. 图 4 :用于尾气处理,防倒吸 B. 甲、乙两种物质中 W 的化合价相同 Y + [W X W] - R + [W Z W] -
“宏观辨识与微观探析”是化学学科核心素养之一。下列有关宏观辨识与微观探析的
五种元素中, 和 形成的简单离子半径: 大于
8. C. Y Z Y Z 甲 W 乙 W
说法,错误的是
甲、乙两种物质中阴离子空间结构相同
D.
选项 宏观辨识 微观探析 活性炭 臭氧氧化氨氮的机理如图所示。 表示吸附在活性炭表面的物种,· 为羟
12. * OH
溶解度( ): ( )大于 ( ) 阴离子电荷不同 基自由基,其氧化性比 更强。下列有关说法错误的是
A 20℃ Na2CO3 29g NaHCO3 8g O3
在水中的溶解度大于 是极性分子, 是非极性分子
B O3 O2 O3 O2 O3 N2
- +
石墨的导电性只能沿石墨平面的方向 石墨晶体中相邻碳原子平面之间相隔较远 OH NH4
C
- +
在标准状况下呈液态 分子之间存在氢键 一一一一一*H一一O 一一*·一一OH一一一一一一*N一一H4 一一一一一一一
D HF HF 活性炭
一一一一一一一一一一一一一一一一一一一一一一一一一一
物质类别和核心元素的价态是我们学习元素及其化合物性质的两个重要认识视角。
9. ·中氧元素的化合价一为一一一一价一一一一一一一一一一一一一一一一一一一一一
A.HO -1
以下是硫元素形成物质的“价 类”二维图及含硫物质相互转化的部分信息。下列说
- 活性炭 臭氧氧化氨氮的机理可描述为 与活性炭表面吸附的 作用生
-
法不正确的是 B. O3 OH
成· ,· 将活性炭表面吸附的 转化为
+
实验室制备 可以用启普发生器 硫元素 OH OH NH4 N2
A. A 化合价 随着 的增大,氨氮去除速率一定明显增大
硫元素在自然界以游离态和化合态的形式 +6 D E H C. pH
B.
上述过程没有非极性键的断裂,但是有非极性键的形成
存在 +4 C F G D.
某文章报道了一种两相无膜锌 吩噻嗪电池,其放电时的工作原理如图所示( 在
-
中阴离子的检验试剂为稀硝酸和氯化钡 13. / PF6
C.H
水系 非水系电解液界面上来回穿梭,维持电荷守恒)。
溶液 0 B /
食品中加入适量的 可起到漂白、防腐、抗 -2 A
氢 单 氧 酸 盐 物质类别
D. C Zn
氧化等作用 化 质 化 的
物 物 Z水n溶SO液4+KPF6
2+
内酯 可由 通过电解合成,并在一定条件下转化为 ,转化路线如下: Zn -
10. Y X Z
PF6
-
O O O OC 2 H 5 PTZ + PF6 PTZ 的PTZ+TBA溶PF液6
C
OH
电解 C
O
C
催
2H
化
5O
剂
H C OH
石墨毡
CH₂Cl₂
已知: 的密度为 ,难溶于水。
3
X Y Z
CH2Cl2 1.33g/cm
下列说法错误的是
下列说法正确的是
的核磁共振氢谱有 组峰 放电时,负极反应为 - 2+
A.X 7 A. Zn-2e =Zn
、、中所有原子一定处于同一平面 充电时,石墨毡连电源的正极
B.X Y Z B.
相同物质的量的 、、与 反应,消耗 的物质的量相同 放电时,电池不能倒置, - 由水层移向 层
C. X Y Z NaOH NaOH C. PF6 CH2Cl2
通过分子结构可以推测, 在水中溶解度较小 放电时, 板每减轻 ,水层增重
D. Y D. Zn 6.5g 35.5g
化学试题 第 页(共 页) 化学试题 第 页(共 页)
3 8 4 8已知 为二元可溶性弱酸。 时,分别向 溶液和
14. H2X 25℃ 1L0.1mol/LNH4HX 1L0.1mol/L
溶液中加 固体(忽略溶液体积变化),所得结果如下图,下列说法正
NH4HCO3 NaOH
确的是
c
/(mol/L)
0.10
0.08
0.06 X 2- NH3·H2O
- P HX 0.04 + NH4 0.02
0
0
化学试题 第 页(共 页) 化学试题 第 页(共 页)
5 8 6 8
50.0 01.0 51.0 02.0 52.0 03.0
c
/(mol/L)
0.10
0.08 NH3·H2O
0.06
Q 0.04 - 0.02 HCO3
+
NH4
0
0
n
/(NaOH)/mol
50.0 01.0 51.0 02.0 52.0 03.0
( 分)
16. 14
“一碳化学”是指以分子中只含有一个碳原子的化合物(如 、 、 等)为原
CO CO2 CH3OH
料合成一系列化工产品的化学。回答下列问题:
()已知:断开 化学键所需能量如表所示。
1 1mol
化学键 ( ) — — —
C O CO H H C H O H
2- 所需能量( ) CO3
/ kJ/mol 1076 436 413 463 a 则反应 () () () () H ;该反应 CO g + 3H₂ g CH4 g + H₂O g Δ = ▲ kJ/mol
在 (填“高温”“低温”或“任意温度”)下能自发进行。
▲
()甲醛在医药方面有重要用途。工业上可利用反应: () ()
n 2 CH3OH g HCHO g
/(NaOH)/mol () H 来合成甲醛。T 时,向体积恒为 的密闭容器中充入
氢氧化钠固体加入两种溶液中,先和酸式酸根离子反应 +H2 g Δ 1 = +85.2 kJ/mol ℃ 2 L
A. ()发生反应, 后反应达到平衡,测得混合体系中 ()的体积分
、 两点 :点 点 8molCH3OH g 5min HCHO g
B.P Q pH P >Q 数为 。
20%
当n( ) 时,两种溶液中 均大于
C. NaOH =0.20mol pH 7 下列事实不能说明该反应已达到化学平衡状态的是 (填字母)。
① ▲
当a 时,所对应的溶液中:c(
+
) c( ) c( -) c(
2-
)
v ( ) v ( ) 体系压强保持不变
D. =0.14mol NH4 + NH3·H2O = HCO3 + CO3 A. 正 HCHO = 逆 CH3OH B.
二、非选择题:本题共 小题,共 分。 体积分数保持不变 混合气体的密度保持不变
4 58 C.H2 D.
( 分) 体系温度保持不变
15. 14 E.
硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是 内,v( ) ( )(填“ ”“ ”或“ ”)。
②2.5min CH3OH ▲ 0.2mol/ L·min > < =
起始压强为P,达到平衡时,K (用含P 的表达式表示)(用平衡分压代
将氨经过一系列反应得到硝酸。下图是模拟工业制硝酸的实验装置(支撑装置省略)。
③ 0 P= ▲ 0
替平衡浓度计算,分压 总压 物质的量分数)。
陶瓷 = ×
1氧
气
L
或氧气
M
加
C
热
H
棒催化剂
(
3
)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
瓶 历程
空气 水 ⅰ CH3OH→·H+·CH2OH
历程 ·
电源 ⅱ CH2OH→·H+HCHO
碱石灰 历程 ·
ⅲ CH2OH→3·H+CO
氨水 历程 ·
ⅳ H+·H→H2
一定条件下测得相同时间内温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如
回答下列问题:
n 生成的
下图所示[甲醛的选择性(Y) ( HCHO) ]。 时,推测甲醛选
()实验时,怎样产生氨气? 。 = n 转化的 ×100% 550~750℃
1 ▲ ( CH3OH)
()碱石灰能否换成氯化钙? (填“能”或“不能”)。 择性变化的原因: 。
2 ▲ ▲
()实验开始时,先通入的气体是 (填字母)( 空气 氧气),原因
3 ▲ A. B. 100
是 。
▲ 80
()实验结束时,最后停止通入的气体是 (填字母)( 空气 氧气),原因
4 ▲ A. B. 60
是 。
▲ 40
()氨气在催化剂表面发生反应的化学方程式为 ,使用玻璃纤维毡堆放催化
5 ▲ 20
剂的原因是 。
▲ 0
()此实验中,氮氧化物生成硝酸的化学方程式为 。 500 550 600 650 700 750 800
6 ▲
Y或X
%/
甲醇的转化率
甲醛的选择性
温度
/℃已知 为二元可溶性弱酸。 时,分别向 溶液和
14. H2X 25℃ 1L0.1mol/LNH4HX 1L0.1mol/L
溶液中加 固体(忽略溶液体积变化),所得结果如下图,下列说法正
NH4HCO3 NaOH
确的是
c
/(mol/L)
0.10
0.08
0.06 X 2- NH3·H2O
- P HX 0.04 + NH4 0.02
0
0
化学试题 第 页(共 页) 化学试题 第 页(共 页)
5 8 6 8
50.0 01.0 51.0 02.0 52.0 03.0
c
/(mol/L)
0.10
0.08 NH3·H2O
0.06
Q 0.04 - 0.02 HCO3
+
NH4
0
0
n
/(NaOH)/mol
50.0 01.0 51.0 02.0 52.0 03.0
( 分)
16. 14
“一碳化学”是指以分子中只含有一个碳原子的化合物(如 、 、 等)为原
CO CO2 CH3OH
料合成一系列化工产品的化学。回答下列问题:
()已知:断开 化学键所需能量如表所示。
1 1mol
化学键 ( ) — — —
C O CO H H C H O H
2- 所需能量( ) CO3
/ kJ/mol 1076 436 413 463 a 则反应 () () () () H ;该反应 CO g + 3H₂ g CH4 g + H₂O g Δ = ▲ kJ/mol
在 (填“高温”“低温”或“任意温度”)下能自发进行。
▲
()甲醛在医药方面有重要用途。工业上可利用反应: () ()
n 2 CH3OH g HCHO g
/(NaOH)/mol () H 来合成甲醛。T 时,向体积恒为 的密闭容器中充入
氢氧化钠固体加入两种溶液中,先和酸式酸根离子反应 +H2 g Δ 1 = +85.2 kJ/mol ℃ 2 L
A. ()发生反应, 后反应达到平衡,测得混合体系中 ()的体积分
、 两点 :点 点 8molCH3OH g 5min HCHO g
B.P Q pH P >Q 数为 。
20%
当n( ) 时,两种溶液中 均大于
C. NaOH =0.20mol pH 7 下列事实不能说明该反应已达到化学平衡状态的是 (填字母)。
① ▲
当a 时,所对应的溶液中:c(
+
) c( ) c( -) c(
2-
)
v ( ) v ( ) 体系压强保持不变
D. =0.14mol NH4 + NH3·H2O = HCO3 + CO3 A. 正 HCHO = 逆 CH3OH B.
二、非选择题:本题共 小题,共 分。 体积分数保持不变 混合气体的密度保持不变
4 58 C.H2 D.
( 分) 体系温度保持不变
15. 14 E.
硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。工业上制硝酸的原理是 内,v( ) ( )(填“ ”“ ”或“ ”)。
②2.5min CH3OH ▲ 0.2mol/ L·min > < =
起始压强为P,达到平衡时,K (用含P 的表达式表示)(用平衡分压代
将氨经过一系列反应得到硝酸。下图是模拟工业制硝酸的实验装置(支撑装置省略)。
③ 0 P= ▲ 0
替平衡浓度计算,分压 总压 物质的量分数)。
陶瓷 = ×
1氧
气
L
或氧气
M
加
C
热
H
棒催化剂
(
3
)在催化剂作用下,甲醇脱氢制甲醛的部分机理如下:
瓶 历程
空气 水 ⅰ CH3OH→·H+·CH2OH
历程 ·
电源 ⅱ CH2OH→·H+HCHO
碱石灰 历程 ·
ⅲ CH2OH→3·H+CO
氨水 历程 ·
ⅳ H+·H→H2
一定条件下测得相同时间内温度对甲醇的转化率(X)、甲醛的选择性(Y)的影响如
回答下列问题:
n 生成的
下图所示[甲醛的选择性(Y) ( HCHO) ]。 时,推测甲醛选
()实验时,怎样产生氨气? 。 = n 转化的 ×100% 550~750℃
1 ▲ ( CH3OH)
()碱石灰能否换成氯化钙? (填“能”或“不能”)。 择性变化的原因: 。
2 ▲ ▲
()实验开始时,先通入的气体是 (填字母)( 空气 氧气),原因
3 ▲ A. B. 100
是 。
▲ 80
()实验结束时,最后停止通入的气体是 (填字母)( 空气 氧气),原因
4 ▲ A. B. 60
是 。
▲ 40
()氨气在催化剂表面发生反应的化学方程式为 ,使用玻璃纤维毡堆放催化
5 ▲ 20
剂的原因是 。
▲ 0
()此实验中,氮氧化物生成硝酸的化学方程式为 。 500 550 600 650 700 750 800
6 ▲
Y或X
%/
甲醇的转化率
甲醛的选择性
温度
/℃( 分)
17. 15
主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为 ,含少量
Co2O3 Co2O3
、 及铝、镁、钙等金属元素的氧化物)制取 的工艺流程如下。
Fe2O3 SiO2 Co2O3
稀硫酸 NaF ( )
Na2SO3 H2O2 Na2CO3 NH4 2C2O4
钴
沉淀 煅烧
矿 溶浸 氧化 调节 沉钴
石
pH 除杂 CoC2O4·2H2O Co2O3
滤渣 滤渣
1 2 滤渣
3
部分阳离子以氢氧化物形式沉淀时溶液 如下表。
pH
沉淀物 ( ) ( ) ( ) ( )
Fe OH 3 Fe OH 2 Co OH 2 Al OH 3
开始沉淀的 pH 1.5 6.3 6.6 3.4
完全沉淀的
pH 3.7 9.6 9.2 5.2
回答下列问题:
() 在元素周期表中的位置是 。 1 Co ▲
()溶浸过程中适当升温的目的是 ,滤渣 的主要成分是 ,滤渣 的主
2 ▲ 1 ▲ 3
要成分是 。
▲
()氧化过程中,主要发生反应的离子方程式为 ,说明氧化性:
3+
3 ▲ Co ▲
(填“ ”或“ ”)。
H2O2 > <
()调节 的范围为 。
4 pH ▲
()所得 可用于合成钛酸钴。一种钛酸钴的晶胞
5 Co2O3
结构如图所示,该立方晶胞参数为a ,(体心)位于 形
pm Ti O
成的 (填“四面体”或“八面体”)空隙中心。设N 为阿
▲ A
伏加德罗常数的值,该钛酸钴晶体的密度为 3
▲ g/cm
(列出计算式)。
() 是制备钴的氧化物的重要原料。下图为二水合草酸钴( )在
6 CoC2O4 CoC2O4·2H2O
空气中受热的质量变化曲线,曲线中 及以上所得固体均为钴氧化物。
300℃
18.3
( , )
A 150℃ 14.70g
16 ( , )
B 225℃ 14.70g
12
8 ( , )
C 330℃ 8.03g
150 300 450 600 750 900
量质的留残体固
g/
( 分)
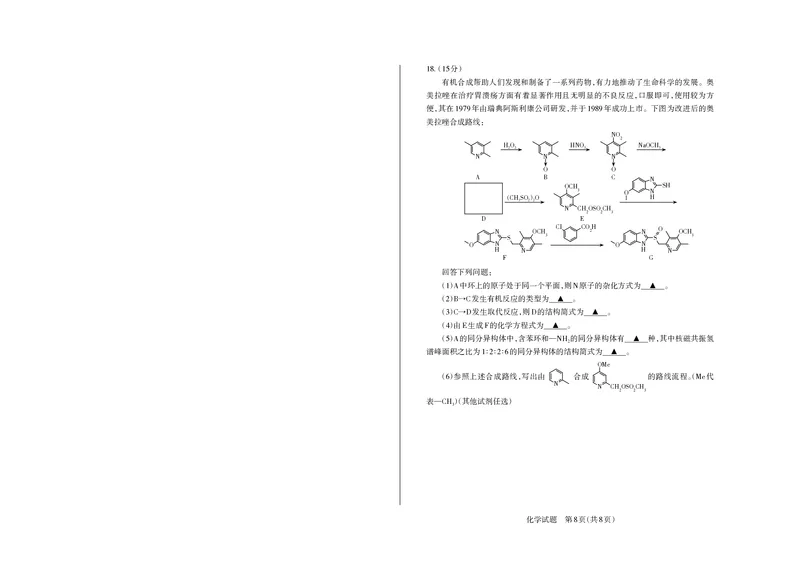
18. 15
有机合成帮助人们发现和制备了一系列药物,有力地推动了生命科学的发展。奥
美拉唑在治疗胃溃疡方面有着显著作用且无明显的不良反应,口服即可,使用较为方
便,其在 年由瑞典阿斯利康公司研发,并于 年成功上市。下图为改进后的奥
1979 1989
美拉唑合成路线:
NO
2
H2O2 HNO3 NaOCH3
N N N
O O
A B C
N
OCH SH ( ) 3 O N
CH3SO2 2O H
N CHOSOCH
2 2 3
D E
N OCH Cl CO 2 H N O OCH 3 3
S S
O N O N
H N H N
F G
回答下列问题:
() 中环上的原子处于同一个平面,则 原子的杂化方式为 。
1 A N ▲
() 发生有机反应的类型为 。
2 B→C ▲
() 发生取代反应,则 的结构简式为 。
Ti 3 C→D D ▲
()由 生成 的化学方程式为 。
Co 4 E F ▲
() 的同分异构体中,含苯环和— 的同分异构体有 种,其中核磁共振氢
O
5 A NH2 ▲
谱峰面积之比为 ∶∶∶ 的同分异构体的结构简式为 。
1 2 2 6 ▲
a
pm OMe
()参照上述合成路线,写出由 合成 的路线流程。( 代
6 Me
N N CHOSOCH
2 2 3
表— )(其他试剂任选)
CH3
化
温度
/℃
通过计算确定 点剩余固体的化学成分为 (填化学式)。
C ▲
化学试题 第 页(共 页) 化学试题 第 页(共 页)
7 8 8 8( 分)
17. 15
主要用作颜料、釉料及磁性材料,利用一种钴矿石(主要成分为 ,含少量
Co2O3 Co2O3
、 及铝、镁、钙等金属元素的氧化物)制取 的工艺流程如下。
Fe2O3 SiO2 Co2O3
稀硫酸 NaF ( )
Na2SO3 H2O2 Na2CO3 NH4 2C2O4
钴
沉淀 煅烧
矿 溶浸 氧化 调节 沉钴
石
pH 除杂 CoC2O4·2H2O Co2O3
滤渣 滤渣
1 2 滤渣
3
部分阳离子以氢氧化物形式沉淀时溶液 如下表。
pH
沉淀物 ( ) ( ) ( ) ( )
Fe OH 3 Fe OH 2 Co OH 2 Al OH 3
开始沉淀的 pH 1.5 6.3 6.6 3.4
完全沉淀的
pH 3.7 9.6 9.2 5.2
回答下列问题:
() 在元素周期表中的位置是 。 1 Co ▲
()溶浸过程中适当升温的目的是 ,滤渣 的主要成分是 ,滤渣 的主
2 ▲ 1 ▲ 3
要成分是 。
▲
()氧化过程中,主要发生反应的离子方程式为 ,说明氧化性:
3+
3 ▲ Co ▲
(填“ ”或“ ”)。
H2O2 > <
()调节 的范围为 。
4 pH ▲
()所得 可用于合成钛酸钴。一种钛酸钴的晶胞
5 Co2O3
结构如图所示,该立方晶胞参数为a ,(体心)位于 形
pm Ti O
成的 (填“四面体”或“八面体”)空隙中心。设N 为阿
▲ A
伏加德罗常数的值,该钛酸钴晶体的密度为 3
▲ g/cm
(列出计算式)。
() 是制备钴的氧化物的重要原料。下图为二水合草酸钴( )在
6 CoC2O4 CoC2O4·2H2O
空气中受热的质量变化曲线,曲线中 及以上所得固体均为钴氧化物。
300℃
18.3
( , )
A 150℃ 14.70g
16 ( , )
B 225℃ 14.70g
12
8 ( , )
C 330℃ 8.03g
150 300 450 600 750 900
量质的留残体固
g/
( 分)
18. 15
有机合成帮助人们发现和制备了一系列药物,有力地推动了生命科学的发展。奥
美拉唑在治疗胃溃疡方面有着显著作用且无明显的不良反应,口服即可,使用较为方
便,其在 年由瑞典阿斯利康公司研发,并于 年成功上市。下图为改进后的奥
1979 1989
美拉唑合成路线:
NO
2
H2O2 HNO3 NaOCH3
N N N
O O
A B C
N
OCH SH ( ) 3 O N
CH3SO2 2O H
N CHOSOCH
2 2 3
D E
N OCH Cl CO 2 H N O OCH 3 3
S S
O N O N
H N H N
F G
回答下列问题:
() 中环上的原子处于同一个平面,则 原子的杂化方式为 。
1 A N ▲
() 发生有机反应的类型为 。
2 B→C ▲
() 发生取代反应,则 的结构简式为 。
Ti 3 C→D D ▲
()由 生成 的化学方程式为 。
Co 4 E F ▲
() 的同分异构体中,含苯环和— 的同分异构体有 种,其中核磁共振氢
O
5 A NH2 ▲
谱峰面积之比为 ∶∶∶ 的同分异构体的结构简式为 。
1 2 2 6 ▲
a
pm OMe
()参照上述合成路线,写出由 合成 的路线流程。( 代
6 Me
N N CHOSOCH
2 2 3
表— )(其他试剂任选)
CH3
化
温度
/℃
通过计算确定 点剩余固体的化学成分为 (填化学式)。
C ▲
化学试题 第 页(共 页) 化学试题 第 页(共 页)
7 8 8 8