文档内容
让更多的孩子得到更好的教育
中考总复习:综合计算技巧(基础)
撰稿:李伟 审稿:熊亚军
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
1.某不纯的铁粉5.6g与足量的稀硫酸反应生成0.19gH ,则不纯的铁中混有的杂质不可能是( )
2
A.Mg B.Zn C.Cu D.Ag
2. KCl是一种常用的钾肥,其溶解度如表。下列说法正确的是( )
A.KCl饱和溶液中不能再溶解其他物质
B.60℃的KCl饱和溶液降温至20℃,有晶体析出
C.40℃时,KCl饱和溶液的质量分数为40.0%
D.20℃时,100 g KCl饱和溶液中含KCl 34.0 g
3.(2012天宁)由Mg(OH)和MgO组成的混合物,测得其中含镁元素的质量分数为48%.取该混合物
2
5g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为( )
A.6g B.12g C.18g D.24g
4.天平两边各放质量相等的烧杯,并分别盛有100g 溶质质量分数为7.3%的稀盐酸,此时天平平衡.若向
左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平仍平衡的是( )
A.锌6.5g,铁6.5g B.锌15g,碳酸钠15g
C.碳酸钠10g,氧化钠5.6g D.碳酸钠4.2g,硝酸银4.2g
5.锌粉、铝粉、铁粉、镁粉的混合物3.8g与一定质量溶质质量分数为25%的稀硫酸恰好完全反应,将反应
后的混合物蒸发水份得固体(不含结晶水)13.4g,则参加反应的硫酸质量为( )
A.2.45g B.9.6 g C.9.8 g D.39.2g
6.为探究某稀硫酸中溶质的质量分数,小明和小勇分别取质量分数相等的稀硫酸100g.小明向其中加入
6.5g锌粒,反应结束时观察到锌粒完全消失;小勇向其中加入13g锌粒,反应结束时观察到锌粒有剩余.
有关实验的推理一定正确的是( )
A.反应后小明所得溶液中的溶质只有硫酸锌
B.反应后小勇所得溶液中可能含硫酸
C.两位同学实验中生成氢气的质量均少于0.4g
D.原稀硫酸中溶质的质量分数一定大于9.8%小于19.6%
二、填空题
7.当氧元素质量相等时CO和CO 的质量比为_____________。
2
8.(2012贵阳)一定质量的稀HSO 与40g溶质质量分数为10%的NaOH溶液恰好完全反应.求:
2 4
(1)参加反应的NaOH溶液中溶质的质量为___________ g。
(2)反应生成NaSO 的质量_____________g。
2 4
三、计算题
9.(2012安顺)已知氯化钠溶液和硝酸银溶液反应生成氯化银(AgCl〕沉淀和硝酸钠溶液。为测定某氯化
钠溶液的溶质质量分数,将该溶液与一定量的硝酸银溶液混合,恰好完全反应,有关实验数据如表:
反应前 反应后
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共5页让更多的孩子得到更好的教育
氯化钠溶液的质量 加入硝酸银溶液的质量 过滤后剩余溶液的质量
实验数据
117g 140g 228.3g
(1)反应后生成氯化银的质量是_____g。
(2)计算该氯化钠溶液的溶质质量分数。
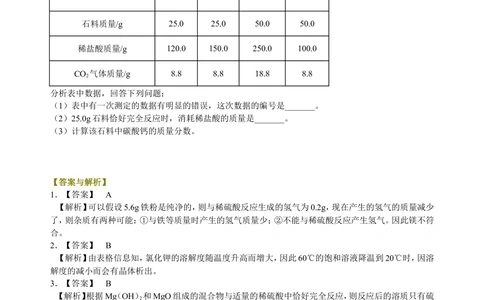
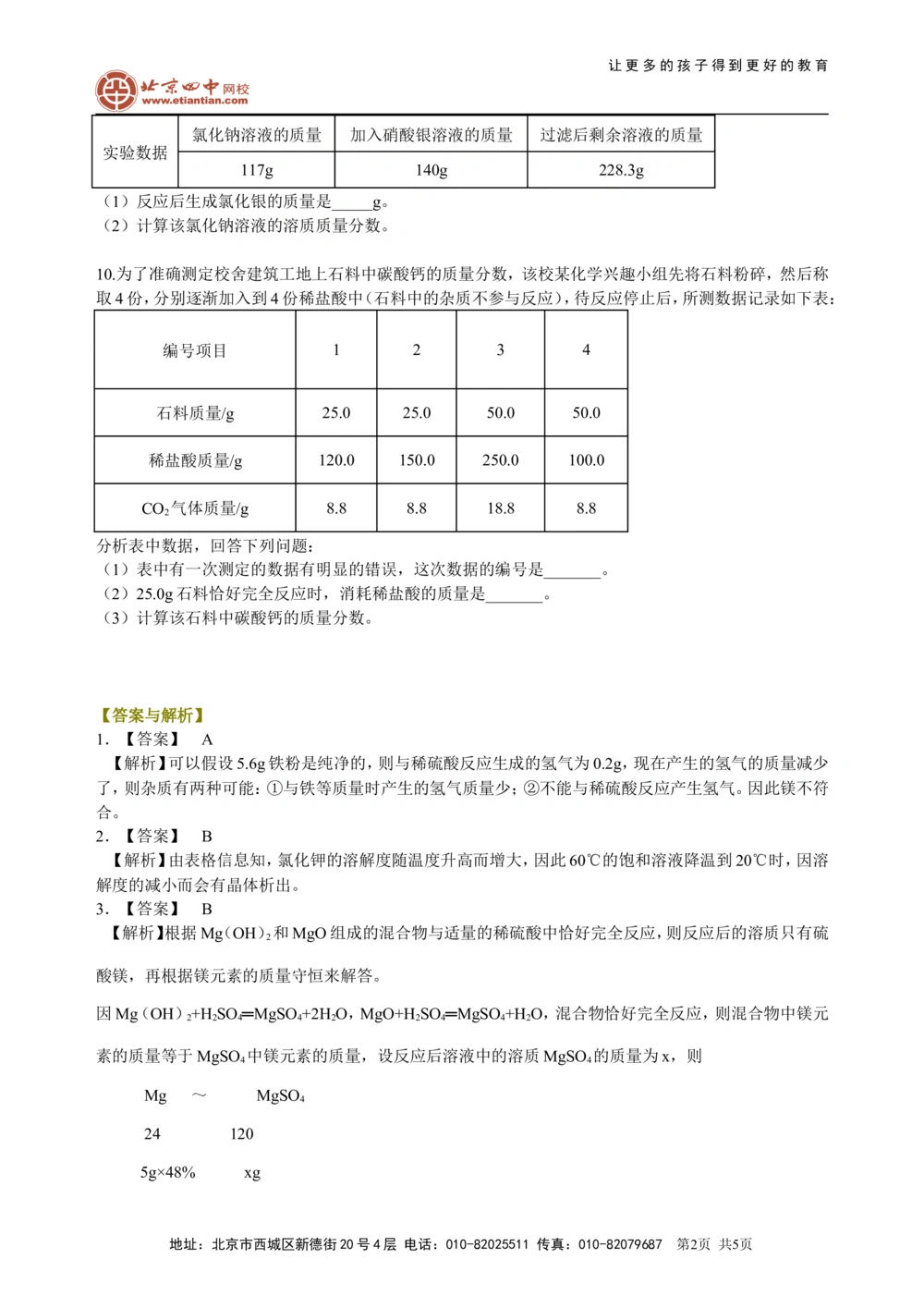
10.为了准确测定校舍建筑工地上石料中碳酸钙的质量分数,该校某化学兴趣小组先将石料粉碎,然后称
取4份,分别逐渐加入到4份稀盐酸中(石料中的杂质不参与反应),待反应停止后,所测数据记录如下表:
编号项目 1 2 3 4
石料质量/g 25.0 25.0 50.0 50.0
稀盐酸质量/g 120.0 150.0 250.0 100.0
CO 气体质量/g 8.8 8.8 18.8 8.8
2
分析表中数据,回答下列问题:
(1)表中有一次测定的数据有明显的错误,这次数据的编号是_______。
(2)25.0g石料恰好完全反应时,消耗稀盐酸的质量是_______。
(3)计算该石料中碳酸钙的质量分数。
【答案与解析】
1.【答案】 A
【解析】可以假设5.6g铁粉是纯净的,则与稀硫酸反应生成的氢气为0.2g,现在产生的氢气的质量减少
了,则杂质有两种可能:①与铁等质量时产生的氢气质量少;②不能与稀硫酸反应产生氢气。因此镁不符
合。
2.【答案】 B
【解析】由表格信息知,氯化钾的溶解度随温度升高而增大,因此60℃的饱和溶液降温到20℃时,因溶
解度的减小而会有晶体析出。
3.【答案】 B
【解析】根据Mg(OH)和MgO组成的混合物与适量的稀硫酸中恰好完全反应,则反应后的溶质只有硫
2
酸镁,再根据镁元素的质量守恒来解答。
因Mg(OH)+H SO ═MgSO+2H O,MgO+H SO ═MgSO+H O,混合物恰好完全反应,则混合物中镁元
2 2 4 4 2 2 4 4 2
素的质量等于MgSO 中镁元素的质量,设反应后溶液中的溶质MgSO 的质量为x,则
4 4
Mg ~ MgSO
4
24 120
5g×48% xg
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共5页让更多的孩子得到更好的教育
解得x=12g
4.【答案】 A
【解析】因为加入的盐酸质量相等,所以需要判断两端加入一定量物质后增加质量是否相等,增加质量
相等时天平能仍然保持平衡,不相等时天平发生偏转。稀盐酸中溶质的质量是:100g×7.3%=7.3g,可根据
化学方程式,借助关系式和差量法进行分析比较。A中根据Zn→2HCl和Fe→2HCl的关系可知,锌恰好反
应,铁有剩余,100g 溶质质量分数为7.3%的稀盐酸全部反应,产生的氢气一样多,因此天平平衡; B中锌
15g,碳酸钠15g分别与盐酸反应产生的气体不一样多,因此天平不平衡; C中根据NaCO→CO 的关系
2 3 2
可知:10g碳酸钠与盐酸反应产生4.2g二氧化碳气体,碳酸钠与二氧化碳的差值是5.8g,大于5.6g,因此
天平不平衡; D中碳酸钠放出气体,而硝酸银不产生气体,因此天平不平衡。
5.【答案】 C
【解析】根据质量守恒定律可知,反应物的质量之和等于生成物的质量之和,反应前后元素的种类,原子
的数目均不变。混合物和硫酸恰好完全反应,因此混合物和纯硫酸(HSO )的质量之和等于剩余固体和氢
2 4
气的质量之和。反应前后硫酸根的质量=(13.4克-3.8克)=9.6克,则纯硫酸的质量=9.6克÷ =9.8克。
6.【答案】 C
【解析】A中小明的实验结束时观察到锌粒完全消失,可得知反应后溶液中含有硫酸锌,但由于不能确
定稀硫酸是否完全反应,因此不能判断反应后溶液中是否含有未反应的硫酸,即不能得出反应后溶液中
溶质只有硫酸锌的结论;B中小勇在反应结束时观察到锌粒有剩余,可判断稀硫酸量不足完全反应,因此
反应后的溶液中不含有硫酸;C中小明在反应结束后,6.5g锌完全反应,此时产生氢气的质量=
×6.5g=0.2g<0.4g,若13g锌完全反应,产生氢气的质量= × 13g=0.4g,而小勇反应结束后所加入的13g
锌有剩余而未完全反应,因此所得到氢气的质量小于0.4g;D中小明同学的实验无法确定稀硫酸中的硫
酸是否完全反应,不能确定稀硫酸中硫酸的质量,小勇实验可以判断硫酸完全反应,但却无法计算硫酸的
质量,因此,两个实验的数据都不能确定稀硫酸的溶质的质量分数。
7.【答案】 14:11
【解析】由于2CO和CO 的氧原子个数相等,即氧元素的质量相等,故可按“等效化学式”巧解此题。
2
关系式: 2CO ~ CO
2
物质质量比: 56 44
56份质量的CO和44份质量的CO 中所含有氧元素的质量相等,即56:44,化简为14:11。
2
8.【答案】 4 7.1
【解析】(1)参加反应的NaOH溶液中溶质的质量为40g×10%=4g;
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共5页让更多的孩子得到更好的教育
(2)设生成的硫酸钠质量为x。
2NaOH + HSO ═ NaSO + 2HO
2 4 2 4 2
80 142
4g x
x=7.1g
9.【答案】 (1)28.7
(2)设氯化钠溶液的溶质的质量为x。
NaCl+AgNO ═AgCl↓+NaNO
3 3
58.5 143.5
x 28.7g
解得:x=11.7g
该氯化钠溶液的溶质质量分数为: ×100%=10%
答:该氯化钠溶液的溶质质量分数为10%。
【解析】(1)生成氯化银的质量为:117g+140g-228.3g=28.7g;
(2)设氯化钠溶液的溶质的质量为x。
NaCl+AgNO ═AgCl↓+NaNO
3 3
58.5 143.5
x 28.7g
解得:x=11.7g
该氯化钠溶液的溶质质量分数为: ×100%=10%
答:该氯化钠溶液的溶质质量分数为10%。
10.【答案】 (1)3 (2)100
(3)解:设石料中CaCO 的质量为x。
3
CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
100 44
x 8.8g
解得x=20.0g
故CaCO 的质量分数= ×100%=80.0%
3
答:石料中CaCO 的质量分数为80.0%。
3
【解析】(1)第1次和第2次实验比较可知:25g石料完全反应只能生成8.8g二氧化碳,如果第三次中
50g石料完全反应只能生成17.6g,不可能产生18.8g二氧化碳,所以第3次数据错误;
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共5页让更多的孩子得到更好的教育
(2)第1次和第2次实验比较可知25g石料完全反应只能生成8.8g二氧化碳,再根据第1次实验和第4次
实验进行比较,可知50g石料完全反应生成17.6g二氧化碳,所以第4次是按照100g稀盐酸反应制取8.8g
二氧化碳,所以25.0g石料恰好完全反应时,消耗稀盐酸的质量是100g;
(3)解:设石料中CaCO 的质量为x。
3
CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
100 44
x 8.8g
解得x=20.0g
故CaCO 的质量分数为: ×100%=80.0%
3
答:石料中CaCO 的质量分数为80.0%。
3
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共5页