文档内容
扬州中学高三下学期化学自主学习效果评估
可能用到的相对原子质量:H—1 O—16 S—32 Cl—35.5 Ni—59 Zn—65
一、单项选择题:共13小题,每小题3分,共计39分。每小题只有一个选项符合题意。
1. “绿色、智能、节俭、文明”的第19届亚运会在杭州圆满闭幕。下列说法不正确的是
A. 会场“莲花碗”采取自然采光方式有利于实现“碳中和”
B. 吉祥物“江南忆”机器人所采用芯片的主要成分中含有晶体硅
C. 氢燃料汽车使用的燃料电池是将化学能转化为电能
D. 火炬“薪火”的燃料“零碳甲醇”是用CO 和H 合成的,“零碳甲醇”使用时不生成
2 2
CO
2
2. 下列化学用语表述不正确的是
A. 次氯酸钠的电子式:
B. 固体HF中的链状结构:
C. 基态Fe2+的电子排布式:[Ar]3d54s1
D. 的 模型
3. 实验室制备水合肼(N H·H O)溶液的反应原理为NaClO+2NH ===N H·H O+NaCl,
2 4 2 3 2 4 2
NH·H O能与NaClO发生剧烈反应。下列装置和操作能达到实验目的的是
2 4 2
A. 用装置甲制取Cl B. 用装置乙制备NaClO溶液
2
1
学科网(北京)股份有限公司C. 用装置丙制备水合肼溶液 D. 用装置丁分离水合肼和NaCl混合溶液
4. 黑火药主要成分是硫磺、硝酸钾和木炭。下列说法正确的是
A.半径:r(K+)>r(S2-) B.第一电离能:I(N)>I(S)
1 1
C.电负性:x(C)>x(O) D.稳定性:HS>HO
2 2
阅读下列材料,完成5~7题。
催化反应广泛存在,如植物光合作用、铁触媒催化合成氨、合成火箭燃料NH (液
2 4
态,燃烧热为622kJ/mol)、铜催化重整CH 和HO制H 和CO等。催化剂有选择性,如
4 2 2
酸性条件下锑电催化还原CO,生成HCOOH的选择性大于CO,通过选择性催化还原技
2
术,NH 将柴油车尾气中的NO 转化为N。
3 2 2
5. 下列说法不正确的是
A.植物光合作用过程中,酶能提高CO 和HO分子的能量使之成为活化分子
2 2
B.NH 将NO 转化为N 的反应中催化剂能加快化学反应速率
3 2 2
C.酸性条件下锑电催化还原CO 时,HCOOH的生成速率大于CO
2
D.铁触媒催化合成氨的反应中,铁触媒能减小反应的活化能
6. 下列化学反应表示正确的是
A.NH 的燃烧:NH(l) +O(g) = N(g) +2HO(g) △H=-622kJ/mol
2 4 2 4 2 2 2
B.CH 和HO催化重整制H 和CO:CH + HO CO + 3H
4 2 2 4 2 2
C.锑电催化还原CO 生成HCOOH的阴极反应:CO-2e﹣+2H+ = HCOOH
2 2
D.NH 将柴油车尾气中的NO 无害化:NH +NO N+HO
3 2 3 2 2 2
7. 下列有关反应描述不正确的是
A.合成氨温度选择400~500℃的原因之一是铁触媒在该温度范围内活性大
B.铁触媒催化合成氨时,铁触媒提高了单位时间内N 的转化率
2
C.催化重整CH 和HO制H 时,H 在催化剂铜表面脱附过程的△S<0
4 2 2 2
D.CO 转化为HCOOH时,C原子轨道的杂化类型发生了变化
2
8.下列物质的结构与性质或性质与用途具有对应关系的是
A.N 中化学键非常牢固,可用作保护气
2
B.乙醇易溶于水,可用于消毒杀菌
C.浓硫酸具有强氧化性,可用于与CaF 反应制HF
2
D.SO 是极性分子,可用于漂白纸浆
2
2
学科网(北京)股份有限公司9. 化合物Y是合成丹参醇的中间体,其合成路线如下:
下列说法正确的是
A. X分子中含手性碳原子
B. X转化为Y的过程中, 与CHMgBr反应生成
3
C. Y与Br 以物质的量1∶1发生加成反应时可得3种产物(不考虑立体异构)
2
D. X、Y可用酸性KMnO 溶液进行鉴别
4
10.科学家基于水/有机双相电解质开发了一种新型铜锌二次电池,双相电解质建立了离
子选择性界面,仅允许氯离子迁移,其放电时的工作原理如图所示。下列说法不正确的
是
A. 充电时,石墨电极与电源正极相连
B. 充电时,石墨电极上可发生电极反应
[CuCl] 1-x-e﹣=[CuCl] 2-x
x x
C. 放电时,氯离子向锌电极迁移
D. 放电时,理论上电路中每转移2mol电子,锌电极质量增加136g
11. 根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向 FeSO 溶液中先加入 KSCN 溶液,再加入 HO 溶还原性:
A 4 2 2
液,溶液变成红色 Fe2+<HO
2 2
向 NaHCO 溶液中加入等浓度、等体积的 NaAlO 溶结合H+的能力:
B 3 2
液,出现白色沉淀 AlO>CO
向ZnS和NaS的悬浊液中滴加CuSO 溶液,生成黑色溶度积:
C 2 4
沉淀 K (CuS)<K (ZnS)
sp sp
D 将稀盐酸滴入硅酸钠溶液中,振荡,观察现象 非金属性:Cl>Si
3
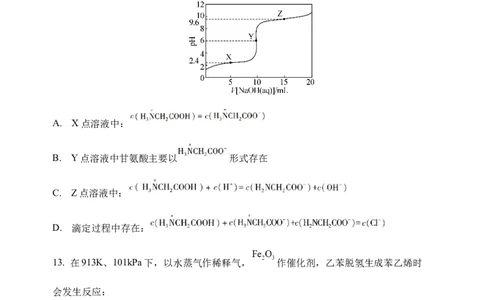
学科网(北京)股份有限公司12. 甘氨酸盐酸盐(ClH NCH COOH)可用作食品添加剂,已知:
3 2
K =1×10-2.4
a1
K =1×10-9.6
a2
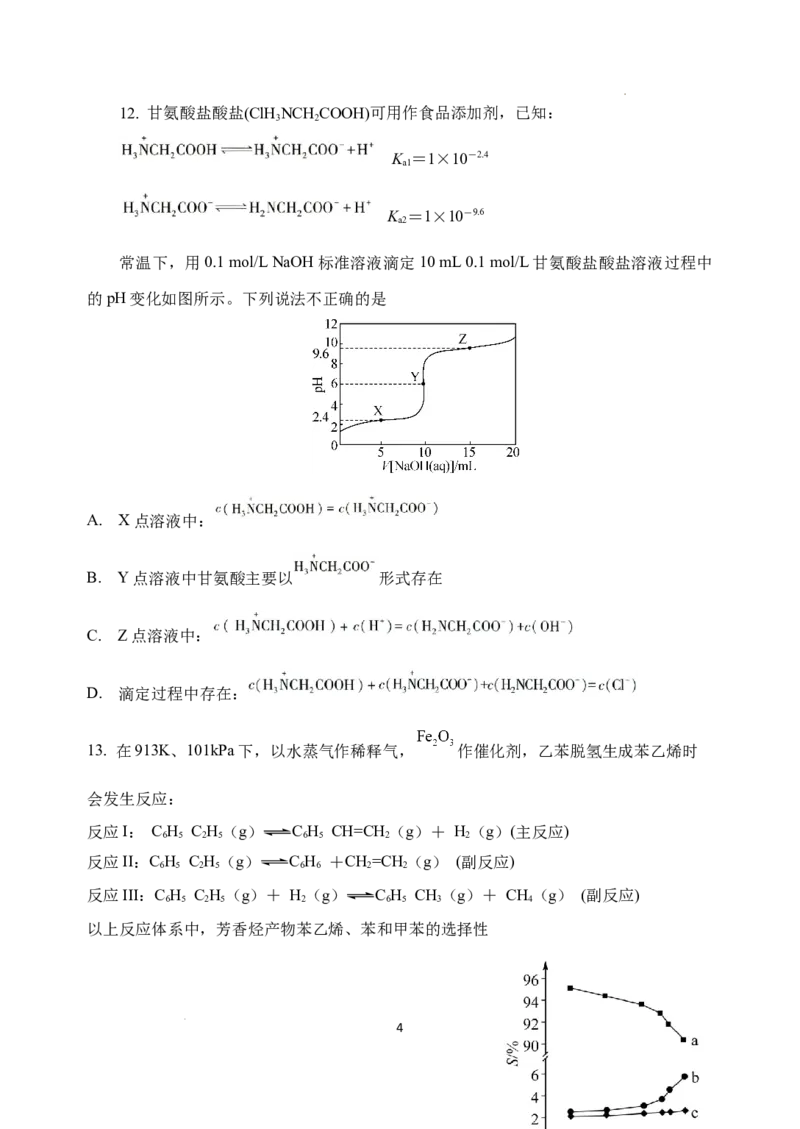
常温下,用0.1 mol/L NaOH标准溶液滴定10 mL 0.1 mol/L甘氨酸盐酸盐溶液过程中
的pH变化如图所示。下列说法不正确的是
A. X点溶液中:
B. Y点溶液中甘氨酸主要以 形式存在
C. Z点溶液中:
D. 滴定过程中存在:
13. 在913K、101kPa下,以水蒸气作稀释气, 作催化剂,乙苯脱氢生成苯乙烯时
会发生反应:
反应I: C H C H(g) C H CH=CH(g)+ H(g)(主反应)
6 5 2 5 6 5 2 2
反应II:C H C H(g) C H +CH=CH(g) (副反应)
6 5 2 5 6 6 2 2
反应III:C H C H(g)+ H(g) C H CH(g)+ CH(g) (副反应)
6 5 2 5 2 6 5 3 4
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性
4
学科网(北京)股份有限公司随乙苯转化率的变化曲线如图所示。下列说法正确的是
A. 曲线b代表的产物是苯
B. 加入 可改变乙苯的平衡转化率
C. 曲线a下降是由于反应I的平衡逆向移动
D. 增加水蒸气的充入量,可提高乙苯的平衡转化率
二、 非选择题:本题共4小题,共61分。
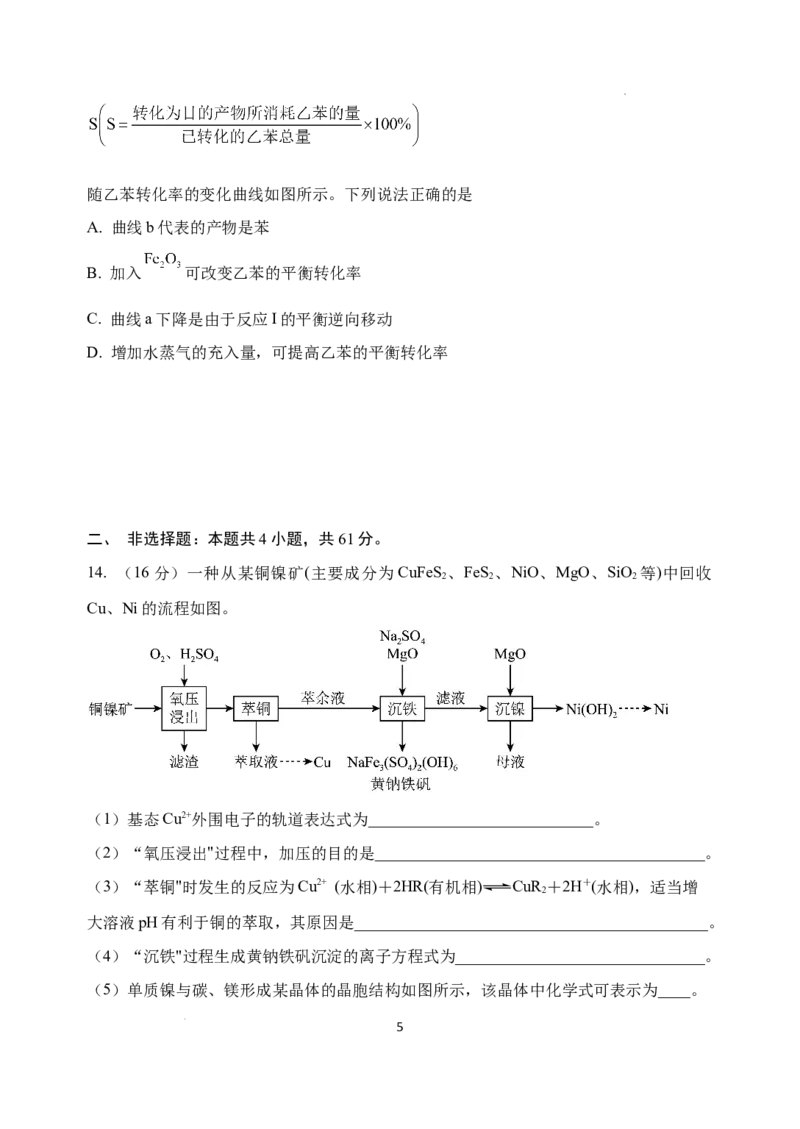
14. (16分)一种从某铜镍矿(主要成分为CuFeS 、FeS 、NiO、MgO、SiO 等)中回收
2 2 2
Cu、Ni的流程如图。
(1)基态Cu2+外围电子的轨道表达式为____________________________。
(2)“氧压浸出"过程中,加压的目的是_________________________________________。
(3)“萃铜"时发生的反应为Cu2+ (水相)+2HR(有机相) CuR +2H+(水相),适当增
2
大溶液pH有利于铜的萃取,其原因是____________________________________________。
(4)“沉铁"过程生成黄钠铁矾沉淀的离子方程式为_______________________________。
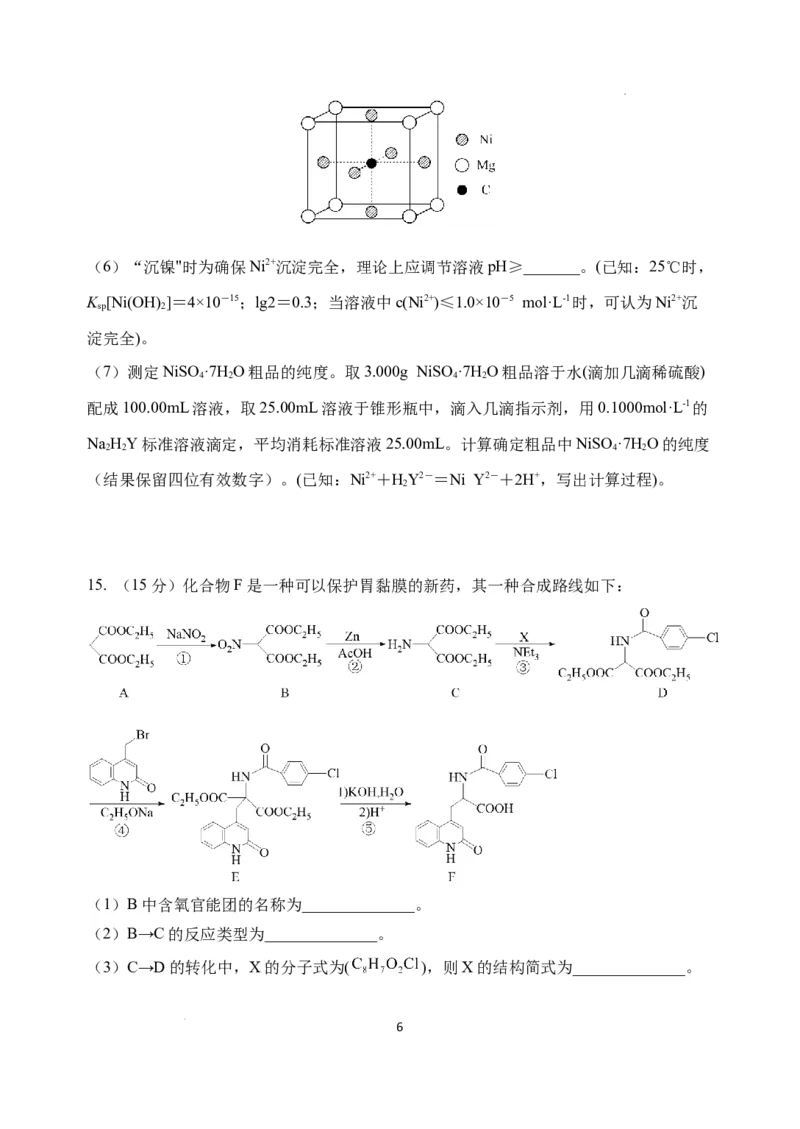
(5)单质镍与碳、镁形成某晶体的晶胞结构如图所示,该晶体中化学式可表示为____。
5
学科网(北京)股份有限公司(6)“沉镍"时为确保Ni2+沉淀完全,理论上应调节溶液pH≥_______。(已知:25℃时,
K [Ni(OH) ]=4×10-15;lg2=0.3;当溶液中c(Ni2+)≤1.0×10-5 mol·L-1时,可认为Ni2+沉
sp 2
淀完全)。
(7)测定NiSO ·7HO粗品的纯度。取3.000g NiSO ·7HO粗品溶于水(滴加几滴稀硫酸)
4 2 4 2
配成100.00mL溶液,取25.00mL溶液于锥形瓶中,滴入几滴指示剂,用0.1000mol·L-1的
NaHY标准溶液滴定,平均消耗标准溶液25.00mL。计算确定粗品中NiSO ·7HO的纯度
2 2 4 2
(结果保留四位有效数字)。(已知:Ni2++HY2-=Ni Y2-+2H+,写出计算过程)。
2
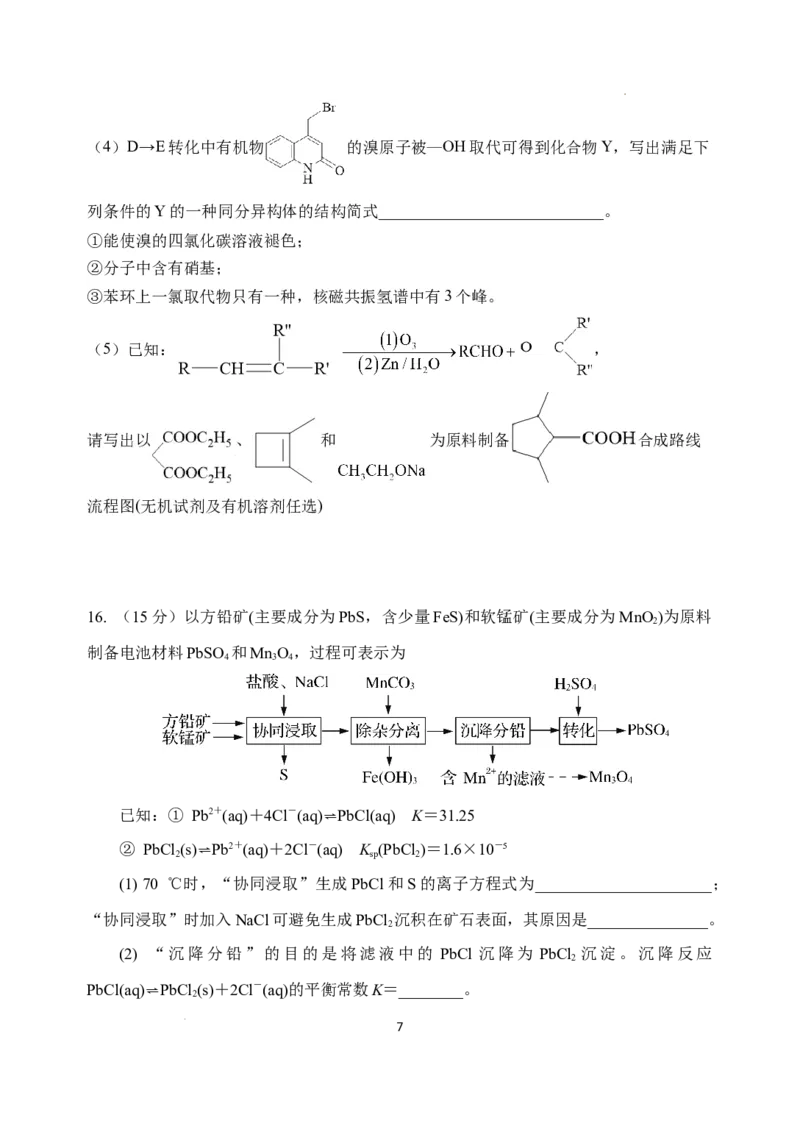
15. (15分)化合物F是一种可以保护胃黏膜的新药,其一种合成路线如下:
(1)B中含氧官能团的名称为______________。
(2)B→C的反应类型为______________。
(3)C→D的转化中,X的分子式为( ),则X的结构简式为______________。
6
学科网(北京)股份有限公司(4)D→E转化中有机物 的溴原子被—OH取代可得到化合物Y,写出满足下
列条件的Y的一种同分异构体的结构简式____________________________。
①能使溴的四氯化碳溶液褪色;
②分子中含有硝基;
③苯环上一氯取代物只有一种,核磁共振氢谱中有3个峰。
(5)已知: ,
请写出以 、 和 为原料制备 合成路线
流程图(无机试剂及有机溶剂任选)
16. (15分)以方铅矿(主要成分为PbS,含少量FeS)和软锰矿(主要成分为MnO )为原料
2
制备电池材料PbSO 和MnO,过程可表示为
4 3 4
已知:① Pb2+(aq)+4Cl-(aq)⇌PbCl(aq) K=31.25
② PbCl
2
(s)⇌Pb2+(aq)+2Cl-(aq) K
sp
(PbCl
2
)=1.6×10-5
(1) 70 ℃时,“协同浸取”生成PbCl和S的离子方程式为______________________;
“协同浸取”时加入NaCl可避免生成PbCl 沉积在矿石表面,其原因是_______________。
2
(2) “沉降分铅”的目的是将滤液中的 PbCl 沉降为 PbCl 沉淀。沉降反应
2
PbCl(aq)⇌PbCl
2
(s)+2Cl-(aq)的平衡常数K=________。
7
学科网(北京)股份有限公司(3) 络合萃取剂全氟聚醚二(甲基吡啶)胺通过氮原子与Pb2+形成配位键的方式萃取铅。
已知氮原子的电子云密度越大配位能力越强,全氟聚醚二(甲基吡啶)胺中氮原子和含氟基
团相连使得配位能力下降,若在氮原子和含氟基团间引入“—CHCHCH—”基团配位
2 2 2
能力会增强,其原因分别是____________________________________________。
(4) 制备MnO 。MnO(难溶于水的黑色晶体)可通过空气氧化Mn2+制得,制备时溶
3 4 3 4
液的温度和pH对MnO 的产率影响如图所示。请补充完整由净化后的含Mn2+的滤液制
3 4
备较纯净的 MnO 的实验方案:取一定量的含 Mn2+的滤液于三颈烧瓶中,
3 4
______________,真空40 ℃干燥得产品MnO(须使用的试剂:空气、蒸馏水、氨水、稀
3 4
硝酸、AgNO 溶液)。
3
17. (15分) 环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。工业
上用乙烯制备EO。
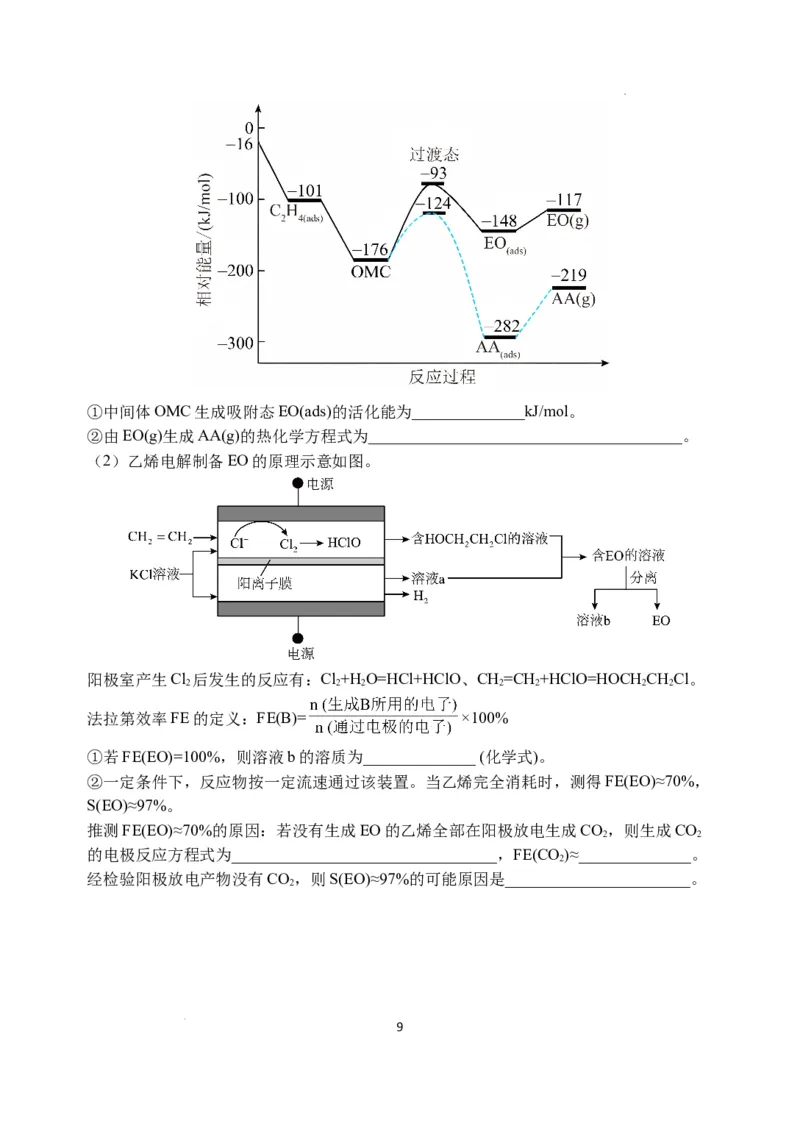
(1)一定条件下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)的过程中部分物料与能
量变化如图所示。
8
学科网(北京)股份有限公司①中间体OMC生成吸附态EO(ads)的活化能为______________kJ/mol。
②由EO(g)生成AA(g)的热化学方程式为_______________________________________。
(2)乙烯电解制备EO的原理示意如图。
阳极室产生Cl 后发生的反应有:Cl+H O=HCl+HClO、CH=CH +HClO=HOCH CHCl。
2 2 2 2 2 2 2
法拉第效率FE的定义:FE(B)= ×100%
①若FE(EO)=100%,则溶液b的溶质为______________ (化学式)。
②一定条件下,反应物按一定流速通过该装置。当乙烯完全消耗时,测得FE(EO)≈70%,
S(EO)≈97%。
推测FE(EO)≈70%的原因:若没有生成EO的乙烯全部在阳极放电生成CO,则生成CO
2 2
的电极反应方程式为_________________________________,FE(CO)≈______________。
2
经检验阳极放电产物没有CO,则S(EO)≈97%的可能原因是_______________________。
2
9
学科网(北京)股份有限公司扬州中学高三下学期化学自主学习效果评估参考答案
题号 1 2 3 4 5 6 7
答案 D C B B A B C
题号 8 9 10 11 12 13
答案 A C D B C D
14.(16分)
(1)略(2分) (2)增大氧气浓度,加快铜镍矿氧化浸出的速率(2分)
(3)增大溶液pH使c(H+)减小,可促进萃取反应正向进行(2分)
(4)Na++3Fe3++ 2SO 2-+3MgO+3HO=NaFe (SO )(OH) ↓+3Mg2+ (3分)
4 2 3 4 2 6
(5)MgNiC(2分) (6)9.3(2分)
3
(7)93.67%(3分)
已知:Ni2++HY2-=Ni Y2-+2H+,
2
则n(Ni2+)=n(HY2-)=0.2000mol/L×25.00×10-3L=2.5000×10-3mol(1分)
2
粗品中 (1分)
粗品中 的纯度 (1分)
15.(1)硝基、酯基(2分) (2)还原反应(2分)
(3) (3分)
(4) 或 (3分)
(5) CHCOCH CHCOCH
3 2 2 3
CHCH(OH)CH CHCH(OH)CH CHCHBrCH CHCHBrCH
3 2 2 3 3 2 2 3
10
学科网(北京)股份有限公司;(5分)
16. (15分)(1) PbS+MnO +4Cl-+4H+=====Mn2++PbCl+S+2HO(3分)
2 2
氯离子浓度增大,促进PbCl (或Pb2+)转化为可溶的PbCl(2分)
2
(2) 2 000(2分)
(3) 含氟基团是吸电子基团,使氮原子上电子云密度下降,配位能力减弱;含氟基团与氮
原子之间引入的“—CHCHCH—”是推电子基团且较大,会减弱含氟基团对氮原子的
2 2 2
影响,配位能力增强(3分)
(4) 将三颈烧瓶水浴加热并保温在50 ℃,(1分)不断搅拌下,通入空气(1分)并滴加
氨水调节溶液的pH并维持在8.5左右(1分),直至有大量黑色沉淀生成时,静置,过
滤,用蒸馏水洗涤沉淀,(1分)至最后一次洗涤滤液中滴加稀硝酸酸化,再滴加硝酸银
无沉淀生成(1分)(共5分)
17.(15分)
(1) ①83 (2分)
(g) = CHCHO(g) ΔH=-102kJ/mol (写EO、AA也可以)(3
3
②
分)
(2) ①KCl (2分)
C H+4H O-12e-=2CO +12H+ (3分)
2 4 2 2
②13 (2分)
溶液a与HOCH CHCl反应不完全 (3分)
2 2
11
学科网(北京)股份有限公司