文档内容
专题09 物质的量浓度
1.【2023年山东卷】一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定有机醇
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸酐完
全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
甲醇标准溶液滴定至终点,消耗标准溶液 。 样品中羟基含量(质量分数)计
算正确的是
A. B.
C. D.
2.【2023年全国甲卷】实验室将粗盐提纯并配制 的 溶液。下列仪器中,本实验必须用
到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
3.(2021·广东真题)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
上述操作中,不需要用到的仪器为A. B. C. D.
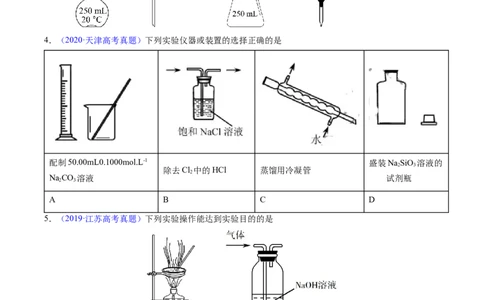
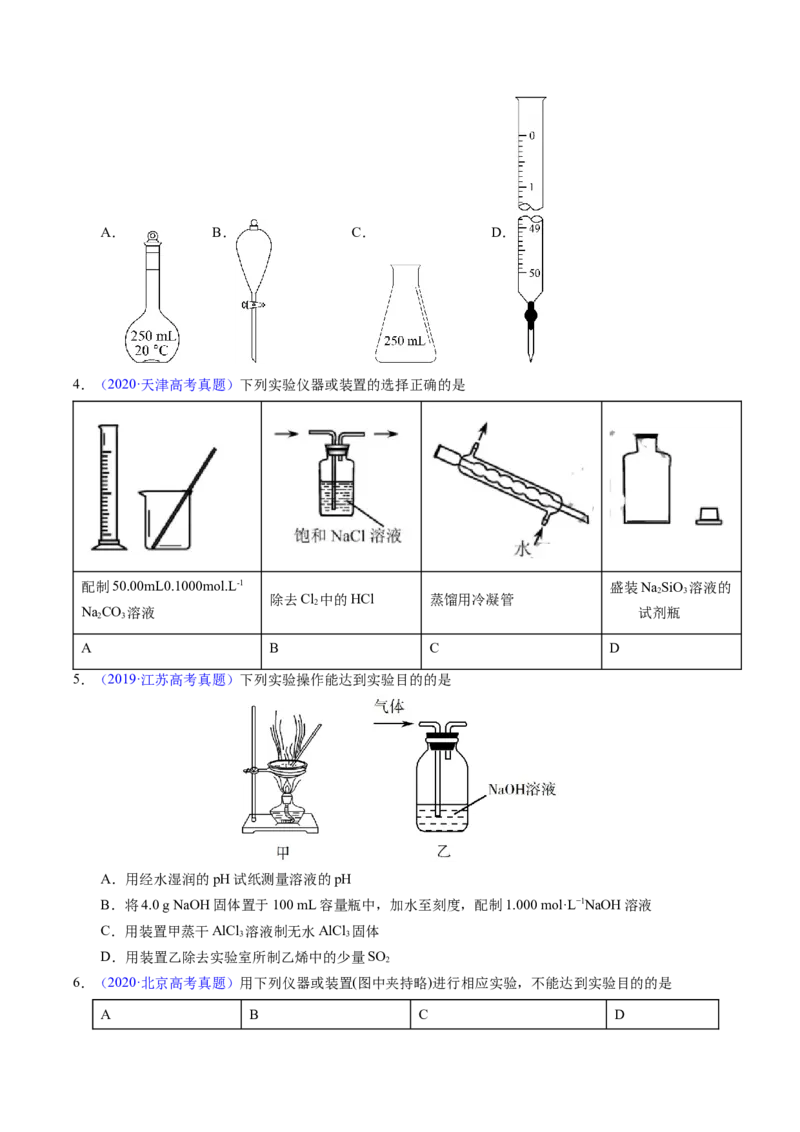
4.(2020·天津高考真题)下列实验仪器或装置的选择正确的是
配制50.00mL0.1000mol.L-1 盛装NaSiO 溶液的
2 3
除去Cl 中的HCl 蒸馏用冷凝管
2
NaCO 溶液 试剂瓶
2 3
A B C D
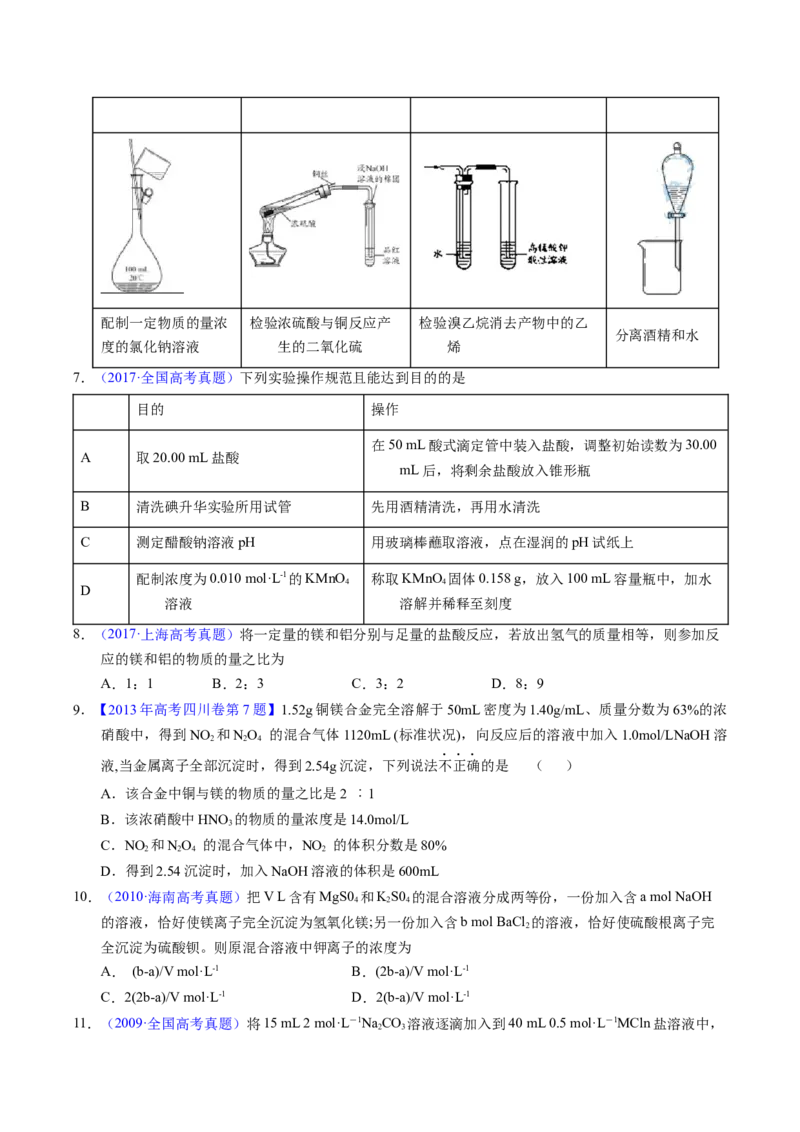
5.(2019·江苏高考真题)下列实验操作能达到实验目的的是
A.用经水湿润的pH试纸测量溶液的pH
B.将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L−1NaOH溶液
C.用装置甲蒸干AlCl 溶液制无水AlCl 固体
3 3
D.用装置乙除去实验室所制乙烯中的少量SO
2
6.(2020·北京高考真题)用下列仪器或装置(图中夹持略)进行相应实验,不能达到实验目的的是
A B C D配制一定物质的量浓 检验浓硫酸与铜反应产 检验溴乙烷消去产物中的乙
分离酒精和水
度的氯化钠溶液 生的二氧化硫 烯
7.(2017·全国高考真题)下列实验操作规范且能达到目的的是
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00
A 取20.00 mL盐酸
mL后,将剩余盐酸放入锥形瓶
B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010 mol·L-1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量瓶中,加水
4 4
D
溶液 溶解并稀释至刻度
8.(2017·上海高考真题)将一定量的镁和铝分别与足量的盐酸反应,若放出氢气的质量相等,则参加反
应的镁和铝的物质的量之比为
A.1:1 B.2:3 C.3:2 D.8:9
9.【2013年高考四川卷第7题】1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓
硝酸中,得到NO 和NO 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶
2 2 4
液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是 ( )
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO 的物质的量浓度是14.0mol/L
3
C.NO 和NO 的混合气体中,NO 的体积分数是80%
2 2 4 2
D.得到2.54沉淀时,加入NaOH溶液的体积是600mL
10.(2010·海南高考真题)把V L含有MgS0 和KS0 的混合溶液分成两等份,一份加入含a mol NaOH
4 2 4
的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl 的溶液,恰好使硫酸根离子完
2
全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A. (b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(2b-a)/V mol·L-1 D.2(b-a)/V mol·L-1
11.(2009·全国高考真题)将15 mL 2 mol·L-1NaCO 溶液逐滴加入到40 mL 0.5 mol·L-1MCln盐溶液中,
2 3恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
12.(2010·湖南高考真题)把500 有BaCl 和KCl的混合溶液分成5等份,取一份加入含 硫酸
2
钠的溶液,恰好使钡离子完全沉淀;另取一份加入含 硝酸银的溶液,恰好使氯离子完全沉淀。
则该混合溶液中钾离子浓度为
A. B.
C. D.
13.(2017·浙江高考真题)用无水NaCO 固体配制250 mL 0.100 0 mol·L-1的溶液。
2 3
请回答下列问题:
(1)在配制过程中不必要的玻璃仪器是________。
A.烧杯 B.量筒 C.玻璃棒 D.胶头滴管 E.容量瓶
(2)定容时的操作:当液面接近容量瓶刻度线时,______________________________________,再将容
量瓶塞盖好,反复上下颠倒,摇匀。
(3)下列操作会使配得的NaCO 溶液浓度偏低的是________。
2 3
A.称取相同质量的NaCO·10H O固体进行配制
2 3 2
B.定容时俯视容量瓶的刻度线
C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制
14.(2017·天津高考真题)[2017天津]用沉淀滴定法快速测定NaI等碘化物溶液中c(I−),实验过程包括准
备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO 基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光
3
保存,备用。
b.配制并标定100 mL 0.1000 mol·L−1 NH SCN标准溶液,备用。
4
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00 mL于锥形瓶中。
b.加入25.00 mL 0.1000 mol·L−1 AgNO 溶液(过量),使I−完全转化为AgI沉淀。
3
c.加入NH Fe(SO ) 溶液作指示剂。
4 4 2
d.用0.1000 mol·L−1 NH SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,
4
停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗NH SCN标准溶液体积/mL 10.24 10.02 9.98
4
f.数据处理。
回答下列问题:(1)将称得的AgNO 配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有__________。
3
(2)AgNO 标准溶液放在棕色试剂瓶中避光保存的原因是___________________________。
3
(3)滴定应在pH<0.5的条件下进行,其原因是___________________________________。
(4)b和c两步操作是否可以颠倒________________,说明理由________________________。
(5)所消耗的NH SCN标准溶液平均体积为_____mL,测得c(I−)=_________________ mol·L−1。
4
(6)在滴定管中装入NH SCN标准溶液的前一步,应进行的操作为________________________。
4
(7)判断下列操作对c(I−)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,则测定结果_______________。
3
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果____________________。
15.(2014·上海高考真题)硫有多种含氧酸,亚硫酸(HSO )、硫酸(HSO )、焦硫酸
2 3 2 4
(HSO ·SO )、硫代硫酸(HSO)等等,其中硫酸最为重要,在工业上有广泛的应用。在实验室,
2 4 3 2 2 3
浓硫酸是常用的干燥剂。完成下列计算:
(1)焦硫酸(HSO ·SO )溶于水,其中的SO 都转化为硫酸。若将445g焦硫酸溶于水配成4.00L硫酸,
2 4 3 3
该硫酸的物质的量浓度为________mol/L。
(2)若以浓硫酸吸水后生成的HSO ·H O计算,250g质量分数为98%的硫酸能吸收_____g水
2 4 2
(3)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:
3FeS+8O=Fe O+6SO 4FeS+11 O =2Fe O+8SO
2 2 3 4 2 2 2 2 3 2
若48mol FeS 完全反应耗用氧气2934.4L(标准状况),计算反应产物中Fe O 与Fe O 物质的量之比
2 3 4 2 3
_______。
(4)用硫化氢制取硫酸,既能充分利用资源又能保护环境,是一种很有发展前途的制备硫酸的方法。
硫化氢体积分数为0.84的混合气体(HS、HO、N)在空气中完全燃烧,若空气过量77%,计算产
2 2 2
物气体中SO 体积分数________(水是气体)。(已知空气组成:N 体积分数0.79、O 体积分数
2 2 2
0.21)
16.(2017·上海高考真题)(2017·上海卷)10.7g 氯化铵和足量的氢氧化钙混合后充分加热,再将所生成的
气体完全溶于水后得 50 mL 溶液,计算:
(1)可生成标准状况下的氨气多少升?______________
(2)所得溶液的物质的量浓度是多少? ______________
17.(2017·上海高考真题)6克冰醋酸完全溶于水配成500毫升溶液,用此醋酸溶液滴定20毫升某一未知
浓度的氢氧化钠溶液,共消耗这种醋酸溶液30毫升。求:
(1)醋酸溶液的物质的量的浓度_________。
(2)未知氢氧化钠溶液的物质的量的浓度________________。
18.(2017·上海高考真题)有3克镁铝合金完全溶于盐酸后得到标准状况下的氢气3360毫升,在所得的
溶液中加入足量的浓氨水可得沉淀质量_________克。
19.(2015·江苏高考真题)软锰矿(主要成分MnO ,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中
2
SO 反应可制备MnSO ·H O,反应的化学方程式为MnO +SO MnSO 。
2 4 2 2 2 4
(1)质量为17.40 g纯净MnO 最多能氧化____L(标准状况)SO 。
2 2(2)已知:K [Al(OH) ]=1×10-33,K [Fe(OH) ]=3×10-39,pH=7.1时Mn(OH) 开始沉淀。室温下,除去
sp 3 sp 3 2
MnSO 溶液中的Fe3+、Al3+(使其浓度均小于1×10-6mol·L-1),需调节溶液pH范围为____。
4
(3)下图可以看出,从MnSO 和MgSO 混合溶液中结晶MnSO ·H O晶体,需控制结晶温度范围为____。
4 4 4 2
(4)准确称取0.171 0 g MnSO ·H O样品置于锥形瓶中,加入适量HPO 和NH NO 溶液,加热使Mn2+全
4 2 3 4 4 3
部氧化成Mn3+,用c(Fe2+)=0.050 0 mol·L-1的标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),消
耗Fe2+溶液20.00 mL。计算MnSO ·H O样品的纯度(请给出计算过程)_____。
4 2
20.(2007·上海高考真题)一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液
(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。
(1)原NaOH溶液的质量分数为___________
(2)所得溶液中Cl-的物质的量为_______mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl ):n(H )=_____________。
2 2
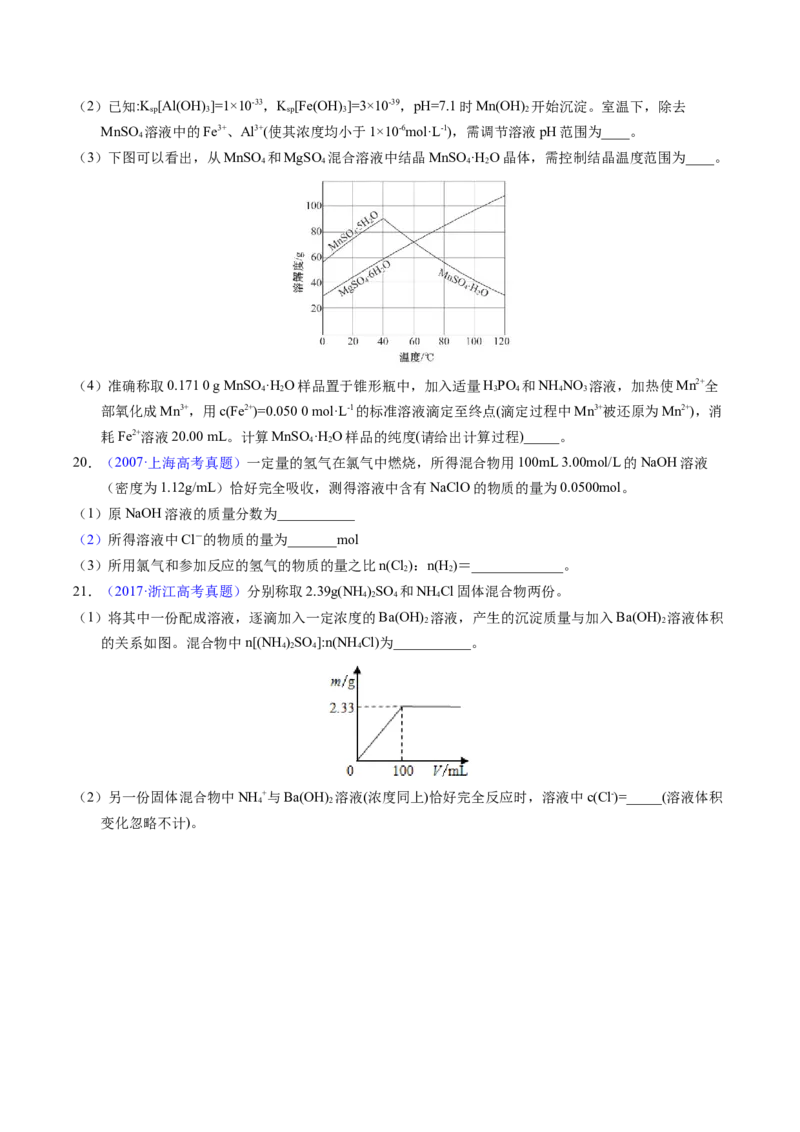
21.(2017·浙江高考真题)分别称取2.39g(NH)SO 和NH Cl固体混合物两份。
4 2 4 4
(1)将其中一份配成溶液,逐滴加入一定浓度的Ba(OH) 溶液,产生的沉淀质量与加入Ba(OH) 溶液体积
2 2
的关系如图。混合物中n[(NH )SO ]:n(NH Cl)为___________。
4 2 4 4
(2)另一份固体混合物中NH +与Ba(OH) 溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_____(溶液体积
4 2
变化忽略不计)。