文档内容
化学参考答案· 第1⻚(共10⻚)
学科⽹(北京)股份有限公司
⻄南名校联盟2025 届“ 3+3+3” ⾼考备考诊断性联考(⼆)
化学参考答案
⼀、选择题:本题共14 ⼩题,每⼩题3 分。
题号
1
2
3
4
5
6
7
答案
B
A
D
C
B
D
D
题号
8
9
10
11
12
13
14
答案
A
C
C
B
D
D
A
【解析】
1.⻘铜为铜锡合⾦,A 正确。黏⼟在⾼温中烧结,会发⽣⼀系列的化学反应,此过程有新化
学键的形成,该过程涉及化学变化,B 错误。清《午端图》宣纸画是将画作在宣纸上,纸
的主要成分是纤维素,C 正确。松⽊在窑中不完全燃烧会⽣成碳单质,可以⽤来制造墨块,
D 正确;故答案选B。
2.CaO 是离⼦化合物,电⼦式为
,A 正确。
主链有6 个碳原⼦,3 号碳原
⼦上连有1 个甲基,化学名称:3−甲基⼰烷,B 错误。氯化氢为共价化合物,形成过程为
,C 错误。图中是由两个氯原⼦的p 轨道肩并肩形成的p−p π键不是σ
键,D 错误;答案选A。
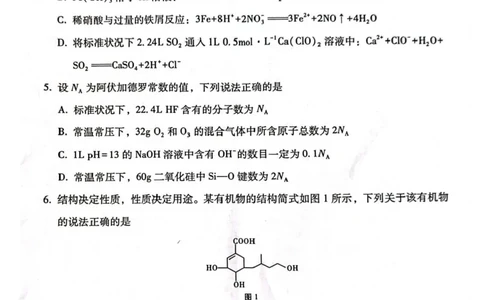
3.亚硝酸钠是⼀种常⽤⻝品添加剂,具有抑菌、发⾊、抗氧化和改善⻛味的作⽤,⼴泛应⽤
于⾁制品的防腐,但不能⼤量使⽤,A 错误。清晨树林间光亮的通路是胶体的丁达尔效应,
未发⽣化学变化,不涉及氧化还原反应,B 错误。⻘砖中铁元素主要以Fe2O3 存在,C 错误。
太阳能、⻛能和氢能等均为清洁能源,替代化⽯能源,可减少⼆氧化碳的排放,有利于实
现低碳经济,D 正确;故选D。
4.盐酸中有⼤量氢离⼦,钠优先与盐酸中的氢离⼦反应,故离⼦⽅程式为2Na
+2H+=2Na++H2↑,A 错误。Fe(OH)3 难溶于⽔,应写化学式,离⼦⽅程式为2Fe
(OH)3+2I−+6H+=2Fe2++
I2+6H2O,B 错误。过量的铁屑可与Fe3+继续反应⽣成Fe2+,C 正确。标准状况下2.24LSO2
物质的量为0.1mol,通⼊1L 0.5mol· L−1Ca(ClO)2 溶液中,SO2 不⾜,部分ClO−与SO2 发
⽣氧化还原反应,⽣成Cl−和
,未反应的ClO−会与产⽣的氢离⼦反应⽣成HClO,
=
,D 错误;故选C。
5.标准状况下,氟化氢为液态,⽆法计算22.4L 氟化氢的物质的量和含有的分⼦数⽬,A 错
化学参考答案· 第2⻚(共10⻚)
学科⽹(北京)股份有限公司
误。O2 和O3 均是氧原⼦构成的单质,即常温常压下32g O2 和O3 的混合⽓体中所含氧原
⼦物质的量为2mol,即总数为
,B 正确。由于温度不同,⽔的离⼦积不同,所以pH=13
的NaOH 溶液中含有的氢氧根离⼦不⼀定为0.1mol,C 错误。60g SiO2 的物质的量是1mol,
由于在SiO2 晶体中每个Si 原⼦与4 个O 原⼦形成4 个Si—O 共价键,故1mol SiO2 中含有
的Si—O 共价键数⽬是4NA,D 错误;故选B。
6.羧基和羟基均可以与⾦属钠发⽣反应产⽣氢⽓,因此2mol 该化合物与⾜量的⾦属钠反应
产⽣氢⽓的物质的量为4mol,A 错误。该物质中有sp3 杂化,并连接4 个不相同取代基的
碳,B 错误。根据有机物结构简式得到分⼦式为C12H20O5,发⽣加聚反应形成⾼聚物时不会脱
落⼩分⼦,故形成⾼聚物的分⼦式为C12nH20nO5n,C 错误。该有机物分⼦中有羟基(—OH)、
羧基(—COOH)两种含氧官能团,D 正确;选D。
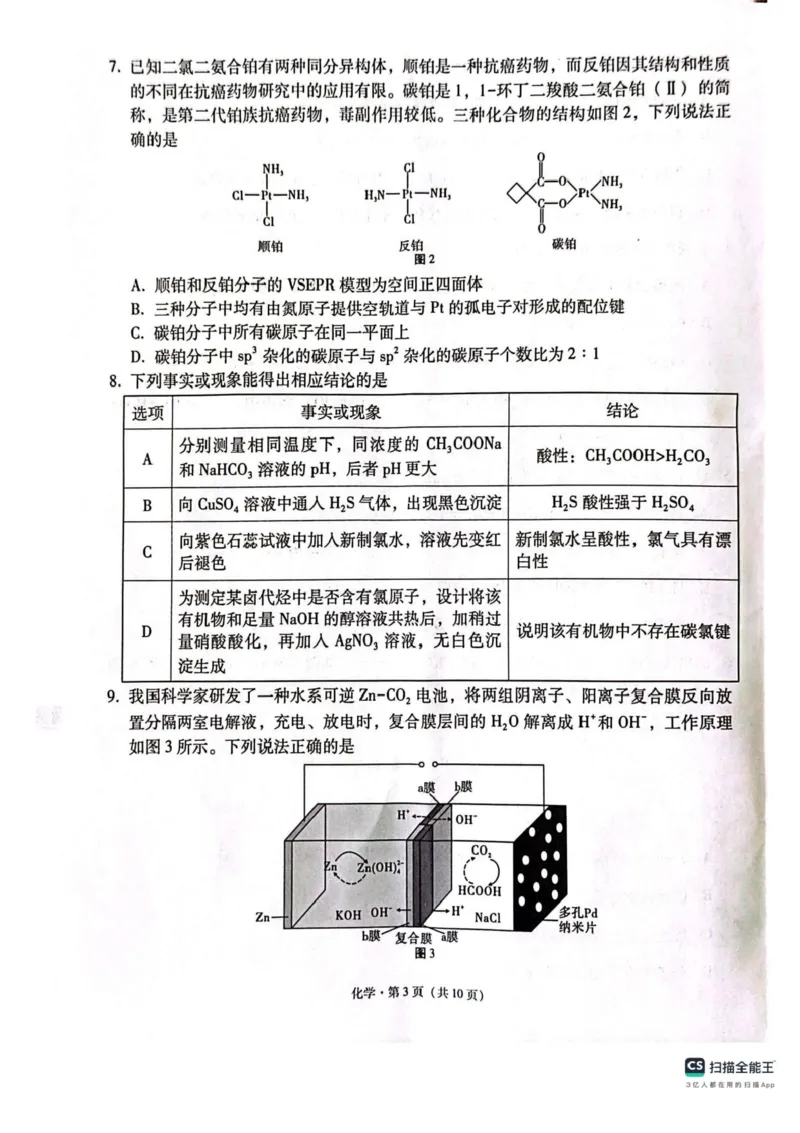
7.若顺铂和反铂的VSEPR 模型为正四⾯体结构,则就不会有顺反两种同分异构,所以两种
分⼦的VSEPR 模型应该为平⾯正⽅形,A 错误。三种分⼦中氮原⼦价层电⼦对数均为4,
氮的杂化⽅式是sp3,氨中氮原⼦的孤电⼦对与Pt 的空轨道形成了配位键,B 错误。根据
甲烷是正四⾯体结构,碳铂分⼦中有⼀个碳原⼦与四个碳原⼦相连,则碳铂分⼦中所有碳
原⼦⼀定不在同⼀平⾯上,C 错误。碳铂分⼦中sp3 杂化的碳原⼦有4 个(左边4 个),sp2
杂化的碳原⼦为碳氧双键的碳原⼦,有2 个,因此个数⽐为2∶1,D 正确;综上所述,答
案为D。
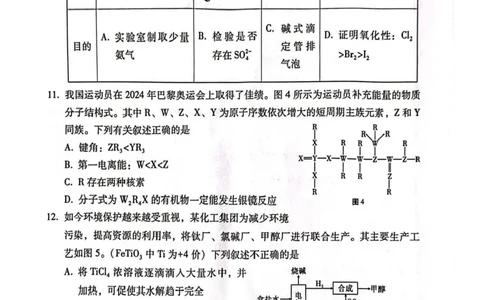
8.相同温度下相同浓度的钠盐溶液中,弱酸根离⼦⽔解程度越⼤,溶液的pH 越⼤,则相同
温度下相同浓度的CH3COONa 与NaHCO3 溶液,后者的pH ⼤,⽔解程度:CH3COO−<
,故可说明酸性:CH3COOH>H2CO3,A 正确。出现⿊⾊沉淀CuS,是因为硫化铜
的Ksp 较⼩,因此反应能进⾏,并不能说明酸性强弱,B 错误。向紫⾊⽯蕊试液中加⼊新
制氯⽔,新制氯⽔中含有HCl,呈酸性,则溶液先变红,氯⽓还含有次氯酸,次氯酸具有
漂⽩性使溶液褪⾊,C 错误。⻧代烃在NaOH 醇溶液中加热发⽣消去反应,由于不是所有
的⻧代烃都能发⽣消去反应,故将待测有机物和⾜量NaOH 的醇溶液共热后,加稍过量硝
酸酸化,再加⼊AgNO3 溶液,⽆⽩⾊沉淀⽣成,不能说明有机物中是否含有氯原⼦,D 错
误;故选A。
9.根据图示可知,放电时是原电池,放电时,负极为锌,锌在负极失去电⼦⽣成锌离⼦,结
合复合膜层电离出的氢氧根离⼦⽣成
,负极的电极反应式为Zn+4OH−−2e−
=
,多孔Pd 纳⽶⽚为正极,⼆氧化碳在正极得到电⼦转化为甲酸,电极反应为CO2
+ 2 H + + 2 e −= H C O O H ,总的电极反应为Z n + 2 O H −+ 2 H 2 O + C O 2=
+HCOOH,充电时的电极反应与放电时的反应相反。由图可知,a 膜释放出氢离
⼦,是阳离⼦膜,b 膜释放出氢氧根离⼦,是阴离⼦膜,A 错误。CO2 得电⼦⽣成HCOOH,
化学参考答案· 第3⻚(共10⻚)
学科⽹(北京)股份有限公司
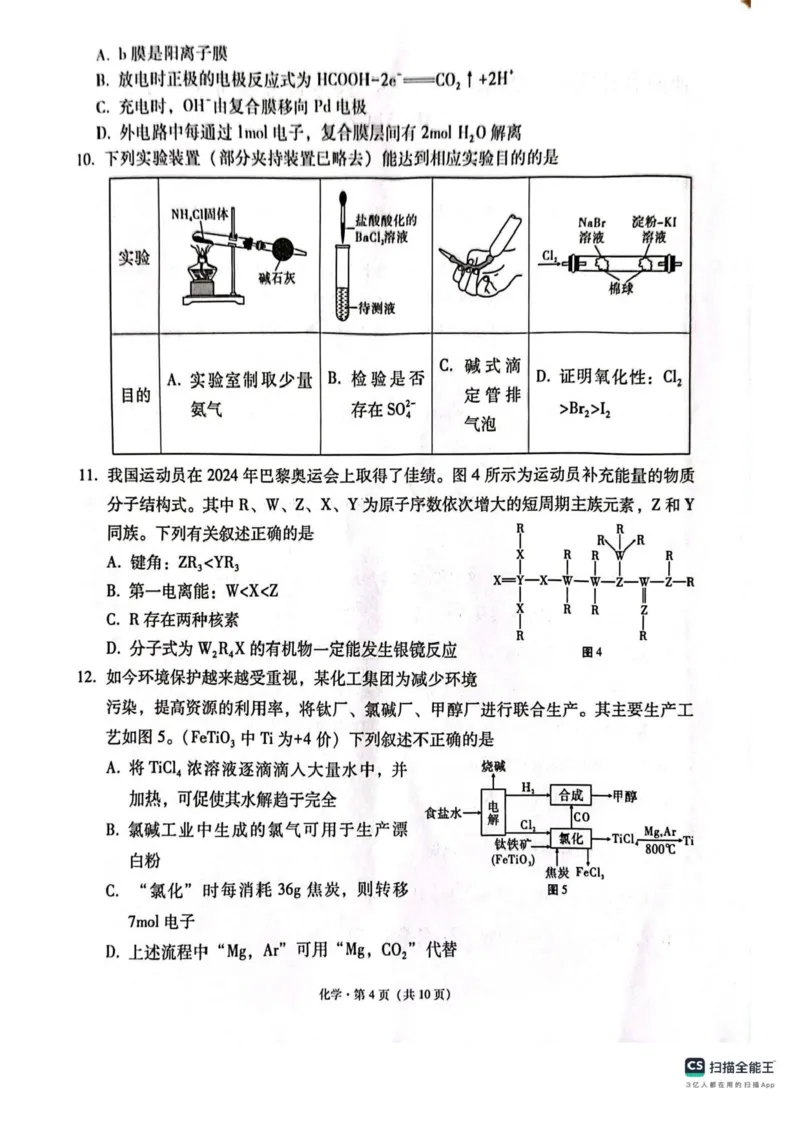
电极反应为CO2+2e−+2H+=HCOOH,B 错误。充电时,阴离⼦向阳极移动,OH−由双
极膜移向Pd 电极,C 正确。根据两极的电极反应⽅程式可知,复合膜层间的H2O 解离成
H+和OH−,外电路中每通过1mol 电⼦,复合膜层间有1mol H+和1mol OH−分别向两极移
动,有1mol H2O 解离,D 错误;故选C。
10.直接加热氯化铵固体不能制得氨⽓,氯化铵受热分解⽣成氨⽓和氯化氢,但在试管⼝遇冷,
氨⽓和氯化氢会重新化合为氯化铵,实验室制取少量氨⽓应该是氯化铵和氢氧化钙固体
加热,不能达到实验⽬的,A 错误。在待测液中加⼊盐酸酸化的氯化钡溶液⽣成⽩⾊沉淀,
沉淀可能为氯化银,不能说明待测液中存在
,不能达到实验⽬的,B 错误。排掉碱
式滴定管⽓泡正确操作为使橡胶管弯曲,管尖斜向上约45 度,然后轻轻挤压玻璃球使尖
嘴部分充满碱液,C 正确。氯⽓也能与碘化钾反应⽣成碘单质使淀粉变蓝⾊,不能证明氧
化性Br2>I2,不能达到实验⽬的,D 错误;故选C。
11.Y 可形成5 个共价键,Z 可形成3 个共价键,Z 和Y 同族,Y 原⼦序数⽐Z ⼤,即Z 为N
元素,Y 为P 元素,W 可形成4 个共价键,原⼦序数⽐N ⼩,即W 为C 元素,R 可形成
1 个共价键,原⼦序数⽐C ⼩,即R 为H 元素,X 可形成2 个共价键,原⼦序数在N 和
P 之间,即X 为O 元素,综上所述,R 为H 元素、W 为C 元素、Z 为N 元素、X 为O
元素、Y 为P 元素。由于N 的电负性⽐P 强,NH3 中共⽤电⼦对更靠近N,因此电⼦对
间的斥⼒较⼤,键⻆较⼤,⽽PH3 中共⽤电⼦对相对于NH3 来说离的中⼼原⼦P 更远⼀
些,因此电⼦对间的斥⼒较⼩,键⻆较⼩,故键⻆NH3>PH3,A 错误。同周期元素从左
到右第⼀电离能有增⼤趋势,第ⅡA 族、第ⅤA 族原⼦第⼀电离能⼤于同周期相邻元素,
即第⼀电离能C<O<N,B 正确。R 为氢,存在
、
、
三种核素,C 错误。C2H4O
存在同分异构体,其中含有醛基的CH3CHO 可以发⽣银镜反应,⽽环氧⼄烷(
)中不
含醛基,不能发⽣银镜反应,D 错误;故选B。
12.利⽤TiCl4 ⽔解制TiO2· xH2O 时,应加⼊⼤量的⽔,并且加热以促进其⽔解反应正向进
⾏,但不能加强热,以免使TiO2· xH2O 受热失去结晶⽔,A 正确。氯碱⼯业中⽣成的氯
⽓与⽯灰乳反应,可⽤于⽣产漂⽩粉,B 正确。“氯化”反应,7Cl2
+2FeTiO3+6C=6CO+2TiCl4+2FeCl3,每消耗36g 焦炭即3mol,则转移7mol 电⼦,C
正确。⼆氧化碳和镁会反应,因此不能⽤⼆氧化碳来作保护⽓,D 错误;故选D。
13.酸性:HCOOH>CH3COOH,表明HCOOH ⽐CH3COOH 易发⽣电离,也就是前者羟基
的极性⽐后者羟基的极性强,A 错误。H2O 中O 原⼦的价层电⼦对数为
,
化学参考答案· 第4⻚(共10⻚)
学科⽹(北京)股份有限公司
采⽤
杂化,
中S 原⼦的价层电⼦对数为
,采⽤
杂化,⼆者中⼼
原⼦的杂化⽅式不同,B 错误。⾦属性越强,其最⾼价氧化物对应⽔化物的碱性越强,C
错误。冠醚12−冠−4 能够与Li+形成超分⼦,是因为Li+半径⼩与冠醚的空腔匹配,K+半
径⼤,与该冠醚的空腔不匹配,故不能与之形成超分⼦,D 正确;故选D。
14.由于AgI、AgSCN 中阴、阳离⼦均为1∶1,则两者图像平⾏,且相同条件下
溶解
度⼤于AgI,即Ksp(
)>Ksp(AgI),所以曲线②表示AgSCN,曲线③表示AgI,曲线
①表示Ag2CrO4。由分析,曲线②为AgSCN 沉淀溶解平衡曲线,曲线③对应AgI,A 正
确。由点(8.1,8.1)可知,
,同理,由点(6,
6)可知,
,当碘离⼦完全沉淀时
,
,此时对
SCN−⽽⾔,
,
没有⽣成沉淀,故浓度均
为
的
和
可通过分步沉淀进⾏分离,B 错误。
,数量级为
,C 错误。由图,a 点在
曲线②上⽅,则QKsp,为过饱和溶液,故能⽣成AgI 沉淀,D 错误;故选A。
⼆、⾮选择题:本题共4 ⼩题,共58 分。
15.(除特殊标注外,每空2 分,共15 分)
(1)恒压分液漏⽃(1 分,答恒压滴液漏⽃给分,答分液漏⽃不给分)
将部分NO 转
化为NO2,形成NO 和NO2 混合⽓体(答到将部分NO 转化为NO2 给2 分,只答将NO
转化成NO2 不给分)
(2)(NH4)2CO3+NO2+NO=2NH4NO2+CO2(化学式有错,物质有缺漏不给分,⽅程式
未配平扣1 分)
(有错不给分)
(3)(NH4)2SO4
羟胺(NH2OH)受热易分解,所以过滤后将滤液进⾏减压蒸馏,防⽌
其分解(答到蒸馏温度⾼羟胺受热易分解,就可得分)
(4)410cV%(不写成百分数不给分)
BC(答对⼀个给1 分,有错不给分)
【解析】装置A 为恒压分液漏⽃。铜与稀硝酸反应制NO,为避免NO 被氧⽓完全氧化成
NO2,先⽤氮⽓排净整个装置的空⽓,之后制取的NO 从e ⼝进⼊,打开k3,仅使部分
化学参考答案· 第5⻚(共10⻚)
学科⽹(北京)股份有限公司
NO 被氧⽓氧化转化成NO2,得到NO 和NO2 的混合⽓体,从f ⼝出,连b 进⼊三颈
烧瓶;⽤70%左右的硫酸与亚硫酸钠固体制取⼆氧化硫,从c ⼝进⼊三颈烧瓶,反应
后继续通氮⽓,将没有反应完的NO、NO2、SO2 排出,进⾏尾⽓吸收。步骤Ⅰ是NO、
NO2 与碳酸铵溶液反应得到NH4NO2,根据元素守恒可知⽓体为CO2,其化学⽅程式
为(NH4)2CO3+NO2+NO=2NH4NO2+CO2。
(2)接受质⼦能⼒越强,对应的碱溶液碱性越强,则其盐溶液的⽔解程度越弱,所以等
浓度的(NH3OH)2SO4 和(NH4)2SO4 的混合溶液中离⼦浓度由⼤到⼩的顺序为
。
(3)分离(NH3OH)2SO4 和(NH4)2SO4,向混合溶液中加⼊氨⽔,(NH3OH)2SO4 与氨⽔发⽣
反应⽣成NH2OH 和(NH4)2SO4 的混合溶液,羟胺(NH2OH)易溶于甲醇,
在
甲醇中溶解度较⼩,所以加⼊甲醇会得到(NH4)2SO4 晶体,⼜因为羟胺(NH2OH)受热易
分解,所以过滤后将滤液进⾏减压蒸馏,防⽌其分解。
(4)(NH3OH)2SO4 中氮元素化合价为−1 价,氧化产物⼀氧化⼆氮中氮元素化合价为+
1 价,与铁离⼦反应时,铁离⼦被还原为+2 价,根据氧化还原反应电⼦得失守恒可
得出:(NH3OH)2SO4~4Fe3+~4Fe2+,⽤⾼锰酸钾滴定时⾼锰酸钾与亚铁离⼦的关系
为
5Fe2+~KMnO4,所以
5(NH3OH)2SO4~4KMnO4,样品的纯度为
。未⼲燥锥形瓶,不影响锥形瓶中待测液的物质的量,对结果⽆
影响,A 错误。未⽤待测液润洗滴定管,相当于直接稀释待测液,所测浓度偏低,B 正确。
观察读数时,滴定前仰视,则标准液初次读数读⼤,滴定后俯视,则标准液末次读数读⼩,
相当于标准液的体积读数⼩,所测结果偏低,C 正确。滴定前滴定管尖嘴部分有⽓泡,滴
定后⽓泡消失,相当于标准液体积偏⼤,所测结果偏⾼,D 错误;故选BC。
16.(除特殊标注外,每空2 分,共14 分)
(1)搅拌(或将阳极泥粉碎等)(按标准答案给分)
(2)H2O>H2Se>H2S(不填化学式不给分)
(3)CuSe+4H2SO4(浓)△CuSO4+3SO2↑+SeO2+4H2O(化学式有错,物质有缺漏不给分,
⽅程式未配平扣1 分,加热符号,⽓体符号没写不扣分)
(4)H2SO4(不填化学式不给分)
蒸发浓缩(1 分)(加热浓缩也给分,蒸发结晶不给
分)
冷却结晶(1 分)(降温结晶也给分)
(5)①4
②
(算出化简正确也给分)(合理答案均给分)
化学参考答案· 第6⻚(共10⻚)
学科⽹(北京)股份有限公司
【解析】(1)“ 硫酸化焙烧” 即将阳极泥与浓硫酸混合均匀,在350~500℃下焙烧,为了
加快该过程反应速率,该过程中可采取的措施可以是搅拌、将阳极泥粉碎等。
(2)H2O、H2Se、H2S 都为分⼦晶体,⽔分⼦之间存在氢键。相对分⼦质量H2Se>H2S,
分⼦间作⽤⼒H2Se>H2S,则沸点H2O>H2Se>H2S。
(3)CuSe 与浓H2SO4 发⽣氧化还原反应,产⽣SO2、SeO2 的混合⽓体,同时⽣成CuSO4,
根据电⼦守恒、原⼦守恒,可得反应的化学⽅程式为CuSe+4H2SO4(浓)△CuSO4+3SO2↑
+SeO2+4H2O。
(4)根据2RH+Cu2+
R2Cu+2H+,增⼤氢离⼦浓度,反应逆向进⾏,反萃取得到硫酸
铜溶液,则“ 反萃取剂” 最好选⽤H2SO4 溶液;得到的⽔相中含有CuSO4 溶液,从中获
得胆矾,根据CuSO4 的溶解度受温度的影响变化较⼤,可采⽤的操作Ⅱ为蒸发浓缩、冷
却结晶、过滤、洗涤、⼲燥。
(5)Li 位于顶点和体内,个数为
,Fe 位于⾯上,个数为
,Se 位于棱
上和体内,个数为
,该超导材料的化学式为LiFe2Se2;由晶胞图可知距离Se
原⼦最近的Fe 原⼦的个数为4;晶胞的质量为
,晶胞的体积为
,晶体密度为
。
17.(每空2 分,共14 分)
Ⅰ.(1)
=
(若系数翻倍,反应热数值正
确也给分,物质状态未写扣1 分,单位未写扣1 分,数值错误扣1 分,没有负号扣1 分)
(2)C
在1423K~1473K 区间内,⽤C 作还原剂时,
更⼩,热⼒学趋势更⼤(答到
更⼩,反应更容易进⾏也得分)
Ⅱ.(1)c
(2)17.9
(3)B
(4)图甲中曲线c 在1273K 时积碳⼏乎为零,则主要发⽣反应Ⅰ,温度升⾼反应Ⅰ向正
反应⽅向移动,产物H2、CO 增多(合理答案也给分)
【解析】Ⅰ.(1)燃烧热是在101kPa 时,1mol 物质完全燃烧⽣成稳定的氧化物时所放出
化学参考答案· 第7⻚(共10⻚)
学科⽹(北京)股份有限公司
的热量;由盖斯定律可知,
反应
反应
反应2,可得
=
,其
。
(2)⼯业还原熔炼粗锑的温度⼀般为1423K~1473K,结合图,⽤C 作还原剂,原因是在
1423K~1473K 区间内,⽤C 作还原剂时,
更⼩,热⼒学趋势更⼤。
Ⅱ.
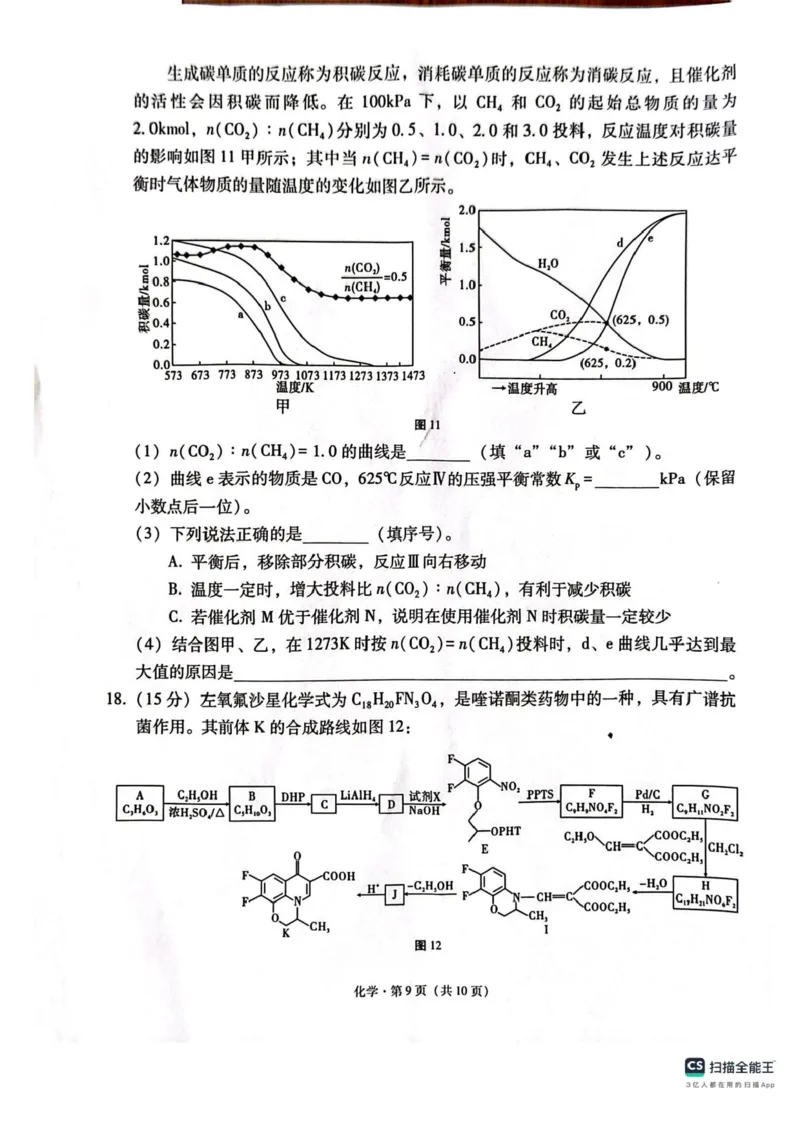
(1)结合图像中
∶
时积碳量最⾼,其
∶
分别为1.0、
2.0 和3.0 时降低,说明随着CO2 的量增多,积碳量减少,故
∶
的曲
线是c。
(2)初始投料
,
时
,
,由H 元素守恒可知
,反应Ⅳ
。
(3)积碳为固体,平衡后,移除部分积碳,反应Ⅲ不移动,A 错误。根据图像随着CO2
的量增多,积碳量减少,故温度⼀定时,增⼤投料⽐
∶
,有利于减少积碳,
B 正确。催化剂只改变反应速率,不能改变积碳量,即使催化剂M 优于催化剂N,使⽤
催化剂N 时积碳量也不会减少,C 错误;故选B。
(4)结合图甲、⼄,在1273K 时按
=
投料时,d、e 曲线⼏乎达到最⼤值的
原因是图甲中曲线c 在1273K 时积碳⼏乎为零,则主要发⽣反应Ⅰ,温度升⾼反应Ⅰ向
正反应⽅向移动,产物H2、CO 增多。
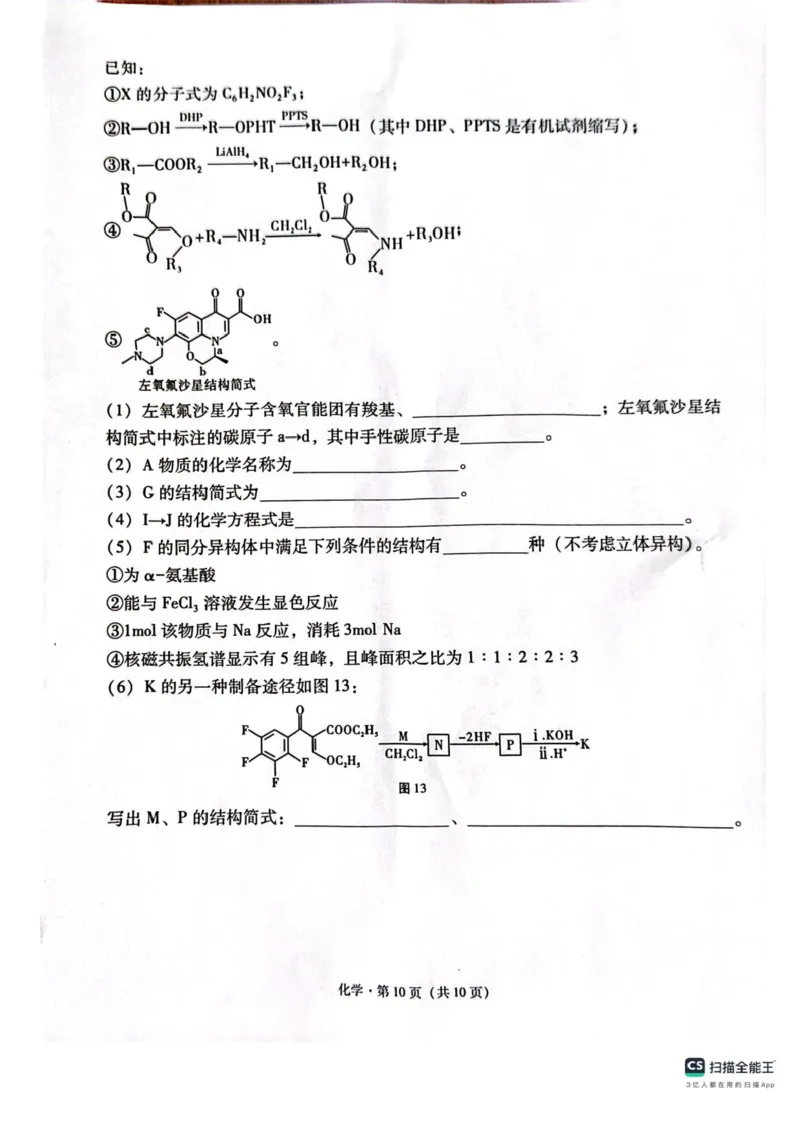
18.(除特殊标注外,每空2 分,共15 分)
(1)醚键、羰基(每个1 分,多答倒扣分,有错别字不给分)
a(1 分)(多答不给分)
(2)2−羟基丙酸(或α−羟基丙酸)
(3)
化学参考答案· 第8⻚(共10⻚)
学科⽹(北京)股份有限公司
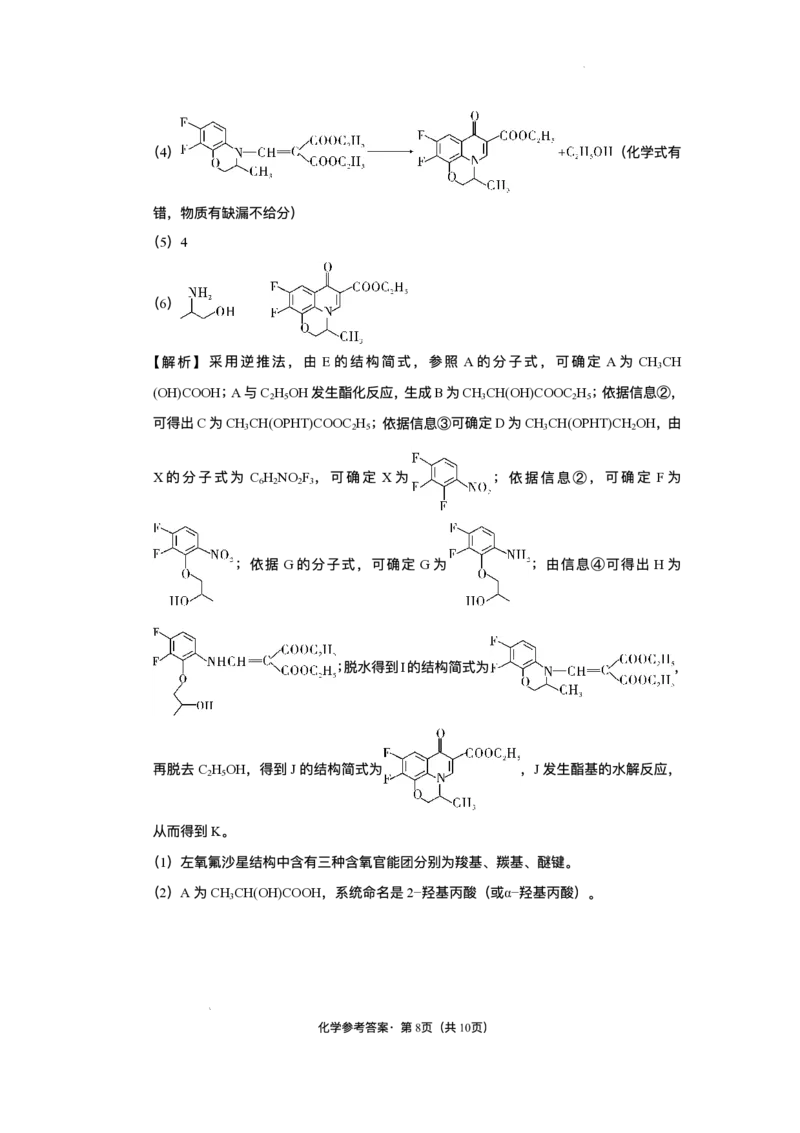
(4)
(化学式有
错,物质有缺漏不给分)
(5)4
(6)
【解析】采⽤逆推法,由E 的结构简式,参照A 的分⼦式,可确定A 为CH3CH
(OH)COOH;A 与C2H5OH 发⽣酯化反应,⽣成B 为CH3CH(OH)COOC2H5;依据信息②,
可得出C 为CH3CH(OPHT)COOC2H5;依据信息③可确定D 为CH3CH(OPHT)CH2OH,由
X 的分⼦式为C6H2NO2F3,可确定X 为
;依据信息②,可确定F 为
;依据G 的分⼦式,可确定G 为
;由信息④可得出H 为
;脱⽔得到I的结构简式为
,
再脱去C2H5OH,得到J 的结构简式为
,J 发⽣酯基的⽔解反应,
从⽽得到K。
(1)左氧氟沙星结构中含有三种含氧官能团分别为羧基、羰基、醚键。
(2)A 为CH3CH(OH)COOH,系统命名是2−羟基丙酸(或α−羟基丙酸)。
化学参考答案· 第9⻚(共10⻚)
学科⽹(北京)股份有限公司
(3)根据分析可知G 为F 发⽣还原反应得到的,结构简式为
。
(4)I(
)→J(
),发⽣取代反应,
化学⽅程式是
。
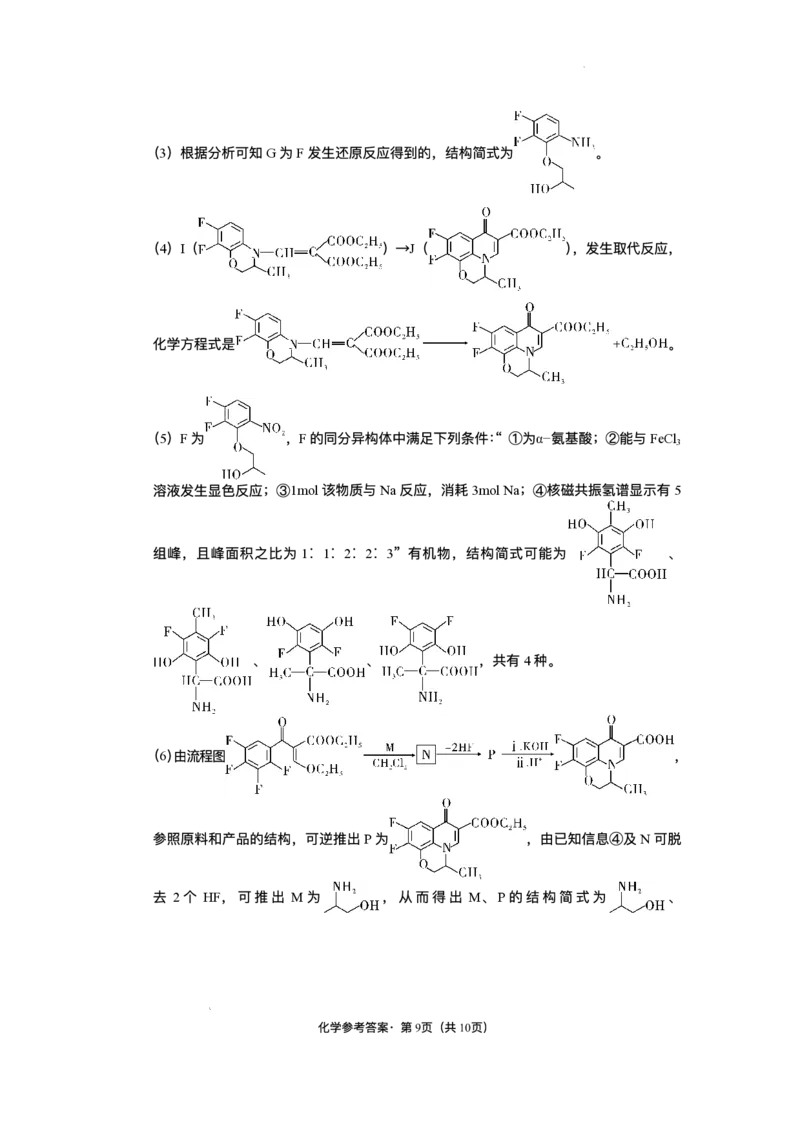
(5)F 为
,F 的同分异构体中满⾜下列条件:“ ①为α−氨基酸;②能与FeCl3
溶液发⽣显⾊反应;③1mol 该物质与Na 反应,消耗3mol Na;④核磁共振氢谱显示有5
组峰,且峰⾯积之⽐为1∶1∶2∶2∶3” 有机物,结构简式可能为
、
、
、
,共有4 种。
(6)由流程图
,
参照原料和产品的结构,可逆推出P 为
,由已知信息④及N 可脱
去2 个HF,可推出M 为
,从⽽得出M、P 的结构简式为
、
化学参考答案· 第10⻚(共10⻚)
学科⽹(北京)股份有限公司
。