文档内容
2023 年高考考前押题密卷(全国乙卷)
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Al-27 P-31 S-32 K-39 Co-59
一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项符合题目要求。
7.化学与生活、生产及环境密切相关,下列说法错误的是
A.常规融雪剂(CaCl 、NaCl等)的使用对桥梁和环境有破坏作用
2
B.“北溪”管道输送的天然气主要成分是烷烃,其中己烷占绝大多数
C.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
D.葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒
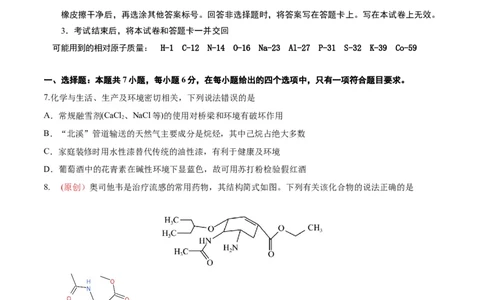
8. (原创)奥司他韦是治疗流感的常用药物,其结构简式如图。下列有关该化合物的说法正确的是
A.与 互为同系物 B.该物质可以酸性重铬酸钾溶液褪色
C.1mol该物质可以与3molH 发生加成反应 D.该物质与NaOH或HCl均可发生成盐反应
2
9.下列实验操作和现象可得出相应结论的是
选
实验操作 现象 结论
项
1
学科网(北京)股份有限公司产生红棕色气 碳与浓硝酸反应生
A 将红热的木炭加入浓硝酸中
体 成了
室温时,将等浓度的弱酸HA和弱碱BOH
B 溶液变红
等体积混合,并滴加紫色石蕊溶液
非金属性:
向KBr溶液中依次滴加过量氯水、淀粉−KI 溶液依次变为
C
溶液 橙色和蓝色 Cl>Br>I
向1 mL 0.1 mol∙L−1 溶液中依次滴加2 依次产生白色
D
滴0.1 mol∙L−1NaCl溶液和0.1 mol∙L−1KI溶液 和黄色沉淀
10.(原创)能正确表示下列反应的离子方程式为
A.向 溶液中加入少量 溶液:
B.向 中加入 :
C.FeCl 溶液中加入HO 溶液并调节pH=4:2Fe2++HO+2H+= 2Fe3++HO
2 2 2 2 2 2
D.次氯酸钠溶液中通入少量二氧化硫:SO +ClO- +H O=SO +2H+ +Cl-
2 2
11.化合物A是一种常用的表面活性剂,结构如图所示。已知X、Y、Z、W、M均为短周期常见元素,W
是形成物质种类最多的元素,X、Y同族,Z、M同族,Z原子半径在同周期最大。下列说法错误的是
A.原子半径Z>Y>X>M
B.非金属性X>Y>W>M>Z
C.四元素中简单氢化物熔沸点最高的是X的氢化物
D.均由X、Y、Z、M四种元素组成的两种盐可以发生反应
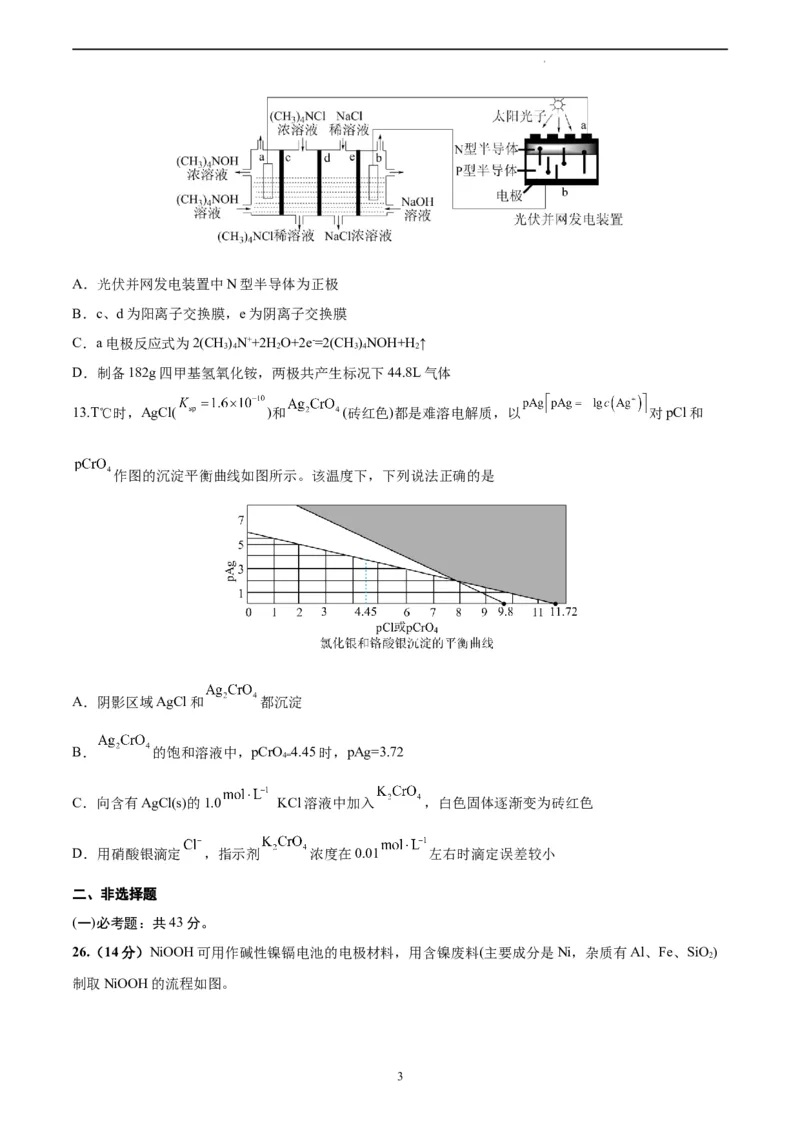
12.2022年我国光伏发电并装机容量突破3亿千瓦,稳居全球首位。已知四甲基氢氧化铵[(CH )NOH]常用
3 4
作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成[(CH )NOH],工作原理如图。
3 4 3 4
下列说法正确的是
2
学科网(北京)股份有限公司A.光伏并网发电装置中N型半导体为正极
B.c、d为阳离子交换膜,e为阴离子交换膜
C.a电极反应式为2(CH)N++2H O+2e-=2(CH )NOH+H ↑
3 4 2 3 4 2
D.制备182g四甲基氢氧化铵,两极共产生标况下44.8L气体
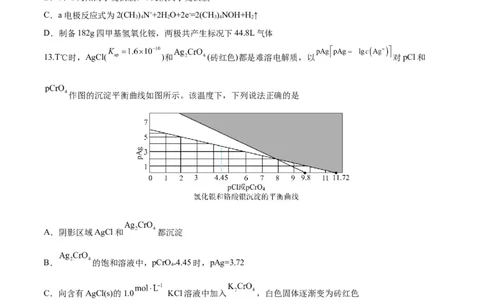
13.T℃时,AgCl( )和 (砖红色)都是难溶电解质,以 对pCl和
作图的沉淀平衡曲线如图所示。该温度下,下列说法正确的是
A.阴影区域AgCl和 都沉淀
B. 的饱和溶液中,pCrO 4.45时,pAg=3.72
4=
C.向含有AgCl(s)的1.0 KCl溶液中加入 ,白色固体逐渐变为砖红色
D.用硝酸银滴定 ,指示剂 浓度在0.01 左右时滴定误差较小
二、非选择题
(一)必考题:共43分。
26.(14分)NiOOH可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是Ni,杂质有Al、Fe、SiO)
2
制取NiOOH的流程如图。
3
学科网(北京)股份有限公司已知:i.镍、铁同族,但Ni2+的性质较稳定;
ii.常温下,该工艺条件下金属阳离子生成氢氧化物沉淀时的pH范围如表所示。
沉淀物
开始沉淀时pH 3.0 1.5 5.9 7.1
完全沉淀时pH 4.7 3.2 9.0 9.2
回答下列问题:
(1)“酸浸”前将废料粉碎的目的是___________,“滤渣2”的主要成分是___________。
(2)加入 的目的是___________,实际生产中发现 的实际用量比理论用量多,原因是___________。
(3)“调pH”时pH的范围是___________,当溶液中离子浓度小于或等于 时认为该离子沉淀完
全,则常温下 ___________,“氧化2”中反应的离子方程式为___________。
(4)锌镍电池是一种可充电电池,其充电时总反应为 ,则放电
时正极的电极反应式为___________,充电时阴极周围溶液pH___________(填“增大”“减小”或“不
变”)。
27.(14分) (三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验室中可由金属钴及
其他原料制备 。微信搜索“高中试卷君”公众号 领取押题卷联考卷
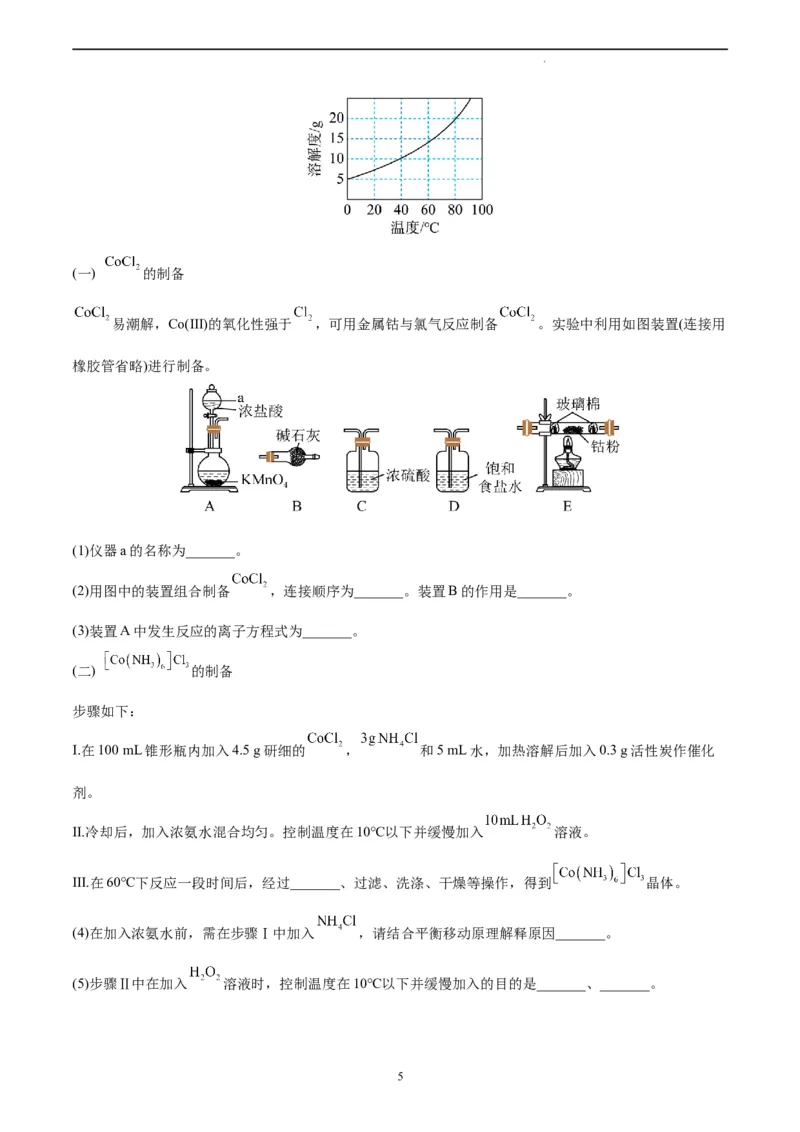
已知: 在 时恰好完全沉淀为 ;②不同温度下 在水中的溶解度如图所
示。
4
学科网(北京)股份有限公司(一) 的制备
易潮解,Co(Ⅲ)的氧化性强于 ,可用金属钴与氯气反应制备 。实验中利用如图装置(连接用
橡胶管省略)进行制备。
(1)仪器a的名称为_______。
(2)用图中的装置组合制备 ,连接顺序为_______。装置B的作用是_______。
(3)装置A中发生反应的离子方程式为_______。
(二) 的制备
步骤如下:
Ⅰ.在100 mL锥形瓶内加入4.5 g研细的 , 和5 mL水,加热溶解后加入0.3 g活性炭作催化
剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入 溶液。
Ⅲ.在60℃下反应一段时间后,经过_______、过滤、洗涤、干燥等操作,得到 晶体。
(4)在加入浓氨水前,需在步骤Ⅰ中加入 ,请结合平衡移动原理解释原因_______。
(5)步骤Ⅱ中在加入 溶液时,控制温度在10℃以下并缓慢加入的目的是_______、_______。
5
学科网(北京)股份有限公司(6)制备 的总反应的化学方程式为_______。
(7)步骤Ⅲ中的操作名称为_______。
28.(15分)我国力争于2030年前做到碳达峰,2060年前实现碳中和,因此CO 的综合利用是研究热点之
2
一。
(1)以CO 为原料可制取甲醇。
2
已知:
①H(g)、CHOH(l)的燃烧热ΔH分别为-285.8kJ·mol-1和-726.5kJ·mol-1
2 3
②CH OH(l) CHOH(g) ΔH=+38kJ·mol-1
3 3
③H
2
O(l) H⇌2 O(g) ΔH=+44kJ·mol-1
则反应C⇌O
2
(g)+3H
2
(g) CH
3
OH(l)+H
2
O(g)的ΔH
1
=_______kJ·mol-1。
(2)利用CO
2
与H
2
合成⇌甲醇涉及的主要反应如下:
I.CO (g)+3H(g) CHOH(l)+H O(g) ΔH
2 2 3 2 1
II.CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O ΔH
2
=+41kJ·mol-1
一定条件下向某⇌刚性容器中充入物质的量之比为1:3的CO
2
和H
2
发生上述反应,在不同催化剂(catl,
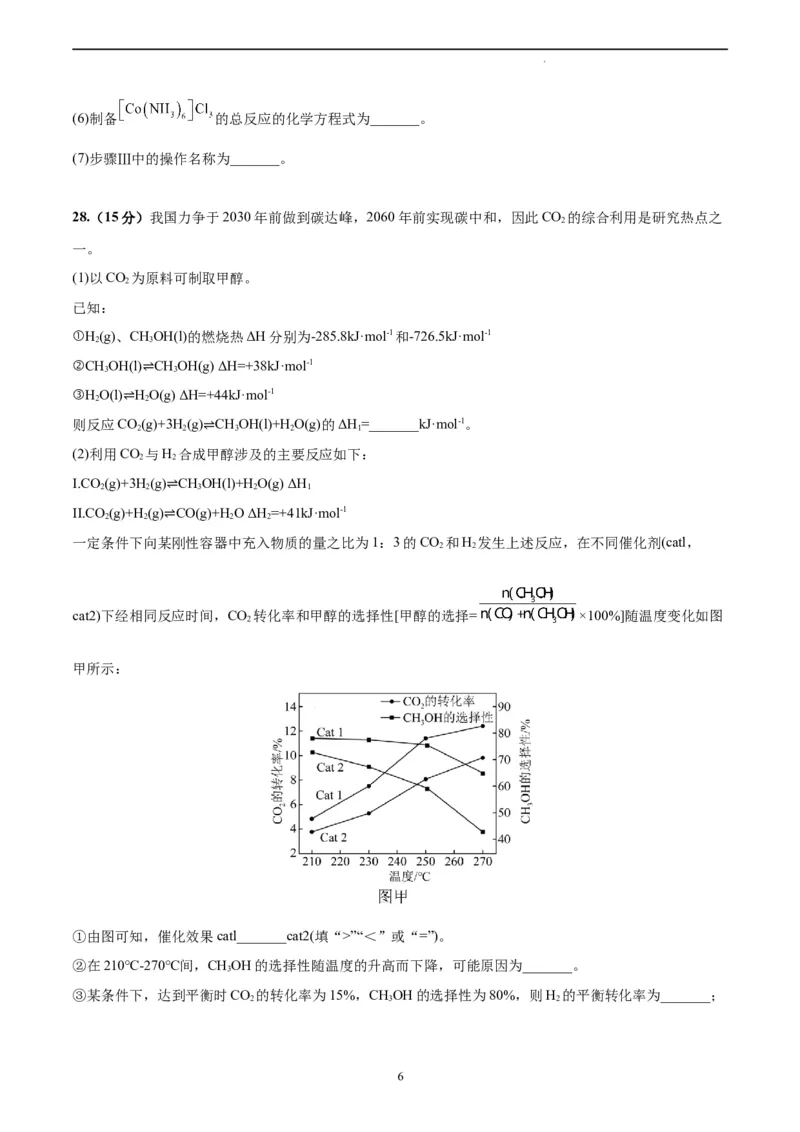
cat2)下经相同反应时间,CO 转化率和甲醇的选择性[甲醇的选择= ×100%]随温度变化如图
2
甲所示:
①由图可知,催化效果catl_______cat2(填“>”“<”或“=”)。
②在210℃-270℃间,CHOH的选择性随温度的升高而下降,可能原因为_______。
3
③某条件下,达到平衡时CO 的转化率为15%,CHOH的选择性为80%,则H 的平衡转化率为_______;
2 3 2
6
学科网(北京)股份有限公司反应II的平衡常数K=_______(列出算式即可)。
p
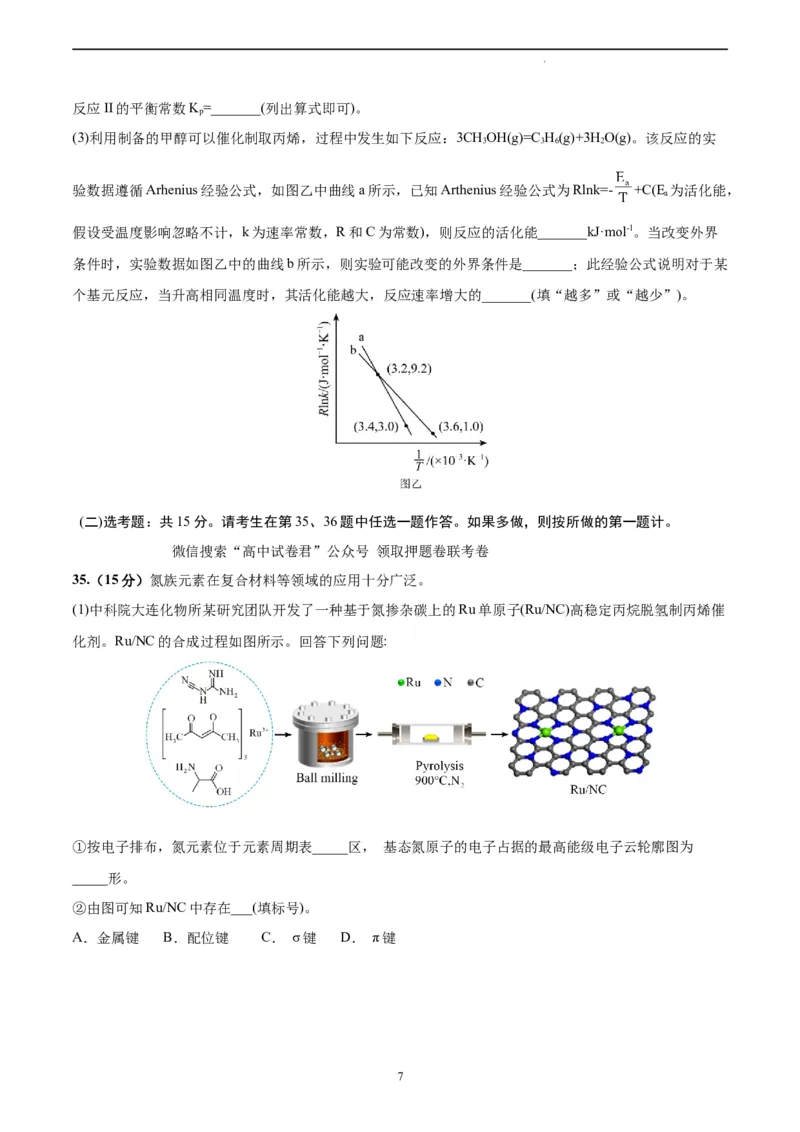
(3)利用制备的甲醇可以催化制取丙烯,过程中发生如下反应:3CHOH(g)=C H(g)+3HO(g)。该反应的实
3 3 6 2
验数据遵循Arhenius经验公式,如图乙中曲线a所示,已知Arthenius经验公式为Rlnk=- +C(E 为活化能,
a
假设受温度影响忽略不计,k为速率常数,R和C为常数),则反应的活化能_______kJ·mol-1。当改变外界
条件时,实验数据如图乙中的曲线b所示,则实验可能改变的外界条件是_______;此经验公式说明对于某
个基元反应,当升高相同温度时,其活化能越大,反应速率增大的_______(填“越多”或“越少”)。
(二)选考题:共15分。请考生在第35、36题中任选一题作答。如果多做,则按所做的第一题计。
微信搜索“高中试卷君”公众号 领取押题卷联考卷
35.(15分)氮族元素在复合材料等领域的应用十分广泛。
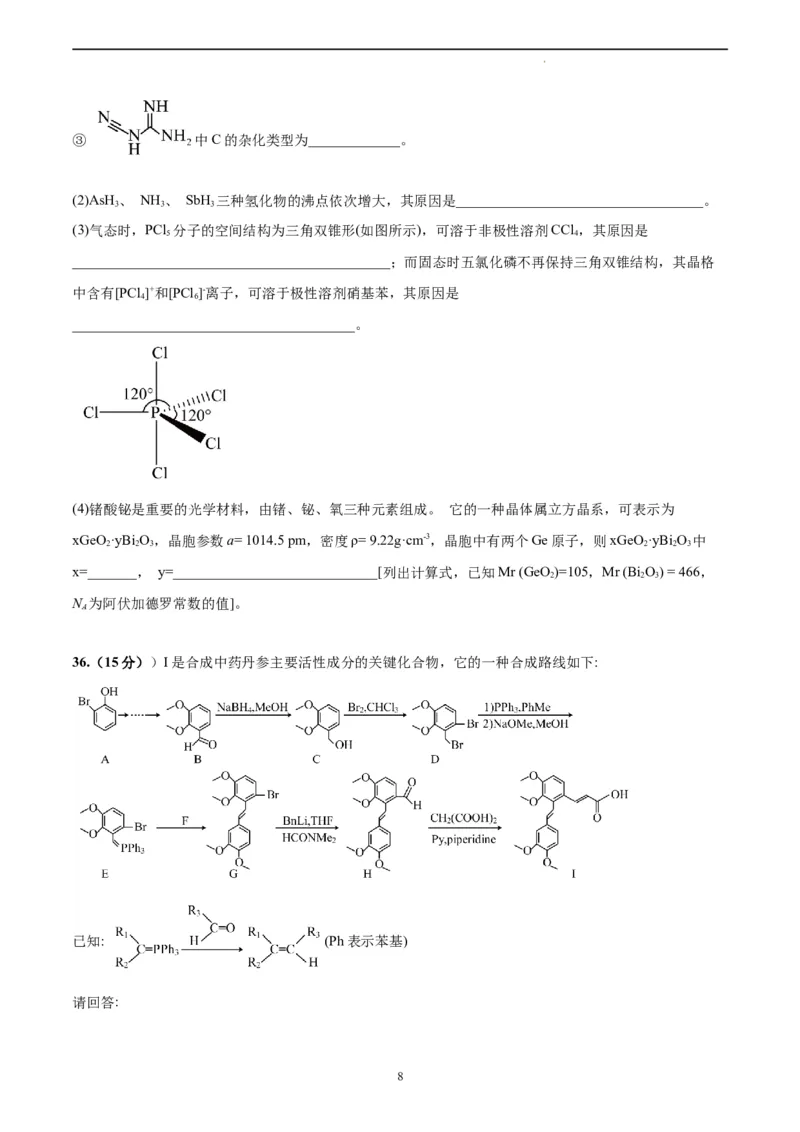
(1)中科院大连化物所某研究团队开发了一种基于氮掺杂碳上的Ru单原子(Ru/NC)高稳定丙烷脱氢制丙烯催
化剂。Ru/NC的合成过程如图所示。回答下列问题:
①按电子排布,氮元素位于元素周期表_____区, 基态氮原子的电子占据的最高能级电子云轮廓图为
_____形。
②由图可知Ru/NC中存在___(填标号)。
A.金属键 B.配位键 C. σ键 D. π键
7
学科网(北京)股份有限公司③ 中C的杂化类型为_____________。
(2)AsH、 NH 、 SbH 三种氢化物的沸点依次增大,其原因是___________________________________。
3 3 3
(3)气态时,PCl 分子的空间结构为三角双锥形(如图所示),可溶于非极性溶剂CCl ,其原因是
5 4
_____________________________________________;而固态时五氯化磷不再保持三角双锥结构,其晶格
中含有[PCl ]+和[PCl ]-离子,可溶于极性溶剂硝基苯,其原因是
4 6
________________________________________。
(4)锗酸铋是重要的光学材料,由锗、铋、氧三种元素组成。 它的一种晶体属立方晶系,可表示为
xGeO ·yBi O,晶胞参数a= 1014.5 pm,密度ρ= 9.22g·cm-3,晶胞中有两个Ge原子,则xGeO ·yBi O 中
2 2 3 2 2 3
x=_______, y=_____________________________[列出计算式,已知Mr (GeO )=105,Mr (Bi O) = 466,
2 2 3
N 为阿伏加德罗常数的值]。
A
36.(15分))I是合成中药丹参主要活性成分的关键化合物,它的一种合成路线如下:
已知: (Ph表示苯基)
请回答:
8
学科网(北京)股份有限公司(1)A的名称是_____________________。
(2)I的官能团的名称是_________________________。
(3)C →D的反应类型为____________________________。
(4)写出E与F反应生成G的化学方程式_____________________________________。
(5)写出同时满足下列条件的B的同分异构体的结构简式____________________。
(i)能发生银镜反应;
(ii) 能发生水解反应;
(iii) 核磁共振氢谱表明有4组峰且峰面积之比为6:2:1:1.
(6)参考上述合成路线,以溴苯为原料,设计合成 (反应条件可不写)______。
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司